علم السموم الجيني ، بحكم التعريف ، هو دراسة كيفية تأثير العوامل الكيميائية أو الفيزيائية على عملية الوراثة المعقدة. تُعرَّف المواد الكيميائية السامة للجينات بأنها مركبات قادرة على تعديل المادة الوراثية للخلايا الحية. يعتمد احتمال أن تسبب مادة كيميائية معينة ضررًا وراثيًا حتمًا على عدة متغيرات ، بما في ذلك مستوى تعرض الكائن الحي للمادة الكيميائية ، وتوزيع المادة الكيميائية والاحتفاظ بها بمجرد دخولها الجسم ، وكفاءة التنشيط الأيضي و / أو أنظمة إزالة السموم في الأنسجة المستهدفة ، وتفاعل المادة الكيميائية أو نواتجها مع الجزيئات الكبيرة الحرجة داخل الخلايا. يعتمد احتمال أن يتسبب الضرر الجيني في المرض في نهاية المطاف على طبيعة الضرر ، وقدرة الخلية على إصلاح أو تضخيم الضرر الجيني ، وفرصة التعبير عن أي تغيير تم إحداثه ، وقدرة الجسم على التعرف على تكاثر وتثبيته. الخلايا الشاذة.
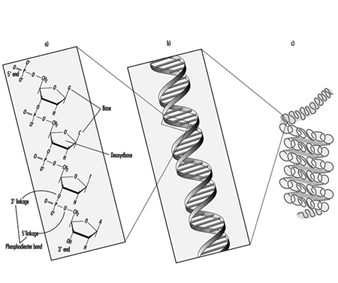
في الكائنات الحية الأعلى ، يتم تنظيم المعلومات الوراثية في الكروموسومات. تتكون الكروموسومات من خيوط مكثفة بإحكام من الحمض النووي المرتبط بالبروتين. داخل كروموسوم واحد ، يوجد كل جزيء DNA كزوج من سلاسل طويلة غير متفرعة من الوحدات الفرعية للنيوكليوتيدات المرتبطة ببعضها البعض بواسطة روابط phosphodiester التي تنضم إلى الكربون الخامس لشق ديوكسيريبوز واحد إلى الكربون الثالث التالي (الشكل 5). بالإضافة إلى ذلك ، يتم إرفاق واحدة من أربع قواعد نيوكليوتيدات مختلفة (الأدينين ، السيتوزين ، الجوانين أو الثايمين) بكل وحدة فرعية ديوكسيريبوز مثل الخرز على سلسلة. ثلاثي الأبعاد ، يشكل كل زوج من خيوط الحمض النووي حلزونًا مزدوجًا مع توجيه جميع القواعد نحو داخل اللولب. داخل اللولب ، ترتبط كل قاعدة بقاعدتها التكميلية على خيط DNA المقابل ؛ تملي الرابطة الهيدروجينية الاقتران القوي غير التساهمي للأدينين مع الثايمين والجوانين مع السيتوزين (الشكل 3). نظرًا لأن تسلسل قواعد النوكليوتيدات مكمل طوال طول جزيء الحمض النووي المزدوج ، فإن كلا الخيطين يحملان نفس المعلومات الجينية بشكل أساسي. في الواقع ، أثناء تكرار الحمض النووي ، يعمل كل خيط كقالب لإنتاج حبلا شريك جديد.
الشكل 1. (أ) الأساسي ، (ب) الثانوي ، (ج) التنظيم العالي للمعلومات الوراثية البشرية
 باستخدام RNA ومجموعة من البروتينات المختلفة ، تقوم الخلية في النهاية بفك شفرة المعلومات المشفرة بواسطة التسلسل الخطي للقواعد داخل مناطق معينة من الحمض النووي (الجينات) وتنتج بروتينات ضرورية لبقاء الخلية الأساسية وكذلك النمو الطبيعي والتمايز. في جوهرها ، تعمل النيوكليوتيدات مثل الأبجدية البيولوجية التي تُستخدم لترميز الأحماض الأمينية ، وهي اللبنات الأساسية للبروتينات.
باستخدام RNA ومجموعة من البروتينات المختلفة ، تقوم الخلية في النهاية بفك شفرة المعلومات المشفرة بواسطة التسلسل الخطي للقواعد داخل مناطق معينة من الحمض النووي (الجينات) وتنتج بروتينات ضرورية لبقاء الخلية الأساسية وكذلك النمو الطبيعي والتمايز. في جوهرها ، تعمل النيوكليوتيدات مثل الأبجدية البيولوجية التي تُستخدم لترميز الأحماض الأمينية ، وهي اللبنات الأساسية للبروتينات.
عندما يتم إدخال نيوكليوتيدات غير صحيحة أو فقدان نيوكليوتيدات ، أو عند إضافة نيوكليوتيدات غير ضرورية أثناء تخليق الحمض النووي ، يسمى الخطأ طفرة. تشير التقديرات إلى حدوث أقل من طفرة واحدة لكل 109 تم دمج النيوكليوتيدات أثناء التكاثر الطبيعي للخلايا. على الرغم من أن الطفرات ليست بالضرورة ضارة ، فإن التغييرات التي تسبب تعطيل أو زيادة التعبير عن الجينات المهمة يمكن أن تؤدي إلى مجموعة متنوعة من الاضطرابات ، بما في ذلك السرطان والأمراض الوراثية والتشوهات التنموية والعقم والموت الجنيني أو في الفترة المحيطة بالولادة. في حالات نادرة جدًا ، يمكن أن تؤدي الطفرة إلى تعزيز البقاء على قيد الحياة ؛ مثل هذه التكرارات هي أساس الانتقاء الطبيعي.
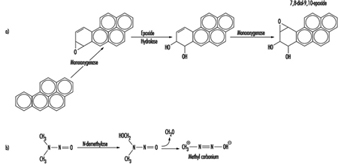
على الرغم من أن بعض المواد الكيميائية تتفاعل مباشرة مع الحمض النووي ، إلا أن معظمها يتطلب تنشيط التمثيل الغذائي. في الحالة الأخيرة ، تكون الوسائط المحبة للكهرباء مثل الإيبوكسيدات أو أيونات الكربون هي المسؤولة في النهاية عن إحداث الآفات في مجموعة متنوعة من المواقع المحبة للنواة داخل المادة الوراثية (الشكل 2). في حالات أخرى ، يتم التوسط في السمية الجينية من خلال المنتجات الثانوية للتفاعل المركب مع الدهون داخل الخلايا أو البروتينات أو الأكسجين.
الشكل 2. التنشيط الحيوي لما يلي: أ) بنزو (أ) بيرين ؛ و ب) N- نيتروسودي ميثيل أمين
بسبب وفرتها النسبية في الخلايا ، فإن البروتينات هي الهدف الأكثر شيوعًا للتفاعلات السامة. ومع ذلك ، يعد تعديل الحمض النووي مصدر قلق أكبر بسبب الدور المركزي لهذا الجزيء في تنظيم النمو والتمايز من خلال أجيال متعددة من الخلايا.
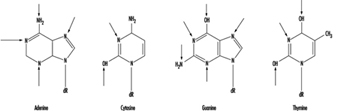
على المستوى الجزيئي ، تميل المركبات المحبة للكهرباء إلى مهاجمة الأكسجين والنيتروجين في الحمض النووي. المواقع الأكثر عرضة للتعديل موضحة في الشكل 3. على الرغم من أن الأكسجين داخل مجموعات الفوسفات في العمود الفقري للحمض النووي هي أيضًا أهداف للتعديل الكيميائي ، يُعتقد أن الضرر الذي يلحق بالقواعد أكثر صلة من الناحية البيولوجية نظرًا لأن هذه المجموعات تعتبر المعلومات الأساسية عناصر في جزيء الحمض النووي.
الشكل 3. المواقع الأولية لتلف الحمض النووي الناجم كيميائياً
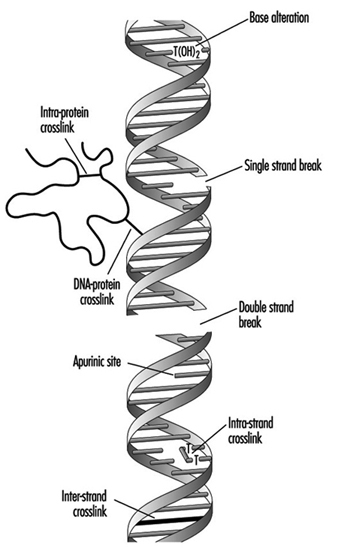
عادةً ما تمارس المركبات التي تحتوي على جزء محب للكهرباء السمية الجينية عن طريق إنتاج أحاديات المقربة في الحمض النووي. وبالمثل ، يمكن للمركبات التي تحتوي على شقين تفاعليين أو أكثر أن تتفاعل مع مركزين مختلفين للنواة ، وبالتالي تنتج روابط متقاطعة داخل أو بين الجزيئات في المادة الوراثية (الشكل 4). يمكن أن تكون الارتباطات المتقاطعة بين DNA-DNA و DNA-البروتين سامة للخلايا بشكل خاص لأنها يمكن أن تشكل كتل كاملة لتكرار الحمض النووي. ولأسباب واضحة ، فإن موت الخلية يقضي على احتمالية تحورها أو تحوّلها الورمي. يمكن أن تعمل العوامل السامة للجينات أيضًا عن طريق إحداث فواصل في العمود الفقري للفوسفوديستر ، أو بين القواعد والسكريات (إنتاج مواقع غير أساسية) في الحمض النووي. قد تكون هذه الفواصل نتيجة مباشرة للتفاعل الكيميائي في موقع الضرر ، أو قد تحدث أثناء إصلاح أحد الأنواع المذكورة أعلاه من آفة الحمض النووي.
الشكل 4. أنواع مختلفة من الأضرار التي لحقت بمركب البروتين والحمض النووي
على مدى الثلاثين إلى الأربعين عامًا الماضية ، تم تطوير مجموعة متنوعة من التقنيات لرصد نوع الضرر الجيني الناجم عن المواد الكيميائية المختلفة. يتم وصف هذه الاختبارات بالتفصيل في مكان آخر من هذا الفصل و موسوعة.
قد يؤدي اختلال "التكاثر الدقيق" مثل المقاربات الأحادية أو المواقع اللاهوائية أو الفواصل أحادية الخيط في النهاية إلى بدائل زوج القاعدة النوكليوتيدية ، أو إدخال أو حذف شظايا عديد النوكليوتيد القصيرة في الحمض النووي الصبغي. في المقابل ، قد تؤدي "التحولات الكبيرة" ، مثل التقريب الضخم ، أو الروابط المتقاطعة ، أو الفواصل المزدوجة الجديلة إلى اكتساب أو فقدان أو إعادة ترتيب قطع كبيرة نسبيًا من الكروموسومات. على أي حال ، يمكن أن تكون العواقب مدمرة للكائن الحي لأن أيًا من هذه الأحداث يمكن أن يؤدي إلى موت الخلايا أو فقدان الوظيفة أو التحول الخبيث للخلايا. إن الكيفية الدقيقة التي يتسبب بها تلف الحمض النووي في الإصابة بالسرطان غير معروفة إلى حد كبير. يُعتقد حاليًا أن العملية قد تنطوي على تنشيط غير مناسب للجينات المسرطنة الأولية مثل myc و رأسو / أو تعطيل الجينات المثبطة للورم التي تم تحديدها مؤخرًا مثل p53. يؤدي التعبير غير الطبيعي لأي نوع من الجينات إلى إبطال الآليات الخلوية الطبيعية للتحكم في تكاثر الخلايا و / أو التمايز.
تشير كثرة الأدلة التجريبية إلى أن تطور السرطان بعد التعرض للمركبات المحبة للكهرباء يعد حدثًا نادرًا نسبيًا. يمكن تفسير ذلك جزئيًا بالقدرة الذاتية للخلية على التعرف على الحمض النووي التالف وإصلاحه أو فشل الخلايا ذات الحمض النووي التالف في البقاء على قيد الحياة. أثناء الإصلاح ، تتم إزالة القاعدة التالفة أو النيوكليوتيدات أو الامتداد القصير من النيوكليوتيدات المحيطة بموقع الضرر و (باستخدام الشريط المعاكس كقالب) يتم تصنيع قطعة جديدة من الحمض النووي وتقسيمها في مكانها. لكي تكون فعالة ، يجب أن يتم إصلاح الحمض النووي بدقة كبيرة قبل انقسام الخلية ، قبل فرص انتشار الطفرة.
أظهرت الدراسات السريرية أن الأشخاص الذين يعانون من عيوب وراثية في القدرة على إصلاح تلف الحمض النووي غالبًا ما يصابون بالسرطان و / أو تشوهات النمو في سن مبكرة (الجدول 1). توفر مثل هذه الأمثلة دليلاً قوياً يربط بين تراكم تلف الحمض النووي والأمراض التي تصيب الإنسان. وبالمثل ، فإن العوامل التي تعزز تكاثر الخلايا (مثل خلات tetradecanoylphorbol) غالبًا ما تعزز التسرطن. بالنسبة لهذه المركبات ، قد يكون الاحتمال المتزايد للتحول الورمي نتيجة مباشرة لانخفاض الوقت المتاح للخلية لإجراء إصلاح مناسب للحمض النووي.
الجدول 1. الاضطرابات الوراثية المعرضة للسرطان والتي يبدو أنها تنطوي على عيوب في إصلاح الحمض النووي
| أعراض | أعراض | النمط الظاهري الخلوي |
| ترنح توسع الشعريات | التدهور العصبي نقص المناعة ارتفاع معدل الإصابة بسرطان الغدد الليمفاوية |
فرط الحساسية للإشعاع المؤين وبعض عوامل الألكلة. تكرار غير منظم للحمض النووي التالف (قد يشير إلى تقصير الوقت لإصلاح الحمض النووي) |
| متلازمة بلوم | تشوهات النمو آفات على الجلد المكشوف ارتفاع نسبة الإصابة بأورام الجهاز المناعي والجهاز الهضمي |
ارتفاع معدل الانحرافات الصبغية خلل في الربط المرتبط بإصلاح الحمض النووي |
| فقر فانسوني | تأخر النمو ارتفاع معدل الإصابة بسرطان الدم |
فرط الحساسية لعوامل التشابك ارتفاع معدل الانحرافات الصبغية الإصلاح المعيب للروابط المتقاطعة في الحمض النووي |
| سرطان القولون الوراثي nonpolyposis | ارتفاع نسبة الإصابة بسرطان القولون | خلل في إصلاح عدم تطابق الحمض النووي (عندما يحدث إدخال نيوكليوتيد خاطئ أثناء النسخ المتماثل) |
| جفاف الجلد المصطبغ | ارتفاع نسبة الإصابة بورم الظهارة في المناطق المكشوفة من الجلد ضعف عصبي (في كثير من الحالات) |
فرط الحساسية للأشعة فوق البنفسجية والعديد من المواد الكيميائية المسرطنة عيوب في إصلاح الختان و / أو تكرار الحمض النووي التالف |
يمكن إرجاع النظريات المبكرة حول كيفية تفاعل المواد الكيميائية مع الحمض النووي إلى الدراسات التي أجريت أثناء تطوير غاز الخردل لاستخدامه في الحرب. نما مزيد من الفهم من الجهود المبذولة لتحديد العوامل المضادة للسرطان التي من شأنها أن توقف بشكل انتقائي تكاثر الخلايا السرطانية سريعة الانقسام. أدى القلق العام المتزايد بشأن المخاطر في بيئتنا إلى إجراء مزيد من البحث في آليات وعواقب التفاعل الكيميائي مع المادة الوراثية. يتم عرض أمثلة على أنواع مختلفة من المواد الكيميائية التي تمارس السمية الجينية في الجدول 2.
الجدول 2. أمثلة على المواد الكيميائية التي تظهر السمية الجينية في الخلايا البشرية
| فئة المواد الكيميائية | مثال | مصدر التعرض | الآفة المحتملة السمية الجينية |
| الأفلاتوكسين | أفلاتوكسين ب 1 | طعام ملوث | تقارب الحمض النووي الضخم |
| الأمينات العطرية | 2-أسيتامينوفلورين | بيئي | تقارب الحمض النووي الضخم |
| كينونات أزيريديني | ميتوميسين ج | العلاج الكيميائي للسرطان | المقاربات الأحادية ، الروابط المتشابكة المتداخلة والفواصل أحادية الخيط في الحمض النووي. |
| الهيدروكربونات المكلورة | كلوريد الفينيل | بيئي | المقاربات الأحادية في الحمض النووي |
| المعادن والمركبات المعدنية | سيسبلاتين | العلاج الكيميائي للسرطان | كل من الروابط المتقاطعة داخل وبين حبلا في الحمض النووي |
| مركبات النيكل | بيئي | المقاربات الأحادية والكسر أحادي الخيط في الحمض النووي | |
| خردل النيتروجين | سيكلوفوسفاميد | العلاج الكيميائي للسرطان | المقاربات الأحادية والارتباطات المتشابكة في الحمض النووي |
| النتروزامين | N- نيتروسوديميثيل أمين | طعام ملوث | المقاربات الأحادية في الحمض النووي |
| الهيدروكربونات العطرية متعددة الحلقات | بنزو (أ) بيرين | بيئي | تقارب الحمض النووي الضخم |