تتمثل وظائف الجهاز المناعي في حماية الجسم من غزو العوامل المعدية وتوفير المراقبة المناعية ضد الخلايا السرطانية الناشئة. له خط دفاع أول غير محدد ويمكن أن يبدأ تفاعلات المستجيب نفسه ، وفرعًا محددًا مكتسبًا ، تحمل فيه الخلايا الليمفاوية والأجسام المضادة خصوصية التعرف والتفاعل اللاحق تجاه المستضد.
تم تعريف علم السموم المناعية على أنه "التخصص المعني بدراسة الأحداث التي يمكن أن تؤدي إلى تأثيرات غير مرغوب فيها نتيجة تفاعل الكائنات الحيوية الغريبة مع جهاز المناعة. قد تنتج هذه الأحداث غير المرغوب فيها نتيجة (1) تأثير مباشر و / أو غير مباشر للحيوية الغريبة (و / أو منتج التحول البيولوجي الخاص بها) على جهاز المناعة ، أو (2) استجابة مضيفة تعتمد على المناعة للمركب و / أو المستقلب (المستقلبات) أو المستضدات المضيفة المعدلة بواسطة المركب أو مستقلباته "(برلين وآخرون 1987).
عندما يعمل الجهاز المناعي كهدف سلبي للإهانات الكيميائية ، يمكن أن تكون النتيجة انخفاض المقاومة للعدوى وأنواع معينة من الأورام ، أو عدم تنظيم / تحفيز المناعة الذي يمكن أن يؤدي إلى تفاقم الحساسية أو المناعة الذاتية. في حالة أن الجهاز المناعي يستجيب لخصوصية المستضد للأجانب الحيوية أو مستضد العائل المعدل بواسطة المركب ، يمكن أن تظهر السمية كأنواع الحساسية أو أمراض المناعة الذاتية.
تم تطوير نماذج حيوانية للتحقيق في قمع المناعة الناجم عن المواد الكيميائية ، وتم التحقق من صحة عدد من هذه الطرق (Burleson ، Munson ، و Dean 1995 ؛ IPCS 1996). لأغراض الاختبار ، يتم اتباع نهج متدرج لإجراء اختيار مناسب من العدد الهائل من المقايسات المتاحة. بشكل عام ، الهدف من المستوى الأول هو تحديد المواد السامة للمناعة المحتملة. إذا تم تحديد السمية المناعية المحتملة ، يتم إجراء المستوى الثاني من الاختبار لتأكيد وتوصيف التغييرات الملحوظة. تشمل تحقيقات المستوى الثالث دراسات خاصة حول آلية عمل المركب. تم تحديد العديد من الكائنات الحية الغريبة على أنها مواد سامة للمناعة تسبب كبت المناعة في مثل هذه الدراسات التي أجريت على حيوانات المختبر.
قاعدة البيانات الخاصة باضطرابات وظائف المناعة لدى البشر بسبب المواد الكيميائية البيئية محدودة (Descotes 1986؛ NRC Subcommittee on Immunotoxicology 1992). لم يحظ استخدام علامات السمية المناعية باهتمام كبير في الدراسات السريرية والوبائية للتحقيق في تأثير هذه المواد الكيميائية على صحة الإنسان. لم يتم إجراء مثل هذه الدراسات بشكل متكرر ، ولا يسمح تفسيرها في كثير من الأحيان باستخلاص استنتاجات لا لبس فيها ، على سبيل المثال بسبب الطبيعة غير المنضبطة للتعرض. لذلك ، في الوقت الحاضر ، يشكل تقييم السمية المناعية في القوارض ، مع الاستقراء اللاحق للإنسان ، أساس القرارات المتعلقة بالخطر والمخاطر.
تفاعلات فرط الحساسية ، لا سيما الربو التحسسي والتهاب الجلد التماسي ، هي مشاكل صحية مهنية مهمة في البلدان الصناعية (Vos، Younes and Smith 1995). تم التحقيق في ظاهرة التحسس التلامسي أولاً في خنزير غينيا (Andersen and Maibach 1985). حتى وقت قريب ، كان هذا هو النوع المفضل للاختبار التنبئي. تتوفر العديد من طرق اختبار خنازير غينيا ، وأكثرها استخدامًا هو اختبار تعظيم خنزير غينيا واختبار الرقعة المغطاة لـ Buehler. تزود اختبارات خنازير غينيا والأساليب الأحدث التي تم تطويرها في الفئران ، مثل اختبارات تورم الأذن وفحص العقدة الليمفاوية المحلية ، أخصائي السموم بالأدوات اللازمة لتقييم مخاطر حساسية الجلد. يختلف الوضع فيما يتعلق بتوعية الجهاز التنفسي اختلافًا كبيرًا. لا توجد حتى الآن طرق معتمدة جيدًا أو مقبولة على نطاق واسع لتحديد المواد المسببة للحساسية التنفسية الكيميائية على الرغم من إحراز تقدم في تطوير نماذج حيوانية للتحقيق في الحساسية التنفسية الكيميائية في خنزير غينيا والفأر.
تظهر البيانات البشرية أن العوامل الكيميائية ، وخاصة الأدوية ، يمكن أن تسبب أمراض المناعة الذاتية (Kammüller، Bloksma and Seinen 1989). هناك عدد من النماذج الحيوانية التجريبية لأمراض المناعة الذاتية البشرية. يشمل هذا كلا من علم الأمراض العفوي (على سبيل المثال الذئبة الحمامية الجهازية في الفئران السوداء النيوزيلندية) وظواهر المناعة الذاتية الناتجة عن التحصين التجريبي باستخدام مستضد ذاتي تفاعلي (على سبيل المثال التهاب المفاصل المستحث H37Ra في فئران سلالة لويس). يتم تطبيق هذه النماذج في التقييم قبل السريري للأدوية المثبطة للمناعة. تناول عدد قليل جدًا من الدراسات إمكانات هذه النماذج لتقييم ما إذا كان أحد الكائنات الحية الغريبة يؤدي إلى تفاقم المناعة الذاتية المستحثة أو الخلقية. النماذج الحيوانية المناسبة للتحقيق في قدرة المواد الكيميائية على إحداث أمراض المناعة الذاتية غير متوفرة تقريبًا. أحد النماذج المستخدمة إلى حدٍ محدود هو اختبار العقدة الليمفاوية المأبضية في الفئران. كما هو الحال عند البشر ، تلعب العوامل الوراثية دورًا حاسمًا في تطور أمراض المناعة الذاتية (AD) في حيوانات المختبر ، مما سيحد من القيمة التنبؤية لمثل هذه الاختبارات.
الجهاز المناعي
تتمثل الوظيفة الرئيسية لجهاز المناعة في الدفاع ضد البكتيريا والفيروسات والطفيليات والفطريات والخلايا الورمية. ويتحقق ذلك من خلال أعمال أنواع مختلفة من الخلايا ووسائطها القابلة للذوبان في حفل موسيقي مضبوط بدقة. يمكن تقسيم دفاع المضيف تقريبًا إلى مقاومة غير محددة أو فطرية ومناعة محددة أو مكتسبة بوساطة الخلايا الليمفاوية (Roitt، Brostoff and Male 1989).
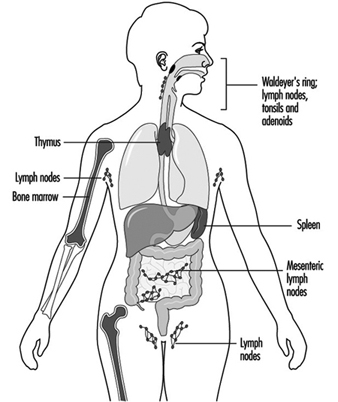
مكونات الجهاز المناعي موجودة في جميع أنحاء الجسم (جونز وآخرون 1990). تم العثور على حجرة الخلايا الليمفاوية داخل الأعضاء الليمفاوية (الشكل 1). يتم تصنيف نخاع العظم والغدة الصعترية كأعضاء لمفاوية أولية أو مركزية. تشمل الأعضاء الليمفاوية الثانوية أو المحيطية العقد الليمفاوية والطحال والأنسجة اللمفاوية على طول الأسطح الإفرازية مثل الجهاز الهضمي والجهاز التنفسي ، ما يسمى بالأنسجة اللمفاوية المرتبطة بالغشاء المخاطي (MALT). يوجد حوالي نصف الخلايا الليمفاوية في الجسم في أي وقت في MALT. بالإضافة إلى ذلك ، يعد الجلد عضوًا مهمًا لتحفيز الاستجابات المناعية لمولدات المضادات الموجودة على الجلد. من المهم في هذه العملية خلايا لانجرهانز الموجودة في البشرة والتي لها وظيفة تقديم المستضد.
الشكل 1. الأعضاء والأنسجة اللمفاوية الأولية والثانوية
تحدث الخلايا البلعمية من سلالة الوحيدات / البلاعم ، والتي تسمى نظام البلعمة أحادي النواة (MPS) ، في الأعضاء اللمفاوية وأيضًا في المواقع الخارجية ؛ تشمل الخلايا البلعمية الخارجية خلايا كوبفر في الكبد ، والضامة السنخية في الرئة ، والضامة المسراق في الكلية ، والخلايا الدبقية في الدماغ. توجد الكريات البيض متعددة الأشكال (PMNs) بشكل رئيسي في الدم ونخاع العظام ، ولكنها تتراكم في مواقع الالتهاب.
دفاع غير محدد
يتم تنفيذ خط الدفاع الأول للكائنات الحية الدقيقة بواسطة حاجز فيزيائي وكيميائي ، مثل الجلد والجهاز التنفسي والجهاز الهضمي. يتم مساعدة هذا الحاجز من خلال آليات وقائية غير محددة بما في ذلك الخلايا البلعمية ، مثل البلاعم والخلايا البيضاء متعددة الأشكال ، القادرة على قتل مسببات الأمراض ، والخلايا القاتلة الطبيعية ، والتي يمكنها أن تتلاشى الخلايا السرطانية والخلايا المصابة بالفيروس. كما يشارك النظام التكميلي وبعض مثبطات الميكروبات (مثل الليزوزيم) في الاستجابة غير النوعية.
مناعة محددة
بعد الاتصال الأولي للمضيف مع الممرض ، يتم إحداث استجابات مناعية محددة. السمة المميزة لخط الدفاع الثاني هذا هي التعرف على المحددات ، ما يسمى بالمستضدات أو الحواتم ، لمسببات الأمراض عن طريق المستقبلات الموجودة على سطح الخلية للخلايا اللمفاوية B و T. بعد التفاعل مع المستضد المحدد ، يتم تحفيز الخلية الحاملة للمستقبلات للخضوع للتكاثر والتمايز ، مما ينتج عنه استنساخ من الخلايا السلالة الخاصة بالمستضد المستخرج. تساعد الاستجابات المناعية المحددة في الدفاع غير المحدد المقدم لمسببات الأمراض عن طريق تحفيز فعالية الاستجابات غير المحددة. السمة الأساسية لمناعة معينة هي أن الذاكرة تتطور. يؤدي الاتصال الثانوي مع نفس المستضد إلى استجابة أسرع وأكثر قوة ولكن منظمة بشكل جيد.
لا يمتلك الجينوم القدرة على حمل رموز مجموعة من مستقبلات المستضدات الكافية للتعرف على عدد المستضدات التي يمكن مواجهتها. يتطور ذخيرة الخصوصية من خلال عملية إعادة ترتيب الجينات. هذه عملية عشوائية ، يتم خلالها خلق خصائص مختلفة. يتضمن هذا خصوصيات المكونات الذاتية ، والتي هي غير مرغوب فيها. عملية الانتقاء التي تحدث في الغدة الصعترية (الخلايا التائية) أو نخاع العظام (الخلايا البائية) تعمل على حذف هذه الخصائص غير المرغوب فيها.
تعتمد وظيفة المستجيب المناعي الطبيعي والتنظيم الاستتباري للاستجابة المناعية على مجموعة متنوعة من المنتجات القابلة للذوبان ، والمعروفة مجتمعة باسم السيتوكينات ، والتي يتم تصنيعها وإفرازها بواسطة الخلايا الليمفاوية وأنواع الخلايا الأخرى. السيتوكينات لها تأثيرات متعددة الموجات على الاستجابات المناعية والالتهابية. التعاون بين مجموعات الخلايا المختلفة مطلوب للاستجابة المناعية - تنظيم استجابات الأجسام المضادة ، وتراكم الخلايا والجزيئات المناعية في مواقع الالتهاب ، وبدء استجابات المرحلة الحادة ، والتحكم في وظيفة البلاعم السامة للخلايا والعديد من العمليات الأخرى المركزية لمقاومة المضيف . تتأثر هذه السيتوكينات ، وتعتمد عليها في كثير من الحالات ، بشكل فردي أو جماعي.
يتم التعرف على ذراعي مناعة محددة - المناعة الخلطية والحصانة الخلوية أو الخلوية:
الحصانة الخلطية. يتم تحفيز الخلايا الليمفاوية B في الذراع الخلطية بعد التعرف على المستضد بواسطة مستقبلات سطح الخلية. مستقبلات المستضد على الخلايا الليمفاوية B هي الغلوبولين المناعي (Ig). تبدأ الخلايا البائية الناضجة (خلايا البلازما) في إنتاج الغلوبولين المناعي الخاص بالمستضد الذي يعمل كأجسام مضادة في مصل الدم أو على طول الأسطح المخاطية. هناك خمس فئات رئيسية من الغلوبولين المناعي: (1) IgM ، Ig خماسي مع قدرة التراص المثلى ، والتي يتم إنتاجها لأول مرة بعد تحفيز المستضد ؛ (2) IgG ، Ig الرئيسي المتداول ، والذي يمكن أن يمر عبر المشيمة ؛ (3) IgA ، إفرازي Ig لحماية الأسطح المخاطية ؛ (4) IgE، Ig fixing to mast cells or basophilic granulocytes المشاركة في تفاعلات فرط الحساسية الفورية و (5) IgD ، وظيفتها الرئيسية كمستقبل على الخلايا اللمفاوية البائية.
مناعة خلوية. يتم التوسط في الذراع الخلوية لجهاز المناعة المحدد بواسطة الخلايا اللمفاوية التائية. تحتوي هذه الخلايا أيضًا على مستقبلات مستضد على أغشيتها. يتعرفون على المستضد إذا تم تقديمه بواسطة الخلايا العارضة للمستضد في سياق مستضدات التوافق النسيجي. ومن ثم ، فإن هذه الخلايا لها قيود بالإضافة إلى خصوصية المستضد. تعمل الخلايا التائية كخلايا مساعدة للعديد من الاستجابات المناعية (بما في ذلك الخلطية) ، وتتوسط في تجنيد الخلايا الالتهابية ، ويمكنها ، كخلايا تي سامة للخلايا ، أن تقتل الخلايا المستهدفة بعد التعرف على مستضد معين.
آليات السمية المناعية
المناعة
تعتمد مقاومة المضيف الفعالة على السلامة الوظيفية لجهاز المناعة ، والتي تتطلب بدورها أن تكون الخلايا والجزيئات المكونة للاستجابات المناعية متوفرة بأعداد كافية وفي شكل تشغيلي. غالبًا ما يتسم نقص المناعة الخلقي عند البشر بعيوب في بعض سلالات الخلايا الجذعية ، مما يؤدي إلى ضعف أو غياب إنتاج الخلايا المناعية. عن طريق القياس مع أمراض نقص المناعة الخلقية والمكتسبة ، قد ينتج كبت المناعة الناتج عن المواد الكيميائية ببساطة عن انخفاض عدد الخلايا الوظيفية (IPCS ، 1996). قد يكون لغياب الخلايا الليمفاوية أو انخفاض عددها تأثيرات عميقة أكثر أو أقل على حالة المناعة. ارتبطت بعض حالات نقص المناعة والتثبيط المناعي الشديد ، كما يمكن أن يحدث في عمليات الزرع أو العلاج المثبط للخلايا ، على وجه الخصوص بزيادة حالات العدوى الانتهازية وبعض الأمراض الورمية. يمكن أن تكون العدوى بكتيرية أو فيروسية أو فطرية أو من الأوالي ، ويعتمد النوع السائد من العدوى على نقص المناعة المرتبط. قد يُتوقع أن يؤدي التعرض للمواد الكيميائية البيئية المثبطة للمناعة إلى أشكال أكثر دقة من كبت المناعة ، والتي قد يكون من الصعب اكتشافها. قد يؤدي ذلك ، على سبيل المثال ، إلى زيادة معدل الإصابة بعدوى مثل الأنفلونزا أو نزلات البرد.
نظرًا لتعقيد جهاز المناعة ، مع وجود مجموعة متنوعة من الخلايا والوسطاء والوظائف التي تشكل شبكة معقدة وتفاعلية ، تتمتع المركبات السامة للمناعة بفرص عديدة لإحداث تأثير. على الرغم من أن طبيعة الآفات الأولية التي تسببها العديد من المواد الكيميائية السامة للمناعة لم يتم توضيحها بعد ، إلا أن هناك معلومات متزايدة متاحة ، مشتقة في الغالب من الدراسات التي أجريت على حيوانات المختبر ، فيما يتعلق بالتغيرات المناعية التي تؤدي إلى اكتئاب وظيفة المناعة (دين وآخرون 1994) . قد تحدث التأثيرات السامة في الوظائف الحاسمة التالية (وبعض الأمثلة معروضة لمركبات سامة للمناعة تؤثر على هذه الوظائف):
- تطوير وتوسيع مجموعات الخلايا الجذعية المختلفة (يؤدي البنزين إلى تأثيرات سامة للمناعة على مستوى الخلايا الجذعية ، مما يتسبب في قلة اللمفاويات)
- تكاثر الخلايا الليمفاوية والخلايا النخاعية المختلفة وكذلك الأنسجة الداعمة التي تنضج فيها هذه الخلايا وتعمل (مركبات القصدير العضوي السامة للمناعة تكبح النشاط التكاثري للخلايا الليمفاوية في قشرة الغدة الصعترية من خلال السمية الخلوية المباشرة ؛ التأثير السام للغدة من 2,3,7,8،XNUMX،XNUMX،XNUMX-رباعي الكلور -ديبنزو- ب- ديوكسين (TCDD) والمركبات ذات الصلة من المحتمل أن يكون بسبب خلل في وظيفة الخلايا الظهارية الصعترية ، بدلاً من السمية المباشرة للخلايا التوتية)
- امتصاص المستضد ومعالجته وعرضه بواسطة الضامة والخلايا الأخرى التي تقدم المستضد (أحد أهداف 7,12،XNUMX-ثنائي ميثيل بنز (أ) أنثراسين (DMBA) والرصاص هو عرض مستضد بواسطة الضامة ؛ هدف الأشعة فوق البنفسجية هو المستضد- تقديم خلية لانجرهانز)
- الوظيفة التنظيمية للخلايا T-helper و T-suppressor (تتأثر وظيفة الخلية المساعدة T بسبب القصدير العضوي والألديكارب وثنائي الفينيل متعدد الكلور (PCBs) و TCDD و DMBA ؛ يتم تقليل وظيفة الخلايا التائية القاتلة عن طريق العلاج بجرعة منخفضة من السيكلوفوسفاميد)
- إنتاج السيتوكينات المختلفة أو الإنترلوكينات (benzo (a) pyrene (BP) يثبط إنتاج interleukin-1 ؛ الأشعة فوق البنفسجية تغير إنتاج السيتوكينات بواسطة الخلايا الكيراتينية)
- يتم قمع تخليق فئات مختلفة من الغلوبولين المناعي IgM و IgG بعد علاج ثنائي الفينيل متعدد الكلور وأكسيد ثلاثي بوتيل القصدير (TBT) ، ويزيد بعد التعرض لسداسي كلورو البنزين (HCB)).
- التنظيم التكميلي والتفعيل (يتأثر بـ TCDD)
- وظيفة الخلايا التائية السامة للخلايا (3-ميثيل كولانثرين (3-MC) ، DMBA ، و TCDD تثبط نشاط الخلايا التائية السامة للخلايا)
- وظيفة الخلية القاتلة الطبيعية (NK) (يتم قمع نشاط NK الرئوي بواسطة الأوزون ؛ نشاط NK الطحال يضعف بالنيكل)
- البلاعم والتركيز الكيميائي للكريات البيض متعددة الأشكال والوظائف السامة للخلايا (الأوزون وثاني أكسيد النيتروجين يضعفان النشاط البلعمي للبلاعم السنخية).
حساسية
حساسية يمكن تعريفها على أنها الآثار الصحية الضارة التي تنتج عن تحريض واستنباط استجابات مناعية محددة. عندما تحدث تفاعلات فرط الحساسية دون تدخل الجهاز المناعي ، فإن هذا المصطلح الحساسية الزائفة يستخدم. في سياق علم السموم المناعية ، تنتج الحساسية من استجابة مناعية محددة للمواد الكيميائية والأدوية ذات الأهمية. ترتبط قدرة مادة كيميائية على توعية الأفراد عمومًا بقدرتها على الارتباط تساهميًا ببروتينات الجسم. قد تتخذ تفاعلات الحساسية أشكالًا متنوعة وتختلف هذه فيما يتعلق بكل من الآليات المناعية الأساسية وسرعة التفاعل. تم التعرف على أربعة أنواع رئيسية من تفاعلات الحساسية: تفاعلات فرط الحساسية من النوع الأول ، والتي يتم تفعيلها بواسطة الأجسام المضادة IgE حيث تظهر الأعراض في غضون دقائق من تعرض الشخص المصاب بالحساسية. تنجم تفاعلات فرط الحساسية من النوع الثاني عن تلف أو تدمير الخلايا المضيفة بواسطة الجسم المضاد. في هذه الحالة تظهر الأعراض في غضون ساعات. تفاعلات فرط الحساسية من النوع الثالث ، أو آرثوس ، هي أيضًا تفاعلات جسم مضاد ، ولكن ضد مستضد قابل للذوبان ، وتنتج عن العمل المحلي أو النظامي للمجمعات المناعية. النوع الرابع ، أو فرط الحساسية من النوع المتأخر ، تتأثر بالخلايا اللمفاوية التائية وتتطور الأعراض عادة من 24 إلى 48 ساعة بعد تعرض الشخص المصاب بالحساسية.
نوعان من الحساسية الكيميائية الأكثر صلة بالصحة المهنية هما حساسية التلامس أو حساسية الجلد وحساسية الجهاز التنفسي.
فرط الحساسية التلامسية. هناك عدد كبير من المواد الكيميائية القادرة على التسبب في حساسية الجلد. بعد التعرض الموضعي لفرد حساس لمسببات الحساسية الكيميائية ، يتم تحفيز استجابة الخلايا اللمفاوية التائية في العقد الليمفاوية النازفة. يتفاعل مسبب الحساسية في الجلد بشكل مباشر أو غير مباشر مع خلايا لانجرهانز الموجودة في البشرة ، والتي تنقل المادة الكيميائية إلى الغدد الليمفاوية وتقدمها في شكل مناعي إلى الخلايا اللمفاوية التائية المستجيبة. تتكاثر الخلايا اللمفاوية التائية المنشطة للحساسية ، مما يؤدي إلى توسع نسيلي. أصبح الفرد الآن حساسًا وسيستجيب لتعرض جلدي ثانٍ لنفس المادة الكيميائية باستجابة مناعية أكثر عدوانية ، مما يؤدي إلى التهاب الجلد التماسي التحسسي. يكون التفاعل الالتهابي الجلدي الذي يميز التهاب الجلد التماسي التحسسي ثانويًا للتعرف على مسببات الحساسية في الجلد بواسطة الخلايا اللمفاوية التائية المحددة. يتم تنشيط هذه الخلايا الليمفاوية ، وتطلق السيتوكينات وتتسبب في التراكم المحلي للكريات البيض وحيدة النواة الأخرى. تظهر الأعراض بعد حوالي 24 إلى 48 ساعة بعد تعرض الشخص المصاب بالحساسية ، وبالتالي فإن التهاب الجلد التماسي التحسسي يمثل شكلاً من أشكال فرط الحساسية المتأخرة. تشمل الأسباب الشائعة لالتهاب الجلد التماسي التحسسي المواد الكيميائية العضوية (مثل 2,4،XNUMX-dinitrochlorobenzene) والمعادن (مثل النيكل والكروم) والمنتجات النباتية (مثل urushiol من اللبلاب السام).
فرط الحساسية التنفسية. عادة ما تعتبر فرط الحساسية التنفسية تفاعل فرط الحساسية من النوع الأول. ومع ذلك ، قد تتضمن تفاعلات المرحلة المتأخرة والأعراض المزمنة المرتبطة بالربو عمليات مناعية بوساطة الخلايا (النوع الرابع). الأعراض الحادة المصاحبة لحساسية الجهاز التنفسي تتأثر بالجسم المضاد IgE ، الذي يتم تحفيز إنتاجه بعد تعرض الفرد المعرض للحساسية الكيميائية المحرضة. يتوزع الجسم المضاد IgE بشكل منهجي ويرتبط ، عبر مستقبلات الغشاء ، بالخلايا البدينة الموجودة في الأنسجة الوعائية ، بما في ذلك الجهاز التنفسي. بعد استنشاق نفس المادة الكيميائية سيحدث تفاعل فرط حساسية في الجهاز التنفسي. ترتبط المواد المسببة للحساسية بالبروتين وتتصل بالجسم المضاد IgE المرتبط بالخلايا البدينة ويرتبط بها. وهذا بدوره يتسبب في تحلل الخلايا البدينة وإطلاق الوسطاء الالتهابيين مثل الهيستامين والليوكوترين. يسبب هؤلاء الوسطاء تضيق القصبات وتوسع الأوعية ، مما يؤدي إلى أعراض حساسية الجهاز التنفسي ؛ الربو و / أو التهاب الأنف. تشمل المواد الكيميائية المعروفة بأنها تسبب فرط الحساسية في الجهاز التنفسي لدى الإنسان أنهيدريد حامض (مثل أنهيدريد التريميليت) ، وبعض ثنائي أيزوسيانات (مثل التولوين ثنائي أيزوسيانات) ، وأملاح البلاتين وبعض الأصباغ التفاعلية. ومن المعروف أيضًا أن التعرض المزمن للبريليوم يسبب فرط الحساسية لأمراض الرئة.
المناعة الذاتية
المناعة الذاتية يمكن تعريفه على أنه تحفيز الاستجابات المناعية المحددة الموجهة ضد المستضدات الذاتية "الذاتية". يمكن أن تنتج المناعة الذاتية المستحثة إما عن تغيرات في توازن الخلايا الليمفاوية التائية التنظيمية أو من ارتباط كائن حيوي غريب بمكونات الأنسجة الطبيعية مثل جعلها مناعية ("الذات المتغيرة"). الأدوية والمواد الكيميائية المعروفة بإحداث أو تفاقم تأثيرات مثل أمراض المناعة الذاتية (AD) في الأفراد المعرضين للإصابة هي مركبات منخفضة الوزن الجزيئي (الوزن الجزيئي 100 إلى 500) والتي تعتبر بشكل عام غير مناعية. آلية مرض الزهايمر عن طريق التعرض للمواد الكيميائية غير معروفة في الغالب. يمكن أن ينتج المرض مباشرة عن طريق تدوير الجسم المضاد ، بشكل غير مباشر من خلال تكوين معقدات مناعية ، أو كنتيجة لمناعة خلوية ، ولكن من المحتمل أن يحدث من خلال مجموعة من الآليات. يُعرف التسبب في المرض بشكل أفضل في اضطرابات انحلال الدم المناعي التي تحدثها الأدوية:
- يمكن أن يلتصق الدواء بغشاء الخلية الحمراء ويتفاعل مع الجسم المضاد الخاص بالعقار.
- يمكن للدواء أن يغير غشاء الخلية الحمراء بحيث يعتبر الجهاز المناعي الخلية غريبة.
- يشكل الدواء والأجسام المضادة الخاصة به مركبات مناعية تلتصق بغشاء الخلية الحمراء لتسبب الإصابة.
- تحدث حساسية الخلايا الحمراء بسبب إنتاج الأجسام المضادة للخلايا الحمراء.
تم العثور على مجموعة متنوعة من المواد الكيميائية والعقاقير ، ولا سيما الأخيرة ، للحث على استجابات تشبه المناعة الذاتية (Kamüller، Bloksma and Seinen 1989). قد يؤدي التعرض المهني للمواد الكيميائية بشكل عرضي إلى متلازمات شبيهة بمرض الزهايمر. قد يؤدي التعرض لكلوريد الفينيل الأحادي وثلاثي كلورو الإيثيلين والبيركلورو إيثيلين وراتنجات الإيبوكسي وغبار السيليكا إلى حدوث متلازمات تشبه تصلب الجلد. تم وصف متلازمة شبيهة بالذئبة الحمامية الجهازية (SLE) بعد التعرض للهيدرازين. ارتبط التعرض لمادة ثنائي أيزوسيانات التولوين بتحريض فرفرية نقص الصفيحات. المعادن الثقيلة مثل الزئبق متورطة في بعض حالات التهاب كبيبات الكلى المعقد المناعي.
تقييم المخاطر البشرية
يتم إجراء تقييم حالة المناعة البشرية بشكل أساسي باستخدام الدم المحيطي لتحليل المواد الخلطية مثل الغلوبولين المناعي والمكملات ، وكريات الدم البيضاء لتكوين المجموعات الفرعية ووظائف المجموعات السكانية الفرعية. عادة ما تكون هذه الطرق هي نفسها المستخدمة في فحص المناعة الخلطية والخلوية بالإضافة إلى المقاومة غير النوعية للمرضى الذين يشتبه في إصابتهم بمرض نقص المناعة الخلقي. بالنسبة للدراسات الوبائية (على سبيل المثال ، للسكان المعرضين مهنياً) ، يجب اختيار المعلمات على أساس قيمتها التنبؤية في التجمعات البشرية ، والنماذج الحيوانية التي تم التحقق من صحتها ، والبيولوجيا الأساسية للواسمات (انظر الجدول 1). تعتمد استراتيجية فحص التأثيرات السمية المناعية بعد التعرض (العرضي) للملوثات البيئية أو غيرها من المواد السامة إلى حد كبير على الظروف ، مثل نوع نقص المناعة المتوقع ، والوقت بين التعرض وتقييم الحالة المناعية ، ودرجة التعرض وعدد الأفراد المعرضين. عملية تقييم مخاطر السمية المناعية لحيوان أجنبي معين في البشر صعبة للغاية وغالباً ما تكون مستحيلة ، ويرجع ذلك إلى حد كبير إلى وجود عوامل مربكة مختلفة من أصل داخلي أو خارجي المنشأ التي تؤثر على استجابة الأفراد للضرر السام. هذا صحيح بشكل خاص للدراسات التي تبحث في دور التعرض للمواد الكيميائية في أمراض المناعة الذاتية ، حيث تلعب العوامل الوراثية دورًا حاسمًا.
الجدول 1. تصنيف الاختبارات لعلامات المناعة
| فئة الاختبار | الخصائص | اختبارات محددة |
| أساسيات عامة يجب تضمينها مع اللوحات العامة |
مؤشرات الصحة العامة وحالة نظام الجهاز | نيتروجين اليوريا في الدم ، جلوكوز الدم ، إلخ. |
| المناعة الأساسية يجب تضمينها مع اللوحات العامة |
المؤشرات العامة للحالة المناعية تكلفة منخفضة نسبيًا يتم توحيد طرق الفحص بين المختبرات النتائج خارج النطاقات المرجعية قابلة للتفسير سريريًا |
تعداد الدم الكامل مستويات مصل IgG و IgA و IgM الأنماط الظاهرية للعلامة السطحية لمجموعات فرعية من الخلايا الليمفاوية الرئيسية |
| التركيز / المنعكس يجب تضمينها عند الإشارة إليها من خلال النتائج السريرية أو حالات التعرض المشتبه بها أو نتائج الاختبار السابقة |
مؤشرات وظائف / أحداث مناعية محددة التكلفة تختلف يتم توحيد طرق الفحص بين المختبرات النتائج خارج النطاقات المرجعية قابلة للتفسير سريريًا |
التركيب الجيني التوافق النسيجي الأجسام المضادة للعوامل المعدية إجمالي مصل IgE IgE الخاص بمسببات الحساسية الأجسام المضادة اختبارات الجلد لفرط الحساسية انفجار مؤكسد المحببات علم التشريح المرضي (خزعة الأنسجة) |
| أبحاث يجب تضمينها فقط مع مجموعات التحكم وتصميم الدراسة الدقيق |
مؤشرات وظائف / أحداث مناعية عامة أو محددة التكلفة تختلف. غالبًا ما تكون باهظة الثمن عادة لا يتم توحيد طرق الفحص بين المختبرات غالبًا ما تكون النتائج خارج النطاقات المرجعية غير قابلة للتفسير سريريًا |
فحوصات التحفيز في المختبر علامات سطح تنشيط الخلية تركيزات مصل السيتوكين فحوصات استنساخ (جسم مضاد ، خلوي ، وراثي) اختبارات السمية الخلوية |
نظرًا لأن البيانات البشرية المناسبة نادرًا ما تتوفر ، فإن تقييم مخاطر التثبيط المناعي الناجم عن المواد الكيميائية لدى البشر يعتمد في معظم الحالات على دراسات أجريت على الحيوانات. يتم تحديد xenobiotics المحتملة السامة للمناعة في المقام الأول في الدراسات الخاضعة للرقابة في القوارض. تقدم دراسات التعرض في الجسم الحي ، في هذا الصدد ، النهج الأمثل لتقدير إمكانات السمية المناعية للمركب. هذا يرجع إلى الطبيعة المتعددة العوامل والمعقدة لجهاز المناعة والاستجابات المناعية. الدراسات في المختبر لها قيمة متزايدة في توضيح آليات السمية المناعية. بالإضافة إلى ذلك ، من خلال التحقيق في تأثيرات المركب باستخدام خلايا من أصل حيواني وبشري ، يمكن إنشاء بيانات لمقارنة الأنواع ، والتي يمكن استخدامها في نهج "متوازي الأضلاع" لتحسين عملية تقييم المخاطر. إذا كانت البيانات متاحة لثلاثة أحجار زاوية في متوازي الأضلاع (في الحيوان الحي ، وفي الحيوانات المختبرية والإنسان) ، فقد يكون من الأسهل التنبؤ بالنتيجة في حجر الزاوية المتبقي ، أي الخطر على البشر.
عندما يجب أن يعتمد تقييم مخاطر التثبيط المناعي الناجم عن المواد الكيميائية فقط على البيانات من الدراسات على الحيوانات ، يمكن اتباع نهج في الاستقراء للإنسان عن طريق تطبيق عوامل عدم اليقين على مستوى التأثير الضار غير الملحوظ (NOAEL). يمكن أن يعتمد هذا المستوى على معلمات محددة في النماذج ذات الصلة ، مثل فحوصات مقاومة المضيف والتقييم في الجسم الحي لتفاعلات فرط الحساسية وإنتاج الجسم المضاد. من الناحية المثالية ، تتطلب أهمية هذا النهج لتقييم المخاطر تأكيدًا من خلال الدراسات التي أجريت على البشر. يجب أن تجمع هذه الدراسات بين تحديد وقياس السمية والبيانات الوبائية وتقييمات الحالة المناعية.
للتنبؤ بفرط الحساسية التلامسية ، تتوفر نماذج لخنازير غينيا وقد تم استخدامها في تقييم المخاطر منذ السبعينيات. على الرغم من أن هذه الاختبارات حساسة وقابلة للتكرار ، إلا أن لها قيودًا لأنها تعتمد على التقييم الذاتي ؛ يمكن التغلب على هذا من خلال طرق أحدث وأكثر كمية تم تطويرها في الماوس. فيما يتعلق بفرط الحساسية الناتج عن المواد الكيميائية الناجم عن استنشاق أو ابتلاع المواد المسببة للحساسية ، يجب تطوير الاختبارات وتقييمها من حيث قيمتها التنبؤية في الإنسان. عندما يتعلق الأمر بتحديد مستويات التعرض المهني الآمن لمسببات الحساسية المحتملة ، يجب مراعاة الطبيعة ثنائية الطور للحساسية: مرحلة التحسس ومرحلة الاستثارة. التركيز المطلوب لإثارة رد فعل تحسسي لدى فرد حساس سابقًا أقل بكثير من التركيز اللازم للحث على التحسس لدى الفرد الساذج مناعيًا ولكنه حساس.
نظرًا لعدم وجود نماذج حيوانية للتنبؤ بالمناعة الذاتية الناتجة عن المواد الكيميائية ، يجب التركيز على تطوير مثل هذه النماذج. لتطوير مثل هذه النماذج ، يجب تطوير معرفتنا بالمناعة الذاتية التي تسببها المواد الكيميائية في البشر ، بما في ذلك دراسة العلامات الجينية وعلامات الجهاز المناعي لتحديد الأفراد المعرضين للإصابة. يقدم البشر الذين يتعرضون للعقاقير التي تحفز المناعة الذاتية مثل هذه الفرصة.