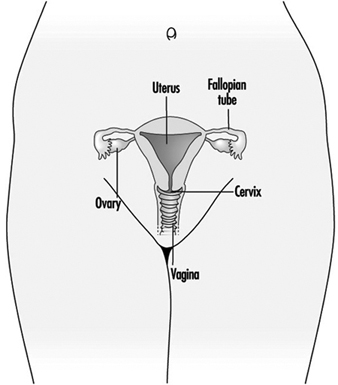
Figura 1. El aparato reproductor femenino.
El sistema reproductivo femenino está controlado por componentes del sistema nervioso central, incluidos el hipotálamo y la hipófisis. Está formado por los ovarios, las trompas de Falopio, el útero y la vagina (Figura 1). Los ovarios, las gónadas femeninas, son la fuente de ovocitos y también sintetizan y secretan estrógenos y progestágenos, las principales hormonas sexuales femeninas. Las trompas de Falopio transportan ovocitos y espermatozoides desde el útero. El útero es un órgano muscular en forma de pera, cuya parte superior se comunica a través de las trompas de Falopio con la cavidad abdominal, mientras que la parte inferior es contigua a través del estrecho canal del cuello uterino con la vagina, que pasa al exterior. La Tabla 1 resume los compuestos, las manifestaciones clínicas, el sitio y los mecanismos de acción de los posibles tóxicos para la reproducción.
Cuadro 1. Tóxicos potenciales para la reproducción femenina
| Compuesto | Manifestación clínica | Planta | Mecanismo/objetivo |
| Reaccion quimica | |||
| alquilante agentes |
menstruaciones alteradas Amenorrea atrofia ovárica Disminución de la fertilidad Menopausia prematura |
Ovario Útero |
Citotoxicidad de las células de la granulosa Citotoxicidad de ovocitos Citotoxicidad de células endometriales |
| Lidera | menstruaciones anormales atrofia ovárica Disminución de la fertilidad |
hipotálamo Pituitaria Ovario |
FSH disminuida Progesterona disminuida |
| Mercurio | menstruaciones anormales | hipotálamo Ovario |
Alteración de la producción y secreción de gonadotropinas Toxicidad folicular Proliferación de células de la granulosa |
| Cadmio | atresia folicular diestro persistente |
Ovario Pituitaria hipotálamo |
Toxicidad vascular Citotoxicidad de las células de la granulosa Citotoxicidad |
| similitud estructural | |||
| La azatioprina | Reducción del número de folículos | Ovario Ovogénesis |
Análogo de purina Interrupción de la síntesis de ADN/ARN |
| clordecona | Fertilidad deteriorada | hipotálamo | Agonista de estrógeno |
| DDT | menstruaciones alteradas | Pituitaria | Alteración de FSH, LH |
| 2,4-D | Esterilidad | ||
| Lindano | Amenorrea | ||
| Toxafeno | Hipermenorrea | ||
| PCB, PBB | menstruaciones anormales | Alteración de FSH, LH | |
Fuente: De Plowchalk, Meadows and Mattison 1992. Se sugiere que estos compuestos son tóxicos reproductivos de acción directa basados principalmente en pruebas de toxicidad en animales de experimentación.
El Hipotálamo y la Pituitaria
El hipotálamo se encuentra en el diencéfalo, que se asienta sobre el tronco encefálico y está rodeado por los hemisferios cerebrales. El hipotálamo es el principal intermediario entre los sistemas nervioso y endocrino, los dos principales sistemas de control del cuerpo. El hipotálamo regula la glándula pituitaria y la producción de hormonas.
Los mecanismos por los cuales una sustancia química puede alterar la función reproductiva del hipotálamo generalmente incluyen cualquier evento que pueda modificar la liberación pulsátil de la hormona liberadora de gonadotropina (GnRH). Esto puede implicar una alteración en la frecuencia o la amplitud de los pulsos de GnRH. Los procesos susceptibles de daño químico son los involucrados en la síntesis y secreción de GnRH, más específicamente, la transcripción o traducción, el empaquetamiento o transporte axonal y los mecanismos secretores. Estos procesos representan sitios donde los compuestos químicamente reactivos de acción directa podrían interferir con la síntesis hipotalámica o la liberación de GnRH. Una frecuencia o amplitud alterada de los pulsos de GnRH podría deberse a interrupciones en las vías de estimulación o inhibición que regulan la liberación de GnRH. Las investigaciones sobre la regulación del generador de pulsos de GnRH han demostrado que las catecolaminas, la dopamina, la serotonina, el ácido γ-aminobutírico y las endorfinas tienen cierto potencial para alterar la liberación de GnRH. Por lo tanto, los xenobióticos que son agonistas o antagonistas de estos compuestos podrían modificar la liberación de GnRH, interfiriendo así en la comunicación con la hipófisis.
La prolactina, la hormona estimulante del folículo (FSH) y la hormona luteinizante (LH) son tres hormonas proteicas secretadas por la pituitaria anterior que son esenciales para la reproducción. Estos juegan un papel fundamental en el mantenimiento del ciclo ovárico, controlando el reclutamiento y la maduración de los folículos, la esteroidogénesis, la finalización de la maduración del óvulo, la ovulación y la luteinización.
El control preciso y finamente ajustado del sistema reproductivo lo realiza la hipófisis anterior en respuesta a las señales de retroalimentación positivas y negativas de las gónadas. La liberación apropiada de FSH y LH durante el ciclo ovárico controla el desarrollo folicular normal, y la ausencia de estas hormonas es seguida por amenorrea y atrofia gonadal. Las gonadotropinas desempeñan un papel fundamental en el inicio de cambios en la morfología de los folículos ováricos y en sus microambientes esteroidales a través de la estimulación de la producción de esteroides y la inducción de poblaciones de receptores. La liberación oportuna y adecuada de estas gonadotropinas también es esencial para los eventos ovulatorios y una fase lútea funcional. Debido a que las gonadotropinas son esenciales para la función ovárica, la síntesis, el almacenamiento o la secreción alterados pueden alterar gravemente la capacidad reproductiva. La interferencia con la expresión génica, ya sea en la transcripción o la traducción, los eventos postraduccionales o el empaquetamiento o los mecanismos secretores, puede modificar el nivel de gonadotropinas que llegan a las gónadas. Las sustancias químicas que actúan por medio de la similitud estructural o la homeostasis endocrina alterada pueden producir efectos por interferencia con los mecanismos normales de retroalimentación. Los agonistas y antagonistas de los receptores de esteroides pueden iniciar una liberación inapropiada de gonadotropinas de la hipófisis, induciendo así enzimas metabolizadoras de esteroides, reduciendo la vida media de los esteroides y, posteriormente, el nivel circulante de esteroides que llega a la hipófisis.
el ovario
El ovario en los primates es responsable del control de la reproducción a través de sus principales productos, los ovocitos y las hormonas esteroides y proteicas. La foliculogénesis, que implica mecanismos reguladores tanto intraováricos como extraováricos, es el proceso mediante el cual se producen ovocitos y hormonas. El ovario en sí tiene tres subunidades funcionales: el folículo, el ovocito y el cuerpo lúteo. Durante el ciclo menstrual normal, estos componentes, bajo la influencia de la FSH y la LH, funcionan en conjunto para producir un óvulo viable para la fertilización y un entorno adecuado para la implantación y la gestación subsiguiente.
Durante el período preovulatorio del ciclo menstrual, el reclutamiento y el desarrollo de los folículos ocurren bajo la influencia de la FSH y la LH. Este último estimula la producción de andrógenos por las células de la teca, mientras que el primero estimula la aromatización de andrógenos en estrógenos por parte de las células de la granulosa y la producción de inhibina, una hormona proteica. La inhibina actúa en la pituitaria anterior para disminuir la liberación de FSH. Esto evita la estimulación excesiva del desarrollo folicular y permite el desarrollo continuo del folículo dominante, el folículo destinado a ovular. La producción de estrógeno aumenta, estimulando tanto el pico de LH (que da como resultado la ovulación) como los cambios celulares y secretores en la vagina, el cuello uterino, el útero y el oviducto que mejoran la viabilidad y el transporte de los espermatozoides.
En la fase postovulatoria, las células de la teca y la granulosa que quedan en la cavidad folicular del óvulo ovulado forman el cuerpo lúteo y secretan progesterona. Esta hormona estimula el útero para proporcionar un entorno adecuado para la implantación del embrión si se produce la fertilización. A diferencia de la gónada masculina, la gónada femenina tiene un número finito de células germinales al nacer y, por lo tanto, es excepcionalmente sensible a los tóxicos para la reproducción. Tal exposición de la mujer puede conducir a una disminución de la fecundidad, un aumento de los embarazos perdidos, una menopausia precoz o infertilidad.
Como unidad reproductiva básica del ovario, el folículo mantiene el delicado entorno hormonal necesario para apoyar el crecimiento y la maduración de un ovocito. Como se señaló anteriormente, este proceso complejo se conoce como foliculogénesis e involucra la regulación tanto intraovárica como extraovárica. Numerosos cambios morfológicos y bioquímicos ocurren a medida que un folículo primordial progresa a un folículo preovulatorio (que contiene un ovocito en desarrollo), y cada etapa del crecimiento folicular exhibe patrones únicos de sensibilidad a las gonadotropinas, producción de esteroides y vías de retroalimentación. Estas características sugieren que hay varios sitios disponibles para la interacción xenobiótica. Además, existen diferentes poblaciones de folículos dentro del ovario, lo que complica aún más la situación al permitir la toxicidad diferencial de los folículos. Esto crea una situación en la que los patrones de infertilidad inducidos por un agente químico dependerían del tipo de folículo afectado. Por ejemplo, la toxicidad de los folículos primordiales no produciría signos inmediatos de infertilidad pero, en última instancia, acortaría la vida reproductiva. Por otro lado, la toxicidad para los folículos antrales o preovulatorios daría como resultado una pérdida inmediata de la función reproductiva. El complejo folicular está compuesto por tres componentes básicos: las células de la granulosa, las células de la teca y el ovocito. Cada uno de estos componentes tiene características que pueden hacerlo especialmente susceptible a daños químicos.
Varios investigadores han explorado la metodología para la selección de xenobióticos para la toxicidad de las células de la granulosa mediante la medición de los efectos sobre la producción de progesterona por parte de las células de la granulosa en cultivo. La supresión con estradiol de la producción de progesterona por parte de las células de la granulosa se ha utilizado para verificar la capacidad de respuesta de las células de la granulosa. El pesticida p,p'-DDT y su isómero o,p'-DDT producen la supresión de la producción de progesterona aparentemente con potencias iguales a las del estradiol. Por el contrario, los pesticidas malatión, aratión y dieldrín y el fungicida hexaclorobenceno no tienen efecto. Se necesita un análisis más detallado de las respuestas de las células de la granulosa aisladas a los xenobióticos para definir la utilidad de este sistema de ensayo. El atractivo de los sistemas aislados como este es la economía y la facilidad de uso; sin embargo, es importante recordar que las células de la granulosa representan solo un componente del sistema reproductivo.
Las células de la teca proporcionan precursores de los esteroides sintetizados por las células de la granulosa. Se cree que las células de la teca se reclutan a partir de las células del estroma ovárico durante la formación y el crecimiento del folículo. El reclutamiento puede implicar proliferación celular del estroma así como migración a regiones alrededor del folículo. Los xenobióticos que alteran la proliferación, migración y comunicación celular tendrán un impacto en la función celular de la teca. Los xenobióticos que alteran la producción de andrógenos tecales también pueden afectar la función del folículo. Por ejemplo, las células de la teca proporcionan los andrógenos metabolizados a estrógenos por las células de la granulosa. Se espera que las alteraciones en la producción de andrógenos de las células de la teca, ya sea aumentos o disminuciones, tengan un efecto significativo en la función del folículo. Por ejemplo, se cree que la producción excesiva de andrógenos por parte de las células de la teca provocará atresia folicular. Además, la producción deficiente de andrógenos por parte de las células de la teca puede conducir a una disminución de la producción de estrógenos por parte de las células de la granulosa. Cualquiera de las circunstancias tendrá un impacto claro en el desempeño reproductivo. Actualmente, se sabe poco sobre la vulnerabilidad de las células tecales a los xenobióticos.
Aunque existe una gran cantidad de información que define la vulnerabilidad de las células ováricas a los xenobióticos, existen datos que demuestran claramente que dichos agentes pueden dañar o destruir los ovocitos. Los agentes alquilantes destruyen los ovocitos en humanos y animales de experimentación. El plomo produce toxicidad ovárica. El mercurio y el cadmio también producen daño ovárico que puede estar mediado por la toxicidad de los ovocitos.
Fertilización a la Implantación
La gametogénesis, la liberación y la unión de células germinales masculinas y femeninas son todos eventos preliminares que conducen a un cigoto. Los espermatozoides depositados en la vagina deben ingresar al cuello uterino y moverse a través del útero y hacia la trompa de Falopio para encontrarse con el óvulo. la penetración del óvulo por el esperma y la fusión de su respectivo ADN comprenden el proceso de fertilización. Después de la fecundación se inicia la división celular y continúa durante los siguientes tres o cuatro días, formando una masa sólida de células llamada mórula. Las células de la mórula continúan dividiéndose y, cuando el embrión en desarrollo llega al útero, es una bola hueca llamada blastocisto.
Después de la fertilización, el embrión en desarrollo migra a través de la trompa de Falopio hacia el útero. El blastocisto ingresa al útero y se implanta en el endometrio aproximadamente siete días después de la ovulación. En este momento el endometrio se encuentra en la fase postovulatoria. La implantación permite que el blastocisto absorba nutrientes o sustancias tóxicas de las glándulas y los vasos sanguíneos del endometrio.