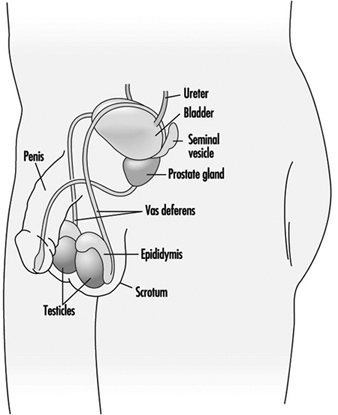
La spermatogenesi e la spermiogenesi sono i processi cellulari che producono cellule sessuali maschili mature. Questi processi hanno luogo all'interno dei tubuli seminiferi dei testicoli del maschio sessualmente maturo, come mostrato nella Figura 1. I tubuli seminiferi umani sono lunghi da 30 a 70 cm e hanno un diametro da 150 a 300 mm (Zaneveld 1978). Gli spermatogoni (cellule staminali) sono posti lungo la membrana basale dei tubuli seminiferi e sono le cellule base per la produzione dello sperma.
Figura 1. Il sistema riproduttivo maschile
Gli spermatozoi maturano attraverso una serie di divisioni cellulari in cui gli spermatogoni proliferano e diventano spermatociti primari. Gli spermatociti primari a riposo migrano attraverso giunzioni strette formate dalle cellule del Sertoli verso il lato luminale di questa barriera testicolare. Quando gli spermatociti raggiungono la barriera di membrana nel testicolo, la sintesi del DNA, il materiale genetico nel nucleo della cellula, è sostanzialmente completa. Quando gli spermatociti primari incontrano effettivamente il lume del tubulo seminifero, questi subiscono un particolare tipo di divisione cellulare che avviene solo nelle cellule germinali ed è nota come meiosi. La divisione cellulare meiotica provoca la scissione delle coppie di cromosomi nel nucleo, in modo che ogni cellula germinale risultante contenga solo una singola copia di ciascun filamento cromosomico anziché una coppia corrispondente.
Durante la meiosi i cromosomi cambiano forma condensandosi e diventando filamentosi. Ad un certo punto, la membrana nucleare che li circonda si rompe ei fusi microtubulari si attaccano alle coppie cromosomiche provocandone la separazione. Questo completa la prima divisione meiotica e si formano due spermatociti secondari aploidi. Gli spermatociti secondari subiscono quindi una seconda divisione meiotica per formare un numero uguale di cromosomi X e Y portatori di spermatidi.
La trasformazione morfologica degli spermatidi in spermatozoi è chiamata spermiogenesi. Quando la spermiogenesi è completa, ogni cellula spermatica viene rilasciata dalla cellula del Sertoli nel lume del tubulo seminifero mediante un processo denominato spermiogenesi. Gli spermatozoi migrano lungo il tubulo verso la rete testis e nella testa dell'epididimo. Gli spermatozoi che escono dai tubuli seminiferi sono immaturi: incapaci di fecondare un ovulo e incapaci di nuotare. Gli spermatozoi rilasciati nel lume del tubulo seminifero sono sospesi nel fluido pprodotto principalmente dalle cellule del Sertoli. Gli spermatozoi concentrati sospesi all'interno di questo fluido scorrono continuamente dai tubuli seminiferi, attraverso lievi cambiamenti nell'ambiente ionico all'interno della rete testis, attraverso i vasa efferentia e nell'epididimo. L'epididimo è un unico tubo molto arrotolato (da cinque a sei metri di lunghezza) in cui lo sperma trascorre da 12 a 21 giorni.
All'interno dell'epididimo, gli spermatozoi acquisiscono progressivamente motilità e capacità fecondante. Ciò può essere dovuto alla natura mutevole del fluido di sospensione nell'epididimo. Cioè, mentre le cellule maturano, l'epididimo assorbe i componenti dal fluido, comprese le secrezioni delle cellule di Sertoli (p. es., la proteina legante gli androgeni), aumentando così la concentrazione di spermatozoi. L'epididimo contribuisce anche con le proprie secrezioni al fluido di sospensione, comprese le sostanze chimiche glicerilfosforilcolina (GPC) e carnitina.
La morfologia degli spermatozoi continua a trasformarsi nell'epididimo. La gocciolina citoplasmatica viene eliminata e il nucleo dello sperma si condensa ulteriormente. Mentre l'epididimo è il principale serbatoio di stoccaggio per lo sperma fino all'eiaculazione, circa il 30% dello sperma in un eiaculato è stato immagazzinato nei vasi deferenti. L'eiaculazione frequente accelera il passaggio dello sperma attraverso l'epididimo e può aumentare il numero di spermatozoi immaturi (infertili) nell'eiaculato (Zaneveld 1978).
Eiaculazione
Una volta all'interno del dotto deferente, gli spermatozoi vengono trasportati dalle contrazioni muscolari dell'eiaculazione piuttosto che dal flusso del fluido. Durante l'eiaculazione, i fluidi vengono espulsi con la forza dalle ghiandole sessuali accessorie dando origine al plasma seminale. Queste ghiandole non espellono le loro secrezioni contemporaneamente. Piuttosto, la ghiandola bulbouretrale (di Cowper) prima espelle un fluido chiaro, seguito dalle secrezioni prostatiche, dai fluidi concentrati di spermatozoi dagli epididimi e dall'ampolla dei vasi deferenti, e infine dalla frazione più grande principalmente dalle vescicole seminali. Pertanto, il plasma seminale non è un fluido omogeneo.
Azioni tossiche su spermatogenesi e spermiogenesi
Le sostanze tossiche possono interrompere la spermatogenesi in diversi punti. I più dannosi, a causa dell'irreversibilità, sono i tossici che uccidono o alterano geneticamente (oltre i meccanismi di riparazione) gli spermatogoni o le cellule del Sertoli. Gli studi sugli animali sono stati utili per determinare lo stadio in cui una sostanza tossica attacca il processo spermatogenico. Questi studi impiegano l'esposizione a breve termine a una sostanza tossica prima del campionamento per determinare l'effetto. Conoscendo la durata di ogni stadio spermatogenico, è possibile estrapolare per stimare lo stadio interessato.
L'analisi biochimica del plasma seminale fornisce informazioni sulla funzione delle ghiandole sessuali accessorie. Le sostanze chimiche secrete principalmente da ciascuna delle ghiandole sessuali accessorie sono tipicamente selezionate per fungere da marker per ciascuna rispettiva ghiandola. Ad esempio, l'epididimo è rappresentato dal GPC, le vescicole seminali dal fruttosio e la ghiandola prostatica dallo zinco. Si noti che questo tipo di analisi fornisce solo informazioni grossolane sulla funzione ghiandolare e poche o nessuna informazione sugli altri costituenti secretori. La misurazione del pH e dell'osmolalità del seme fornisce ulteriori informazioni generali sulla natura del plasma seminale.
Il plasma seminale può essere analizzato per la presenza di una sostanza tossica o del suo metabolita. I metalli pesanti sono stati rilevati nel plasma seminale mediante spettrofotometria di assorbimento atomico, mentre gli idrocarburi alogenati sono stati misurati nel liquido seminale mediante gascromatografia dopo estrazione o filtrazione con limitazione delle proteine (Stachel et al. 1989; Zikarge 1986).
La vitalità e la motilità degli spermatozoi nel plasma seminale è tipicamente un riflesso della qualità del plasma seminale. Alterazioni della vitalità degli spermatozoi, misurate mediante esclusione della colorazione o gonfiore ipoosmotico, o alterazioni dei parametri di motilità degli spermatozoi suggerirebbero effetti tossici post-testicolari.
Le analisi del seme possono anche indicare se la produzione di spermatozoi è stata influenzata da una sostanza tossica. La conta degli spermatozoi e la morfologia degli spermatozoi forniscono indici dell'integrità della spermatogenesi e della spermiogenesi. Pertanto, il numero di spermatozoi nell'eiaculato è direttamente correlato al numero di cellule germinali per grammo di testicolo (Zukerman et al. 1978), mentre la morfologia anormale è probabilmente il risultato di una spermiogenesi anomala. Gli spermatozoi morti o immobili riflettono spesso gli effetti di eventi post-testicolari. Pertanto, il tipo o la tempistica di un effetto tossico può indicare l'obiettivo del tossico. Ad esempio, l'esposizione di ratti maschi al 2-metossietanolo ha provocato una riduzione della fertilità dopo quattro settimane (Chapin et al. 1985). Questa evidenza, corroborata dall'esame istologico, indica che il bersaglio della tossicità è lo spermatocita (Chapin et al. 1984). Sebbene non sia etico esporre intenzionalmente gli esseri umani a sospette sostanze tossiche per la riproduzione, le analisi del seme di eiaculati seriali di uomini inavvertitamente esposti per un breve periodo a potenziali sostanze tossiche possono fornire informazioni utili simili.
L'esposizione occupazionale all'1,2-dibromocloropropano (DBCP) ha ridotto la concentrazione di spermatozoi negli eiaculati da una mediana di 79 milioni di cellule/ml negli uomini non esposti a 46 milioni di cellule/ml nei lavoratori esposti (Whorton et al. 1979). Dopo aver rimosso i lavoratori dall'esposizione, quelli con conta spermatica ridotta hanno sperimentato un recupero parziale, mentre gli uomini che erano stati azoospermici sono rimasti sterili. La biopsia testicolare ha rivelato che l'obiettivo del DBCP era la spermatogonia. Ciò conferma la gravità dell'effetto quando le cellule staminali sono il bersaglio di sostanze tossiche. Non c'erano indicazioni che l'esposizione al DBCP degli uomini fosse associata a esiti avversi della gravidanza (Potashnik e Abeliovich 1985). Un altro esempio di sostanza tossica mirata alla spermatogenesi/spermiogenesi è stato lo studio dei lavoratori esposti all'etilene dibromuro (EDB). Avevano più spermatozoi con teste affusolate e meno spermatozoi per eiaculato rispetto ai controlli (Ratcliffe et al. 1987).
Il danno genetico è difficile da rilevare nello sperma umano. Diversi studi sugli animali che utilizzano il dosaggio letale dominante (Ehling et al. 1978) indicano che l'esposizione paterna può produrre un esito avverso della gravidanza. Studi epidemiologici su vaste popolazioni hanno dimostrato una maggiore frequenza di aborti spontanei nelle donne i cui mariti lavoravano come meccanici di autoveicoli (McDonald et al. 1989). Tali studi indicano la necessità di metodi per rilevare danni genetici nello sperma umano. Tali metodi sono in fase di sviluppo da diversi laboratori. Questi metodi includono sonde del DNA per discernere mutazioni genetiche (Hecht 1987), cariotipo del cromosoma spermatico (Martin 1983) e valutazione della stabilità del DNA mediante citometria a flusso (Evenson 1986).
Figura 2. Esposizioni positivamente associate a effetti negativi sulla qualità del seme
La figura 2 elenca le esposizioni note per influenzare la qualità dello sperma e la tabella 1 fornisce un riepilogo dei risultati degli studi epidemiologici sugli effetti paterni sugli esiti riproduttivi.
Tabella 1. Studi epidemiologici sugli effetti paterni sull'esito della gravidanza
| Riferimento | Tipo di esposizione o occupazione | Associazione con l'esposizione1 | Entourage |
| Studi di popolazione basati su record | |||
| Lindbohm et al. 1984 | solventi | - | Aborto spontaneo |
| Lindbohm et al. 1984 | Stazione di servizio | + | Aborto spontaneo |
| Daniell e Vaughan 1988 | Solventi organici | - | Aborto spontaneo |
| McDonald et al. 1989 | Meccanica | + | Aborto spontaneo |
| McDonald et al. 1989 | Alimentare | + | Difetti dello sviluppo |
| Lindbohm et al. 1991a | Ossido di etilene | + | Aborto spontaneo |
| Lindbohm et al. 1991a | Raffineria di petrolio | + | Aborto spontaneo |
| Lindbohm et al. 1991a | Impregnati di legno | + | Aborto spontaneo |
| Lindbohm et al. 1991a | Prodotti chimici per la gomma | + | Aborto spontaneo |
| Olsen et al. 1991 | metalli | + | Rischio di cancro infantile |
| Olsen et al. 1991 | macchinisti | + | Rischio di cancro infantile |
| Olsen et al. 1991 | Smiths | + | Rischio di cancro infantile |
| Kristensen et al. 1993 | solventi | + | Nascita prematura |
| Kristensen et al. 1993 | Piombo e solventi | + | Nascita prematura |
| Kristensen et al. 1993 | Portare | + | Morte perinatale |
| Kristensen et al. 1993 | Portare | + | Morbilità del bambino maschio |
| Studi caso-controllo | |||
| Kucera 1968 | Industria della stampa | (+) | Labbro leporino |
| Kucera 1968 | Verniciatura | (+) | Palato leporino |
| Olsen 1983 | Verniciatura | + | Danni al sistema nervoso centrale |
| Olsen 1983 | solventi | (+) | Danni al sistema nervoso centrale |
| Sever et al. 1988 | Radiazioni di basso livello | + | Difetti del tubo neurale |
| Taskinen et al. 1989 | Solventi organici | + | Aborto spontaneo |
| Taskinen et al. 1989 | Idrocarburi aromatici | + | Aborto spontaneo |
| Taskinen et al. 1989 | Polvere | + | Aborto spontaneo |
| Gardner et al. 1990 | Radiazione | + | Leucemia infantile |
| Bonde1992 | Saldatura | + | Tempo al concepimento |
| Wilkins e affonda 1990 | Agricoltura | (+) | Tumore al cervello infantile |
| Wilkins e affonda 1990 | Edilizia | (+) | Tumore al cervello infantile |
| Wilkins e affonda 1990 | Lavorazione alimentare/tabacco | (+) | Tumore al cervello infantile |
| Wilkins e affonda 1990 | Metallo | + | Tumore al cervello infantile |
| Lindbohmn et al. 1991 b | Portare | (+) | Aborto spontaneo |
| Salman et al. 1992 | Portare | (+) | Difetti congeniti |
| Veulemans et al. 1993 | Etere di glicole etilenico | + | Spermiogramma anormale |
| Chia et al. 1992 | metalli | + | Cadmio nello sperma |
1 – nessuna associazione significativa; (+) associazione marginalmente significativa; + associazione significativa.
Fonte: adattato da Taskinen 1993.
Sistema neuroendocrino
Il funzionamento complessivo del sistema riproduttivo è controllato dal sistema nervoso e dagli ormoni prodotti dalle ghiandole (il sistema endocrino). L'asse neuroendocrino riproduttivo del maschio coinvolge principalmente il sistema nervoso centrale (SNC), la ghiandola pituitaria anteriore ei testicoli. Gli input dal SNC e dalla periferia sono integrati dall'ipotalamo, che regola direttamente la secrezione delle gonadotropine da parte della ghiandola pituitaria anteriore. Le gonadotropine, a loro volta, agiscono principalmente sulle cellule di Leydig all'interno dell'interstizio e sulle cellule di Sertoli e germinali all'interno dei tubuli seminiferi per regolare la spermatogenesi e la produzione di ormoni da parte dei testicoli.
Asse ipotalamo-ipofisi
L'ipotalamo secerne il neurormone che rilascia l'ormone di rilascio della gonadotropina (GnRH) nel sistema vascolare portale ipofisario per il trasporto alla ghiandola pituitaria anteriore. La secrezione pulsatile di questo decapeptide provoca il rilascio concomitante dell'ormone luteinizzante (LH), e con minore sincronia e un quinto della potenza, il rilascio dell'ormone follicolo-stimolante (FSH) (Bardin 1986). Esistono prove sostanziali a sostegno della presenza di un ormone di rilascio di FSH separato, sebbene nessuno sia stato ancora isolato (Savy-Moore e Schwartz 1980; Culler e Negro-Vilar 1986). Questi ormoni sono secreti dalla ghiandola pituitaria anteriore. LH agisce direttamente sulle cellule di Leydig per stimolare la sintesi e il rilascio di testosterone, mentre l'FSH stimola l'aromatizzazione del testosterone in estradiolo da parte delle cellule di Sertoli. La stimolazione gonadotropica provoca il rilascio di questi ormoni steroidei nella vena spermatica.
La secrezione di gonadotropine è, a sua volta, controllata dal testosterone e dall'estradiolo attraverso meccanismi di feedback negativo. Il testosterone agisce principalmente sull'ipotalamo per regolare la secrezione di GnRH e quindi riduce la frequenza degli impulsi, principalmente, del rilascio di LH. L'estradiolo, d'altra parte, agisce sulla ghiandola pituitaria per ridurre l'entità del rilascio di gonadotropine. Attraverso questi cicli di feedback endocrini, la funzione testicolare in generale e la secrezione di testosterone in particolare vengono mantenute a uno stato relativamente stabile.
Asse pituitario-testicolare
LH e FSH sono generalmente considerati necessari per la normale spermatogenesi. Presumibilmente l'effetto dell'LH è secondario all'induzione di alte concentrazioni intratesticolari di testosterone. Pertanto, l'FSH della ghiandola pituitaria e il testosterone delle cellule di Leydig agiscono sulle cellule del Sertoli all'interno dell'epitelio del tubulo seminifero per avviare la spermatogenesi. La produzione di spermatozoi persiste, anche se quantitativamente ridotta, dopo aver rimosso l'LH (e presumibilmente le alte concentrazioni intratesticolari di testosterone) o l'FSH. L'FSH è necessario per iniziare la spermatogenesi alla pubertà e, in misura minore, per riavviare la spermatogenesi che è stata arrestata (Matsumoto 1989; Sharpe 1989).
Il sinergismo ormonale che serve a mantenere la spermatogenesi può comportare il reclutamento da parte dell'FSH di spermatogoni differenziati per entrare nella meiosi, mentre il testosterone può controllare specifici stadi successivi della spermatogenesi. FSH e testosterone possono anche agire sulla cellula del Sertoli per stimolare la produzione di uno o più fattori paracrini che possono influenzare il numero di cellule di Leydig e la produzione di testosterone da parte di queste cellule (Sharpe 1989). L'FSH e il testosterone stimolano la sintesi proteica da parte delle cellule del Sertoli, inclusa la sintesi della proteina legante gli androgeni (ABP), mentre l'FSH da solo stimola la sintesi dell'aromatasi e dell'inibina. L'ABP è secreto principalmente nel liquido tubulare seminifero ed è trasportato nella porzione prossimale dell'epididimo caput, probabilmente fungendo da trasportatore locale di androgeni (Bardin 1986). L'aromatasi catalizza la conversione del testosterone in estradiolo nelle cellule del Sertoli e in altri tessuti periferici.
L'inibina è una glicoproteina costituita da due subunità dissimili legate al disolfuro, a e b. Sebbene l'inibina preferenzialmente inibisca il rilascio di FSH, può anche attenuare il rilascio di LH in presenza di stimolazione con GnRH (Kotsugi et al. 1988). FSH e LH stimolano il rilascio di inibina con potenza approssimativamente uguale (McLachlan et al. 1988). È interessante notare che l'inibina viene secreta nel sangue della vena spermatica sotto forma di impulsi sincroni a quelli del testosterone (Winters 1990). Questo probabilmente non riflette le azioni dirette dell'LH o del testosterone sull'attività delle cellule del Sertoli, ma piuttosto gli effetti di altri prodotti delle cellule di Leydig secreti negli spazi interstiziali o nella circolazione.
La prolattina, anch'essa secreta dalla ghiandola pituitaria anteriore, agisce in sinergia con LH e testosterone per promuovere la funzione riproduttiva maschile. La prolattina si lega a recettori specifici sulla cellula di Leydig e aumenta la quantità di complesso del recettore degli androgeni all'interno del nucleo dei tessuti sensibili agli androgeni (Baker et al. 1977). L'iperprolattinemia è associata alla riduzione delle dimensioni dei testicoli e della prostata, del volume del seme e delle concentrazioni circolanti di LH e testosterone (Segal et al. 1979). L'iperprolattinemia è stata anche associata all'impotenza, apparentemente indipendente dall'alterazione della secrezione di testosterone (Torner et al. 1977).
Se si misurano i metaboliti degli ormoni steroidei nelle urine, è necessario considerare la possibilità che l'esposizione studiata possa alterare il metabolismo dei metaboliti escreti. Ciò è particolarmente pertinente poiché la maggior parte dei metaboliti è formata dal fegato, bersaglio di molte sostanze tossiche. Il piombo, ad esempio, riduceva la quantità di steroidi solfatati escreti nelle urine (Apostoli et al. 1989). I livelli ematici di entrambe le gonadotropine diventano elevati durante il sonno quando il maschio entra nella pubertà, mentre i livelli di testosterone mantengono questo schema diurno durante l'età adulta negli uomini (Plant 1988). Pertanto, i campioni di sangue, urina o saliva dovrebbero essere raccolti approssimativamente alla stessa ora del giorno per evitare variazioni dovute ai pattern di secrezione diurna.
È molto probabile che gli effetti palesi dell'esposizione tossica che colpisce il sistema neuroendocrino riproduttivo vengano rivelati attraverso manifestazioni biologiche alterate degli androgeni. Le manifestazioni significativamente regolate dagli androgeni nell'uomo adulto che possono essere rilevate durante un esame fisico di base includono: (1) ritenzione di azoto e sviluppo muscolare; (2) mantenimento dei genitali esterni e degli organi sessuali accessori; (3) mantenimento della laringe allargata e delle corde vocali ispessite che causano la voce maschile; (4) barba, crescita dei peli ascellari e pubici e recessione temporale dei peli e calvizie; (5) libido e prestazioni sessuali; (6) proteine organo-specifiche nei tessuti (ad es. fegato, reni, ghiandole salivari); e (7) comportamento aggressivo (Bardin 1986). Le modifiche in uno qualsiasi di questi tratti possono indicare che la produzione di androgeni è stata influenzata.
Esempi di effetti tossici
Il piombo è un classico esempio di sostanza tossica che colpisce direttamente il sistema neuroendocrino. Le concentrazioni sieriche di LH erano elevate negli uomini esposti al piombo per meno di un anno. Questo effetto non è progredito negli uomini esposti per più di cinque anni. I livelli sierici di FSH non sono stati influenzati. D'altra parte, i livelli sierici di ABP erano elevati e quelli del testosterone totale erano ridotti negli uomini esposti al piombo per più di cinque anni. I livelli sierici di testosterone libero erano significativamente ridotti dopo l'esposizione al piombo per tre-cinque anni (Rodamilans et al. 1988). Al contrario, le concentrazioni sieriche di LH, FSH, testosterone totale, prolattina e 17-chetosteroidi neutri totali non erano alterate nei lavoratori con livelli circolanti inferiori di piombo, anche se la frequenza di distribuzione del numero di spermatozoi era alterata (Assennato et al. 1986). .
Anche l'esposizione dei pittori dei cantieri navali al 2-etossietanolo ha ridotto il numero di spermatozoi senza un concomitante cambiamento nelle concentrazioni sieriche di LH, FSH o testosterone (Welch et al. 1988). Pertanto, le sostanze tossiche possono influenzare la produzione di ormoni e le misure dello sperma in modo indipendente.
I lavoratori di sesso maschile coinvolti nella produzione del nematocida DBCP hanno sperimentato livelli sierici elevati di LH e FSH e riduzione del numero di spermatozoi e della fertilità. Questi effetti sono apparentemente sequele delle azioni del DBCP sulle cellule di Leydig per alterare la produzione o l'azione degli androgeni (Mattison et al. 1990).
Diversi composti possono esercitare tossicità in virtù della somiglianza strutturale con gli ormoni steroidei riproduttivi. Pertanto, legandosi al rispettivo recettore endocrino, le sostanze tossiche possono agire come agonisti o antagonisti per interrompere le risposte biologiche. Clordecone (Kepone), un insetticida che si lega ai recettori degli estrogeni, riduce il numero e la motilità degli spermatozoi, arresta la maturazione degli spermatozoi e riduce la libido. Sebbene sia allettante suggerire che questi effetti derivino dall'interferenza del clordecone con le azioni degli estrogeni a livello neuroendocrino o testicolare, in questi studi non è stato dimostrato che i livelli sierici di testosterone, LH e FSH siano alterati in modo simile agli effetti della terapia con estradiolo. . Anche il DDT ei suoi metaboliti presentano proprietà steroidee e ci si potrebbe aspettare che alterino la funzione riproduttiva maschile interferendo con le funzioni degli ormoni steroidei. Gli xenobiotici come i bifenili policlorurati, i bifenili polibromurati e i pesticidi organoclorurati possono anche interferire con le funzioni riproduttive maschili esercitando attività estrogenica agonista/antagonista (Mattison et al. 1990).
Funzione sessuale
La funzione sessuale umana si riferisce alle attività integrate dei testicoli e delle ghiandole sessuali secondarie, ai sistemi di controllo endocrino e alle componenti comportamentali e psicologiche della riproduzione (libido) basate sul sistema nervoso centrale. Erezione, eiaculazione e orgasmo sono tre eventi distinti, indipendenti, fisiologici e psicodinamici che normalmente si verificano contemporaneamente negli uomini.
Sono disponibili pochi dati affidabili sugli effetti dell'esposizione professionale sulla funzione sessuale a causa dei problemi sopra descritti. È stato dimostrato che le droghe influenzano ciascuno dei tre stadi della funzione sessuale maschile (Fabro 1985), indicando la possibilità che le esposizioni professionali esercitino effetti simili. Gli antidepressivi, gli antagonisti del testosterone e gli stimolanti del rilascio di prolattina riducono efficacemente la libido negli uomini. I farmaci antiipertensivi che agiscono sul sistema nervoso simpatico inducono impotenza in alcuni uomini, ma sorprendentemente priapismo in altri. La fenossibenzamina, un antagonista adrenocettivo, è stata utilizzata clinicamente per bloccare l'emissione seminale ma non l'orgasmo (Shilon, Paz e Homonnai 1984). I farmaci antidepressivi anticolinergici consentono l'emissione seminale mentre bloccano l'espulsione seminale e l'orgasmo, il che si traduce in una fuoriuscita di plasma seminale dall'uretra piuttosto che essere espulso.
Le droghe ricreative influenzano anche la funzione sessuale (Fabro 1985). L'etanolo può ridurre l'impotenza aumentando la libido. Cocaina, eroina e alte dosi di cannabinoidi riducono la libido. Gli oppiacei ritardano o compromettono anche l'eiaculazione.
La vasta e variegata gamma di prodotti farmaceutici che hanno dimostrato di influenzare il sistema riproduttivo maschile fornisce supporto all'idea che le sostanze chimiche trovate sul posto di lavoro possano anche essere tossiche per la riproduzione. Per valutare questa importante area della tossicologia riproduttiva sono necessari metodi di ricerca affidabili e pratici per le condizioni di studio sul campo.