Poco dopo la fine della prima guerra mondiale, mentre svolgeva ricerche per trovare un materiale in grado di sostituire il diamante negli ugelli di trafilatura dei metalli, Karl Schoeter brevettò a Berlino un processo di sinterizzazione (pressurizzazione più riscaldamento a 1,500°C) di una miscela di tungsteno fine polvere di carburo (WC) con il 10% di cobalto per produrre “metallo duro”. Le caratteristiche principali di questo agglomerato sono l'estrema durezza, solo di poco inferiore a quella del diamante, e il mantenimento delle sue proprietà meccaniche alle alte temperature; queste caratteristiche lo rendono idoneo all'impiego nella trafilatura dei metalli, per inserti saldati, e per utensili ad alta velocità per la lavorazione di metalli, pietra, legno e materiali con elevata resistenza all'usura o al calore, in campo meccanico, aeronautico e balistico. L'uso del metallo duro è in continua espansione in tutto il mondo. Nel 1927 Krupp estese l'uso del metallo duro nel campo degli utensili da taglio, chiamandolo “Widia” (come Diamant—come diamante), un nome ancora in uso oggi.
La sinterizzazione rimane la base di tutta la produzione di metallo duro: le tecniche sono migliorate dall'introduzione di altri carburi metallici - carburo di titanio (TiC) e carburo di tantalio (TaC) - e dal trattamento di parti in metallo duro per inserti da taglio mobili con uno o più strati di nitruro di titanio o ossido di alluminio e di altri composti molto duri applicati con deposizione chimica da fase vapore (CVD) o deposizione fisica da fase vapore (PVD). Gli inserti fissi saldati agli utensili non possono essere placcati, ma vengono ripetutamente affilati da una mola diamantata (figure 1 e 2).
Figura 1. (A) Esempi di alcuni inserti mobili trafilati in metallo duro, rivestiti con nitruro di tungsteno giallo oro; (B) inserto saldato all'utensile e lavorante in trafilato di acciaio.
Figura 2. Inserti fissi saldati a (A) punta per pietra e (B) disco per sega.
Il metallo duro sinterizzato è formato da particelle di carburi metallici inglobate in una matrice formata da cobalto, che fonde durante la sinterizzazione, interagendo e occupando gli interstizi. Il cobalto è quindi il materiale collante della struttura, che assume caratteristiche metallo-ceramiche (figure 3, 4 e 5).
Figura 3. Microstruttura di una sinterizzazione WC/Co; Le particelle di WC sono incorporate nella matrice Co light (1,500x).
Figura 4. Microstruttura di una sinterizzazione WC + TiC + TaC + Co. Insieme alle particelle prismatiche WC, si osservano particelle globulari formate da una soluzione solida di TiC + TaC. La matrice di luce è formata da Co (1,500x).
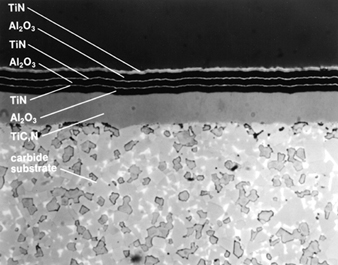
Figura 5. Microstruttura di sinterizzazione placcata da più strati molto duri (2,000x).
Il processo di sinterizzazione utilizza polveri finissime di carburo metallico (diametri medi da 1 a 9μm) e polveri di cobalto (diametro medio da 1 a 4μm) che vengono miscelate, trattate con soluzione di paraffina, pressate in stampo, decerate a bassa temperatura, pre- sinterizzato a 700-750°C e sinterizzato a 1,500°C (Brookes 1992).
Quando la sinterizzazione viene effettuata con metodi inadeguati, tecniche improprie e scarsa igiene industriale, le polveri possono inquinare l'atmosfera dell'ambiente di lavoro: i lavoratori sono quindi esposti al rischio di inalazione di polveri di carburi metallici e polveri di cobalto. Oltre al processo primario esistono altre attività che possono esporre i lavoratori al rischio di inalazione di aerosol di metallo duro. L'affilatura degli inserti fissi saldati agli utensili viene normalmente effettuata mediante molatura diamantata a secco o, più frequentemente, raffreddata con liquidi di varia natura, producendo polveri o nebbie formate da piccolissime gocce contenenti particelle metalliche. Particelle di metallo duro sono utilizzate anche nella produzione di uno strato ad alta resistenza su superfici in acciaio soggette ad usura, applicate attraverso metodi (processo di rivestimento al plasma e altri) basati sulla combinazione di uno spruzzo di polvere con un arco elettrico o un'esplosione controllata di una miscela di gas ad alta temperatura. L'arco elettrico o il flusso esplosivo del gas determina la fusione delle particelle metalliche e il loro impatto sulla superficie da placcare.
Le prime osservazioni sulle "malattie da metalli duri" furono descritte in Germania negli anni '1940. Hanno riportato una fibrosi polmonare diffusa e progressiva, chiamata Hartmetallungenfibrose. Durante i successivi 20 anni sono stati osservati e descritti casi paralleli in tutti i paesi industriali. I lavoratori interessati erano nella maggior parte dei casi responsabili della sinterizzazione. Dal 1970 ad oggi, diversi studi indicano che la patologia all'apparato respiratorio è causata dall'inalazione di particelle di metallo duro. Colpisce solo i soggetti predisposti, e si compone dei seguenti sintomi:
- acuto: rinite, asma
- subacuta: alveolite fibrosa
- cronico: fibrosi interstiziale diffusa e progressiva.
Colpisce non solo gli addetti alla sinterizzazione, ma chiunque inali aerosol contenenti metalli duri e in particolare cobalto. È causato principalmente e forse esclusivamente dal cobalto.
La definizione di malattia da metalli duri comprende oggi un gruppo di patologie dell'apparato respiratorio, diverse tra loro per gravità clinica e prognosi, ma accomunate da una variabile reattività individuale al fattore eziologico cobalto.
Più recenti informazioni epidemiologiche e sperimentali concordano sul ruolo causale del cobalto per i sintomi acuti delle prime vie respiratorie (riniti, asma) e per i sintomi subacuti e cronici del parenchima bronchiale (alveolite fibrosante e fibrosi interstiziale cronica).
Il meccanismo patogenetico si basa sull'induzione da parte del Co di una immunoreazione ipersensibile: infatti solo alcuni dei soggetti presentano patologie dopo brevi esposizioni a concentrazioni relativamente basse, o anche dopo esposizioni più lunghe e intense. Le concentrazioni di co nei campioni biologici (sangue, urine, pelle) non sono significativamente differenti in chi ha la patologia e chi no; non c'è correlazione tra dose e risposta a livello tissutale; sono stati individuati anticorpi specifici (immunoglobine IgE e IgG) contro un composto della Co-albumina negli asmatici, e il patch test del Co è positivo nei soggetti con alveolite o fibrosi; gli aspetti citologici dell'alveolite a cellule giganti sono compatibili con l'immunoreazione ei sintomi acuti o subacuti tendono a regredire quando i soggetti vengono allontanati dall'esposizione al Co (Parkes 1994).
La base immunologica dell'ipersensibilità al Co non è stata ancora spiegata in modo soddisfacente; non è possibile, quindi, identificare un marcatore affidabile di suscettibilità individuale.
Patologie identiche a quelle riscontrate nei soggetti esposti a metalli duri sono state osservate anche nei tagliatori di diamanti, che utilizzano dischi formati da microdiamanti cementati con Co e che quindi inalano solo Co e particelle di diamante.
Non è ancora del tutto dimostrato che il Co puro (escluse tutte le altre particelle inalate) sia in grado da solo di produrre le patologie e soprattutto la fibrosi interstiziale diffusa: le particelle inalate con il Co potrebbero avere un effetto sinergico oltre che modulante. Studi sperimentali sembrano dimostrare che la reattività biologica ad una miscela di particelle di Co e di tungsteno è maggiore di quella provocata dal solo Co, e non si riscontrano patologie significative negli addetti alla produzione di polvere di Co puro (Science of Ambiente totale 1994).
I sintomi clinici della malattia da metalli duri, che, sulla base delle attuali conoscenze eziopatogenetiche, dovrebbero più precisamente essere definiti “malattia del cobalto”, sono, come accennato in precedenza, acuti, subacuti e cronici.
I sintomi acuti comprendono una specifica irritazione respiratoria (rinite, laringo-tracheite, edema polmonare) causata dall'esposizione ad alte concentrazioni di polvere di Co o fumo di Co; sono osservabili solo in casi eccezionali. L'asma è osservato più frequentemente. Compare dal 5 al 10% dei lavoratori esposti a concentrazioni di cobalto di 0.05 mg/m3, l'attuale valore limite di soglia (TLV) statunitense. I sintomi di costrizione toracica con dispnea e tosse tendono a comparire alla fine del turno di lavoro o durante la notte. La diagnosi di asma bronchiale allergico professionale da cobalto può essere sospettata sulla base di criteri anamnestici, ma è confermata da uno specifico test di stimolazione bronchiale che determina la comparsa di una risposta broncospastica immediata, ritardata o duale. Anche i test di capacità respiratoria effettuati all'inizio e alla fine del turno di lavoro possono aiutare la diagnosi. I sintomi asmatici dovuti al cobalto tendono a scomparire quando il soggetto viene allontanato dall'esposizione, ma, analogamente a tutte le altre forme di asma allergico professionale, i sintomi possono diventare cronici e irreversibili quando l'esposizione si protrae per lungo tempo (anni), nonostante la presenza di disturbi respiratori. I soggetti fortemente broncoreattivi possono presentare sintomi asmatici eziologici non allergici, con risposta aspecifica all'inalazione di cobalto e altre polveri irritanti. In un'alta percentuale di casi con asma bronchiale allergico, è stata riscontrata nel siero IgE una reazione specifica verso un composto di Co-sieroalbumina umana. Il reperto radiologico non varia: solo in rari casi si possono riscontrare forme miste di asma più alveolite con alterazione radiologica specificatamente causata da alveolite. La terapia broncodilatatoria, insieme ad un'immediata esposizione al termine dell'attività lavorativa, porta alla completa guarigione per i casi di recente insorgenza, non ancora cronici.
I sintomi subacuti e cronici comprendono l'alveolite fibrosa e la fibrosi interstiziale cronica diffusa e progressiva (DIPF). L'esperienza clinica sembra indicare che il passaggio dall'alveolite alla fibrosi interstiziale è un processo che evolve gradualmente e lentamente nel tempo: si possono riscontrare casi di alveolite iniziale pura reversibili con sospensione dall'esposizione più terapia con corticosteroidi; oppure casi con componente fibrotica già presente, che possono migliorare ma non raggiungere la completa guarigione togliendo il soggetto dall'esposizione, anche con terapia aggiuntiva; e, infine, i casi in cui la situazione predominante è quella di un DIPF irreversibile. L'incidenza di tali casi è bassa nei lavoratori esposti, molto inferiore alla percentuale di casi di asma allergico.
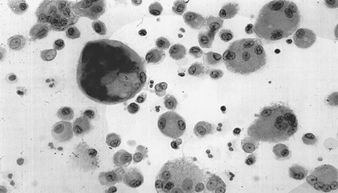
L'alveolite è oggi facilmente studiabile nelle sue componenti citologiche attraverso il lavaggio bronco-alveolare (BAL); è caratterizzato da un forte aumento del numero totale di cellule, formate principalmente da macrofagi, con numerose cellule giganti multinucleari e dal tipico aspetto di cellule giganti da corpo estraneo contenenti a volte cellule citoplasmatiche (figura 6); è frequente anche un aumento assoluto o relativo dei linfociti, con diminuzione del rapporto CD4/CD8, associato ad un forte aumento degli eosinofili e dei mastociti. Raramente l'alveolite è prevalentemente linfocitaria, con rapporto CD4/CD8 invertito, come avviene nelle pneumopatie da ipersensibilità.
Figura 6. BAL citologico in un caso di alveolite cellulare gigante mononucleare macrofagica causata da metallo duro. Tra i macrofagi mononucleari e il linfocita si osserva un tipo di cellula gigante da corpo estraneo (400x).
I soggetti con alveolite riferiscono dispnea associata a stanchezza, perdita di peso e tosse secca. Crepitazione è presente nel polmone inferiore con alterazione funzionale di tipo restrittivo e diffusa opacità radiologica rotonda o irregolare. Il patch test per il cobalto è positivo nella maggior parte dei casi. Nei soggetti predisposti l'alveolite si manifesta dopo un periodo relativamente breve di esposizione lavorativa, di uno o pochi anni. Nelle sue fasi iniziali questa forma è reversibile fino alla completa guarigione con la semplice rimozione dall'esposizione, con risultati migliori se abbinata alla terapia con cortisone.
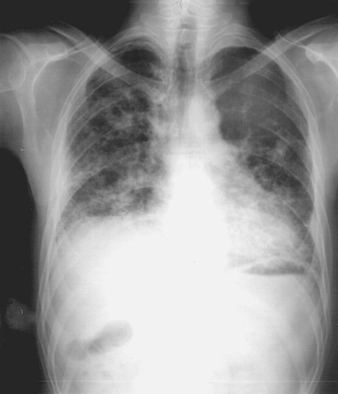
Lo sviluppo della fibrosi interstiziale diffusa aggrava la sintomatologia clinica con un peggioramento della dispnea, che compare anche dopo minimo sforzo e poi anche a riposo, con peggioramento della compromissione ventilatoria restrittiva che è legata ad una riduzione della diffusione capillare-alveolare, e con comparsa di opacità radiografiche di tipo lineare ea nido d'ape (figura 7). Il quadro istologico è quello di un'alveolite fibrosante di tipo “murale”.
Figura 7. Radiografia toracica di un soggetto affetto da fibrosi interstiziale da metallo duro. Si osservano opacità lineari e diffuse e aspetti a nido d'ape.
L'evoluzione è rapidamente progressiva; le terapie sono inefficaci e la prognosi dubbia. Uno dei casi diagnosticati dall'autore alla fine ha richiesto un trapianto di polmone.
La diagnosi occupazionale si basa sull'anamnesi, sul pattern citologico del BAL e sul patch test al cobalto.
La prevenzione della malattia da metalli duri, o, più precisamente, da cobalto, è oggi principalmente tecnica: proteggere i lavoratori attraverso l'eliminazione di polveri, fumi o nebbie con un'adeguata ventilazione delle aree di lavoro. Infatti, la mancanza di conoscenza dei fattori che determinano l'ipersensibilità individuale al cobalto rende impossibile l'identificazione delle persone suscettibili e deve essere fatto il massimo sforzo per ridurre le concentrazioni atmosferiche.
Il numero di persone a rischio è sottostimato perché molte attività di affilatura vengono svolte in piccole industrie o da artigiani. In tali luoghi di lavoro, il TLV statunitense di 0.05 mg/m3 viene spesso superato. C'è anche qualche dubbio sull'adeguatezza del TLV per proteggere i lavoratori contro la malattia da cobalto poiché le relazioni dose-effetto per i meccanismi patologici che coinvolgono l'ipersensibilità non sono completamente comprese.
La sorveglianza di routine deve essere sufficientemente accurata da identificare le patologie da cobalto nelle loro prime fasi. Deve essere somministrato un questionario annuale mirato principalmente ai sintomi temporanei, insieme a una visita medica che comprende test di funzionalità polmonare e altri esami medici appropriati. Poiché è stato dimostrato che esiste una buona correlazione tra le concentrazioni di cobalto nell'ambiente di lavoro e l'escrezione urinaria del metallo, è opportuno effettuare la misurazione semestrale del cobalto nelle urine (CoU) su campioni prelevati alla fine del la settimana lavorativa. Quando l'esposizione è al livello del TLV, l'indice di esposizione biologica (BEI) è stimato pari a 30μg Co/litro urina.
Le visite mediche pre-esposizione per la presenza di malattie respiratorie preesistenti e ipersensibilità bronchiale possono essere utili nella consulenza e nel collocamento dei lavoratori. I test della metacolina sono un utile indicatore di iperreattività bronchiale aspecifica e possono essere utili in alcuni contesti.
Si raccomanda vivamente la standardizzazione internazionale dei metodi di sorveglianza ambientale e medica per i lavoratori esposti al cobalto.