免疫系の機能は、病原体の侵入から身体を保護し、発生する腫瘍細胞に対する免疫監視を提供することです。 それは、非特異的でエフェクター反応自体を開始できる防御の最前線と、リンパ球と抗体が認識の特異性とその後の抗原に対する反応性を運ぶ後天的な特異的分岐を持っています。
免疫毒性学は、「生体異物と免疫系との相互作用の結果として望ましくない影響をもたらす可能性がある事象の研究に関する学問分野」と定義されています。 これらの望ましくない事象は、(1) 免疫系に対する生体異物 (および/またはその生体内変換産物) の直接的および/または間接的な影響、または (2) 化合物に対する免疫学的に基づく宿主応答および/またはその代謝産物、または化合物またはその代謝産物によって修飾された宿主抗原」(Berlin et al. 1987)。
免疫系が化学的傷害の受動的標的として機能すると、その結果、感染や特定の形態の新形成に対する抵抗力が低下したり、アレルギーや自己免疫を悪化させる可能性のある免疫調節不全/刺激が生じる可能性があります. 免疫系が化合物によって修飾された生体異物または宿主抗原の抗原特異性に応答する場合、毒性はアレルギーまたは自己免疫疾患として現れる可能性があります。
化学物質による免疫抑制を調査するための動物モデルが開発されており、これらの方法の多くが検証されています (Burleson、Munson、および Dean 1995; IPCS 1996)。 テストの目的で、利用可能なアッセイの圧倒的な数から適切な選択を行うために、段階的なアプローチに従います。 一般に、第 XNUMX 段階の目的は、潜在的な免疫毒性物質を特定することです。 潜在的な免疫毒性が確認された場合、観察された変化を確認し、さらに特徴付けるために、第 XNUMX 段階のテストが行われます。 第三段階の調査には、化合物の作用メカニズムに関する特別な調査が含まれます。 いくつかの生体異物は、実験動物を用いたこのような研究で免疫抑制を引き起こす免疫毒性物質として同定されています。
環境化学物質によるヒトの免疫機能障害に関するデータベースは限られている (Descotes 1986; NRC Subcommittee on Immunotoxicology 1992)。 免疫毒性のマーカーの使用は、これらの化学物質が人間の健康に及ぼす影響を調査するための臨床研究および疫学研究ではほとんど注目されていません。 そのような研究は頻繁には行われておらず、例えば暴露の制御されていない性質のために、それらの解釈では明確な結論を導き出すことができないことが多い. したがって、現時点では、げっ歯類における免疫毒性評価とその後のヒトへの外挿が、危険性とリスクに関する決定の基礎を形成しています。
過敏症反応、特にアレルギー性喘息および接触性皮膚炎は、先進国における重要な職業上の健康問題です (Vos、Younes、および Smith 1995)。 接触感作の現象は、最初にモルモットで調査された (Andersen and Maibach 1985)。 最近まで、これは予測試験に最適な種でした。 多くのモルモット試験方法が利用可能であり、最も頻繁に使用されるのは、モルモット最大化試験とビューラーの閉塞パッチ試験です。 モルモット試験と、マウスで開発された耳腫脹試験や局所リンパ節アッセイなどの新しいアプローチは、毒物学者に皮膚感作の危険性を評価するためのツールを提供します。 気道の感作に関する状況は非常に異なります。 モルモットとマウスで化学的呼吸器アレルギーを調査するための動物モデルの開発が進んでいるが、化学的呼吸器アレルゲンの同定に利用できる、十分に検証された、または広く受け入れられている方法はまだない。
人間のデータは、化学物質、特に薬物が自己免疫疾患を引き起こす可能性があることを示しています (Kammüller、Bloksma、および Seinen 1989)。 ヒト自己免疫疾患の実験動物モデルは数多くあります。 これには、自発的な病理学 (たとえば、ニュージーランドのブラック マウスにおける全身性エリテマトーデス) と、交差反応性自己抗原による実験的免疫によって誘発される自己免疫現象 (たとえば、Lewis 系統ラットにおける H37Ra アジュバント誘発関節炎) の両方が含まれます。 これらのモデルは、免疫抑制剤の前臨床評価に適用されます。 生体異物が誘発性自己免疫または先天性自己免疫を悪化させるかどうかを評価するためのこれらのモデルの可能性に取り組んだ研究はほとんどありません。 自己免疫疾患を誘発する化学物質の能力を調査するのに適した動物モデルは事実上不足しています。 限られた範囲で使用される XNUMX つのモデルは、マウスの膝窩リンパ節アッセイです。 人間の状況と同様に、遺伝的要因は実験動物の自己免疫疾患 (AD) の発症に重要な役割を果たし、そのような検査の予測値を制限します。
免疫システム
免疫系の主な機能は、細菌、ウイルス、寄生虫、菌類、腫瘍細胞に対する防御です。 これは、細かく調整されたコンサートでのさまざまな細胞タイプとそれらの可溶性メディエーターの作用によって達成されます。 宿主の防御は、非特異的または先天的な耐性と、リンパ球によって媒介される特異的または獲得免疫に大まかに分けることができます (Roitt, Brostoff and Male 1989)。
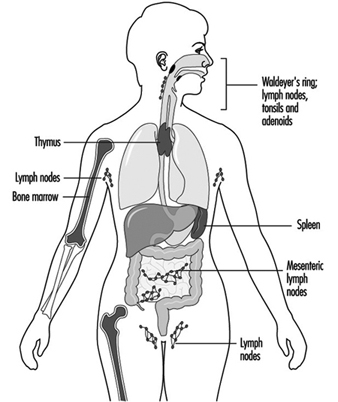
免疫系の構成要素は全身に存在します (Jones et al. 1990)。 リンパ球コンパートメントは、リンパ器官内にあります (図 1)。 骨髄と胸腺は、一次または中央リンパ器官として分類されます。 二次または末梢リンパ器官には、リンパ節、脾臓、および消化管や気道などの分泌面に沿ったリンパ組織、いわゆる粘膜関連リンパ組織(MALT)が含まれます。 体のリンパ球の約半分は常に MALT に存在します。 さらに、皮膚は、皮膚に存在する抗原に対する免疫応答を誘導するための重要な器官です。 この過程で重要なのは、抗原提示機能を持つ表皮ランゲルハンス細胞です。
単核食細胞系 (MPS) と呼ばれる単球/マクロファージ系統の食細胞は、リンパ器官および節外部位で発生します。 節外食細胞には、肝臓のクッパー細胞、肺の肺胞マクロファージ、腎臓のメサンギウムマクロファージ、脳のグリア細胞が含まれます。 多形核白血球 (PMN) は、主に血液と骨髄に存在しますが、炎症部位に蓄積します。
非特異的防御
微生物に対する防御の最前線は、皮膚、気道、消化管などの物理的および化学的障壁によって実行されます。 この障壁は、病原体を殺すことができるマクロファージや多形核白血球などの貪食細胞や、腫瘍細胞やウイルス感染細胞を溶解できるナチュラルキラー細胞などの非特異的な保護メカニズムによって助けられています。 補体系および特定の微生物阻害剤 (例えば、リゾチーム) も非特異的応答に関与します。
特定の免疫
宿主が病原体と最初に接触した後、特異的な免疫応答が誘導されます。 この第 XNUMX の防御線の特徴は、B および T リンパ球の細胞表面上の受容体による病原体の決定基、いわゆる抗原またはエピトープの特異的認識です。 特定の抗原との相互作用に続いて、受容体を有する細胞が刺激されて増殖と分化が起こり、誘発抗原に特異的な子孫細胞のクローンが生成されます。 特異的免疫応答は、非特異的応答の有効性を刺激することにより、病原体に提示される非特異的防御を助けます。 特異的免疫の基本的な特徴は、記憶が発達することです。 同じ抗原との二次接触は、より速く、より活発であるが十分に調節された反応を引き起こします。
ゲノムには、遭遇する可能性のある抗原の数を認識するのに十分な数の抗原受容体の配列のコードを運ぶ能力がありません。 特異性のレパートリーは、遺伝子再編成のプロセスによって発達します。 これはランダムなプロセスであり、その間にさまざまな特異性がもたらされます。 これには、望ましくない自己成分の特異性が含まれます。 胸腺 (T 細胞) または骨髄 (B 細胞) で行われる選択プロセスは、これらの望ましくない特異性を削除するように機能します。
正常な免疫エフェクター機能と免疫応答の恒常性調節は、リンパ球や他の細胞型によって合成および分泌されるサイトカインとして総称されるさまざまな可溶性産物に依存しています。 サイトカインは、免疫および炎症反応に多面的な効果をもたらします。 免疫応答には、異なる細胞集団間の協力が必要です。抗体応答の調節、炎症部位での免疫細胞と分子の蓄積、急性期応答の開始、マクロファージの細胞傷害機能の制御、および宿主耐性の中心となる他の多くのプロセスです。 . これらは、個々に、または協調して作用するサイトカインの影響を受け、多くの場合、サイトカインに依存しています。
特異的免疫には、液性免疫と細胞性または細胞性免疫の XNUMX つの腕が認められています。
液性免疫. 液性アームでは、細胞表面受容体による抗原の認識に続いて、B リンパ球が刺激されます。 B リンパ球の抗原受容体は免疫グロブリン (Ig) です。 成熟 B 細胞 (形質細胞) は、血清中または粘膜表面に沿って抗体として作用する抗原特異的免疫グロブリンの産生を開始します。 免疫グロブリンには 1 つの主要なクラスがあります。(2) IgM、最適な凝集能を持つ五量体 Ig。 (3) 胎盤を通過できる循環中の主要な Ig である IgG。 (4) IgA、粘膜表面の保護のための分泌型 Ig。 (5) IgE、マスト細胞または好塩基性顆粒球への Ig 定着は、即時型過敏反応に関与します。(XNUMX) IgD は、主な機能は B リンパ球上の受容体です。
細胞性免疫. 特定の免疫系の細胞部門は、T リンパ球によって媒介されます。 これらの細胞は、膜上に抗原受容体も持っています。 それらは、組織適合性抗原との関連で抗原提示細胞によって提示された場合、抗原を認識します。 したがって、これらの細胞は抗原特異性に加えて制限があります。 T 細胞は、さまざまな (体液性を含む) 免疫応答のヘルパー細胞として機能し、炎症細胞の動員を仲介し、細胞傷害性 T 細胞として、抗原特異的認識後に標的細胞を殺すことができます。
免疫毒性のメカニズム
免疫抑制
効果的な宿主抵抗性は、免疫系の機能的完全性に依存しており、免疫応答を調整する構成細胞および分子が十分な数で機能する形で利用可能である必要があります。 ヒトの先天性免疫不全症は、多くの場合、特定の幹細胞株の欠陥によって特徴付けられ、免疫細胞の産生が損なわれるか、または欠如します。 先天性および後天性のヒト免疫不全疾患との類推により、化学物質による免疫抑制は、単に機能細胞数の減少に起因する可能性があります (IPCS 1996)。 リンパ球の欠如または数の減少は、多かれ少なかれ免疫状態に深刻な影響を与える可能性があります. 移植または細胞増殖抑制療法で発生する可能性のある一部の免疫不全状態および重度の免疫抑制は、特に日和見感染症および特定の腫瘍性疾患の発生率の増加と関連しています。 感染症は、細菌、ウイルス、真菌、または原生動物である可能性があり、感染の主なタイプは、関連する免疫不全によって異なります。 免疫抑制環境化学物質への曝露は、検出が困難な、より微妙な形態の免疫抑制をもたらすと予想される場合があります。 これらは、例えば、インフルエンザや風邪などの感染症の発生率の増加につながる可能性があります。
多種多様な細胞、メディエーター、および機能が複雑で相互作用的なネットワークを形成する免疫系の複雑さを考慮すると、免疫毒性化合物は効果を発揮する機会が数多くあります。 多くの免疫毒性化学物質によって引き起こされる初期病変の性質はまだ解明されていませんが、免疫機能の低下をもたらす免疫生物学的変化に関して、主に実験動物での研究から得られた情報が増えています (Dean et al. 1994)。 . 毒性効果は、次の重要な機能で発生する可能性があります (これらの機能に影響を与える免疫毒性化合物のいくつかの例が示されています)。
- さまざまな幹細胞集団の発生と拡大 (ベンゼンは幹細胞レベルで免疫毒性作用を発揮し、リンパ球減少症を引き起こします)
- さまざまなリンパ系および骨髄系細胞、ならびにこれらの細胞が成熟して機能する支持組織の増殖 (免疫毒性有機スズ化合物は、直接的な細胞毒性により胸腺皮質におけるリンパ球の増殖活性を抑制する; 2,3,7,8-テトラクロロの胸腺毒性作用-ジベンゾ-p-ダイオキシン (TCDD) および関連化合物は、胸腺細胞に対する直接毒性ではなく、胸腺上皮細胞の機能障害による可能性が高い)
- マクロファージおよび他の抗原提示細胞による抗原の取り込み、処理および提示 (7,12-ジメチルベンズ(a)アントラセン (DMBA) および鉛の標的の XNUMX つはマクロファージによる抗原提示であり、紫外線の標的は抗原です。ランゲルハンス細胞を提示)
- ヘルパー T 細胞およびサプレッサー細胞の調節機能 (ヘルパー T 細胞機能は、有機スズ、アルジカルブ、ポリ塩化ビフェニル (PCB)、TCDD、および DMBA によって損なわれます。T サプレッサー細胞機能は、低用量のシクロホスファミド処理によって低下します)
- さまざまなサイトカインまたはインターロイキンの産生(ベンゾ(a)ピレン(BP)はインターロイキン-1の産生を抑制し、紫外線はケラチノサイトによるサイトカインの産生を変化させます)
- さまざまなクラスの免疫グロブリン IgM および IgG の合成は、PCB および酸化トリブチルスズ (TBT) 処理後に抑制され、ヘキサクロロベンゼン (HCB) 曝露後に増加します)。
- 補体の調節と活性化 (TCDD の影響を受ける)
- 細胞傷害性 T 細胞機能 (3-メチルコラントレン (3-MC)、DMBA、および TCDD は細胞傷害性 T 細胞活性を抑制します)
- ナチュラル キラー (NK) 細胞機能 (肺の NK 活性はオゾンによって抑制され、脾臓の NK 活性はニッケルによって損なわれます)
- マクロファージと多形核白血球の走化性と細胞毒性機能 (オゾンと二酸化窒素は、肺胞マクロファージの貪食活性を損なう)。
アレルギー
アレルギー 特定の免疫応答の誘導および誘発から生じる健康への悪影響として定義することができます。 免疫系の関与なしに過敏反応が起こる場合 疑似アレルギー 使用されている。 免疫毒性学の文脈では、アレルギーは対象となる化学物質や薬物に対する特定の免疫反応から生じます。 個人を感作する化学物質の能力は、一般に、体のタンパク質に共有結合する能力に関連しています。 アレルギー反応はさまざまな形態をとる可能性があり、これらは基礎となる免疫学的メカニズムと反応速度の両方に関して異なります。 24 つの主要なタイプのアレルギー反応が認識されています。 IgE 抗体によって引き起こされ、感作された個人が曝露してから数分以内に症状が現れる I 型過敏反応。 II型過敏症反応は、抗体による宿主細胞の損傷または破壊に起因します。 この場合、症状は数時間以内に現れます。 III型過敏症、またはアルサス反応も抗体媒介性であるが、可溶性抗原に対するものであり、免疫複合体の局所的または全身的作用から生じる。 IV型、または遅発型過敏反応は、Tリンパ球によって引き起こされ、通常、感作された個人が暴露されてから48時間からXNUMX時間後に症状が現れます。
職業上の健康に最も関連性の高い XNUMX 種類の化学物質アレルギーは、接触過敏症または皮膚アレルギーと気道アレルギーです。
接触過敏症. 多数の化学物質が皮膚感作を引き起こす可能性があります。 感受性のある個人が化学アレルゲンに局所的に暴露された後、流出リンパ節で T リンパ球応答が誘導されます。 皮膚では、アレルゲンは表皮のランゲルハンス細胞と直接的または間接的に相互作用し、化学物質をリンパ節に輸送し、応答性の T リンパ球に免疫原性の形で提示します。 アレルゲンで活性化された T リンパ球が増殖し、クローンが拡大します。 個体は現在感作されており、同じ化学物質への 24 回目の皮膚暴露に対してより攻撃的な免疫反応で反応し、アレルギー性接触皮膚炎を引き起こします。 アレルギー性接触皮膚炎の特徴である皮膚の炎症反応は、特定の T リンパ球による皮膚のアレルゲンの認識に続くものです。 これらのリンパ球は活性化され、サイトカインを放出し、他の単核白血球の局所蓄積を引き起こします。 症状は、感作された個人の曝露から約 48 時間から 2,4 時間後に発現するため、アレルギー性接触皮膚炎は遅延型過敏症の一種です。 アレルギー性接触皮膚炎の一般的な原因には、有機化学物質 (XNUMX-ジニトロクロロベンゼンなど)、金属 (ニッケルやクロムなど)、植物製品 (ツタウルシのウルシオールなど) が含まれます。
呼吸過敏症. 呼吸器過敏症は通常、I 型過敏症反応であると考えられています。 しかし、喘息に関連する後期相反応およびより慢性的な症状には、細胞性(IV型)免疫プロセスが関与している可能性があります。 呼吸器アレルギーに関連する急性症状は、IgE 抗体によって影響を受けます。IgE 抗体の産生は、影響を受けやすい個人が誘発化学アレルゲンにさらされた後に誘発されます。 IgE 抗体は全身に分布し、膜受容体を介して気道を含む血管組織に見られるマスト細胞に結合します。 同じ化学物質を吸入すると、呼吸器過敏反応が誘発されます。 アレルゲンはタンパク質と会合し、マスト細胞に結合した IgE 抗体に結合して架橋します。 これによりマスト細胞の脱顆粒が起こり、ヒスタミンやロイコトリエンなどの炎症メディエーターが放出されます。 このようなメディエーターは気管支収縮と血管拡張を引き起こし、呼吸器アレルギーの症状を引き起こします。 喘息および/または鼻炎。 人に呼吸器過敏症を引き起こすことが知られている化学物質には、酸無水物 (トリメリット酸無水物など)、一部のジイソシアネート (トルエンジイソシアネートなど)、白金塩、および一部の反応染料が含まれます。 また、ベリリウムへの慢性暴露は、過敏性肺疾患を引き起こすことが知られています。
自己免疫
自己免疫 内因性「自己」抗原に対する特定の免疫応答の刺激として定義できます。 誘発された自己免疫は、制御性 T リンパ球のバランスの変化、または生体異物と正常組織成分との会合 (「自己変化」) のいずれかから生じる可能性があります。 影響を受けやすい個人の自己免疫疾患 (AD) のような影響を偶発的に誘発または悪化させることが知られている薬物および化学物質は、一般にそれ自体は免疫原性がないと考えられている低分子量化合物 (分子量 100 ~ 500) です。 化学物質への暴露による AD のメカニズムはほとんど知られていません。 疾患は、抗体の循環によって直接的に、免疫複合体の形成を通じて間接的に、または細胞性免疫の結果として生じる可能性がありますが、メカニズムの組み合わせによって発生する可能性があります。 病因は、薬物によって誘発される免疫溶血性疾患で最もよく知られています。
- 薬は赤血球膜に付着し、薬に特異的な抗体と相互作用することができます。
- この薬は、免疫系が細胞を異物と見なすように赤血球膜を変化させることができます。
- 薬とその特異的抗体は、赤血球膜に付着して損傷を引き起こす免疫複合体を形成します。
- 赤血球感作は、赤血球自己抗体の産生によって起こります。
さまざまな化学物質や薬物、特に後者は、自己免疫様反応を誘発することがわかっています (Kamüller、Bloksma、および Seinen 1989)。 化学物質への職業的曝露は、偶然にもAD様症候群につながる可能性があります. 単量体の塩化ビニル、トリクロロエチレン、パークロロエチレン、エポキシ樹脂、およびシリカ粉塵への曝露は、強皮症様症候群を誘発する可能性があります。 全身性エリテマトーデス (SLE) に似た症候群は、ヒドラジンへの曝露後に報告されています。 トルエンジイソシアネートへの曝露は、血小板減少性紫斑病の誘発と関連しています。 水銀などの重金属は、免疫複合体糸球体腎炎の一部の症例に関与しています。
ヒューマンリスクアセスメント
ヒトの免疫状態の評価は、主に末梢血を使用して免疫グロブリンや補体などの体液性物質を分析し、白血球のサブセット構成とサブ集団の機能を分析します。 これらの方法は通常、先天性免疫不全疾患が疑われる患者の体液性および細胞性免疫、ならびに非特異的耐性を調査するために使用されるものと同じです。 疫学的研究(例えば、職業的に暴露された集団)の場合、パラメータは、ヒト集団における予測値、検証済みの動物モデル、およびマーカーの基礎となる生物学に基づいて選択する必要があります(表 1 を参照)。 環境汚染物質または他の毒性物質への (偶発的な) 曝露後の免疫毒性効果のスクリーニング戦略は、予想される免疫不全の種類、曝露から免疫状態の評価までの時間、曝露の程度、および曝露された個人の数などの状況に大きく依存します。 ヒトにおける特定の生体異物の免疫毒性リスクを評価するプロセスは、毒性損傷に対する個人の反応に影響を与える内因性または外因性起源のさまざまな交絡因子の存在により、非常に困難であり、多くの場合不可能です。 これは、遺伝的要因が重要な役割を果たす自己免疫疾患における化学物質曝露の役割を調査する研究に特に当てはまります。
表 1. 免疫マーカー検査の分類
| 試験区分 | 特性 | 特定のテスト |
| 基本一般 一般的なパネルに含める必要があります |
一般的な健康状態と臓器系の状態の指標 | 血中尿素窒素、血糖など |
| 基礎免疫 一般的なパネルに含める必要があります |
免疫状態の一般的な指標 比較的低コスト アッセイ方法は研究所間で標準化されています 基準範囲外の結果は臨床的に解釈可能です |
完全な血球計算 血清IgG、IgA、IgMレベル 主要なリンパ球サブセットの表面マーカー表現型 |
| 集中/反射 臨床所見、曝露の疑い、または以前の検査結果によって示される場合に含める必要があります |
特定の免疫機能/イベントの指標 費用は異なります アッセイ方法は研究所間で標準化されています 基準範囲外の結果は臨床的に解釈可能です |
組織適合遺伝子型 感染因子に対する抗体 総血清 IgE アレルゲン特異的IgE 自己抗体 過敏症の皮膚テスト 顆粒球酸化バースト 病理組織学(組織生検) |
| 研究 コントロール集団と慎重な研究デザインにのみ含める必要があります |
一般的または特定の免疫機能/イベントの指標 費用はさまざまです。 しばしば高価 通常、検査方法は研究所間で標準化されていません 基準範囲外の結果は臨床的に解釈できないことが多い |
インビトロ刺激アッセイ 細胞活性化表面マーカー サイトカイン血清濃度 クローン性アッセイ(抗体、細胞、遺伝子) 細胞毒性試験 |
十分なヒトのデータが入手できることはめったにないため、ヒトにおける化学物質誘発性免疫抑制のリスク評価は、ほとんどの場合、動物実験に基づいています。 潜在的な免疫毒性生体異物の同定は、主にげっ歯類を対象とした対照研究で行われています。 この点に関して、in vivo 曝露研究は、化合物の免疫毒性の可能性を推定するための最適なアプローチを示しています。 これは、免疫系と免疫応答の多因子的で複雑な性質によるものです。 インビトロ研究は、免疫毒性のメカニズムの解明においてますます価値があります。 さらに、動物およびヒト由来の細胞を使用して化合物の効果を調査することにより、種の比較のためのデータを生成することができ、リスク評価プロセスを改善するための「平行四辺形」アプローチで使用できます。 平行四辺形の XNUMX つの要点 (in vivo 動物、in vitro 動物およびヒト) のデータが利用可能である場合、残りの要点、つまりヒトのリスクでの結果を予測することはより容易になる可能性があります。
化学物質誘発性免疫抑制のリスク評価が動物実験のデータのみに依存しなければならない場合、無毒性量 (NOAEL) に不確実係数を適用することにより、人への外挿法に従うことができます。 このレベルは、宿主耐性アッセイや過敏症反応と抗体産生の in vivo 評価など、関連するモデルで決定されたパラメーターに基づくことができます。 理想的には、リスク評価に対するこのアプローチの関連性は、ヒトでの研究による確認が必要です。 このような研究では、毒物、疫学的データ、および免疫状態の評価の特定と測定を組み合わせる必要があります。
接触過敏症を予測するために、モルモット モデルが利用可能であり、1970 年代からリスク評価に使用されてきました。 感度が高く再現性がありますが、主観的な評価に依存するため、これらのテストには限界があります。 これは、マウスで開発されたより新しく、より定量的な方法によって克服できます。 アレルゲンの吸入または摂取によって誘発される化学物質誘発性過敏症に関しては、試験を開発し、ヒトにおける予測値の観点から評価する必要があります。 潜在的アレルゲンの安全な職業暴露レベルの設定に関しては、アレルギーの二相性の性質、つまり感作段階と誘発段階を考慮する必要があります。 以前に感作された個人でアレルギー反応を誘発するために必要な濃度は、免疫学的にナイーブであるが感受性のある個人で感作を誘発するために必要な濃度よりもかなり低い.
化学物質誘発性自己免疫を予測する動物モデルが事実上不足しているため、そのようなモデルの開発に重点を置かなければなりません。 このようなモデルの開発のために、影響を受けやすい個人を特定するための遺伝的および免疫系マーカーの研究を含め、ヒトにおける化学物質誘発性自己免疫に関する私たちの知識を進める必要があります。 自己免疫を誘発する薬物にさらされている人間は、そのような機会を提供します。