人體生物監測使用體液樣本或其他容易獲得的生物材料來測量對特定或非特定物質和/或其代謝物的暴露或測量這種暴露的生物學效應。 生物監測可以讓人們通過不同的暴露途徑(肺、皮膚、胃腸道)和不同的暴露源(空氣、飲食、生活方式或職業)來估計個體的總暴露量。 還已知在工作場所經常遇到的複雜暴露情況下,不同的暴露劑可能會相互作用,從而增強或抑制單個化合物的作用。 由於個體的遺傳構成不同,因此他們對化學暴露的反應也表現出差異。 因此,直接在暴露的個人或群體中尋找早期影響可能比試圖根據與單一化合物有關的數據預測複雜暴露模式的潛在危害更為合理。 這是早期效應遺傳生物監測的一個優勢,該方法採用的技術側重於替代人體組織中的細胞遺傳學損傷、點突變或 DNA 加合物(參見本章中的“一般原則”一文)。
什麼是基因毒性?
化學試劑的遺傳毒性是一種內在的化學特性,基於試劑與細胞大分子(如脫氧核糖核酸、DNA,遺傳信息的載體)中的親核位點結合的親電勢。 因此,遺傳毒性是細胞遺傳物質中表現出的毒性。
正如共識報告 (IARC 1992) 中所討論的那樣,遺傳毒性的定義很廣泛,包括對 DNA 的直接和間接影響:(1) 在分子水平上誘導突變(基因、染色體、基因組、重組)類似於已知與致癌作用有關的事件,(2) 與誘變相關的間接替代事件(例如,計劃外 DNA 合成 (UDS) 和姐妹染色單體交換 (SCE),或 (3) DNA 損傷(例如,加合物的形成),最終可能導致突變。
遺傳毒性、致突變性和致癌性
突變是細胞系中的永久性遺傳變化,無論是在體細胞中水平變化還是在身體的生髮(性)細胞中垂直變化。 也就是說,突變可能通過體細胞的變化影響生物體本身,或者它們可能通過性細胞的改變傳遞給其他世代。 因此,遺傳毒性先於致突變性,儘管大多數遺傳毒性已被修復並且從未表現為突變。 體細胞突變是在細胞水平上誘導的,如果它們導致細胞死亡或惡性腫瘤,可能會表現為組織或生物體本身的各種疾病。 體細胞突變被認為與衰老效應或動脈粥樣硬化斑塊的誘導有關(見圖 1 和關於 癌症).
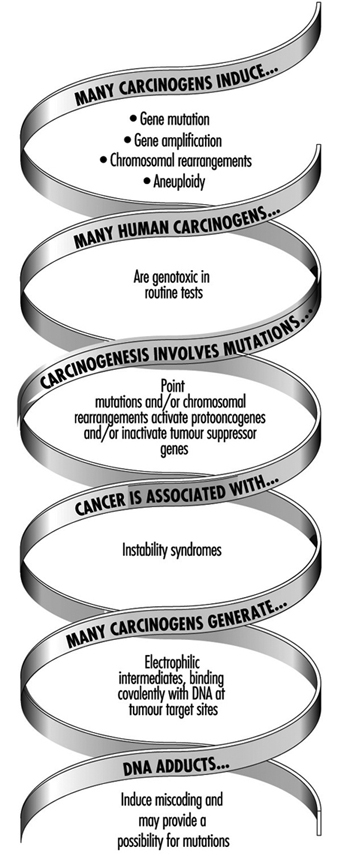
圖 1. 遺傳毒理學和人類健康影響的科學範式示意圖
生殖細胞系中的突變可能會轉移到合子——受精卵細胞——並在後代中表達(另見本章 生殖系統). 在新生兒中發現的最重要的突變病症是由配子發生(生殖細胞的發育)期間染色體的錯誤分離引起的,並導致嚴重的染色體綜合徵(例如,21 三體或唐氏綜合徵,以及單體性 X 或特納綜合徵)。
從暴露到預期影響的遺傳毒理學範例可以簡化,如圖 1 所示。
遺傳毒性與致癌性的關係得到各種間接研究事實的充分支持,如圖 2 所示。
圖 2. 遺傳毒性和致癌性的相互關係
這種相關性為應用遺傳毒性生物標誌物作為癌症危害指標用於人類監測提供了基礎。
危害識別中的遺傳毒性
遺傳變化在致癌作用中的作用強調了遺傳毒性測試在鑑定潛在致癌物中的重要性。 已經開發出各種短期測試方法,這些方法能夠檢測一些據稱與致癌作用相關的遺傳毒性終點。
已經進行了幾項廣泛的調查,以將化學品的致癌性與通過短期測試檢查它們獲得的結果進行比較。 普遍的結論是,由於沒有任何一個經過驗證的測試可以提供所有上述遺傳終點的信息; 有必要在不止一次的化驗中測試每一種化學物質。 此外,遺傳毒性短期試驗對預測化學致癌性的價值也得到反复討論和審查。 在這些審查的基礎上,國際癌症研究機構 (IARC) 的一個工作組得出結論,大多數人類致癌物在常規使用的短期測試中給出陽性結果,例如 沙門氏菌 檢測和染色體畸變檢測(表 1)。 然而,必須認識到表觀遺傳致癌物——例如激素活性化合物可以增加基因毒性活性而本身不具有基因毒性——不能通過短期測試檢測到,短期測試僅測量物質的內在基因毒性活性。
表 1. IARC 專論 (6) 增補 7 和 1986 中評估的化學品的遺傳毒性
|
致癌性分類 |
遺傳毒性/致癌性的證據比率 |
% |
|
1:人類致癌物 |
24/30 |
80 |
|
2A:可能的人類致癌物 |
14/20 |
70 |
|
2B:可能的人類致癌物 |
72/128 |
56 |
|
3:不可分類 |
19/66 |
29 |
遺傳生物監測
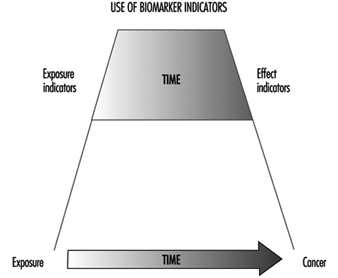
遺傳監測利用遺傳毒理學方法對一組在工作場所或通過環境或生活方式確定暴露的個體進行遺傳效應的生物監測或遺傳毒性暴露的評估。 因此,基因監測有可能及早識別一組人的遺傳毒性暴露,並能夠識別高風險人群,從而確定乾預的優先順序。 有必要在暴露人群中使用預測性生物標誌物以節省時間(與流行病學技術相比)並防止不必要的最終影響,即癌症(圖 3)。
圖 3. 生物標誌物的預測性有助於採取預防措施來降低人群健康風險
表 2 列出了目前用於遺傳毒性暴露和早期生物學效應的生物監測方法。用於生物監測的樣品必須滿足幾個標準,包括必須易於獲得併與目標組織進行比較。
表 2. 遺傳毒性暴露的遺傳監測中的生物標誌物和最常用的細胞/組織樣本。
|
基因監測標記 |
細胞/組織樣本 |
|
染色體畸變 (CA) |
淋巴細胞 |
|
姐妹染色單體交換 (SCE) |
淋巴細胞 |
|
微核 (MN) |
淋巴細胞 |
|
點突變(如 HPRT 基因) |
淋巴細胞和其他組織 |
|
DNA加合物 |
從細胞/組織中分離的 DNA |
|
蛋白質加合物 |
血紅蛋白、白蛋白 |
|
DNA鏈斷裂 |
從細胞/組織中分離的 DNA |
|
癌基因激活 |
分離的 DNA 或特定蛋白質 |
|
突變/癌蛋白 |
各種細胞和組織 |
|
DNA修復 |
從血液樣本中分離細胞 |
分子可識別的 DNA 損傷類型包括 DNA 加合物的形成和 DNA 序列的重組。 這些類型的損傷可以通過使用各種技術測量 DNA 加合物來檢測,例如,32P 後標記或檢測 DNA 加合物的單克隆抗體。 DNA 鏈斷裂的測量通常使用鹼性洗脫或解旋測定法進行。 可以通過對特定基因(例如 HPRT 基因)的 DNA 進行測序來檢測突變。
已經出現了一些詳細討論表 2 技術的方法報告(CEC 1987;IARC 1987、1992、1993)。
遺傳毒性也可以通過測量蛋白質加合物(即血紅蛋白而不是 DNA)或 DNA 修復活性的監測來間接監測。 作為一種測量策略,監控活動可以是一次性的,也可以是連續的。 在所有情況下,結果都必須應用於安全工作條件的發展。
細胞遺傳學生物監測
理論和經驗的基本原理將癌症與染色體損傷聯繫起來。 改變生長因子基因活性或表達的突變事件是致癌作用的關鍵步驟。 許多類型的癌症都與特定或非特定的染色體畸變有關。 在幾種遺傳性人類疾病中,染色體不穩定性與癌症易感性增加有關。
對暴露於致癌和/或致突變化學品或輻射的人進行細胞遺傳學監測可以揭示對相關個人遺傳物質的影響。 幾十年來,對暴露於電離輻射的人的染色體畸變研究一直被用於生物劑量測定,但目前只有少數化學致癌物有充分記錄的陽性結果。
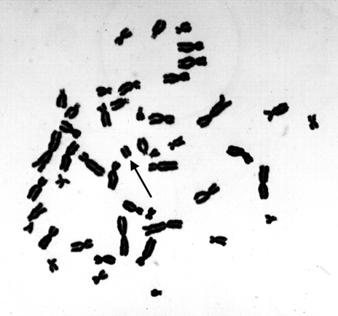
顯微鏡下可識別的染色體損傷包括染色體結構畸變 (CA),其中染色體的形態(形狀)發生了嚴重變化,以及姐妹染色單體交換 (SCE)。 SCE是兩條姐妹染色單體之間染色體物質的對稱交換。 微核 (MN) 可以來自無著絲粒染色體片段或來自滯後的整個染色體。 這些類型的變化如圖 4 所示。
圖 4. 中期人類淋巴細胞染色體,揭示了誘導的染色體突變(箭頭指向無著絲粒片段)
人類的外周血淋巴細胞是適合用於監測研究的細胞,因為它們易於獲取,而且它們可以在相對較長的生命週期內整合暴露。 暴露於各種化學誘變劑可能導致暴露個體的血液淋巴細胞中 CA 和/或 SCE 的頻率增加。 此外,損害的程度與接觸程度大致相關,儘管只有少數化學品顯示了這一點。
當外周血淋巴細胞的細胞遺傳學檢測顯示遺傳物質已受損時,結果只能用於估計人群水平的風險。 人群中 CA 頻率的增加應被視為癌症風險增加的指徵,但細胞遺傳學測試本身並不能預測癌症的個體風險。
通過外周血淋巴細胞樣本的狹窄窗口觀察到的體細胞遺傳損傷的健康意義對個體的健康意義不大或沒有意義,因為大多數攜帶遺傳損傷的淋巴細胞死亡並被替換。
人體生物監測研究中的問題及其控制
嚴格的研究設計在任何人體生物監測方法的應用中都是必要的,因為許多與感興趣的特定化學暴露無關的個體間因素可能會影響所研究的生物反應。 由於人體生物監測研究在許多方面都是乏味和困難的,因此仔細的預先計劃非常重要。 在進行人類細胞遺傳學研究時,實驗確認暴露劑的染色體損傷潛力應始終是實驗先決條件。
在細胞遺傳學生物監測研究中,已經記錄了兩種主要類型的變異。 第一個因素包括與載玻片讀數差異和培養條件相關的技術因素,特別是與培養基類型、溫度和化學品濃度(如溴脫氧尿苷或細胞鬆弛素 B)有關。 此外,採樣時間可以通過改變 T 淋巴細胞和 B 淋巴細胞亞群來改變染色體畸變率,也可能改變 SCE 發病率的發現。 在微核分析中,方法學差異(例如,使用由細胞鬆弛素 B 誘導的雙核細胞)非常明顯地影響評分結果。
化學暴露在淋巴細胞 DNA 中引起的損傷會導致結構性染色體畸變、姐妹染色單體交換和微核的形成,這些損傷必須持續存在 体内 直到抽血,然後 體外 直到培養的淋巴細胞開始合成DNA。 因此,重要的是在第一次分裂後(在染色體畸變或微核的情況下)或第二次分裂後(姐妹染色單體交換)直接對細胞進行評分,以獲得對誘導損傷的最佳估計。
評分構成細胞遺傳學生物監測中極其重要的元素。 載玻片必須隨機化和編碼,以盡可能避免評分者偏差。 應保持一致的評分標準、質量控制和標準化的統計分析和報告。 第二類變異性是由於與受試者相關的條件,例如年齡、性別、藥物和感染。 個體差異也可能由對環境因素的遺傳易感性引起。
獲得一個同時控制組至關重要,該控制組在性別和年齡等內部因素以及吸煙狀況、病毒感染和疫苗接種、酒精和藥物攝入以及 X 射線暴露等因素上盡可能匹配. 此外,有必要獲得定性(工作類別、暴露年數)和定量(例如,如果可能,用於化學分析和特定代謝物的呼吸區空氣樣本)估計或工作場所中假定的遺傳毒性劑的暴露。 應特別注意對結果進行適當的統計處理。
遺傳生物監測與癌症風險評估的相關性
反复顯示可誘導人類細胞遺傳學變化的藥物數量仍然相對有限,但大多數已知的致癌物都會引起淋巴細胞染色體損傷。
損害的程度是暴露水平的函數,例如氯乙烯、苯、環氧乙烷和烷基化抗癌劑的情況就是如此。 即使細胞遺傳學終點對於檢測當今職業環境中發生的暴露不是非常敏感或特異,即使沒有直接證據表明體細胞染色體損傷不利的健康結果。
大多數細胞遺傳學生物監測應用的經驗都來自“高暴露”的職業情況。 幾項獨立研究證實了極少數接觸,其中大部分是使用染色體畸變生物監測進行的。 國際癌症研究機構的數據庫在其更新的 IARC 專論第 43-50 卷中列出了第 14、1A 或 2B 組中的 2 種職業致癌物,在大多數情況下,這些物質都有陽性的人類細胞遺傳學數據得到相應動物細胞遺傳學的支持(表 3)。 這個有限的數據庫表明,致癌化學物質有致染色體斷裂的趨勢,而致染色體斷裂往往與已知的人類致癌物有關。 然而,很明顯,並非所有致癌物都會對人類或實驗動物造成細胞遺傳學損傷 体内. 動物數據為陽性而人類發現為陰性的情況可能代表暴露水平的差異。 此外,工作中復雜和長期的人類暴露可能無法與短期動物實驗相提並論。
表 3. 存在職業暴露且已在人類和實驗動物中測量細胞遺傳學終點的已證實、可能和可能的人類致癌物
|
細胞遺傳學發現1 |
||||||
|
人類 |
動物 |
|||||
|
代理/曝光 |
CA |
SCE |
MN |
CA |
SCE |
MN |
|
第 1 組,人類致癌物 |
||||||
|
砷及砷化合物 |
? |
? |
|
+ |
|
+ |
|
石棉 |
|
? |
|
- |
|
- |
|
苯 |
+ |
|
|
+ |
+ |
+ |
|
雙(氯甲基)醚和氯甲基甲基醚(工業級) |
(+), |
|
|
- |
|
|
|
環磷酰胺 |
+ |
+ |
|
+ |
+ |
+ |
|
六價鉻化合物 |
+ |
+ |
|
+ |
+ |
+ |
|
馬法蘭 |
+ |
+ |
|
+ |
|
|
|
鎳化合物 |
+ |
- |
|
? |
|
|
|
氡 |
+ |
|
|
- |
|
|
|
煙 |
+ |
+ |
+ |
|
+ |
|
|
氯乙烯 |
+ |
? |
|
+ |
+ |
+ |
|
第 2A 組,可能的人類致癌物 |
||||||
|
丙烯腈 |
- |
|
|
- |
|
- |
|
阿黴素 |
+ |
+ |
|
+ |
+ |
+ |
|
鎘及鎘化合物 |
- |
(-) |
|
- |
|
|
|
順鉑 |
|
+ |
|
+ |
+ |
|
|
表氯醇 |
+ |
|
|
? |
+ |
- |
|
二溴乙烯 |
- |
- |
|
- |
+ |
- |
|
環氧乙烷 |
+ |
+ |
+ |
+ |
+ |
+ |
|
甲醛 |
? |
? |
|
- |
|
- |
|
第 2B 組,可能的人類致癌物 |
||||||
|
氯苯氧基除草劑(2,4-D 和 2,4,5-T) |
- |
- |
|
+ |
+ |
- |
|
滴滴涕 |
? |
|
|
+ |
|
- |
|
二甲基甲酰胺 |
(+), |
|
|
|
- |
- |
|
先導化合物 |
? |
? |
|
? |
- |
? |
|
苯乙烯 |
+ |
? |
+ |
? |
+ |
+ |
|
2,3,7,8-四氯二苯並對二噁英 |
? |
|
|
- |
- |
- |
|
焊接煙氣 |
+ |
+ |
|
- |
- |
|
1 CA,染色體畸變; SCE,姐妹染色單體交換; MN,微核。
(–) = 一項研究的負相關關係; – = 負相關;
(+) = 一項研究的正相關關係; + = 正相關;
? = 不確定; 空白區域=未研究
資料來源:國際癌症研究機構,1987 年; 通過 IARC 專論的第 43-50 卷更新。
暴露人類的遺傳毒性研究包括染色體終點以外的各種終點,例如 DNA 損傷、DNA 修復活性以及 DNA 和蛋白質中的加合物。 對於致癌危害的預測,這些終點中的一些可能比其他終點更相關。 穩定的遺傳變化(例如,染色體重排、缺失和點突變)具有高度相關性,因為已知這些類型的損傷與致癌作用有關。 DNA 加合物的重要性取決於它們的化學鑑定和它們由暴露產生的證據。 一些終點,如 SCE、UDS、SSB、DNA 鏈斷裂,是遺傳事件的潛在指標和/或標記; 然而,如果對其導致遺傳事件的能力缺乏機械理解,它們的價值就會降低。 顯然,與人類最相關的遺傳標記是特定突變的誘導,該突變與暴露於所研究藥物的囓齒動物的癌症直接相關(圖 5)。
圖 5. 不同遺傳生物監測效應與潛在癌症風險的相關性
遺傳生物監測的倫理考慮
分子遺傳技術的快速發展、人類基因組測序速度的提高以及腫瘤抑制基因和原癌基因在人類致癌過程中的作用的鑑定,在解釋、交流和使用這種基因組時引發了倫理問題。個人信息。 快速改進人類基因分析技術將很快允許在健康、無症狀的個體中識別出更多的遺傳易感基因(美國技術評估辦公室 1990),從而將它們用於基因篩查。
如果基因篩查的應用很快成為現實,將會引發許多社會和倫理關注的問題。 目前已有大約 50 種新陳代謝、酶多態性和 DNA 修復的遺傳特徵被懷疑具有特定的疾病敏感性,並且診斷 DNA 測試可用於大約 300 種遺傳病。 是否應該在工作場所進行任何基因篩查? 誰來決定誰將接受測試,這些信息將如何用於就業決策? 誰將有權訪問從基因篩查中獲得的信息,結果將如何傳達給相關人員? 其中許多問題與社會規範和普遍的道德價值觀密切相關。 主要目標必須是預防疾病和人類痛苦,但必須尊重個人的意志和道德前提。 在任何工作場所生物監測研究開始之前必須回答的一些相關倫理問題在表 4 中給出,並在本章中進行了討論 倫理道德問題.
表 4. 與職業遺傳生物監測研究中的知情必要性相關的一些倫理原則
|
向其提供信息的群體 |
|||
|
給出的信息 |
研究人員 |
職業健康股 |
雇主 |
|
正在研究什麼 |
|||
|
為什麼要進行這項研究 |
|||
|
是否涉及風險 |
|||
|
保密問題 |
|||
|
為可能的衛生改善做好準備,表明減少接觸 |
|||
任何基因生物監測研究的計劃階段都必須投入時間和精力,所有必要的各方——僱員、雇主和合作工作場所的醫務人員——必須在研究前充分了解情況,並將結果公之於眾他們在研究之後也是如此。 通過適當的護理和可靠的結果,基因生物監測可以幫助確保更安全的工作場所並改善工人的健康。