簡介
根據是發生在工業生產還是使用過程中,人類接觸農藥具有不同的特徵(表 1)。 商業產品的配方(通過將活性成分與其他助劑混合)與農業中的農藥使用具有一些共同的暴露特徵。 事實上,由於配製通常由在連續操作中生產許多不同產品的小型工業進行,因此工人會在短時間內接觸幾種農藥中的每一種。 在公共衛生和農業中,通常使用多種化合物,儘管在某些特定應用中(例如,棉花脫葉或瘧疾控制計劃)可能會使用單一產品。
表 1 農藥生產和使用過程暴露特徵比較
|
生產曝光 |
使用時暴露 |
|
|
暴露時間 |
持續而持久 |
多變和間歇 |
|
暴露程度 |
相當穩定 |
極其多變 |
|
曝光類型 |
對一種或幾種化合物 |
對許多化合物依次或伴隨 |
|
皮膚吸收 |
易於控制 |
根據工作程序可變 |
|
環境監測 |
有用 |
很少提供信息 |
|
生物監測 |
環境監測的補充 |
可用時非常有用 |
來源:WHO 1982a,修改。
生物暴露指標的測量對於殺蟲劑使用者特別有用,因為通過環境空氣監測進行暴露評估的傳統技術幾乎不適用。 大多數殺蟲劑是可滲透皮膚的脂溶性物質。 經皮(皮膚)吸收的發生使得生物指示劑的使用在評估這些情況下的暴露水平時非常重要。
有機磷殺蟲劑
作用生物學指標:
膽鹼酯酶是導致有機磷酸酯 (OP) 對昆蟲和哺乳動物物種產生毒性的目標酶。 人體中有兩種主要類型的膽鹼酯酶:乙酰膽鹼酯酶 (ACHE) 和血漿膽鹼酯酶 (PCHE)。 OP 通過抑制神經系統中的突觸乙酰膽鹼酯酶對人類產生毒性作用。 乙酰膽鹼酯酶也存在於紅細胞中,其功能未知。 血漿膽鹼酯酶是一個通用術語,涵蓋神經膠質細胞、血漿、肝臟和其他一些器官中存在的一組不均勻的酶。 PCHE 被 OP 抑制,但其抑制不會產生已知的功能紊亂。
血液 ACHE 和 PCHE 活性的抑制與 OP 暴露的強度和持續時間高度相關。 血液 ACHE 與導致神經系統急性 OP 毒性的分子靶點相同,是比 PCHE 更具體的指標。 然而,血液 ACHE 和 PCHE 對 OP 抑制的敏感性因不同的 OP 化合物而異:在相同的血液濃度下,一些抑制更多的 ACHE,而另一些抑制更多的 PCHE。
血液 ACHE 活性與急性毒性的臨床體徵之間存在合理的相關性(表 2)。 當抑制速率更快時,相關性往往更好。 當抑制發生緩慢時,如慢性低水平暴露,與疾病的相關性可能很低或完全不存在。 必須注意的是,血液 ACHE 抑制不能預測慢性或延遲效應。
表 2. 不同 ACHE 抑制水平下急性 OP 毒性的嚴重程度和預後
|
疼痛 抑制 (%) |
水平 中毒 |
臨床症狀 |
預測 |
|
50-60 |
中等 |
虛弱、頭痛、頭暈、噁心、流涎、流淚、瞳孔縮小、中度支氣管痙攣 |
1-3天恢復 |
|
60-90 |
中度 |
突然虛弱、視力障礙、流涎過多、出汗、嘔吐、腹瀉、心動過緩、肌張力亢進、手和頭震顫、步態紊亂、瞳孔縮小、胸部疼痛、粘膜發紺 |
1-2週恢復 |
|
90-100 |
嚴重 |
突發性震顫、全身性抽搐、精神障礙、強烈發紺、肺水腫、昏迷 |
死於呼吸或心力衰竭 |
已在健康人和特定的病理生理條件下觀察到 ACHE 和 PCHE 活性的變化(表 3)。 因此,通過採用個體暴露前值作為參考,可以提高這些測試在監測 OP 暴露方面的敏感性。 然後將暴露後的膽鹼酯酶活性與個體基線值進行比較。 僅當暴露前膽鹼酯酶水平未知時,才應使用人群膽鹼酯酶活性參考值(表 4)。
表 3. 健康人和特定病理生理條件下 ACHE 和 PCHE 活性的變化
|
條件 |
疼痛活動 |
PCHE活性 |
|
健康的人 |
||
|
個體差異1 |
10–18% |
15–25% |
|
個體差異1 |
3–7% |
6% |
|
性別差異 |
沒有 |
男性高出 10–15% |
|
年齡 |
減至 6 個月大 |
|
|
身體質量 |
正相關 |
|
|
血清膽固醇 |
正相關 |
|
|
季節性變化 |
沒有 |
沒有 |
|
晝夜節律變化 |
沒有 |
沒有 |
|
經期 |
減少 |
|
|
懷孕 |
減少 |
|
|
病理狀況 |
||
|
減少活動 |
白血病、腫瘤 |
肝病; 尿毒症; 癌症; 心臟衰竭; 過敏反應 |
|
活動增加 |
紅細胞增多症; 地中海貧血; 其他先天性血液惡液質 |
甲狀腺機能亢進; 其他高代謝率的情況 |
1 資料來源:Augustinsson 1955 和 Gage 1967。
表 4. 使用選定方法測量未接觸 OP 的健康人的膽鹼酯酶活性
|
選項 |
性別 |
疼痛* |
聚氯乙烯* |
|
米歇爾1 (DpH/小時) |
男 女 |
0.77± 0.08 0.75± 0.08 |
0.95± 0.19 0.82± 0.19 |
|
滴定法1 (毫摩爾/分鐘毫升) |
男/女 |
13.2± 0.31 |
4.90± 0.02 |
|
埃爾曼氏改良2 (用戶界面/毫升) |
男 女 |
4.01± 0.65 3.45± 0.61 |
3.03± 0.66 3.03± 0.68 |
* 平均結果,± 標準偏差。
資源: 1 法律 1991。 2 阿爾奇尼等人。 1988.
最好在暴露後兩小時內採集血液樣本。 靜脈穿刺優於從手指或耳垂中提取毛細血管血,因為採樣點可能會被暴露對像皮膚上殘留的殺蟲劑污染。 建議三個連續樣本在暴露前為每個工人建立正常基線 (WHO 1982b)。
有幾種分析方法可用於測定血液 ACHE 和 PCHE。 根據 WHO 的說法,Ellman 分光光度法(Ellman et al. 1961)應作為參考方法。
暴露的生物指標。
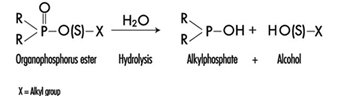
尿液中源自 OP 分子磷酸烷基酯部分的代謝物或 P-X 鍵水解產生的殘留物(圖 1)的測定已被用於監測 OP 暴露。
圖 1. OP 殺蟲劑的水解
烷基磷酸酯代謝物。
表 5 列出了可在尿液中檢測到的磷酸烷基酯代謝物及其來源的主要母體化合物。無法檢測到血漿或紅細胞膽鹼酯酶抑制。 已經針對不同的暴露條件和各種 OP 化合物測量了烷基磷酸鹽的尿液排泄(表 6)。 一些研究已經確定了 OP 的外部劑量與磷酸烷基酯尿液濃度之間存在關係。 在一些研究中,還證實了膽鹼酯酶活性與尿液中磷酸烷基酯水平之間的顯著關係。
表 5. 尿液中可檢測到的磷酸烷基酯作為有機磷殺蟲劑的代謝物
|
代謝物 |
縮寫 |
主要母體化合物 |
|
磷酸一甲酯 |
MMP |
馬拉硫磷、對硫磷 |
|
磷酸二甲酯 |
DMP |
敵敵畏、敵百蟲、毒敵磷、馬拉奧磷、樂果、敵百蟲 |
|
磷酸二乙酯 |
DEP |
對氧磷、內吸磷-氧磷、二嗪磷-氧磷、敵百蟲 |
|
硫代磷酸二甲酯 |
DMTP |
殺螟松、殺蟲磷、馬拉硫磷、樂果 |
|
硫代磷酸二乙酯 |
二乙基TP |
二嗪農、地美松、對硫磷、敵草磷 |
|
二甲基二硫代磷酸鹽 |
二甲基二甲基苯胺 |
馬拉硫磷、樂果、谷硫磷 |
|
二乙基二硫代磷酸鹽 |
二乙二胺四乙酸 |
雙硫磷、甲拌磷 |
|
苯基磷酸 |
輕磷,EPN |
表 6. 在暴露於 OP 的各種條件下測得的尿烷基磷酸鹽水平示例
|
複合 |
接觸條件 |
暴露途徑 |
代謝物濃度1 (毫克/升) |
|
對硫磷2 |
非致命性中毒 |
口服 |
部門= 0.5 二乙基TP=3.9 |
|
敵磺通2 |
配方師 |
皮膚/吸入 |
介電常數=0.01-4.40 DETP=0.01-1.57 DEDTP = <0.01-.05 |
|
磷酸鹽2 |
配方師 |
皮膚/吸入 |
介電常數=0.02-5.14 DETP=0.08-4.08 DEDTP = <0.01-0.43 |
|
馬拉硫磷3 |
噴霧器 |
皮膚的 |
DMDTP = <0.01 |
|
殺螟松3 |
噴霧器 |
皮膚的 |
DMP=0.01-0.42 二甲基吡啶=0.02-0.49 |
|
久效磷4 |
噴霧器 |
皮膚/吸入 |
DMP = <0.04-6.3/24 小時 |
1 縮寫見表 27.12 [BMO12TE]。
2 狄龍和何 1987 年。
3 里希特 1993。
4 van Sittert 和 Dumas 1990。
烷基磷酸酯通常在短時間內隨尿液排出。 工作日結束後不久收集的樣品適用於代謝物測定。
尿液中磷酸烷基酯的測量需要一種相當複雜的分析方法,該方法基於化合物的衍生化和氣液色譜檢測(Shafik 等人 1973a;Reid 和 Watts 1981)。
水解殘留物。
p-硝基苯酚 (PNP) 是對硫磷、甲基對硫磷和乙基對硫磷的酚類代謝物,EPN。 尿液中 PNP 的測量(Cranmer 1970)已被廣泛使用,並已證明在評估對硫磷暴露方面是成功的。 尿 PNP 與對硫磷的吸收劑量密切相關。 當 PNP 尿濃度高達 2 mg/l 時,對硫磷的吸收不會引起症狀,並且很少或沒有觀察到膽鹼酯酶活性降低。 PNP 排泄迅速發生,並且 PNP 的尿水平在暴露後 48 小時變得微不足道。 因此,應在暴露後立即收集尿液樣本。
氨基甲酸酯
生物指標的影響。
氨基甲酸酯類農藥包括殺蟲劑、殺菌劑和除草劑。 殺蟲氨基甲酸酯的毒性是由於突觸 ACHE 的抑制,而除草和殺真菌氨基甲酸酯還涉及其他毒性機制。 因此,只能通過測定紅細胞 (ACHE) 或血漿 (PCHE) 中的膽鹼酯酶活性來監測氨基甲酸酯殺蟲劑的暴露情況。 ACHE 通常比 PCHE 對氨基甲酸酯抑製劑更敏感。 在血液 ACHE 活性低於個體基線水平的 70% 的氨基甲酸酯暴露工人中通常會觀察到膽鹼能症狀(WHO 1982a)。
氨基甲酸酯對膽鹼酯酶的抑制是快速可逆的。 因此,如果暴露和生物採樣之間或採樣和分析之間的時間過長,則可能會獲得假陰性結果。 為避免此類問題,建議在暴露後四小時內採集血液樣本並進行分析。 應優先考慮採血後立即測定膽鹼酯酶活性的分析方法,如對有機磷酸酯的討論。
暴露的生物指標。
迄今為止,氨基甲酸酯代謝物的尿排泄測量作為一種監測人體暴露的方法僅適用於少數化合物和有限的研究。 表 7 總結了相關數據。 由於氨基甲酸酯會迅速從尿液中排出,因此在暴露結束後不久收集的樣本適合用於代謝物測定。 Dawson 等人報導了測量尿液中氨基甲酸酯代謝物的分析方法。 (1964); DeBernardinis 和 Wargin (1982) 以及 Verberk 等人。 (1990)。
表 7. 實地研究中測得的尿液氨基甲酸酯代謝物水平
|
複合 |
生物指標 |
接觸條件 |
環境濃度 |
成績 |
參考 |
|
西維因 |
萘酚 萘酚 萘酚 |
配方師 混合器/塗抹器 未暴露人群 |
0.23–0.31 毫克/立方米3 |
x=18.5 毫克/升1 , 最大限度。 排泄率 = 80 毫克/天 x=8.9 毫克/升,範圍 = 0.2–65 毫克/升 範圍 = 1.5–4 毫克/升 |
世界衛生組織 1982a |
|
抗蚜威 |
代謝物一2 和V.3 |
塗抹器 |
範圍 = 1–100 毫克/升 |
Verberk 等人。 1990 |
1 偶爾有全身中毒的報導。
2 2-二甲基氨基-4-羥基-5,6-二甲基嘧啶。
3 2-甲基氨基-4-羥基-5,6-二甲基嘧啶。
x = 標準偏差。
二硫代氨基甲酸鹽
暴露的生物指標。
二硫代氨基甲酸鹽 (DTC) 是廣泛使用的殺菌劑,化學上分為三類:秋蘭姆、二甲基二硫代氨基甲酸鹽和亞乙基雙二硫代氨基甲酸鹽。
二硫化碳(CS2) 及其主要代謝物 2-thiothiazolidine-4-carboxylic acid (TTCA) 是幾乎所有 DTC 共有的代謝物。 對於不同的暴露條件和各種 DTC 殺蟲劑,已觀察到這些化合物的尿液濃度顯著增加。 亞乙基硫脲 (ETU) 是亞乙基雙二硫代氨基甲酸鹽的重要尿液代謝產物。 它也可能作為雜質存在於市場配方中。 由於 ETU 已被確定為大鼠和其他物種的致畸劑和致癌劑,並且與甲狀腺毒性有關,因此它已被廣泛應用於監測亞乙基雙二硫代氨基甲酸酯暴露。 ETU 不是特定化合物,因為它可能源自代森錳、代森錳鋅或鋅鋅。
已提議測量 DTC 中存在的金屬作為監測 DTC 暴露的替代方法。 在暴露於代森錳鋅的工人中觀察到錳的尿液排泄增加(表 8)。
表 8. 實地研究中測得的尿液二硫代氨基甲酸鹽代謝物水平
|
複合 |
生物指標 |
條件 曝光 |
環境濃度* ± 標準差 |
結果±標準偏差 |
參考 |
|
吉拉姆 |
二硫化碳(CS2) TTCA1 |
配方師 配方師 |
1.03 ± 0.62 毫克/米3 |
3.80 ± 3.70 毫克/升 0.45 ± 0.37 毫克/升 |
馬羅尼等。 1992 |
|
代森錳/代森錳鋅 |
埃圖2 |
塗抹器 |
範圍 = < 0.2–11.8 毫克/升 |
庫爾蒂奧等。 1990 |
|
|
代森錳鋅 |
錳 |
塗抹器 |
57.2 毫克/平方米3 |
暴露前:0.32 ± 0.23 mg/g 肌酐; 暴露後:0.53 ± 0.34 mg/g 肌酐 |
卡諾莎等人。 1993 |
* 根據 Maroni 等人的平均結果。 1992.
1 TTCA = 2-thiothiazolidine-4-carbonylic acid。
2 ETU = 亞乙基硫脲。
CS2、TTCA 和錳常見於未暴露受試者的尿液中。 因此,建議在暴露前測量這些化合物的尿水平。 應在停止暴露後的早晨收集尿液樣本。 CS測量的分析方法2, TTCA 和 ETU 已被 Maroni 等人報導。 (1992)。
合成擬除蟲菊酯
暴露的生物指標。
合成擬除蟲菊酯是類似於天然除蟲菊酯的殺蟲劑。 通過對人類誌願者的研究,已經確定了適用於暴露的生物監測的尿液代謝物。 酸性代謝物 3-(2,2'-二氯-乙烯基)-2,2'-二甲基-環丙烷甲酸 (Cl2CA) 由口服氯菊酯和氯氰菊酯以及溴類似物 (Br2CA)由用溴氰菊酯治療的受試者。 在接受氯氰菊酯治療的志願者中,還發現了一種苯氧基代謝物 4-羥基苯氧基苯甲酸 (4-HPBA)。 然而,由於需要復雜的分析技術,這些測試並不常用於監測職業暴露(Eadsforth、Bragt 和 van Sittert,1988 年;Kolmodin-Hedman、Swensson 和 Akerblom,1982 年)。 在暴露於氯氰菊酯的塗藥器中,Cl 的尿液水平2已發現 CA 的範圍為 0.05 至 0.18 mg/l,而在暴露於 α-氯氰菊酯的配方設計師中,已發現 4-HPBA 的尿液水平低於 0.02 mg/l。
建議在暴露結束後開始 24 小時的尿液收集期以進行代謝物測定。
有機氯
暴露的生物指標。
有機氯 (OC) 殺蟲劑在 1950 年代和 1960 年代被廣泛使用。 隨後,由於這些化合物的持久性和隨之而來的環境污染,許多國家停止使用其中的許多化合物。
OC 暴露的生物監測可以通過測定血液或血清中的完整農藥或其代謝物來進行(Dale、Curley 和 Cueto 1966 年;Barquet、Morgade 和 Pfaffenberger 1981 年)。 吸收後,艾氏劑迅速代謝為狄氏劑,可按血液中的狄氏劑測定。 Endrin 在血液中的半衰期非常短。 因此,異狄氏劑血液濃度僅用於確定近期暴露水平。 尿液代謝物抗 12-羥基異狄氏劑的測定也已證明可用於監測異狄氏劑暴露(van Sittert 和 Tordoir 1987)。
對於某些 OC 化合物,已經證明生物指示劑的濃度與毒性作用的發生之間存在顯著相關性。 艾氏劑和狄氏劑暴露引起的毒性實例與血液中狄氏劑水平超過 200 微克/升有關。 就神經體徵和症狀而言,血液中的林丹濃度為 20 微克/升,已被確定為臨界上限。 血液異狄氏劑濃度低於 50 微克/升的工人沒有急性不良反應的報告。 在尿液抗 12-羥基異狄氏劑濃度低於 130 μg/g 肌酐時反复暴露於異狄氏劑以及在 DDT 或 DDE 血清濃度低於 250 時反复暴露於 DDT 表明沒有早期不良反應(誘導肝微粒體酶)微克/升。
在普通人群的血液或尿液中可能會發現低濃度的 OC。 觀察值示例如下:林丹血液濃度高達 1 μg/l,狄氏劑高達 10 μg/l,DDT 或 DDE 高達 100 μg/l,抗 12-羥基異狄氏劑高達 1 μg/g肌酐。 因此,建議在暴露前進行基線評估。
對於暴露的受試者,應在單次暴露結束後立即採集血樣。 對於長期暴露的情況,採集血樣的時間並不重要。 應在暴露結束時收集用於尿液代謝物測定的尿液斑點樣本。
三嗪類
暴露的生物指標。
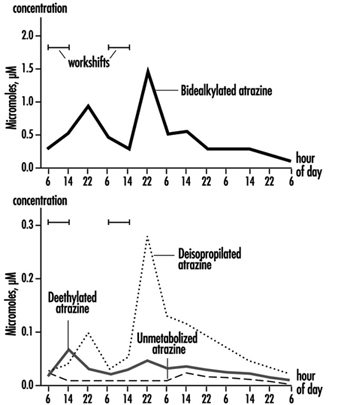
在有限的研究中,已將三嗪代謝物和未修飾母體化合物的尿液排泄測量應用於暴露於阿特拉津的受試者。 圖 2 顯示了一名製造業工人阿特拉津代謝物的尿液排泄曲線,其皮膚接觸阿特拉津範圍為 174 至 275 μmol/班次(Catenacci 等人,1993 年)。 由於其他氯三嗪(西瑪津、丙哌嗪、特丁津)遵循阿特拉津的相同生物轉化途徑,因此可以確定脫烷基化三嗪代謝物的水平,以監測所有氯三嗪除草劑的暴露情況。
圖 2. 阿特拉津代謝物的尿液排泄曲線
尿液中未修飾化合物的測定可能有助於定性確認產生暴露的化合物的性質。 建議在接觸開始時開始 24 小時尿液收集期以測定代謝物。
最近,通過使用酶聯免疫吸附試驗(ELISA 試驗),阿特拉津的硫醇尿酸結合物已被確定為其暴露工人的主要尿液代謝物。 已發現該化合物的濃度至少比任何脫烷基化產品的濃度高 10 倍。 已經觀察到在 10 天內累積的皮膚和吸入暴露與排出的硫醇尿酸共軛物總量之間的關係(Lucas 等人,1993 年)。
香豆素衍生物
生物指標的影響。
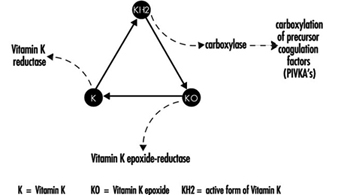
香豆素類滅鼠劑抑制哺乳動物(包括人類)肝臟中維生素 K 循環酶的活性(圖 3),從而導致維生素 K 依賴性凝血因子(即因子 II(凝血酶原))的合成劑量相關減少、VII、IX 和 X。當凝血因子的血漿水平下降到低於正常水平的大約 20% 時,就會出現抗凝作用。
圖 3. 維生素 K 循環
這些維生素 K 拮抗劑已分為所謂的“第一代”化合物(例如華法林)和“第二代”化合物(例如溴鼠靈、地醚靈),後者的特點是生物半衰期非常長(100 至 200 天) ).
凝血酶原時間的測定廣泛用於監測香豆素暴露情況。 然而,該測試僅對凝血因子降低正常血漿水平的大約 20% 敏感。 該測試不適用於檢測暴露的早期影響。 為此,建議測定血漿中的凝血酶原濃度。
將來,這些測試可能會被凝血因子前體 (PIVKA) 的測定所取代,PIVKA 是只有在維生素 K 循環被香豆素阻斷的情況下才能在血液中檢測到的物質。
在長時間接觸的情況下,採血時間並不重要。 在急性過度暴露的情況下,鑑於抗凝作用的潛伏期,應在事件發生後至少五天進行生物監測。 為提高這些測試的靈敏度,建議在暴露前測量基線值。
暴露的生物指標。
血液中未改性香豆素的測量已被提議作為監測人體暴露的測試。 然而,應用這些指數的經驗非常有限,主要是因為與監測對凝血系統的影響所需的分析技術相比,分析技術要復雜得多(並且標準化程度較低)(Chalermchaikit、Felice 和 Murphy 1993)。
苯氧除草劑
暴露的生物指標。
苯氧基除草劑幾乎不會在哺乳動物體內發生生物轉化。 在人類中,超過 95% 的 2,4-二氯苯氧乙酸 (2,4-D) 劑量在五天內以原形從尿液中排出,而 2,4,5-三氯苯氧乙酸 (2,4,5-T)和 4-氯-2-甲基苯氧乙酸 (MCPA) 在口服吸收後的幾天內也主要通過尿液原形排出。 尿液中未變化化合物的測量已應用於監測這些除草劑的職業暴露。 在現場研究中,已發現接觸工人的尿液濃度範圍為 0.10-D 為 8 至 2,4 μg/l,0.05-T 為 4.5 至 2,4,5 μg/l,低於 0.1 μg/l MCPA 至 15 μg/l。 建議從暴露結束時開始收集 24 小時的尿液,以測定未變化的化合物。 Draper (1982) 報告了測量尿液中苯氧基除草劑的分析方法。
季銨化合物
暴露的生物指標。
敵草快和百草枯是幾乎不被人體生物轉化的除草劑。 由於它們的高水溶性,它們很容易以原形從尿液中排出。 在接觸百草枯的工人中經常觀察到尿液濃度低於分析檢測限(0.01 微克/升); 而在熱帶國家,百草枯處理不當後的濃度高達 0.73 微克/升。 據報導,皮膚接觸 0.047 至 0.17 μg/h 且吸入接觸低於 1.82 μg/h 的受試者的尿液敵草快濃度低於分析檢測限 (0.01 μg/l)。 理想情況下,應使用暴露結束時收集的 24 小時尿液樣本進行分析。 當這不切實際時,可以在工作日結束時使用現場樣品。
測定血清中的百草枯水平有助於急性中毒情況下的預後:攝入後 0.1 小時血清百草枯水平高達 XNUMX 微克/升的患者很可能存活下來。
Summers(1980 年)審查了百草枯和敵草快測定的分析方法。
雜項農藥
4,6-二硝基鄰甲酚 (DNOC)。
DNOC 是一種於 1925 年推出的除草劑,但由於其對植物和人類的高毒性,該化合物的使用已逐漸減少。 由於血液 DNOC 濃度在一定程度上與不良健康影響的嚴重程度相關,因此已提議測量血液中未變化的 DNOC 以監測職業暴露和評估中毒的臨床過程。
五氯苯酚。
五氯苯酚 (PCP) 是一種廣譜殺菌劑,對雜草、昆蟲和真菌具有殺蟲作用。 血液或尿液未變化的 PCP 測量值已被推薦為監測職業暴露的合適指標(Colosio 等人,1993 年),因為這些參數與 PCP 身體負荷顯著相關。 對於長期接觸 PCP 的工人,採血時間並不重要,而應在接觸後的第二天早上收集尿液樣本。
Shafik 等人 (1973b) 描述了一種用於測量鹵代和硝基酚類農藥的多殘留方法。
表 9. 文獻中提出的農藥暴露生物學監測的其他指標
|
複合 |
生物指標 |
|
|
尿 |
血 |
|
|
溴磷 |
溴磷 |
溴磷 |
|
卡普坦 |
四氫鄰苯二甲酰亞胺 |
|
|
克百威 |
3-羥基呋喃丹 |
|
|
殺蟲脒 |
4-氯-o-甲苯胺衍生物 |
|
|
氯苯甲酸 |
,p-1-二氯二苯甲酮 |
|
|
二氯丙烯 |
硫醇酸代謝物 |
|
|
殺螟松 |
p-硝基甲酚 |
|
|
福美 |
福美雙 |
|
|
氟嘧草酯 |
氟嘧啶 |
|
|
氟蟲脲 |
氟蟲脲 |
|
|
草甘膦 |
草甘膦 |
|
|
馬拉硫磷 |
馬拉硫磷 |
馬拉硫磷 |
|
有機錫化合物 |
錫 |
錫 |
|
三苯嗎啉 |
嗎啉、三苯甲醇 |
|
|
吉拉姆 |
福美雙 |
|
結論
用於監測農藥接觸的生物指標已應用於許多實驗和實地研究。
一些測試,例如血液中的膽鹼酯酶或尿液或血液中選定的未改性殺蟲劑的測試,已通過大量經驗得到驗證。 已針對這些測試提出了生物暴露限值(表 10)。 其他測試,特別是血液或尿液代謝物的測試,由於分析困難或結果解釋的局限性而受到更大的限制。
表 10. 推薦的生物學限值(截至 1996 年)
|
複合 |
生物指標 |
歐洲投資銀行1 |
英美煙草2 |
HBBL3 |
乙肝病毒4 |
|
疼痛抑製劑 |
血液中的疼痛 |
企業排放佔全球 70% |
企業排放佔全球 70% |
70%, |
|
|
挪威石油公司 |
血液中的 DNOC |
20毫克/升, |
|||
|
林丹 |
血液中的林丹 |
0.02mg /升 |
0.02mg /升 |
||
|
對硫磷 |
尿液中的 PNP |
0.5mg /升 |
0.5mg /升 |
||
|
五氯苯酚 (PCP) |
尿液中的五氯苯酚 血漿中的 PCP |
2毫克/升 5毫克/升 |
0.3mg /升 1毫克/升 |
||
|
狄氏劑/艾氏劑 |
血液中的狄氏劑 |
100毫克/升 |
|||
|
異狄氏劑 |
尿液中的抗 12-羥基異丙醇 |
130毫克/升 |
|||
|
滴滴涕 |
血清中的 DDT 和 DDE |
250毫克/升 |
|||
|
香豆素 |
血漿凝血酶原時間 血漿中凝血酶原濃度 |
高於基線 10% 基線的 60% |
|||
|
MCPA |
尿液中的 MCPA |
0.5毫克/升 |
|||
|
2,4-D |
尿液中的 2,4-D |
0.5毫克/升 |
1 美國政府工業衛生學家會議 (ACGIH 1995) 推薦了生物暴露指數 (BEI)。
2 生物耐受值 (BAT) 是由德國工作區化合物健康危害調查委員會 (DFG 1992) 推薦的。
3 WHO 研究小組 (WHO 1982a) 推薦了基於健康的生物限度 (HBBLs)。
4 生物限值 (BLV) 是由國際職業衛生委員會農藥科學委員會的一個研究小組提出的(Tordoir 等人,1994 年)。 如果超過此值,則需要評估工作條件。
該領域正在快速發展,鑑於使用生物指標評估這些物質暴露的重要性,將不斷開發和驗證新的測試。