10. Респираторни систем
Уредници поглавља: Алоис Давид и Грегори Р. Вагнер
Преглед садржаја
Табеле и слике
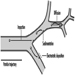
Структура и функција
Мортон Липпманн
Испитивање функције плућа
Улф Улфварсон и Моника Далквист
Болести изазване респираторним иритантима и токсичним хемикалијама
Давид ЛС Рион и Виллиам Н. Ром
Професионална астма
Џорџ Фридман-Хименез и Едвард Л. Петсонк
Болести узроковане органском прашином
Рагнар Риландер и Рицхард СФ Сцхиллинг
Берилијумска болест
Хомаиоун Каземи
Пнеумокониоза: дефиниција
Алоис Давид
Међународна класификација радиографија пнеумокониоза МОР
Мицхел Лесаге
Етиопатогенеза пнеумокониоза
Патрицк Себастиен и Раимонд Бегин
Силикоза
Јохн Е. Паркер и Грегори Р. Вагнер
Плућне болести радника угља
Мицхаел Д. Аттфиелд, Едвард Л. Петсонк и Грегори Р. Вагнер
Болести повезане са азбестом
Маргарет Р. Бецклаке
Болест тврдог метала
Героламо Цхиаппино
Респираторни систем: Разноврсност пнеумокониоза
Стевен Р. Схорт и Едвард Л. Петсонк
Хронична опструктивна болест плућа
Казимиерз Марек и Јан Е. Зејда
Здравствени ефекти вештачких влакана
Џејмс Е. Локи и Клара С. Рос
Респираторни рак
Паоло Бофета и Елисабете Вајдерпас
Професионално стечене инфекције плућа
Ентони А. Марфин, Ен Ф. Хабс, Карл Џ. Масгрејв и Џон Е. Паркер
Столови
Кликните на везу испод да видите табелу у контексту чланка.
1. Региони респираторног тракта и модели депозиције честица
2. Критеријуми за удисање, торакалну и респираторну прашину
3. Резиме респираторних иританата
4. Механизми повреде плућа инхалационим супстанцама
5. Једињења способна за токсичност плућа
6. Дефиниција медицинског случаја професионалне астме
7. Кораци у дијагностичкој евалуацији астме на радном месту
8. Сензибилизујућа средства која могу изазвати професионалну астму
9. Примери извора опасности од излагања органској прашини
КСНУМКС. Агенси у органској прашини са потенцијалном биолошком активношћу
КСНУМКС. Болести изазване органском прашином и њиховим ИЦД кодовима
КСНУМКС. Дијагностички критеријуми за бисинозу
КСНУМКС. Особине берилијума и његових једињења
КСНУМКС. Опис стандардних радиографија
КСНУМКС. ИЛО 1980 Класификација: Радиографије пнеумокониоза
КСНУМКС. Болести и стања у вези са азбестом
КСНУМКС. Главни комерцијални извори, производи и употреба азбеста
КСНУМКС. Преваленција ХОБП
КСНУМКС. Фактори ризика умешани у ХОБП
КСНУМКС. Губитак вентилационе функције
КСНУМКС. Дијагностичка класификација, хронични бронхитис и емфизем
КСНУМКС. Тестирање плућне функције код ХОБП
КСНУМКС. Синтетичка влакна
КСНУМКС. Утврђени респираторни карциногени код људи (ИАРЦ)
КСНУМКС. Вјероватни респираторни карциногени код људи (ИАРЦ)
КСНУМКС. Професионално стечене респираторне заразне болести
фигуре
Поставите показивач на сличицу да бисте видели наслов слике, кликните да бисте видели слику у контексту чланка.
Хронична опструктивна болест плућа
Хронични респираторни поремећаји који се карактеришу различитим степеном диспнеје, кашља, искашљавања слузи и функционалног респираторног оштећења укључени су у општу категорију хроничне неспецифичне болести плућа (ЦНСЛД). Оригинална дефиниција ЦНСЛД, прихваћена на Циба симпозијуму 1959. године, покривала је хронични бронхитис, емфизем и астму. Након тога, дијагностичка терминологија хроничног бронхитиса је редефинисана у складу са концептом да онемогућавање ограничења протока ваздуха представља завршну фазу процеса који непрестано напредује који почиње као бенигно искашљавање изазвано продуженим или понављаним удисањем бронхијалних иританса („Британска хипотеза“) . Концепт је доведен у питање 1977. године и од тада се хиперсекреција и опструкција протока ваздуха сматрају неповезаним процесима. Алтернативна хипотеза, позната као „холандска хипотеза“, прихватајући улогу пушења и загађења ваздуха у етиологији хроничног ограничења протока ваздуха, указује на кључну и могуће узрочну улогу осетљивости домаћина, која се манифестује као нпр. астматична склоност. Накнадне студије су показале да обе хипотезе могу допринети разумевању природне историје хроничне болести дисајних путева. Иако је закључак о безначајној прогностичкој вредности хиперсекреторног синдрома генерално прихваћен као утемељен, скорашња истраживања су показала значајну повезаност хиперсекреторног поремећаја и повећаног ризика од развоја ограничења протока ваздуха и респираторног морталитета.
Тренутно, термин ЦНСЛД комбинује две главне категорије хроничних респираторних поремећаја, астму (о којој се говори у посебном чланку овог поглавља) и хроничну опструктивну болест плућа (ХОБП).
Дефиниција
У документу који је објавило Америчко торакално друштво (АТС) (1987), ХОБП је дефинисана као поремећај који карактеришу абнормални тестови експираторног тока који се не мењају значајно током периода посматрања од неколико месеци. Узимајући у обзир функционалне и структурне узроке ограничења протока ваздуха, дефиниција укључује следеће неастматичне поремећаје дисајних путева: хронични бронхитис, емфизем и болест периферних дисајних путева. Важне заједничке карактеристике ХОБП су изражене патофизиолошке абнормалности које се углавном испољавају као различит степен хроничног ограничења протока ваздуха (ЦАЛ). Хронично ограничење протока ваздуха може се наћи код субјекта са било којом болешћу укљученом у рубрику ХОБП.
Хронични бронхитис се дефинише као абнормално стање респираторног тракта, које карактерише упоран и прекомерно продуктиван кашаљ, који одражава хиперсекрецију слузокоже у дисајним путевима. У епидемиолошке сврхе, дијагноза хроничног бронхитиса је заснована на одговорима на скуп стандардних питања укључених у упитник Савета за медицинска истраживања (МРЦ) или АТС упитник о респираторним симптомима. Поремећај се дефинише као кашаљ и искашљавање слузи који се јављају већином дана током најмање три месеца у години, током најмање две узастопне године.
Емфизем се дефинише као анатомска промена плућа коју карактерише абнормално повећање ваздушних простора дистално од терминалне бронхиоле, праћено деструкцијом ацинарне архитектуре. Емфизем често коегзистира са хроничним бронхитисом.
Термин периферних дисајних путева болест or болест малих дисајних путева користи се за описивање абнормалног стања дисајних путева пречника мањег од 2 до 3 мм. Упала, опструкција и вишак производње слузи у овом делу бронхијалног стабла примећени су код различитих клиничких ентитета, укључујући хронични бронхитис и емфизем. Патолошки докази локалних структурних абнормалности и концепт да уочене промене могу представљати рану фазу у природној историји хроничне болести дисајних путева, стимулисали су касних 1960-их и 1970-их на брз развој функционалних тестова дизајнираних да испитају физиолошка својства дисајних путева. периферних дисајних путева. Сходно томе, термин болест периферних дисајних путева генерално се подразумева да се односи на структурне абнормалности или функционални дефект.
ЦАЛ је функционални знак ХОБП. Израз се односи на повећан отпор протоку ваздуха, што резултира упорним успоравањем током принудног издисања. Њихова дефиниција и основно клиничко и патофизиолошко знање имплицирају два важна дијагностичка трага. Прво, мора се показати да стање има хронични ток, а рана препорука из 1958. захтевала је присуство ЦАЛ-а дуже од једне године да би се испунили дијагностички критеријуми. Временски оквир који је недавно предложен је мање ригорозан и односи се на демонстрацију квара у периоду од три месеца. У надзору ЦАЛ-а у вези са радом, стандардна спирометријска процена пружа довољно средстава за идентификацију ЦАЛ-а, на основу смањења запремине принудног издисаја у једној секунди (ФЕВ1) и/или у односу ФЕВ1 на форсирани витални капацитет (ФВЦ).
Обично се ЦАЛ дијагностикује када се ФЕВ1 вредност се смањује испод 80% предвиђене вредности. Према функционалној класификацији ЦАЛ-а коју препоручује Америчко торакално друштво:
- благо оштећење настаје када вредност ФЕВ1 је испод 80% и изнад 60% предвиђене вредности
- умерено оштећење се јавља када ФЕВ1 је у распону од 40% до 59% предвиђене вредности
- тешко оштећење се јавља када ФЕВ1 је испод 40% предвиђене вредности.
Када се степен оштећења процени вредношћу ФЕВ1/ФВЦ однос, благи дефект се дијагностикује ако однос пада између 60% и 74%; умерено оштећење ако се тај однос креће од 41% до 59%; и озбиљно оштећење ако је тај однос 40% или мањи.
Преваленција ХОБП
Акумулирани докази указују да је ХОБП чест проблем у многим земљама. Његова преваленција је већа код мушкараца него код жена и расте са годинама. Хронични бронхитис, добро стандардизован дијагностички облик ХОБП, је два до три пута чешћи код мушкараца него код жена. Велика истраживања показују да обично између 10% и 20% одраслих мушкараца у општој популацији испуњава дијагностичке критеријуме хроничног бронхитиса (Табела 18). Болест је много чешћа код пушача, и код мушкараца и код жена. Појава ХОБП у професионалним популацијама је разматрана у наставку.
Табела 1. Преваленција ХОБП у одабраним земљама – резултати великих истраживања
| земља | година | становништво | Мушкарци | Женке | ||||
| СМК (%) | ЦБ (%) | ЦОПД/ЦАЛ (%) | СМК (%) | ЦБ (%) | ЦОПД/ЦАЛ (%) | |||
| САД | 1978 | 4,699 | 56.6 | 16.5 | Не | 36.2 | 5.9 | Не |
| САД | 1982 | 2,540 | 52.8 | 13.0 | 5.2 | 32.2 | 4.1 | 2.5 |
| UK | 1961 | 1,569 | 17.0 | Не | Не | 8.0 | Не | |
| Италија | 1988 | 3,289 | 49.2 | 13.1 | Не | 26.9 | 2.8 | Не |
| Пољска | 1986 | 4,335 | 59.6 | 24.2 | 8.5 | 26.7 | 10.4 | 4.9 |
| Непал | 1984 | 2,826 | 78.3 | 17.6 | Не | 58.9 | 18.9 | Не |
| Јапан | 1977 | 22,590 | Не | 5.8 | Не | Не | 3.1 | Не |
| Аустралија | 1968 | 3,331 | Не | 6.3 | Не | Не | 2.4 | Не |
Легенда: СМК = навика пушења; ЦБ = хронични бронхитис; ЦОПД/ЦАЛ = хронична опструктивна болест плућа/хронично ограничење дисајних путева; бр = није пријављено.
Измењено уз дозволу: Воолцоцк 1989.
Фактори ризика од ХОБП, укључујући ефекат професионалне изложености
ХОБП је поремећај мултифакторске етиологије. Бројне студије су пружиле доказе о узрочној зависности ХОБП од многих фактора ризика, категорисаних као домаћин и фактори животне средине. Улога професионалне изложености међу факторима ризика животне средине у настанку ХОБП је препозната акумулацијом епидемиолошких доказа објављених у периоду од 1984. до 1988. године. Недавно су потврђени независни ефекти пушења и професионалне изложености, на основу резултата објављених студија. од 1966. до 1991. Табела 2 сумира тренутно стање знања о мултифакторској етиологији ХОБП.
Табела 2. Фактори ризика укључени у ХОБП
| Фактор повезан са |
Установљени | Претпостављено |
| Домаћин | Пол Аге Недостатак антитрипсина | Атопија Породични фактори Повећана реактивност дисајних путева Прошло здравље |
| животна средина | Дувански дим (лични) | Дувански дим (еколошка) Загађење ваздуха Професионална изложеност |
Репродуковано уз дозволу: Бецклаке ет ал. 1988.
Појава хроничног бронхитиса у професионалним популацијама је потенцијални маркер значајне изложености професионалним иритантима. Значајан утицај изложености индустријској прашини на развој хроничног бронхитиса документован је код радника запослених у рударству угља, индустрији гвожђа и челика, као и у текстилној, грађевинској и пољопривредној индустрији. Генерално, прашњава средина је повезана са већом преваленцом симптома хроничног искашљавања. Студије преваленције, међутим, подлежу „ефекту здравог радника“, пристрасности која резултира потцењивањем утицаја штетног излагања на радном месту на здравље. Уверљивији, али мање доступни су подаци о учесталости болести. У одређеним занимањима стопа инциденције хроничног бронхитиса је висока и креће се од 197-276/10,000 код фармера до 380/10,000 код инжењерских радника и 724/10,000 код рудара и каменолома, у поређењу са 108/10,000 код белих радника.
Овај образац, као и узрочни ефекат пушења, у складу су са концептом да хронични бронхитис представља уобичајени одговор на хронично удисање респираторних иританата.
Сматра се да штетан ефекат оптерећења плућном прашином доводи до хроничне неспецифичне упале бронхијалног зида. Ова врста инфламаторног одговора је документована код радника изложених органској прашини и њеним састојцима, као што су на пример зрно и ендотоксин, оба одговорна за неутрофилну упалу. Улога индивидуалне осетљивости се не може искључити, а познати фактори везани за домаћина укључују прошле респираторне инфекције, ефикасност механизама уклањања и лоше одређене генетске факторе, док пушење цигарета остаје један од најснажнијих еколошких узрока хроничног бронхитиса.
Допринос професионалне изложености етиологији емфизема није јасно схваћен. Претпостављени узрочни фактори укључују азотни оксид, озон и кадмијум, као што сугеришу експериментална запажања. Подаци које пружа епидемиологија занимања су мање убедљиви и може бити тешко добити због обично ниског нивоа изложености на радном месту и преовлађујућег ефекта пушења. Ово је посебно важно у случају тзв центриацинарни емфизем. Други патолошки облик болести, панацинарни емфизем, сматра се наследним и повезан је са алфа1- недостатак антитрипсина.
Бронхиоларна и перибронхиоларна инфламација, праћена прогресивним сужавањем захваћеног сегмента бронхијалног стабла (болест периферних дисајних путева или констриктивни бронхиолитис) може се видети у различитим стањима која су у основи симптома ХОБП, у различитим фазама природне историје. У професионалном окружењу, болест обично прати акутну повреду плућа услед удисања токсичних испарења, као што су сумпор-диоксид, амонијак, хлор и оксиди азота. Међутим, професионална епидемиологија констриктивног бронхиолитиса углавном остаје нејасна. Очигледно, његове ране фазе је тешко идентификовати због неспецифичне симптоматологије и ограничења дијагностичке процедуре. Више се зна о случајевима након индустријских удеса. У супротном, болест може проћи неоткривена до развоја очигледне симптоматологије и објективног респираторног оштећења (тј. хроничног ограничења протока ваздуха).
ЦАЛ се не ретко налази у различитим групама занимања и, као што је документовано контролисаним студијама, његова преваленција код плавих овратника може премашити ону код белих овратника. Због сложене етиологије ЦАЛ-а, укључујући ефекат пушења и факторе ризика у вези са домаћином, ране студије о повезаности хроничног ограничења протока ваздуха са изложеношћу на радном месту биле су неуверљиве. Модерна професионална епидемиологија, која користи циљно оријентисан дизајн и моделирање односа изложеност-одговор, пружила је доказе о повезаности капацитета протока ваздуха са изложеношћу минералној и органској прашини, димовима и гасовима.
Лонгитудиналне студије засноване на радној снази спроведене на радницима изложеним минералној и органској прашини, испарењима и гасовима показују да је губитак плућне функције повезан са професионалним излагањем. Резултати сажети у табели 3 доказују значајан утицај изложености прашини у рударству угља и гвожђа, азбестно-цементној индустрији, радницима у челичанима и топионицама и у фабрикама целулозе. Један број анализираних изложености се састоји од изложености прашини и димовима (као што су нехалогенизовани угљоводоници, боје, смоле или лакови) као и гасовима (као што су сумпор-диоксид или оксиди азота). Према резултатима свеобухватног прегледа, ограниченог на најважеће и најсистематскије анализиране чланке о ХОБП и изложености прашини на радном месту, може се проценити да се може очекивати да ће 80 од 1,000 рудара непушача развити најмање 20% губитка ФЕВ-а.1 након 35 година рада са средњом концентрацијом прашине која се може удахнути од 2 мг/м3, а за рударе злата који не пуше, одговарајући ризик би могао бити три пута већи.
Табела 3. Губитак вентилационе функције у односу на професионалну изложеност: резултати одабраних лонгитудиналних студија заснованих на радној снази
| Земља (година) | Предмети и експозиције | Коришћен тест | Годишњи губитак функције* | |||
| NE | E | NS | S | |||
| Велика Британија (КСНУМКС) | 1,677 рудара угља | ФЕВ мл | 37 | 41 (ав) 57 (мак) |
37 | 48 |
| САД (КСНУМКС) | 1,072 рудара угља | ФЕВ мл | 40 | 47 | 40 | 49 |
| Италија (КСНУМКС) | 65 радника азбестног цемента | ФЕВ мл | 9 | 49 | Није дато | Није дато |
| Шведска (КСНУМКС) | 70 радника азбестног цемента | ФЕВ% | 4.2 | 9.2 | 3.7 | 9.4 |
| Француска (КСНУМКС) | 871 рудара гвожђа | ФЕВ% | 6 | 8 | 5 | 7 |
| Француска (КСНУМКС) | 159 челичана | ФЕВ% | 0.6 | 7.4 | Није дато | Није дато |
| Канада (КСНУМКС) | 179 радника рудника и топионице | ФЕВ/ФВЦ% | 1.6 | 3.1 | 2.0 | 3.4 |
| Француска (КСНУМКС) | 556 радника у фабрикама | ФЕВ мл | 42 | 50 52 (прашина) 47 (гасови) 55 (топлота) |
40 | 48 |
| Финска (КСНУМКС) | 659 радника целулозе | ФЕВ мл | Без ефекта | Без ефекта | 37 | 49 |
| Канада (КСНУМКС) | 972 радника рудника и топионице | ФЕВ мл | 69 (печење) 49 (пећ) 33 (рударство) |
41 | 54 | |
* Табела приказује просечан годишњи губитак плућне функције код изложених (Е) у поређењу са неекспонираним (НЕ), и код пушача (С) у поређењу са непушачима (НС). Независни ефекти пушења (С) и/или изложености (Е) показали су се значајним у анализама које су спровели аутори у свим студијама осим у финској студији.
Измењено уз дозволу од: Бецклаке 1989.
Одабране студије спроведене на радницима у житарицама показују утицај професионалне изложености органској прашини на лонгитудиналне промене функције плућа. Иако су ограничени по броју и трајању праћења, налази документују независну везу пушења са годишњим губитком плућне функције (у односу на излагање прашини од житарица).
patogeneza
Централни патофизиолошки поремећај ХОБП је хронично ограничење протока ваздуха. Поремећај је резултат сужења дисајних путева – стање које има сложен механизам код хроничног бронхитиса – док код емфизема опструкција дисајних путева настаје углавном услед ниског еластичног трзаја плућног ткива. Оба механизма често коегзистирају.
Структурне и функционалне абнормалности које се виде код хроничног бронхитиса укључују хипертрофију и хиперплазију субмукозних жлезда удружене са хиперсекрецијом слузокоже. Инфламаторне промене доводе до хиперплазије глатких мишића и отока слузокоже. Хиперсекреција слузокоже и сужавање дисајних путева погодују бактеријским и вирусним инфекцијама респираторног тракта, што може додатно повећати опструкцију дисајних путева.
Ограничење протока ваздуха код емфизема одражава губитак еластичног трзаја као последицу деструкције еластинских влакана и колапса бронхиоларног зида услед високе савитљивости плућа. Сматра се да је уништење еластинских влакана резултат неравнотеже у протеолитичко-антипротеолитичком систему, у процесу познатом и као недостатак инхибитора протеазе. Алпха1-антитрипсин је најмоћнија протеаза која инхибира ефекат еластазе на алвеоле код људи. Неутрофили и макрофаги који ослобађају еластазу се акумулирају као одговор на локалне инфламаторне медијаторе и удисање различитих респираторних иританата, укључујући дувански дим. Други, мање моћни инхибитори су а2-макроглобулин и инхибитор еластазе мале тежине, који се ослобађа из субмукозних жлезда.
Недавно је хипотеза о недостатку антиоксиданса испитивана због њене улоге у патогенетским механизмима емфизема. Хипотеза тврди да оксиданти, ако их не инхибирају антиоксиданси, узрокују оштећење плућног ткива, што доводи до емфизема. Познати оксиданти укључују егзогене факторе (озон, хлор, оксиди азота и дувански дим) и ендогене факторе као што су слободни радикали. Најважнији антиоксидативни фактори укључују природне антиоксиданте као што су витамини Е и Ц, каталаза, супероксид дисмутаза, глутатион, церулоплазмин и синтетички антиоксиданси као што су Н-ацетилцистеин и алопуринол. Све је више доказа о синергизму у погледу механизама недостатка антиоксиданса и инхибитора протеазе у патогенези емфизема.
Патологија
Патолошки, хронични бронхитис карактерише хипертрофија и хиперплазија жлезда у субмукози великих дисајних путева. Као резултат тога, однос дебљине бронхијалне жлезде и дебљине зида бронхија (тзв. Реид индек) повећава. Друге патолошке абнормалности укључују метаплазију цилијарног епитела, хиперплазију глатких мишића и неутрофилне и лимфоцитне инфилтрације. Промене у великим дисајним путевима често су праћене патолошким абнормалностима малих бронхиола.
Патолошке промене у малим бронхиолама су доследно документоване као различити степен инфламаторног процеса зидова дисајних путева. Након увођења концепта болести малих дисајних путева, фокус је био на морфологији појединих сегмената бронхиола. Хистолошка процена мембранозних бронхиола, проширених касније на респираторне бронхиоле, показује запаљење зида, фиброзу, хипертрофију мишића, таложење пигмента, епителни пехар и сквамозну метаплазију и интралуминалне макрофаге. Патолошке абнормалности горе описаног типа су назване „болест дисајних путева изазвана минералном прашином“. Повезано стање које се показује у овом сегменту респираторног тракта је перибронхиоларни фиброзирајући алвеолитис, за који се сматра да представља рану реакцију плућног ткива на удисање минералне прашине.
Патолошке промене код емфизема могу се категорисати као центриацинарни емфизем or панацинарни емфизем. Први ентитет је углавном ограничен на центар ацинуса, док други облик укључује промене у свим структурама ацинуса. Иако се сматра да панацинарни емфизем одражава наследни недостатак инхибитора протеазе, оба облика могу коегзистирати. Код емфизема терминалне бронхиоле показују знаке упале и дистални ваздушни простори су ненормално увећани. Структурна деструкција укључује алвеоле, капиларе и може довести до стварања великих абнормалних ваздушних простора (емфизем булосум). Центриацинарни емфизем се обично налази у горњим режњевима плућа, док се панацинарни емфизем обично налази у доњим плућним режњевима.
Клинички симптоми
Хронични кашаљ и искашљавање слузи су два главна симптома хроничног бронхитиса, док је диспнеја (кратко дисање) клиничка карактеристика емфизема. У напредним случајевима, симптоми хроничног искашљавања и диспнеје обично коегзистирају. Почетак и напредак диспнеје сугерише развој хроничног ограничења протока ваздуха. Према симптомима и физиолошком статусу, клиничка слика хроничног бронхитиса обухвата три облика болести: једноставан, мукопурулентни и опструктивни бронхитис.
Код хроничног бронхитиса, резултати аускултације грудног коша могу открити нормалне звукове даха. У узнапредовалим случајевима може доћи до продуженог времена издисаја, звиждања и хрипања који се чују током издисања. Цијаноза је честа код узнапредовалог опструктивног бронхитиса.
Клиничка дијагноза емфизема је тешка у раној фази. Диспнеја може бити појединачни налаз. Пацијент са узнапредовалим емфиземом може имати грудни кош и знаке хипервентилације. Као резултат хиперинфлације плућа, други налази укључују хиперрезонанцију, смањење екскурзије дијафрагме и смањене звукове даха. Цијаноза је ретка.
Због сличних узрочних фактора (претежно ефекат дуванског дима) и сличне презентације дијагноза хроничног бронхитиса у односу на емфизем може бити тешка, посебно ако хронично ограничење протока ваздуха доминира сликом. Табела 4 пружа неке назнаке који су од помоћи за дијагнозу. Напредни облик ХОБП може имати два екстремна типа: преовлађујући бронхитис („плави надувавање“) или предоминантни емфизем („ружичасти пудер“).
Табела 4. Дијагностичка класификација два клиничка типа ХОБП, хроничног бронхитиса и емфизема
| Знаци/симптоми | Преовлађујући бронхитис („Плави надувац“) |
Преовлађујући емфизем („Пинк Пуффер“) |
| Телесна маса | povećana | Смањено |
| Цијаноза | чести | Ријетко |
| Кашљати | Преовлађујући симптом | Испрекидано |
| Спутум | Велика количина | Редак |
| диспнеја | Обично се обележава током вежбања | Преовлађујући симптом |
| Звукови даха | Нормално или благо смањено, адвентивни плућни звуци |
Смањено |
| Плућно | чести | Ријетко |
| Респираторне инфекције | чести | Ријетко |
Радиологија грудног коша има ограничену дијагностичку вредност код хроничног бронхитиса и раних стадијума емфизема. Узнапредовали емфизем показује радиолошки образац повећане радиолуценције (хиперинфлације). Компјутеризована томографија даје бољи увид у локацију и величину емфизематозних промена, укључујући диференцијацију између центриацинарног и панацинарног емфизема.
Тестирање плућне функције има добро утврђену позицију у дијагностичкој евалуацији ХОБП (табела 5). Батерија тестова који су од практичног значаја у функционалној процени хроничног бронхитиса и емфизема обухвата функционални резидуални капацитет (ФРЦ), резидуални волумен (РВ), укупан капацитет плућа (ТЛЦ), ФЕВ.1 и ФЕВ1/ВЦ, отпор дисајних путева (Рaw), статичка усклађеност (Цst), еластични трзај (ПЛ,ел), гасови из крви (ПаО2, ПаЦО2) и капацитет дифузије (ДЛЦО).
Табела 5. Испитивање плућне функције у диференцијалној дијагнози два клиничка типа ХОБП, хроничног бронхитиса и емфизема
| Тест функције плућа | Преовлађујући бронхитис („Плави надувац“) |
Преовлађујући емфизем („Пинк Пуффер“) |
| РВ, ФРЦ, ТЛЦ | Нормално или благо повећано | Значајно повећан |
| ФЕВ1 , ФЕВ1 /ВЦ | Смањено | Смањено |
| Raw | Значајно повећан | Нешто повећано |
| Cst | нормалан | Значајно повећан |
| PЛ,ел | нормалан | Значајно повећан |
| ПаО2 | Значајно повећан | Нешто смањено |
| ПаЦО2 | povećana | нормалан |
| DЛЦО | Нормално или благо смањено | Смањено |
РВ = резидуални волумен; ФРЦ = функционални преостали капацитет; ТЛЦ = укупан капацитет плућа; ФЕВ1 = запремина форсираног издисаја у првој секунди и ВЦ = витални капацитет; Рaw = отпор дисајних путева; Цst = статичка усклађеност; ПЛ,ел = еластични трзај; ПаО2 и ПаЦО2 = гасови из крви; ДЛЦО = капацитет дифузије.
Клиничка дијагноза болести периферних дисајних путева није могућа. Веома често болест прати хронични бронхитис или емфизем или чак претходи клиничкој презентацији оба потоња облика или ХОБП. Изоловани облик болести периферних дисајних путева може се истражити испитивањем плућне функције, иако је функционални статус периферних дисајних путева тешко проценити. Овај део бронхијалног стабла доприноси мање од 20% укупног отпора протока ваздуха и изоловане, благе абнормалности у малим дисајним путевима се сматрају испод нивоа детектабилности конвенционалне спирометрије. Осетљивије методе дизајниране за мерење функције периферних дисајних путева укључују низ тестова, међу којима се најчешће користе следећи: максимална брзина средњег издисаја (ФЕФ25-75), брзине протока при малим запреминама плућа (МЕФ50, МЕФ25), индекс азота у једном даху (СБН2/л), капацитет затварања (ЦЦ), проводљивост протока ваздуха узводно (Гus) и усклађеност зависна од фреквенције (Цfd). Генерално, сматра се да ови тестови имају ниску специфичност. На теоријским основама ФЕФ25-75 и МЕФ50,25 треба пре свега да одражава механизме ограничавања калибра, док СБН2Сматра се да је /л специфичнији за механичка својства ваздушних простора. Први индекси се најчешће користе у епидемиологији рада.
Диференцијална дијагноза
Основне разлике између хроничног бронхитиса и емфизема приказане су у табелама 4 и 5. Међутим, у појединачним случајевима диференцијалну дијагнозу је тешко и понекад немогуће спровести са приличним степеном поверења. У неким случајевима је такође тешко разликовати ХОБП и астму. У пракси, астма и ХОБП нису јасни ентитети и постоји велики степен преклапања између ове две болести. Код астме, опструкција дисајних путева је обично повремена, док је код ХОБП константна. Ток ограничења протока ваздуха је варијабилнији код астме него код ХОБП.
Управљање предметима
Клиничко лечење ХОБП подразумева престанак пушења, што је једина најефикаснија мера. Професионално излагање респираторним иритантима треба прекинути или избегавати. Клинички менаџмент треба да се фокусира на правилно лечење респираторних инфекција и треба да укључује редовне вакцинације против грипа. Бронходилатациона терапија је оправдана код пацијената са ограниченим протоком ваздуха и требало би да обухвата б2-адренергички агонисти и антихолинергици, који се дају као монотерапија или у комбинацији, пожељно као аеросол. Теофилин је још увек у употреби иако је његова улога у лечењу ХОБП контроверзна. Дуготрајна терапија кортикостероидима може бити ефикасна у неким случајевима. Бронхијална хиперсекреција се често лечи мукоактивним лековима који утичу на производњу слузи, структуру слузи или мукоцилијарни клиренс. Процена ефеката муколитичке терапије је тешка јер се ови лекови не користе као монотерапија ХОБП. Пацијенти са хипоксемијом (ПаО2 једнак или мањи од 55 мм Хг) квалификују се за дуготрајну терапију кисеоником, третман који је олакшан приступом преносивим оксигенаторима. Терапија повећања са алфа1-антитрипсин се може сматрати код емфизема са потврђеном алфа1-недостатак антитрипсина (фенотип ПиЗЗ). Истражује се ефекат антиоксидативних лекова (као што су витамин Е и Ц) на напредовање емфизема.
Превенција
Превенција ХОБП би требало да почне кампањама против пушења које су усмерене и на општу популацију и на ризичне групе занимања. У радном окружењу, контрола и превенција изложености респираторним иритантима су од суштинског значаја и увек представљају приоритет. Ове активности треба да имају за циљ ефикасно смањење загађења ваздуха на безбедне нивое, обично дефинисане такозваним дозвољеним нивоима изложености. Пошто број загађивача ваздуха није регулисан или није адекватно регулисан, сваки напор да се смањи изложеност је оправдан. У околностима у којима је такво смањење немогуће постићи, потребна је лична заштита за дисање да би се смањио ризик од индивидуалног излагања штетним агенсима.
Медицинска превенција ХОБП у радном окружењу укључује два важна корака: програм надзора респираторног здравља и програм едукације запослених.
Програм надзора респираторног здравља укључује редовну евалуацију респираторног здравља; почиње са иницијалном проценом (анамнеза, физички преглед, рендгенски снимак грудног коша и стандардно испитивање плућне функције) и наставља да се обавља периодично током периода запослења. Програм има за циљ да процени основно респираторно здравље радника (и да идентификује раднике са субјективним и/или објективним респираторним оштећењем) пре почетка рада и да открије ране знаке респираторног оштећења током сталног надзора радника. Раднике са позитивним налазима треба повући из излагања и упутити на даљу дијагностичку евалуацију.
Програм образовања запослених треба да се заснива на поузданом препознавању респираторних опасности присутних у радном окружењу и треба да га осмисле здравствени радници, индустријски хигијеничари, инжењери безбедности и менаџмент. Програм треба да пружи радницима одговарајуће информације о респираторним опасностима на радном месту, потенцијалним респираторним ефектима изложености и релевантним прописима. Такође би требало да укључује промоцију безбедних радних пракси и здравог начина живота.
Здравствени ефекти вештачких влакана
Индустријска употреба различитих врста вештачких влакана је у порасту, посебно откако су постављена ограничења на употребу азбеста с обзиром на његове познате опасности по здравље. Потенцијал штетних ефеката на здравље у вези са производњом и употребом вештачких влакана се још увек проучава. Овај чланак ће пружити преглед општих принципа у вези са потенцијалом токсичности у вези са таквим влакнима, преглед различитих типова влакана у производњи (као што је наведено у табели 1) и ажурирање у вези са постојећим и текућим студијама њихових потенцијалних утицаја на здравље .
Табела 1. Синтетичка влакна
| Умјетна влакна |
Алуминијум оксид Угљеник/графит Кевлар® Пара-Арамид Силицијум карбидна влакна и |
|
| Умјетна стаклена влакна |
Стаклена влакна
Минерална вуна
Ватростална керамичка влакна |
Стаклена вуна Камена вуна |
Одреднице токсичности
Примарни фактори који се односе на потенцијал за токсичност услед излагања влакнима су:
- димензија влакана
- издржљивост влакана и
- доза до циљног органа.
Генерално, влакна која су дуга и танка (али величине која се може удахнути) и издржљива имају највећи потенцијал за изазивање штетних ефеката ако се испоруче у плућа у довољној концентрацији. Токсичност влакана је у корелацији у краткорочним студијама инхалације на животињама са упалом, цитотоксичношћу, измењеном функцијом макроцита и биоперзистенцијом. Карциногени потенцијал је највероватније повезан са оштећењем ћелијске ДНК путем формирања радикала без кисеоника, формирања кластогених фактора или погрешне сегрегације хромозома у ћелијама у митози – самостално или у комбинацији. Влакна која се могу удахнути су она пречника мањег од 3.0 до 3.5 мм и дужине мање од 200 μм. Према „Стантоновој хипотези“, карциногени потенцијал влакана (како је утврђено студијама имплантације плеуре на животињама) је повезан са њиховом димензијом (највећи ризик је повезан са влакнима пречника мањег од 0.25 μм и дужине веће од 8 мм) и издржљивости (Стантон ет ал. 1981). Природна минерална влакна, као што је азбест, постоје у поликристалној структури која има склоност да се цепа дуж уздужних равни, стварајући тања влакна са већим односом дужине и ширине, која имају већи потенцијал за токсичност. Велика већина вештачких влакана је некристална или аморфна и ломиће се окомито на своју уздужну раван у краћа влакна. Ово је важна разлика између азбестних и неазбестних влакнастих силиката и вештачких влакана. Трајност влакана таложених у плућима зависи од способности плућа да очисте влакна, као и од физичких и хемијских својстава влакана. Трајност вештачких влакана може се променити у процесу производње, у складу са захтевима крајње употребе, додавањем одређених стабилизатора као што је Ал.2O3. Због ове варијабилности у хемијским састојцима и величини вештачких влакана, њихова потенцијална токсичност се мора проценити на основу типа влакна по тип влакна.
Умјетна влакна
Алуминијум оксидна влакна
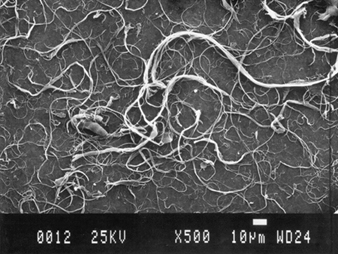
Токсичност кристалног алуминијум-оксидног влакна је сугерисана у извештају о случају плућне фиброзе код радника запосленог у топионици алуминијума 19 година (Једерлиниц ет ал. 1990). Његов рендгенски снимак грудног коша открио је интерстицијску фиброзу. Анализа плућног ткива техникама електронске микроскопије показала је 1.3×109 кристалних влакана по граму сувог плућног ткива, или десет пута више влакана од броја азбестних влакана пронађених у плућном ткиву од рудара хризотилног азбеста са азбестозом. Потребно је даље проучавање да би се утврдила улога кристалних влакана алуминијум оксида (слика 1) и плућне фиброзе. Овај извештај случаја, међутим, сугерише потенцијал за фибризацију када постоје одговарајући услови околине, као што је повећан проток ваздуха кроз растопљене материјале. И фазно-контрастна светлосна микроскопија и електронска микроскопија са рендгенском анализом дисперзије енергије треба да се користе за идентификацију потенцијалних влакана у ваздуху у радном окружењу и у узорцима плућног ткива у случајевима када постоје клинички налази у складу са пнеумокониозом изазваном влакнима.
Слика 1. Скенирајући електронски микрограф (СЕМ) влакана од алуминијум оксида.
Љубазношћу Т. Хестерберга.
Карбон/графитна влакна
Угљична смола, рајонска или полиакрилонитрилна влакна загрејана на 1,200°Ц формирају аморфна угљенична влакна, а када се загреју изнад 2,20°Ц формирају кристална графитна влакна (слика 2). Могу се додати везива од смоле да би се повећала чврстоћа и омогућило обликовање и машинска обрада материјала. Генерално, ова влакна имају пречник од 7 до 10 μм, али се варијације у величини јављају због процеса производње и механичке манипулације. Композити угљеник/графит се користе у индустрији авиона, аутомобила и спортске опреме. Изложеност честицама угљеника/графита величине удисања може се десити током процеса производње и механичком манипулацијом. Штавише, мале количине влакана величине удисања могу се произвести када се композити загреју на 900 до 1,10 °Ц. Постојећа сазнања о овим влакнима су неадекватна да дају дефинитивне одговоре о њиховом потенцијалу за изазивање штетних ефеката на здравље. Студије које су укључивале интратрахеално убризгавање различитих композитних прахова графитних влакана код пацова дале су хетерогене резултате. Три испитана узорка прашине су показала минималну токсичност, а два узорка су произвела конзистентну токсичност што се манифестује цитотоксичношћу за алвеоларне макрофаге и разликама у укупном броју ћелија из плућа (Мартин, Меиер и Луцхтел 1989). Кластогени ефекти су уочени у студијама мутагености влакана на бази смоле, али не и угљеничних влакана на бази полиакрилонитрила. Десетогодишња студија радника у производњи угљеничних влакана, који производе влакна пречника 8 до 10 мм, није открила никакве абнормалности (Јонес, Јонес и Лиле 1982). Док не буду доступне даље студије, препоручује се да изложеност угљичним/графитним влакнима величине удисања буде 1 влакно/мл (ф/мл) или ниже, и да се изложеност честицама композитних честица које се могу удахнути одржава испод тренутног стандарда за удисање прашине за досадна прашина.
Слика 2. СЕМ карбонских влакана.
Кевлар пара-арамидна влакна
Кевлар пара-арамидна влакна су приближно 12 μм у пречнику, а закривљена врпцаста влакна на површини влакана су мања од 1 мм ширине (слика 3). Влакна се делимично љуште од влакана и спајају се са другим фибрилима да формирају грудве које се не могу удисати. Физичка својства Кевлар влакна укључују значајну отпорност на топлоту и затезну чврстоћу. Имају много различитих употреба, служећи као средство за ојачање у пластици, тканинама и гуми, и као материјал за трење кочница у аутомобилима. Осмочасовни временски пондерисани просек (ТВА) нивоа фибрила током производње и примене у крајњој употреби креће се од 0.01 до 0.4 ф/мл (Мерриман 1989). Веома низак ниво Кевлар арамидна влакна се стварају у прашини када се користе у материјалима за трење. Једини доступни подаци о утицајима на здравље су из студија на животињама. Студије инхалације пацова које су укључивале временске периоде од једне до две године и излагање фибрилима при 25, 100 и 400 ф/мл откриле су алвеоларну бронхиоларизацију која је била зависна од дозе. Лагана фиброза и фиброзне промене алвеоларног канала такође су примећене при вишим нивоима изложености. Фиброза је можда била повезана са преоптерећењем механизама плућног клиренса. Тип тумора јединствен за пацове, цистични кератинизирајући тумор сквамозних ћелија, развио се код неколико испитиваних животиња (Лее ет ал. 1988). Краткорочне студије инхалације пацова показују да фибриле имају малу издржљивост у плућном ткиву и да се брзо чисте (Вархеит ет ал. 1992). Нема доступних студија о утицају излагања на људско здравље Кевлар пара-арамидна влакна. Међутим, с обзиром на доказе о смањеној биоперзистентности и с обзиром на физичку структуру Кевлар, здравствени ризици би требало да буду минимални ако се изложеност фибрилима одржава на 0.5 ф/мл или мање, као што је сада случај у комерцијалним применама.
Слика 3. СЕМ кевлар пара-арамидних влакана.
Силицијум карбидна влакна и бркови
Силицијум карбид (карборунд) је широко коришћен абразивни и ватростални материјал који се производи комбиновањем силицијум диоксида и угљеника на 2,400°Ц. Силицијум карбидна влакна и бркови—слика 4 (Харпер ет ал. 1995)—могу да се генеришу као нуспроизводи производње кристала силицијум карбида или се могу наменски производити као поликристална влакна или монокристални бркови. Влакна су углавном мањег од 1 до 2 μм у пречнику и крећу се од 3 до 30 μм у дужини. Бркови су просечно 0.5 μм у пречнику и 10 μм у дужини. Уградња силицијум карбидних влакана и бркова додаје снагу производима као што су композити са металном матрицом, керамика и керамичке компоненте. Изложеност влакнима и брковима може се десити током процеса производње и производње и потенцијално током процеса машинске обраде и завршне обраде. На пример, показало се да краткотрајна изложеност током руковања рециклираним материјалима достиже нивое до 5 ф/мл. Машинска обрада металних и керамичких матричних композита је резултирала осмочасовним ТВА концентрацијама излагања од 0.031 ф/мл и до 0.76 ф/мл, респективно (Сцансетти, Пиолатто и Ботта 1992; Бие 1985).
Слика 4. СЕМ влакана од силицијум карбида (А) и бркова (Б).
A.
Постојећи подаци из студија на животињама и људима указују на дефинитиван фиброгени и могући карциногени потенцијал. Ин витро Студије културе ћелија миша које су укључивале бркове од силицијум карбида откриле су цитотоксичност једнаку или већу од оне која је резултат крокидолитног азбеста (Јохнсон ет ал. 1992; Ваугхан ет ал. 1991). Перзистентна аденоматозна хиперплазија плућа пацова је показана у субакутној инхалационој студији (Лапин ет ал. 1991). Студије инхалације оваца које су укључивале прашину силицијум карбида откриле су да су честице инертне. Међутим, излагање влакнима силицијум карбида довело је до фиброзног алвеолитиса и повећане активности раста фибробласта (Бегин ет ал. 1989). Студије узорака плућног ткива радника у производњи силицијум карбида откриле су силикотичне нодуле и гвоздена тела и показале да су влакна силицијум карбида издржљива и могу постојати у високим концентрацијама у плућном паренхиму. Радиографије грудног коша су такође биле у складу са нодуларним и неправилним интерстицијским променама и плеуралним плаковима.
Силицијум-карбидна влакна и бркови су удахнута по величини, издржљива и имају одређени фиброген потенцијал у плућном ткиву. Произвођач бркова од силицијум карбида поставио је интерни стандард на 0.2 ф/мл као осмочасовни ТВА (Беаумонт 1991). Ово је разумна препорука заснована на тренутно доступним здравственим информацијама.
Умјетна стаклена влакна
Умјетна стаклена влакна (ММВФ) се генерално класификују као:
- стаклена влакна (стаклена вуна или фиберглас, непрекидна стаклена филамента и стаклена влакна специјалне намене)
- минерална вуна (камена вуна и вуна од шљаке) и
- керамичка влакна (керамичка текстилна влакна и ватростална керамичка влакна).
Процес производње почиње топљењем сировина са накнадним брзим хлађењем, што резултира производњом некристалних (или стаклених) влакана. Неки производни процеси дозвољавају велике варијације у погледу величине влакана, при чему је доња граница пречника 1 мм или мање (слика 5). Стабилизатори (као што је Ал2O3, ТиО2 и ЗнО) и модификатори (као што су МгО, Ли2О, БаО, ЦаО, На2О и К2О) може се додати да би се променила физичка и хемијска својства као што су затезна чврстоћа, еластичност, издржљивост и топлотни непренос.
Слика 5. СЕМ вуне од шљаке.
Камена вуна, стаклена влакна и ватростална керамичка влакна су по изгледу идентична.
Стаклена влакна се производе од силицијум диоксида и различитих концентрација стабилизатора и модификатора. Већина стаклене вуне се производи коришћењем ротационог процеса који резултира дисконтинуираним влакнима просечног пречника од 3 до 15 μм са варијацијама до 1 μм или мање у пречнику. Влакна стаклене вуне се везују заједно, најчешће фенол формалдехидним смолама, а затим пролазе кроз процес полимеризације топлотног очвршћавања. У зависности од производног процеса, могу се додати и други агенси, укључујући мазива и средства за влажење. Континуирани процес производње стаклених филамената резултира мањим одступањима од просечног пречника влакана у поређењу са стакленом вуном и стакленим влакнима посебне намене. Непрекидна стаклена влакна имају пречник од 3 до 25 μм. Производња стаклених влакана специјалне намене укључује процес фибризације пригушења пламена који производи влакна просечног пречника мањег од 3 μм.
Производња шљаке и камене вуне укључује топљење и фибризацију шљаке из металне руде и магматске стене. Производни процес укључује точак у облику посуде и процес центрифугирања точка. Производи дисконтинуирана влакна просечног пречника од 3.5 до 7 μм чија величина може да се креће у распону који се може удахнути. Минерална вуна се може производити са или без везива, у зависности од крајње употребе.
Ватростална керамичка влакна се производе кроз центрифугу на точковима или процес фибризације парним млазом користећи растопљену каолинску глину, глиницу/силицијум или глиницу/силицијум/цирконијум. Просечни пречници влакана крећу се од 1 до 5 μм. Када се загреју на температуру изнад 1,000°Ц, ватростална керамичка влакна могу се претворити у кристобалит (кристални силицијум диоксид).
ММВФ са различитим пречникима влакана и хемијским саставом се користе у преко 35,000 апликација. Стаклена вуна се користи у стамбеним и комерцијалним апликацијама за звучну и топлотну изолацију, као и у системима за обраду ваздуха. Континуирана стаклена филамента се користи у тканинама и као ојачавајућа средства у пластици, као што се користи у аутомобилским деловима. Стаклена влакна специјалне намене се користе у специјалним апликацијама, на пример у авионима, који захтевају високе карактеристике топлотне и звучне изолације. Камена и шљака вуна без везива користи се као дувана изолација и у плафонским плочама. Камена и шљака вуна са везивом од фенолне смоле се користи у изолационим материјалима, као што су изолациони покривачи и летве. Ватростална керамичка влакна чине 1 до 2% светске производње ММВФ-а. Ватростална керамичка влакна се користе у специјализованим индустријским апликацијама на високим температурама, као што су пећи и пећи. Стаклена вуна, непрекидна стаклена филамента и минерална вуна се производе у највећим количинама.
Сматра се да ММВФ имају мањи потенцијал од природних влакнастих силиката (као што је азбест) за стварање штетних ефеката на здравље због њиховог некристалног стања и њихове склоности ломљењу у краћа влакна. Постојећи подаци сугеришу да најчешће коришћени ММВФ, стаклена вуна, има најмањи ризик од штетних ефеката на здравље, затим камена и шљака, а затим и стаклена влакна специјалне намене са повећаном издржљивошћу и ватростална керамичка влакна. Стаклена влакна специјалне намене и ватростална керамичка влакна имају највећи потенцијал за постојање влакана која се могу удахнути јер су углавном мања од 3 мм у пречнику. Стаклена влакна специјалне намене (са повећаном концентрацијом стабилизатора као што је Ал2O3) и ватростална керамичка влакна су такође издржљива у физиолошким течностима. Континуиране стаклене филаменте су величине које се не могу удисати и стога не представљају потенцијални ризик по здравље плућа.
Доступни здравствени подаци су прикупљени из студија инхалације на животињама и студија морбидитета и морталитета радника укључених у производњу ММВФ. Студије инхалације које су укључивале излагање пацова два комерцијална изолациона материјала од стаклене вуне у просеку 1 μм у пречнику и 20 μм у дужини откриле су благи плућни ћелијски одговор који се делимично променио након прекида излагања. Слични налази су резултат студије инхалације на животињама врсте вуне од шљаке. Минимална фиброза је доказана код излагања животиња каменој вуни инхалацијом. Испитивања инхалације ватросталних керамичких влакана довела су до рака плућа, мезотелиома и плеуралне и плућне фиброзе код пацова и мезотелиома и плеуралне и плућне фиброзе код хрчака при максимално толерисаној дози од 250 ф/мл. При 75 ф/мл и 120 ф/мл, један мезотелиом и минимална фиброза су демонстрирани код пацова, а при 25 ф/мл, постојао је плућни ћелијски одговор (Бунн ет ал. 1993).
Може доћи до иритације коже, ока, горњих и доњих дисајних путева и зависи од нивоа изложености и радних обавеза. Иритација коже је најчешћи забележени ефекат на здравље и може довести до тога да до 5% нових радника у фабрици ММВФ напусти посао у року од неколико недеља. Настаје механичком траумом коже од влакана пречника већег од 4 до 5 μм. Може се спречити одговарајућим мерама контроле животне средине, укључујући избегавање директног контакта коже са влакнима, ношење широког кроја, одеће дугих рукава и одвојено прање радне одеће. Симптоми горњих и доњих респираторних органа могу се јавити у неуобичајено прашњавим ситуацијама, посебно у производњи ММВФ производа и апликацијама за крајњу употребу и у стамбеним окружењима када се ММВФ не рукује, не инсталира или поправља правилно.
Студије респираторног морбидитета, мерене симптомима, рендгенским снимцима грудног коша и тестовима плућне функције међу радницима у производним погонима генерално нису открили никакве нежељене ефекте. Међутим, текућа студија радника у фабрици за производњу ватросталних керамичких влакана открила је повећану преваленцију плеуралних плакова (Лемастерс ет ал. 1994). Студије на радницима у секундарној производњи и крајњим корисницима ММВФ-а су ограничене и отежане су вероватноћом збуњујућег фактора претходне изложености азбесту.
Студије смртности радника у фабрикама за производњу стаклених влакана и минералне вуне се настављају у Европи и Сједињеним Државама. Подаци из студије у Европи открили су свеукупно повећање смртности од рака плућа на основу националних, али не и локалних стопа смртности. Постојао је растући тренд рака плућа у кохортама стаклене и минералне вуне са временом од првог запослења, али не и са трајањем запослења. Користећи локалне стопе морталитета, дошло је до повећања морталитета од рака плућа у најранијој фази производње минералне вуне (Симонато, Флетцхер и Цхеррие 1987; Боффетта ет ал. 1992). Подаци из студије у Сједињеним Државама показали су статистички значајан повећан ризик од рака респираторних органа, али нису успели да пронађу везу између развоја рака и различитих индекса изложености влакнима (Марсх ет ал. 1990). Ово је у складу са другим студијама случаја контроле радника у фабрикама за производњу шљаке и стаклених влакана које су откриле повећан ризик од рака плућа повезан са пушењем цигарета, али не у мери изложености ММВФ (Вонг, Фолиарт и Трент 1991; Цхиаззе, Ваткинс и Фриар 1992). Студија морталитета радника у производњи континуираних стаклених филамената није открила повећан ризик од смртности (Сханнон ет ал. 1990). У Сједињеним Државама је у току студија смртности која укључује раднике на ватросталним керамичким влакнима. Студије морталитета радника укључених у производњу производа и крајњих корисника ММВФ-а су веома ограничене.
1987. године, Међународна агенција за истраживање рака (ИАРЦ) класификовала је стаклену вуну, камену вуну, вуну од шљаке и керамичка влакна као могуће карциногене за људе (група 2Б). Текуће студије на животињама и студије морбидитета и морталитета радника укључених у ММВФ ће помоћи да се даље дефинише сваки потенцијални ризик по здравље људи. На основу доступних података, здравствени ризик од излагања ММВФ-у је знатно нижи од онога што је повезано са изложеношћу азбесту и са становишта морбидитета и морталитета. Огромна већина студија на људима је, међутим, из производних погона ММВФ-а где се нивои изложености генерално одржавају испод нивоа од 0.5 до 1 ф/мл током осмочасовног радног дана. Недостатак података о морбидитету и морталитету код секундарних и крајњих корисника ММВФ чини мудрим да се контролише изложеност респиративним влакнима на или испод ових нивоа кроз мере контроле животне средине, радне праксе, обуку радника и програме заштите респираторних органа. Ово је посебно применљиво код излагања издржљивој ватросталној керамици и стаклу специјалне намене ММВФ и било којој другој врсти вештачких влакана која се могу удисати и која су издржљива у биолошким медијима и која се стога могу депоновати и задржати у плућном паренхима.
Респираторни рак
Рак плућа
Рак плућа је најчешћи рак широм света. У 1985, процењује се да се у свету 676,500 случајева догодило код мушкараца и 219,300 случајева код жена, што представља 11.8% свих нових карцинома, а ова бројка расте по стопи од око 0.5% годишње (Паркин, Писани и Ферлаи 1993). . Око 60% ових случајева јавља се у индустријализованим земљама, од којих је рак плућа водећи узрок смрти од рака међу мушкарцима. И у индустријализованим земљама иу земљама у развоју, мушкарци имају већу учесталост него жене, при чему се однос полова креће од два до десет пута. Међународне међуродне варијације у учесталости рака плућа у великој мери се објашњавају варијацијама у садашњим и прошлим обрасцима пушења.
Већи ризик од рака плућа је доследно примећен у урбаним у поређењу са руралним подручјима. У индустријализованим земљама, јасна, инверзна веза је очигледна код мушкараца у учесталости рака плућа и морталитету према друштвеној класи, док жене показују мање јасне и доследне обрасце. Разлике у друштвеној класи код мушкараца углавном одражавају другачији образац пушења. У земљама у развоју, међутим, изгледа да постоји већи ризик код мушкараца из више друштвене класе него код других мушкараца: овај образац вероватно одражава раније усвајање западних навика од стране имућних група становништва.
Подаци о инциденцији из СЕЕР програма Националног института за рак Сједињених Држава за период 1980-86 указују, слично као у претходним годинама, да црни мушкарци имају већу инциденцу од белаца, док се инциденција за жене не разликује по раси. Ове разлике међу етничким групама у Сједињеним Државама се заправо могу приписати социо-економским разликама између црнаца и белаца (Бакует ет ал. 1991).
Инциденција карцинома плућа расте скоро линеарно са годинама, када је приказана у лог-лог скали; само у најстаријим старосним групама може се уочити силазна крива. Учесталост и смртност од рака плућа су нагло порасли током овог века и настављају да расту у већини земаља.
Постоје четири главна хистолошка типа карцинома плућа: карцином сквамозних ћелија, аденокарцином, карцином великих ћелија и карцином малих ћелија (СЦЛЦ). Прва три се такође називају раком плућа не-малих ћелија (НСЦЛЦ). Пропорције сваког хистолошког типа се мењају у зависности од пола и старости.
Карцином сквамозних ћелија је веома снажно повезан са пушењем и представља најчешћи тип рака плућа у многим популацијама. Најчешће се јавља у проксималним бронхима.
Аденокарцином је мање повезан са пушењем. Овај тумор је периферног порекла и може се појавити као усамљени периферни чвор, мултифокална болест или брзо прогресивни пнеумонични облик, који се шири од режња до режња.
Карцином великих ћелија представља мањи удео од свих карцинома плућа и има слично понашање као и аденокарцином.
СЦЛЦ представља мали удео (10 до 15%) свих карцинома плућа; типично настаје на централној ендобронхијалној локацији и има тенденцију развоја раних метастаза.
Знаци и симптоми рака плућа зависе од локације тумора, ширења и ефеката метастатског раста. Многи пацијенти се јављају са асимптоматском лезијом откривеном случајно на рендгенском снимку. Међу пацијентима са НСЦЛЦ, умор, смањена активност, упорни кашаљ, диспнеја, смањен апетит и губитак тежине су уобичајени. Пиштање или стридор се такође могу развити у узнапредовалим фазама. Континуирани раст може довести до ателектазије, упале плућа и формирања апсцеса. Клинички знаци код пацијената са СЦЛЦ су мање изражени него код оних са НСЦЛЦ и обично су повезани са ендобронхијалном локацијом.
Рак плућа може метастазирати практично у било који орган. Најчешће локације метастатских лезија су плеура, лимфни чворови, кост, мозак, надбубрежне жлезде, перикард и јетра. У тренутку постављања дијагнозе, већина пацијената са карциномом плућа има метастазе.
Прогноза варира у зависности од стадијума болести. Укупно петогодишње преживљавање пацијената са карциномом плућа у Европи (1983-85) било је између 7% и 9% (Беррино ет ал. 1995.).
Тренутно није доступна метода популацијског скрининга за рак плућа.
Рак назофаринкса
Рак назофаринкса је редак у већини популација, али је чест код оба пола у областима као што су југоисточна Азија, јужна Кина и северна Африка. Мигранти из јужне Кине задржавају висок ризик у великој мери, али кинески мигранти друге и треће генерације у Сједињеним Државама имају мање од половине ризика од миграната прве генерације.
Карциноми назофаринкса су претежно сквамозног епителног порекла. Према СЗО, ови тумори су класификовани као: тип 1, кератинизирајући карцином сквамозних ћелија; тип 2, не-кератинизирајући карцином; и тип 3, недиференцирани карцином, који је најчешћи хистолошки тип. Тип 1 има неконтролисани локални раст, а метастатско ширење се налази код 60% пацијената. Типови 2 и 3 имају метастатско ширење код 80 до 90% пацијената.
Маса у врату се примећује код приближно 90% пацијената са назофарингеалним карциномом. Могу се приметити промене у слуху, серозни отитис средњег уха, тинитус, зачепљење носа, бол и симптоми повезани са растом тумора у суседне анатомске структуре.
Укупно петогодишње преживљавање пацијената са раком назофаринкса у Европи између 1983. и 1985. било је око 35%, варирајући у зависности од стадијума тумора и његове локације (Беррино ет ал. 1995.).
Конзумација слане рибе у кинеском стилу је фактор ризика од рака назофаринкса; улога других нутритивних фактора и вируса, посебно Епстеин-Барр вируса, иако се сумња, није потврђена. Није познато да професионални фактори узрокују рак назофаринкса. Тренутно нису доступне никакве превентивне мере (Хиггинсон, Муир и Муноз 1992).
Синонасал Цанцер
Неоплазме носа и носних шупљина су релативно ретке. Заједно, рак носа и назалног синуса – укључујући максиларне, етмоидне, сфеноидне и фронталне синусе – чине мање од 1% свих карцинома. У већини случајева ови тумори се класификују као сквамозни карциноми. У западним земљама, рак носа је чешћи од карцинома назалног синуса (Хиггинсон, Муир и Муноз 1992).
Јављају се чешће код мушкараца и међу црначким популацијама. Највећа инциденција је забележена у Кувајту, Мартинику и Индији. Врхунац развоја болести се јавља током шесте деценије живота. Главни познати узрок синоназалног карцинома је излагање дрвној прашини, посебно од тврдог дрвета. Чини се да пушење дувана није повезано са овом врстом рака.
Већина тумора носне шупљине и параназалног синуса су добро диференцирани и споро расту. Симптоми могу укључивати чир који се не зацељује, крварење, зачепљење носа и симптоме који се односе на израстање у усну шупљину, орбиту и птеригоидну јаму. Болест је обично узнапредовала у време дијагнозе.
Укупно петогодишње преживљавање пацијената са карциномом носа и синуса носа у Европи између 1983. и 1985. било је око 35%, варирајући у зависности од величине лезије при постављању дијагнозе (Беррино ет ал. 1995.).
Рак ларинкса
Највећа инциденција рака ларинкса забележена је у Сао Паолу (Бразил), Навари (Шпанија) и Варезеу (Италија). Висок морталитет је такође забележен у Француској, Уругвају, Мађарској, Југославији, Куби, Блиском истоку и северној Африци. Рак ларинкса је претежно мушки карцином: процењује се да је 120,500 случајева међу мушкарцима и 20,700 случајева међу женама забележено 1985. (Паркин, Писани и Ферлаи 1993.). Уопштено говорећи, инциденција је већа међу црним становништвом у поређењу са белцима, ау урбаним срединама у поређењу са руралним.
Скоро сви карциноми ларинкса су сквамозни карциноми. Већина се налази у глотису, али се могу развити иу супраглотису или, ретко, у субглотису.
Симптоми се можда неће појавити или бити веома суптилни. У зависности од локације и стадијума лезије могу бити присутни бол, осећај гребања, промена толеранције на топлу или хладну храну, склоност ка аспирацији течности, промена дисајних путева, незнатна промена гласа током неколико недеља и цервикална аденопатија.
Већина карцинома ларинкса је видљива прегледом ларинкса или ендоскопијом. Пре-неопластичне лезије могу се идентификовати у ларинксу пушача (Хиггинсон, Муир и Муноз 1992).
Укупно петогодишње преживљавање пацијената са раком ларинкса у Европи између 1983. и 1985. било је око 55% (Беррино ет ал. 1995.).
Мезотелиом плеуре
Мезотелиоми могу настати из плеуре, перитонеума и перикарда. Малигни мезотелиом представља најважнији тумор плеуре; јавља се углавном између пете и седме деценије живота.
Плеурални мезотелиом је некада био редак тумор и остао је у већини женских популација, док се код мушкараца у индустријализованим земљама повећао за 5 до 10% годишње током последњих деценија. Генерално, мушкарци су погођени пет пута више него жене. Прецизне процене инциденције и морталитета су проблематичне због потешкоћа у хистолошкој дијагнози и промена у Међународној класификацији болести (МКБ) (Хиггинсон, Муир и Муноз 1992). Међутим, чини се да стопе инциденције представљају веома важне локалне варијације: оне су веома високе у областима где је присутно ископавање азбеста (нпр. у северозападном Кејп провинцији у Јужној Африци), у великим градовима поморских бродоградилишта и у регионима са загађеним влакнима из животне средине, као што је нпр. као поједине области централне Турске.
Пацијенти могу бити асимптоматски и њихова болест се дијагностикује случајно на рендгенским снимцима грудног коша, или могу имати диспнеју и бол у грудима.
Мезотелиоми имају тенденцију да буду инвазивни. Средње преживљавање је 4 до 18 месеци у различитим серијама.
Професионални фактори ризика од рака респираторних органа
Осим дуванског дима, према Међународној агенцији за истраживање рака (ИАРЦ) доказана је узрочна повезаност са раком дисајних путева за 13 агенаса или смеша и девет околности изложености (видети табелу 1). Штавише, постоји осам агенаса, смеша или околности изложености које су према ИАРЦ-у вероватно канцерогене за један или више органа у респираторном тракту (табела 2). Све осим азатиоприна, имуносупресивног лека, су првенствено изложености на радном месту (ИАРЦ 1971-94).
Табела 1. Утврђени респираторни карциногени људи према ИАРЦ
| Агенти Индивидуални агенти | Циљне локације |
| Азбест | Плућа, ларинкс, плеура |
| Арсен и једињења арсена | Лунг |
| Берилијум и једињења берилијума | Лунг |
| Бис (хлорометил) етар | Лунг |
| Кадмијум и једињења кадмијума | Лунг |
| Хлорометил метил етар (технички квалитет) | Лунг |
| Једињења хрома (ВИ). | Нос, плућа |
| Иперит | Плућа, ларинкс |
| Једињења никла | Нос, плућа |
| Талк који садржи азбестиформна влакна | Плућа, плеура |
| Комплексне мешавине | |
| Угљени катрани | Лунг |
| Угљени катран смоле | Лунг |
| чађи | Лунг |
| Дувански дим | Нос, плућа, ларинкс |
| Околности изложености | |
| Производња алуминијума | Лунг |
| Производња и поправка чизама и ципела | нос |
| Гасификација угља | Лунг |
| Производња кокса | Лунг |
| Ливарство гвожђа и челика | Лунг |
| Израда намештаја и ормана | нос |
| Јака магла неорганске киселине која садржи сумпорну киселину (изложеност на радном месту) | Ларинк |
| Сликари (професионална изложеност као) | Лунг |
| Радон и производи његовог распадања | Лунг |
| Подземно ископавање хематита (са изложеношћу радону) | Лунг |
Извор: ИАРЦ, 1971-1994.
Табела 2. Вероватни респираторни карциногени људи према ИАРЦ
| Агенти Индивидуални агенти | Сумња на циљане локације |
| Акрилонитрил | Лунг |
| Азатиоприн | Лунг |
| Формалдехид | Нос, ларинкс |
| Силицијум (кристални) | Лунг |
| Комплексне мешавине | |
| Издувни гас дизел мотора | Лунг |
| Испарења за заваривање | Лунг |
| Околности изложености | |
| Гумарска индустрија | Лунг |
| Прскање и примена инсектицида (изложеност на радном месту у) | Лунг |
Извор: ИАРЦ, 1971-1994.
Професионалне групе које показују повећан ризик од рака плућа након излагања једињењима арсена укључују раднике у топионици обојених метала, руковаоце крзном, произвођаче једињења за овчије умаке и раднике у виноградима (ИАРЦ 1987).
Спроведен је велики број епидемиолошких студија о повезаности једињења хрома (ВИ) и појаве карцинома плућа и носа у индустрији хромата, хроматних пигмента и хромирања (ИАРЦ 1990а). Конзистентност налаза и величина ексцеса су показали канцерогени потенцијал једињења хрома (ВИ).
Радници у рафинеријама никла из многих земаља су показали значајно повећан ризик од рака плућа и носа; друге професионалне групе изложене никлу међу којима је откривен повећан ризик од карцинома плућа укључују рударе руде сулфида никла и раднике у производњи легура са високим садржајем никла (ИАРЦ 1990б).
Радници изложени берилијуму имају повећан ризик од рака плућа (ИАРЦ 1994а). Најинформативнији подаци су они добијени из америчког регистра случајева берилијума, у којем су прикупљени случајеви плућних болести повезаних са берилијумом из различитих индустрија.
Утврђен је пораст појаве рака плућа у групама топионица кадмијума и радника на никл-кадмијум батеријама (ИАРЦ 1994б). Истовремена изложеност арсену међу топионицама и никлу међу батеријским радницима не може објаснити такав пораст.
Азбест је важан професионални канцероген. Рак плућа и мезотелиом су главне неоплазме повезане са азбестом, али су пријављени карциноми на другим местима, као што су гастро-интестинални тракт, ларинкс и бубрези, код радника који се баве азбестом. Сви облици азбеста су узрочно повезани са раком плућа и мезотелиомом. Поред тога, показало се да су азбестиформна влакна која садрже талк канцерогена за људска плућа (ИАРЦ 1987). Карактеристична карактеристика рака плућа изазваног азбестом је његов синергистички однос са пушењем цигарета.
Бројне студије међу рударима, радницима у каменолому, ливницама, керамичарима, радницима гранита и резачима камена су показале да особе којима је дијагностикована силикоза након излагања прашини која садржи кристални силицијум имају повећан ризик од рака плућа (ИАРЦ 1987).
Полинуклеарни ароматични угљоводоници (ПАХ) настају углавном као резултат пиролитичких процеса, посебно непотпуног сагоревања органских материјала. Међутим, људи су изложени искључиво мешавинама ПАХ-ова, као што су чађи, угљени катран и смоле од угљеног катрана. Кохортне студије морталитета међу димњачарима показале су повећан ризик од рака плућа, који се приписује изложености чађи. Неколико епидемиолошких студија показало је вишак рака респираторних органа међу радницима који су били изложени испарењима смоле у производњи алуминијума, производњи калцијум карбида и покривању кровова. У овим индустријама такође долази до излагања катрану, а посебно катрану угља. Друге индустрије у којима је вишак респираторног карцинома узрокован излагањем испарењима угљеног катрана су гасификација угља и производња кокса (ИАРЦ 1987). Повећани ризик од карцинома дисајних путева (углавном плућа) пронађен је код неких, али нису све студије покушале да анализирају изложеност издувним гасовима дизел мотора одвојено од других производа сагоревања; професионалне групе које су проучаване укључују железничаре, докере, раднике у аутобуским гаражама, запосленике аутобуске компаније и професионалне возаче камиона (ИАРЦ 1989а). Друге мешавине ПАХ-а које су проучаване због њихове канцерогености за људе укључују чађу, издувне гасове бензинских мотора, минерална уља, уља из шкриљаца и битумене. Уља из шкриљаца и необрађена и благо третирана минерална уља су канцерогена за људе, док су издувни гасови из бензинских мотора вероватно канцерогени, а високо рафинисана минерална уља, битумени и чађи се не могу класификовати према њиховој канцерогености за људе (ИАРЦ 1987, 1989а). Иако ове мешавине садрже ПАХ, карциногени ефекат на људска плућа није доказан ни за једну од њих, а докази о карциногености за необрађена и благо третирана минерална уља и за уља из шкриљаца заснивају се на повећаном ризику од рака на другим местима осим респираторни органи (углавном кожа и скротум) код изложених радника.
Бис(б-хлоретил)сулфид, познат као иперит, био је широко коришћен током Првог светског рата, а студије војника изложених ипериту као и радника запослених у његовој производњи откриле су каснији развој рака плућа и носа. (ИАРЦ 1987).
Бројне епидемиолошке студије су показале да радници изложени хлорометил метил етру и/или бис(хлорометил)-етру имају повећан ризик од рака плућа, првенствено од СЦЛЦ (ИАРЦ 1987).
У неким, али не свим студијама које су спроведене међу радницима у производњи текстилних влакана, полимеризацији акрилонитрила и гумарској индустрији утврђено је да су радници изложени акрилонитрилу изложени већем ризику од рака плућа (ИАРЦ 1987).
Прекомерна појава је пријављена за раднике изложене формалдехиду, укључујући хемијске раднике, дрвне раднике и произвођаче и кориснике формалдехида (ИАРЦ 1987). Докази су најјачи за рак носа и назофаринкса: појава ових карцинома показала је градијент доза-одговор у више од једне студије, иако је број изложених случајева често био мали. Друге неоплазме са могућим повећаним ризиком су рак плућа и мозга и леукемија.
Повећани ризик од карцинома ларинкса откривен је у неколико студија на радницима изложеним магли и парама сумпорне и других јаких неорганских киселина, као што су радници у операцијама кисељења челика, у производњи сапуна и петрохемијским радницима (ИАРЦ 1992). Ризик од рака плућа је такође повећан у неким, али не у свим, од ових студија. Штавише, пронађен је вишак синоназалног карцинома код групе радника у производњи изопропанола користећи процес јаке киселине.
Обрађивачи дрвета су под повећаним ризиком од рака носа, посебно аденокарцинома (ИАРЦ 1987). Ризик је потврђен за произвођаче намештаја и ормара; студије о радницима у столарству и столарству су сугерисале сличан вишак ризика, али су неке студије дале негативне резултате. Остале дрвне индустрије, као што су пилане и производња целулозе и папира, нису биле класификоване по свом канцерогеном ризику. Иако ИАРЦ није проценио карциногеност дрвне прашине, могуће је сматрати да је дрвна прашина одговорна за барем део повећаног ризика од назалног аденокарцинома међу дрвопрерађивачима. Чини се да дрвопрерађивачи нису изложени повећаном ризику од рака других респираторних органа.
Аденокарцином носа је такође узрокован запошљавањем у производњи и поправци чизама и ципела (ИАРЦ 1987). С друге стране, нема јасних доказа да су радници запослени у производњи кожних производа и у штављењу и преради коже изложени повећаном ризику од рака респираторних органа. Тренутно није познато да ли је вишак назалног аденокарцинома у индустрији чизама и обуће последица кожне прашине или других изложености. ИАРЦ није проценио карциногеност кожне прашине.
Рак плућа био је чест међу рударима уранијума, подземним рударима хематита и неколико других група рудара метала (ИАРЦ 1988; БЕИР ИВ Комитет за биолошке ефекте јонизујућег зрачења 1988). Заједнички фактор за сваку од ових група занимања је излагање а-зрачењу које емитују честице радона у инхалацији. Главни извор података о раку након излагања јонизујућем зрачењу изведен је из праћења преживелих од атомске бомбе (Престон ет ал. 1986; Схимизу ет ал. 1987). Ризик од рака плућа је повећан међу преживјелима од атомске бомбе, као и међу људима који су примили терапију зрачењем (Смитх и Долл 1982). Међутим, тренутно нема убедљивих доказа о постојању повећаног ризика од рака плућа међу радницима изложеним ниском јонизујућем зрачењу, као што су они који се јављају у нуклеарној индустрији (Берал и др. 1987; БЕИР В, Комитет за биолошке ефекте јонизујућег зрачења 1990). ИАРЦ није проценио карциногеност јонизујућег зрачења.
Повећан ризик од рака плућа међу сликарима је пронађен у три велике кохортне студије и у осам малих кохортних и пописних студија, као и у једанаест студија случаја-контроле из различитих земаља. С друге стране, мало доказа о повећању ризика од рака плућа пронађено је међу радницима укљученим у производњу боја (ИАРЦ 1989б).
Бројне друге хемикалије, смеше, занимања и индустрије за које је ИАРЦ оценио да су канцерогене за људе (ИАРЦ Група 1) немају плућа као примарни циљни орган. Без обзира на то, повећана је могућност повећања ризика од рака плућа за неке од ових хемикалија, као што је винил хлорид (ИАРЦ 1987), и занимања, као што су прскање и примена инсектицида (ИАРЦ 1991а), али докази нису доследни. .
Штавише, неколико агенаса који имају плућа као једну од главних мета, сматрају се могућим канцерогенима за људе (ИАРЦ група 2Б), на основу канцерогене активности код експерименталних животиња и/или ограничених епидемиолошких доказа. Они укључују неорганска једињења олова (ИАРЦ 1987), кобалт (ИАРЦ 1991б), вештачка стаклена влакна (камена вуна, шљака и стаклена вуна) (ИАРЦ 1988б) и испарења од заваривања (ИАРЦ 1990ц).
Професионално стечене инфекције плућа
Иако су епидемиолошке студије професионално стечене пнеумоније (ОАП) ограничене, сматра се да је учесталост плућних инфекција повезаних са радом у опадању широм света. Насупрот томе, ОАП-ови у развијеним земљама могу бити у порасту у занимањима која су повезана са биомедицинским истраживањем или здравственом заштитом. ОАП код болничких радника у великој мери одражава преовлађујуће патогене стечене у заједници, али поновна појава туберкулозе, морбила и пертусиса у здравственим установама представља додатни ризик за занимања заснована на здрављу. У земљама у развоју, иу специфичним занимањима у развијеним земљама, јединствени инфективни патогени који обично не циркулишу у заједници изазивају многе ОАП.
Приписивање инфекције професионалној изложености, а не изложености у заједници може бити тешко, посебно за болничке раднике. У прошлости, професионални ризик је са сигурношћу документован само у ситуацијама када су радници били заражени узрочницима који су се јављали на радном месту, али нису били присутни у заједници. У будућности ће употреба молекуларних техника за праћење специфичних микробних клонова на радном месту иу заједницама учинити одређивање ризика јаснијим.
Као и пнеумонија стечена у заједници, ОАП је резултат микроаспирације бактерија које колонизују орофаринкс, удисања инфективних честица које се могу удисати или хематогеног засејавања плућа. Већина пнеумоније стечене у заједници настаје микроаспирацијом, али ОАП обично настаје услед удисања заразних честица у ваздуху од 0.5 до 10 μм на радном месту. Веће честице не успевају да стигну до алвеола због удара или седиментације на зидове великих дисајних путева и након тога се чисте. Мање честице остају суспендоване током инспираторног и експираторног тока и ретко се таложе у алвеолама. За неке болести, као што је хеморагична грозница са бубрежним синдромом повезаним са хантавирусном инфекцијом, главни начин преношења је инхалација, али примарни фокус болести можда нису плућа. Професионално стечени патогени који се не преносе удисањем могу секундарно захватити плућа, али о њима неће бити речи.
Овај преглед укратко говори о неким од најважнијих професионалних патогена. Опширнија листа професионално стечених плућних поремећаја, класификованих по специфичној етиологији, приказана је у табели 1.
Табела 1. Професионално стечене заразне болести заражене микроаспирацијом или удисањем инфективних честица
|
Болест (патоген) |
Резервоар |
Ризичне популације |
|
Бактерије, кламидија, микоплазме и рикеције |
||
|
бруцелоза (Бруцелла спп.) |
Стока (говеда, козе, свиње) |
Ветеринарски радници, пољопривредни радници, лабораторијски радници, радници кланице |
|
инхалациони антракс (Бациллус антхрацис) |
Производи животињског порекла (вуна, коже) |
Пољопривредни радници, кожари, клаоничари, текстилци, лабораторијски радници |
|
Плућна куга (Иерсиниа пестис) |
Дивљи глодари |
Ветеринарски радници, ловци/трапери, лабораторијски радници |
|
Пертусис (Бордателла пертуссис) |
Људи |
Запослени у домовима за старе, здравствени радници |
|
Легионарска болест (Легионелла спп.) |
Извори контаминиране воде (нпр. расхладни торњеви, кондензатори испаривача) |
Здравствени радници, лабораторијски радници, индустријски лабораторијски радници, багери за воду |
|
мелиоидоза (Псеудомонас псеудомаллеи) |
Земљиште, стајаћа вода, пиринчана поља |
Војно особље, пољопривредни радници |
|
Стрептококус пнеумоние |
Људи |
Здравствени радници, пољопривредни радници, подземни рудари |
|
Неиссериа менингитидис |
Људи |
Здравствени радници, лабораторијски радници, војна лица |
|
пастерелоза (Пастеурелла мултоцида) |
Разноликост домаћих (мачке, пси) и дивљих животиња |
Пољопривредни радници, ветеринарски радници |
|
Респираторна туларемија (Франциселла туларенсис) |
Дивљи глодари и зечеви |
Ручни радници, војна лица, лабораторијски радници, ловци/трапери, пољопривредни радници |
|
орнитоза (Цхламидиа пситтаци) |
Птице |
Радници у продавницама кућних љубимаца, радници у производњи живине, ветеринари, лабораторијски радници |
|
ТВАР пнеумонија (Цхламидиа пнеумониае) |
Људи |
Здравствени радници, војна лица |
|
К грозница (Цокиелла бурнетии) |
Домаће животиње (говеда, овце, козе) |
Лабораторијски радници, текстилци, клаоничари, млечни сточари, ветеринари |
|
Атипична пнеумонија (Мицопласма пнеумониае) |
Људи |
Војно особље, здравствени радници, институционални радници |
|
Гљиве/микобактерије |
||
|
хистоплазмоза (Хистопласма цапсулатум) |
Соил; измет птица или слепих мишева (ендем за источну Северну Америку) |
Пољопривредни радници, лабораторијски радници, физички радници |
|
кокцидиоидомикоза (Цоццидоидеса иммитис) |
Земљиште (ендемско за запад Северне Америке) |
Војно особље, пољопривредни радници, физички радници, текстилци, лабораторијски радници |
|
бластомикоза (Бластомицес дерматитидис) |
Земљиште (ендемично за источну Северну Америку) |
Лабораторијски радници, пољопривредни радници, физички радници, радници у шумарству |
|
паракокцидиоидомикоза (Парацоццидиоидес брасилиенсис) |
Земљиште (ендемично за Венецуелу, Колумбију, Бразил) |
Пољопривредни радници |
|
споротрихоза (Споротхрик сцхенкии) |
Биљни остаци, кора дрвећа и баштенских биљака |
Баштовани, цвећари, рудари |
|
туберкулоза (Мицобацтериум туберцулосис, М. бовис, М. африцанум) |
Људи и нељуди примати, говеда |
Рудари тврдог камена, ливници, здравствени и лабораторијски радници, клаоничари, ветеринарски радници, војна лица, кафански радници |
|
Микобактериоза осим туберкулозе (Мицобацтериум спп..) |
Соил |
Радници изложени силицијум диоксиду, укључујући пескаре |
|
Вируси |
||
|
Хантавирус |
Глодари |
Пољопривредни радници, сточари, радници за дератизацију |
|
Меаслес |
Људи |
Здравствени и лабораторијски радници |
|
Рубела |
Људи |
Здравствени и лабораторијски радници |
|
Грип |
Људи |
Здравствени и лабораторијски радници |
|
Варицелла зостер |
Људи |
Здравствени и лабораторијски радници, војна лица |
|
респираторни синцицијални вирус |
Људи |
Здравствени и лабораторијски радници |
|
Аденовирус |
Људи |
Здравствени и лабораторијски радници, војна лица |
|
Вирус параинфлуенце |
Људи |
Здравствени и лабораторијски радници |
|
Вирус лимфоцитног хориоменингитиса (аренавирус) |
Глодари |
Лабораторијски радници, ветеринарски радници |
|
Ласа грозница (аренавирус) |
Глодари |
Здравствених радника |
|
Вируси Марбург и Ебола (филовирус) |
Људски и нељуди примати, вероватно слепи мишеви |
Лабораторијски радници, ветеринарски радници, здравствени радници, радници у фабрици памука |
Професионалне инфекције код радника у пољопривреди
Поред гасова и органске прашине који утичу на респираторни тракт и опонашају заразне болести, неколико зооноза (патогени заједнички за животиње и људе) и друге заразне болести повезане са животом на селу јединствено погађају пољопривредне раднике. Ове болести се добијају удисањем инфективних аеросола и ретко се преносе са једне особе на другу. Такве болести које се јављају код пољопривредних радника укључују антракс, бруцелозу, К грозницу, орнитозу, туберкулозу и кугу (табела 1). Узрочници гљивица укључују хистоплазмозу, бластомикозу, кокцидиоидомикозу, паракокцидиоидомикозу и криптококозу (табела 1). Осим хантавирусних болести, вирусне болести нису значајан узрок професионалних плућних обољења код пољопривредника.
Сматра се да су неке од ових инфекција чешће, али је њихову инциденцу тешко одредити јер: (1) већина инфекција је субклиничка, (2) клиничка болест је блага или се тешко дијагностикује због неспецифичних симптома, (3) медицински и дијагностичке услуге су ретко доступне за већину пољопривредних радника, (4) не постоји организован систем за пријављивање многих од ових болести и (5) многе од њих су ретке болести у општој заједници и медицинско особље их не препознаје. На пример, иако се епидемијски нефритис изазван вирусом Пуумала, хантавирусом, ретко пријављује у западној Европи, сероистраживања пољопривредних радника показала су преваленце антитела на хантавирусе од 2 до 7%.
Зооноза у развијеним земљама се смањује због активних програма контроле болести усмерених на животињске популације. Упркос овим контролама, пољопривредни радници и особе које раде у пољима повезаним са пољопривредом (као што су ветеринари, прерађивачи меса, прерађивачи живине и радници за косу/коже) и даље су изложени ризику од многих болести.
Хантавирусна инфекција
Хантавирусна инфекција која резултира хеморагијском грозницом са бубрежним синдромом (ХФРС) или епидемијским нефритисом (ЕН) клинички је описана међу пољопривредним радницима, војним особљем и лабораторијским радницима у ендемским областима Азије и Европе више од 50 година. Инфекција настаје удисањем аеросола урина, пљувачке и фекалија заражених глодара. Хеморагијска болест и смањена бубрежна функција се развијају током већине хантавирусних болести, а не пнеумоније, али је плућни едем због повећане васкуларне пермеабилности пријављен код ХФРС и ЕН. Дубоке плућне последице хантавирусних инфекција нису биле у потпуности цењене све до недавног избијања хантавирусног плућног синдрома (ХПС) повезаног са инфекцијом недавно изолованим хантавирусом у западним Сједињеним Државама (Муерто Цанион вирус, Фоур Цорнерс вирус или Син Номбре вирус).
Хантавируси су чланови Буниавиридае, породица РНК вируса. Пет хантавируса је повезано са људским болестима. ХФРС је повезан са вирусом Хантаан у источној Азији, вирусом Добрава на Балкану и вирусом Сеула, који је распрострањен широм света. ЕН је повезан са вирусом Пуумала у западној Европи. ХПС је повезан са новоизолованим хантавирусом у западним Сједињеним Државама. Од 1951. до 1983. године пријављено је 12,000 случајева ХФРС-а из Републике Кореје. Извештава се да се учесталост болести у Кини повећава са епидемијама у руралним и урбаним центрима, а 1980. године 30,500 случајева са 2,000 смртних случајева приписано је ХФРС-у.
Клиничка слика
Са вирусима који изазивају ХФРС или ЕН, инфекција обично резултира асимптоматским развојем анти-хантавирус антитела. Код оболелих, знаци и симптоми ране фазе су неспецифични, а хантавирусна инфекција се може дијагностиковати само серолошким тестирањем. Споро опоравак је уобичајен, али неколико особа напредује до ХФРС или ЕН, развијајући протеинурију, микроскопску хематурију, азотемију и олигурију. Особе са ХФРС такође развијају дубоко крварење због дисеминиране интраваскуларне коагулације, повећане васкуларне пермеабилности и шока. Смртност особа са пуним ХФРС синдромом варира од 5 до 20%.
ХПС карактеришу дифузни интерстицијски плућни инфилтрати и нагли почетак акутног респираторног дистреса и шока. Изражена леукоцитоза може настати као резултат повећања цитокина који карактеришу хантавирусна обољења. Код ХПС, морталитет може бити већи од 50%. Инциденца асимптоматске инфекције или непрепознатог ХПС-а је непотпуно истражена.
Дијагностички тестови
Дијагноза се поставља демонстрирањем присуства имуноглобулина М или растућег титра имуноглобулина Г коришћењем високо специфичних и осетљивих тестова индиректне имунофлуоресценције и неутрализујућих антитела. Друге дијагностичке методе укључују ланчану реакцију полимеразе за вирусну рибонуклеинску киселину и имунохистохемију за вирусни антиген.
Епидемиологија
Инфекција настаје удисањем аеросола урина, пљувачке и фекалија заражених глодара. Заражени глодари немају никакве очигледне болести. До преношења може доћи перкутаном инокулацијом урина, пљувачке или фекалија заражених глодара, али нема доказа о преносу са човека на човека.
Сероепидемиолошка истраживања људи и глодара показала су да су хантавируси ендемични са светском дистрибуцијом у руралним и урбаним срединама. У ендемским руралним срединама, интеракције глодара и човека се повећавају када глодари сезонски нападају куће или се људска активност повећава у областима са високом густином глодара. Особе у руралним занимањима су у највећем ризику од инфекције. У анкетама асимптоматских руралних популација у Италији, 4 до 7% шумарских радника, ренџера, фармера и ловаца имало је анти-хантавирус антитела, у поређењу са 0.7% војника. Код асимптоматских пољопривредних радника у Ирској и Чехословачкој, преваленција анти-хантавирус антитела била је 1 до 2%, односно 20 до 30%. Садња, жетва, вршидба, узгој стада и шумарство су фактори ризика за инфекцију вирусом. Сероистраживања у западним Сједињеним Државама за утврђивање професионалног ризика од инфекције хантавирусом су у току, али у студији здравствених радника (ЗР) који се брину о ХПС пацијентима није идентификована ниједна инфекција. Од првих 68 особа са ХПС-ом, произилази да су пољопривредне активности у стаништима заражених глодара фактори ризика за инфекцију. Пацијенти су чешће орали, чистили просторе за складиштење хране, садили, чистили шупе за животиње и били сточари. Главни резервоар за ХПС је јелен миш, Перомисцус маницулатус.
Остала погођена занимања
У урбаним срединама, резервоар глодара за вирус Сеула је кућни пацов. Градски радници, као што су пристанишни радници, радници у складиштима житарица, радници у зоолошким вртовима и радници за контролу глодара могу бити изложени ризику од инфекције хантавирусом. Истраживачке лабораторије које користе глодаре за истраживања осим истраживања хантавируса повремено су били несумњиви извори хантавирусних инфекција лабораторијских радника. Остала занимања, као што су војно особље и теренски биолози, су у опасности од инфекције хантавирусом.
Лечење
Рибавирин је показао ин витро активност против неколико хантавируса и клиничку ефикасност против инфекције вирусом Хантаан, а коришћен је за лечење особа са ХПС-ом.
Контроле јавног здравља
Вакцина није доступна за употребу, иако постоје стални напори да се развију живе и убијене вакцине. Минимизирање људског контакта са глодарима и смањење популације глодара у људском окружењу смањује ризик од болести. У лабораторијама за истраживање хантавируса, објекти високог нивоа биолошке безбедности ограничавају ризик од размножавања вируса у ћелијској култури или руковања материјалима са високим концентрацијама вируса. У другим истраживачким лабораторијама које користе глодаре, може се размотрити периодични серолошки надзор хантавирусне инфекције колонија глодара.
Лимфоцитни хориоменингитис (ЛЦМ)
ЛЦМ, као и хантавирусне инфекције, природно је инфекција дивљих глодара која се повремено шири на човека. ЛЦМ вирус је аренавирус, али се преношење обично дешава аеросолизацијом. Природни домаћини укључују дивље мишеве, али упорна инфекција домаћих сиријских хрчака је добро документована. Инфекција је, дакле, могућа у већини занимања која укључују аеросолизацију урина глодара. Најновија документована професионална епидемија ове болести десила се код лабораторијског особља које је било изложено голим мишевима са недостатком Т-ћелија који су упорно инфицирани као резултат инокулације контаминираних туморских ћелијских линија.
Клиничка слика
Већина случајева ЛЦМ је асимптоматска или повезана са неспецифичном болешћу налик грипу и стога се не препознаје. Док је респираторни тракт место уласка, респираторни симптоми имају тенденцију да буду неспецифични и самоограничени. Менингитис или менингоенцефалитис се развија код малог процента пацијената и може довести до специфичне дијагнозе.
Дијагностички тестови
Дијагноза се обично поставља серолошком демонстрацијом пораста титра вируса у присуству одговарајућих клиничких знакова. Повремено се користе и изолација вируса и имунофлуоресценција ткива.
Епидемиологија
Приближно 20% дивљих мишева је заражено овим вирусом. Трансплацентални пренос вируса код осетљивих глодара доводи до толеранције Т-ћелија и конгенитално инфицираних мишева (или хрчака) који остају упорно инфицирани током свог живота. Слично томе, мишеви са недостатком Т-ћелија, као што су голи мишеви, могу бити упорно инфицирани вирусом. Људи се инфицирају преносом аеросола. Поред тога, ћелијске линије глодара могу бити контаминиране вирусом и размножавати га. Људи се обично инфицирају аеросолима, иако пренос може бити директан или преко вектора инсеката.
Остала погођена занимања
Свако занимање које укључује излагање прашини контаминираној излучевинама дивљих глодара представља ризик од инфекције ЛЦМ-ом. Чувари животиња у објектима за лабораторијске животиње, радници у индустрији продавница кућних љубимаца и лабораторијски радници који раде са ћелијским линијама глодара могу се заразити.
Лечење
ЛЦМ инфекција је обично самоограничена. У тешким случајевима може бити неопходно лечење.
Контроле јавног здравља
Вакцина није доступна. Скрининг истраживачких мишева, хрчака и ћелијских линија ограничио је већину лабораторијски стечених инфекција. За мишеве са недостатком Т-ћелија, серолошко тестирање захтева употребу имунокомпетентних сентинел мишева. Прикладна је употреба рутинских лабораторијских мера предострожности, као што су рукавице, заштита за очи и лабораторијски мантили. Смањење броја дивљих глодара у људском окружењу важно је у контроли ЛЦМ, хантавируса и куге.
Респираторна хламидиоза
Респираторна хламидиоза због Цхламидиа пситтаци је најчешће пријављиван узрок ОАП-а повезан са клањем животиња (живине) и прерадом меса. Хламидиоза и друге болести су често повезане са излагањем болесним животињама, што може бити једини траг за извор и врсту инфекције. Прерада заражених животиња ствара аеросоле који инфицирају особе које су удаљене од прераде меса, а рад у близини фабрика за прераду меса може бити траг за врсту инфекције. Респираторна хламидиоза може бити повезана са излагањем папагајима (пситакоза) или птицама које нису пситацине (орнитоза). Нептичји извори Цхламидиа пситтаци се обично не сматрају потенцијалним зоонозама, иако су забележени спонтани побачај и коњуктивитис код људи који су били изложени сојевима оваца и коза. Пнеумонија због Ц. пнеумониае је недавно описан уобичајени узрок пнеумоније стечене у заједници за разлику од Ц. пситтаци инфекције. Због свог недавног открића, улога Ц. пнеумониае у ОАП-има је непотпуно истражен и неће се даље расправљати у овом прегледу.
Клиничка слика
Орнитоза варира од благе болести сличне грипу до тешке пнеумоније са енцефалитисом која је, у преантибиотској ери, имала стопу смртности (ЦФР) већу од 20%. Продромална грозница, мрзлица, мијалгија, главобоља и непродуктивни кашаљ могу трајати до три недеље пре постављања дијагнозе пнеумоније. Честе су неуролошке, јетрене и бубрежне промене. Рендгенографски налази укључују консолидацију доњег режња са хиларном лимфаденопатијом. Клиничка сумња након утврђивања радног или другог излагања птицама је кључна за дијагнозу јер нема патогномоничних налаза.
Дијагностички тестови
Орнитоза обично доводи до високог титра антитела за фиксацију комплемента (ЦФ), иако рано лечење тетрациклинима може потиснути стварање антитела. За постављање дијагнозе може се користити један акутни серумски титар ³1:16 разблажења ЦФ антитела са компатибилном клиничком презентацијом или четворострука промена титра ЦФ антитела. Неодговарајуће упарени узорци серума и висока позадина антитела на кламидију у ризичним групама подривају корисност тестова на антитела за дијагностиковање већине хламидијских болести.
Епидемиологија
Ц. пситтаци присутан је у готово свим врстама птица и чест је код сисара. Инфекција обично настаје зоонотским преносом, али је пријављен пренос са особе на особу. Асимптоматска инфекција је честа и до 11% пољопривредника без историје болести има антитела на Ц. пситтаци. Ограничене епидемије остају повремене, али пандемије повезане са трговином егзотичним птицама недавно су се догодиле 1930. У Сједињеним Државама се годишње пријави 70 до 100 случајева орнитозе, а скоро једна трећина ових болести се стекне професионално. Већина професионално стечених инфекција јавља се код радника у индустрији за прераду птица кућних љубимаца или живине и повезана је са аеросолизацијом птичјег ткива или фекалија. У земљама у којима се птице обично држе као кућни љубимци, а увозни карантин се слабо спроводи, епидемије су чешће, али је занимање мањи фактор ризика.
Остала погођена занимања
Болест се најчешће јавља код радника који се баве прерадом живине, али су угрожени радници у дистрибуцији егзотичних птица и карантинским објектима за птице, волијерима за узгој и ветеринарским клиникама.
Лечење
Тетрациклин или еритромицин у трајању од 10 до 14 дана требало би да буде адекватан третман, али клинички рецидив је чест када се лечење даје неадекватно.
Контроле јавног здравља
У Сједињеним Државама, егзотичне птице се стављају у карантин ради хемопрофилаксе са тетрациклинима. Сличне методе се користе у другим земљама у којима постоји трговина егзотичним птицама. За орнитозу није развијена вакцина. Уведени су програми за повећање вентилације да би се разблажила концентрација аеросола, смањила аеросолизација или удисање инфективних честица, или лечење болесних птица у комерцијалним постројењима за прераду, али њихова ефикасност није доказана.
Бруцеллосис
Годишње се око 500,000 случајева бруцелозе јавља широм света, узрокованих неколико врста Бруцелла. Патогеност Бруцелла инфекције зависе од врсте заразе, које обично имају различите резервоаре домаћине. Резервоари за Бруцелла абортус, Б. суис, Б. мелитенсис, Б. овис, Б. цанис, Б. неотомае имају тенденцију да буду говеда, свиње, козе, овце, пси и пацови, респективно.
Бруцелоза може бити последица инфекције различитим путевима, укључујући аеросолизацију. Међутим, већина болести је последица узимања непастеризованих млечних производа од коза. Настала системска болест је узрокована Б. мелитенсис али није повезана са одређеним занимањима. Пнеумонија се јавља у 1% случајева, иако је кашаљ чест налаз.
У развијеним земљама, професионалну бруцелозу обично изазива Бруцелла абортус и резултат је гутања или удисања инфективних аеросола повезаних са плацентама свиња и говеда. Субклиничка инфекција је честа; до 1% пољопривредних радника има антитела на Б. абортус. Болест се развија код око 10% заражених особа. За разлику од болести због Б. мелитенсис, болест повезана са Б. абортус обично стечено професионално и мање је тешко. Особе са акутном бруцелозом развијају високу дневну температуру, артралгију и хепатоспленомегалију. Код примарне бруцела пнеумоније, пнеумонична консолидација је заправо ретка, а плућни налази могу укључивати промуклост или пискање, хиларну аденопатију, перибронхијалне инфилтрате, паренхимске чворове или милијарни образац. Изолација се може направити из коштане сржи у 90% акутних случајева и из крви у 50 до 80% случајева. Дијагноза се може поставити серолошки уз помоћ различитих тестова на антитела. Тетрациклине треба користити четири до шест недеља, а за синергију се може додати рифампин. Узгајивачи говеда, коза, оваца и свиња, млекари, радници у кланицама, ветеринари и месари су примарна угрожена популација. Програми тестирања и искорењивања бруцеле увелико су смањили број заражених животиња и идентификовали она стада која представљају највећи ризик за преношење болести. Када радите са животињама зараженим бруцелом, избегавање или лична заштита, посебно након абортуса или порођаја, су једине ефикасне методе контроле болести.
Инхалациони антракс
Инхалациони антракс се јавља широм света, али је ређи од кожног антракса. Антракс је системска болест код многих животиња и обично се преноси на људе перкутаном инфекцијом прерадом или једењем контаминираног меса. Инхалациони антракс настаје удисањем спора Бациллус антхрацис од костију, длаке или коже оваца, коза или говеда („болест вуне”) или ретко током прераде зараженог меса. Споре се подвргавају фагоцитози алвеоларним макрофагима и транспортују до медијастиналних лимфних чворова, где клијају. Ово доводи до хеморагичног медијастинитиса, али се ретко манифестује као примарна пнеумонија. Болест се карактерише проширеним медијастинумом, плућним едемом, плеуралним изливом, спленомегалијом и брзим напредовањем до респираторне инсуфицијенције. Стопа смртности је 50% или више упркос антибиотицима и респираторној подршци. Позитивне хемокултуре су уобичајене, али се може користити серолошка тестирања помоћу блотинг имунотеста. Болесне особе се лече високим дозама пеницилина или интравенским ципрофлоксацином као алтернативом код особа алергичних на пеницилин. Узгајивачи животиња, ветеринари, ветеринарски радници, прерађивачи длаке и коже и радници у кланицама су под повећаним ризиком. Годишња вакцинација је доступна за животиње у ендемским подручјима и људе са високим ризиком од болести. Специфичне мере контроле против инхалационог антракса укључују деконтаминацију формалдехидом, стерилизацију паром или зрачење косе и коже; забрана увоза коже из ендемских подручја; и личну респираторну заштиту радника.
Пнеумонична куга
Куга, узрокована Иерсиниа пестис, је претежно ензоотична болест коју преносе буве код дивљих глодара. Људи се обично заразе када их угризе заражена бува и често развију септикемију. У Сједињеним Државама од 1970. до 1988. секундарна пнеумонија услед хематогеног ширења развила се код приближно 10% септикемичних особа. Животиње и људи са плућном кугом производе заразне аеросоле. Примарна пнеумонија код људи може настати удисањем инфективног аеросола који се ствара око умирућих животиња са секундарном упалом плућа. Упркос потенцијалу за ширење пнеумоније, пренос са особе на особу је реткост и није се десио у Сједињеним Државама скоро 50 година. Контрола болести укључује изолацију особа са плућном кугом и коришћење личне респираторне заштите од стране здравствених радника. Могуће је преношење аеросола на болничке раднике, а тетрациклинску профилаксу треба размотрити за свакога ко је у контакту са људима или животињама са плућном кугом. Бројна занимања су изложена ризику од преношења аеросола, укључујући биомедицинске и болничке лабораторијске раднике и, у ендемским областима, бројна сеоска занимања, укључујући ветеринаре, раднике за сузбијање глодара, ловце/замке, мамологе, биологе за дивље животиње и пољопривредне раднике. Лицима у високоризичним занимањима препоручује се мртва вакцина.
К грозница
Узроковано удисањем Цокиелла бурнетииК грозница је системско обољење које се манифестује као атипична упала плућа код 10 до 60% заражених особа. Много различитих изолата од Ц. бурнетии производе болести, а теорије вируленције зависне од плазмида су контроверзне. Ц. бурнетии инфицира многе домаће животиње (нпр. овце, говеда, козе, мачке) широм света; распршује се из урина, фецеса, млека, плаценте или ткива материце; формира ендоспоре високе отпорности које остају заразне годинама; и изузетно је заразна.
Клиничка слика
Након периода инкубације од 4 до 40 дана, акутна К грозница се манифестује као болест слична грипу која напредује у атипичну пнеумонију сличну Мицопласма. Акутна болест траје око две недеље, али може трајати до девет недеља. Хронична болест, претежно ендокардитис и хепатитис, може се развити до 20 година након акутне болести.
Дијагностички тестови
Примарна изолација од Ц. бурнетии се ретко изводи јер захтева висок ниво биолошке безбедности. Дијагноза се поставља серолошки демонстрирањем титра ЦФ антитела од 1:8 или већег у одговарајућем клиничком окружењу или четвороструке промене титра ЦФ.
Остала погођена занимања
Пољопривредни (посебно млечни производи и вуна), болнички лабораторији и биомедицински истраживачи су у опасности од инфекције.
Лечење
Не постоји ефикасна вакцина за Ц. бурнетии. За лечење акутне болести користи се двонедељни курс тетрациклина или ципрофлоксацина.
Контроле јавног здравља
Због своје широко распрострањене географске распрострањености, бројних животињских резервоара и отпорности на инактивацију, лична респираторна заштита и инжењерска контрола за задржавање инфективних аеросола једине су ефикасне превентивне мере. Међутим, ове методе контроле је тешко применити у многим пољопривредним срединама (нпр. у узгоју оваца и говеда). Рана дијагноза К грознице од стране медицинског особља може бити олакшана едукацијом радника са високим ризиком за добијање ове ретке болести. Може доћи до преношења на болничко особље, а изолација може ограничити ширење пнеумоније К грознице у болницама.
Разни бактеријски ОАПС пољопривредних радника
Псеудомонас псеудомаллеи је организам повезан са земљиштем и глодарима углавном у југоисточној Азији који изазива мелиоидозу. Болест је повезана са изложеношћу тла и потенцијално дугом латенцијом. Војно особље током и након Вијетнамског рата биле су главне жртве мелиоидозе у Сједињеним Државама. Мултифокална, нодуларна, супуративна или грануломатозна пнеумонија карактерише плућни облик мелиоидозе.
Франциселла туларенсис, етиолошки агенс туларемије, је зооноза повезана са дивљим глодарима и лагоморфима. Ово је потенцијална професионална болест биолога дивљих животиња, мамолога, радника за дератизацију, ловаца, ловаца и ветеринара. Туларемија може бити резултат удисања, директне инокулације, кожног контакта или гутања, или се може преносити векторима. Плућна болест је резултат директног излагања инхалацији или хематогеног ширења септикемије. Плућне лезије туларемије су акутне, мултифокалне, гнојне и некротизирајуће.
Хистоплазмоза
Хистоплазмоза је узроковано Хистопласма цапсулатум, слободно живућа буђ у земљишту повезана са фекалијама птица или слепих мишева. Хистоплазмоза је најважнији узрок гљивичних ОАП-а код пољопривредних радника. Разне гљивичне упале плућа пољопривредних радника описане су у следећем одељку.
Клиничка слика
Након излагања, стопа напада и озбиљност хистоплазмозе варирају у зависности од инфицираног инокулума и нивоа антитела домаћина добијених претходном инфекцијом. Након тешке изложености, до 50% особа развије самоограничену респираторну болест, док остали остају асимптоматски. Најмањи од симптоматских синдрома укључује симптоме „налик грипу“, непродуктиван кашаљ и бол у грудима. Физички преглед може бити значајан за еритем нодозум или мултиформни еритем. Рендгенски снимци грудног коша показују шарене, сегментне инфилтрате, али рендгенски налази не могу специфично разликовати хистоплазмозу од других плућних инфекција. Хиларна или медијастинална лимфаденопатија је честа у свим стадијумима примарне хистоплазмозе.
Прогресивна примарна пнеумонична хистоплазмоза карактерише се дубоким системским тегобама, кашљем са продуктивним гнојним спутумом и хемоптизом. Прогресивне рендгенске промене укључују вишеструке нодуле, лобарну консолидацију и густе, мултилобарне интерстицијалне инфилтрате. Веће изложености повећавају тежину болести и резултирају тешким респираторним обољењем, синдромом акутног респираторног дистреса (АРДС) или ателектазом због опструкције медијастиналном лимфаденопатијом.
Приближно 20% оболелих особа развије друге синдроме хистоплазмозе који су идиосинкратични и нису резултат веће изложености или прогресије примарне болести. Синдроми укључују артритис-еритема нодозум, перикардитис и хроничну плућну хистоплазмозу (фиброзни апикални инфилтрати плућа са кавитацијом). Дисеминована хистоплазмоза се развија код малог процента пацијената, посебно код имуносупресивних.
Дијагностички тестови
Коначна дијагноза се поставља изолацијом или хистопатолошким демонстрирањем организма у одговарајућем клиничком узорку. Нажалост, организам је присутан у малим концентрацијама и осетљивост ових метода је мала. Претпостављене дијагнозе се често постављају на основу географске локације, историје изложености и рендгенских налаза плућа или калцификација у слезини.
Епидемиологија
Х. цапсулатум се налази широм света у вези са специфичним условима земљишта, али се болест јавља првенствено из долина река Охајо и Мисисипи у Сједињеним Државама. Високе концентрације спора налазе се у птичјим склоништима, старим зградама, живинарницама, пећинама или школским двориштима; поремећени су радном активношћу. Концентрација микроконидије је већа у поремећеним, затвореним просторима (нпр. рушење зграда) и доводи до већег инокулума за раднике него на већини локација на отвореном. У ендемским подручјима, особе које чисте птичја склоништа, руше старије контаминиране зграде или врше ископавања за изградњу путева или зграда су у већем ризику од опште популације. У Сједињеним Државама, 15,000 до 20,000 особа сваке године буде хоспитализовано са хистоплазмозом, а приближно 3% њих умре.
Остала погођена занимања
Приписивање професионалног ризика за Хистопласма инфекција је отежана јер организам слободно живи у земљишту, а концентрацију распршених спора повећава ветар и прашњави услови. Инфекција је углавном узрокована географском локацијом. У ендемским подручјима, рурална лица, без обзира на занимање, имају 60 до 80% преваленције позитивног кожног теста на Х. цапсулатум антигени. Стварна болест је резултат великог инфективног инокулума и обично је ограничена на раднике који су укључени у нарушавање тла или уништавање контаминираних зграда.
Лечење
Антифунгални третман за хистоплазмозу и друге гљивичне инфекције стечене на радном месту није индикован за акутну самоограничену плућну болест. Терапија амфотерицином Б (укупна доза од 30 до 35 мг/кг) или кетоконазолом (400 мг/дан током шест месеци) или режими лечења који користе оба лека индикована је за дисеминовану хистоплазмозу, хроничну плућну хистоплазмозу, акутну плућну хистоплазмозу са АРДС-ом или медијастиналну гранулом са симптоматском опструкцијом и може бити корисна за продужену, умерено тешку примарну болест. Лечење резултира стопом одговора од 80 до 100%, али рецидиви су чести и могу бити чак 20% код амфотерицина Б и 50% код кетоконазола. Ефикасност новијих азолних лекова (тј. итраконазола и флуконазола) за професионалне гљивичне инфекције није дефинисана.
Контроле јавног здравља
Није развијена ефикасна вакцина. Хемијска деконтаминација са 3% формалдехида, претходно влажење земље или контаминираних површина да би се смањила аеросолизација и лична респираторна заштита да би се смањило удисање спора у облику аеросола могу смањити инфекцију, али ефикасност ових метода није утврђена.
Разне гљивичне пнеумоније
Разне гљивичне пнеумоније пољопривредних радника укључују аспергилозу, бластомикозу, криптококозу, кокцидиоидомикозу и паракокцидиоидомикозу (табела 1). Ове болести су узроковане Аспергиллус спп., Бластомицес дерматитидис, Цриптоцоццус неоформанс, Цоццидиоидес иммитис парацоццидиоидес брасилиенсис, редом. Иако ове гљиве имају широко распрострањену географску распрострањеност, болест се обично јавља из ендемских подручја. У односу на вирусне и бактеријске узроке пнеумоније, ови поремећаји су ретки и често се у почетку не сумњају. Поремећаји Т-ћелија повећавају осетљивост на хистоплазмозу, бластомикозу, криптококозу, кокцидиоидомикозу и паракокцидиоидомикозу. Међутим, велика почетна изложеност може довести до болести код имунокомпетентног радника. Инфекције са Аспергиллус и сродне гљиве се јављају код пацијената са неутропенијом. Аспергилоза је најчешће ОАП имуносупресивних особа и о њој ће се говорити у одељку о инфекцијама код имуносупресивних.
Цр. неоформанс, као Х. цапсулатум, је обичан становник земљишта контаминираног птичјим фекалијама, и професионална изложеност таквој прашини или другим прашинама контаминираним са Цр. неоформанс може довести до болести. Професионална бластомикоза је повезана са спољним занимањима, посебно у источним и централним Сједињеним Државама. Кокцидиоидомикоза је резултат излагања контаминираној прашини у ендемским областима југозападних Сједињених Држава (отуда синоним грозница долине Сан Хоакин). Професионална изложеност контаминираном земљишту Јужне и Централне Америке често је повезана са паракокцидиоидомикозом. Због потенцијално дуге латенције код паракокцидиоидомикозе, ова изложеност може дуго да претходи појави симптома.
Клиничка слика
Клиничка слика кокцидиоидомикозе, бластомикозе или паракокцидиоидомикозе је слична хистоплазмози. Изложеност аеросолу овим гљивама може произвести ОАП ако је почетни инокулум довољно висок. Међутим, фактори домаћина, као што је претходна изложеност, ограничавају болест код већине појединаца. Код кокцидиоидомикозе, плућни и системски знаци болести су очигледни код малог процента инфицираних; прогресивна болест са дисеминацијом на више органа је ретка у одсуству имуносупресије. Иако су извор инфекције обично плућа, бластомикоза се може манифестовати као плућна болест, кожна болест или системска болест. Најчешћа клиничка слика бластомикозе је хронични кашаљ са пнеумонијом која се не разликује од туберкулозе. Међутим, већина пацијената са клинички очигледном бластомикозом ће имати ванплућне лезије које укључују кожу, кости или генитоуринарни систем. Паракокцидиоидомикоза је болест Мексика, Централне и Јужне Америке која се најчешће манифестује као реактивација претходне инфекције након дугог али променљивог периода латенције. Болест може бити повезана са старењем инфицираних особа, а реактивација може бити изазвана имуносупресијом. Плућна презентација је слична другим гљивичним пнеумонијама, али је екстрапулмонална болест, посебно слузокоже, честа код паракокцидиоидомикозе.
Плућа су уобичајено место за примарну инфекцију Цриптоцоццус неоформанс. Као и код претходно разматраних гљива, плућне инфекције могу бити асимптоматске, самоограничене или прогресивне. Међутим, дисеминација организма, посебно на мождане овојнице и мозак, може се десити без симптоматске респираторне болести. Криптококни менингоенцефалитис без доказа плућне криптококозе, иако ретко, је најчешћа клиничка манифестација Цр. неоформанс инфекције.
Дијагностички тестови
Директна демонстрација ткивног облика организма омогућава коначну дијагнозу у биопсијама и цитолошким препаратима. Имунофлуоресценција може бити корисна потврдна процедура ако морфолошки детаљи нису довољни за утврђивање етиолошког агенса. Ови организми се такође могу узгајати из сумњивих лезија. Позитиван латекс криптококни аглутинин тест у цереброспиналној течности је у складу са криптококним менингоенцефалитисом. Међутим, демонстрација организама можда неће бити довољна за дијагнозу болести. На пример, сапрофитски раст Цр. неоформанс могуће је у дисајним путевима.
Остала погођена занимања
Лабораторијски радници који изолују ове гљиве су у опасности од инфекције.
Лечење
Антифунгална терапија је слична оној за хистоплазмозу.
Контроле јавног здравља
Инжењерске контроле су назначене да би се смањио ризик за лабораторијске раднике. Заштита органа за дисање при раду на земљишту које је јако контаминирано птичијим фекалијама смањиће изложеност Цр. неоформанс.
Професионалне инфекције код здравствених и лабораторијских радника
Удисање инфективних аеросола је најчешћи извор инфекције код болничких радника, а многе врсте вирусних и бактеријских пнеумонија се приписују преношењу на послу (Табела 26). Већина инфекција је вирусна и самоограничава се. Међутим, потенцијално озбиљне епидемије туберкулозе, морбила, пертусиса и пнеумококне пнеумоније су пријављене код болничких радника. О инфекцијама код радника са ослабљеним имунитетом говори се на крају овог одељка.
Дијагностички лабораторијски радници су у опасности од професионално стечених инфекција које су резултат преноса ваздушним путем. Пренос се дешава када се патогени распршују током иницијалне обраде клиничких узорака пацијената са неизвесним заразним болестима и ретко се препознају. На пример, у недавној епидемији бруцелозе у заједници, једна трећина лабораторијских техничара развила је бруцелозу. Запослење у лабораторији је био једини идентификовани фактор ризика. Пренос са особе на особу између запослених у лабораторији, преношење путем хране или воде, или контакт са одређеним клиничким узорком не може се показати као фактор ризика. Рубеола, туберкулоза, варичела-зостер и респираторни синцицијски вирус су професионалне болести које техничари на сличан начин добијају у лабораторији.
Упркос ригорозној ветеринарској нези, процедурама биолошке безбедности и коришћењу лабораторијских животиња које се узгајају у комерцијалним условима, без патогена, инхалација остаје главни начин преношења заразних болести повезан са биомедицинским истраживачима. Поред тога, новооткривени микроорганизми или раније непрепознати резервоари зооноза могу се срести и поткопати ове стратегије контроле болести.
Меаслес
Меаслес, као професионална болест, постала је све већи проблем међу болничким радницима у развијеним земљама. Од 1989. године дошло је до поновног избијања морбила у Сједињеним Државама због лошег поштовања препорука о вакцинама и неуспеха примарне имунизације код примаоца вакцине. Због високог морбидитета и потенцијалног морталитета који је повезан са морбилима код осетљивих радника, посебну пажњу треба посветити морбилама у било ком програму здравствене заштите на раду. Од 1985. до 1989. године, у Сједињеним Државама пријављено је више од 350 случајева професионално стечених морбила, што представља 1% свих пријављених случајева. Скоро 30% болничких радника са професионалним богињама је хоспитализовано. Највеће групе болничких радника оболелих од морбила биле су медицинске сестре и лекари, а 90% њих је оболело од морбила. Иако је 50% ових оболелих особа имало право на вакцинацију, ниједна није вакцинисана. Повећани морбидитет и морталитет од морбила код одраслих повећао је забринутост да заражени радници могу заразити пацијенте и сараднике.
Године 1989. Саветодавни комитет за имунизацију препоручио је две дозе вакцине против малих богиња или доказ о имунитету против морбила у време запослења у здравственој установи. Серолошки и вакцинални статус радника треба документовати. Поред тога, када су присутни пацијенти са богињама, одговарајућа је поновна процена имунолошког статуса ЗР. Примена ових препорука и одговарајућа изолација пацијената са познатим и сумњивим на богиње смањује преношење морбила у медицинским установама.
Клиничка слика
Поред уобичајене презентације малих богиња код одраслих без имунитета, морају се узети у обзир атипичне и модификоване манифестације морбила јер су многи болнички радници претходно примили мртве вакцине или имају делимичан имунитет. Код класичних морбила, након инфекције следи двонедељни период инкубације са благим симптомима горњих дисајних путева. Током овог периода, радник је виремичан и заразан. Након тога следи седмо- до десетодневни ток кашља, коризе и коњуктивитиса и развој морбилиформног осипа и Коплик пега (повишене беле лезије на букалној слузокожи), које су патогномоничне за морбиле. На рендгенском снимку се примећују дифузни ретикулонодуларни инфилтрати са билатералном хиларном лимфаденопатијом, често са суперпонираном бактеријском бронхопнеумонијом. Ови знаци се јављају много након што је особа имала прилику да зарази друге осетљиве особе. Плућне компликације чине 90% смртних случајева од морбила код одраслих. Ниједан специфични антивирусни третман није ефикасан за било који облик морбила, иако високи титар имуноглобулина против морбила може ублажити неке симптоме код одраслих.
Код атипичних малих богиња, које се јављају код особа вакцинисаних убијеном вакцином развијеном 1960-их, честа је тешка плућна захваћеност. Осип је нетипичан, а Коплик пеге су ретке. Код модификованих малих богиња, које се јављају код особа које су претходно примиле живу вакцину, али развијају делимични имунитет, знаци и симптоми су слични класичним богињама, али су блажи и често остају непримећени. Особе са атипичним и модификованим богињама су виремичне и могу ширити вирус морбила.
Дијагноза
Морбиле код болничких радника су често модификоване или атипичне, и ретко се сумња на њих. О морбили треба размотрити код особа са еритематозним макулопапулозним осипом којем претходи фебрилни продром од три до четири дана. Код особа са првом инфекцијом и без претходне имунизације, изолација вируса или детекција антигена је отежана, али се за брзу дијагнозу могу користити ензимски имуносорбентни тестови или тестови флуоресцентних антитела. Код особа са претходним имунизацијама, тумачење ових тестова је тешко, али имунофлуоресцентне мрље антитела ексфолијираних ћелија могу бити од помоћи.
Епидемиологија
Подложне медицинске сестре и лекари имају скоро девет пута већу вероватноћу да оболе од морбила него особе истог узраста које нису ЗР. Као и код свих инфекција морбила, пренос са особе на особу се дешава удисањем инфективног аеросола. Болнички радници добијају богиње од пацијената и сарадника и, заузврат, преносе морбиле на осетљиве пацијенте, сараднике и чланове породице.
Остала погођена занимања
Епидемијске морбиле су се појавиле у академским институцијама у развијеним земљама и међу пољопривредним радницима ограниченим на колективни смештај на плантажама.
Контроле јавног здравља
Стратегије интервенције у јавном здравству укључују програме имунизације, као и програме контроле инфекција за праћење болести морбила и статуса антитела радника. Ако се природна инфекција или одговарајућа вакцинација са две дозе не могу документовати, треба урадити тестове на антитела. Вакцинација трудница је контраиндикована. Вакцинација других ризичних радника је важна помоћ у превенцији болести. Након излагања малим богињама, уклањање осетљивих радника из контакта са пацијентима током 21 дан може смањити ширење болести. Ограничена активност радника који болују од морбила 7 дана након појаве осипа такође може умањити преношење болести. Нажалост, адекватно вакцинисани радници су развили морбиле упркос нивоима заштитних антитела који су документовани пре болести. Као резултат тога, многи препоручују личну респираторну заштиту када се брину о пацијентима са богињама.
Разне вирусне инфекције респираторног тракта
Различити вируси који нису јединствени за окружење здравствене заштите су најчешћи узрок ОАП-а код здравствених радника. Етиолошки агенси су они који изазивају ОАП стечене у заједници, укључујући аденовирус, цитомегаловирус, вирус грипа, вирус параинфлуенце и респираторни синцицијски вирус. Пошто су ови организми такође присутни у заједници, тешко је установити их као узрок индивидуалног ОАП-а. Међутим, серолошке студије сугеришу да су здравствени радници и радници у дневној нези изложени повећаном ризику од изложености овим респираторним патогенима. Ови вируси су такође одговорни за избијање болести у многим ситуацијама када су радници окупљени у скученом простору. На пример, избијања аденовирусне инфекције су честа код војних регрута.
Велики кашаљ
Пертуссис, као и богиње, све се чешће јавља код болничких радника у развијеним земљама. У 1993. години, скоро 6,000 случајева пертусиса је пријављено у Сједињеним Државама, што је повећање од 80% у односу на 1992. годину. За разлику од претходних година, 25% пријављених случајева догодило се код особа старијих од десет година. Број професионално стечених болести код болничких радника је непознат, али се сматра да је недовољно пријављен у развијеним земљама. Због опадања имунитета код одраслих и потенцијала болничких радника да заразе осетљиву бебу, већи је нагласак на дијагностици и надзору пертусиса.
Клиничка слика
Пертуссис може трајати шест до десет недеља без интервенције. У првој недељи, када је оболели најзаразнији, развијају се сув кашаљ, нагризање, коњунктивитис и температура. Код претходно вакцинисаних одраслих особа, упоран, продуктиван кашаљ може трајати неколико недеља, а пертусис се ретко разматра. Клиничка дијагноза је тешка, а клиничку сумњу треба побудити када наиђете на било ког радника са кашљем који траје дуже од седам дана. Број белаца већи од 20,000 са доминацијом лимфоцита може бити једина лабораторијска абнормалност, али се то ретко примећује код одраслих. Рендгенски снимци грудног коша показују конфлуентну бронхопнеумонију у доњим режњевима који зраче из срца дајући карактеристичан знак „чупавог срца“, а ателектаза је присутна у 50% случајева. Због екстремне инфективности овог агенса, неопходна је строга респираторна изолација све док се лечење еритромицином или триметопримом/сулфаметоксазолом не настави пет дана. Блиски контакти заражених особа и болничких радника који нису користили респираторне мере треба да добију 14 дана антибиотске профилаксе без обзира на статус имунизације.
Дијагноза
Изолација од Бордетелла пертуссис, директно имунофлуоресцентно бојење назалних секрета или развој а Б. пертуссис одговор антитела се користи за постављање коначне дијагнозе.
Епидемиологија
Б. пертуссис је веома заразна, преноси се са особе на особу удисањем инфективних аеросола и има стопу напада од 70 до 100%. У прошлости, то није била болест одраслих и није била цењена као ОАП. Током избијања пертусиса у заједници у западним Сједињеним Државама, многи болнички радници су били изложени на послу и развили су пертуссис упркос антибиотској профилакси. Због опадања нивоа заштитних антитела код одраслих који никада нису имали клиничку болест, али су примили ћелијску вакцину после 1940. године, у развијеним земљама расте популација болничких радника осетљивих на пертуссис.
Контроле јавног здравља
Идентификација, изолација и лечење су главне стратегије контроле болести у болницама. Улога ацелуларне вакцине против пертусиса за болничке раднике без адекватних нивоа заштитних антитела је нејасна. Током недавне епидемије у западним Сједињеним Државама, једна трећина вакцинисаних болничких радника пријавила је благе до умерене нуспојаве на вакцину, али 1% је имало „тешке“ системске симптоме. Иако су ови теже погођени радници пропустили дане са посла, нису пријављени никакви неуролошки симптоми.
Туберкулоза
Током 1950-их, опште је познато да су здравствени радници у развијеним земљама изложени већем ризику од туберкулозе (ТБ—грануломатозна болест због Мицобацтериум туберцулосис или блиско сродни организми М. бовис) него општа популација. Од 1970-их до раних 1980-их, истраживања су показала да је ово постао само незнатно повећан ризик. Крајем 1980-их, значајан пораст броја случајева туберкулозе примљених у америчке болнице резултирао је несумњивим преносом М. туберцулосис болничким радницима. Висока позадинска преваленција позитивног туберкулинског кожног теста (ТСТ) у одређеним социо-економским или имигрантским групама из којих су долазили многи болнички радници, и лоша повезаност конверзије ТСТ-а са изложеношћу ТБЦ-у на послу, отежали су квантификацију ризика од Професионални пренос туберкулозе на раднике. Године 1993. у Сједињеним Државама, процењено је да су 3.2% пријављених особа са ТБ били здравствени радници. Упркос проблемима у дефинисању ризика, инфекцију у вези са радом треба узети у обзир када болнички радници развију ТБ или конвертују ТСТ.
М. туберцулосис шири се готово искључиво од особе до особе на инфективним честицама пречника од 1 до 5 мм које су резултат кашљања, разговора или кихања. Ризик од инфекције је директно повезан са интензитетом изложености инфективним аеросолима – малим заједничким просторима, повећаном густином инфективних честица, лошим уклањањем инфективних честица, рециркулацијом ваздуха који садржи инфективне честице и продуженим временом контакта. У здравственим установама, процедуре као што су бронхоскопија, ендотрахеална интубација и третман небулизованим аеросолом повећавају густину инфективних аеросола. Отприлике 30% блиских контаката — особа које деле заједнички простор са заразном особом — се заразе и подвргну конверзији кожним тестом. Након инфекције, 3 до 10% особа ће развити ТБ у року од 12 месеци (тј. примарна болест), а додатних 5 до 10% ће развити ТБ током свог живота (тј. болест реактивације). Ове веће стопе се јављају у земљама у развоју и ситуацијама када је неухрањеност чешћа. Особе заражене ХИВ-ом реактивирају ТБ у већим стопама, отприлике 3 до 8% годишње. ЦФР варира; у развијеним земљама је између 5 и 10%, али у земљама у развоју ове стопе се крећу од 15 до 40%.
Клиничка слика
Пре епидемије ХИВ-а, 85 до 90% особа са туберкулозом имало је захваћеност плућа. Хронични кашаљ, производња спутума, грозница и губитак тежине остају најчешће пријављени симптоми плућне туберкулозе. Осим ретког амфоричног дисања или пост-тусивног пуцкетања над горњим режњевима, физички преглед није од помоћи. Абнормални рендгенски снимак грудног коша налази се у скоро свим случајевима и обично је први налаз који указује на туберкулозу. Код примарне ТБ чест је инфилтрат доњег или средњег режња са ипсилатералном хиларном лимфаденопатијом са ателектазом. Реактивација туберкулозе обично доводи до инфилтрата и кавитације у горњим режњевима плућа. Иако су осетљиви, рендгенски зраци грудног коша немају специфичност и неће дати коначну дијагнозу туберкулозе.
Дијагноза
Коначна дијагноза плућне туберкулозе може се поставити само изолацијом М. туберцулосис из спутума или плућног ткива, иако је могућа дијагноза ако се бацили отпорни на киселину (АФБ) нађу у спутуму особа са компатибилним клиничким сликама. Дијагнозу туберкулозе треба размотрити на основу клиничких знакова и симптома; изолацију и лечење особа са компатибилним болестима не треба одлагати због резултата ТСТ. У земљама у развоју у којима ТСТ реагенси и рендгенски зраци грудног коша нису доступни, СЗО предлаже процену особа са било којим респираторним симптомом у трајању од три недеље, хемоптизом било ког трајања или значајним губитком тежине за туберкулозу. Ове особе треба да имају микроскопски преглед свог спутума на АФБ.
Остала погођена занимања
Од радника до радника и од клијента до радника ваздушни пренос М. туберцулосис је документовано међу болничким радницима, летачким посадама авио-компанија, рударима, радницима поправних установа, чуварима животиња, радницима у бродоградилишту, запосленима у школама и радницима у фабрици шперплоче. Посебна пажња се мора посветити одређеним занимањима као што су радници на фарми, чувари животиња, физички радници, домаћице, домари и радници који припремају храну, иако највећи део ризика може бити последица социо-економског или имиграционог статуса радника.
Посебну пажњу треба посветити плућној ТБ међу рударима и другим групама изложеним силицијум диоксиду. Поред повећаног ризика од примарне инфекције од колега рудара, особе са силикозом имају већу вероватноћу да напредују до туберкулозе и имају већи морталитет специфичан за туберкулозу у поређењу са радницима који немају силикозу. Као и код већине особа, ТБ се реактивира код силикотичних особа од давнина М. туберцулосис инфекције које су претходиле излагању силицијум диоксиду. У експерименталним системима, показало се да изложеност силицијум диоксиду погоршава ток инфекције на начин који зависи од дозе, али није јасно да ли су радници који нису изложени силицијуму изложени већем ризику од развоја туберкулозе. Ливници изложени силицијум диоксиду без радиографске силикозе имају три пута већи ризик од смртности од туберкулозе у поређењу са сличним радницима који нису били изложени силицијум диоксиду. Ниједна друга изложеност прашини на радном месту није повезана са појачаним напредовањем туберкулозе.
Већа је вероватноћа да ће радници мигранти на фарми развити реактивирајућу ТБ него општа популација. Процене позитивних ТСТ код радника миграната крећу се од приближно 45% код особа од 15 до 34 године до скоро 70% код радника старијих од 34 године.
Радници клиничких лабораторија су под повећаним ризиком од професионално стечене туберкулозе путем ваздушног преноса. У недавном десетогодишњем истраживању одабраних болница у Јапану, 0.8% лабораторијских радника развило је туберкулозу. Нису идентификовани извори у заједници, а изложеност у вези са радом идентификована је у само 20% случајева. Највише случајева догодило се међу радницима у патолошким и бактериолошким лабораторијама и салама за обдукцију.
Лечење
Неколико режима лечења показало се ефикасним у различитим амбулантним условима. Међу пацијентима који се придржавају прописа у развијеним земљама, дневне дозе четири лека (укључујући изониазид и рифампин) током два месеца, праћене дневним дозама изониазида и рифампина у наредна четири месеца, постале су стандардни режим лечења. Директно посматрано, примена истих лекова два пута недељно је ефикасна алтернатива код пацијената са мање усаглашености. У земљама у развоју и у ситуацијама када лекови против туберкулозе нису лако доступни, коришћено је 9 до 12 месеци дневног дозирања изониазида и рифампина. Режим лечења треба да буде у складу са националном политиком и да узме у обзир осетљивост организма на стандардне, доступне антитуберкулозне лекове и трајање терапије. Због ограничених ресурса за контролу туберкулозе у земљама у развоју, напори се могу фокусирати на примарне изворе инфекције – пацијенте са размазима спутума који показују АФБ.
У здравственим установама индикована су ограничења рада за инфективне раднике са плућном туберкулозом. У другим окружењима, заразни радници могу једноставно бити изоловани од других радника. Генерално, особе се сматрају неинфективним након две недеље узимања одговарајућих антитуберкулозних лекова ако дође до симптоматског побољшања и смањења густине АФБ у размазу спутума.
Контроле јавног здравља
Главна јавноздравствена контрола преноса туберкулозе на радном месту или у заједници остаје идентификација, изолација и лечење особа са плућном ТБ. Вентилација за разблаживање инфективних аеросола; филтрација и ултраљубичаста светла за деконтаминацију ваздуха који садржи аеросол; или лична респираторна заштита се може користити тамо где је познато да је ризик од преношења изузетно висок, али ефикасност ових метода још увек није позната. Корисност БЦГ-а у заштити радника остаје контроверзна.
Разне бактеријске инфекције у здравственом окружењу
Уобичајене бактеријске инфекције плућа могу се добити од пацијената или унутар заједнице. Преношење бактеријских патогена путем ваздуха у вези са радом као нпр Стрептоцоццус пнеумониае, Хаемопхилус инфлуенза, Неиссериа менингитидис, Мицопласма пнеумониае Легионелла спп (Табела 26) се јављају и настале болести су укључене у многе програме болничког надзора. Професионалне бактеријске инфекције респираторног тракта такође нису ограничене на здравствене раднике. Инфекције са Стрептоцоццус спп су, на пример, добро утврђени узрок избијања болести међу војним регрутима. Међутим, за одређеног радника, преваленција ових поремећаја ван радног места компликује разлику између професионалних и инфекција стечених у заједници. Клиничка слика, дијагностички тестови, епидемиологија и лечење ових поремећаја описани су у стандардним медицинским уџбеницима.
Инфекције код радника са ослабљеним имунитетом
Имуносупресивни радници су под повећаним ризиком од многих ОАП. Поред тога, одређени број организама који не изазивају болест код нормалних појединаца ће изазвати болест код имуносупресивних. Тип имуносупресије ће такође утицати на подложност болести. На пример, инвазивна плућна аспергилоза је чешћа компликација хемотерапије него синдрома стечене имунодефицијенције (АИДС).
Инвазивна плућна аспергилоза се обично виђа код имуносупресивних особа, посебно код особа са неутропенијом. Међутим, инвазивна плућна аспергилоза се повремено јавља код особа без очигледне предиспозиције за болест. Инвазивна плућна аспергилоза се обично манифестује као тешка некротизирајућа пнеумонија са или без системског захвата код пацијената са неутропенијом. Док се инвазивна аспергилоза најчешће посматра као болничка инфекција код пацијената на хемотерапији, ово је веома фатална болест за било ког неутропенијског радника. Технике које смањују болничку аспергилозу — на пример, контрола прашине са грађевинских пројеката — такође могу заштитити подложне раднике.
Различити животињски патогени постају потенцијалне зоонозе само код имуносупресивног пацијента. Зоонозе које се преносе изложеношћу аеросолу које се виде само код имуносупресивних укључују енцефалитозоонозу (због Енцепхалитозоон цуницули), туберкулоза птица (због Мицобацтериум авиум) и Рходоцоццус екуи инфекције. Такве болести су посебно забрињавајуће у пољопривреди. Методе заштите имуносупресивних радника су недовољно истражене.
Код радника са ослабљеним имунитетом, многи потенцијални патогени изазивају инвазивну и тешку болест која се не види код нормалних пацијената. На пример, тешке инфекције са Цандида албицанс Пнеумоцистис царинии су класичне манифестације АИДС-а. Спектар професионалних патогена код радника са ослабљеним имунитетом, стога, потенцијално укључује поремећаје који нису присутни код имунолошки нормалних радника. Болести особа са ослабљеним имунитетом су детаљно размотрене на другим местима и о њима се неће даље расправљати у овом прегледу.
Контроле јавног здравља: Преглед
ОАП се претежно јављају у пет група радника: болнички радници, пољопривредни радници, радници у производњи меса, војно особље и радници биомедицинских лабораторија (табела 1). Избегавање инфективних аеросола је најефикаснији начин смањења инфекције у већини ситуација, али је често тешко. На пример, Цокиелла бурнетии, етиолошки агенс за К грозницу, може бити присутан у било којој средини која је претходно била контаминирана биолошким течностима заражених животиња, али избегавање свих потенцијално заражених аеросола било би непрактично у многим ситуацијама ниског ризика као што су овчарство или родео. Контрола истовремених болести такође може смањити ризик од ОАП-а. Силикоза, на пример, повећава ризик од реактивације туберкулозе, а смањење изложености силицијум диоксиду може смањити ризик од туберкулозе код рудара. За ОАП који имају значајан морталитет и морбидитет у општој популацији, имунизација може бити најважнија јавноздравствена интервенција. Едукација радника о ризику од ОАП-а помаже у усаглашавању радника са програмима контроле професионалних болести и такође помаже у раној дијагнози ових поремећаја.
Међу болничким радницима и војним особљем, пренос са човека на човека је обично главни пут инфекције. Имунизација радника може спречити болест и може бити корисна у контроли патогена високог морбидитета и/или морталитета. Зато што постоји ризик за особе које можда нису биле адекватно вакцинисане; идентификација, изолација и лечење оболелих остаје део контроле болести. Када имунизација и респираторна изолација не успеју или су повезани морбидитет и морталитет неподношљиви, може се размотрити лична заштита или инжењерска контрола за смањење густине или инфективности аеросола.
За раднике у пољопривреди, производњи меса и биомедицинским лабораторијама, пренос са животиње на човека је уобичајен образац преноса. Поред имунизације осетљивих особа када је то могуће, друге стратегије контроле болести могу укључивати имунизацију животиња, антибиотску профилаксу животиња доброг изгледа, карантин новопридошлих животиња, изолацију и лечење болесних животиња и куповину патогена. слободне животиње. Када су ове стратегије неуспешне или постоји висок морбидитет и морталитет, могу се размотрити стратегије као што су лична заштита или инжењерска контрола.
Преношење инфективних агенаса са животне средине на човека уобичајено је међу пољопривредним радницима, укључујући многе раднике. Имунизација радника је могућа када је вакцина доступна, али за многе од ових патогена, учесталост болести у општој популацији је ниска и вакцине су ретко изводљиве. У пољопривредним срединама извори инфекције су широко распрострањени. Као резултат тога, инжењерске контроле за смањење густине или инфективности аеросола су ретко изводљиве. У овим условима могу се узети у обзир средства за влажење или друге методе за смањење прашине, средства за деконтаминацију и лична заштита за дисање. Пошто је контрола ОАП-а код пољопривредних радника често тешка и медицинско особље ретко види ове болести, едукација радника и комуникација између радника и медицинског особља је од суштинског значаја.
" ОДРИЦАЊЕ ОД ОДГОВОРНОСТИ: МОР не преузима одговорност за садржај представљен на овом веб порталу који је представљен на било ком другом језику осим енглеског, који је језик који се користи за почетну производњу и рецензију оригиналног садржаја. Одређене статистике нису ажуриране од продукција 4. издања Енциклопедије (1998).“