La toxicologie mécaniste est l'étude de la façon dont les agents chimiques ou physiques interagissent avec les organismes vivants pour provoquer une toxicité. La connaissance du mécanisme de toxicité d'une substance améliore la capacité à prévenir la toxicité et à concevoir des produits chimiques plus souhaitables ; elle constitue la base de la thérapie en cas de surexposition et permet souvent une meilleure compréhension des processus biologiques fondamentaux. Aux fins de ce Encyclopédie l'accent sera mis sur les animaux pour prédire la toxicité humaine. Les différents domaines de la toxicologie comprennent la toxicologie mécaniste, descriptive, réglementaire, médico-légale et environnementale (Klaassen, Amdur et Doull 1991). Tous ces éléments bénéficient de la compréhension des mécanismes fondamentaux de la toxicité.
Pourquoi comprendre les mécanismes de toxicité ?
Comprendre le mécanisme par lequel une substance provoque une toxicité améliore différents domaines de la toxicologie de différentes manières. La compréhension mécaniste aide le régulateur gouvernemental à établir des limites de sécurité juridiquement contraignantes pour l'exposition humaine. Il aide les toxicologues à recommander des plans d'action concernant le nettoyage ou l'assainissement des sites contaminés et, avec les propriétés physiques et chimiques de la substance ou du mélange, peut être utilisé pour sélectionner le degré d'équipement de protection requis. Les connaissances mécanistes sont également utiles pour former la base de la thérapie et de la conception de nouveaux médicaments pour le traitement des maladies humaines. Pour le toxicologue médico-légal, le mécanisme de la toxicité donne souvent un aperçu de la façon dont un agent chimique ou physique peut causer la mort ou une incapacité.
Si le mécanisme de la toxicité est compris, la toxicologie descriptive devient utile pour prédire les effets toxiques des produits chimiques apparentés. Il est important de comprendre, cependant, qu'un manque d'informations mécanistes ne dissuade pas les professionnels de la santé de protéger la santé humaine. Des décisions prudentes basées sur des études animales et l'expérience humaine sont utilisées pour établir des niveaux d'exposition sûrs. Traditionnellement, une marge de sécurité était établie en utilisant le « niveau sans effet nocif » ou le « niveau le plus faible avec effet nocif » provenant d'études sur des animaux (en utilisant des modèles d'exposition répétée) et en divisant ce niveau par un facteur de 100 pour l'exposition professionnelle ou de 1,000 XNUMX pour l'exposition professionnelle. autre exposition environnementale humaine. Le succès de ce processus est évident d'après les quelques incidents d'effets néfastes sur la santé attribués à l'exposition chimique chez les travailleurs pour lesquels des limites d'exposition appropriées avaient été fixées et respectées dans le passé. De plus, la durée de vie humaine continue d'augmenter, tout comme la qualité de vie. Dans l'ensemble, l'utilisation des données de toxicité a conduit à un contrôle réglementaire et volontaire efficace. Une connaissance détaillée des mécanismes toxiques améliorera la prévisibilité des nouveaux modèles de risque en cours d'élaboration et se traduira par une amélioration continue.
La compréhension des mécanismes environnementaux est complexe et suppose une connaissance des perturbations et de l'homéostasie (équilibre) des écosystèmes. Bien que cela ne soit pas abordé dans cet article, une meilleure compréhension des mécanismes toxiques et de leurs conséquences ultimes dans un écosystème aiderait les scientifiques à prendre des décisions prudentes concernant la manipulation des déchets municipaux et industriels. La gestion des déchets est un domaine de recherche en plein essor et continuera d'être très importante à l'avenir.
Techniques d'étude des mécanismes de toxicité
La majorité des études mécanistes débutent par une étude toxicologique descriptive chez l'animal ou des observations cliniques chez l'homme. Idéalement, les études animales comprennent des observations comportementales et cliniques minutieuses, un examen biochimique minutieux des éléments du sang et de l'urine à la recherche de signes de fonctionnement indésirable des principaux systèmes biologiques de l'organisme, et une évaluation post-mortem de tous les systèmes d'organes par examen microscopique pour vérifier blessure (voir les directives d'essai de l'OCDE ; les directives de la CE sur l'évaluation des produits chimiques ; les règles d'essai de l'EPA des États-Unis ; la réglementation japonaise sur les produits chimiques). Ceci est analogue à un examen physique humain approfondi qui aurait lieu dans un hôpital sur une période de deux à trois jours, à l'exception de l'autopsie.
Comprendre les mécanismes de la toxicité est l'art et la science de l'observation, la créativité dans la sélection de techniques pour tester diverses hypothèses et l'intégration innovante des signes et des symptômes dans une relation causale. Les études mécanistes commencent par l'exposition, suivent la distribution temporelle et le devenir dans le corps (pharmacocinétique) et mesurent l'effet toxique résultant à un certain niveau du système et à un certain niveau de dose. Différentes substances peuvent agir à différents niveaux du système biologique en provoquant une toxicité.
Exposition
La voie d'exposition dans les études mécanistes est généralement la même que pour l'exposition humaine. La voie est importante parce qu'il peut y avoir des effets qui se produisent localement au site d'exposition en plus des effets systémiques après que le produit chimique a été absorbé dans le sang et distribué dans tout le corps. Un exemple simple mais convaincant d'un effet local serait l'irritation et la corrosion éventuelle de la peau suite à l'application de solutions acides ou alcalines fortes conçues pour nettoyer les surfaces dures. De même, une irritation et une mort cellulaire peuvent survenir dans les cellules tapissant le nez et/ou les poumons suite à une exposition à des vapeurs ou des gaz irritants tels que les oxydes d'azote ou l'ozone. (Les deux sont des constituants de la pollution de l'air, ou smog). Suite à l'absorption d'un produit chimique dans le sang par la peau, les poumons ou le tractus gastro-intestinal, la concentration dans tout organe ou tissu est contrôlée par de nombreux facteurs qui déterminent la pharmacocinétique du produit chimique dans le corps. Le corps a la capacité d'activer et de détoxifier divers produits chimiques, comme indiqué ci-dessous.
Rôle de la pharmacocinétique dans la toxicité
La pharmacocinétique décrit les relations temporelles pour l'absorption chimique, la distribution, le métabolisme (altérations biochimiques dans le corps) et l'élimination ou l'excrétion du corps. Par rapport aux mécanismes de toxicité, ces variables pharmacocinétiques peuvent être très importantes et, dans certains cas, déterminer si la toxicité se produira ou non. Par exemple, si un matériau n'est pas absorbé en quantité suffisante, la toxicité systémique (à l'intérieur du corps) ne se produira pas. À l'inverse, un produit chimique hautement réactif qui est détoxifié rapidement (en quelques secondes ou minutes) par des enzymes digestives ou hépatiques peut ne pas avoir le temps de provoquer une toxicité. Certaines substances et mélanges halogénés polycycliques ainsi que certains métaux comme le plomb n'entraîneraient pas de toxicité significative si l'excrétion était rapide; mais l'accumulation à des niveaux suffisamment élevés détermine leur toxicité puisque l'excrétion n'est pas rapide (parfois mesurée en années). Heureusement, la plupart des produits chimiques n'ont pas une rétention aussi longue dans le corps. L'accumulation d'un matériau inoffensif n'induirait toujours pas de toxicité. Le taux d'élimination du corps et de détoxication est souvent appelé la demi-vie du produit chimique, qui est le temps nécessaire pour que 50 % du produit chimique soit excrété ou transformé en une forme non toxique.
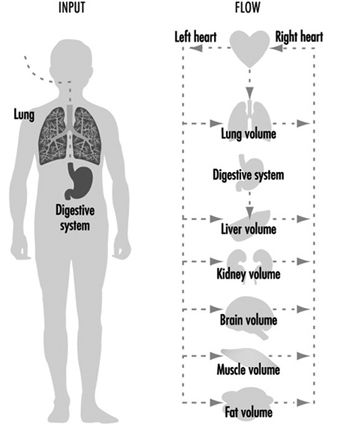
Cependant, si un produit chimique s'accumule dans une cellule ou un organe particulier, cela peut signaler une raison d'examiner plus avant sa toxicité potentielle dans cet organe. Plus récemment, des modèles mathématiques ont été développés pour extrapoler des variables pharmacocinétiques de l'animal à l'homme. Ces modèles pharmacocinétiques sont extrêmement utiles pour générer des hypothèses et tester si l'animal expérimental peut être une bonne représentation pour l'homme. De nombreux chapitres et textes ont été écrits sur ce sujet (Gehring et al. 1976 ; Reitz et al. 1987 ; Nolan et al. 1995). Un exemple simplifié d'un modèle physiologique est illustré à la figure 1.
Figure 1. Un modèle pharmacocinétique simplifié
Différents niveaux et systèmes peuvent être affectés négativement
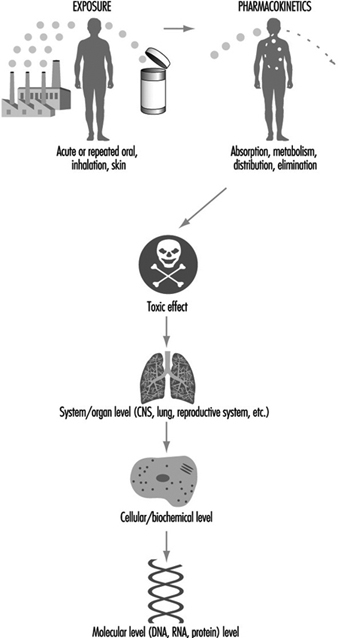
La toxicité peut être décrite à différents niveaux biologiques. La lésion peut être évaluée sur l'ensemble de la personne (ou de l'animal), du système organique, de la cellule ou de la molécule. Les systèmes organiques comprennent les systèmes immunitaire, respiratoire, cardiovasculaire, rénal, endocrinien, digestif, musculo-squelettique, sanguin, reproducteur et nerveux central. Certains organes clés comprennent le foie, les reins, les poumons, le cerveau, la peau, les yeux, le cœur, les testicules ou les ovaires et d'autres organes majeurs. Au niveau cellulaire/biochimique, les effets indésirables comprennent l'interférence avec la fonction normale des protéines, la fonction des récepteurs endocriniens, l'inhibition de l'énergie métabolique ou l'inhibition ou l'induction d'enzymes xénobiotiques (substances étrangères). Les effets indésirables au niveau moléculaire comprennent l'altération de la fonction normale de la transcription ADN-ARN, de la liaison spécifique aux récepteurs cytoplasmiques et nucléaires, et des gènes ou des produits géniques. En fin de compte, le dysfonctionnement d'un système d'organe majeur est probablement causé par une altération moléculaire dans une cellule cible particulière au sein de cet organe. Cependant, il n'est pas toujours possible de retracer un mécanisme jusqu'à une origine moléculaire de causalité, et ce n'est pas non plus nécessaire. L'intervention et la thérapie peuvent être conçues sans une compréhension complète de la cible moléculaire. Cependant, la connaissance du mécanisme spécifique de la toxicité augmente la valeur prédictive et la précision de l'extrapolation à d'autres produits chimiques. La figure 2 est une représentation schématique des différents niveaux où l'interférence des processus physiologiques normaux peut être détectée. Les flèches indiquent que les conséquences pour un individu peuvent être déterminées de haut en bas (exposition, pharmacocinétique à la toxicité du système/organe) ou de bas en haut (modification moléculaire, effet cellulaire/biochimique à la toxicité du système/organe).
Figure 2. Représentation des mécanismes de toxicité
Exemples de mécanismes de toxicité
Les mécanismes de toxicité peuvent être simples ou très complexes. Souvent, il existe une différence entre le type de toxicité, le mécanisme de toxicité et le niveau d'effet, selon que les effets indésirables sont dus à une seule dose aiguë élevée (comme un empoisonnement accidentel) ou à une dose plus faible. exposition répétée (due à une exposition professionnelle ou environnementale). Classiquement, à des fins de test, une dose élevée unique aiguë est administrée par intubation directe dans l'estomac d'un rongeur ou par exposition à une atmosphère de gaz ou de vapeur pendant deux à quatre heures, selon ce qui ressemble le mieux à l'exposition humaine. Les animaux sont observés pendant une période de deux semaines après l'exposition, puis les principaux organes externes et internes sont examinés pour détecter les blessures. Les tests à doses répétées varient de quelques mois à plusieurs années. Pour les espèces de rongeurs, deux ans sont considérés comme une étude chronique (durée de vie) suffisante pour évaluer la toxicité et la cancérogénicité, tandis que pour les primates non humains, deux ans seraient considérés comme une étude subchronique (moins que la durée de vie) pour évaluer la toxicité à doses répétées. Après l'exposition, un examen complet de tous les tissus, organes et fluides est effectué pour déterminer tout effet indésirable.
Mécanismes de toxicité aiguë
Les exemples suivants sont spécifiques aux effets aigus à forte dose pouvant entraîner la mort ou une incapacité grave. Cependant, dans certains cas, l'intervention entraînera des effets transitoires et entièrement réversibles. La dose ou la gravité de l'exposition déterminera le résultat.
Asphyxiants simples. Le mécanisme de toxicité des gaz inertes et de certaines autres substances non réactives est le manque d'oxygène (anoxie). Ces produits chimiques, qui causent une privation d'oxygène au système nerveux central (SNC), sont appelés asphyxiants simples. Si une personne pénètre dans un espace clos contenant de l'azote sans suffisamment d'oxygène, un appauvrissement immédiat en oxygène se produit dans le cerveau et entraîne une perte de conscience et éventuellement la mort si la personne n'est pas rapidement évacuée. Dans les cas extrêmes (proche de zéro oxygène), l'inconscience peut survenir en quelques secondes. Le sauvetage dépend d'un déplacement rapide vers un environnement oxygéné. La survie avec des lésions cérébrales irréversibles peut survenir à la suite d'un sauvetage retardé, en raison de la mort des neurones, qui ne peuvent pas se régénérer.
Asphyxiants chimiques. Le monoxyde de carbone (CO) entre en compétition avec l'oxygène pour se lier à l'hémoglobine (dans les globules rouges) et prive donc les tissus d'oxygène pour le métabolisme énergétique ; la mort cellulaire peut en résulter. L'intervention comprend l'élimination de la source de CO et le traitement à l'oxygène. L'utilisation directe de l'oxygène est basée sur l'action toxique du CO. Un autre asphyxiant chimique puissant est le cyanure. L'ion cyanure interfère avec le métabolisme cellulaire et l'utilisation de l'oxygène pour l'énergie. Le traitement au nitrite de sodium provoque une modification de l'hémoglobine des globules rouges en méthémoglobine. La méthémoglobine a une plus grande affinité de liaison avec l'ion cyanure que la cible cellulaire du cyanure. Par conséquent, la méthémoglobine lie le cyanure et éloigne le cyanure des cellules cibles. Cela constitue la base du traitement antidote.
Dépresseurs du système nerveux central (SNC). La toxicité aiguë est caractérisée par la sédation ou l'inconscience pour un certain nombre de matériaux comme les solvants qui ne sont pas réactifs ou qui sont transformés en intermédiaires réactifs. On suppose que la sédation/anesthésie est due à une interaction du solvant avec les membranes des cellules du SNC, ce qui altère leur capacité à transmettre des signaux électriques et chimiques. Alors que la sédation peut sembler une forme légère de toxicité et a été à la base du développement des premiers anesthésiques, « la dose fait toujours le poison ». Si une dose suffisante est administrée par ingestion ou inhalation, l'animal peut mourir par arrêt respiratoire. Si la mort anesthésique ne se produit pas, ce type de toxicité est généralement facilement réversible lorsque le sujet est retiré de l'environnement ou que le produit chimique est redistribué ou éliminé du corps.
Effets sur la peau. Les effets indésirables sur la peau peuvent aller de l'irritation à la corrosion, selon la substance rencontrée. Les acides forts et les solutions alcalines sont incompatibles avec les tissus vivants et sont corrosifs, provoquant des brûlures chimiques et d'éventuelles cicatrices. La cicatrisation est due à la mort des cellules cutanées profondes du derme responsables de la régénération. Des concentrations plus faibles peuvent simplement provoquer une irritation de la première couche de peau.
Un autre mécanisme toxique spécifique de la peau est celui de la sensibilisation chimique. Par exemple, la sensibilisation se produit lorsque le 2,4-dinitrochlorobenzène se lie aux protéines naturelles de la peau et que le système immunitaire reconnaît le complexe lié aux protéines altérées comme un corps étranger. En réagissant à ce corps étranger, le système immunitaire active des cellules spéciales pour éliminer le corps étranger en libérant des médiateurs (cytokines) qui provoquent une éruption cutanée ou une dermatite (voir « Immunotoxicologie »). C'est la même réaction du système immunitaire lorsque l'exposition à l'herbe à puce se produit. La sensibilisation immunitaire est très spécifique au produit chimique particulier et nécessite au moins deux expositions avant qu'une réponse ne soit déclenchée. La première exposition sensibilise (prépare les cellules à reconnaître le produit chimique) et les expositions suivantes déclenchent la réponse du système immunitaire. Le retrait du contact et le traitement symptomatique avec des crèmes anti-inflammatoires contenant des stéroïdes sont généralement efficaces pour traiter les personnes sensibilisées. Dans les cas graves ou réfractaires, un immunosuppresseur à action systémique comme la prednisone est utilisé en conjonction avec un traitement topique.
Sensibilisation pulmonaire. Une réponse de sensibilisation immunitaire est provoquée par le diisocyanate de toluène (TDI), mais le site cible est les poumons. La surexposition au TDI chez les personnes sensibles provoque un œdème pulmonaire (accumulation de liquide), une constriction bronchique et une altération de la respiration. Il s'agit d'une affection grave qui nécessite de soustraire l'individu à des expositions ultérieures potentielles. Le traitement est avant tout symptomatique. La sensibilisation de la peau et des poumons suit une dose-réponse. Le dépassement du niveau fixé pour l'exposition professionnelle peut entraîner des effets indésirables.
Effets sur les yeux. Les lésions oculaires vont du rougissement de la couche externe (rougeur de la piscine) à la formation de cataracte de la cornée jusqu'aux lésions de l'iris (partie colorée de l'œil). Des tests d'irritation oculaire sont effectués lorsqu'on pense qu'aucune blessure grave ne se produira. De nombreux mécanismes à l'origine de la corrosion cutanée peuvent également provoquer des lésions oculaires. Les matériaux corrosifs pour la peau, comme les acides forts (pH inférieur à 2) et les alcalis (pH supérieur à 11.5), ne sont pas testés dans les yeux des animaux car la plupart provoqueront la corrosion et la cécité en raison d'un mécanisme similaire à celui qui provoque la corrosion cutanée . De plus, les agents tensioactifs tels que les détergents et les tensioactifs peuvent provoquer des lésions oculaires allant de l'irritation à la corrosion. Un groupe de matériaux qui nécessite de la prudence est celui des tensioactifs chargés positivement (cationiques), qui peuvent provoquer des brûlures, une opacité permanente de la cornée et une vascularisation (formation de vaisseaux sanguins). Un autre produit chimique, le dinitrophénol, a un effet spécifique de formation de cataracte. Cela semble être lié à la concentration de ce produit chimique dans l'œil, qui est un exemple de spécificité de distribution pharmacocinétique.
Bien que la liste ci-dessus soit loin d'être exhaustive, elle est conçue pour donner au lecteur une appréciation des divers mécanismes de toxicité aiguë.
Mécanismes de toxicité subchronique et chronique
Lorsqu'ils sont administrés en une seule dose élevée, certains produits chimiques n'ont pas le même mécanisme de toxicité que lorsqu'ils sont administrés à plusieurs reprises à une dose plus faible mais toujours toxique. Lorsqu'une seule dose élevée est administrée, il y a toujours la possibilité de dépasser la capacité de la personne à détoxifier ou à excréter le produit chimique, ce qui peut entraîner une réponse toxique différente de celle obtenue lorsque des doses répétitives plus faibles sont administrées. L'alcool est un bon exemple. De fortes doses d'alcool entraînent des effets primaires sur le système nerveux central, tandis que des doses répétées plus faibles entraînent des lésions hépatiques.
Inhibition de l'anticholinestérase. La plupart des pesticides organophosphorés, par exemple, ont peu de toxicité pour les mammifères jusqu'à ce qu'ils soient activés métaboliquement, principalement dans le foie. Le principal mécanisme d'action des organophosphorés est l'inhibition de l'acétylcholinestérase (AChE) dans le cerveau et le système nerveux périphérique. L'AChE est l'enzyme normale qui termine la stimulation du neurotransmetteur acétylcholine. Une légère inhibition de l'AChE sur une période prolongée n'a pas été associée à des effets indésirables. À des niveaux d'exposition élevés, l'incapacité à mettre fin à cette stimulation neuronale entraîne une surstimulation du système nerveux cholinergique. La surstimulation cholinergique entraîne finalement une foule de symptômes, y compris un arrêt respiratoire, suivi de la mort si elle n'est pas traitée. Le traitement principal est l'administration d'atropine, qui bloque les effets de l'acétylcholine, et l'administration de chlorure de pralidoxime, qui réactive l'AChE inhibée. Par conséquent, la cause et le traitement de la toxicité des organophosphates sont abordés en comprenant la base biochimique de la toxicité.
Activation métabolique. De nombreux produits chimiques, y compris le tétrachlorure de carbone, le chloroforme, l'acétylaminofluorène, les nitrosamines et le paraquat sont métaboliquement activés en radicaux libres ou autres intermédiaires réactifs qui inhibent et interfèrent avec la fonction cellulaire normale. À des niveaux d'exposition élevés, cela entraîne la mort cellulaire (voir « Lésion cellulaire et mort cellulaire »). Alors que les interactions spécifiques et les cibles cellulaires restent inconnues, les systèmes d'organes qui ont la capacité d'activer ces produits chimiques, comme le foie, les reins et les poumons, sont tous des cibles potentielles de blessures. En effet, des cellules particulières au sein d'un organe ont une capacité plus ou moins grande à activer ou détoxifier ces intermédiaires, et cette capacité détermine la susceptibilité intracellulaire au sein d'un organe. Le métabolisme est l'une des raisons pour lesquelles une compréhension de la pharmacocinétique, qui décrit ces types de transformations ainsi que la distribution et l'élimination de ces intermédiaires, est importante pour reconnaître le mécanisme d'action de ces produits chimiques.
Mécanismes du cancer. Le cancer est une multiplicité de maladies, et bien que la compréhension de certains types de cancer s'améliore rapidement grâce aux nombreuses techniques de biologie moléculaire qui ont été développées depuis 1980, il reste encore beaucoup à apprendre. Cependant, il est clair que le développement du cancer est un processus en plusieurs étapes et que les gènes critiques sont essentiels à différents types de cancer. Des altérations de l'ADN (mutations somatiques) d'un certain nombre de ces gènes critiques peuvent entraîner une susceptibilité accrue ou des lésions cancéreuses (voir « Toxicologie génétique »). L'exposition à des produits chimiques naturels (dans les aliments cuits comme le bœuf et le poisson) ou à des produits chimiques synthétiques (comme la benzidine, utilisée comme colorant) ou à des agents physiques (lumière ultraviolette du soleil, radon du sol, rayonnement gamma provenant de procédures médicales ou d'activités industrielles) sont tous contributeurs aux mutations génétiques somatiques. Cependant, il existe des substances naturelles et synthétiques (comme les antioxydants) et des processus de réparation de l'ADN qui protègent et maintiennent l'homéostasie. Il est clair que la génétique est un facteur important dans le cancer, puisque les syndromes de maladies génétiques telles que le xeroderma pigmentosum, où il y a un manque de réparation normale de l'ADN, augmentent considérablement la susceptibilité au cancer de la peau due à l'exposition à la lumière ultraviolette du soleil.
Mécanismes de reproduction. Comme dans le cas du cancer, de nombreux mécanismes de toxicité pour la reproduction et/ou le développement sont connus, mais il reste encore beaucoup à apprendre. On sait que certains virus (comme la rubéole), des infections bactériennes et des médicaments (comme la thalidomide et la vitamine A) nuiront au développement. Récemment, les travaux de Khera (1991), examinés par Carney (1994), montrent de bonnes preuves que les effets anormaux sur le développement dans les tests sur les animaux avec l'éthylène glycol sont attribuables aux métabolites acides métaboliques maternels. Cela se produit lorsque l'éthylène glycol est métabolisé en métabolites acides, notamment l'acide glycolique et l'acide oxalique. Les effets ultérieurs sur le placenta et le fœtus semblent être dus à ce processus de toxicité métabolique.
Conclusion
Le but de cet article est de donner une perspective sur plusieurs mécanismes connus de toxicité et la nécessité d'études futures. Il est important de comprendre que les connaissances mécanistes ne sont pas absolument nécessaires pour protéger la santé humaine ou environnementale. Cette connaissance améliorera la capacité du professionnel à mieux prévoir et gérer la toxicité. Les techniques réelles utilisées pour élucider un mécanisme particulier dépendent des connaissances collectives des scientifiques et de la pensée de ceux qui prennent les décisions concernant la santé humaine.