Les fonctions du système immunitaire sont de protéger le corps contre les agents infectieux envahisseurs et d'assurer une surveillance immunitaire contre les cellules tumorales qui apparaissent. Il possède une première ligne de défense non spécifique qui peut initier elle-même des réactions effectrices, et une branche spécifique acquise, dans laquelle les lymphocytes et les anticorps portent la spécificité de reconnaissance et de réactivité ultérieure vis-à-vis de l'antigène.
L'immunotoxicologie a été définie comme « la discipline concernée par l'étude des événements pouvant entraîner des effets indésirables du fait de l'interaction des xénobiotiques avec le système immunitaire. Ces événements indésirables peuvent résulter (1) d'un effet direct et/ou indirect du xénobiotique (et/ou de son produit de biotransformation) sur le système immunitaire, ou (2) d'une réponse immunologique de l'hôte au composé et/ou son ou ses métabolites, ou des antigènes hôtes modifiés par le composé ou ses métabolites » (Berlin et al. 1987).
Lorsque le système immunitaire agit comme une cible passive d'agressions chimiques, il peut en résulter une diminution de la résistance aux infections et à certaines formes de néoplasie, ou une dérégulation/stimulation immunitaire pouvant exacerber les allergies ou l'auto-immunité. Dans le cas où le système immunitaire répond à la spécificité antigénique du xénobiotique ou de l'antigène hôte modifié par le composé, la toxicité peut se manifester sous forme d'allergies ou de maladies auto-immunes.
Des modèles animaux pour étudier la suppression immunitaire induite par des produits chimiques ont été développés, et un certain nombre de ces méthodes sont validées (Burleson, Munson et Dean 1995 ; IPCS 1996). À des fins de test, une approche à plusieurs niveaux est suivie pour effectuer une sélection adéquate parmi le nombre écrasant de tests disponibles. Généralement, l'objectif du premier niveau est d'identifier les immunotoxiques potentiels. Si une immunotoxicité potentielle est identifiée, un deuxième niveau de test est effectué pour confirmer et caractériser davantage les changements observés. Les enquêtes de troisième niveau comprennent des études spéciales sur le mécanisme d'action du composé. Plusieurs xénobiotiques ont été identifiés comme immunotoxiques provoquant une immunosuppression dans de telles études avec des animaux de laboratoire.
La base de données sur les perturbations de la fonction immunitaire chez les humains par les produits chimiques environnementaux est limitée (Descotes 1986; NRC Subcommittee on Immunotoxicology 1992). L'utilisation de marqueurs d'immunotoxicité a reçu peu d'attention dans les études cliniques et épidémiologiques pour étudier l'effet de ces produits chimiques sur la santé humaine. De telles études n'ont pas été réalisées fréquemment et leur interprétation ne permet souvent pas de tirer des conclusions univoques, en raison par exemple du caractère non contrôlé de l'exposition. Par conséquent, à l'heure actuelle, l'évaluation de l'immunotoxicité chez les rongeurs, avec extrapolation ultérieure à l'homme, constitue la base des décisions concernant les dangers et les risques.
Les réactions d'hypersensibilité, notamment l'asthme allergique et la dermatite de contact, sont d'importants problèmes de santé au travail dans les pays industrialisés (Vos, Younes et Smith 1995). Le phénomène de sensibilisation par contact a d'abord été étudié chez le cobaye (Andersen et Maibach 1985). Jusqu'à récemment, c'était l'espèce de choix pour les tests prédictifs. De nombreuses méthodes de test de cobaye sont disponibles, les plus fréquemment utilisées étant le test de maximisation du cobaye et le patch test occlus de Buehler. Les tests sur le cobaye et les nouvelles approches développées chez la souris, telles que les tests de gonflement des oreilles et le test des ganglions lymphatiques locaux, fournissent au toxicologue les outils nécessaires pour évaluer le risque de sensibilisation cutanée. La situation en matière de sensibilisation des voies respiratoires est très différente. Il n'existe pas encore de méthodes bien validées ou largement acceptées pour l'identification des allergènes respiratoires chimiques, bien que des progrès dans le développement de modèles animaux pour l'étude de l'allergie respiratoire chimique aient été réalisés chez le cobaye et la souris.
Les données humaines montrent que les agents chimiques, en particulier les médicaments, peuvent provoquer des maladies auto-immunes (Kammüller, Bloksma et Seinen 1989). Il existe un certain nombre de modèles animaux expérimentaux de maladies auto-immunes humaines. Ceux-ci comprennent à la fois une pathologie spontanée (par exemple le lupus érythémateux disséminé chez des souris noires de Nouvelle-Zélande) et des phénomènes auto-immuns induits par une immunisation expérimentale avec un auto-antigène à réaction croisée (par exemple l'arthrite induite par l'adjuvant H37Ra chez des rats de souche Lewis). Ces modèles sont appliqués dans l'évaluation préclinique des médicaments immunosuppresseurs. Très peu d'études ont abordé le potentiel de ces modèles pour évaluer si un xénobiotique exacerbe l'auto-immunité induite ou congénitale. Les modèles animaux qui conviennent pour étudier la capacité des produits chimiques à induire des maladies auto-immunes font pratiquement défaut. Un modèle qui est utilisé dans une mesure limitée est le test des ganglions lymphatiques poplités chez la souris. À l'instar de la situation chez l'homme, les facteurs génétiques jouent un rôle crucial dans le développement de maladies auto-immunes (MA) chez les animaux de laboratoire, ce qui limitera la valeur prédictive de tels tests.
Le système immunitaire
La fonction principale du système immunitaire est la défense contre les bactéries, les virus, les parasites, les champignons et les cellules néoplasiques. Ceci est réalisé par les actions de divers types de cellules et de leurs médiateurs solubles dans un concert finement réglé. La défense de l'hôte peut être grossièrement divisée en résistance non spécifique ou innée et en immunité spécifique ou acquise médiée par les lymphocytes (Roitt, Brostoff et Male 1989).
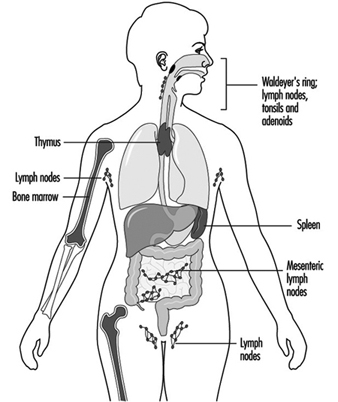
Les composants du système immunitaire sont présents dans tout le corps (Jones et al. 1990). Le compartiment lymphocytaire se trouve au sein des organes lymphoïdes (figure 1). La moelle osseuse et le thymus sont classés comme organes lymphoïdes primaires ou centraux ; les organes lymphoïdes secondaires ou périphériques comprennent les ganglions lymphatiques, la rate et le tissu lymphoïde le long des surfaces de sécrétion telles que les voies gastro-intestinales et respiratoires, le soi-disant tissu lymphoïde associé à la muqueuse (MALT). Environ la moitié des lymphocytes du corps se trouvent à tout moment dans le MALT. De plus, la peau est un organe important pour l'induction de réponses immunitaires aux antigènes présents sur la peau. Les cellules épidermiques de Langerhans qui ont une fonction de présentation d'antigène sont importantes dans ce processus.
Figure 1. Organes et tissus lymphoïdes primaires et secondaires
Les cellules phagocytaires de la lignée monocyte/macrophage, appelées système phagocytaire mononucléaire (MPS), sont présentes dans les organes lymphoïdes et également au niveau des sites extranodaux ; les phagocytes extranodaux comprennent les cellules de Kupffer dans le foie, les macrophages alvéolaires dans les poumons, les macrophages mésangiaux dans les reins et les cellules gliales dans le cerveau. Les leucocytes polymorphonucléaires (PMN) sont présents principalement dans le sang et la moelle osseuse, mais s'accumulent aux sites d'inflammation.
Défense non spécifique
Une première ligne de défense contre les micro-organismes est réalisée par une barrière physique et chimique, telle qu'au niveau de la peau, des voies respiratoires et du tube digestif. Cette barrière est aidée par des mécanismes de protection non spécifiques, notamment les cellules phagocytaires, telles que les macrophages et les leucocytes polymorphonucléaires, qui sont capables de tuer les agents pathogènes, et les cellules tueuses naturelles, qui peuvent lyser les cellules tumorales et les cellules infectées par des virus. Le système du complément et certains inhibiteurs microbiens (par exemple, le lysozyme) participent également à la réponse non spécifique.
Immunité spécifique
Après le contact initial de l'hôte avec l'agent pathogène, des réponses immunitaires spécifiques sont induites. La caractéristique de cette deuxième ligne de défense est la reconnaissance spécifique de déterminants, appelés antigènes ou épitopes, des agents pathogènes par des récepteurs à la surface cellulaire des lymphocytes B et T. Suite à l'interaction avec l'antigène spécifique, la cellule portant le récepteur est stimulée pour subir une prolifération et une différenciation, produisant un clone de cellules descendantes qui sont spécifiques de l'antigène déclenchant. Les réponses immunitaires spécifiques aident la défense non spécifique présentée aux agents pathogènes en stimulant l'efficacité des réponses non spécifiques. Une caractéristique fondamentale de l'immunité spécifique est que la mémoire se développe. Le contact secondaire avec le même antigène provoque une réponse plus rapide et plus vigoureuse mais bien régulée.
Le génome n'a pas la capacité de porter les codes d'un ensemble de récepteurs antigéniques suffisant pour reconnaître le nombre d'antigènes pouvant être rencontrés. Le répertoire de spécificité se développe par un processus de réarrangements de gènes. Il s'agit d'un processus aléatoire, au cours duquel différentes spécificités sont induites. Cela inclut des spécificités pour les composants autonomes, qui ne sont pas souhaitables. Un processus de sélection qui a lieu dans le thymus (cellules T), ou la moelle osseuse (cellules B) opère pour supprimer ces spécificités indésirables.
La fonction effectrice immunitaire normale et la régulation homéostatique de la réponse immunitaire dépendent d'une variété de produits solubles, connus collectivement sous le nom de cytokines, qui sont synthétisés et sécrétés par les lymphocytes et par d'autres types de cellules. Les cytokines ont des effets pléiotropes sur les réponses immunitaires et inflammatoires. La coopération entre différentes populations cellulaires est nécessaire pour la réponse immunitaire - la régulation des réponses d'anticorps, l'accumulation de cellules et de molécules immunitaires sur les sites inflammatoires, l'initiation de réponses de phase aiguë, le contrôle de la fonction cytotoxique des macrophages et de nombreux autres processus essentiels à la résistance de l'hôte . Celles-ci sont influencées par des cytokines agissant individuellement ou de concert, et dans de nombreux cas en dépendent.
Deux bras d'immunité spécifique sont reconnus - l'immunité humorale et l'immunité à médiation cellulaire ou cellulaire :
Immunité humorale. Dans le bras humoral, les lymphocytes B sont stimulés suite à la reconnaissance de l'antigène par les récepteurs de surface cellulaire. Les récepteurs antigéniques sur les lymphocytes B sont des immunoglobulines (Ig). Les lymphocytes B matures (cellules plasmatiques) déclenchent la production d'immunoglobulines spécifiques de l'antigène qui agissent comme des anticorps dans le sérum ou le long des surfaces muqueuses. Il existe cinq grandes classes d'immunoglobulines : (1) IgM, Ig pentamérique à capacité agglutinante optimale, qui est d'abord produite après stimulation antigénique ; (2) IgG, la principale Ig en circulation, qui peut passer le placenta ; (3) IgA, Ig sécrétoire pour la protection des surfaces muqueuses ; (4) IgE, Ig se fixant aux mastocytes ou aux granulocytes basophiles impliqués dans les réactions d'hypersensibilité immédiate et (5) IgD, dont la fonction principale est celle de récepteur sur les lymphocytes B.
Immunité à médiation cellulaire. Le bras cellulaire du système immunitaire spécifique est médié par les lymphocytes T. Ces cellules ont également des récepteurs antigéniques sur leurs membranes. Ils reconnaissent l'antigène s'il est présenté par des cellules présentatrices d'antigène dans le contexte des antigènes d'histocompatibilité. Par conséquent, ces cellules ont une restriction en plus de la spécificité antigénique. Les lymphocytes T fonctionnent comme des cellules auxiliaires pour diverses réponses immunitaires (y compris humorales), interviennent dans le recrutement de cellules inflammatoires et peuvent, en tant que lymphocytes T cytotoxiques, tuer les cellules cibles après la reconnaissance spécifique de l'antigène.
Mécanismes d'immunotoxicité
Immunosuppression
Une résistance efficace de l'hôte dépend de l'intégrité fonctionnelle du système immunitaire, qui à son tour exige que les cellules et molécules constitutives qui orchestrent les réponses immunitaires soient disponibles en nombre suffisant et sous une forme opérationnelle. Les immunodéficiences congénitales chez l'homme sont souvent caractérisées par des défauts dans certaines lignées de cellules souches, entraînant une production altérée ou absente de cellules immunitaires. Par analogie avec les maladies d'immunodéficience humaine congénitale et acquise, l'immunosuppression induite par des produits chimiques peut résulter simplement d'un nombre réduit de cellules fonctionnelles (IPCS 1996). L'absence ou le nombre réduit de lymphocytes peut avoir des effets plus ou moins profonds sur l'état immunitaire. Certains états d'immunodéficience et d'immunosuppression sévère, comme cela peut se produire lors d'une transplantation ou d'une thérapie cytostatique, ont été associés en particulier à des incidences accrues d'infections opportunistes et de certaines maladies néoplasiques. Les infections peuvent être bactériennes, virales, fongiques ou protozoaires, et le type prédominant d'infection dépend de l'immunodéficience associée. On peut s'attendre à ce que l'exposition à des produits chimiques environnementaux immunosuppresseurs entraîne des formes plus subtiles d'immunosuppression, qui peuvent être difficiles à détecter. Ceux-ci peuvent conduire, par exemple, à une incidence accrue d'infections telles que la grippe ou le rhume.
Compte tenu de la complexité du système immunitaire, avec la grande variété de cellules, de médiateurs et de fonctions qui forment un réseau compliqué et interactif, les composés immunotoxiques ont de nombreuses possibilités d'exercer un effet. Bien que la nature des lésions initiales induites par de nombreux produits chimiques immunotoxiques n'ait pas encore été élucidée, de plus en plus d'informations sont disponibles, principalement issues d'études sur des animaux de laboratoire, concernant les changements immunobiologiques qui entraînent une dépression de la fonction immunitaire (Dean et al. 1994) . Des effets toxiques peuvent se produire au niveau des fonctions critiques suivantes (et quelques exemples sont donnés de composés immunotoxiques affectant ces fonctions) :
- développement et expansion de différentes populations de cellules souches (le benzène exerce des effets immunotoxiques au niveau des cellules souches, provoquant une lymphocytopénie)
- prolifération de diverses cellules lymphoïdes et myéloïdes ainsi que des tissus de soutien dans lesquels ces cellules mûrissent et fonctionnent (les composés organostanniques immunotoxiques suppriment l'activité proliférative des lymphocytes dans le cortex thymique par cytotoxicité directe ; l'action thymotoxique du 2,3,7,8-tétrachloro -la dibenzo-p-dioxine (TCDD) et les composés apparentés sont probablement dus à une altération de la fonction des cellules épithéliales thymiques, plutôt qu'à une toxicité directe pour les thymocytes)
- l'absorption, le traitement et la présentation de l'antigène par les macrophages et d'autres cellules présentatrices d'antigène (l'une des cibles du 7,12-diméthylbenz(a)anthracène (DMBA) et du plomb est la présentation de l'antigène par les macrophages ; une cible du rayonnement ultraviolet est l'antigène- présentant la cellule de Langerhans)
- fonction régulatrice des cellules T-helper et T-suppressor (la fonction des cellules T-helper est altérée par les organostanniques, l'aldicarbe, les biphényles polychlorés (PCB), le TCDD et le DMBA ; la fonction des cellules T-suppressor est réduite par un traitement à faible dose de cyclophosphamide)
- production de diverses cytokines ou interleukines (le benzo(a)pyrène (BP) supprime la production d'interleukine-1 ; le rayonnement ultraviolet modifie la production de cytokines par les kératinocytes)
- la synthèse de diverses classes d'immunoglobulines IgM et IgG est supprimée après un traitement aux PCB et à l'oxyde de tributylétain (TBT) et augmentée après une exposition à l'hexachlorobenzène (HCB).
- régulation et activation du complément (affecté par TCDD)
- fonction des cellules T cytotoxiques (le 3-méthylcholanthrène (3-MC), le DMBA et le TCDD suppriment l'activité des cellules T cytotoxiques)
- fonction des cellules tueuses naturelles (NK) (l'activité NK pulmonaire est supprimée par l'ozone; l'activité NK splénique est altérée par le nickel)
- chimiotaxie des macrophages et des leucocytes polymorphonucléaires et fonctions cytotoxiques (l'ozone et le dioxyde d'azote altèrent l'activité phagocytaire des macrophages alvéolaires).
Allergie
Allergie peuvent être définis comme les effets néfastes sur la santé qui résultent de l'induction et du déclenchement de réponses immunitaires spécifiques. Lorsque des réactions d'hypersensibilité surviennent sans implication du système immunitaire, le terme pseudo-allergie est utilisé. Dans le contexte de l'immunotoxicologie, l'allergie résulte d'une réponse immunitaire spécifique aux produits chimiques et aux médicaments d'intérêt. La capacité d'un produit chimique à sensibiliser les individus est généralement liée à sa capacité à se lier de manière covalente aux protéines corporelles. Les réactions allergiques peuvent prendre diverses formes et celles-ci diffèrent en ce qui concerne à la fois les mécanismes immunologiques sous-jacents et la vitesse de la réaction. Quatre types principaux de réactions allergiques ont été reconnus : Réactions d'hypersensibilité de type I, qui sont provoquées par les anticorps IgE et où les symptômes se manifestent dans les minutes suivant l'exposition de l'individu sensibilisé. Les réactions d'hypersensibilité de type II résultent de l'endommagement ou de la destruction des cellules hôtes par les anticorps. Dans ce cas, les symptômes apparaissent en quelques heures. Les réactions d'hypersensibilité de type III, ou Arthus, sont également médiées par des anticorps, mais contre un antigène soluble, et résultent de l'action locale ou systémique de complexes immuns. Les réactions d'hypersensibilité de type IV, ou de type retardé, sont provoquées par les lymphocytes T et normalement les symptômes se développent 24 à 48 heures après l'exposition de l'individu sensibilisé.
Les deux types d'allergie chimique les plus pertinents pour la santé au travail sont la sensibilité de contact ou allergie cutanée et l'allergie des voies respiratoires.
Hypersensibilité de contact. Un grand nombre de produits chimiques sont capables de provoquer une sensibilisation cutanée. Suite à l'exposition topique d'un individu sensible à un allergène chimique, une réponse lymphocytaire T est induite dans les ganglions lymphatiques drainants. Dans la peau, l'allergène interagit directement ou indirectement avec les cellules épidermiques de Langerhans, qui transportent le produit chimique vers les ganglions lymphatiques et le présentent sous une forme immunogène aux lymphocytes T réactifs. Les lymphocytes T activés par les allergènes prolifèrent, entraînant une expansion clonale. L'individu est maintenant sensibilisé et répondra à une deuxième exposition cutanée au même produit chimique par une réponse immunitaire plus agressive, entraînant une dermatite de contact allergique. La réaction inflammatoire cutanée qui caractérise la dermatite allergique de contact est secondaire à la reconnaissance de l'allergène dans la peau par des lymphocytes T spécifiques. Ces lymphocytes s'activent, libèrent des cytokines et provoquent l'accumulation locale d'autres leucocytes mononucléaires. Les symptômes se développent environ 24 à 48 heures après l'exposition de l'individu sensibilisé, et la dermatite allergique de contact représente donc une forme d'hypersensibilité de type retardé. Les causes courantes de dermatite de contact allergique comprennent les produits chimiques organiques (tels que le 2,4-dinitrochlorobenzène), les métaux (tels que le nickel et le chrome) et les produits végétaux (tels que l'urushiol de l'herbe à puce).
Hypersensibilité respiratoire. L'hypersensibilité respiratoire est généralement considérée comme une réaction d'hypersensibilité de type I. Cependant, les réactions de phase tardive et les symptômes plus chroniques associés à l'asthme peuvent impliquer des processus immunitaires à médiation cellulaire (type IV). Les symptômes aigus associés à l'allergie respiratoire sont provoqués par des anticorps IgE dont la production est provoquée suite à l'exposition de l'individu sensible à l'allergène chimique inducteur. L'anticorps IgE se distribue de manière systémique et se lie, via des récepteurs membranaires, aux mastocytes qui se trouvent dans les tissus vascularisés, y compris les voies respiratoires. Suite à l'inhalation du même produit chimique, une réaction d'hypersensibilité respiratoire sera déclenchée. L'allergène s'associe aux protéines et se lie aux anticorps IgE liés aux mastocytes et les réticule. Cela provoque à son tour la dégranulation des mastocytes et la libération de médiateurs inflammatoires tels que l'histamine et les leucotriènes. De tels médiateurs provoquent une bronchoconstriction et une vasodilatation, entraînant des symptômes d'allergie respiratoire ; asthme et/ou rhinite. Les produits chimiques connus pour provoquer une hypersensibilité respiratoire chez l'homme comprennent les anhydrides acides (tels que l'anhydride trimellitique), certains diisocyanates (tels que le diisocyanate de toluène), les sels de platine et certains colorants réactifs. De plus, l'exposition chronique au béryllium est connue pour causer une maladie pulmonaire d'hypersensibilité.
auto-immunité
auto-immunité peut être défini comme la stimulation de réponses immunitaires spécifiques dirigées contre des antigènes endogènes du "soi". L'auto-immunité induite peut résulter soit d'altérations de l'équilibre des lymphocytes T régulateurs, soit de l'association d'un xénobiotique avec des composants tissulaires normaux de manière à les rendre immunogènes ("altéred self"). Les médicaments et les produits chimiques connus pour induire ou exacerber accidentellement des effets comme ceux de la maladie auto-immune (MA) chez les personnes sensibles sont des composés de faible poids moléculaire (poids moléculaire de 100 à 500) qui sont généralement considérés comme non immunogènes eux-mêmes. Le mécanisme de la MA par exposition chimique est pour la plupart inconnu. La maladie peut être produite directement au moyen d'anticorps circulants, indirectement par la formation de complexes immuns ou à la suite d'une immunité à médiation cellulaire, mais elle se produit probablement par une combinaison de mécanismes. La pathogénie est surtout connue dans les troubles hémolytiques immunitaires induits par les médicaments :
- Le médicament peut se fixer à la membrane des globules rouges et interagir avec un anticorps spécifique au médicament.
- Le médicament peut altérer la membrane des globules rouges de sorte que le système immunitaire considère la cellule comme étrangère.
- Le médicament et son anticorps spécifique forment des complexes immuns qui adhèrent à la membrane des globules rouges pour produire des lésions.
- La sensibilisation des globules rouges se produit en raison de la production d'auto-anticorps anti-globules rouges.
Une variété de produits chimiques et de médicaments, en particulier ces derniers, se sont avérés induire des réponses de type auto-immune (Kamüller, Bloksma et Seinen 1989). L'exposition professionnelle à des produits chimiques peut incidemment entraîner des syndromes de type MA. L'exposition au chlorure de vinyle monomère, au trichloroéthylène, au perchloroéthylène, aux résines époxy et à la poussière de silice peut induire des syndromes de type sclérodermique. Un syndrome similaire au lupus érythémateux disséminé (LED) a été décrit après exposition à l'hydrazine. L'exposition au diisocyanate de toluène a été associée à l'induction de purpura thrombocytopénique. Les métaux lourds tels que le mercure ont été impliqués dans certains cas de glomérulonéphrite à complexes immuns.
Évaluation des risques humains
L'évaluation de l'état immunitaire humain est effectuée principalement à l'aide de sang périphérique pour l'analyse de substances humorales telles que les immunoglobulines et le complément, et de leucocytes sanguins pour la composition de sous-ensembles et la fonctionnalité de sous-populations. Ces méthodes sont généralement les mêmes que celles utilisées pour étudier l'immunité humorale et à médiation cellulaire ainsi que la résistance non spécifique des patients suspectés d'immunodéficience congénitale. Pour les études épidémiologiques (par exemple, des populations professionnellement exposées), les paramètres doivent être sélectionnés sur la base de leur valeur prédictive dans les populations humaines, des modèles animaux validés et la biologie sous-jacente des marqueurs (voir tableau 1). La stratégie de dépistage des effets immunotoxiques après une exposition (accidentelle) à des polluants environnementaux ou à d'autres substances toxiques dépend beaucoup des circonstances, telles que le type d'immunodéficience à prévoir, le temps écoulé entre l'exposition et l'évaluation de l'état immunitaire, le degré d'exposition et le nombre d'individus exposés. Le processus d'évaluation du risque immunotoxique d'un xénobiotique particulier chez l'homme est extrêmement difficile et souvent impossible, en grande partie en raison de la présence de divers facteurs de confusion d'origine endogène ou exogène qui influencent la réponse des individus aux dommages toxiques. Cela est particulièrement vrai pour les études qui étudient le rôle de l'exposition chimique dans les maladies auto-immunes, où les facteurs génétiques jouent un rôle crucial.
Tableau 1. Classification des tests pour les marqueurs immunitaires
| Catégorie d'essai | Caractéristiques | Tests spécifiques |
| Général de base Doit être inclus avec les panneaux généraux |
Indicateurs de la santé générale et de l'état du système organique | Azote uréique sanguin, glycémie, etc. |
| Immunité basique Doit être inclus avec les panneaux généraux |
Indicateurs généraux de l'état immunitaire Coût relativement bas Les méthodes d'analyse sont standardisées entre les laboratoires Les résultats en dehors des plages de référence sont cliniquement interprétables |
Numérations sanguines complètes Taux sériques d'IgG, IgA, IgM Phénotypes de marqueurs de surface pour les principaux sous-ensembles de lymphocytes |
| Concentré/réflexe Doit être inclus lorsque cela est indiqué par des résultats cliniques, des expositions suspectées ou des résultats de tests antérieurs |
Indicateurs de fonctions/événements immunitaires spécifiques Le coût varie Les méthodes d'analyse sont standardisées entre les laboratoires Les résultats en dehors des plages de référence sont cliniquement interprétables |
Génotype d'histocompatibilité Anticorps contre les agents infectieux IgE sériques totales IgE spécifique de l'allergène Auto-anticorps Tests cutanés pour l'hypersensibilité Sursaut oxydatif des granulocytes Histopathologie (biopsie tissulaire) |
| Recherche Doit être inclus uniquement avec des populations témoins et une conception d'étude minutieuse |
Indicateurs de fonctions/événements immunitaires généraux ou spécifiques Le coût varie; souvent cher Les méthodes d'analyse ne sont généralement pas standardisées entre les laboratoires Les résultats en dehors des plages de référence ne sont souvent pas interprétables cliniquement |
Essais de stimulation in vitro Marqueurs de surface d'activation cellulaire Concentrations sériques de cytokines Essais de clonalité (anticorps, cellulaire, génétique) Tests de cytotoxicité |
Comme des données humaines adéquates sont rarement disponibles, l'évaluation du risque d'immunosuppression induite par des produits chimiques chez l'homme est dans la majorité des cas basée sur des études animales. L'identification des xénobiotiques immunotoxiques potentiels est entreprise principalement dans des études contrôlées chez les rongeurs. Les études d'exposition in vivo présentent, à cet égard, l'approche optimale pour estimer le potentiel immunotoxique d'un composé. Cela est dû à la nature multifactorielle et complexe du système immunitaire et des réponses immunitaires. Les études in vitro sont de plus en plus utiles pour élucider les mécanismes de l'immunotoxicité. De plus, en étudiant les effets du composé à l'aide de cellules d'origine animale et humaine, des données peuvent être générées pour la comparaison des espèces, qui peuvent être utilisées dans l'approche «parallélogramme» pour améliorer le processus d'évaluation des risques. Si des données sont disponibles pour les trois pierres angulaires du parallélogramme (animal in vivo, et animal in vitro et humain), il peut être plus facile de prédire le résultat à la pierre angulaire restante, c'est-à-dire le risque chez l'homme.
Lorsque l'évaluation du risque d'immunosuppression induite par des produits chimiques doit reposer uniquement sur des données provenant d'études animales, une approche peut être suivie dans l'extrapolation à l'homme en appliquant des facteurs d'incertitude à la dose sans effet nocif observé (NOAEL). Ce niveau peut être basé sur des paramètres déterminés dans des modèles pertinents, tels que des tests de résistance de l'hôte et une évaluation in vivo des réactions d'hypersensibilité et de la production d'anticorps. Idéalement, la pertinence de cette approche pour l'évaluation des risques nécessite une confirmation par des études chez l'homme. Ces études devraient combiner l'identification et la mesure de la substance toxique, les données épidémiologiques et les évaluations de l'état immunitaire.
Pour prédire l'hypersensibilité de contact, des modèles de cobayes sont disponibles et sont utilisés dans l'évaluation des risques depuis les années 1970. Bien que sensibles et reproductibles, ces tests ont des limites car ils dépendent d'une évaluation subjective ; cela peut être surmonté par des méthodes plus récentes et plus quantitatives développées chez la souris. Concernant l'hypersensibilité chimique induite par l'inhalation ou l'ingestion d'allergènes, des tests doivent être développés et évalués quant à leur valeur prédictive chez l'homme. Lorsqu'il s'agit de fixer des niveaux d'exposition professionnelle sûrs aux allergènes potentiels, il faut tenir compte de la nature biphasique de l'allergie : la phase de sensibilisation et la phase de déclenchement. La concentration requise pour déclencher une réaction allergique chez un individu précédemment sensibilisé est considérablement inférieure à la concentration nécessaire pour induire une sensibilisation chez l'individu immunologiquement naïf mais sensible.
Comme les modèles animaux pour prédire l'auto-immunité induite par des produits chimiques font pratiquement défaut, l'accent devrait être mis sur le développement de tels modèles. Pour le développement de tels modèles, nos connaissances sur l'auto-immunité induite par des produits chimiques chez l'homme doivent être avancées, y compris l'étude des marqueurs génétiques et du système immunitaire pour identifier les individus sensibles. Les humains qui sont exposés à des médicaments qui induisent l'auto-immunité offrent une telle opportunité.