La chimie et la physique du feu
Le feu est une manifestation de combustion incontrôlée. Il s'agit de matériaux combustibles que l'on trouve autour de nous dans les bâtiments dans lesquels nous vivons, travaillons et nous divertissons, ainsi que d'une large gamme de gaz, de liquides et de solides que l'on rencontre dans l'industrie et le commerce. Ils sont généralement à base de carbone et peuvent être appelés collectivement carburants dans le cadre de cette discussion. Malgré la grande variété de ces combustibles dans leurs états chimiques et physiques, ils partagent en cas d'incendie des caractéristiques qui leur sont communes. On rencontre des différences dans la facilité avec laquelle le feu peut être déclenché (allumage), la vitesse à laquelle le feu peut se développer (propagation de la flamme), et la puissance qui peut être générée (taux de dégagement de chaleur), mais à mesure que notre compréhension de la science du feu s'améliore, nous devenons mieux à même de quantifier et de prédire le comportement du feu et d'appliquer nos connaissances à la sécurité incendie en général. Le but de cette section est d'examiner certains des principes sous-jacents et de fournir des conseils pour comprendre les processus d'incendie.
Concepts de base
Les matériaux combustibles sont partout autour de nous. Dans les circonstances appropriées, on peut les faire brûler en les soumettant à une source d'allumage capable de déclencher une réaction auto-entretenue. Dans ce processus, le « carburant » réagit avec l'oxygène de l'air pour libérer de l'énergie (chaleur), tout en étant converti en produits de combustion, dont certains peuvent être nocifs. Les mécanismes d'inflammation et de combustion doivent être clairement compris.
La plupart des incendies quotidiens impliquent des matériaux solides (par exemple, le bois, les produits du bois et les polymères synthétiques), bien que les combustibles gazeux et liquides ne soient pas rares. Un bref examen de la combustion des gaz et des liquides est souhaitable avant de discuter de certains des concepts de base.
Flammes diffusion et prémélange
Un gaz inflammable (p. ex. propane, C3H8) peut être brûlé de deux manières : un flux ou un jet de gaz provenant d'un tuyau (cf. le bec Bunsen simple avec l'entrée d'air fermée) peut être allumé et brûlera comme un flamme de diffusion dans lequel la combustion se produit dans les régions où le combustible gazeux et l'air se mélangent par des processus de diffusion. Une telle flamme a une luminosité jaune caractéristique, indiquant la présence de minuscules particules de suie formées à la suite d'une combustion incomplète. Certains d'entre eux brûleront dans la flamme, mais d'autres émergeront de la pointe de la flamme pour former fumée.
Si le gaz et l'air sont intimement mélangés avant l'allumage, alors une combustion prémélangée se produira, à condition que le mélange gaz/air se situe dans une plage de concentrations délimitée par les valeurs inférieure et supérieure. limites d'inflammabilité (voir tableau 1). En dehors de ces limites, le mélange est ininflammable. (Notez qu'un flamme prémélangée est stabilisé à l'embouchure d'un bec Bunsen lorsque l'entrée d'air est ouverte.) Si un mélange est inflammable, il peut être enflammé par une petite source d'inflammation, telle qu'une étincelle électrique. Le stoechiométrique le mélange est le plus facilement enflammé, dans lequel la quantité d'oxygène présente est dans la bonne proportion pour brûler tout le carburant en dioxyde de carbone et en eau (voir l'équation ci-dessous, dans laquelle l'azote peut être vu comme étant présent dans la même proportion que dans l'air mais ne participe pas à la réaction). Propane (C3H8) est le matériau combustible dans cette réaction :
C3H8 + 5O2 + 18.8N2 = 3CO2 + 4H2O + 18.8N2
Une décharge électrique aussi petite que 0.3 mJ est suffisante pour enflammer un mélange stoechiométrique propane/air dans la réaction illustrée. Cela représente une étincelle statique à peine perceptible, telle que vécue par quelqu'un qui a marché sur un tapis synthétique et touché un objet mis à la terre. Des quantités d'énergie encore plus faibles sont nécessaires pour certains gaz réactifs tels que l'hydrogène, l'éthylène et l'éthyne. Dans l'oxygène pur (comme dans la réaction ci-dessus, mais sans azote présent comme diluant), des énergies encore plus faibles sont suffisantes.
Tableau 1. Limites inférieure et supérieure d'inflammabilité dans l'air
|
Faible inflammabilité |
Inflammabilité supérieure |
|
|
Monoxyde de carbone |
12.5 |
74 |
|
Méthane |
5.0 |
15 |
|
Propane |
2.1 |
9.5 |
|
n-Hexane |
1.2 |
7.4 |
|
n-Décane |
0.75 |
5.6 |
|
Méthanol |
6.7 |
36 |
|
Ethanol |
3.3 |
19 |
|
Acétone |
2.6 |
13 |
|
Benzène |
1.3 |
7.9 |
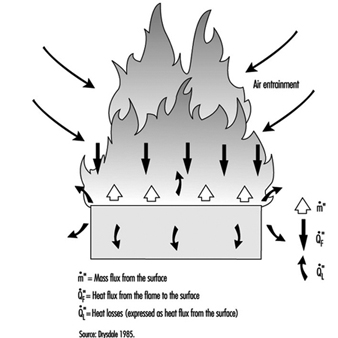
La flamme de diffusion associée à un flux de combustible gazeux illustre le mode de combustion observé lorsqu'un combustible liquide ou solide subit une combustion flamboyante. Cependant, dans ce cas, la flamme est alimentée par des vapeurs de combustible générées à la surface de la phase condensée. La vitesse d'apport de ces vapeurs est couplée à leur vitesse de combustion dans la flamme de diffusion. L'énergie est transférée de la flamme à la surface, fournissant ainsi l'énergie nécessaire pour produire les vapeurs. Il s'agit d'un processus d'évaporation simple pour les combustibles liquides, mais pour les solides, suffisamment d'énergie doit être fournie pour provoquer la décomposition chimique du combustible, brisant les grosses molécules polymères en fragments plus petits qui peuvent se vaporiser et s'échapper de la surface. Ce retour thermique est essentiel pour maintenir le flux de vapeurs, et donc soutenir la flamme de diffusion (figure 1). Les flammes peuvent être éteintes en interférant avec ce processus de plusieurs façons (voir ci-dessous).
Figure 1. Représentation schématique d'une surface brûlante montrant les processus de transfert de chaleur et de masse.
Le transfert de chaleur
Une compréhension du transfert de chaleur (ou d'énergie) est la clé pour comprendre le comportement et les processus du feu. Le sujet mérite une étude approfondie. Il y a beaucoup d'excellents textes vers lesquels on peut se tourner (Welty, Wilson et Wicks 1976 ; DiNenno 1988), mais pour les besoins actuels, il suffit d'attirer l'attention sur les trois mécanismes : conduction, convection et rayonnement. Les équations de base pour le transfert de chaleur en régime permanent () sont :
Conduction: ![]()
Convection: ![]()
Radiation: ![]()
La conduction est pertinente pour le transfert de chaleur à travers les solides; (k est une propriété matérielle connue sous le nom de conductivité thermique (kW/mK) et l est la distance (m) sur laquelle la température chute de T1 à T2 (en degrés Kelvin). La convection dans ce contexte fait référence au transfert de chaleur d'un fluide (dans ce cas, l'air, les flammes ou les produits du feu) à une surface (solide ou liquide); h est le coefficient de transfert de chaleur par convection kW/m2K) et dépend de la configuration de la surface et de la nature de l'écoulement du fluide devant cette surface. Le rayonnement est similaire à la lumière visible (mais avec une longueur d'onde plus longue) et ne nécessite aucun milieu intermédiaire (il peut traverser un vide); e est l'émissivité (efficacité avec laquelle une surface peut rayonner), s est la constante de Stefan-Boltzman (). Le rayonnement thermique se propage à la vitesse de la lumière (3 x 108 m/s) et un objet solide intermédiaire projettera une ombre.
Taux de combustion et taux de dégagement de chaleur
Le transfert de chaleur des flammes à la surface des combustibles condensés (liquides et solides) implique un mélange de convection et de rayonnement, bien que ce dernier domine lorsque le diamètre effectif du feu dépasse 1 m. La vitesse de combustion (, (g/s)) peut être exprimée par la formule :
![]()
![]() est le flux de chaleur de la flamme à la surface (kW/m2);
est le flux de chaleur de la flamme à la surface (kW/m2); ![]() est la perte de chaleur de la surface (par exemple, par rayonnement et par conduction à travers le solide) exprimée en flux (kW/m2); Acarburant est la surface du combustible (m2); et Lv est la chaleur de gazéification (équivalente à la chaleur latente d'évaporation d'un liquide) (kJ/g). Si un incendie se développe dans un espace confiné, les gaz fumigènes chauds s'élevant du feu (poussés par la flottabilité) sont déviés sous le plafond, chauffant les surfaces supérieures. La couche de fumée qui en résulte et les surfaces chaudes rayonnent vers la partie inférieure de l'enceinte, notamment vers la surface du combustible, augmentant ainsi la vitesse de combustion :
est la perte de chaleur de la surface (par exemple, par rayonnement et par conduction à travers le solide) exprimée en flux (kW/m2); Acarburant est la surface du combustible (m2); et Lv est la chaleur de gazéification (équivalente à la chaleur latente d'évaporation d'un liquide) (kJ/g). Si un incendie se développe dans un espace confiné, les gaz fumigènes chauds s'élevant du feu (poussés par la flottabilité) sont déviés sous le plafond, chauffant les surfaces supérieures. La couche de fumée qui en résulte et les surfaces chaudes rayonnent vers la partie inférieure de l'enceinte, notamment vers la surface du combustible, augmentant ainsi la vitesse de combustion :
![]()
De ![]() est la chaleur supplémentaire apportée par le rayonnement de la partie supérieure de l'enveloppe (kW/m2). Cette rétroaction supplémentaire conduit à des taux de combustion considérablement accrus et au phénomène de flashover dans les espaces clos où il y a un apport d'air adéquat et suffisamment de combustible pour entretenir le feu (Drysdale 1985).
est la chaleur supplémentaire apportée par le rayonnement de la partie supérieure de l'enveloppe (kW/m2). Cette rétroaction supplémentaire conduit à des taux de combustion considérablement accrus et au phénomène de flashover dans les espaces clos où il y a un apport d'air adéquat et suffisamment de combustible pour entretenir le feu (Drysdale 1985).
Le taux de combustion est modéré par l'ampleur de la valeur de Lv, la chaleur de gazéification. Celle-ci a tendance à être faible pour les liquides et relativement élevée pour les solides. Par conséquent, les solides ont tendance à brûler beaucoup plus lentement que les liquides.
Il a été avancé que le paramètre le plus important qui détermine le comportement au feu d'un matériau (ou d'un assemblage de matériaux) est le taux de dégagement de chaleur (RHR) qui est couplé au taux de combustion à travers l'équation :
![]()
où est la chaleur effective de combustion du carburant (kJ/g). De nouvelles techniques sont maintenant disponibles pour mesurer le RHR à différents flux de chaleur (par exemple, le calorimètre à cône), et il est désormais possible de mesurer le RHR de gros articles, tels que les meubles rembourrés et les revêtements muraux dans des calorimètres à grande échelle qui utilisent la consommation d'oxygène. mesures pour déterminer le taux de dégagement de chaleur (Babrauskas et Grayson 1992).
Il convient de noter qu'à mesure qu'un feu grandit, non seulement le taux de dégagement de chaleur augmente, mais le taux de production de «produits du feu» augmente également. Ceux-ci contiennent des espèces toxiques et nocives ainsi que des fumées particulaires dont les rendements augmenteront lorsqu'un incendie se développant dans l'enceinte d'un bâtiment devient sous-ventilé.
Allumage
L'allumage d'un liquide ou d'un solide implique l'élévation de la température de surface jusqu'à ce que des vapeurs se dégagent à une vitesse suffisante pour entretenir une flamme après que les vapeurs ont été allumées. Les combustibles liquides peuvent être classés selon leur points d'éclair, la température la plus basse à laquelle il existe un mélange vapeur/air inflammable à la surface (c'est-à-dire que la pression de vapeur correspond à la limite inférieure d'inflammabilité). Celles-ci peuvent être mesurées à l'aide d'un appareil standard, et des exemples typiques sont donnés dans le tableau 2. Une température légèrement plus élevée est nécessaire pour produire un flux de vapeurs suffisant pour supporter une flamme de diffusion. Ceci est connu comme le point de feu. Pour les solides combustibles, les mêmes concepts sont valables, mais des températures plus élevées sont nécessaires car une décomposition chimique est impliquée. Le point de feu est généralement supérieur à 300 ° C, selon le combustible. En général, les matériaux ignifuges ont des points de feu significativement plus élevés (voir tableau 2).
Tableau 2. Points d'éclair et points de feu des combustibles liquides et solides
|
Point éclair en vase clos1 (° C) |
Point de feu2 (° C) |
|
|
Essence (octane 100) (l) |
-38 |
- |
|
n-Décane (l) |
46 |
61.5 |
|
n-Dodécane (l) |
74 |
103 |
|
Polyméthylméthacrylate(s) |
- |
310 |
|
FR polyméthylméthacrylate(s) |
- |
377 |
|
Polypropylène(s) |
- |
330 |
|
Polypropylène(s) FR |
- |
397 |
|
Polystyrène(s) |
- |
367 |
|
polystyrène(s) FR |
- |
445 |
l = liquide ; s = solide.
1 Par Pensky-Martens appareil à coupelle fermée.
2 Liquides : par un appareil à vase ouvert de Cleveland. Solides : Drysdale et Thomson (1994).
(Notez que les résultats pour les espèces ignifuges se réfèrent à un flux de chaleur de 37 kW/m2).
La facilité d'inflammation d'un matériau solide dépend donc de la facilité avec laquelle sa température de surface peut être élevée jusqu'au point de feu, par exemple par exposition à une chaleur rayonnante ou à un flux de gaz chauds. Cela dépend moins de la chimie du processus de décomposition que de l'épaisseur et des propriétés physiques du solide, à savoir sa conductivité thermique (k), densité (r) et capacité thermique (c). Les solides minces, tels que les copeaux de bois (et toutes les sections minces), peuvent être enflammés très facilement car ils ont une faible masse thermique, c'est-à-dire qu'il faut relativement peu de chaleur pour élever la température au point de feu. Cependant, lorsque la chaleur est transférée à la surface d'un solide épais, une partie sera conduite de la surface dans le corps du solide, modérant ainsi l'élévation de température de la surface. On peut montrer théoriquement que le taux d'augmentation de la température de surface est déterminé par la inertie thermique du matériau, c'est-à-dire du produit krc. Cela se vérifie dans la pratique, puisque des matériaux épais à forte inertie thermique (ex. chêne, polyuréthane massif) mettront longtemps à s'enflammer sous un flux de chaleur donné, alors que dans des conditions identiques des matériaux épais à faible inertie thermique (ex. panneaux isolants en fibres, mousse de polyuréthane) s'enflammeront rapidement (Drysdale 1985).
Sources d'allumage
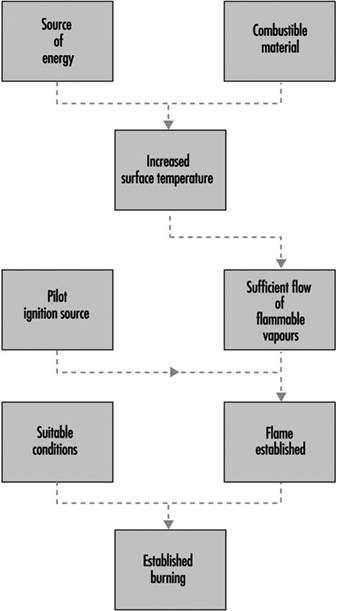
L'allumage est illustré schématiquement à la figure 2 (allumage piloté). Pour un allumage réussi, un source d'allumage doit être capable non seulement d'élever la température de surface jusqu'au point de feu ou au-dessus, mais aussi de provoquer l'inflammation des vapeurs. Une flamme incidente agira dans les deux cas, mais un flux radiatif imposé provenant d'une source éloignée peut entraîner le dégagement de vapeurs à une température supérieure au point de feu, sans que les vapeurs ne s'enflamment. Cependant, si les vapeurs dégagées sont suffisamment chaudes (ce qui nécessite que la température de surface soit bien supérieure au point de feu), elles peuvent s'enflammer spontanément en se mélangeant à l'air. Ce processus est connu sous le nom de inflammation spontanée.
Figure 2. Scénario d'allumage piloté.
Un grand nombre de sources d'inflammation peuvent être identifiées, mais elles ont une chose en commun, c'est qu'elles sont le résultat d'une certaine forme de négligence ou d'inaction. Une liste typique inclurait les flammes nues, les "matériels pour fumeurs", le chauffage par friction, les appareils électriques (chauffages, fers à repasser, cuisinières, etc.) et ainsi de suite. Une excellente enquête peut être trouvée dans Cote (1991). Certains d'entre eux sont résumés dans le tableau 3.
Tableau 3. Sources d'inflammation
|
|
Exemples
|
|
Matériel électrique |
Radiateurs électriques, sèche-cheveux, couvertures électriques, etc. |
|
Source de flamme nue |
Allumette, allume-cigare, chalumeau, etc. |
|
Équipement au gaz |
Foyer au gaz, radiateur, cuisinière, etc. |
|
Autres équipements alimentés |
Poêle à bois, etc. |
|
Produit du tabac allumé |
Cigare, pipe, etc. |
|
Objet chaud |
Tuyaux chauds, étincelles mécaniques, etc. |
|
Exposition au chauffage |
Feu adjacent, etc. |
|
Chauffage spontané |
Chiffons imbibés d'huile de lin, tas de charbon, etc. |
|
Réaction chimique |
Rare-par exemple, permanganate de potassium avec glycérol |
Il convient de noter que les cigarettes qui couvent ne peuvent pas déclencher directement une combustion enflammée (même dans les combustibles gazeux courants), mais peuvent provoquer fumant dans les matériaux qui ont tendance à subir ce type de combustion. Ceci n'est observé qu'avec des matériaux qui se carbonisent en chauffant. La combustion lente implique l'oxydation de la surface du charbon, qui génère suffisamment de chaleur localement pour produire du charbon frais à partir du combustible non brûlé adjacent. C'est un processus très lent, mais qui peut éventuellement subir une transition vers le flambage. Par la suite, le feu se développera très rapidement.
Les matériaux qui ont tendance à brûler peuvent également présenter le phénomène d'auto-échauffement (Bowes 1984). Cela se produit lorsqu'un tel matériau est stocké en grande quantité et de telle sorte que la chaleur générée par l'oxydation lente de surface ne puisse s'échapper, entraînant une élévation de température au sein de la masse. Si les conditions sont réunies, cela peut conduire à un processus d'emballement se transformant finalement en une réaction de combustion lente en profondeur dans le matériau.
Propagation de la flamme
Un élément majeur dans la croissance de tout incendie est la vitesse à laquelle la flamme se propagera sur les surfaces combustibles adjacentes. La propagation de la flamme peut être modélisée comme un front d'allumage avancé dans lequel le bord d'attaque de la flamme agit comme une source d'allumage pour le combustible qui ne brûle pas encore. Le taux de propagation est déterminé en partie par les mêmes propriétés matérielles qui contrôlent la facilité d'allumage et en partie par l'interaction entre la flamme existante et la surface devant le front. La propagation verticale vers le haut est la plus rapide car la flottabilité garantit que les flammes s'écoulent vers le haut, exposant la surface au-dessus de la zone de combustion au transfert de chaleur direct des flammes. Cela doit être opposé à la propagation sur une surface horizontale lorsque les flammes de la zone de combustion s'élèvent verticalement, loin de la surface. En effet, il est d'expérience courante que la propagation verticale est la plus dangereuse (par exemple, la propagation des flammes sur les rideaux et les tentures et sur les vêtements amples tels que les robes et les chemises de nuit).
La vitesse de propagation est également affectée par un flux de chaleur rayonnante imposé. Lors du développement d'un incendie dans une pièce, la zone de l'incendie augmentera plus rapidement sous l'augmentation du niveau de rayonnement qui s'accumule au fur et à mesure que l'incendie progresse. Cela contribuera à l'accélération de la croissance du feu qui est caractéristique du flashover.
Théorie de l'extinction des incendies
L'extinction et la suppression des incendies peuvent être examinées en fonction de l'aperçu ci-dessus de la théorie des incendies. Les processus de combustion en phase gazeuse (c'est-à-dire les réactions à la flamme) sont très sensibles aux inhibiteurs chimiques. Certains ignifuges utilisés pour améliorer les « propriétés au feu » des matériaux reposent sur le fait que de petites quantités d'inhibiteur libérées avec les vapeurs de carburant supprimeront l'établissement de la flamme. La présence d'un retardateur de flamme ne peut pas rendre un matériau combustible incombustible, mais elle peut rendre l'allumage plus difficile, empêchant peut-être complètement l'allumage à condition que la source d'allumage soit petite. Cependant, si un matériau ignifuge est impliqué dans un incendie existant, il brûlera car les flux de chaleur élevés submergent l'effet du retardateur.
L'extinction d'un incendie peut se faire de plusieurs manières :
1. arrêt de l'alimentation en vapeurs de carburant
2. extinction de la flamme par des extincteurs chimiques (inhibiteur)
3. supprimer l'apport d'air (oxygène) au feu (étouffement)
4. « éruption ».
Contrôler le flux de vapeurs de carburant
La première méthode, l'arrêt de l'alimentation en vapeurs de combustible, est clairement applicable à un feu à jet de gaz dans lequel l'alimentation en combustible peut simplement être coupée. Cependant, c'est aussi la méthode la plus courante et la plus sûre pour éteindre un incendie impliquant des combustibles condensés. Dans le cas d'un incendie impliquant un solide, cela nécessite que la surface du combustible soit refroidie en dessous du point de feu, lorsque le flux de vapeurs devient trop faible pour supporter une flamme. Ceci est réalisé le plus efficacement par l'application d'eau, soit manuellement, soit au moyen d'un système automatique (asperseurs, pulvérisation d'eau, etc.). En général, les feux de liquide ne peuvent pas être traités de cette manière : les combustibles liquides à bas point de feu ne peuvent tout simplement pas être suffisamment refroidis, alors que dans le cas d'un combustible à haut point de feu, une vaporisation vigoureuse de l'eau lorsqu'elle entre en contact avec le liquide chaud au surface peut entraîner l'éjection de carburant brûlant hors du conteneur. Cela peut avoir des conséquences très graves pour ceux qui luttent contre l'incendie. (Il existe des cas particuliers dans lesquels un système automatique de pulvérisation d'eau à haute pression peut être conçu pour faire face à ce dernier type d'incendie, mais ce n'est pas courant.)
Les incendies de liquide sont couramment éteints à l'aide de mousses extinctrices (Cote 1991). Ceci est produit en aspirant un concentré de mousse dans un courant d'eau qui est ensuite dirigé vers le feu à travers une buse spéciale qui permet à l'air d'être entraîné dans le flux. Cela produit une mousse qui flotte au-dessus du liquide, réduisant le débit d'alimentation en vapeurs de carburant par un effet de blocage et en protégeant la surface du transfert de chaleur des flammes. La mousse doit être appliquée avec précaution pour former un « radeau » qui grossit progressivement pour recouvrir la surface du liquide. Les flammes diminueront de taille au fur et à mesure que le radeau grandira, et en même temps la mousse se décomposera progressivement, libérant de l'eau qui favorisera le refroidissement de la surface. Le mécanisme est en fait complexe, même si le résultat net est de contrôler le flux de vapeurs.
Il existe plusieurs émulseurs disponibles, il est important d'en choisir un compatible avec les liquides à protéger. Les « mousses protéiques » originales ont été développées pour les feux d'hydrocarbures liquides, mais se décomposent rapidement si elles sont mises en contact avec des combustibles liquides solubles dans l'eau. Une gamme de « mousses synthétiques » a été développée pour faire face à l'ensemble des feux liquides pouvant être rencontrés. L'une d'elles, la mousse filmogène aqueuse (AFFF), est une mousse tout usage qui produit également un film d'eau à la surface du combustible liquide, augmentant ainsi son efficacité.
Éteindre la flamme
Cette méthode utilise des suppresseurs chimiques pour éteindre la flamme. Les réactions qui se produisent dans la flamme impliquent des radicaux libres, une espèce hautement réactive qui n'a qu'une existence éphémère mais qui est continuellement régénérée par un processus à chaîne ramifiée qui maintient des concentrations suffisamment élevées pour permettre à la réaction globale (par exemple, une réaction de type R1) de se dérouler. à un rythme rapide. Les suppresseurs chimiques appliqués en quantité suffisante entraîneront une chute spectaculaire de la concentration de ces radicaux, éteignant efficacement la flamme. Les agents les plus courants qui fonctionnent de cette manière sont les halons et les poudres sèches.
Les halons réagissent dans la flamme pour générer d'autres espèces intermédiaires avec lesquelles les radicaux de la flamme réagissent préférentiellement. Des quantités relativement faibles de halons sont nécessaires pour éteindre un incendie et, pour cette raison, elles étaient traditionnellement considérées comme hautement souhaitables; les concentrations extinctrices sont « respirables » (bien que les produits générés lors du passage à travers la flamme soient nocifs). Les poudres sèches agissent de la même manière, mais dans certaines circonstances, elles sont beaucoup plus efficaces. Les particules fines sont dispersées dans la flamme et provoquent la terminaison des chaînes radicalaires. Il est important que les particules soient petites et nombreuses. Ceci est réalisé par les fabricants de nombreuses marques propriétaires de poudres sèches en sélectionnant une poudre qui "décrépite", c'est-à-dire que les particules se fragmentent en particules plus petites lorsqu'elles sont exposées aux températures élevées de la flamme.
Pour une personne dont les vêtements ont pris feu, un extincteur à poudre sèche est reconnu comme le meilleur moyen de contrôler les flammes et de protéger cette personne. Une intervention rapide donne un "renversement" rapide, minimisant ainsi les blessures. Cependant, la flamme doit être complètement éteinte car les particules tombent rapidement au sol et toute flamme résiduelle reprendra rapidement du terrain. De même, les halons ne resteront efficaces que si les concentrations locales sont maintenues. S'il est appliqué à l'extérieur, la vapeur de halon se disperse rapidement, et à nouveau le feu se rétablira rapidement s'il reste une flamme résiduelle. Plus important encore, la perte du suppresseur sera suivie d'un réallumage du carburant si les températures de surface sont suffisamment élevées. Ni les halons ni les poudres sèches n'ont d'effet de refroidissement significatif sur la surface du combustible.
Suppression de l'arrivée d'air
La description suivante est une simplification excessive du processus. Bien que "supprimer l'alimentation en air" provoque certainement l'extinction du feu, il suffit pour cela de réduire la concentration d'oxygène en dessous d'un niveau critique. Le « test de l'indice d'oxygène » bien connu classe les matériaux combustibles en fonction de la concentration minimale en oxygène dans un mélange oxygène/azote qui supportera juste la flamme. De nombreux matériaux courants brûlent à des concentrations d'oxygène jusqu'à environ 14 % à température ambiante (environ 20 °C) et en l'absence de tout transfert de chaleur imposé. La concentration critique dépend de la température et diminue à mesure que la température augmente. Ainsi, un feu qui brûle depuis un certain temps sera capable d'entretenir des flammes à des concentrations peut-être aussi faibles que 7 %. Un incendie dans une pièce peut être maîtrisé et peut même s'éteindre si l'apport d'oxygène est limité en gardant les portes et les fenêtres fermées. La flamme peut cesser, mais la combustion se poursuivra à des concentrations d'oxygène très inférieures. L'admission d'air en ouvrant une porte ou en brisant une fenêtre avant que la pièce ne se soit suffisamment refroidie peut entraîner une éruption vigoureuse du feu, connue sous le nom de contre-courantou backdraft.
L'« élimination de l'air » est difficile à réaliser. Cependant, une atmosphère peut être rendue « inerte » par noyage total au moyen d'un gaz qui n'entretiendra pas la combustion, tel que l'azote, le dioxyde de carbone ou les gaz issus d'un processus de combustion (par exemple, les moteurs d'un navire) qui sont pauvres en oxygène et à haute teneur en oxygène. en dioxyde de carbone. Cette technique ne peut être utilisée que dans des espaces clos car il est nécessaire de maintenir la concentration requise du « gaz inerte » jusqu'à ce que l'incendie soit complètement éteint ou que les opérations de lutte contre l'incendie puissent commencer. L'inondation totale a des applications spéciales, comme pour les cales des navires et les collections de livres rares dans les bibliothèques. Les concentrations minimales requises des gaz inertes sont indiquées dans le tableau 4. Celles-ci sont basées sur l'hypothèse que le feu est détecté à un stade précoce et que l'inondation est effectuée avant que trop de chaleur ne se soit accumulée dans l'espace.
Tableau 4 : Comparaison des concentrations des différents gaz nécessaires à l'inertage
|
Agent |
Concentration minimale (% volume) |
|
Halons 1301 |
8.0 |
|
Halons 1211 |
8.1 |
|
Azote |
|
|
Gaz carbonique |
|
L'« élimination de l'air » peut être effectuée à proximité immédiate d'un petit incendie par l'application locale d'un extincteur à l'aide d'un extincteur. Le dioxyde de carbone est le seul gaz utilisé de cette manière. Cependant, comme ce gaz se disperse rapidement, il est indispensable d'éteindre toute flamme lors de l'attaque du feu ; sinon, le flambage se rétablira. Le rallumage est également possible car le dioxyde de carbone a peu ou pas d'effet de refroidissement. Il est à noter qu'une fine pulvérisation d'eau entraînée dans une flamme peut provoquer l'extinction sous l'effet combiné de l'évaporation des gouttelettes (qui refroidit la zone de combustion) et de la réduction de la concentration en oxygène par dilution par la vapeur d'eau (qui agit de la même manière sous forme de dioxyde de carbone). De fines pulvérisations d'eau et des brouillards sont envisagés comme des substituts possibles aux halons.
Il convient de mentionner ici qu'il est déconseillé d'éteindre une flamme de gaz à moins que le flux de gaz ne puisse être arrêté immédiatement après. Sinon, un volume substantiel de gaz inflammable peut s'accumuler et ensuite s'enflammer, avec des conséquences potentiellement graves.
Éteindre
Cette méthode est incluse ici par souci d'exhaustivité. Une flamme d'allumette peut facilement être soufflée en augmentant la vitesse de l'air au-dessus d'une valeur critique à proximité de la flamme. Le mécanisme fonctionne en déstabilisant la flamme au voisinage du combustible. En principe, les incendies plus importants peuvent être contrôlés de la même manière, mais des charges explosives sont normalement nécessaires pour générer des vitesses suffisantes. Les incendies de puits de pétrole peuvent être éteints de cette manière.
Enfin, une caractéristique commune qu'il convient de souligner est que la facilité avec laquelle un incendie peut être éteint diminue rapidement à mesure que l'incendie prend de l'ampleur. Une détection précoce permet une extinction avec des quantités minimales de suppresseur, avec des pertes réduites. Lors du choix d'un système d'extinction, il faut tenir compte du taux potentiel de développement du feu et du type de système de détection disponible.
Explosions
Une explosion se caractérise par la libération soudaine d'énergie, produisant une onde de choc, ou onde de choc, qui peut être capable de causer des dommages à distance. Il existe deux types distincts de sources, à savoir l'explosif brisant et l'éclatement sous pression. L'explosif puissant est caractérisé par des composés tels que le trinitrotoluène (TNT) et la cyclotriméthylènetrinitramine (RDX). Ces composés sont des espèces hautement exothermiques, se décomposant pour libérer des quantités substantielles d'énergie. Bien que thermiquement stables (bien que certains le soient moins et nécessitent une désensibilisation pour les rendre sûrs à manipuler), ils peuvent être amenés à exploser, avec décomposition, se propageant à la vitesse du son à travers le solide. Si la quantité d'énergie libérée est suffisamment élevée, une onde de choc se propagera à partir de la source avec le potentiel de causer des dommages importants à distance.
En évaluant les dommages à distance, on peut estimer la taille de l'explosion en « équivalent TNT » (normalement en tonnes métriques). Cette technique repose sur la grande quantité de données qui ont été recueillies sur le potentiel de dommages du TNT (une grande partie en temps de guerre) et utilise des lois d'échelle empiriques qui ont été développées à partir d'études des dommages causés par des quantités connues de TNT.
En temps de paix, les explosifs brisants sont utilisés dans diverses activités, notamment les mines, les carrières et les grands travaux de génie civil. Leur présence sur un site représente un danger particulier qui nécessite une gestion spécifique. Cependant, l'autre source d'« explosions » peut être tout aussi dévastatrice, en particulier si le danger n'a pas été reconnu. Les surpressions conduisant à des coups de bélier peuvent être le résultat de processus chimiques au sein des usines ou d'effets purement physiques, comme cela se produira si un récipient est chauffé de l'extérieur, entraînant une surpression. Le terme BLEVE (explosion de vapeur en expansion de liquide bouillant) a ses origines ici, se référant à l'origine à la défaillance des chaudières à vapeur. Il est maintenant également couramment utilisé pour décrire l'événement dans lequel un récipient sous pression contenant un gaz liquéfié tel que le GPL (gaz de pétrole liquéfié) échoue dans un incendie, libérant le contenu inflammable, qui s'enflamme ensuite pour produire une "boule de feu".
D'autre part, la surpression peut être provoquée en interne par un processus chimique. Dans les industries de process, l'auto-échauffement peut conduire à un emballement de la réaction, générant des températures et des pressions élevées capables de provoquer une explosion de pression. Cependant, le type d'explosion le plus courant est causé par l'inflammation d'un mélange gaz/air inflammable qui est confiné à l'intérieur d'un élément d'une usine ou même à l'intérieur de toute structure ou enceinte de confinement. La condition préalable est la formation d'un mélange inflammable, un événement qui devrait être évité par une bonne conception et une bonne gestion. En cas de rejet accidentel, une atmosphère inflammable existera partout où la concentration du gaz (ou de la vapeur) se situe entre les limites inférieure et supérieure d'inflammabilité (tableau 1). Si une source d'allumage est introduite dans l'une de ces régions, une flamme prémélangée se propagera rapidement à partir de la source, convertissant le mélange carburant/air en produits de combustion à une température élevée. Celle-ci peut aller jusqu'à 2,100 300 K, indiquant que dans un système complètement fermé initialement à 7 K, une surpression aussi élevée que XNUMX bars est possible. Seuls les récipients sous pression spécialement conçus sont capables de contenir de telles surpressions. Les bâtiments ordinaires tomberont s'ils ne sont pas protégés par des panneaux de décompression ou des disques de rupture ou par un système d'extinction d'explosion. Si un mélange inflammable se forme à l'intérieur d'un bâtiment, l'explosion qui s'ensuit peut causer des dommages structurels importants - peut-être une destruction totale - à moins que l'explosion ne puisse s'évacuer vers l'extérieur par des ouvertures (par exemple, la défaillance de fenêtres) créées au cours des premières étapes de l'explosion.
Les explosions de ce type sont également associées à l'inflammation de poussières en suspension dans l'air (Palmer 1973). Ceux-ci se produisent lorsqu'il y a une accumulation substantielle de poussière «explosible» qui est délogée des étagères, des chevrons et des rebords à l'intérieur d'un bâtiment pour former un nuage, qui est ensuite exposé à une source d'inflammation (par exemple, dans les minoteries, les élévateurs à grains, etc. .). La poussière doit (évidemment) être combustible, mais toutes les poussières combustibles ne sont pas explosibles à température ambiante. Des tests standards ont été conçus pour déterminer si une poussière est explosible. Celles-ci peuvent également être utilisées pour illustrer que les poussières explosives présentent des « limites d'explosibilité », similaires dans leur concept aux « limites d'inflammabilité » des gaz et des vapeurs. En général, une explosion de poussière a le potentiel de faire beaucoup de dégâts car l'événement initial peut provoquer le délogement de plus de poussière, formant un nuage de poussière encore plus grand qui s'enflammera inévitablement, pour produire une explosion encore plus grande.
Ventilation d'explosionou secours d'explosion, ne fonctionnera avec succès que si le taux de développement de l'explosion est relativement lent, tel qu'associé à la propagation d'une flamme prémélangée à travers un mélange inflammable stationnaire ou un nuage de poussière explosible. La ventilation d'explosion n'est d'aucune utilité si une détonation est impliquée. La raison en est que les ouvertures de décompression doivent être créées à un stade précoce de l'événement lorsque la pression est encore relativement faible. Si une détonation se produit, la pression monte trop rapidement pour que le soulagement soit efficace, et le récipient ou l'élément d'une usine qui l'entoure subit des pressions internes très élevées qui conduiront à une destruction massive. Détonation d'un mélange gazeux inflammable peut se produire si le mélange est contenu dans un long tuyau ou conduit. Dans certaines conditions, la propagation de la flamme prémélangée poussera le gaz non brûlé devant le front de flamme à une vitesse qui augmentera la turbulence, qui à son tour augmentera la vitesse de propagation. Cela fournit une boucle de rétroaction qui fera accélérer la flamme jusqu'à ce qu'une onde de choc se forme. Ceci, combiné au processus de combustion, est une onde de détonation qui peut se propager à des vitesses bien supérieures à 1,000 XNUMX m/s. Ceci peut être comparé avec le vitesse de combustion fondamentale d'un mélange stoechiométrique propane/air de 0.45 m/s. (Il s'agit de la vitesse à laquelle une flamme se propagera à travers un mélange propane/air au repos (c'est-à-dire non turbulent).)
L'importance de la turbulence sur le développement de ce type d'explosion ne peut être sous-estimée. Le bon fonctionnement d'un système de protection contre les explosions repose sur une ventilation précoce ou une suppression précoce. Si le rythme de développement de l'explosion est trop rapide, le système de protection ne sera pas efficace et des surpressions inacceptables pourront se produire.
Une alternative au soulagement d'explosion est suppression des explosions. Ce type de protection nécessite que l'explosion soit détectée à un stade très précoce, le plus près possible de l'inflammation. Le détecteur est utilisé pour initier la libération rapide d'un suppresseur dans le trajet de la propagation de la flamme, arrêtant efficacement l'explosion avant que la pression n'ait augmenté à un degré auquel l'intégrité des limites d'enceinte est menacée. Les halons ont été couramment utilisés à cette fin, mais comme ils sont progressivement éliminés, l'attention est désormais portée sur l'utilisation de systèmes de pulvérisation d'eau à haute pression. Ce type de protection est très coûteux et d'application limitée car il ne peut être utilisé que dans des volumes relativement petits dans lesquels l'agent d'extinction peut être distribué rapidement et uniformément (par exemple, des conduits transportant des vapeurs inflammables ou des poussières explosibles).
Analyse des informations pour la protection incendie
En termes généraux, la science du feu n'a été développée que récemment à un stade où elle est capable de fournir la base de connaissances sur laquelle des décisions rationnelles concernant la conception technique, y compris les questions de sécurité, peuvent être fondées. Traditionnellement, la sécurité incendie s'est développée sur une ad hoc sur une base efficace, en répondant efficacement aux incidents en imposant des réglementations ou d'autres restrictions pour s'assurer qu'il ne se reproduira pas. De nombreux exemples pourraient être cités. Par exemple, le grand incendie de Londres en 1666 a conduit en temps voulu à l'établissement des premiers règlements (ou codes) de construction et au développement de l'assurance incendie. Des incidents plus récents, tels que les incendies d'immeubles de bureaux de grande hauteur à São Paulo, au Brésil, en 1972 et 1974, ont entraîné des modifications des codes du bâtiment, conçues de manière à prévenir des incendies similaires à décès multiples à l'avenir. D'autres problèmes ont été traités de manière similaire. En Californie, aux États-Unis, le danger associé à certains types de meubles rembourrés modernes (en particulier ceux contenant de la mousse de polyuréthane standard) a été reconnu et, finalement, des réglementations strictes ont été introduites pour contrôler sa disponibilité.
Il s'agit de cas simples où l'observation des conséquences d'un incendie a conduit à imposer un ensemble de règles destinées à améliorer la sécurité de l'individu et de la collectivité en cas d'incendie. La décision d'agir sur toute question doit être justifiée sur la base d'une analyse de notre connaissance des incidents d'incendie. Il faut montrer que le problème est réel. Dans certains cas, comme les incendies de São Paulo, cet exercice est académique, mais dans d'autres, comme « prouver » que l'ameublement moderne est un problème, il est nécessaire de s'assurer que les coûts associés sont dépensés à bon escient. Cela nécessite une base de données fiable sur les incendies qui, sur un certain nombre d'années, est capable de montrer les tendances du nombre d'incendies, du nombre de décès, de l'incidence d'un type particulier d'inflammation, etc. Des techniques statistiques peuvent alors être utilisées pour examiner si une tendance ou un changement est significatif et des mesures appropriées sont prises.
Dans un certain nombre de pays, les pompiers sont tenus de soumettre un rapport sur chaque incendie survenu. Au Royaume-Uni et aux États-Unis, l'officier responsable remplit un formulaire de rapport qui est ensuite soumis à un organisme central (le Home Office au Royaume-Uni, la National Fire Protection Association, NFPA, aux États-Unis) qui code ensuite et traite les données de la manière prescrite. Les données sont ensuite disponibles pour inspection par les organismes gouvernementaux et autres parties intéressées. Ces bases de données sont précieuses pour mettre en évidence (par exemple) les principales sources d'inflammation et les premiers éléments enflammés. Un examen de l'incidence des décès et de leur relation avec les sources d'inflammation, etc. a montré que le nombre de personnes qui meurent dans des incendies déclenchés par des produits pour fumeurs est nettement disproportionné par rapport au nombre d'incendies qui se déclenchent de cette manière.
La fiabilité de ces bases de données dépend de la compétence avec laquelle les pompiers mènent l'enquête incendie. L'enquête sur les incendies n'est pas une tâche facile et nécessite des capacités et des connaissances considérables, en particulier une connaissance de la science des incendies. Le service d'incendie du Royaume-Uni a l'obligation légale de soumettre un formulaire de rapport d'incendie pour chaque incendie auquel il assiste, ce qui impose une responsabilité considérable à l'officier responsable. La construction du formulaire est cruciale, car il doit obtenir les informations requises de manière suffisamment détaillée. Le « formulaire de rapport d'incident de base » recommandé par la NFPA est présenté dans le Manuel de protection contre les incendies (Côté 1991).
Les données peuvent être utilisées de deux manières, soit pour identifier un problème d'incendie, soit pour fournir l'argument rationnel nécessaire pour justifier une ligne de conduite particulière qui peut nécessiter des dépenses publiques ou privées. Une base de données établie de longue date peut être utilisée pour montrer les effets des actions entreprises. Les dix points suivants ont été tirés des statistiques de la NFPA sur la période 1980 à 1989 (Cote 1991) :
1. Les détecteurs de fumée domestiques sont largement utilisés et très efficaces (mais des lacunes importantes subsistent dans la stratégie de détection).
2. Les gicleurs automatiques réduisent considérablement les pertes de vie et de biens. L'utilisation accrue d'équipements de chauffage portables et de surface a fortement augmenté les incendies domestiques impliquant des équipements de chauffage.
3. Les incendies incendiaires et suspects ont continué à diminuer par rapport au pic des années 1970, mais les dommages matériels associés ont cessé de diminuer.
4. Une grande partie des décès de pompiers sont attribués à des crises cardiaques et à des activités en dehors du lieu de l'incendie.
5. Les zones rurales ont les taux de mortalité par incendie les plus élevés.
6. Les matières à fumer qui enflamment les meubles rembourrés, les matelas ou la literie produisent les scénarios d'incendie résidentiel les plus meurtriers.
7. Les taux de mortalité par incendie aux États-Unis et au Canada sont parmi les plus élevés de tous les pays développés.
8. Les États du Vieux Sud aux États-Unis ont les taux de mortalité par incendie les plus élevés.
9. Les personnes âgées courent un risque particulièrement élevé de mourir dans un incendie.
Ces conclusions sont, bien sûr, propres à chaque pays, bien qu'il existe certaines tendances communes. Une utilisation prudente de ces données peut fournir les moyens de formuler des politiques judicieuses concernant la sécurité incendie dans la communauté. Cependant, il faut se rappeler que ceux-ci sont inévitablement « réactifs », plutôt que « proactifs ». Des mesures proactives ne peuvent être introduites qu'après une évaluation détaillée des risques d'incendie. Une telle ligne de conduite a été progressivement mise en place, en commençant par l'industrie nucléaire et en se déplaçant dans les industries chimiques, pétrochimiques et offshore où les risques sont beaucoup plus facilement définissables que dans d'autres industries. Leur application aux hôtels et aux bâtiments publics est généralement beaucoup plus difficile et nécessite l'application de techniques de modélisation du feu pour prédire le cours d'un incendie et la manière dont les produits du feu se propageront à travers le bâtiment pour affecter les occupants. Des avancées majeures ont été réalisées dans ce type de modélisation, même s'il faut dire qu'il reste encore beaucoup de chemin à parcourir avant que ces techniques puissent être utilisées en toute confiance. L'ingénierie de la sécurité incendie a encore besoin de beaucoup de recherche fondamentale en science de la sécurité incendie avant que des outils fiables d'évaluation des risques d'incendie puissent être largement disponibles.