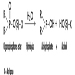Kinder Kategorien

27. Biologische Überwachung (6)

27. Biologische Überwachung
Kapitelherausgeber: Robert Lauwerys
Inhaltsverzeichnis
Tabellen und Abbildungen
Allgemeine Grundsätze
Vito Foà und Lorenzo Alessio
Qualitätssicherung
D. Gompertz
Metalle und metallorganische Verbindungen
P. Hoet und Robert Lauwerys
Organische Lösungsmittel
Masayuki Ikeda
Genotoxische Chemikalien
Marja Sorsa
Pestizide
Marco Maroni und Adalberto Ferioli
Tische
Klicken Sie unten auf einen Link, um die Tabelle im Artikelkontext anzuzeigen.
1. ACGIH, DFG & andere Grenzwerte für Metalle
2. Beispiele für Chemikalien- und biologisches Monitoring
3. Biologische Überwachung auf organische Lösungsmittel
4. Genotoxizität von Chemikalien, bewertet von IARC
5. Biomarker und einige Zell-/Gewebeproben und Genotoxizität
6. Menschliche Karzinogene, berufliche Exposition und zytogenetische Endpunkte
8. Exposition durch Produktion und Verwendung von Pestiziden
9. Akute OP-Toxizität bei verschiedenen Graden der ACHE-Hemmung
10 Variationen von ACHE & PCHE & ausgewählten Gesundheitszuständen
11 Cholinesterase-Aktivitäten von nicht exponierten gesunden Menschen
12 Alkylphosphate im Urin und OP-Pestizide
13 Alkylphosphatmessungen im Urin & OP
14 Carbamat-Metaboliten im Urin
15 Dithiocarbamat-Metaboliten im Urin
16 Vorgeschlagene Indizes für die biologische Überwachung von Pestiziden
17 Empfohlene biologische Grenzwerte (Stand 1996)
Zahlen
Zeigen Sie auf eine Miniaturansicht, um die Bildunterschrift anzuzeigen, klicken Sie, um die Abbildung im Artikelkontext anzuzeigen.

28. Epidemiologie und Statistik (12)

28. Epidemiologie und Statistik
Kapitel-Editoren: Franco Merletti, Colin L. Soskolne und Paolo Vineis
Inhaltsverzeichnis
Tabellen und Abbildungen
Epidemiologische Methode für Arbeitssicherheit und Gesundheitsschutz
Franco Merletti, Colin L. Soskolne und Paolo Vineis
Expositionsbewertung
M. Gerald Ott
Zusammenfassung der Expositionsmaßnahmen im Arbeitsleben
Colin L. Soskolne
Messung der Auswirkungen von Expositionen
Shelia Hoar Zahm
Fallbeispiel: Maßnahmen
Franco Merletti, Colin L. Soskolne und Paola Vineis
Optionen im Studiendesign
Sven Herberg
Validitätsprobleme im Studiendesign
Annie J. Sasco
Einfluss zufälliger Messfehler
Paolo Vineis und Colin L. Soskolne
Statistische Methoden
Annibale Biggeri und Mario Braga
Kausalitätsbewertung und Ethik in der epidemiologischen Forschung
Paolo Vineis
Fallstudien zur Veranschaulichung methodischer Probleme bei der Überwachung von Berufskrankheiten
Jung-Der Wang
Fragebögen in der epidemiologischen Forschung
Steven D. Stellman und Colin L. Soskolne
Asbest Historische Perspektive
Laurent Garfinkel
Tische
Klicken Sie unten auf einen Link, um die Tabelle im Artikelkontext anzuzeigen.
1. Fünf ausgewählte zusammenfassende Maßnahmen zur Exposition im Berufsleben
2. Maße für das Auftreten von Krankheiten
3. Assoziationsmaße für eine Kohortenstudie
4. Assoziationsmaße für Fall-Kontroll-Studien
5. Allgemeines Häufigkeitstabellenlayout für Kohortendaten
6. Musterlayout von Fallkontrolldaten
7. Layout-Fallkontrolldaten – eine Kontrolle pro Fall
8. Hypothetische Kohorte von 1950 Individuen zu T2
9. Indizes der zentralen Tendenz und Streuung
10 Ein binomiales Experiment & Wahrscheinlichkeiten
11 Mögliche Ergebnisse eines binomialen Experiments
12 Binomialverteilung, 15 Erfolge/30 Versuche
13 Binomialverteilung, p = 0.25; 30 Versuche
14 Fehler XNUMX. Art & Leistung; x = 12, n = 30, a = 0.05
15 Fehler XNUMX. Art & Leistung; x = 12, n = 40, a = 0.05
16 632 Arbeitnehmer, die 20 Jahre oder länger Asbest ausgesetzt waren
17 O/E Zahl der Todesfälle unter 632 Asbestarbeitern
Zahlen
Zeigen Sie auf eine Miniaturansicht, um die Bildunterschrift anzuzeigen, klicken Sie, um die Abbildung im Artikelkontext anzuzeigen.

29. Ergonomie (27)

29. Ergonomie
Kapitel-Editoren: Wolfgang Laurig und Joachim Vedder
Inhaltsverzeichnis
Tabellen und Abbildungen
Überblick
Wolfgang Laurig und Joachim Vedder
Ziele, Prinzipien und Methoden
Wesen und Ziele der Ergonomie
William T. Singleton
Analyse von Aktivitäten, Aufgaben und Arbeitssystemen
Véronique De Keyser
Ergonomie und Standardisierung
Friedhelm Nachreiner
Prüflisten
Pranab Kumar Nag
Physikalische und physiologische Aspekte
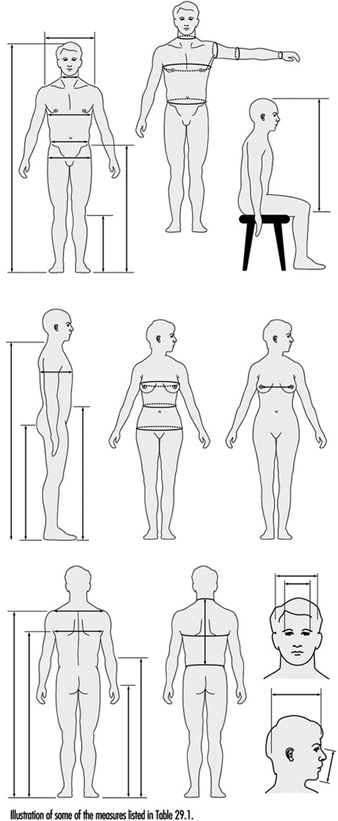
Anthropometrie
Melchiorre Masali
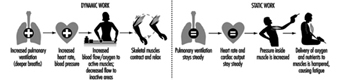
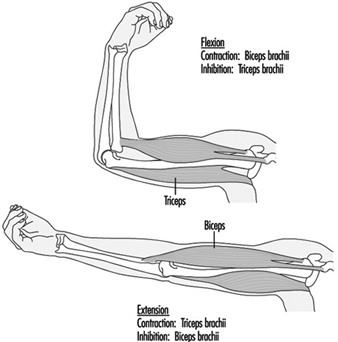
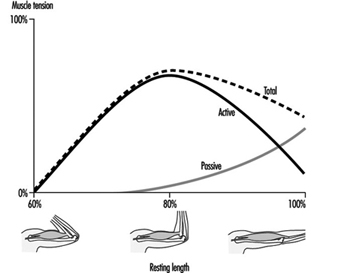
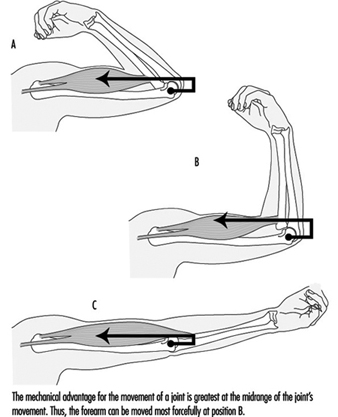
Muskelarbeit
Juhani Smolander und Veikko Louhevaara
Körperhaltungen bei der Arbeit
Ilkka Kurinka
Biomechanik
Frank Darby
Allgemeine Müdigkeit
Etienne Grandjean
Müdigkeit und Erholung
Rolf Helbig und Walter Rohmert
Psychologische Aspekte
Geistige Arbeitsbelastung
Winfried Hacker
Wachsamkeit
Herbert Heuer
Geistige Müdigkeit
Peter Richter
Organisatorische Aspekte der Arbeit
Arbeitsorganisation
Eberhard Ulich und Gudela Grote
Schlafentzug
Kazutaka Kogi
Gestaltung von Arbeitssystemen
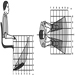
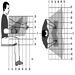
Workstations
Roland Kadefors
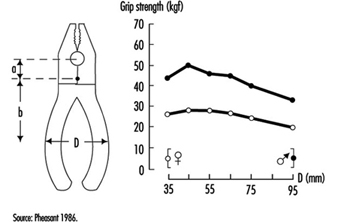
Tools
TM Fraser
Bedienelemente, Anzeigen und Bedienfelder
Karl HE Kroemer
Informationsverarbeitung und Design
Andries F. Sanders
Designen für alle
Entwerfen für bestimmte Gruppen
Witz H. Grady-van den Nieuwboer
Fallstudie: Die internationale Klassifikation der Funktionseinschränkung beim Menschen
Kulturelle Unterschiede
Houshang Shahnavaz
Ältere Arbeitnehmer
Antoine Laville und Serge Volkoff
Arbeitnehmer mit besonderen Bedürfnissen
Witz H. Grady-van den Nieuwboer
Vielfalt und Bedeutung der Ergonomie – zwei Beispiele
Systemdesign in der Diamantherstellung
Issachar Gilad
Missachtung ergonomischer Gestaltungsprinzipien: Tschernobyl
Wladimir M. Munipov
Tische
Klicken Sie unten auf einen Link, um die Tabelle im Artikelkontext anzuzeigen.
1. Grundlegende anthropometrische Kernliste
2. Ermüdung und Erholung abhängig vom Aktivitätsniveau
3. Regeln der Kombinationswirkung zweier Stressfaktoren auf die Belastung
4. Es wird zwischen mehreren negativen Folgen psychischer Belastung unterschieden
5. Arbeitsorientierte Prinzipien zur Produktionsgestaltung
6. Partizipation im organisatorischen Kontext
7. Benutzerbeteiligung am Technologieprozess
8. Unregelmäßige Arbeitszeiten und Schlafentzug
9. Aspekte von Früh-, Anker- und Verzögerungsschlaf
10 Kontrollieren Sie Bewegungen und erwartete Effekte
11 Steuerungs-Wirkungs-Beziehungen gängiger Handsteuerungen
12 Regeln für die Anordnung von Kontrollen
Zahlen
Zeigen Sie auf eine Miniaturansicht, um die Bildunterschrift anzuzeigen, klicken Sie, um die Abbildung im Artikelkontext anzuzeigen.

30. Arbeitshygiene (6)

30. Arbeitshygiene
Kapitel-Editor: Robert F. Herrick
Inhaltsverzeichnis
Tabellen und Abbildungen
Ziele, Definitionen und allgemeine Informationen
Berenice I. Ferrari Goelzer
Gefahren erkennen
Linnea Lillienberg
Bewertung der Arbeitsumgebung
Lori A. Todd
Arbeitshygiene: Expositionskontrolle durch Intervention
James Stewart
Die biologische Grundlage für die Expositionsbewertung
Dick Heederik
Arbeitsplatzgrenzwerte
Dennis J. Pausenbach
Tische
1. Gefahren durch Chemikalien; biologische und physikalische Wirkstoffe
2. Arbeitsplatzgrenzwerte (OELs) – verschiedene Länder
Zahlen

31. Personenschutz (7)

31. Persönlicher Schutz
Kapitel-Editor: Robert F. Herrick
Inhaltsverzeichnis
Tabellen und Abbildungen
Überblick und Philosophie des Personenschutzes
Robert F. Herrick
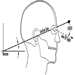
Augen- und Gesichtsschutz
Kikuzi Kimura
Fuß- und Beinschutz
Toyohiko Miura
Kopfschutz
Isabelle Balty und Alain Mayer
Gehörschutz
John R. Franks und Elliott H. Berger
Schutzkleidung
S.Zack Mansdorf
Atemschutz
Thomas J. Nelson
Tische
Klicken Sie unten auf einen Link, um die Tabelle im Artikelkontext anzuzeigen.
1. Transmissionsanforderungen (ISO 4850-1979)
2. Schutzmaßstäbe - Gasschweißen & Lötschweißen
3. Schutzwaage - Sauerstoffschneiden
4. Schutzmaßstäbe - Plasmalichtbogenschneiden
5. Schutzwaagen - Lichtbogenschweißen oder Fugenhobeln
6. Schutzmaßstäbe - Plasma-Lichtbogen-Direktschweißen
7. Schutzhelm: ISO-Norm 3873-1977
8. Geräuschreduzierungsbewertung eines Gehörschutzes
9. Berechnung der A-bewerteten Rauschunterdrückung
10 Beispiele für Hautgefahrenkategorien
11 Physikalische, chemische und biologische Leistungsanforderungen
12 Sachgefahren im Zusammenhang mit bestimmten Tätigkeiten
13 Zugewiesene Schutzfaktoren aus ANSI Z88 2 (1992)
Zahlen
Zeigen Sie auf eine Miniaturansicht, um die Bildunterschrift anzuzeigen, klicken Sie, um die Abbildung im Artikelkontext anzuzeigen.

32. Aufzeichnungssysteme und Überwachung (9)

32. Aufzeichnungssysteme und Überwachung
Kapitel-Editor: Steven D. Stellman
Inhaltsverzeichnis
Tabellen und Abbildungen
Überwachungs- und Meldesysteme für Berufskrankheiten
Steven B. Markowitz
Überwachung von Arbeitsgefahren
David H. Wegman und Steven D. Stellman
Überwachung in Entwicklungsländern
David Koh und Kee-Seng Chia
Entwicklung und Anwendung eines Klassifizierungssystems für Arbeitsunfälle und Berufskrankheiten
Elyce Biddle
Risikoanalyse von nicht tödlichen Verletzungen und Krankheiten am Arbeitsplatz
John W. Ruser
Fallstudie: Arbeitnehmerschutz und Statistiken zu Unfällen und Berufskrankheiten - HVBG, Deutschland
Martin Butz und Burkhard Hoffmann
Fallstudie: Wismut – Eine Neuauflage der Uranexposition
Heinz Otten und Horst Schulz
Messstrategien und -techniken für die berufsbedingte Expositionsabschätzung in der Epidemiologie
Frank Bochmann und Helmut Blome
Fallstudie: Arbeitsmedizinische Erhebungen in China
Tische
Klicken Sie unten auf einen Link, um die Tabelle im Artikelkontext anzuzeigen.
1. Angiosarkom der Leber - Weltregister
2. Berufskrankheit, USA, 1986 versus 1992
3. US-Todesfälle durch Pneumokoniose und Pleuramesotheliom
4. Musterliste meldepflichtiger Berufskrankheiten
5. Codestruktur für die Meldung von Krankheiten und Verletzungen, USA
6. Nichttödliche Arbeitsunfälle und Berufskrankheiten, USA 1993
7. Risiko von Arbeitsunfällen und Berufskrankheiten
8. Relatives Risiko für sich wiederholende Bewegungszustände
9. Arbeitsunfälle, Deutschland, 1981-93
10 Schleifmaschinen bei Unfällen in der Metallverarbeitung, Deutschland, 1984-93
11 Berufskrankheit, Deutschland, 1980-93
12 Infektionskrankheiten, Deutschland, 1980-93
13 Strahlenbelastung in den Wismut-Bergwerken
14 Berufskrankheiten im Wismuter Uranbergwerk 1952-90
Zahlen
Zeigen Sie auf eine Miniaturansicht, um die Bildunterschrift anzuzeigen, klicken Sie, um die Abbildung im Artikelkontext anzuzeigen.

33. Toxikologie (21)

33. Toxikologie
Kapitelherausgeberin: Ellen K. Silbergeld
Inhaltsverzeichnis
Tabellen und Abbildungen
Einleitung
Ellen K. Silbergeld, Kapitelredakteurin
Allgemeine Prinzipien der Toxikologie
Definitionen und Konzepte
Bo Holmberg, Johan Hogberg und Gunnar Johanson
Toxikokinetik
Dušan Djuric
Zielorgan und kritische Wirkungen
Marek Jakubowski
Auswirkungen von Alter, Geschlecht und anderen Faktoren
Spomenka Telisman
Genetische Determinanten der toxischen Reaktion
Daniel W. Nebert und Ross A. McKinnon
Mechanismen der Toxizität
Einführung und Konzepte
Philip G. Watanabe
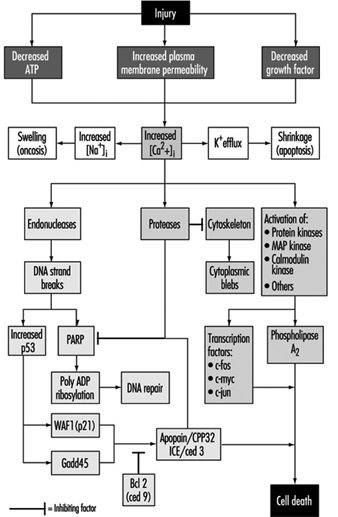
Zellschädigung und Zelltod
Benjamin F. Trump und Irene K. Berezesky
Genetische Toxikologie
R. Rita Misra und Michael P. Waalkes
Immuntoxikologie
Joseph G. Vos und Henk van Loveren
Zielorgan-Toxikologie
Ellen K. Silbergeld
Toxikologische Testmethoden
Biomarker
Philipp Grandjean
Bewertung der genetischen Toxizität
David M. DeMarini und James Huff
In-vitro-Toxizitätstest
Joanne Zürlo
Aktivitätsbeziehungen strukturieren
Ellen K. Silbergeld
Regulatorische Toxikologie
Toxikologie in der Gesundheits- und Sicherheitsverordnung
Ellen K. Silbergeld
Prinzipien der Gefahrenidentifizierung - Der japanische Ansatz
Masayuki Ikeda
Der Ansatz der Vereinigten Staaten zur Risikobewertung von reproduktionstoxischen und neurotoxischen Wirkstoffen
Ellen K. Silbergeld
Ansätze zur Gefahrenidentifizierung - IARC
Harri Vainio und Julian Wilbourn
Anhang – Gesamtbewertungen der Karzinogenität beim Menschen: IARC-Monographien, Bände 1–69 (836)
Karzinogen-Risikobewertung: Andere Ansätze
Cees A. van der Heijden
Tische
Klicken Sie unten auf einen Link, um die Tabelle im Artikelkontext anzuzeigen.
- Beispiele für kritische Organe und kritische Effekte
- Grundlegende Wirkungen möglicher Mehrfachwechselwirkungen von Metallen
- Hämoglobinaddukte bei Arbeitern, die Anilin und Acetanilid ausgesetzt waren
- Erbliche, krebsanfällige Erkrankungen und Defekte in der DNA-Reparatur
- Beispiele für Chemikalien, die in menschlichen Zellen genotoxisch wirken
- Klassifizierung von Tests für Immunmarker
- Beispiele für Biomarker der Exposition
- Vor- und Nachteile von Methoden zur Identifizierung von Krebsrisiken beim Menschen
- Vergleich von In-vitro-Systemen für Hepatotoxizitätsstudien
- Vergleich von SAR- und Testdaten: OECD/NTP-Analysen
- Regulierung chemischer Stoffe durch Gesetze, Japan
- Prüfgegenstände gemäß dem Gesetz zur Kontrolle chemischer Substanzen, Japan
- Chemische Substanzen und das Gesetz zur Kontrolle chemischer Substanzen
- Ausgewählte größere Neurotoxizitätsvorfälle
- Beispiele für spezialisierte Tests zur Messung der Neurotoxizität
- Endpunkte in der Reproduktionstoxikologie
- Vergleich von Niedrigdosis-Extrapolationsverfahren
- Häufig zitierte Modelle zur Charakterisierung des Karzinogenrisikos
Zahlen
Zeigen Sie auf eine Miniaturansicht, um die Bildunterschrift anzuzeigen, klicken Sie, um die Abbildung im Artikelkontext anzuzeigen.
Pestizide
Einleitung
Die Exposition des Menschen gegenüber Pestiziden weist unterschiedliche Merkmale auf, je nachdem, ob sie während der industriellen Produktion oder Verwendung auftritt (Tabelle 1). Die Formulierung kommerzieller Produkte (durch Mischen von Wirkstoffen mit anderen Beistoffen) hat einige Expositionsmerkmale gemeinsam mit der Verwendung von Pestiziden in der Landwirtschaft. Da die Formulierung typischerweise von kleinen Industrien durchgeführt wird, die viele verschiedene Produkte in aufeinanderfolgenden Arbeitsgängen herstellen, sind die Arbeiter für kurze Zeit jedem von mehreren Pestiziden ausgesetzt. Im öffentlichen Gesundheitswesen und in der Landwirtschaft ist die Verwendung einer Vielzahl von Verbindungen im Allgemeinen die Regel, obwohl in einigen spezifischen Anwendungen (z. B. Baumwollentlaubung oder Malariakontrollprogramme) ein einziges Produkt verwendet werden kann.
Tabelle 1. Vergleich der Expositionseigenschaften bei der Herstellung und Verwendung von Pestiziden
|
Exposition gegenüber der Produktion |
Exposition bei der Verwendung |
|
|
Dauer der Exposition |
Kontinuierlich und verlängert |
Variabel und intermittierend |
|
Grad der Exposition |
Ziemlich konstant |
Extrem variabel |
|
Art der Exposition |
Zu einer oder wenigen Verbindungen |
Zu zahlreichen Verbindungen entweder nacheinander oder gleichzeitig |
|
Aufnahme durch die Haut |
Einfach zu kontrollieren |
Variabel je nach Arbeitsablauf |
|
Umgebungsüberwachung |
Nützlich |
Selten informativ |
|
Biologische Überwachung |
Ergänzend zur Umgebungsüberwachung |
Sehr nützlich, wenn verfügbar |
Quelle: WHO 1982a, modifiziert.
Die Messung biologischer Expositionsindikatoren ist besonders nützlich für Pestizidanwender, bei denen die herkömmlichen Techniken der Expositionsbewertung durch Überwachung der Umgebungsluft kaum anwendbar sind. Die meisten Pestizide sind fettlösliche Substanzen, die in die Haut eindringen. Das Auftreten einer perkutanen (Haut-)Absorption macht die Verwendung von biologischen Indikatoren sehr wichtig bei der Beurteilung des Expositionsniveaus unter diesen Umständen.
Organophosphat-Insektizide
Biologische Wirkungsindikatoren:
Cholinesterasen sind die Zielenzyme, die für die Toxizität von Organophosphaten (OP) gegenüber Insekten- und Säugetierspezies verantwortlich sind. Es gibt zwei Haupttypen von Cholinesterasen im menschlichen Organismus: Acetylcholinesterase (ACHE) und Plasmacholinesterase (PCHE). OP verursacht beim Menschen toxische Wirkungen durch die Hemmung der synaptischen Acetylcholinesterase im Nervensystem. Acetylcholinesterase kommt auch in roten Blutkörperchen vor, deren Funktion unbekannt ist. Plasmacholinesterase ist ein allgemeiner Begriff, der eine inhomogene Gruppe von Enzymen umfasst, die in Gliazellen, Plasma, Leber und einigen anderen Organen vorhanden sind. PCHE wird durch OPs gehemmt, aber seine Hemmung erzeugt keine bekannten funktionellen Störungen.
Die Hemmung der ACHE- und PCHE-Aktivität im Blut korreliert stark mit der Intensität und Dauer der OP-Exposition. Blut-ACHE, das dasselbe molekulare Ziel wie dasjenige ist, das für die akute OP-Toxizität im Nervensystem verantwortlich ist, ist ein spezifischerer Indikator als PCHE. Die Empfindlichkeit von Blut-ACHE und PCHE gegenüber OP-Hemmung variiert jedoch zwischen den einzelnen OP-Verbindungen: bei der gleichen Blutkonzentration hemmen einige mehr ACHE und andere mehr PCHE.
Es besteht eine vernünftige Korrelation zwischen der ACHE-Aktivität im Blut und den klinischen Anzeichen einer akuten Toxizität (Tabelle 2). Die Korrelation ist tendenziell besser, da die Hemmungsrate schneller ist. Wenn die Hemmung langsam eintritt, wie bei chronischen Expositionen auf niedrigem Niveau, kann die Korrelation mit Krankheit gering oder gar nicht vorhanden sein. Es muss beachtet werden, dass die Hemmung von Blut-ACHE keine Vorhersage für chronische oder verzögerte Wirkungen ist.
Tabelle 2. Schweregrad und Prognose der akuten OP-Toxizität bei verschiedenen Graden der ACHE-Hemmung
|
SCHMERZEN Hemmung (%) |
Mechanisierungsgrad Vergiftung |
Klinische Symptome |
Prognose |
|
50-60 |
Mild |
Schwäche, Kopfschmerzen, Schwindel, Übelkeit, Speichelfluss, Tränenfluss, Miosis, mäßiger Bronchialkrampf |
Rekonvaleszenz in 1-3 Tagen |
|
60-90 |
Moderat |
Plötzliche Schwäche, Sehstörungen, übermäßiger Speichelfluss, Schwitzen, Erbrechen, Durchfall, Bradykardie, Hypertonie, Zittern der Hände und des Kopfes, Gangstörungen, Miosis, Brustschmerzen, Zyanose der Schleimhäute |
Rekonvaleszenz in 1-2 Wochen |
|
90-100 |
Schwer |
Abruptes Zittern, generalisierte Krämpfe, psychische Störungen, intensive Zyanose, Lungenödem, Koma |
Tod durch Atem- oder Herzversagen |
Variationen der ACHE- und PCHE-Aktivitäten wurden bei gesunden Menschen und bei bestimmten physiopathologischen Zuständen beobachtet (Tabelle 3). Somit kann die Sensitivität dieser Tests bei der Überwachung der OP-Exposition erhöht werden, indem individuelle Präexpositionswerte als Referenz verwendet werden. Die Cholinesterase-Aktivitäten nach der Exposition werden dann mit den individuellen Ausgangswerten verglichen. Referenzwerte für die Populationscholinesteraseaktivität sollten nur verwendet werden, wenn die Cholinesterasespiegel vor der Exposition nicht bekannt sind (Tabelle 4).
Tabelle 3. Variationen der ACHE- und PCHE-Aktivitäten bei gesunden Menschen und bei ausgewählten physiopathologischen Zuständen
|
Anforderungen |
ACHE-Aktivität |
PCHE-Aktivität |
|
Gesunde Menschen |
||
|
Interindividuelle Variation1 |
10-18% |
15-25% |
|
Intraindividuelle Variation1 |
3-7% |
6% |
|
Geschlechtsunterschiede |
Nein |
10–15 % höher bei Männern |
|
Alter |
Bis 6 Monate reduziert |
|
|
Körpermasse |
Positive Korrelation |
|
|
Serum Cholesterin |
Positive Korrelation |
|
|
Saisonale Unterschiede |
Nein |
Nein |
|
Zirkadiane Variation |
Nein |
Nein |
|
Menstruation |
Verringert |
|
|
Schwangerschaft |
Verringert |
|
|
Pathologische Zustände |
||
|
Reduzierte Aktivität |
Leukämie, Neubildung |
Leber erkrankung; Urämie; Krebs; Herzfehler; allergische Reaktionen |
|
Erhöhte Aktivität |
Polyzythämie; Thalassämie; andere angeborene Blutdyskrasie |
Hyperthyreose; andere Zustände mit hoher Stoffwechselrate |
1 Quelle: Augustinsson 1955 und Gage 1967.
Tabelle 4. Mit ausgewählten Methoden gemessene Cholinesterase-Aktivitäten von gesunden Menschen ohne OP-Exposition
|
Versandart |
Geschlecht |
SCHMERZEN* |
PCE* |
|
Michel1 (DpH/h) |
männlich weiblich |
0.77 0.08 ± 0.75 0.08 ± |
0.95 0.19 ± 0.82 0.19 ± |
|
Titrimetrisch1 (mmol/min ml) |
männlich Weiblich |
13.2 0.31 ± |
4.90 0.02 ± |
|
Ellman ist modifiziert2 (UI/ml) |
männlich weiblich |
4.01 0.65 ± 3.45 0.61 ± |
3.03 0.66 ± 3.03 0.68 ± |
* Mittelwert, ± Standardabweichung.
Quelle: 1 Gesetze 1991. 2 Alciniet al. 1988.
Blutproben sollten vorzugsweise innerhalb von zwei Stunden nach der Exposition entnommen werden. Die Venenpunktion wird der Entnahme von Kapillarblut aus einem Finger oder Ohrläppchen vorgezogen, da die Entnahmestelle mit Pestiziden kontaminiert sein kann, die sich bei exponierten Personen auf der Haut befinden. Es werden drei aufeinanderfolgende Proben empfohlen, um für jeden Arbeiter vor der Exposition einen normalen Ausgangswert festzulegen (WHO 1982b).
Zur Bestimmung von ACHE und PCHE im Blut stehen mehrere Analysemethoden zur Verfügung. Als Referenzmethode soll laut WHO die spektrophotometrische Methode nach Ellman (Ellman et al. 1961) dienen.
Biologische Expositionsindikatoren.
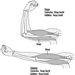
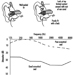
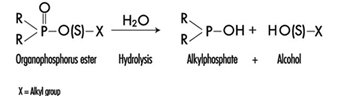
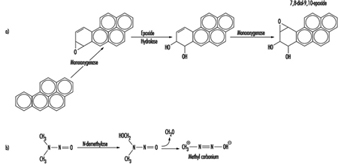
Die Bestimmung von Metaboliten im Urin, die von der Alkylphosphateinheit des OP-Moleküls stammen, oder von Rückständen, die durch die Hydrolyse der P-X-Bindung entstehen (Abbildung 1), wurde zur Überwachung der OP-Exposition verwendet.
Abbildung 1. Hydrolyse von OP-Insektiziden
Alkylphosphat-Metaboliten.
Die im Urin nachweisbaren Alkylphosphat-Metaboliten und die Hauptausgangsverbindung, von der sie abstammen können, sind in Tabelle 5 aufgeführt. Alkylphosphate im Urin sind empfindliche Indikatoren für die Exposition gegenüber OP-Verbindungen: Die Ausscheidung dieser Metaboliten im Urin ist normalerweise bei einer Expositionshöhe von nachweisbar welche Hemmung der Plasma- oder Erythrozyten-Cholinesterase nicht nachweisbar ist. Die Urinausscheidung von Alkylphosphaten wurde für verschiedene Expositionsbedingungen und für verschiedene OP-Verbindungen gemessen (Tabelle 6). Die Existenz einer Beziehung zwischen externen Dosen von OP und Alkylphosphat-Konzentrationen im Urin wurde in einigen Studien festgestellt. In einigen Studien wurde auch ein signifikanter Zusammenhang zwischen Cholinesterase-Aktivität und Alkylphosphatspiegeln im Urin nachgewiesen.
Tabelle 5. Im Urin nachweisbare Alkylphosphate als Metaboliten von OP-Pestiziden
|
Metabolite |
Abkürzung |
Hauptstammverbindungen |
|
Monomethylphosphat |
MMP |
Malathion, Parathion |
|
Dimethylphosphat |
DMP |
Dichlorvos, Trichlorfon, Mevinphos, Malaoxon, Dimethoat, Fenchlorphos |
|
Diethylphosphat |
DEP |
Paraoxon, Demeton-Oxon, Diazinon-Oxon, Dichlorfenthion |
|
Dimethylthiophosphat |
DMTP |
Fenitrothion, Fenchlorphos, Malathion, Dimethoat |
|
Diethylthiophosphat |
DETP |
Diazinon, Demethon, Parathion, Fenchlorphos |
|
Dimethyldithiophosphat |
DMDTP |
Malathion, Dimethoat, Azinphos-methyl |
|
Diethyldithiophosphat |
DEDTP |
Disulfoton, Phorat |
|
Phenylphosphorsäure |
Leptophos, EPN |
Tabelle 6. Beispiele für Konzentrationen von Alkylphosphaten im Urin, gemessen unter verschiedenen OP-Expositionsbedingungen
|
Compounds |
Bedingung der Exposition |
Expositionsweg |
Metabolitenkonzentrationen1 (mg/L) |
|
Parathion2 |
Nicht tödliche Vergiftung |
Mündlich |
DEP = 0.5 DETP = 3.9 |
|
Disulfoton2 |
Formulierer |
Dermal/Inhalation |
DEP = 0.01-4.40 DETP = 0.01–1.57 DEDTP = <0.01-05 |
|
Phorate2 |
Formulierer |
Dermal/Inhalation |
DEP = 0.02-5.14 DETP = 0.08–4.08 DEDTP = <0.01–0.43 |
|
Malathion3 |
Pflanzenschutzspritzen |
dermal |
DMDTP = <0.01 |
|
Fenitrothion3 |
Pflanzenschutzspritzen |
dermal |
DMP = 0.01-0.42 DMTP = 0.02–0.49 |
|
Monocrotophos4 |
Pflanzenschutzspritzen |
Dermal/Inhalation |
DMP = < 0.04–6.3/24 h |
1 Abkürzungen siehe Tabelle 27.12 [BMO12TE].
2 Dillon und Ho 1987.
3 Richter 1993.
4 van Sittert und Dumas 1990.
Alkylphosphate werden in der Regel innerhalb kurzer Zeit mit dem Urin ausgeschieden. Zur Metabolitenbestimmung eignen sich Proben, die kurz nach Feierabend entnommen werden.
Die Messung von Alkylphosphaten im Urin erfordert ein ziemlich ausgeklügeltes analytisches Verfahren, basierend auf der Derivatisierung der Verbindungen und dem Nachweis durch Gas-Flüssigkeits-Chromatographie (Shafik et al. 1973a; Reid und Watts 1981).
Hydrolyserückstände.
p-Nitrophenol (PNP) ist der phenolische Metabolit von Parathion, Methylparathion und Ethylparathion, EPN. Die Messung von PNP im Urin (Cranmer 1970) ist weit verbreitet und hat sich bei der Bewertung der Exposition gegenüber Parathion als erfolgreich erwiesen. PNP im Urin korreliert gut mit der absorbierten Dosis von Parathion. Bei PNP-Konzentrationen im Urin von bis zu 2 mg/l verursacht die Resorption von Parathion keine Symptome, und es wird eine geringe oder keine Verringerung der Cholinesterase-Aktivitäten beobachtet. Die Ausscheidung von PNP erfolgt schnell und die PNP-Spiegel im Urin werden 48 Stunden nach der Exposition unbedeutend. Daher sollten Urinproben bald nach der Exposition gesammelt werden.
Carbamate
Biologische Wirkungsindikatoren.
Carbamat-Pestizide umfassen Insektizide, Fungizide und Herbizide. Die Toxizität von insektiziden Carbamaten beruht auf der Hemmung von synaptischem Schmerz, während bei herbiziden und fungiziden Carbamaten andere Toxizitätsmechanismen beteiligt sind. Somit kann nur die Exposition gegenüber Carbamat-Insektiziden durch den Assay der Cholinesterase-Aktivität in roten Blutkörperchen (ACHE) oder Plasma (PCHE) überwacht werden. ACHE ist normalerweise empfindlicher gegenüber Carbamat-Inhibitoren als PCHE. Cholinerge Symptome wurden gewöhnlich bei Carbamat-exponierten Arbeitern mit einer ACHE-Aktivität im Blut von weniger als 70 % des individuellen Ausgangswertes beobachtet (WHO 1982a).
Die Hemmung von Cholinesterasen durch Carbamate ist schnell reversibel. Daher können falsch negative Ergebnisse erhalten werden, wenn zwischen Exposition und biologischer Probenahme oder zwischen Probenahme und Analyse zu viel Zeit vergeht. Um solche Probleme zu vermeiden, wird empfohlen, Blutproben innerhalb von vier Stunden nach der Exposition zu entnehmen und zu analysieren. Den Analysemethoden, die die Bestimmung der Cholinesterase-Aktivität unmittelbar nach der Blutentnahme ermöglichen, ist der Vorzug zu geben, wie für Organophosphate diskutiert.
Biologische Expositionsindikatoren.
Die Messung der Urinausscheidung von Carbamat-Metaboliten als Methode zur Überwachung der Exposition des Menschen wurde bisher nur auf wenige Verbindungen und in begrenzten Studien angewendet. Tabelle 7 fasst die relevanten Daten zusammen. Da Carbamate zeitnah mit dem Urin ausgeschieden werden, eignen sich zeitnah nach Expositionsende entnommene Proben zur Metabolitenbestimmung. Analytische Verfahren zur Messung von Carbamat-Metaboliten im Urin wurden von Dawson et al. (1964); DeBernardinis und Wargin (1982) und Verberk et al. (1990).
Tabelle 7. In Feldstudien gemessene Konzentrationen von Carbamat-Metaboliten im Urin
|
Compounds |
Biologische Kennzahl |
Bedingung der Exposition |
Umweltkonzentrationen |
Die Ergebnisse |
Bibliographie |
|
Carbaryl |
a-Naphthol a-Naphthol a-Naphthol |
Formulierer Mischer/Applikatoren nicht exponierte Bevölkerung |
0.23–0.31 mg/mXNUMX3 |
x = 18.5 mg/l1 , max. Ausscheidungsrate = 80 mg/Tag x = 8.9 mg/l, Bereich = 0.2–65 mg/l Bereich = 1.5–4 mg/l |
WER 1982a |
|
Pirimicarb |
Metaboliten I2 und V3 |
Applikatoren |
Bereich = 1–100 mg/l |
Verberk et al. 1990 |
1 Systemische Vergiftungen wurden gelegentlich berichtet.
2 2-Dimethylamino-4-hydroxy-5,6-dimethylpyrimidin.
3 2-Methylamino-4-hydroxy-5,6-dimethylpyrimidin.
x = Standardabweichung.
Dithiocarbamate
Biologische Expositionsindikatoren.
Dithiocarbamate (DTC) sind weit verbreitete Fungizide, die chemisch in drei Klassen eingeteilt werden: Thiurame, Dimethyldithiocarbamate und Ethylen-bis-dithiocarbamate.
Schwefelkohlenstoff (CS2) und sein Hauptmetabolit 2-Thiothiazolidin-4-Carbonsäure (TTCA) sind Metaboliten, die fast allen DTC gemeinsam sind. Ein signifikanter Anstieg der Urinkonzentrationen dieser Verbindungen wurde bei verschiedenen Expositionsbedingungen und bei verschiedenen DTC-Pestiziden beobachtet. Ethylenthioharnstoff (ETU) ist ein wichtiger Harnmetabolit von Ethylen-bis-dithiocarbamaten. Es kann auch als Verunreinigung in Marktformulierungen vorhanden sein. Da festgestellt wurde, dass ETU bei Ratten und anderen Arten teratogen und karzinogen ist und mit Schilddrüsentoxizität in Verbindung gebracht wurde, wurde es in großem Umfang zur Überwachung der Ethylen-bis-dithiocarbamat-Exposition eingesetzt. ETU ist nicht verbindungsspezifisch, da es von Maneb, Mancozeb oder Zineb abgeleitet sein kann.
Die Messung der im DTC vorhandenen Metalle wurde als alternativer Ansatz zur Überwachung der DTC-Exposition vorgeschlagen. Bei Mancozeb-exponierten Arbeitern wurde eine erhöhte Manganausscheidung im Urin beobachtet (Tabelle 8).
Tabelle 8. In Feldstudien gemessene Konzentrationen von Dithiocarbamat-Metaboliten im Urin
|
Compounds |
Biologische Kennzahl |
Zustand von Belichtung |
Umweltkonzentrationen* ± Standardabweichung |
Ergebnisse ± Standardabweichung |
Bibliographie |
|
Ziram |
Schwefelkohlenstoff (CS2) TTCA1 |
Formulierer Formulierer |
1.03 ± 0.62 mg/mXNUMX3 |
3.80 ± 3.70 mg/l 0.45 ± 0.37 mg/l |
Maroniet al. 1992 |
|
Maneb/Mancozeb |
ETU2 |
Applikatoren |
Bereich = < 0.2–11.8 mg/l |
Kurttio et al. 1990 |
|
|
Mancozeb |
Mangan |
Applikatoren |
57.2 mg/m3 |
Präexposition: 0.32 ± 0.23 mg/g Kreatinin; nach Exposition: 0.53 ± 0.34 mg/g Kreatinin |
Canossaet al. 1993 |
* Mittleres Ergebnis nach Maroni et al. 1992.
1 TTCA = 2-Thiothiazolidin-4-Carbonsäure.
2 ETU = Ethylenthioharnstoff.
CS2, TTCA und Mangan werden häufig im Urin nicht exponierter Personen gefunden. Daher wird die Messung der Urinspiegel dieser Verbindungen vor der Exposition empfohlen. Urinproben sollten morgens nach Beendigung der Exposition gesammelt werden. Analytische Methoden für die Messung von CS2, TTCA und ETU wurden von Maroni et al. (1992).
Synthetische Pyrethroide
Biologische Expositionsindikatoren.
Synthetische Pyrethroide sind den natürlichen Pyrethrinen ähnliche Insektizide. Metaboliten im Urin, die für die Anwendung bei der biologischen Expositionsüberwachung geeignet sind, wurden durch Studien mit freiwilligen Probanden identifiziert. Der saure Metabolit 3-(2,2'-Dichlor-vinyl)-2,2'-dimethyl-cyclopropancarbonsäure (Cl2CA) wird sowohl von Personen ausgeschieden, denen Permethrin und Cypermethrin oral verabreicht wurden, als auch von dem Bromanalog (Br2CA) von mit Deltamethrin behandelten Probanden. Bei den mit Cypermethrin behandelten Probanden wurde auch ein Phenoxymetabolit, 4-Hydroxyphenoxybenzoesäure (4-HPBA), identifiziert. Diese Tests wurden jedoch wegen der erforderlichen komplexen Analysetechniken nicht oft zur Überwachung beruflicher Expositionen eingesetzt (Eadsforth, Bragt und van Sittert 1988; Kolmodin-Hedman, Swensson und Akerblom 1982). Bei Anwendern, die Cypermethrin ausgesetzt waren, lagen die Urinspiegel von Cl2Es wurde festgestellt, dass CA im Bereich von 0.05 bis 0.18 mg/l liegt, während bei Formulierern, die a-Cypermethrin ausgesetzt waren, 4-HPBA-Konzentrationen im Urin unter 0.02 mg/l liegen.
Für Metabolitenbestimmungen wird eine 24-stündige Urinsammelperiode empfohlen, die nach Expositionsende beginnt.
Organochlore
Biologische Expositionsindikatoren.
Organochlorinsektizide (OC) wurden in den 1950er und 1960er Jahren weit verbreitet eingesetzt. Anschließend wurde die Verwendung vieler dieser Verbindungen in vielen Ländern wegen ihrer Persistenz und der daraus resultierenden Kontamination der Umwelt eingestellt.
Ein biologisches Monitoring der OC-Exposition kann durch die Bestimmung von intakten Pestiziden oder deren Metaboliten im Blut oder Serum erfolgen (Dale, Curley und Cueto 1966; Barquet, Morgade und Pfaffenberger 1981). Nach der Resorption wird Aldrin schnell zu Dieldrin metabolisiert und kann als Dieldrin im Blut gemessen werden. Endrin hat im Blut eine sehr kurze Halbwertszeit. Daher ist die Endrin-Blutkonzentration nur zur Bestimmung der jüngsten Expositionswerte von Nutzen. Auch die Bestimmung des Urinmetaboliten Anti-12-hydroxy-endrin hat sich zur Überwachung der Endrin-Exposition bewährt (van Sittert und Tordoir 1987) .
Für einige OC-Verbindungen wurden signifikante Korrelationen zwischen der Konzentration biologischer Indikatoren und dem Einsetzen toxischer Wirkungen nachgewiesen. Fälle von Toxizität aufgrund einer Aldrin- und Dieldrin-Exposition wurden mit Dieldrin-Konzentrationen im Blut über 200 μg/l in Verbindung gebracht. Als oberer kritischer Wert für neurologische Symptome wurde eine Lindankonzentration im Blut von 20 µg/l angegeben. Bei Arbeitern mit Blutendrinkonzentrationen unter 50 μg/l wurden keine akuten Nebenwirkungen berichtet. Das Fehlen früher Nebenwirkungen (Induktion von mikrosomalen Leberenzymen) wurde bei wiederholter Exposition gegenüber Endrin bei anti-12-Hydroxy-Endrin-Konzentrationen im Urin unter 130 μg/g Kreatinin und bei wiederholter Exposition gegenüber DDT bei DDT- oder DDE-Serumkonzentrationen unter 250 gezeigt μg/l.
OC kann in geringen Konzentrationen im Blut oder Urin der Allgemeinbevölkerung gefunden werden. Beispiele für beobachtete Werte sind: Lindan-Blutkonzentrationen bis 1 μg/l, Dieldrin bis 10 μg/l, DDT oder DDE bis 100 μg/l und Anti-12-hydroxy-endrin bis 1 μg/g Kreatinin. Daher wird eine Ausgangsbeurteilung vor der Exposition empfohlen.
Bei exponierten Personen sollten Blutproben unmittelbar nach dem Ende einer einzelnen Exposition entnommen werden. Bei Langzeitexposition ist der Zeitpunkt der Entnahme der Blutprobe nicht kritisch. Am Ende der Exposition sollten Urinproben zur Metabolitenbestimmung im Urin entnommen werden.
Triazine
Biologische Expositionsindikatoren.
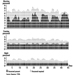
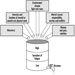
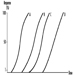
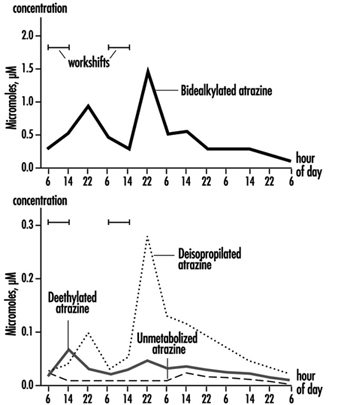
Die Messung der Urinausscheidung von Triazin-Metaboliten und der unmodifizierten Ausgangsverbindung wurde in begrenzten Studien an Probanden durchgeführt, die Atrazin ausgesetzt waren. Abbildung 2 zeigt die Ausscheidungsprofile von Atrazin-Metaboliten im Urin eines Arbeiters in der Produktion mit einer dermalen Exposition gegenüber Atrazin im Bereich von 174 bis 275 μmol/Arbeitsschicht (Catenacci et al. 1993). Da andere Chlortriazine (Simazin, Propazin, Terbuthylazin) dem gleichen Biotransformationsweg wie Atrazin folgen, können die Konzentrationen von dealkylierten Triazin-Metaboliten bestimmt werden, um die Exposition gegenüber allen Chlortriazin-Herbiziden zu überwachen.
Abbildung 2. Urinausscheidungsprofile von Atrazin-Metaboliten
Die Bestimmung nicht modifizierter Verbindungen im Urin kann als qualitative Bestätigung der Art der Verbindung, die die Exposition verursacht hat, nützlich sein. Für die Metabolitenbestimmung wird eine 24-Stunden-Urinsammelperiode empfohlen, die zu Beginn der Exposition beginnt.
Kürzlich wurde unter Verwendung eines enzymgebundenen Immunadsorptionstests (ELISA-Test) ein Mercaptursäurekonjugat von Atrazin als sein Hauptmetabolit im Urin bei exponierten Arbeitern identifiziert. Diese Verbindung wurde in Konzentrationen gefunden, die mindestens zehnmal höher sind als die aller dealkylierten Produkte. Ein Zusammenhang zwischen der kumulativen dermalen und inhalativen Exposition und der Gesamtmenge des über einen Zeitraum von 10 Tagen ausgeschiedenen Mercaptursäure-Konjugats wurde beobachtet (Lucas et al. 10).
Cumarin-Derivate
Biologische Wirkungsindikatoren.
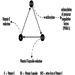
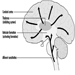
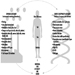
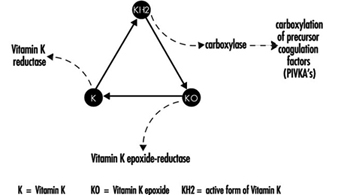
Cumarin-Rodentizide hemmen die Aktivität der Enzyme des Vitamin-K-Zyklus in der Leber von Säugetieren einschließlich des Menschen (Abbildung 3) und bewirken so eine dosisabhängige Verringerung der Synthese von Vitamin-K-abhängigen Gerinnungsfaktoren, nämlich Faktor II (Prothrombin) , VII, IX und X. Antikoagulatorische Wirkungen treten auf, wenn die Plasmaspiegel der Gerinnungsfaktoren unter etwa 20 % des Normalwerts gefallen sind.
Abbildung 3. Vitamin-K-Zyklus
Diese Vitamin-K-Antagonisten wurden in Verbindungen der sogenannten „ersten Generation“ (z. B. Warfarin) und der „zweiten Generation“ (z. B. Brodifacoum, Difenacoum) eingeteilt, wobei letztere durch eine sehr lange biologische Halbwertszeit (100 bis 200 Tage) gekennzeichnet sind ).
Die Bestimmung der Prothrombinzeit wird häufig zur Überwachung der Exposition gegenüber Cumarinen verwendet. Dieser Test reagiert jedoch nur auf eine Abnahme des Gerinnungsfaktors um etwa 20 % der normalen Plasmaspiegel. Der Test ist nicht geeignet, um frühe Wirkungen einer Exposition zu erkennen. Zu diesem Zweck wird die Bestimmung der Prothrombinkonzentration im Plasma empfohlen.
Diese Tests könnten in Zukunft durch die Bestimmung von Gerinnungsfaktorvorläufern (PIVKA) ersetzt werden, also Substanzen, die nur bei einer Blockade des Vitamin-K-Kreislaufs durch Cumarine im Blut nachweisbar sind.
Bei längerer Exposition ist der Zeitpunkt der Blutentnahme nicht kritisch. Bei akuter Überexposition sollte wegen der Latenz der gerinnungshemmenden Wirkung ein biologisches Monitoring für mindestens fünf Tage nach dem Ereignis durchgeführt werden. Um die Sensitivität dieser Tests zu erhöhen, wird die Messung der Ausgangswerte vor der Exposition empfohlen.
Biologische Expositionsindikatoren.
Die Messung von unmodifizierten Cumarinen im Blut wurde als Test zur Überwachung der menschlichen Exposition vorgeschlagen. Die Erfahrung mit der Anwendung dieser Indizes ist jedoch sehr begrenzt, hauptsächlich weil die analytischen Techniken viel komplexer (und weniger standardisiert) sind im Vergleich zu denen, die zur Überwachung der Auswirkungen auf das Gerinnungssystem erforderlich sind (Chalermchaikit, Felice und Murphy 1993).
Phenoxy-Herbizide
Biologische Expositionsindikatoren.
Phenoxy-Herbizide werden in Säugetieren kaum biotransformiert. Beim Menschen werden mehr als 95 % einer Dosis von 2,4-Dichlorphenoxyessigsäure (2,4-D) innerhalb von fünf Tagen unverändert im Urin ausgeschieden, und 2,4,5-Trichlorphenoxyessigsäure (2,4,5-T) und 4-Chlor-2-methylphenoxyessigsäure (MCPA) werden innerhalb weniger Tage nach oraler Aufnahme ebenfalls größtenteils unverändert über den Urin ausgeschieden. Die Messung unveränderter Verbindungen im Urin wurde zur Überwachung der beruflichen Exposition gegenüber diesen Herbiziden angewendet. In Feldstudien wurden Werte im Urin von exponierten Arbeitern im Bereich von 0.10 bis 8 μg/l für 2,4-D, von 0.05 bis 4.5 μg/l für 2,4,5-T und von unter 0.1 μg/l gefunden auf 15 μg/l für MCPA. Für die Bestimmung unveränderter Verbindungen wird eine 24-stündige Urinsammlung ab Expositionsende empfohlen. Analytische Verfahren zur Messung von Phenoxy-Herbiziden im Urin wurden von Draper (1982) beschrieben.
Quartäre Ammoniumverbindungen
Biologische Expositionsindikatoren.
Diquat und Paraquat sind vom menschlichen Organismus kaum biotransformierbare Herbizide. Aufgrund ihrer hohen Wasserlöslichkeit werden sie ohne Weiteres unverändert im Urin ausgeschieden. Bei Paraquat-exponierten Arbeitern wurden häufig Urinkonzentrationen unterhalb der analytischen Nachweisgrenze (0.01 μg/l) beobachtet; während in tropischen Ländern nach unsachgemäßem Umgang mit Paraquat Konzentrationen bis zu 0.73 μg/l gemessen wurden. Diquat-Konzentrationen im Urin unter der analytischen Nachweisgrenze (0.047 μg/l) wurden bei Personen mit dermaler Exposition von 0.17 bis 1.82 μg/h und inhalativer Exposition von weniger als 0.01 μg/h berichtet. Idealerweise sollte eine 24-Stunden-Urinprobenahme am Ende der Exposition für die Analyse verwendet werden. Wenn dies nicht praktikabel ist, kann eine Stichprobe am Ende des Arbeitstages verwendet werden.
Die Bestimmung des Paraquat-Spiegels im Serum ist für prognostische Zwecke im Falle einer akuten Vergiftung nützlich: Patienten mit Serum-Paraquat-Spiegeln von bis zu 0.1 μg/l XNUMX Stunden nach der Einnahme werden wahrscheinlich überleben.
Die analytischen Methoden zur Bestimmung von Paraquat und Diquat wurden von Summers (1980) zusammengefasst.
Verschiedene Pestizide
4,6-Dinitro-o-kresol (DNOC).
DNOC ist ein Herbizid, das 1925 eingeführt wurde, aber die Verwendung dieser Verbindung wurde aufgrund ihrer hohen Toxizität für Pflanzen und Menschen zunehmend verringert. Da die Blut-DNOC-Konzentrationen bis zu einem gewissen Grad mit der Schwere gesundheitlicher Beeinträchtigungen korrelieren, wurde die Messung von unverändertem DNOC im Blut zur Überwachung beruflicher Expositionen und zur Beurteilung des klinischen Verlaufs von Vergiftungen vorgeschlagen.
Pentachlorphenol.
Pentachlorphenol (PCP) ist ein Breitbandbiozid mit pestizider Wirkung gegen Unkräuter, Insekten und Pilze. Messungen von unverändertem PCP im Blut oder Urin wurden als geeignete Indizes zur Überwachung beruflicher Expositionen empfohlen (Colosio et al. 1993), da diese Parameter signifikant mit der PCP-Körperbelastung korrelieren. Bei Arbeitern mit längerer PCP-Exposition ist der Zeitpunkt der Blutentnahme nicht kritisch, während Urinfleckproben am Morgen nach der Exposition entnommen werden sollten.
Eine Methode mit mehreren Rückständen zur Messung von halogenierten und nitrophenolischen Pestiziden wurde von Shafik et al. (1973b) beschrieben.
Andere Tests, die für die biologische Überwachung der Pestizidexposition vorgeschlagen werden, sind in Tabelle 9 aufgeführt.
Tabelle 9. Andere in der Literatur vorgeschlagene Indizes für die biologische Überwachung der Pestizidexposition
|
Compounds |
Biologische Kennzahl |
|
|
Urin |
Blut |
|
|
Bromophos |
Bromophos |
Bromophos |
|
Captan |
Tetrahydrophthalimid |
|
|
Carbofuran |
3-Hydroxycarbofuran |
|
|
Chlordimeform |
4-Chlor-o-Toluidinderivate |
|
|
Chlorbenzilat |
p,p-1-Dichlorbenzophenon |
|
|
Dichlorpropen |
Mercaptursäure-Metabolite |
|
|
Fenitrothion |
p-Nitrokresol |
|
|
Ferbam |
Thirami |
|
|
Fluazifop-Butyl |
Fluazifop |
|
|
Flufenoxuron |
Flufenoxuron |
|
|
Glyphosat |
Glyphosat |
|
|
Malathion |
Malathion |
Malathion |
|
Organozinnverbindungen |
Zinn |
Zinn |
|
Trifenomorph |
Morpholin, Triphenylcarbinol |
|
|
Ziram |
Thirami |
|
Schlussfolgerungen
Biologische Indikatoren zur Überwachung der Pestizidexposition wurden in einer Reihe von experimentellen und Feldstudien angewendet.
Einige Tests, wie die für Cholinesterase im Blut oder für ausgewählte unmodifizierte Pestizide im Urin oder Blut, wurden durch umfangreiche Erfahrung validiert. Für diese Tests wurden Grenzwerte für die biologische Exposition vorgeschlagen (Tabelle 10). Andere Tests, insbesondere solche für Metabolite aus Blut oder Urin, unterliegen größeren Einschränkungen aufgrund von analytischen Schwierigkeiten oder aufgrund von Einschränkungen bei der Interpretation der Ergebnisse.
Tabelle 10. Empfohlene biologische Grenzwerte (Stand 1996)
|
Compounds |
Biologische Kennzahl |
BEI1 |
BAT2 |
HBBL3 |
BLV4 |
|
ACHE-Hemmer |
SCHMERZ im Blut |
70% |
70% |
70%, |
|
|
DNOC |
DNOC im Blut |
20mg/l, |
|||
|
Lindan |
Lindan im Blut |
0.02mg / l |
0.02mg / l |
||
|
Parathion |
PNP im Urin |
0.5mg / l |
0.5mg / l |
||
|
Pentachlorphenol (PCP) |
PCP im Urin PCP im Plasma |
2 mg / l 5 mg / l |
0.3mg / l 1 mg / l |
||
|
Dieldrin/Aldrin |
Dieldrin im Blut |
100 mg / l |
|||
|
Endrin |
Anti-12-Hydroxy-Endrin im Urin |
130 mg / l |
|||
|
DDT |
DDT- und DDEin-Serum |
250 mg / l |
|||
|
Cumarine |
Prothrombinzeit im Plasma Prothrombinkonzentration im Plasma |
10 % über dem Ausgangswert 60 % der Basis |
|||
|
MCPA |
MCPA im Urin |
0.5 mg / l |
|||
|
2,4-D |
2,4-D im Urin |
0.5 mg / l |
1 Biologische Expositionsindizes (BEIs) werden von der American Conference of Governmental Industrial Hygienists (ACGIH 1995) empfohlen.
2 Biologische Toleranzwerte (BVT) werden von der Deutschen Kommission zur Untersuchung gesundheitsgefährdender Arbeitsstoffe (DFG 1992) empfohlen.
3 Health-based Biological Limits (HBBLs) werden von einer WHO-Studiengruppe empfohlen (WHO 1982a).
4 Biologische Grenzwerte (BLVs) werden von einer Studiengruppe des Wissenschaftlichen Ausschusses für Pestizide der Internationalen Kommission für Arbeitsmedizin vorgeschlagen (Tordoir et al. 1994). Wird dieser Wert überschritten, ist eine Bewertung der Arbeitsbedingungen erforderlich.
Dieser Bereich befindet sich in einer rasanten Entwicklung, und angesichts der enormen Bedeutung der Verwendung biologischer Indikatoren zur Bewertung der Exposition gegenüber diesen Stoffen werden ständig neue Tests entwickelt und validiert.
Epidemiologische Methode für Arbeitssicherheit und Gesundheitsschutz
Epidemiologie
Die Epidemiologie ist sowohl als wissenschaftliche Grundlage der Präventivmedizin als auch als Grundlage für den Prozess der öffentlichen Gesundheitspolitik anerkannt. Es wurden mehrere operative Definitionen der Epidemiologie vorgeschlagen. Die einfachste ist, dass Epidemiologie die Untersuchung des Auftretens von Krankheiten oder anderen gesundheitsbezogenen Merkmalen in Menschen- und Tierpopulationen ist. Epidemiologen untersuchen nicht nur die Häufigkeit von Krankheiten, sondern ob sich die Häufigkeit zwischen Personengruppen unterscheidet; dh sie untersuchen die Ursache-Wirkungs-Beziehung zwischen Exposition und Krankheit. Krankheiten treten nicht zufällig auf; sie haben Ursachen – sehr oft menschengemachte Ursachen – die vermeidbar sind. So könnten viele Krankheiten verhindert werden, wenn die Ursachen bekannt wären. Die Methoden der Epidemiologie waren entscheidend für die Identifizierung vieler ursächlicher Faktoren, die wiederum zu einer Gesundheitspolitik geführt haben, die darauf abzielt, Krankheiten, Verletzungen und vorzeitigen Tod zu verhindern.
Welche Aufgabe hat die Epidemiologie und wo liegen ihre Stärken und Schwächen, wenn Definitionen und Konzepte der Epidemiologie auf den betrieblichen Gesundheitsschutz übertragen werden? Dieses Kapitel befasst sich mit diesen Fragen und den Möglichkeiten, wie arbeitsbedingte Gesundheitsgefahren mit epidemiologischen Methoden untersucht werden können. Dieser Artikel stellt die Ideen vor, die in aufeinanderfolgenden Artikeln in diesem Kapitel zu finden sind.
Berufsepidemiologie
Berufsepidemiologie ist definiert als die Untersuchung der Auswirkungen von Expositionen am Arbeitsplatz auf die Häufigkeit und Verbreitung von Krankheiten und Verletzungen in der Bevölkerung. Sie ist damit eine expositionsorientierte Disziplin mit Bezügen sowohl zur Epidemiologie als auch zur Arbeitsmedizin (Checkoway et al. 1989). Als solche verwendet sie Methoden, die denen der Epidemiologie im Allgemeinen ähneln.
Das Hauptziel der Arbeitsepidemiologie ist die Prävention durch die Ermittlung der gesundheitlichen Folgen von Expositionen am Arbeitsplatz. Dies unterstreicht den präventiven Fokus der Arbeitsepidemiologie. Tatsächlich sollte jede Forschung auf dem Gebiet des Arbeitsschutzes präventiven Zwecken dienen. Daher kann und sollte epidemiologisches Wissen leicht umsetzbar sein. Während das Interesse der öffentlichen Gesundheit immer das Hauptanliegen der epidemiologischen Forschung sein sollte, können Interessengruppen Einfluss nehmen, und es muss darauf geachtet werden, diesen Einfluss auf die Formulierung, Durchführung und/oder Interpretation von Studien zu minimieren (Soskolne 1985; Soskolne 1989).
Ein zweites Ziel der Berufsepidemiologie ist es, Ergebnisse aus spezifischen Settings zu nutzen, um Gefährdungen in der Bevölkerung insgesamt zu reduzieren oder zu eliminieren. Daher spielen die Ergebnisse aus berufsepidemiologischen Studien nicht nur Informationen über die gesundheitlichen Auswirkungen von Expositionen am Arbeitsplatz, sondern auch eine Rolle bei der Einschätzung des Risikos, das mit denselben Expositionen verbunden ist, jedoch auf dem niedrigeren Niveau, das die allgemeine Bevölkerung allgemein erfährt. Umweltverschmutzung durch industrielle Prozesse und Produkte würde normalerweise zu geringeren Expositionsniveaus führen als am Arbeitsplatz.
Die Anwendungsebenen der Berufsepidemiologie sind:
- Überwachung, um das Auftreten von Krankheiten in verschiedenen Kategorien von Arbeitnehmern zu beschreiben und so Frühwarnsignale für unerkannte Berufsgefahren zu liefern
- Generierung und Prüfung einer Hypothese, dass eine bestimmte Exposition schädlich sein kann, und die Quantifizierung einer Wirkung
- Bewertung einer Intervention (z. B. einer vorbeugenden Maßnahme wie der Reduzierung von Expositionswerten) durch Messung der Veränderungen des Gesundheitszustands einer Bevölkerung im Laufe der Zeit.
Die ursächliche Rolle, die berufsbedingte Expositionen bei der Entstehung von Krankheiten, Verletzungen und vorzeitigem Tod spielen können, wurde schon vor langer Zeit erkannt und ist Teil der Geschichte der Epidemiologie. Hinzuweisen ist auf Bernardino Ramazzini, Begründer der Arbeitsmedizin und einer der ersten, der die hippokratische Tradition der Abhängigkeit der Gesundheit von identifizierbaren natürlichen äußeren Faktoren wiederbelebte und ergänzte. Im Jahr 1700 schrieb er in seinem „De Morbis Artificum Diatriba“ (Ramazzini 1705; Saracci 1995):
Der Arzt muss den Patienten viele Fragen stellen. Hippokrates erklärt in De Affectionibus: „Wenn Sie einem Kranken gegenüberstehen, sollten Sie ihn fragen, woran er leidet, aus welchem Grund, seit wie vielen Tagen, was er isst und wie sein Stuhlgang ist. Zu all diesen Fragen sollte noch eine hinzugefügt werden: ‚Welche Arbeit macht er?‘.“
Dieses Wiedererwachen der klinischen Beobachtung und der Aufmerksamkeit für die Umstände des Auftretens von Krankheiten veranlasste Ramazzini, viele Berufskrankheiten zu identifizieren und zu beschreiben, die später von Arbeitsmedizinern und Epidemiologen untersucht wurden.
Mit diesem Ansatz berichtete Pott erstmals 1775 (Pott 1775) über die mögliche Verbindung zwischen Krebs und Beruf (Clayson 1962). Seine Beobachtungen zum Hodensackkrebs bei Schornsteinfegern begannen mit einer Beschreibung der Krankheit und setzten sich fort:
Das Schicksal dieser Menschen scheint einzigartig hart: In ihrer frühen Kindheit werden sie am häufigsten mit großer Brutalität behandelt und vor Kälte und Hunger fast ausgehungert; sie werden in enge und manchmal heiße Schornsteine geschoben, wo sie verletzt, verbrannt und fast erstickt werden; und wenn sie die Pubertät erreichen, werden sie besonders anfällig für eine höchst lästige, schmerzhafte und tödliche Krankheit.
Über diesen letzten Umstand gibt es nicht den geringsten Zweifel, obgleich vielleicht nicht ausreichend darauf geachtet wurde, um ihn allgemein bekannt zu machen. Andere Menschen haben Krebs der gleichen Teile; und so haben andere, außer Bleiarbeitern, die Poitou-Kolik und die daraus resultierende Lähmung; aber es ist dennoch eine Krankheit, für die sie besonders anfällig sind; und Schornsteinfeger zu Hoden- und Hodenkrebs.
Die Krankheit scheint bei diesen Menschen ihren Ursprung in einer Rußablagerung in der Hodensackfalte zu haben und zunächst keine Gewohnheitskrankheit zu sein … aber hier sind die Probanden jung, im Allgemeinen zumindest bei guter Gesundheit zunaechst; die Krankheit, die ihnen durch ihren Beruf zugefügt wurde, und aller Wahrscheinlichkeit nach lokal; welcher letzte Umstand kann, denke ich, ziemlich davon ausgegangen werden, dass er immer dieselben Teile ergreift; All dies macht es (zunächst) zu einem ganz anderen Fall als ein Krebs, der bei einem älteren Mann auftritt.
Dieser erste Bericht über einen Berufskrebs bleibt immer noch ein Musterbeispiel an Klarheit. Die Art der Krankheit, der betroffene Beruf und der wahrscheinliche Erreger sind klar definiert. Es wird eine erhöhte Inzidenz von Hodenkrebs bei Schornsteinfegern festgestellt, obwohl keine quantitativen Daten zur Untermauerung dieser Behauptung vorgelegt werden.
Weitere fünfzig Jahre vergingen, bis Ayrton-Paris 1822 (Ayrton-Paris 1822) die häufige Entwicklung von Hodenkrebs bei den Kupfer- und Zinnhütten von Cornwall bemerkte und vermutete, dass Arsendämpfe die Ursache sein könnten. Von Volkmann berichtete 1874 von Hauttumoren bei Paraffinarbeitern in Sachsen, und kurz darauf schlug Bell 1876 vor, dass Schieferöl für Hautkrebs verantwortlich sei (Von Volkmann 1874; Bell 1876). Berichte über die berufliche Entstehung von Krebs wurden dann relativ häufiger (Clayson 1962).
Zu den frühen Beobachtungen von Berufskrankheiten gehörte das vermehrte Auftreten von Lungenkrebs bei Schneeberger Bergleuten (Harting und Hesse 1879). Es ist bemerkenswert (und tragisch), dass eine aktuelle Fallstudie zeigt, dass die Lungenkrebsepidemie in Schneeberg mehr als ein Jahrhundert nach der ersten Beobachtung im Jahr 1879 immer noch ein großes Problem für die öffentliche Gesundheit darstellt. Ein Ansatz zur Identifizierung einer „Zunahme“ von Krankheiten und sogar zu quantifizieren, war in der Geschichte der Arbeitsmedizin präsent. Wie beispielsweise Axelson (1994) betonte, untersuchte WA Guy 1843 die „Lungenschwindsucht“ bei Buchdruckern und fand ein höheres Risiko bei Setzern als bei Druckern; Dies geschah durch Anwendung eines dem Fall-Kontroll-Ansatz ähnlichen Designs (Lilienfeld und Lilienfeld 1979). Dennoch begann sich die moderne Berufsepidemiologie und ihre Methodik erst in den frühen 1950er Jahren zu entwickeln. Wichtige Beiträge zu dieser Entwicklung waren die Studien über Blasenkrebs bei Färbereiarbeitern (Case und Hosker 1954) und Lungenkrebs bei Gasarbeitern (Doll 1952).
Probleme der Berufsepidemiologie
Die Artikel in diesem Kapitel stellen sowohl die Philosophie als auch die Werkzeuge der epidemiologischen Untersuchung vor. Sie konzentrieren sich auf die Bewertung der Expositionserfahrung von Arbeitnehmern und auf die Krankheiten, die in diesen Bevölkerungsgruppen auftreten. Probleme beim Ziehen gültiger Schlussfolgerungen über mögliche ursächliche Zusammenhänge auf dem Weg von der Exposition gegenüber gefährlichen Stoffen bis zur Entstehung von Krankheiten werden in diesem Kapitel behandelt.
Den Kern der Berufsepidemiologie bildet die Erhebung der individuellen Expositionserfahrung im Arbeitsleben. Die Aussagekraft einer epidemiologischen Studie hängt in erster Linie von der Qualität und dem Umfang der verfügbaren Expositionsdaten ab. Zweitens müssen die gesundheitlichen Auswirkungen (oder die Krankheiten), die für den Berufsepidemiologen von Belang sind, für eine klar definierte und zugängliche Gruppe von Arbeitnehmern genau bestimmbar sein. Schließlich sollten dem Epidemiologen Daten über andere potenzielle Einflüsse auf die interessierende Krankheit zur Verfügung stehen, damit alle aus der Studie ermittelten Wirkungen der beruflichen Exposition der beruflichen Exposition zugeschrieben werden können an sich eher als auf andere bekannte Ursachen der betreffenden Krankheit. In einer Gruppe von Arbeitnehmern, die möglicherweise mit einer Chemikalie arbeiten, von der vermutet wird, dass sie Lungenkrebs verursacht, haben einige Arbeitnehmer möglicherweise auch eine Vorgeschichte des Tabakrauchens, einer weiteren Ursache für Lungenkrebs. In der letzteren Situation müssen Arbeitsepidemiologen feststellen, welche Exposition (oder welcher Risikofaktor – die Chemikalie oder der Tabak oder sogar beides in Kombination) für eine Erhöhung des Lungenkrebsrisikos in der Gruppe der Arbeitnehmer verantwortlich ist studiert.
Expositionsabschätzung
Wenn eine Studie nur Zugriff auf die Tatsache hat, dass ein Arbeitnehmer in einer bestimmten Branche beschäftigt war, können die Ergebnisse einer solchen Studie gesundheitliche Auswirkungen nur mit dieser Branche in Verbindung bringen. Auch wenn für die Berufe der Arbeitnehmer Kenntnisse über die Exposition vorliegen, können nur in Bezug auf die Berufe direkt Rückschlüsse gezogen werden. Es können indirekte Rückschlüsse auf chemische Expositionen gezogen werden, aber ihre Zuverlässigkeit muss von Situation zu Situation bewertet werden. Wenn eine Studie jedoch Zugang zu Informationen über die Abteilung und/oder Berufsbezeichnung jedes Arbeitnehmers hat, können Rückschlüsse auf diese feinere Ebene der Arbeitsplatzerfahrung gezogen werden. Wenn dem Epidemiologen (in Zusammenarbeit mit einem Industriehygieniker) Informationen über die tatsächlichen Substanzen bekannt sind, mit denen eine Person arbeitet, dann wäre dies die beste verfügbare Ebene von Expositionsinformationen, da selten verfügbare Dosimetrien fehlen. Darüber hinaus können die Ergebnisse solcher Studien der Industrie nützlichere Informationen zur Schaffung sicherer Arbeitsplätze liefern.
Die Epidemiologie war bisher eine Art „Black Box“-Disziplin, weil sie die Beziehung zwischen Exposition und Krankheit (den beiden Extremen der Kausalkette) untersuchte, ohne die mechanistischen Zwischenschritte zu berücksichtigen. Dieser Ansatz war trotz seines offensichtlichen Mangels an Verfeinerung äußerst nützlich: Tatsächlich wurden beispielsweise alle bekannten Ursachen von Krebs beim Menschen mit den Werkzeugen der Epidemiologie entdeckt.
Die epidemiologische Methode basiert auf verfügbaren Aufzeichnungen – Fragebögen, Berufsbezeichnungen oder anderen „Proxies“ der Exposition; dies macht die Durchführung epidemiologischer Studien und die Interpretation ihrer Ergebnisse relativ einfach.
Die Grenzen des groberen Ansatzes zur Expositionsbewertung sind jedoch in den letzten Jahren deutlich geworden, da Epidemiologen vor komplexeren Problemen stehen. Beschränken wir unsere Betrachtung auf die berufliche Krebsepidemiologie, so wurden die meisten bekannten Risikofaktoren aufgrund der hohen Exposition in der Vergangenheit entdeckt; eine begrenzte Anzahl von Aufnahmen für jeden Job; große Populationen exponierter Arbeiter; und eine eindeutige Übereinstimmung zwischen „Proxy“-Informationen und Expositionen gegenüber Chemikalien (z. B. Schuharbeiter und Benzol, Werften und Asbest usw.). Heutzutage ist die Situation wesentlich anders: Die Expositionsniveaus sind in den westlichen Ländern erheblich niedriger (diese Einschränkung sollte immer betont werden); Arbeitnehmer sind in derselben Berufsbezeichnung vielen verschiedenen Chemikalien und Mischungen ausgesetzt (z. B. Landarbeiter); homogene Populationen exponierter Arbeitnehmer sind schwieriger zu finden und in der Regel zahlenmäßig klein; und die Übereinstimmung zwischen „Proxy“-Informationen und tatsächlicher Exposition wird zunehmend schwächer. In diesem Zusammenhang haben die Werkzeuge der Epidemiologie aufgrund der Fehlklassifizierung der Exposition eine reduzierte Sensitivität.
Darüber hinaus hat sich die Epidemiologie in den meisten Kohortenstudien auf „harte“ Endpunkte wie den Tod verlassen. Arbeitnehmer ziehen es jedoch möglicherweise vor, etwas anderes als „Körperzahlen“ zu sehen, wenn die potenziellen gesundheitlichen Auswirkungen beruflicher Expositionen untersucht werden. Daher hätte die Verwendung direkterer Indikatoren sowohl für die Exposition als auch für die frühe Reaktion einige Vorteile. Biologische Marker können nur ein Werkzeug sein.
Biologische Marker
Die Verwendung von biologischen Markern, wie beispielsweise Bleiwerten in Blut- oder Leberfunktionstests, ist in der Arbeitsepidemiologie nicht neu. Der Einsatz molekularer Techniken in epidemiologischen Studien hat jedoch die Verwendung von Biomarkern zur Bewertung der Exposition gegenüber Zielorganen, zur Bestimmung der Anfälligkeit und zur Feststellung früher Erkrankungen ermöglicht.
Einsatzmöglichkeiten von Biomarkern im Rahmen der Berufsepidemiologie sind:
- Expositionsbewertung in Fällen, in denen traditionelle epidemiologische Instrumente nicht ausreichen (insbesondere bei niedrigen Dosen und niedrigen Risiken)
- die ursächliche Rolle einzelner chemischer Agenzien oder Substanzen bei Mehrfachexposition oder Mischungen zu entwirren
- Abschätzung der Gesamtbelastung durch Chemikalien mit demselben mechanistischen Ziel
- Untersuchung pathogenetischer Mechanismen
- Untersuchung der individuellen Anfälligkeit (z. B. metabolische Polymorphismen, DNA-Reparatur) (Vineis 1992)
- Exposition und/oder Krankheit genauer zu klassifizieren und damit die Aussagekraft der Statistik zu erhöhen.
In der wissenschaftlichen Gemeinschaft ist große Begeisterung über diese Verwendungen entstanden, aber, wie oben erwähnt, sollte die methodische Komplexität der Verwendung dieser neuen „molekularen Werkzeuge“ dazu dienen, vor übermäßigem Optimismus zu warnen. Biomarker für chemische Belastungen (wie DNA-Addukte) haben mehrere Mängel:
- Sie spiegeln in der Regel aktuelle Expositionen wider und sind daher in Fall-Kontroll-Studien von begrenztem Nutzen, während sie für die Verwendung in Kohortenuntersuchungen wiederholte Probenahmen über längere Zeiträume erfordern.
- Obwohl sie sehr spezifisch sein können und somit die Fehleinstufung der Exposition verbessern, bleiben die Ergebnisse oft schwer zu interpretieren.
- Wenn komplexe chemische Belastungen untersucht werden (z. B. Luftverschmutzung oder Tabakrauch in der Umwelt), ist es möglich, dass der Biomarker eine bestimmte Komponente des Gemischs widerspiegelt, während die biologische Wirkung auf eine andere zurückzuführen sein könnte.
- In vielen Situationen ist nicht klar, ob ein Biomarker eine relevante Exposition, ein Korrelat der relevanten Exposition, eine individuelle Anfälligkeit oder ein frühes Krankheitsstadium widerspiegelt, wodurch kausale Rückschlüsse eingeschränkt werden.
- Die Bestimmung der meisten Biomarker erfordert einen teuren Test oder ein invasives Verfahren oder beides, wodurch Einschränkungen für eine angemessene Studiengröße und statistische Aussagekraft entstehen.
- Ein Biomarker der Exposition ist nur ein Stellvertreter für das eigentliche Ziel einer epidemiologischen Untersuchung, die in der Regel auf eine vermeidbare Umweltexposition abzielt (Trichopoulos 1995; Pearce et al. 1995).
Noch wichtiger als die methodischen Mängel ist die Überlegung, dass molekulare Techniken uns dazu veranlassen könnten, unseren Fokus von der Identifizierung von Risiken in der exogenen Umgebung auf die Identifizierung von Personen mit hohem Risiko umzulenken und dann personalisierte Risikobewertungen durch Messung von Phänotyp, Adduktbelastung und erworbenen Mutationen vorzunehmen. Dies würde unseren Fokus, wie von McMichael angemerkt, auf eine Form der klinischen Bewertung lenken, anstatt auf eine Epidemiologie der öffentlichen Gesundheit. Die Konzentration auf Einzelpersonen könnte uns von dem wichtigen Ziel der öffentlichen Gesundheit ablenken, eine weniger gefährliche Umgebung zu schaffen (McMichael 1994).
Zwei weitere wichtige Fragen ergeben sich in Bezug auf die Verwendung von Biomarkern:
- Der Einsatz von Biomarkern in der Berufsepidemiologie muss von einer klaren Politik der informierten Einwilligung begleitet werden. Der Arbeitnehmer kann mehrere Gründe haben, die Zusammenarbeit abzulehnen. Ein sehr praktischer Grund ist, dass die Identifizierung von beispielsweise einer Veränderung eines frühen Reaktionsmarkers wie Schwesterchromatidaustausch die Möglichkeit einer Diskriminierung durch Kranken- und Lebensversicherer und durch Arbeitgeber impliziert, die den Arbeitnehmer möglicherweise meiden, weil er oder sie möglicherweise anfälliger ist zu Krankheit. Ein zweiter Grund betrifft das genetische Screening: Da die Verteilung von Genotypen und Phänotypen je nach ethnischer Gruppe unterschiedlich ist, könnten die Beschäftigungsmöglichkeiten für Minderheiten durch das genetische Screening behindert werden. Drittens können Zweifel an der Vorhersagbarkeit von Gentests geäußert werden: Da der Vorhersagewert von der Prävalenz der Erkrankung abhängt, die der Test identifizieren soll, ist der Vorhersagewert gering, wenn letztere selten ist, und der praktische Nutzen des Screenings Test wird fraglich sein. Bisher wurde keiner der genetischen Screening-Tests als im Feld anwendbar beurteilt (Ashford et al. 1990).
- Vor dem Einsatz von Biomarkern müssen ethische Grundsätze beachtet werden. Diese Grundsätze wurden von einer interdisziplinären Arbeitsgruppe des Technischen Büros der Europäischen Gewerkschaften mit Unterstützung der Kommission der Europäischen Gemeinschaften für Biomarker zur Identifizierung individueller Krankheitsanfälligkeit evaluiert (Van Damme et al. 1995); Ihr Bericht hat die Ansicht bekräftigt, dass Tests nur mit dem Ziel durchgeführt werden können, Krankheiten bei einer Belegschaft vorzubeugen. Unter anderem müssen Tests verwendet werden hört niemals .
- dienen als Mittel zur „Auswahl der Stärksten“
- verwendet werden, um die Umsetzung wirksamer Präventivmaßnahmen zu vermeiden, wie z. B. die Identifizierung und Substitution von Risikofaktoren oder Verbesserungen der Bedingungen am Arbeitsplatz
- soziale Ungleichheit schaffen, bestätigen oder verstärken
- eine Kluft zwischen den am Arbeitsplatz befolgten ethischen Grundsätzen und den ethischen Grundsätzen schaffen, die in einer demokratischen Gesellschaft aufrechterhalten werden müssen
- eine Person, die eine Stelle sucht, dazu verpflichten, personenbezogene Daten offenzulegen, die nicht unbedingt für die Erlangung der Stelle erforderlich sind.
Schließlich mehren sich die Hinweise darauf, dass die metabolische Aktivierung oder Inaktivierung gefährlicher Substanzen (insbesondere von Karzinogenen) in menschlichen Populationen sehr unterschiedlich und teilweise genetisch bedingt ist. Darüber hinaus kann die interindividuelle Variabilität der Anfälligkeit gegenüber Karzinogenen bei geringer beruflicher und umweltbedingter Exposition besonders wichtig sein (Vineis et al. 1994). Solche Erkenntnisse können Regulierungsentscheidungen stark beeinflussen, die den Risikobewertungsprozess auf die anfälligsten Personen konzentrieren (Vineis und Martone 1995).
Studiendesign und Validität
Hernbergs Artikel über epidemiologische Studiendesigns und ihre Anwendung in der Arbeitsmedizin konzentriert sich auf das Konzept der „Studienbasis“, definiert als die Morbiditätserfahrung (in Bezug auf eine bestimmte Exposition) einer Bevölkerung, während sie im Laufe der Zeit verfolgt wird. Die Untersuchungsgrundlage ist also nicht nur eine Population (also eine Personengruppe), sondern die Erfahrung des Krankheitsgeschehens dieser Population in einem bestimmten Zeitraum (Miettinen 1985, Hernberg 1992). Wenn dieses vereinheitlichende Konzept einer Studienbasis übernommen wird, ist es wichtig zu erkennen, dass die unterschiedlichen Studiendesigns (z. B. Fall-Kontroll- und Kohortendesigns) einfach unterschiedliche Arten der „Ernte“ von Informationen sowohl über die Exposition als auch über die Krankheit aus derselben Studie sind Base; es handelt sich nicht um diametral unterschiedliche Ansätze.
Der Artikel zur Validität im Studiendesign von Sasco befasst sich mit Definitionen und der Bedeutung von Confounding. Studienforscher müssen bei berufsbezogenen Studien immer die Möglichkeit von Confounding berücksichtigen, und es kann nie genug betont werden, dass die Identifizierung potenziell verwirrender Variablen ein integraler Bestandteil jedes Studiendesigns und jeder Analyse ist. Zwei Aspekte des Confounding müssen in der Berufsepidemiologie adressiert werden:
- Negative Confounding sollte untersucht werden: Beispielsweise sind einige industrielle Bevölkerungsgruppen aufgrund eines rauchfreien Arbeitsplatzes nur gering mit lebensstilbedingten Risikofaktoren konfrontiert; Glasbläser neigen dazu, weniger zu rauchen als die allgemeine Bevölkerung.
- Wenn Confounding in Betracht gezogen wird, sollte eine Schätzung seiner Richtung und seiner potenziellen Auswirkung bewertet werden. Dies gilt insbesondere dann, wenn die Daten zur Kontrolle des Confounding spärlich sind. Beispielsweise ist Rauchen ein wichtiger Confounder in der Berufsepidemiologie und sollte immer berücksichtigt werden. Wenn jedoch keine Daten zum Rauchen verfügbar sind (was häufig in Kohortenstudien der Fall ist), ist es unwahrscheinlich, dass das Rauchen einen großen Risikoüberschuss erklären kann, der in einer Berufsgruppe gefunden wird. Dies wird in einem Artikel von Axelson (1978) schön beschrieben und von Greenland (1987) weiter diskutiert. Als in der Literatur detaillierte Daten sowohl zum Beruf als auch zum Rauchen verfügbar waren, schien Confounding die Schätzungen zum Zusammenhang zwischen Lungenkrebs und Beruf nicht stark zu verzerren (Vineis und Simonato 1991). Darüber hinaus führt eine vermutete Verwechslung nicht immer zu ungültigen Assoziationen. Da die Forscher auch Gefahr laufen, durch andere unentdeckte Beobachtungs- und Auswahlverzerrungen in die Irre geführt zu werden, sollten diese beim Design einer Studie ebenso viel Gewicht erhalten wie die Frage der Verwirrung (Stellman 1987).
Zeitliche und zeitbezogene Variablen wie Risikoalter, Kalenderzeitraum, Zeit seit Einstellung, Zeit seit erster Exposition, Expositionsdauer und deren Behandlung in der Analysephase gehören zu den komplexesten methodischen Fragestellungen der Arbeitsepidemiologie. Sie werden in diesem Kapitel nicht behandelt, aber es wird auf zwei relevante und neuere methodische Referenzen hingewiesen (Pearce 1992; Robins et al. 1992).
Statistiken
Der statistische Artikel von Biggeri und Braga sowie der Titel dieses Kapitels weisen darauf hin, dass statistische Methoden nicht von epidemiologischer Forschung getrennt werden können. Dies liegt daran, dass: (a) ein solides Verständnis der Statistik wertvolle Einblicke in das richtige Design einer Untersuchung liefern kann und (b) Statistik und Epidemiologie ein gemeinsames Erbe teilen und die gesamte quantitative Grundlage der Epidemiologie auf dem Begriff der Wahrscheinlichkeit basiert ( Clayton 1992; Clayton und Hills 1993). In vielen der folgenden Artikel werden empirische Beweise und Beweise für hypothetische kausale Zusammenhänge mit probabilistischen Argumenten und geeigneten Studiendesigns bewertet. Beispielsweise wird der Schwerpunkt auf die Schätzung des Risikomaßes von Interesse gelegt, wie Zinssätze oder relative Risiken, und auf die Konstruktion von Konfidenzintervallen um diese Schätzungen herum, anstatt statistische Wahrscheinlichkeitstests durchzuführen (Poole 1987; Gardner und Altman 1989; Greenland 1990 ). Es wird eine kurze Einführung in das statistische Denken unter Verwendung der Binomialverteilung gegeben. Statistik sollte ein Begleiter des wissenschaftlichen Denkens sein. Aber es ist wertlos, wenn es an richtig konzipierter und durchgeführter Forschung mangelt. Statistiker und Epidemiologen sind sich bewusst, dass die Wahl der Methoden bestimmt, was und in welchem Umfang wir Beobachtungen machen. Die wohlüberlegte Auswahl der Gestaltungsmöglichkeiten ist daher von grundlegender Bedeutung, um valide Beobachtungen zu gewährleisten.
Ethik
Der letzte Artikel von Vineis befasst sich mit ethischen Fragen in der epidemiologischen Forschung. Die in dieser Einführung zu erwähnenden Punkte beziehen sich auf die Epidemiologie als eine Disziplin, die per Definition präventive Maßnahmen impliziert. Spezifische ethische Aspekte im Hinblick auf den Schutz der Arbeitnehmer und der Bevölkerung insgesamt erfordern die Anerkennung, dass:
- Epidemiologische Studien im betrieblichen Umfeld sollten Präventionsmaßnahmen am Arbeitsplatz keinesfalls verzögern.
- Berufsepidemiologie bezieht sich nicht auf Lebensstilfaktoren, sondern auf Situationen, in denen bei der Wahl der Exposition normalerweise keine oder nur eine geringe persönliche Rolle gespielt wird. Dies impliziert ein besonderes Engagement für eine wirksame Prävention und die unverzügliche Übermittlung von Informationen an die Arbeitnehmer und die Öffentlichkeit.
- Forschung deckt Gesundheitsgefahren auf und liefert das Wissen für vorbeugende Maßnahmen. Die ethischen Probleme, wenn es möglich ist, keine Forschung durchzuführen, sollten berücksichtigt werden.
- Die Benachrichtigung der Arbeitnehmer über die Ergebnisse epidemiologischer Studien ist sowohl ein ethisches als auch ein methodisches Problem in der Risikokommunikation. Der Forschung zur Bewertung der potenziellen Auswirkungen und Wirksamkeit der Benachrichtigung sollte hohe Priorität eingeräumt werden (Schulte et al. 1993).
Ausbildung in Berufsepidemiologie
In die Spezialisierung Berufsepidemiologie finden Menschen mit unterschiedlichsten Hintergründen den Weg. Medizin, Krankenpflege und Statistik sind einige der wahrscheinlicheren Hintergründe, die unter Fachleuten auf diesem Gebiet zu finden sind. In Nordamerika hat etwa die Hälfte aller ausgebildeten Epidemiologen einen naturwissenschaftlichen Hintergrund, während die andere Hälfte den Weg zum Doktor der Medizin eingeschlagen hat. In Ländern außerhalb Nordamerikas haben die meisten Spezialisten für Berufsepidemiologie den Doktortitel erreicht. In Nordamerika werden Menschen mit medizinischer Ausbildung eher als „Inhaltsexperten“ betrachtet, während diejenigen, die auf dem wissenschaftlichen Weg ausgebildet wurden, als „methodische Experten“ gelten. Oft ist es für einen Inhaltsexperten von Vorteil, sich mit einem Methodenexperten zusammenzuschließen, um die bestmögliche Studie zu konzipieren und durchzuführen.
Für das Fach Berufsepidemiologie sind nicht nur Kenntnisse in epidemiologischen Methoden, Statistiken und Computern erforderlich, sondern auch Kenntnisse in Toxikologie, Arbeitshygiene und Krankheitsregistern (Merletti und Comba 1992). Da große Studien eine Verknüpfung mit Krankheitsregistern erfordern können, ist die Kenntnis von Quellen für Bevölkerungsdaten hilfreich. Auch Kenntnisse der Arbeits- und Unternehmensorganisation sind wichtig. Diplomarbeiten auf Master-Ebene und Dissertationen auf Doktorats-Ausbildungsebene statten die Studierenden mit dem Wissen aus, das für die Durchführung umfangreicher datensatzbasierter und interviewbasierter Studien unter Arbeitnehmern erforderlich ist.
Anteil der berufsbedingten Erkrankungen
Der Anteil der Erkrankungen, der entweder bei einer Gruppe exponierter Arbeitnehmer oder in der Allgemeinbevölkerung auf berufliche Expositionen zurückzuführen ist, wird zumindest im Hinblick auf Krebs in einem anderen Teil davon erfasst Enzyklopädie. Hier sollten wir bedenken, dass, wenn eine Schätzung berechnet wird, diese für eine bestimmte Krankheit (und einen bestimmten Ort im Fall von Krebs), einen bestimmten Zeitraum und ein bestimmtes geografisches Gebiet gelten sollte. Darüber hinaus sollte es auf genauen Messungen des Anteils exponierter Personen und des Expositionsgrads beruhen. Dies impliziert, dass der Anteil der berufsbedingten Erkrankungen von sehr niedrig oder null in bestimmten Bevölkerungsgruppen bis zu sehr hoch in anderen in Industriegebieten reichen kann, wo beispielsweise bis zu 40 % der Lungenkrebsfälle auf berufliche Exposition zurückzuführen sind (Vineis und Simonato 1991). Schätzungen, die nicht auf einer detaillierten Überprüfung gut konzipierter epidemiologischer Studien beruhen, können bestenfalls als fundierte Vermutungen angesehen werden und sind von begrenztem Wert.
Übertragung gefährlicher Industrien
Die meisten epidemiologischen Forschungen werden in den Industrieländern durchgeführt, wo die Regulierung und Kontrolle bekannter Berufsgefahren das Krankheitsrisiko in den letzten Jahrzehnten verringert hat. Gleichzeitig fand jedoch eine große Verlagerung gefährlicher Industrien in die Entwicklungsländer statt (Jeyaratnam 1994). Chemikalien, die zuvor in den Vereinigten Staaten oder Europa verboten waren, werden jetzt in Entwicklungsländern hergestellt. Beispielsweise wurde die Asbestzerkleinerung von den USA nach Mexiko verlagert und die Benzidinproduktion aus europäischen Ländern in das ehemalige Jugoslawien und nach Korea (Simonato 1986; LaDou 1991; Pearce et al. 1994).
Ein indirektes Zeichen für das Berufsrisiko und die Arbeitsbedingungen in den Entwicklungsländern ist die Epidemie akuter Vergiftungen, die in einigen dieser Länder auftritt. Einer Schätzung zufolge gibt es jedes Jahr weltweit etwa 20,000 Todesfälle durch akute Pestizidvergiftung, aber dies ist wahrscheinlich eine erhebliche Unterschätzung (Kogevinas et al. 1994). Schätzungen zufolge ereignen sich 99 % aller Todesfälle durch akute Pestizidvergiftung in Entwicklungsländern, wo nur 20 % der weltweiten Agrochemikalien verwendet werden (Kogevinas et al. 1994). Das heißt, selbst wenn die epidemiologische Forschung auf eine Verringerung der Berufsrisiken hinzuweisen scheint, könnte dies einfach darauf zurückzuführen sein, dass der größte Teil dieser Forschung in den Industrieländern durchgeführt wird. Die berufsbedingten Gefahren könnten einfach auf die Entwicklungsländer übertragen worden sein, und die Belastung durch die berufsbedingte Exposition insgesamt könnte weltweit gestiegen sein (Vineis et al. 1995).
Veterinärepidemiologie
Aus offensichtlichen Gründen ist die Veterinär-Epidemiologie nicht direkt relevant für Arbeitsmedizin und Berufsepidemiologie. Dennoch können epidemiologische Studien an Tieren aus mehreren Gründen Hinweise auf umweltbedingte und berufliche Ursachen von Krankheiten liefern:
- Die Lebensspanne von Tieren ist im Vergleich zu der von Menschen relativ kurz, und die Latenzzeit für Krankheiten (z. B. die meisten Krebsarten) ist bei Tieren kürzer als bei Menschen. Dies impliziert, dass eine Krankheit, die bei einem Wild- oder Haustier auftritt, als Sentinel-Ereignis dienen kann, um uns auf das Vorhandensein eines potenziellen Umweltgiftes oder Karzinogens für den Menschen aufmerksam zu machen, bevor es auf andere Weise identifiziert worden wäre (Glickman 1993).
- Expositionsmarker wie Hämoglobinaddukte oder Absorptions- und Ausscheidungsniveaus von Toxinen können bei Wild- und Heimtieren gemessen werden, um die Umweltkontamination durch industrielle Quellen zu bewerten (Blondin und Viau 1992; Reynolds et al. 1994; Hungerford et al. 1995). .
- Tiere werden einigen Faktoren nicht ausgesetzt, die in Studien am Menschen als Störfaktoren wirken können, und Untersuchungen an Tierpopulationen können daher ohne Berücksichtigung dieser potenziellen Störfaktoren durchgeführt werden. Beispielsweise könnte eine Studie über Lungenkrebs bei Haushunden signifikante Zusammenhänge zwischen der Krankheit und der Exposition gegenüber Asbest erkennen (z. B. über die asbestbezogenen Berufe der Besitzer und die Nähe zu industriellen Asbestquellen). Natürlich würde eine solche Studie die Wirkung des aktiven Rauchens als Confounder beseitigen.
Tierärzte sprechen von einer epidemiologischen Revolution in der Veterinärmedizin (Schwabe 1993) und es sind Lehrbücher über das Fach erschienen (Thrusfield 1986; Martin et al. 1987). Sicherlich stammen Hinweise auf Umwelt- und Berufsgefahren aus den gemeinsamen Bemühungen von Human- und Tierepidemiologen. Unter anderem die Wirkung von Phenoxyherbiziden bei Schafen und Hunden (Newell et al. 1984; Hayes et al. 1990), von Magnetfeldern (Reif et al. 1995) und mit asbestähnlichen Verbindungen kontaminierten Pestiziden (insbesondere Flohpräparaten) bei Hunden (Glickman et al. 1983) sind bemerkenswerte Beiträge.
Partizipative Forschung, Ergebnisvermittlung und Prävention
Es ist wichtig anzuerkennen, dass viele epidemiologische Studien auf dem Gebiet der Gesundheit am Arbeitsplatz durch die Erfahrung und Besorgnis der Arbeitnehmer selbst initiiert werden (Olsen et al. 1991). Oft glaubten die Arbeiter – diejenigen, die historisch und/oder gegenwärtig exponiert waren –, dass etwas nicht stimmte, lange bevor dies durch die Forschung bestätigt wurde. Berufsepidemiologie kann als eine Möglichkeit betrachtet werden, die Erfahrungen der Arbeitnehmer „zu verstehen“, die Daten systematisch zu sammeln und zu gruppieren und Rückschlüsse auf die beruflichen Ursachen ihrer Krankheit zu ziehen. Darüber hinaus sind die Arbeitnehmer selbst, ihre Vertreter und die für die Gesundheit der Arbeitnehmer zuständigen Personen die am besten geeigneten Personen, um die gesammelten Daten zu interpretieren. Sie sollten daher immer aktiv an allen am Arbeitsplatz durchgeführten Ermittlungen teilnehmen. Nur ihre direkte Beteiligung garantiert, dass der Arbeitsplatz auch nach der Abreise der Forschenden sicher bleibt. Das Ziel jeder Studie ist die Nutzung der Ergebnisse zur Prävention von Krankheiten und Behinderungen, und der Erfolg davon hängt zu einem großen Teil davon ab, sicherzustellen, dass die Exponierten an der Gewinnung und Interpretation der Studienergebnisse teilnehmen. Die Rolle und Verwendung von Forschungsergebnissen in Rechtsstreitigkeiten, wenn Arbeitnehmer Entschädigung für Schäden verlangen, die durch Exposition am Arbeitsplatz verursacht wurden, geht über den Rahmen dieses Kapitels hinaus. Für diesbezügliche Einblicke wird der Leser an anderer Stelle verwiesen (Soskolne, Lilienfeld und Black 1994).
Partizipative Ansätze zur Sicherstellung der Durchführung berufsepidemiologischer Forschung sind mancherorts gängige Praxis in Form von Lenkungsausschüssen geworden, die die Forschungsinitiative von der Anfänge bis zum Abschluss begleiten. Diese Ausschüsse sind in ihrer Struktur mehrteilig, darunter Arbeitnehmer, Wissenschaft, Verwaltung und/oder Regierung. Mit Vertretern aller Stakeholder-Gruppen im Forschungsprozess wird die Ergebniskommunikation durch ihre erhöhte Glaubwürdigkeit effektiver, da „einer aus der eigenen“ die Forschung beaufsichtigt und die Ergebnisse an die jeweiligen Personen kommuniziert Wahlkreis. Auf diese Weise ist wahrscheinlich das größte Maß an wirksamer Prävention zu erwarten.
Diese und andere partizipative Ansätze in der arbeitsmedizinischen Forschung werden unter Einbeziehung derer durchgeführt, die von dem besorgniserregenden expositionsbedingten Problem betroffen oder anderweitig davon betroffen sind. Dies sollte häufiger in der gesamten epidemiologischen Forschung beobachtet werden (Laurell et al. 1992). Es ist wichtig, sich daran zu erinnern, dass das Ziel der Analyse in der epidemiologischen Arbeit die Abschätzung des Ausmaßes und der Verteilung des Risikos ist, in der partizipativen Forschung aber auch die Vermeidbarkeit des Risikos ein Ziel ist (Loewenson und Biocca 1995). Diese Komplementarität von Epidemiologie und effektiver Prävention ist Teil der Botschaft davon Enzyklopädie und dieses Kapitels.
Wahrung der Relevanz für die öffentliche Gesundheit
Obwohl neue Entwicklungen in der epidemiologischen Methodik, in der Datenanalyse und in der Expositionsabschätzung und -messung (wie neue molekularbiologische Techniken) willkommen und wichtig sind, können sie auch zu einem reduktionistischen Ansatz beitragen, der sich auf Einzelpersonen statt auf Bevölkerungsgruppen konzentriert. Es wurde gesagt, dass:
… Epidemiologie hat weitgehend aufgehört, als Teil eines multidisziplinären Ansatzes zum Verständnis der Krankheitsursachen in Bevölkerungen zu fungieren, und ist zu einer Reihe generischer Methoden zur Messung von Zusammenhängen zwischen Exposition und Krankheit bei Einzelpersonen geworden. … Derzeit werden soziale, wirtschaftliche und kulturelle Aspekte vernachlässigt , historische, politische und andere Bevölkerungsfaktoren als Hauptursachen für Krankheiten … Die Epidemiologie muss sich wieder in die öffentliche Gesundheit integrieren und die Bevölkerungsperspektive neu entdecken (Pearce 1996).
Arbeits- und Umweltepidemiologen spielen eine wichtige Rolle, nicht nur bei der Entwicklung neuer epidemiologischer Methoden und Anwendungen für diese Methoden, sondern auch bei der Sicherstellung, dass diese Methoden immer in die richtige Bevölkerungsperspektive integriert werden.
Anthropometrie
Dieser Artikel ist eine Adaption der 3. Auflage der Encyclopaedia of Occupational Health and Safety.
Anthropometrie ist ein grundlegender Zweig der physikalischen Anthropologie. Es repräsentiert den quantitativen Aspekt. Ein breites Theorie- und Praxissystem widmet sich der Definition von Methoden und Variablen, um die Ziele in den verschiedenen Anwendungsbereichen in Beziehung zu setzen. In den Bereichen Arbeitsschutz, Arbeitssicherheit und Ergonomie befassen sich anthropometrische Systeme hauptsächlich mit Körperbau, -zusammensetzung und -konstitution sowie mit den Dimensionen der Wechselbeziehungen des menschlichen Körpers zu Arbeitsplatzdimensionen, Maschinen, dem industriellen Umfeld und der Kleidung.
Anthropometrische Variablen
Eine anthropometrische Größe ist ein messbares Merkmal des Körpers, das definiert, standardisiert und auf eine Maßeinheit bezogen werden kann. Lineare Variablen werden im Allgemeinen durch Landmarken definiert, die sich genau auf den Körper zurückführen lassen. Es gibt im Allgemeinen zwei Arten von Orientierungspunkten: skelettanatomische, die durch Abtasten von Knochenvorsprüngen durch die Haut gefunden und verfolgt werden können, und virtuelle Orientierungspunkte, die einfach als maximale oder minimale Entfernungen unter Verwendung der Zweige eines Messschiebers gefunden werden.
Anthropometrische Variablen haben sowohl genetische als auch Umweltkomponenten und können verwendet werden, um individuelle und Populationsvariabilität zu definieren. Die Auswahl der Variablen muss sich auf den spezifischen Forschungszweck beziehen und mit anderen Forschungen auf demselben Gebiet standardisiert werden, da die Anzahl der in der Literatur beschriebenen Variablen sehr groß ist und bis zu 2,200 für den menschlichen Körper beschrieben wurden.
Anthropometrische Variablen sind hauptsächlich linear Maße wie Höhen, Entfernungen von Orientierungspunkten bei stehender oder sitzender Versuchsperson in standardisierter Körperhaltung; Durchmesser, wie z. B. Entfernungen zwischen bilateralen Orientierungspunkten; Längen, wie z. B. Entfernungen zwischen zwei verschiedenen Orientierungspunkten; gebogene Maßnahmen, nämlich Bögen, wie Abstände auf der Körperoberfläche zwischen zwei Landmarken; und GurteB. geschlossene Rundummaßnahmen an Körperoberflächen, in der Regel an mindestens einer Landmarke oder in definierter Höhe positioniert.
Andere Variablen können spezielle Methoden und Instrumente erfordern. Beispielsweise wird die Hautfaltendicke mit speziellen Konstantdruck-Messschiebern gemessen. Volumen werden durch Berechnung oder durch Eintauchen in Wasser gemessen. Um vollständige Informationen über die Eigenschaften der Körperoberfläche zu erhalten, kann eine Computermatrix von Oberflächenpunkten unter Verwendung biostereometrischer Techniken gezeichnet werden.
Instrumente
Obwohl hochentwickelte anthropometrische Instrumente im Hinblick auf eine automatisierte Datensammlung beschrieben und verwendet wurden, sind grundlegende anthropometrische Instrumente ziemlich einfach und leicht zu verwenden. Es muss viel Sorgfalt darauf verwendet werden, häufige Fehler zu vermeiden, die aus einer Fehlinterpretation von Orientierungspunkten und falschen Körperhaltungen von Subjekten resultieren.
Das übliche anthropometrische Instrument ist das Anthropometer – ein 2 Meter langer, starrer Stab mit zwei Zählerablesungsskalen, mit dem vertikale Körpermaße, wie Höhen von Orientierungspunkten vom Boden oder Sitz, und Quermaße, wie Durchmesser, abgenommen werden können.
Üblicherweise kann die Rute in 3 oder 4 Teile geteilt werden, die ineinander passen. Ein verschiebbarer Ast mit gerader oder gebogener Klaue ermöglicht das Messen von Abständen vom Boden für Höhen oder von einem festen Ast für Durchmesser. Ausgefeiltere Anthropometer haben eine einzige Skala für Höhen und Durchmesser, um Skalenfehler zu vermeiden, oder sind mit digitalen mechanischen oder elektronischen Lesegeräten ausgestattet (Abbildung 1).
Abbildung 1. Ein Anthropometer
Ein Stadiometer ist ein festes Anthropometer, das im Allgemeinen nur für die Statur verwendet wird und häufig mit einer Gewichtsbalkenwaage verbunden ist.
Für Querdurchmesser kann eine Reihe von Messschiebern verwendet werden: das Pelvimeter für Messungen bis 600 mm und das Cephalometer bis 300 mm. Letzteres eignet sich besonders für Kopfmessungen in Verbindung mit einem Gleitkompass (Bild 2).
Abbildung 2. Ein Cephalometer zusammen mit einem verschiebbaren Kompass
Das Fußbrett dient zur Vermessung der Füße und das Kopfbrett liefert kartesische Koordinaten des Kopfes bei Orientierung in der „Frankfurter Ebene“ (einer horizontal verlaufenden Ebene). Portion und orbital Orientierungspunkte des Kopfes).
Die Hautfaltendicke wird mit einem Hautfaltenzirkel mit konstantem Druck im Allgemeinen mit einem Druck von 9.81 x 10 gemessen4 Pa (der Druck, der durch ein Gewicht von 10 g auf eine Fläche von 1 mm ausgeübt wird2).
Für Bögen und Gurte wird ein schmales, flexibles Stahlband mit flachem Querschnitt verwendet. Selbstrichtende Stahlbänder sind zu vermeiden.
Systeme von Variablen
Ein System anthropometrischer Variablen ist ein kohärenter Satz von Körpermaßen zur Lösung bestimmter Probleme.
Im Bereich Ergonomie und Sicherheit besteht das Hauptproblem darin, Geräte und Arbeitsplatz an den Menschen anzupassen und Kleidung auf die richtige Größe zuzuschneiden.
Ausrüstung und Arbeitsbereich erfordern hauptsächlich lineare Maße von Gliedmaßen und Körpersegmenten, die leicht aus Höhen und Durchmessern von Orientierungspunkten berechnet werden können, während Schneidergrößen hauptsächlich auf Bögen, Umfang und flexiblen Bandlängen basieren. Beide Systeme können je nach Bedarf kombiniert werden.
In jedem Fall ist es zwingend erforderlich, für jede Messung einen genauen Raumbezug zu haben. Die Orientierungspunkte müssen daher durch Höhen und Durchmesser verbunden sein und jeder Bogen oder Umfang muss eine definierte Orientierungspunktreferenz haben. Höhen und Neigungen müssen angegeben werden.
Bei einer bestimmten Erhebung muss die Anzahl der Variablen auf ein Minimum beschränkt werden, um eine übermäßige Belastung der Versuchsperson und des Bedieners zu vermeiden.
Ein grundlegender Satz von Variablen für den Arbeitsbereich wurde auf 33 gemessene Variablen (Abbildung 3) plus 20 durch eine einfache Berechnung abgeleitete Variablen reduziert. Für eine militärische Allzweckumfrage verwenden Hertzberg und Mitarbeiter 146 Variablen. Für Kleidung und allgemeine biologische Zwecke hat das Italian Fashion Board (Geben Sie Italiano della Moda ein) verwendet einen Satz von 32 allgemeinen und 28 technischen Variablen. Die deutsche Norm (DIN 61 516) der Kontrollkörpermaße für Kleidung umfasst 12 Variablen. Die Empfehlung der Internationalen Organisation für Normung (ISO) für Anthropometrie enthält eine Kernliste von 36 Variablen (siehe Tabelle 1). Die von der ILO veröffentlichten International Data on Anthropometry-Tabellen listen 19 Körpermaße für die Bevölkerung von 20 verschiedenen Regionen der Welt auf (Jürgens, Aune und Pieper 1990).
Abbildung 3. Grundlegender Satz anthropometrischer Variablen
Tabelle 1. Grundlegende anthropometrische Kernliste
1.1 Vorwärtsreichweite (zum Handgriff, während der Proband aufrecht an einer Wand steht)
1.2 Statur (vertikaler Abstand vom Boden zum Scheitel des Kopfes)
1.3 Augenhöhe (vom Boden bis zum inneren Augenwinkel)
1.4 Schulterhöhe (vom Boden bis zum Schulterdach)
1.5 Ellenbogenhöhe (vom Boden bis zur radialen Vertiefung des Ellenbogens)
1.6 Schritthöhe (vom Boden bis zum Schambein)
1.7 Fingerspitzenhöhe (vom Boden bis zur Griffachse der Faust)
1.8 Schulterbreite (Biakromialdurchmesser)
1.9 Hüftbreite, stehend (der maximale Abstand über den Hüften)
2.1 Sitzhöhe (von Sitzfläche bis Kopfscheitel)
2.2 Augenhöhe sitzend (vom Sitz bis zum inneren Augenwinkel)
2.3 Schulterhöhe sitzend (vom Sitz bis zum Schulterdach)
2.4 Ellbogenhöhe sitzend (vom Sitz bis zum tiefsten Punkt des gebeugten Ellbogens)
2.5 Kniehöhe (von der Fußstütze bis zur Oberschenkeloberseite)
2.6 Unterschenkellänge (Höhe der Sitzfläche)
2.7 Unterarm-Hand-Länge (von der Rückseite des gebeugten Ellbogens bis zur Griffachse)
2.8 Körpertiefe sitzend (Sitztiefe)
2.9 Gesäß-Knie-Länge (von der Kniescheibe bis zum hintersten Punkt des Gesäßes)
2.10 Ellbogen zu Ellbogenbreite (Abstand zwischen den Seitenflächen der Ellbogen)
2.11 Hüftbreite sitzend (Sitzbreite)
3.1 Zeigefingerbreite, proximal (am Gelenk zwischen Mittel- und Grundphalangen)
3.2 Zeigefingerbreite, distal (am Gelenk zwischen End- und Mittelglied)
3.3 Zeigefingerlänge
3.4 Handlänge (von der Spitze des Mittelfingers bis zum Griffel)
3.5 Handbreite (an Mittelhand)
3.6 Umfang des Handgelenks
4.1 Fußbreite
4.2 Fußlänge
5.1 Wärmeumfang (bei Glabella)
5.2 Sagittalbogen (von Glabella bis Inion)
5.3 Kopflänge (von Glabella bis Opisthocranion)
5.4 Kopfbreite (maximal über dem Ohr)
5.5 Bitragionsbogen (über dem Kopf zwischen den Ohren)
6.1 Taillenumfang (am Nabel)
6.2 Tibiahöhe (vom Boden bis zum höchsten Punkt am anteromedialen Rand des Glenoids der Tibia)
6.3 Halswirbelsäule sitzend (bis zur Spitze des Dornfortsatzes des 7. Halswirbels).
Quelle: Adaptiert von ISO/DP 7250 1980).
Präzision und Fehler
Die Präzision lebender Körpermaße muss stochastisch betrachtet werden, da der menschliche Körper sowohl als statische als auch als dynamische Struktur höchst unberechenbar ist.
Ein einzelnes Individuum kann in seiner Muskulatur und Fettleibigkeit wachsen oder sich verändern; aufgrund von Alter, Krankheit oder Unfällen Skelettveränderungen erleiden; oder Verhalten oder Körperhaltung ändern. Verschiedene Fächer unterscheiden sich durch Proportionen, nicht nur durch allgemeine Abmessungen. Hochgewachsene Personen sind nicht bloße Vergrößerungen von Kleinwüchsigen; Konstitutionstypen und Somatotypen variieren wahrscheinlich mehr als allgemeine Dimensionen.
Die Verwendung von Schaufensterpuppen, insbesondere von Schaufensterpuppen, die das 5., 50. und 95. Perzentil darstellen, für Anprobeversuche kann sehr irreführend sein, wenn Körpervariationen bei den Körperproportionen nicht berücksichtigt werden.
Fehler resultieren aus der Fehlinterpretation von Orientierungspunkten und der falschen Verwendung von Instrumenten (persönlicher Fehler), ungenauen oder ungenauen Instrumenten (instrumenteller Fehler) oder Änderungen in der Haltung des Subjekts (Subjektfehler – letzteres kann auf Kommunikationsschwierigkeiten zurückzuführen sein, wenn der kulturelle oder sprachliche Hintergrund von das Thema unterscheidet sich von dem des Betreibers).
Statistische Behandlung
Anthropometrische Daten müssen mit statistischen Verfahren behandelt werden, hauptsächlich im Bereich der Inferenzmethoden, die univariate (Mittelwert, Modus, Perzentile, Histogramme, Varianzanalyse usw.), bivariate (Korrelation, Regression) und multivariate (multiple Korrelation und Regression, Faktorenanalyse) anwenden , usw.) Methoden. Zur Klassifizierung von Menschentypen wurden verschiedene grafische Methoden entwickelt, die auf statistischen Anwendungen basieren (Anthropometrogramme, Morphosomatogramme).
Probenahme und Erhebung
Da anthropometrische Daten nicht für die gesamte Population erhoben werden können (außer im seltenen Fall einer besonders kleinen Population), ist in der Regel eine Stichprobenziehung erforderlich. Ausgangspunkt jeder anthropometrischen Erhebung sollte eine grundsätzlich stichprobenartige Stichprobe sein. Um die Zahl der gemessenen Probanden auf einem vertretbaren Niveau zu halten, muss in der Regel auf eine mehrstufig geschichtete Stichprobe zurückgegriffen werden. Dies ermöglicht eine möglichst homogene Unterteilung der Bevölkerung in mehrere Klassen oder Schichten.
Die Bevölkerung kann nach Geschlecht, Altersgruppe, geografischem Gebiet, sozialen Variablen, körperlicher Aktivität usw. unterteilt werden.
Erhebungsbögen müssen unter Berücksichtigung sowohl des Messverfahrens als auch der Datenverarbeitung gestaltet werden. Eine genaue ergonomische Untersuchung des Messverfahrens sollte durchgeführt werden, um die Ermüdung des Bedieners und mögliche Fehler zu reduzieren. Aus diesem Grund müssen Variablen nach dem verwendeten Instrument gruppiert und der Reihe nach geordnet werden, um die Anzahl der Körperbeugungen zu reduzieren, die der Bediener ausführen muss.
Um die Auswirkungen persönlicher Fehler zu verringern, sollte die Umfrage von einem Bediener durchgeführt werden. Wenn mehr als ein Bediener verwendet werden muss, ist eine Schulung erforderlich, um die Reproduzierbarkeit der Messungen sicherzustellen.
Bevölkerungsanthropometrie
Ungeachtet des stark kritisierten Begriffs „Rasse“ sind menschliche Populationen dennoch sehr unterschiedlich in der Größe der Individuen und in der Größenverteilung. Im Allgemeinen sind menschliche Populationen nicht streng mendelsch; sie sind üblicherweise das Ergebnis einer Beimischung. Manchmal leben zwei oder mehr Populationen mit unterschiedlicher Herkunft und Anpassung im selben Gebiet zusammen, ohne sich zu kreuzen. Dies erschwert die theoretische Verteilung von Merkmalen. Aus anthropometrischer Sicht sind Geschlechter unterschiedliche Populationen. Populationen von Arbeitnehmern entsprechen möglicherweise nicht genau der biologischen Population desselben Gebiets als Folge einer möglichen Eignungsauswahl oder automatischen Auswahl aufgrund der Berufswahl.
Populationen aus verschiedenen Gebieten können sich aufgrund unterschiedlicher Anpassungsbedingungen oder biologischer und genetischer Strukturen unterscheiden.
Wenn eine enge Anpassung wichtig ist, ist eine Erhebung an einer Stichprobe erforderlich.
Anpassungsversuche und Regulierung
Die Anpassung des Arbeitsplatzes oder der Ausrüstung an den Benutzer kann nicht nur von den Körpermaßen abhängen, sondern auch von solchen Variablen wie Unbequemlichkeit und Art der Tätigkeiten, Kleidung, Werkzeuge und Umgebungsbedingungen. Es kann eine Kombination aus einer Checkliste relevanter Faktoren, einem Simulator und einer Reihe von Anpassungsversuchen unter Verwendung einer Stichprobe von Probanden verwendet werden, die ausgewählt wurden, um den Bereich der Körpergrößen der erwarteten Benutzerpopulation darzustellen.
Ziel ist es, Toleranzbereiche für alle Probanden zu finden. Wenn sich die Bereiche überschneiden, ist es möglich, einen engeren Endbereich zu wählen, der nicht außerhalb der Toleranzgrenzen eines Subjekts liegt. Wenn es keine Überlappung gibt, ist es notwendig, die Struktur verstellbar zu machen oder sie in verschiedenen Größen bereitzustellen. Wenn mehr als zwei Dimensionen einstellbar sind, kann ein Proband möglicherweise nicht entscheiden, welche der möglichen Einstellungen am besten zu ihm passt.
Die Einstellbarkeit kann eine komplizierte Angelegenheit sein, insbesondere wenn unbequeme Körperhaltungen zu Ermüdung führen. Dem Benutzer, der häufig wenig oder gar nichts über seine eigenen anthropometrischen Eigenschaften weiß, müssen daher genaue Angaben gemacht werden. Im Allgemeinen sollte ein genaues Design den Anpassungsbedarf auf ein Minimum reduzieren. Auf jeden Fall sollte man sich immer vor Augen halten, dass es sich um Anthropometrie handelt, nicht nur um Technik.
Dynamische Anthropometrie
Statische Anthropometrie kann umfassende Informationen über Bewegungen liefern, wenn ein geeigneter Satz von Variablen ausgewählt wurde. Wenn Bewegungen jedoch kompliziert sind und eine enge Anpassung an das industrielle Umfeld erwünscht ist, wie bei den meisten Benutzer-Maschine- und Mensch-Fahrzeug-Schnittstellen, ist eine genaue Erfassung von Körperhaltungen und Bewegungen erforderlich. Dies kann mit geeigneten Attrappen, die das Nachzeichnen von Reichweiten ermöglichen, oder durch Fotografie erfolgen. In diesem Fall ermöglicht eine mit einem Teleobjektiv und einem anthropometrischen Stab ausgestattete Kamera, die in der Sagittalebene des Objekts platziert ist, standardisierte Aufnahmen mit geringer Bildverzerrung. Kleine Markierungen an den Artikulationen der Probanden ermöglichen die genaue Bewegungsverfolgung.
Eine andere Möglichkeit, Bewegungen zu studieren, besteht darin, Haltungsänderungen gemäß einer Reihe horizontaler und vertikaler Ebenen zu formalisieren, die durch die Artikulationen verlaufen. Auch hier ist die Verwendung computergestützter menschlicher Modelle mit CAD-Systemen (Computer Aided Design) ein praktikabler Weg, dynamische Anthropometrie in die ergonomische Arbeitsplatzgestaltung einzubeziehen.
Einführung und Konzepte
Mechanistische Toxikologie ist die Lehre davon, wie chemische oder physikalische Stoffe mit lebenden Organismen interagieren, um Toxizität zu verursachen. Die Kenntnis des Toxizitätsmechanismus einer Substanz verbessert die Fähigkeit, Toxizität zu verhindern und wünschenswertere Chemikalien zu entwickeln; sie bildet die Grundlage für die Therapie bei Überexposition und ermöglicht häufig ein tieferes Verständnis grundlegender biologischer Prozesse. Zu diesem Zweck Enzyklopädie Der Schwerpunkt liegt auf Tieren, um die Humantoxizität vorherzusagen. Verschiedene Bereiche der Toxikologie umfassen mechanistische, deskriptive, regulatorische, forensische und Umwelttoxikologie (Klaassen, Amdur und Doull 1991). All dies profitiert vom Verständnis der grundlegenden Toxizitätsmechanismen.
Warum Toxizitätsmechanismen verstehen?
Das Verständnis des Mechanismus, durch den eine Substanz Toxizität verursacht, verbessert verschiedene Bereiche der Toxikologie auf unterschiedliche Weise. Das mechanistische Verständnis hilft der staatlichen Regulierungsbehörde, rechtsverbindliche Sicherheitsgrenzwerte für die Exposition des Menschen festzulegen. Es hilft Toxikologen bei der Empfehlung von Maßnahmen zur Sanierung oder Sanierung kontaminierter Standorte und kann zusammen mit den physikalischen und chemischen Eigenschaften des Stoffes oder Gemisches zur Auswahl des erforderlichen Schutzausrüstungsgrades herangezogen werden. Mechanistisches Wissen ist auch nützlich, um die Grundlage für die Therapie und das Design neuer Arzneimittel zur Behandlung menschlicher Krankheiten zu bilden. Für den forensischen Toxikologen liefert der Toxizitätsmechanismus oft einen Einblick, wie ein chemischer oder physikalischer Stoff zum Tod oder zur Handlungsunfähigkeit führen kann.
Wenn der Toxizitätsmechanismus verstanden ist, wird die deskriptive Toxikologie nützlich, um die toxischen Wirkungen verwandter Chemikalien vorherzusagen. Es ist jedoch wichtig zu verstehen, dass ein Mangel an mechanistischen Informationen Gesundheitsfachkräfte nicht davon abhält, die menschliche Gesundheit zu schützen. Es werden umsichtige Entscheidungen auf der Grundlage von Tierversuchen und menschlicher Erfahrung getroffen, um sichere Expositionsniveaus festzulegen. Herkömmlicherweise wurde eine Sicherheitsspanne festgelegt, indem die „Stufe ohne nachteilige Wirkung“ oder eine „Stufe mit der niedrigsten nachteiligen Wirkung“ aus Tierversuchen (unter Verwendung von Designs mit wiederholter Exposition) verwendet und diese Stufe durch einen Faktor von 100 für berufliche Exposition oder 1,000 für berufliche Exposition dividiert wurde andere menschliche Umweltexposition. Der Erfolg dieses Prozesses zeigt sich an den wenigen Vorfällen von gesundheitsschädlichen Wirkungen, die der Exposition gegenüber Chemikalien bei Arbeitern zugeschrieben werden, bei denen in der Vergangenheit angemessene Expositionsgrenzwerte festgelegt und eingehalten wurden. Zudem nimmt die Lebenserwartung der Menschen weiter zu, ebenso wie die Lebensqualität. Insgesamt hat die Verwendung von Toxizitätsdaten zu einer wirksamen behördlichen und freiwilligen Kontrolle geführt. Detailliertes Wissen über toxische Mechanismen wird die Vorhersagbarkeit neuerer Risikomodelle, die derzeit entwickelt werden, verbessern und zu kontinuierlichen Verbesserungen führen.
Das Verständnis von Umweltmechanismen ist komplex und setzt ein Wissen über Ökosystemstörungen und Homöostase (Gleichgewicht) voraus. Obwohl in diesem Artikel nicht diskutiert, würde ein verbessertes Verständnis der toxischen Mechanismen und ihrer endgültigen Folgen in einem Ökosystem den Wissenschaftlern helfen, umsichtige Entscheidungen in Bezug auf den Umgang mit kommunalen und industriellen Abfallmaterialien zu treffen. Die Abfallwirtschaft ist ein wachsendes Forschungsgebiet und wird auch in Zukunft sehr wichtig sein.
Techniken zur Untersuchung von Toxizitätsmechanismen
Die meisten mechanistischen Studien beginnen mit einer deskriptiven toxikologischen Studie an Tieren oder klinischen Beobachtungen am Menschen. Idealerweise umfassen Tierversuche sorgfältige Verhaltens- und klinische Beobachtungen, eine sorgfältige biochemische Untersuchung von Elementen des Blutes und Urins auf Anzeichen einer nachteiligen Funktion wichtiger biologischer Systeme im Körper und eine Post-Mortem-Bewertung aller Organsysteme durch mikroskopische Untersuchung zur Überprüfung Verletzungen (siehe OECD-Testrichtlinien; EG-Richtlinien zur Chemikalienbewertung; US EPA-Testregeln; japanische Chemikalienvorschriften). Dies entspricht einer gründlichen körperlichen Untersuchung beim Menschen, die in einem Krankenhaus über einen Zeitraum von zwei bis drei Tagen mit Ausnahme der Obduktion stattfinden würde.
Toxizitätsmechanismen zu verstehen, ist die Kunst und Wissenschaft der Beobachtung, der Kreativität bei der Auswahl von Techniken zum Testen verschiedener Hypothesen und der innovativen Integration von Anzeichen und Symptomen in eine kausale Beziehung. Mechanistische Studien beginnen mit der Exposition, verfolgen die zeitbezogene Verteilung und den Verbleib im Körper (Pharmakokinetik) und messen die resultierende toxische Wirkung auf einer bestimmten Ebene des Systems und auf einer bestimmten Dosisebene. Verschiedene Substanzen können auf verschiedenen Ebenen des biologischen Systems wirken, indem sie Toxizität verursachen.
Belichtung
Der Expositionsweg in mechanistischen Studien ist normalerweise derselbe wie bei der Exposition beim Menschen. Der Weg ist wichtig, da neben den systemischen Wirkungen, nachdem die Chemikalie ins Blut aufgenommen und im ganzen Körper verteilt wurde, auch lokale Wirkungen am Expositionsort auftreten können. Ein einfaches, aber überzeugendes Beispiel für eine lokale Wirkung wäre eine Reizung und eventuelle Verätzung der Haut nach dem Auftragen starker Säure- oder Alkalilösungen, die zum Reinigen harter Oberflächen bestimmt sind. In ähnlicher Weise können Reizungen und Zelltod in Zellen auftreten, die die Nase und/oder Lungen auskleiden, nachdem sie reizenden Dämpfen oder Gasen, wie Stickoxiden oder Ozon, ausgesetzt wurden. (Beide sind Bestandteile der Luftverschmutzung oder des Smogs). Nach Aufnahme einer Chemikalie ins Blut durch Haut, Lunge oder Magen-Darm-Trakt wird die Konzentration in jedem Organ oder Gewebe durch viele Faktoren gesteuert, die die Pharmakokinetik der Chemikalie im Körper bestimmen. Der Körper hat die Fähigkeit, verschiedene Chemikalien zu aktivieren und zu entgiften, wie unten angegeben.
Rolle der Pharmakokinetik bei der Toxizität
Die Pharmakokinetik beschreibt die zeitlichen Zusammenhänge von chemischer Aufnahme, Verteilung, Stoffwechsel (biochemische Veränderungen im Körper) und Ausscheidung bzw. Ausscheidung aus dem Körper. In Bezug auf Toxizitätsmechanismen können diese pharmakokinetischen Variablen sehr wichtig sein und in einigen Fällen bestimmen, ob eine Toxizität auftritt oder nicht. Wenn beispielsweise ein Material nicht in ausreichender Menge absorbiert wird, tritt keine systemische Toxizität (innerhalb des Körpers) auf. Umgekehrt hat eine hochreaktive Chemikalie, die schnell (Sekunden oder Minuten) durch Verdauungs- oder Leberenzyme entgiftet wird, möglicherweise nicht die Zeit, Toxizität zu verursachen. Einige polyzyklische halogenierte Substanzen und Gemische sowie bestimmte Metalle wie Blei würden bei schneller Ausscheidung keine signifikante Toxizität verursachen; aber die Akkumulation auf ausreichend hohe Niveaus bestimmt ihre Toxizität, da die Ausscheidung nicht schnell erfolgt (manchmal in Jahren gemessen). Glücklicherweise bleiben die meisten Chemikalien nicht so lange im Körper. Die Ansammlung eines unschädlichen Materials würde immer noch keine Toxizität hervorrufen. Die Ausscheidungsrate aus dem Körper und die Entgiftung wird häufig als Halbwertszeit der Chemikalie bezeichnet, das ist die Zeit, in der 50 % der Chemikalie ausgeschieden oder in eine nicht toxische Form umgewandelt werden.
Wenn sich jedoch eine Chemikalie in einer bestimmten Zelle oder einem bestimmten Organ anreichert, kann dies ein Grund dafür sein, ihre potenzielle Toxizität in diesem Organ weiter zu untersuchen. In jüngerer Zeit wurden mathematische Modelle entwickelt, um pharmakokinetische Variablen von Tieren auf Menschen zu extrapolieren. Diese pharmakokinetischen Modelle sind äußerst nützlich, um Hypothesen zu generieren und zu testen, ob das Versuchstier eine gute Repräsentation für den Menschen sein kann. Zahlreiche Kapitel und Texte wurden zu diesem Thema verfasst (Gehring et al. 1976; Reitz et al. 1987; Nolan et al. 1995). Ein vereinfachtes Beispiel eines physiologischen Modells ist in Abbildung 1 dargestellt.
Abbildung 1. Ein vereinfachtes pharmakokinetisches Modell
Verschiedene Ebenen und Systeme können beeinträchtigt werden
Die Toxizität kann auf verschiedenen biologischen Ebenen beschrieben werden. Die Verletzung kann am ganzen Menschen (oder Tier), am Organsystem, an der Zelle oder am Molekül beurteilt werden. Organsysteme umfassen das Immun-, Atmungs-, Herz-Kreislauf-, Nieren-, Hormon-, Verdauungs-, Muskel-Skelett-, Blut-, Fortpflanzungs- und Zentralnervensystem. Einige Schlüsselorgane sind Leber, Niere, Lunge, Gehirn, Haut, Augen, Herz, Hoden oder Eierstöcke und andere wichtige Organe. Auf zellulärer/biochemischer Ebene umfassen Nebenwirkungen die Beeinträchtigung der normalen Proteinfunktion, der endokrinen Rezeptorfunktion, die Hemmung der Stoffwechselenergie oder die Hemmung oder Induktion xenobiotischer (Fremdsubstanzen) Enzyme. Unerwünschte Wirkungen auf molekularer Ebene umfassen eine Veränderung der normalen Funktion der DNA-RNA-Transkription, der spezifischen zytoplasmatischen und nukleären Rezeptorbindung und von Genen oder Genprodukten. Letztendlich wird eine Funktionsstörung in einem wichtigen Organsystem wahrscheinlich durch eine molekulare Veränderung in einer bestimmten Zielzelle innerhalb dieses Organs verursacht. Die Rückverfolgung eines Mechanismus auf einen molekularen Verursachungsursprung ist jedoch nicht immer möglich und auch nicht erforderlich. Intervention und Therapie können ohne vollständiges Verständnis des molekularen Ziels entworfen werden. Das Wissen um den spezifischen Mechanismus der Toxizität erhöht jedoch den Vorhersagewert und die Genauigkeit der Extrapolation auf andere Chemikalien. Fig. 2 ist eine schematische Darstellung der verschiedenen Ebenen, auf denen eine Störung normaler physiologischer Prozesse festgestellt werden kann. Die Pfeile zeigen an, dass die Folgen für eine Person von oben nach unten (Exposition, Pharmakokinetik bis hin zu System-/Organtoxizität) oder von unten nach oben (molekulare Veränderung, zelluläre/biochemische Wirkung bis hin zu System-/Organtoxizität) bestimmt werden können.
Abbildung 2. Repräsentation von Toxizitätsmechanismen
Beispiele für Toxizitätsmechanismen
Toxizitätsmechanismen können einfach oder sehr komplex sein. Häufig besteht ein Unterschied zwischen der Art der Toxizität, dem Toxizitätsmechanismus und dem Ausmaß der Wirkung, je nachdem, ob die Nebenwirkungen auf eine einzelne, akute hohe Dosis (wie eine versehentliche Vergiftung) oder eine niedrigere Dosis zurückzuführen sind wiederholte Exposition (durch berufliche oder umweltbedingte Exposition). Klassischerweise wird zu Testzwecken eine akute, einzelne hohe Dosis durch direkte Intubation in den Magen eines Nagetiers oder durch zwei- bis vierstündiges Aussetzen gegenüber einer Gas- oder Dampfatmosphäre verabreicht, je nachdem, was der Exposition beim Menschen am ähnlichsten ist. Die Tiere werden nach der Exposition über einen Zeitraum von zwei Wochen beobachtet, und dann werden die wichtigsten äußeren und inneren Organe auf Verletzungen untersucht. Tests mit wiederholter Gabe reichen von Monaten bis zu Jahren. Bei Nagetierspezies gelten zwei Jahre als chronische (lebenslange) Studie, die ausreicht, um Toxizität und Karzinogenität zu bewerten, während bei nichtmenschlichen Primaten zwei Jahre als subchronische (weniger als lebenslange) Studie zur Bewertung der Toxizität bei wiederholter Verabreichung angesehen würden. Nach der Exposition wird eine vollständige Untersuchung aller Gewebe, Organe und Flüssigkeiten durchgeführt, um etwaige nachteilige Wirkungen festzustellen.
Akute Toxizitätsmechanismen
Die folgenden Beispiele sind spezifisch für hochdosierte, akute Wirkungen, die zum Tod oder zu schwerer Handlungsunfähigkeit führen können. In einigen Fällen führt die Intervention jedoch zu vorübergehenden und vollständig reversiblen Wirkungen. Die Dosis oder Schwere der Exposition bestimmt das Ergebnis.
Einfache Erstickungsmittel. Der Toxizitätsmechanismus für Inertgase und einige andere nicht reaktive Substanzen ist Sauerstoffmangel (Anoxie). Diese Chemikalien, die Sauerstoffentzug im Zentralnervensystem (ZNS) verursachen, werden als Sauerstoffmangel bezeichnet einfache Erstickungsmittel. Wenn eine Person einen geschlossenen Raum betritt, der Stickstoff ohne ausreichend Sauerstoff enthält, kommt es im Gehirn zu einem sofortigen Sauerstoffmangel und führt zu Bewusstlosigkeit und schließlich zum Tod, wenn die Person nicht schnell entfernt wird. In extremen Fällen (fast null Sauerstoff) kann innerhalb weniger Sekunden Bewusstlosigkeit eintreten. Die Rettung hängt von der schnellen Entfernung in eine sauerstoffreiche Umgebung ab. Ein Überleben mit irreversiblen Hirnschäden kann durch verzögerte Rettung aufgrund des Todes von Neuronen erfolgen, die sich nicht regenerieren können.
Chemische Erstickungsmittel. Kohlenmonoxid (CO) konkurriert mit Sauerstoff um die Bindung an Hämoglobin (in roten Blutkörperchen) und entzieht dem Gewebe daher Sauerstoff für den Energiestoffwechsel; Zelltod kann die Folge sein. Die Intervention umfasst die Entfernung von der CO-Quelle und die Behandlung mit Sauerstoff. Die direkte Verwendung von Sauerstoff basiert auf der toxischen Wirkung von CO. Ein weiteres starkes chemisches Erstickungsmittel ist Cyanid. Das Cyanidion stört den Zellstoffwechsel und die Nutzung von Sauerstoff zur Energiegewinnung. Die Behandlung mit Natriumnitrit bewirkt eine Veränderung des Hämoglobins in den roten Blutkörperchen zu Methämoglobin. Methämoglobin hat eine größere Bindungsaffinität zum Cyanidion als das zelluläre Ziel von Cyanid. Folglich bindet das Methämoglobin das Cyanid und hält das Cyanid von den Zielzellen fern. Dies bildet die Grundlage für eine Antidottherapie.
Beruhigungsmittel des zentralen Nervensystems (ZNS).. Akute Toxizität ist bei einer Reihe von Stoffen wie Lösungsmitteln, die nicht reaktiv sind oder in reaktive Zwischenprodukte umgewandelt werden, durch Sedierung oder Bewusstlosigkeit gekennzeichnet. Es wird die Hypothese aufgestellt, dass die Sedierung/Anästhesie auf eine Wechselwirkung des Lösungsmittels mit den Membranen von Zellen im ZNS zurückzuführen ist, was deren Fähigkeit zur Übertragung elektrischer und chemischer Signale beeinträchtigt. Während die Sedierung als milde Form der Toxizität erscheinen mag und die Grundlage für die Entwicklung der frühen Anästhetika war, „macht die Dosis immer noch das Gift“. Wenn eine ausreichende Dosis durch Verschlucken oder Einatmen verabreicht wird, kann das Tier an Atemstillstand sterben. Wenn der Narkosetod nicht eintritt, ist diese Art von Toxizität normalerweise leicht reversibel, wenn das Subjekt aus der Umgebung entfernt wird oder die Chemikalie neu verteilt oder aus dem Körper eliminiert wird.
Skin-Effekte. Schädliche Wirkungen auf die Haut können je nach angetroffener Substanz von Reizungen bis zu Ätzwirkungen reichen. Starke Säuren und alkalische Lösungen sind mit lebendem Gewebe nicht kompatibel und ätzend, was zu chemischen Verbrennungen und möglichen Narbenbildungen führen kann. Die Narbenbildung ist auf den Tod der dermalen, tiefen Hautzellen zurückzuführen, die für die Regeneration verantwortlich sind. Niedrigere Konzentrationen können lediglich zu Reizungen der ersten Hautschicht führen.
Ein weiterer spezifischer toxischer Mechanismus der Haut ist die chemische Sensibilisierung. Beispielsweise tritt eine Sensibilisierung auf, wenn 2,4-Dinitrochlorbenzol an natürliche Proteine in der Haut bindet und das Immunsystem den veränderten proteingebundenen Komplex als Fremdmaterial erkennt. Als Reaktion auf diesen Fremdstoff aktiviert das Immunsystem spezielle Zellen, um den Fremdstoff durch Freisetzung von Mediatoren (Zytokinen) zu eliminieren, die einen Hautausschlag oder eine Dermatitis verursachen (siehe „Immuntoxikologie“). Dies ist die gleiche Reaktion des Immunsystems, wenn es Giftefeu ausgesetzt wird. Die Immunsensibilisierung ist sehr spezifisch für die jeweilige Chemikalie und erfordert mindestens zwei Expositionen, bevor eine Reaktion hervorgerufen wird. Die erste Exposition sensibilisiert (setzt die Zellen in die Lage, die Chemikalie zu erkennen), und nachfolgende Expositionen lösen die Reaktion des Immunsystems aus. Kontaktentfernung und symptomatische Therapie mit steroidhaltigen entzündungshemmenden Cremes sind in der Regel wirksam bei der Behandlung sensibilisierter Personen. In schweren oder refraktären Fällen wird ein systemisch wirkendes Immunsuppressivum wie Prednison in Verbindung mit einer topischen Behandlung verwendet.
Lungensensibilisierung. Eine Immunsensibilisierungsreaktion wird durch Toluoldiisocyanat (TDI) ausgelöst, aber der Zielort ist die Lunge. TDI-Überexposition bei anfälligen Personen verursacht Lungenödeme (Flüssigkeitsansammlung), Bronchialverengung und Atembeschwerden. Dies ist ein schwerwiegender Zustand und erfordert, dass die Person von möglichen nachfolgenden Expositionen ausgeschlossen wird. Die Behandlung ist in erster Linie symptomatisch. Haut- und Lungensensibilisierung folgen einer Dosisreaktion. Die Überschreitung des für die berufliche Exposition festgelegten Grenzwerts kann schädliche Wirkungen haben.
Augeneffekte. Die Schädigung des Auges reicht von der Rötung der äußeren Schicht (Schwimmbadrötung) über die Kataraktbildung der Hornhaut bis hin zur Schädigung der Iris (farbiger Teil des Auges). Augenreizungstests werden durchgeführt, wenn davon ausgegangen wird, dass keine ernsthaften Verletzungen auftreten werden. Viele der Mechanismen, die Hautverätzungen verursachen, können auch Augenverletzungen verursachen. Für die Haut ätzende Materialien wie starke Säuren (pH-Wert unter 2) und Laugen (pH-Wert über 11.5) werden nicht in den Augen von Tieren getestet, da die meisten aufgrund eines ähnlichen Mechanismus wie der Hautverätzung zu Verätzungen und Erblindung führen . Darüber hinaus können oberflächenaktive Mittel wie Reinigungsmittel und Tenside Augenverletzungen verursachen, die von Reizungen bis hin zu Korrosion reichen. Eine Gruppe von Stoffen, bei denen Vorsicht geboten ist, sind die positiv geladenen (kationischen) Tenside, die Verbrennungen, dauerhafte Trübung der Hornhaut und Vaskularisierung (Bildung von Blutgefäßen) verursachen können. Eine andere Chemikalie, Dinitrophenol, hat eine spezifische Wirkung auf die Kataraktbildung. Dies scheint mit der Konzentration dieser Chemikalie im Auge zusammenzuhängen, was ein Beispiel für pharmakokinetische Verteilungsspezifität ist.
Obwohl die obige Auflistung bei weitem nicht erschöpfend ist, soll sie dem Leser eine Wertschätzung für verschiedene akute Toxizitätsmechanismen vermitteln.
Subchronische und chronische Toxizitätsmechanismen
Wenn sie als einzelne hohe Dosis verabreicht werden, haben einige Chemikalien nicht den gleichen Toxizitätsmechanismus wie wenn sie wiederholt als niedrigere, aber immer noch toxische Dosis verabreicht werden. Wenn eine einzelne hohe Dosis verabreicht wird, besteht immer die Möglichkeit, dass die Fähigkeit der Person, die Chemikalie zu entgiften oder auszuscheiden, überschritten wird, und dies kann zu einer anderen toxischen Reaktion führen als wenn niedrigere wiederholte Dosen verabreicht werden. Alkohol ist ein gutes Beispiel. Hohe Alkoholdosen führen zu primären Wirkungen auf das Zentralnervensystem, während niedrigere wiederholte Dosen zu Leberschäden führen.
Anticholinesterase-Hemmung. Die meisten Organophosphat-Pestizide haben zum Beispiel eine geringe Toxizität für Säugetiere, bis sie metabolisch aktiviert werden, hauptsächlich in der Leber. Der primäre Wirkungsmechanismus von Organophosphaten ist die Hemmung der Acetylcholinesterase (AChE) im Gehirn und im peripheren Nervensystem. AChE ist das normale Enzym, das die Stimulation des Neurotransmitters Acetylcholin beendet. Eine leichte Hemmung der AChE über einen längeren Zeitraum wurde nicht mit Nebenwirkungen in Verbindung gebracht. Bei hohen Expositionsniveaus führt die Unfähigkeit, diese neuronale Stimulation zu beenden, zu einer Überstimulation des cholinergen Nervensystems. Eine cholinerge Überstimulation führt letztendlich zu einer Vielzahl von Symptomen, einschließlich Atemstillstand, gefolgt vom Tod, wenn sie nicht behandelt wird. Die primäre Behandlung ist die Verabreichung von Atropin, das die Wirkung von Acetylcholin blockiert, und die Verabreichung von Pralidoximchlorid, das die gehemmte AChE reaktiviert. Daher werden sowohl die Ursache als auch die Behandlung der Organophosphattoxizität angesprochen, indem die biochemischen Grundlagen der Toxizität verstanden werden.
Stoffwechselaktivierung. Viele Chemikalien, einschließlich Tetrachlorkohlenstoff, Chloroform, Acetylaminofluoren, Nitrosamine und Paraquat, werden metabolisch zu freien Radikalen oder anderen reaktiven Zwischenprodukten aktiviert, die die normale Zellfunktion hemmen und stören. Bei hoher Exposition führt dies zum Zelltod (siehe „Zellschädigung und Zelltod“). Während die spezifischen Wechselwirkungen und zellulären Ziele unbekannt bleiben, sind die Organsysteme, die die Fähigkeit haben, diese Chemikalien zu aktivieren, wie Leber, Niere und Lunge, alle potenzielle Ziele für Verletzungen. Insbesondere haben bestimmte Zellen innerhalb eines Organs eine größere oder geringere Fähigkeit, diese Zwischenprodukte zu aktivieren oder zu entgiften, und diese Fähigkeit bestimmt die intrazelluläre Anfälligkeit innerhalb eines Organs. Der Stoffwechsel ist ein Grund, warum ein Verständnis der Pharmakokinetik, die diese Arten von Umwandlungen und die Verteilung und Eliminierung dieser Zwischenprodukte beschreibt, wichtig ist, um den Wirkungsmechanismus dieser Chemikalien zu erkennen.
Krebsmechanismen. Krebs ist eine Vielzahl von Krankheiten, und obwohl das Verständnis bestimmter Krebsarten aufgrund der vielen molekularbiologischen Techniken, die seit 1980 entwickelt wurden, schnell zunimmt, gibt es noch viel zu lernen. Es ist jedoch klar, dass die Krebsentstehung ein mehrstufiger Prozess ist und kritische Gene der Schlüssel zu verschiedenen Krebsarten sind. Veränderungen in der DNA (somatische Mutationen) in einer Reihe dieser kritischen Gene können eine erhöhte Anfälligkeit oder kanzeröse Läsionen verursachen (siehe „Gentoxikologie“). Die Exposition gegenüber natürlichen Chemikalien (in gekochten Lebensmitteln wie Rindfleisch und Fisch) oder synthetischen Chemikalien (wie Benzidin, das als Farbstoff verwendet wird) oder physikalischen Einwirkungen (ultraviolettes Licht von der Sonne, Radon aus dem Boden, Gammastrahlung aus medizinischen Verfahren oder industriellen Aktivitäten) sind alle Mitwirkende an somatischen Genmutationen. Es gibt jedoch natürliche und synthetische Substanzen (z. B. Antioxidantien) und DNA-Reparaturprozesse, die schützen und die Homöostase aufrechterhalten. Es ist klar, dass die Genetik ein wichtiger Faktor bei Krebs ist, da genetische Krankheitssyndrome wie Xeroderma pigmentosum, bei denen eine normale DNA-Reparatur fehlt, die Anfälligkeit für Hautkrebs durch UV-Licht der Sonne dramatisch erhöhen.
Fortpflanzungsmechanismen. Ähnlich wie bei Krebs sind viele Mechanismen der Reproduktions- und/oder Entwicklungstoxizität bekannt, aber es gibt noch viel zu lernen. Es ist bekannt, dass bestimmte Viren (wie Röteln), bakterielle Infektionen und Medikamente (wie Thalidomid und Vitamin A) die Entwicklung beeinträchtigen. Kürzlich zeigten Arbeiten von Khera (1991), die von Carney (1994) überprüft wurden, gute Beweise dafür, dass die abnormen Entwicklungseffekte in Tierversuchen mit Ethylenglykol auf saure Stoffwechselprodukte der Mutter zurückzuführen sind. Dies tritt auf, wenn Ethylenglykol zu Säuremetaboliten, einschließlich Glykol- und Oxalsäure, metabolisiert wird. Die Folgewirkungen auf Plazenta und Fötus scheinen auf diesen metabolischen Vergiftungsprozess zurückzuführen zu sein.
Fazit
Die Absicht dieses Artikels ist es, einen Überblick über mehrere bekannte Toxizitätsmechanismen und die Notwendigkeit zukünftiger Studien zu geben. Es ist wichtig zu verstehen, dass mechanistisches Wissen nicht unbedingt notwendig ist, um die Gesundheit von Mensch und Umwelt zu schützen. Dieses Wissen wird die Fähigkeit des Fachmanns verbessern, die Toxizität besser vorherzusagen und zu handhaben. Die tatsächlichen Techniken, die zur Aufklärung eines bestimmten Mechanismus verwendet werden, hängen vom kollektiven Wissen der Wissenschaftler und dem Denken derjenigen ab, die Entscheidungen über die menschliche Gesundheit treffen.
Expositionsbewertung
Die Bewertung von Expositionen ist ein entscheidender Schritt bei der Identifizierung von Gefahren am Arbeitsplatz durch epidemiologische Untersuchungen. Der Expositionsbeurteilungsprozess kann in eine Reihe von Tätigkeiten unterteilt werden. Diese beinhalten:
- Zusammenstellung eines Verzeichnisses potenziell toxischer Stoffe und Mischungen, die in der angestrebten Arbeitsumgebung vorhanden sind
- Bestimmung, wie Expositionen auftreten und wie wahrscheinlich es ist, dass sie zwischen den Mitarbeitern variieren
- Auswahl geeigneter Messgrößen oder Indizes zur Quantifizierung von Expositionen
- Sammeln von Daten, die es den Studienteilnehmern ermöglichen, qualitative oder quantitative Expositionswerte für jede Maßnahme zuzuordnen. Wenn möglich, sollten diese Tätigkeiten unter Anleitung eines qualifizierten Industriehygienikers durchgeführt werden.
Arbeitsmedizinische Studien werden oft wegen Unzulänglichkeiten bei der Bewertung von Expositionen kritisiert. Unzulänglichkeiten können zu einer differentiellen oder nicht differentiellen Fehlklassifizierung der Exposition und daraus resultierender Verzerrung oder Präzisionsverlust in den Expositions-Wirkungs-Analysen führen. Bemühungen zur Verbesserung der Situation werden durch mehrere kürzlich durchgeführte internationale Konferenzen und Texte zu diesem Thema belegt (ACGIH 1991; Armstrong et al. 1992; Proceedings of the Conference on Retrospective Assessment of Occupational Exposures in Epidemiology 1995). Offensichtlich bieten technische Entwicklungen neue Möglichkeiten zur Verbesserung der Expositionsbewertung. Diese Entwicklungen umfassen Verbesserungen bei der analytischen Instrumentierung, ein besseres Verständnis pharmakokinetischer Prozesse und die Entdeckung neuer Expositions-Biomarker. Da arbeitsmedizinische Studien häufig auf historischen Expositionsinformationen beruhen, für die keine spezifische Überwachung durchgeführt worden wäre, fügt die Notwendigkeit einer rückwirkenden Expositionsbewertung diesen Studien eine zusätzliche Dimension der Komplexität hinzu. Es werden jedoch weiterhin verbesserte Standards für die Bewertung und die Gewährleistung der Zuverlässigkeit solcher Bewertungen entwickelt (Sieemiatycki et al. 1986). Prospektive Expositionsabschätzungen können natürlich leichter validiert werden.
Die Belichtung bezeichnet die Konzentration eines Agens an der Grenze zwischen Individuum und Umwelt. Eine Exposition wird normalerweise angenommen, wenn bekannt ist, dass ein Arbeitsstoff in einer Arbeitsumgebung vorhanden ist, und eine vernünftige Erwartung besteht, dass ein Mitarbeiter mit diesem Arbeitsstoff in Kontakt kommt. Expositionen können als zeitgewichtete durchschnittliche 8-Stunden-Konzentration (TWA) ausgedrückt werden, die ein Maß für die Expositionsintensität ist, die über eine 8-stündige Arbeitsschicht gemittelt wurde. Spitzenkonzentrationen sind Intensitäten, die über kürzere Zeiträume, z. B. 15 Minuten, gemittelt werden. Die kumulative Exposition ist ein Maß für das Produkt aus durchschnittlicher Intensität und Dauer (z. B. eine mittlere 8-Stunden-TWA-Konzentration multipliziert mit den Jahren, in denen bei dieser mittleren Konzentration gearbeitet wurde). Abhängig von der Art der Studie und den interessierenden Gesundheitsergebnissen kann eine Bewertung der Spitzen-, Durchschnittsintensitäts-, kumulativen oder verzögerten Expositionen wünschenswert sein.
Im Gegensatz, empfohlen bezieht sich auf die Abscheidung oder Absorption eines Mittels pro Zeiteinheit. Die Dosis oder die tägliche Aufnahme eines Mittels kann abgeschätzt werden, indem Umgebungsmessdaten mit Standardannahmen bezüglich unter anderem Atemfrequenzen und dermaler Penetration kombiniert werden. Alternativ kann die Aufnahme auf der Grundlage von Biomonitoring-Daten geschätzt werden. Die Dosis würde idealerweise an dem interessierenden Zielorgan gemessen.
Wichtige Faktoren der Expositionsbeurteilung sind:
- Identifizierung der relevanten Agenten
- Bestimmung ihres Vorhandenseins und ihrer Konzentration in geeigneten Umweltmedien (z. B. Luft, Kontaktflächen)
- Bewertung der wahrscheinlichen Aufnahmewege (Inhalation, Aufnahme über die Haut, Verschlucken), des zeitlichen Verlaufs der Exposition (tägliche Schwankungen) und der kumulativen Expositionsdauer, ausgedrückt in Wochen, Monaten oder Jahren
- Bewertung der Wirksamkeit von technischen und persönlichen Kontrollen (z. B. die Verwendung von Schutzkleidung und Atemschutz kann Expositionen vermitteln) und schließlich
- Wirt und andere Erwägungen, die Zielorgankonzentrationen modulieren können.
Dazu gehören das körperliche Niveau der Arbeitstätigkeit und der vorherige Gesundheitszustand von Personen. Bei der Beurteilung der Exposition gegenüber Stoffen, die persistent sind oder zur Bioakkumulation neigen (z. B. bestimmte Metalle, Radionuklide oder stabile organische Verbindungen), ist besondere Sorgfalt geboten. Bei diesen Materialien können die inneren Körperbelastungen selbst bei scheinbar niedrigen Umweltkonzentrationen schleichend zunehmen.
Auch wenn die Situation recht komplex sein kann, ist sie es oft nicht. Sicherlich stammen viele wertvolle Beiträge zur Identifizierung von Berufsgefahren aus Studien, die vernünftige Ansätze zur Expositionsbewertung verwenden. Zu den Informationsquellen, die bei der Identifizierung und Kategorisierung von Expositionen hilfreich sein können, gehören:
- Mitarbeitergespräche
- Personal- und Produktionsaufzeichnungen des Arbeitgebers (dazu gehören Arbeitsaufzeichnungen, Stellenbeschreibungen, Anlagen- und Prozesshistorien und Chemikalieninventare)
- Experten Urteil
- Arbeitshygieneaufzeichnungen (Bereichs-, Personen- und Compliance-Überwachung und Oberflächenwischproben zusammen mit Gesundheitsgefährdungs- oder umfassenden Untersuchungsberichten)
- Interviews mit langjährigen oder pensionierten Mitarbeitern und
- Biomonitoring-Daten.
Eine möglichst detaillierte Kategorisierung einzelner Engagements hat mehrere Vorteile. Die Aussagekraft einer Studie wird natürlich in dem Maße gesteigert, in dem die relevanten Expositionen angemessen beschrieben wurden. Zweitens kann die Glaubwürdigkeit der Befunde erhöht werden, da dem Confounding-Potenzial zufriedenstellender begegnet werden kann. Beispielsweise unterscheiden sich Referenten und exponierte Personen im Expositionsstatus, können sich aber auch in Bezug auf andere gemessene und nicht gemessene erklärende Faktoren für die interessierende Krankheit unterscheiden. Wenn jedoch innerhalb der Studienpopulation ein Expositionsgradient festgestellt werden kann, ist es weniger wahrscheinlich, dass derselbe Grad an Confounding innerhalb der Expositionsuntergruppen bestehen bleibt, wodurch die Studienergebnisse insgesamt gestärkt werden.
Job-Exposure-Matrizen
Einer der praktischeren und häufiger verwendeten Ansätze zur Expositionsbewertung war die indirekte Schätzung der Exposition auf der Grundlage von Berufsbezeichnungen. Die Verwendung von Job-Exposure-Matrizen kann effektiv sein, wenn vollständige Arbeitsverläufe verfügbar sind und sowohl die Aufgaben als auch die Expositionen, die mit den zu studierenden Jobs verbunden sind, eine angemessene Konstanz aufweisen. Im weitesten Sinne wurden standardmäßige Branchen- und Berufsbezeichnungsgruppierungen aus routinemäßig erhobenen Volkszählungsdaten oder Berufsdaten auf Sterbeurkunden entwickelt. Leider beschränken sich die in diesen großen Aktensystemen geführten Informationen oft auf den „aktuellen“ oder „üblichen“ Beruf. Da die Standardgruppierungen außerdem die Bedingungen an bestimmten Arbeitsplätzen nicht berücksichtigen, müssen sie in der Regel als grobe Expositionssurrogate betrachtet werden.
Für gemeinschafts- und registerbasierte Fall-Kontroll-Studien wurde eine detailliertere Expositionsbewertung erreicht, indem Expertenmeinungen verwendet wurden, um Daten aus dem beruflichen Werdegang, die durch persönliche Interviews erhalten wurden, in halbquantitative Bewertungen wahrscheinlicher Expositionen gegenüber bestimmten Wirkstoffen zu übersetzen (Sieemiatycki et al. 1986 ). Experten wie Chemiker und Industriehygieniker werden aufgrund ihres Wissens und ihrer Vertrautheit mit verschiedenen industriellen Prozessen ausgewählt, um bei der Expositionsbewertung zu helfen. Durch die Kombination der detaillierten Fragebogendaten mit dem Wissen über industrielle Prozesse war dieser Ansatz hilfreich bei der Charakterisierung von Expositionsunterschieden zwischen Arbeitsstätten.
Der Job-Exposure-Matrix-Ansatz wurde auch erfolgreich in branchen- und unternehmensspezifischen Studien eingesetzt (Gamble und Spirtas 1976). Individuelle Jobverläufe (eine chronologische Auflistung früherer Abteilungs- und Jobzuweisungen für jeden Mitarbeiter) werden häufig in den Personalakten des Unternehmens aufbewahrt und bieten, sofern verfügbar, einen vollständigen Jobverlauf für die Mitarbeiter, während sie in dieser Einrichtung arbeiten. Diese Daten können durch persönliche Befragungen der Studienteilnehmer ergänzt werden. Im nächsten Schritt werden alle während der Studienzeit verwendeten Berufsbezeichnungen und Abteilungs- bzw. Arbeitsbereichsbezeichnungen inventarisiert. Diese können in großen Anlagen mit mehreren Prozessen oder in Unternehmen innerhalb einer Branche leicht in die Hunderte oder sogar Tausende gehen, wenn Produktion, Wartung, Forschung, Engineering, Anlagenunterstützungsdienste und Verwaltungsaufgaben alle über einen Zeitraum (oft mehrere Jahrzehnte) betrachtet werden. Änderungen in industriellen Prozessen ermöglichen. Die Datenkonsolidierung kann erleichtert werden, indem eine Computerdatei aller Aufzeichnungen des Arbeitsverlaufs erstellt wird und dann Bearbeitungsroutinen verwendet werden, um die Berufsbezeichnungsterminologie zu standardisieren. Diese Jobs mit relativ homogenen Expositionen können kombiniert werden, um den Prozess der Verknüpfung von Expositionen mit einzelnen Jobs zu vereinfachen. Die Gruppierung von Arbeitsplätzen und Arbeitsorten sollte jedoch nach Möglichkeit durch Messdaten gestützt werden, die nach einer fundierten Stichprobenstrategie erhoben wurden.
Auch bei computergestützten Arbeitsverläufen kann eine nachträgliche Zuordnung von Expositionsdaten zu Personen eine schwierige Aufgabe sein. Sicherlich werden sich die Bedingungen am Arbeitsplatz ändern, wenn sich Technologien ändern, sich die Produktnachfrage ändert und neue Vorschriften eingeführt werden. In vielen Branchen kann es auch zu Änderungen bei Produktformulierungen und saisonalen Produktionsmustern kommen. Über einige Änderungen können dauerhafte Aufzeichnungen geführt werden. Es ist jedoch weniger wahrscheinlich, dass Aufzeichnungen über saisonale und andere marginale Prozess- und Produktionsänderungen aufbewahrt werden. Mitarbeiter können auch geschult werden, um mehrere Jobs auszuführen, und dann zwischen den Jobs wechseln, wenn sich die Produktionsanforderungen ändern. All diese Umstände erhöhen die Komplexität der Expositionsprofile der Mitarbeiter. Dennoch gibt es auch Arbeitsumgebungen, die seit vielen Jahren relativ unverändert geblieben sind. Letztendlich muss jede Arbeitseinstellung für sich bewertet werden.
Letztendlich wird es notwendig sein, die Arbeitslebens-Expositionsgeschichte jeder Person in einer Studie zusammenzufassen. Es wurde ein beträchtlicher Einfluss auf die endgültigen Expositions-Wirkungs-Risikomaße nachgewiesen (Suarez-Almazor et al. 1992), und daher muss bei der Auswahl des am besten geeigneten zusammenfassenden Expositionsmaßes große Sorgfalt walten.
Arbeitshygiene – Umweltmessung
Die Überwachung der Arbeitsbelastung ist eine grundlegende kontinuierliche Aktivität zum Schutz der Gesundheit der Mitarbeiter. So können zum Zeitpunkt der Planung einer epidemiologischen Studie bereits arbeitshygienische Aufzeichnungen vorliegen. Wenn dies der Fall ist, sollten diese Daten überprüft werden, um festzustellen, wie gut die Zielpopulation abgedeckt ist, wie viele Jahre Daten in den Dateien vertreten sind und wie einfach die Messungen mit Jobs, Arbeitsbereichen und Personen verknüpft werden können. Diese Feststellungen werden sowohl bei der Beurteilung der Durchführbarkeit der epidemiologischen Studie als auch bei der Identifizierung von Datenlücken hilfreich sein, die durch zusätzliche Probenahmen der Exposition geschlossen werden könnten.
Besonders wichtig ist die Frage, wie Messdaten am besten mit bestimmten Jobs und Personen verknüpft werden können. Probenahmen aus Bereichen und Atemzonen können für Industriehygieniker hilfreich sein, um Emissionsquellen für Korrekturmaßnahmen zu identifizieren, könnten jedoch weniger nützlich sein, um die tatsächliche Exposition der Mitarbeiter zu charakterisieren, es sei denn, es wurden sorgfältige Zeitstudien der Arbeitsaktivitäten der Mitarbeiter durchgeführt. Beispielsweise kann eine kontinuierliche Bereichsüberwachung zu bestimmten Tageszeiten Exkursionsbelastungen erkennen, es bleibt jedoch die Frage, ob sich Mitarbeiter zu diesem Zeitpunkt im Arbeitsbereich aufgehalten haben oder nicht.
Personenbezogene Probenahmedaten liefern im Allgemeinen genauere Schätzungen der Mitarbeiterexposition, solange die Probenahme unter repräsentativen Bedingungen durchgeführt wird, die Verwendung persönlicher Schutzausrüstung angemessen berücksichtigt wird und die Arbeitsaufgaben und Prozessbedingungen von Tag zu Tag relativ konstant sind. Personenbezogene Proben können durch die Verwendung persönlicher Identifikatoren leicht mit dem einzelnen Mitarbeiter verknüpft werden. Diese Daten können nach Bedarf auf andere Mitarbeiter in denselben Jobs und auf andere Zeiträume verallgemeinert werden. Aufgrund ihrer eigenen Erfahrung haben Rappaport et al. (1993) haben davor gewarnt, dass die Expositionskonzentrationen selbst bei Mitarbeitern, die als homogene Expositionsgruppen eingestuft sind, sehr unterschiedlich sein können. Auch hier ist Expertenmeinung erforderlich, um zu entscheiden, ob von homogenen Expositionsgruppen ausgegangen werden kann oder nicht.
Forscher haben erfolgreich einen Arbeitsplatz-Expositions-Matrix-Ansatz mit der Nutzung von Umweltmessdaten kombiniert, um die Expositionen innerhalb der Zellen der Matrix abzuschätzen. Bei fehlenden Messdaten können ggf. Datenlücken durch Expositionsmodellierung geschlossen werden. Im Allgemeinen beinhaltet dies die Entwicklung eines Modells zur Zuordnung von Umweltkonzentrationen zu leichter zu beurteilenden Determinanten von Expositionskonzentrationen (z. B. Produktionsvolumen, physische Eigenschaften der Anlage einschließlich der Verwendung von Abluftsystemen, Flüchtigkeit der Wirkstoffe und Art der Arbeitstätigkeit). Das Modell wird für Arbeitsumgebungen mit bekannten Umweltkonzentrationen konstruiert und dann verwendet, um Konzentrationen in ähnlichen Arbeitsumgebungen abzuschätzen, denen Messdaten fehlen, die jedoch Informationen über solche Parameter wie Bestandteile und Produktionsmengen haben. Dieser Ansatz kann insbesondere für die retrospektive Schätzung von Expositionen hilfreich sein.
Ein weiteres wichtiges Bewertungsthema ist der Umgang mit der Exposition gegenüber Gemischen. Erstens liegt aus analytischer Sicht der separate Nachweis chemisch verwandter Verbindungen und die Eliminierung von Interferenzen durch andere in der Probe vorhandene Substanzen möglicherweise nicht innerhalb der Möglichkeiten des Analyseverfahrens. Die verschiedenen Limitationen der Analyseverfahren zur Bereitstellung von Messdaten müssen evaluiert und die Studienziele entsprechend angepasst werden. Zweitens kann es sein, dass bestimmte Wirkstoffe fast immer zusammen verwendet werden und daher in ungefähr den gleichen relativen Anteilen in der gesamten untersuchten Arbeitsumgebung vorkommen. In diesem Fall interne statistische Auswertungen an sich nicht hilfreich bei der Unterscheidung, ob Wirkungen auf einen oder die anderen Wirkstoffe oder auf eine Kombination der Wirkstoffe zurückzuführen sind. Solche Beurteilungen wären nur auf der Grundlage externer Studien möglich, in denen die gleichen Wirkstoffkombinationen nicht aufgetreten sind. Schließlich kann es in Situationen, in denen je nach Produktspezifikation verschiedene Materialien austauschbar verwendet werden (z. B. die Verwendung verschiedener Farbstoffe, um gewünschte Farbkontraste zu erhalten), unmöglich sein, Wirkungen einem bestimmten Mittel zuzuschreiben.
Biologische Überwachung
Biomarker sind molekulare, biochemische oder zelluläre Veränderungen, die in biologischen Medien wie menschlichem Gewebe, Zellen oder Flüssigkeiten gemessen werden können. Ein Hauptgrund für die Entwicklung von Expositions-Biomarkern ist die Bereitstellung einer Schätzung der internen Dosis für einen bestimmten Wirkstoff. Dieser Ansatz ist besonders nützlich, wenn mehrere Expositionswege wahrscheinlich sind (z. B. Einatmen und Hautabsorption), wenn Schutzkleidung zeitweise getragen wird oder wenn die Expositionsbedingungen unvorhersehbar sind. Biomonitoring kann besonders vorteilhaft sein, wenn bekannt ist, dass die interessierenden Wirkstoffe relativ lange biologische Halbwertszeiten haben. Aus statistischer Sicht kann ein Vorteil des biologischen Monitorings gegenüber dem Luftmonitoring bei Wirkstoffen mit einer Halbwertszeit von nur zehn Stunden gesehen werden, abhängig vom Grad der Umweltvariabilität (Droz und Wu 1991). Die außerordentlich langen Halbwertszeiten von Materialien wie chlorierten Dioxinen (gemessen in Jahren) machen diese Verbindungen zu idealen Kandidaten für die biologische Überwachung. Wie bei Analysemethoden zur Messung von Luftkonzentrationen muss man sich möglicher Interferenzen bewusst sein. Bevor beispielsweise ein bestimmter Metabolit als Biomarker verwendet wird, sollte bestimmt werden, ob andere gängige Substanzen, wie die in bestimmten Medikamenten und im Zigarettenrauch enthaltenen, zum selben Endpunkt metabolisiert werden könnten oder nicht. Im Allgemeinen sind grundlegende Kenntnisse der Pharmakokinetik eines Wirkstoffs erforderlich, bevor das biologische Monitoring als Grundlage für die Expositionsbewertung verwendet wird.
Die häufigsten Messpunkte sind Alveolarluft, Urin und Blut. Alveolarluftproben können hilfreich sein, um kurzfristige hohe Lösungsmittelbelastungen zu charakterisieren, die innerhalb von Minuten oder Stunden nach der Entnahme der Probe aufgetreten sind. Typischerweise werden Urinproben gesammelt, um die Ausscheidungsraten für Metaboliten der interessierenden Verbindung zu bestimmen. Blutproben können zur direkten Messung der Verbindung, zur Messung von Metaboliten oder zur Bestimmung von Protein- oder DNA-Addukten (z. B. Albumin- oder Hämoglobin-Addukte und DNA-Addukte in zirkulierenden Lymphozyten) entnommen werden. Zugängliche Gewebezellen, wie z. B. Epithelzellen aus dem bukkalen Bereich des Mundes, können ebenfalls zur Identifizierung von DNA-Addukten entnommen werden.
Die Bestimmung der Cholinesterase-Aktivität in roten Blutkörperchen und Plasma veranschaulicht die Verwendung biochemischer Veränderungen als Maß für die Exposition. Organophosphor-Pestizide hemmen die Cholinesterase-Aktivität, und daher kann die Messung dieser Aktivität vor und nach einer wahrscheinlichen Exposition gegenüber diesen Verbindungen ein nützlicher Indikator für die Expositionsintensität sein. Je weiter man jedoch durch das Spektrum der biologischen Veränderungen fortschreitet, desto schwieriger wird es, zwischen Expositions- und Wirkungsbiomarkern zu unterscheiden. Im Allgemeinen sind Wirkungsmaße in der Regel unspezifisch für den interessierenden Stoff, und daher müssen möglicherweise andere mögliche Erklärungen für die Wirkung bewertet werden, um die Verwendung dieses Parameters als Expositionsmaß zu unterstützen. Expositionsmessungen sollten entweder direkt mit dem interessierenden Agens verbunden sein oder es sollte eine solide Grundlage für die Verknüpfung jeglicher indirekten Messung mit dem Agens geben. Trotz dieser Einschränkungen ist die biologische Überwachung viel versprechend als Mittel zur Verbesserung der Expositionsabschätzung zur Unterstützung epidemiologischer Studien.
Schlussfolgerungen
Bei Vergleichen in berufsepidemiologischen Studien muss eine Gruppe von Arbeitnehmern mit Exposition gegenüber einer Gruppe von Arbeitnehmern ohne Exposition verglichen werden. Solche Unterscheidungen sind grob, können aber hilfreich sein, um Problembereiche zu identifizieren. Je verfeinerter die Expositionsmessung ist, desto nützlicher wird die Studie jedoch sein, insbesondere im Hinblick auf ihre Fähigkeit, angemessen zielgerichtete Interventionsprogramme zu identifizieren und zu entwickeln.
Muskelarbeit
Muskelarbeit in beruflichen Aktivitäten
In den Industrieländern sind noch etwa 20 % der Erwerbstätigen in Tätigkeiten beschäftigt, die Muskelkraft erfordern (Rutenfranz et al. 1990). Die Zahl der konventionellen schweren körperlichen Tätigkeiten hat abgenommen, andererseits sind viele Tätigkeiten statischer, asymmetrischer und stationärer geworden. In Entwicklungsländern ist Muskelarbeit in allen Formen immer noch weit verbreitet.
Muskelarbeit bei beruflichen Tätigkeiten kann grob in vier Gruppen eingeteilt werden: schwere dynamische Muskelarbeit, manuelle Materialhandhabung, statische Arbeit und repetitive Arbeit. Schwere dynamische Arbeitsaufgaben finden sich beispielsweise in der Forstwirtschaft, der Landwirtschaft und dem Baugewerbe. Die Materialhandhabung ist beispielsweise in der Pflege, im Transportwesen und in der Lagerhaltung üblich, während statische Belastungen in der Büroarbeit, der Elektronikindustrie und bei Reparatur- und Wartungsarbeiten auftreten. Repetitive Arbeitsaufgaben finden sich beispielsweise in der Lebensmittel- und Holz verarbeitenden Industrie.
Es ist wichtig zu beachten, dass manuelle Materialhandhabung und repetitive Arbeit grundsätzlich entweder dynamische oder statische Muskelarbeit oder eine Kombination aus diesen beiden sind.
Physiologie der Muskelarbeit
Dynamische Muskelarbeit
Bei dynamischer Arbeit kontrahieren und entspannen sich aktive Skelettmuskeln rhythmisch. Der Blutfluss zu den Muskeln wird erhöht, um den Stoffwechselanforderungen gerecht zu werden. Die erhöhte Durchblutung wird durch erhöhtes Pumpen des Herzens (Herzzeitvolumen), verringerte Durchblutung in inaktiver Bereiche wie Nieren und Leber und eine erhöhte Anzahl offener Blutgefäße in der arbeitenden Muskulatur erreicht. Herzfrequenz, Blutdruck und Sauerstoffentzug in der Muskulatur steigen linear zur Arbeitsintensität. Auch die Lungenventilation wird durch tieferes Atmen und erhöhte Atemfrequenz erhöht. Der Zweck der Aktivierung des gesamten Herz-Kreislauf-Systems besteht darin, die Sauerstoffzufuhr zu den aktiven Muskeln zu verbessern. Der bei schwerer dynamischer Muskelarbeit gemessene Sauerstoffverbrauch zeigt die Intensität der Arbeit an. Der maximale Sauerstoffverbrauch (VO2max) gibt die maximale Kapazität der Person für aerobes Training an. Sauerstoffverbrauchswerte können in Energieverbrauch umgerechnet werden (1 Liter Sauerstoffverbrauch pro Minute entspricht ca. 5 kcal/min oder 21 kJ/min).
Bei dynamischer Arbeit, wenn die aktive Muskelmasse kleiner ist (wie in den Armen), sind die maximale Arbeitsleistung und der maximale Sauerstoffverbrauch geringer als bei dynamischer Arbeit mit großen Muskeln. Bei gleicher externer Arbeitsleistung ruft dynamische Arbeit mit kleinen Muskeln höhere kardiorespiratorische Reaktionen hervor (z. B. Herzfrequenz, Blutdruck) als Arbeit mit großen Muskeln (Abbildung 1).
Abbildung 1. Statische versus dynamische Arbeit
Statische Muskelarbeit
Bei statischer Arbeit erzeugt die Muskelkontraktion keine sichtbare Bewegung, wie beispielsweise in einem Glied. Statische Arbeit erhöht den Druck innerhalb des Muskels, was zusammen mit der mechanischen Kompression die Blutzirkulation teilweise oder vollständig blockiert. Die Zufuhr von Nährstoffen und Sauerstoff zum Muskel und der Abtransport von Stoffwechselendprodukten aus dem Muskel werden behindert. So ermüden Muskeln bei statischer Arbeit leichter als bei dynamischer Arbeit.
Das auffälligste Kreislaufmerkmal statischer Arbeit ist ein Anstieg des Blutdrucks. Herzfrequenz und Herzzeitvolumen ändern sich nicht wesentlich. Ab einer bestimmten Belastungsintensität steigt der Blutdruck in direktem Zusammenhang mit der Intensität und Dauer der Belastung. Darüber hinaus erzeugt statisches Training mit großen Muskelgruppen bei gleicher relativer Anstrengungsintensität eine stärkere Blutdruckreaktion als Training mit kleineren Muskeln. (Siehe Abbildung 2)
Abbildung 2. Das erweiterte Spannungs-Dehnungs-Modell modifiziert nach Rohmert (1984)
Prinzipiell ist die Regulation von Belüftung und Kreislauf bei statischer Arbeit ähnlich wie bei dynamischer Arbeit, jedoch sind die Stoffwechselsignale der Muskulatur stärker und bewirken ein anderes Reaktionsmuster.
Folgen muskulärer Überlastung bei beruflichen Aktivitäten
Der Grad der körperlichen Belastung, die ein Arbeiter bei Muskelarbeit erfährt, hängt von der Größe der arbeitenden Muskelmasse, der Art der Muskelkontraktionen (statisch, dynamisch), der Intensität der Kontraktionen und individuellen Eigenschaften ab.
Wenn die Muskelbelastung die körperlichen Fähigkeiten des Arbeiters nicht übersteigt, passt sich der Körper an die Belastung an und die Erholung erfolgt schnell, wenn die Arbeit beendet wird. Ist die Muskelbelastung zu hoch, kommt es zu Ermüdung, verminderter Leistungsfähigkeit und verlangsamter Erholung. Spitzenbelastungen oder längere Überlastungen können zu Organschäden (in Form von Berufs- oder arbeitsbedingten Erkrankungen) führen. Andererseits kann Muskelarbeit bestimmter Intensität, Häufigkeit und Dauer auch zu Trainingseffekten führen, während andererseits eine zu geringe muskuläre Beanspruchung zu Detrainingseffekten führen kann. Diese Beziehungen werden durch die sog erweitertes Spannungs-Dehnungs-Konzept entwickelt von Rohmert (1984) (Abbildung 3).
Abbildung 3. Analyse akzeptabler Workloads
Im Allgemeinen gibt es wenig epidemiologische Beweise dafür, dass Muskelüberlastung ein Risikofaktor für Krankheiten ist. In körperlich anstrengenden Berufen, insbesondere bei älteren Arbeitnehmern, treffen jedoch ein schlechter Gesundheitszustand, eine Behinderung und eine subjektive Überlastung am Arbeitsplatz aufeinander. Darüber hinaus hängen viele Risikofaktoren für arbeitsbedingte Muskel-Skelett-Erkrankungen mit verschiedenen Aspekten der muskulären Arbeitsbelastung zusammen, wie z. B. Kraftaufwand, schlechte Arbeitshaltungen, Heben und plötzliche Spitzenbelastungen.
Eines der Ziele der Ergonomie war es, akzeptable Grenzen für Muskelarbeitsbelastungen zu bestimmen, die zur Vorbeugung von Ermüdung und Störungen angewendet werden könnten. Während die Prävention chronischer Wirkungen im Mittelpunkt der Epidemiologie steht, befasst sich die Arbeitsphysiologie meist mit kurzfristigen Wirkungen, also Ermüdung bei Arbeitsaufgaben oder während eines Arbeitstages.
Akzeptable Arbeitsbelastung bei schwerer dynamischer Muskelarbeit
Die Bewertung der akzeptablen Arbeitsbelastung bei dynamischen Arbeitsaufgaben basiert traditionell auf Messungen des Sauerstoffverbrauchs (oder entsprechend des Energieverbrauchs). Der Sauerstoffverbrauch lässt sich relativ einfach im Feld mit tragbaren Geräten (z. B. Douglas-Tasche, Max-Planck-Respirometer, Oxylog, Cosmed) messen oder aus Herzfrequenzmessungen abschätzen, die z. B. am Arbeitsplatz zuverlässig durchgeführt werden können , mit dem SportTester-Gerät. Die Verwendung der Herzfrequenz bei der Schätzung des Sauerstoffverbrauchs erfordert, dass sie individuell gegen den gemessenen Sauerstoffverbrauch in einem Standardarbeitsmodus im Labor kalibriert wird, dh der Untersucher muss den Sauerstoffverbrauch des einzelnen Subjekts bei einer gegebenen Herzfrequenz kennen. Herzfrequenzaufzeichnungen sollten mit Vorsicht behandelt werden, da sie auch von Faktoren wie körperlicher Fitness, Umgebungstemperatur, psychischen Faktoren und der Größe der aktiven Muskelmasse beeinflusst werden. Daher können Herzfrequenzmessungen zu Überschätzungen des Sauerstoffverbrauchs führen, ebenso wie Sauerstoffverbrauchswerte zu Unterschätzungen der globalen physiologischen Belastung führen können, indem sie nur den Energiebedarf widerspiegeln.
Relative aerobe Belastung (RAS) ist definiert als der Bruchteil (ausgedrückt in Prozent) des Sauerstoffverbrauchs eines Arbeiters, gemessen am Arbeitsplatz, relativ zu seiner VO2max im Labor gemessen. Wenn nur Herzfrequenzmessungen verfügbar sind, kann eine gute Annäherung an RAS erfolgen, indem ein Wert für den prozentualen Herzfrequenzbereich (% HF-Bereich) mit der sogenannten Karvonen-Formel wie in Abbildung 3 berechnet wird.
VO2max wird normalerweise auf einem Fahrradergometer oder Laufband gemessen, bei denen der mechanische Wirkungsgrad hoch ist (20-25%). Wenn die aktive Muskelmasse kleiner oder die statische Komponente höher ist, wird VO2max und die mechanische Effizienz wird geringer sein als im Fall von Übungen mit großen Muskelgruppen. Beispielsweise hat sich herausgestellt, dass bei der Sortierung von Postpaketen die VO2max der Arbeiter betrug nur 65 % des auf einem Fahrradergometer gemessenen Maximums, und die mechanische Effizienz der Aufgabe betrug weniger als 1 %. Wenn Richtlinien auf dem Sauerstoffverbrauch basieren, sollte der Testmodus im Maximaltest so nah wie möglich an der realen Aufgabe sein. Dieses Ziel ist jedoch schwer zu erreichen.
Gemäß der klassischen Studie von Åstrand (1960) sollte die RAS während eines achtstündigen Arbeitstages 50 % nicht überschreiten. In ihren Experimenten nahm bei einer Arbeitsbelastung von 50 % das Körpergewicht ab, die Herzfrequenz erreichte nicht den stabilen Zustand und das subjektive Unbehagen nahm im Laufe des Tages zu. Sie empfahl eine RAS-Grenze von 50 % für Männer und Frauen. Später fand sie heraus, dass Bauarbeiter während eines Arbeitstages spontan ein durchschnittliches RAS-Niveau von 40 % (Bereich 25-55 %) wählten. Mehrere neuere Studien haben gezeigt, dass die akzeptable RAS unter 50 % liegt. Die meisten Autoren empfehlen 30-35 % als akzeptables RAS-Niveau für den gesamten Arbeitstag.
Ursprünglich wurden die akzeptablen RAS-Werte für reine dynamische Muskelarbeit entwickelt, die im realen Arbeitsleben selten vorkommt. Es kann vorkommen, dass akzeptable RAS-Werte beispielsweise bei einer Hebeaufgabe nicht überschritten werden, aber die lokale Belastung des Rückens kann akzeptable Werte erheblich überschreiten. Trotz ihrer Einschränkungen wurde die RAS-Bestimmung in großem Umfang zur Bewertung der körperlichen Belastung in verschiedenen Berufen eingesetzt.
Neben der Messung oder Abschätzung des Sauerstoffverbrauchs stehen auch andere nützliche feldphysiologische Methoden zur Quantifizierung der körperlichen Belastung oder Beanspruchung bei schwerer dynamischer Arbeit zur Verfügung. Bei der Abschätzung des Energieverbrauchs können Beobachtungstechniken eingesetzt werden (z. B. mit Hilfe des Edholm-Skala) (Edholm 1966). Bewertung der empfundenen Anstrengung (RPE) gibt die subjektive Anhäufung von Müdigkeit an. Neue ambulante Blutdrucküberwachungssysteme ermöglichen detailliertere Analysen der Kreislaufreaktionen.
Akzeptable Arbeitsbelastung bei der manuellen Materialhandhabung
Die manuelle Materialhandhabung umfasst Arbeitsaufgaben wie das Heben, Tragen, Schieben und Ziehen verschiedener externer Lasten. Der größte Teil der Forschung in diesem Bereich konzentrierte sich auf Probleme im unteren Rücken bei Hebeaufgaben, insbesondere aus biomechanischer Sicht.
Für Hebeaufgaben wurde ein RAS-Wert von 20-35 % empfohlen, wenn die Aufgabe mit einem individuellen maximalen Sauerstoffverbrauch verglichen wird, der aus einem Fahrradergometertest ermittelt wurde.
Empfehlungen für eine maximal zulässige Herzfrequenz sind entweder absolut oder bezogen auf die Ruheherzfrequenz. Die absoluten Werte für Männer und Frauen liegen bei 90-112 Schlägen pro Minute bei kontinuierlicher manueller Materialhandhabung. Diese Werte entsprechen in etwa den empfohlenen Werten für die Steigerung der Herzfrequenz über Ruhewerte, also 30 bis 35 Schläge pro Minute. Diese Empfehlungen gelten auch für schwere dynamische Muskelarbeit für junge und gesunde Männer und Frauen. Wie bereits erwähnt, sollten Herzfrequenzdaten jedoch mit Vorsicht behandelt werden, da sie auch von anderen Faktoren als der Muskelarbeit beeinflusst werden.
Die auf biomechanischen Analysen basierenden Richtlinien für die akzeptable Arbeitsbelastung bei der manuellen Materialhandhabung umfassen mehrere Faktoren, wie z. B. Gewicht der Last, Handhabungshäufigkeit, Hubhöhe, Abstand der Last vom Körper und körperliche Eigenschaften der Person.
In einer großangelegten Feldstudie (Louhevaara, Hakola und Ollila 1990) wurde festgestellt, dass gesunde männliche Arbeiter während einer Schicht 4 bis 5 kg schwere Postpakete ohne Anzeichen objektiver oder subjektiver Ermüdung handhaben konnten. Der größte Teil des Umschlags fand unter Schulterhöhe statt, die durchschnittliche Umschlagshäufigkeit lag unter 8 Paketen pro Minute und die Gesamtzahl der Pakete lag unter 1,500 pro Schicht. Die mittlere Herzfrequenz der Arbeiter betrug 101 Schläge pro Minute und ihr mittlerer Sauerstoffverbrauch 1.0 l/min, was 31 % RAS bezogen auf das Fahrradmaximum entsprach.
Auch Beobachtungen von Arbeitshaltungen und Krafteinsatz, z. B. nach der OWAS-Methode (Karhu, Kansi und Kuorinka 1977), Ratings der empfundenen Anstrengung und ambulante Blutdruckmessungen sind geeignete Methoden zur Belastungsabschätzung im manuellen Materialhandling. Mittels Elektromyographie lassen sich lokale Belastungsreaktionen beispielsweise der Arm- und Rückenmuskulatur beurteilen.
Akzeptable Arbeitsbelastung für statische Muskelarbeit
Statische Muskelarbeit ist vor allem bei der Aufrechterhaltung der Arbeitshaltung erforderlich. Die Dauer der statischen Kontraktion hängt exponentiell von der relativen Kontraktionskraft ab. Das bedeutet beispielsweise, dass bei einer statischen Kontraktion von 20 % der Maximalkraft die Standzeit 5 bis 7 Minuten beträgt und bei einer Relativkraft von 50 % etwa 1 Minute.
Ältere Studien haben gezeigt, dass keine Ermüdung auftritt, wenn die relative Kraft unter 15 % der Maximalkraft liegt. Neuere Studien haben jedoch gezeigt, dass die akzeptable relative Kraft spezifisch für den Muskel oder die Muskelgruppe ist und 2 bis 5 % der maximalen statischen Kraft beträgt. Diese Kraftgrenzen sind jedoch in praktischen Arbeitssituationen schwierig anzuwenden, da sie elektromyographische Aufzeichnungen erfordern.
Für den Praktiker stehen weniger Feldmethoden zur Quantifizierung der Belastung bei statischen Arbeiten zur Verfügung. Es gibt einige Beobachtungsmethoden (z. B. die OWAS-Methode), um den Anteil schlechter Arbeitshaltungen zu analysieren, dh Haltungen, die von normalen Mittelstellungen der Hauptgelenke abweichen. Blutdruckmessungen und Bewertungen der wahrgenommenen Anstrengung können nützlich sein, während die Herzfrequenz nicht so anwendbar ist.
Akzeptable Arbeitsbelastung bei sich wiederholender Arbeit
Repetitive Arbeit mit kleinen Muskelgruppen ähnelt statischer Muskelarbeit im Hinblick auf Kreislauf- und Stoffwechselreaktionen. Typischerweise kontrahieren die Muskeln bei sich wiederholender Arbeit über 30 Mal pro Minute. Wenn die relative Kontraktionskraft 10 % der Maximalkraft übersteigt, beginnen Ausdauer und Muskelkraft abzunehmen. Es gibt jedoch große individuelle Unterschiede in den Ausdauerzeiten. Beispielsweise variiert die Ausdauerzeit zwischen zwei und fünfzig Minuten, wenn sich der Muskel 90 bis 110 Mal pro Minute bei einem relativen Kraftniveau von 10 bis 20 % zusammenzieht (Laurig 1974).
Es ist sehr schwierig, endgültige Kriterien für repetitive Arbeit festzulegen, da selbst sehr leichte Arbeiten (wie bei der Verwendung einer Mikrocomputermaus) zu einem Anstieg des intramuskulären Drucks führen können, der manchmal zu Muskelfaserschwellungen, Schmerzen und Verringerung führen kann an Muskelkraft.
Wiederholte und statische Muskelarbeit führt bei sehr niedrigen relativen Kraftniveaus zu Ermüdung und reduzierter Arbeitskapazität. Daher sollten ergonomische Eingriffe darauf abzielen, die Anzahl sich wiederholender Bewegungen und statischer Kontraktionen so weit wie möglich zu minimieren. Für die Belastungsbewertung bei repetitiven Arbeiten stehen nur sehr wenige Feldmethoden zur Verfügung.
Prävention von Muskelüberlastung
Es gibt relativ wenige epidemiologische Beweise dafür, dass Muskelbelastung gesundheitsschädlich ist. Arbeitsphysiologische und ergonomische Studien weisen jedoch darauf hin, dass Muskelüberlastung zu Ermüdung (dh Abnahme der Arbeitsfähigkeit) führt und die Produktivität und Arbeitsqualität verringern kann.
Die Prävention einer Muskelüberlastung kann sich auf den Arbeitsinhalt, das Arbeitsumfeld und den Arbeitnehmer beziehen. Die Belastung kann durch technische Mittel angepasst werden, die sich auf das Arbeitsumfeld, die Werkzeuge und/oder die Arbeitsweise konzentrieren. Der schnellste Weg, die muskuläre Belastung zu regulieren, ist die individuelle Flexibilisierung der Arbeitszeit. Das bedeutet, Arbeits- und Ruhezeiten zu entwerfen, die die Arbeitsbelastung sowie die Bedürfnisse und Fähigkeiten des einzelnen Arbeitnehmers berücksichtigen.
Statische und sich wiederholende Muskelarbeit sollte auf ein Minimum beschränkt werden. Gelegentliche schwere dynamische Arbeitsphasen können zur Aufrechterhaltung einer ausdauerähnlichen körperlichen Fitness sinnvoll sein. Die wahrscheinlich nützlichste Form der körperlichen Aktivität, die in einen Arbeitstag integriert werden kann, ist zügiges Gehen oder Treppensteigen.
Die Verhinderung einer Muskelüberlastung ist jedoch sehr schwierig, wenn die körperliche Fitness oder die Arbeitsfähigkeiten eines Arbeiters schlecht sind. Ein angemessenes Training verbessert die Arbeitsfertigkeiten und kann die Muskelbelastung bei der Arbeit reduzieren. Auch regelmäßige körperliche Betätigung während der Arbeit oder in der Freizeit erhöht die Muskel- und Herz-Kreislauf-Kapazitäten des Arbeitnehmers.
Zellschädigung und Zelltod
Nahezu die gesamte Medizin widmet sich entweder der Verhinderung des Zelltods bei Krankheiten wie Myokardinfarkt, Schlaganfall, Trauma und Schock oder seiner Verursachung, wie im Fall von Infektionskrankheiten und Krebs. Daher ist es wichtig, die Natur und die beteiligten Mechanismen zu verstehen. Der Zelltod wurde als „zufällig“, d. h. verursacht durch toxische Mittel, Ischämie usw., oder „programmiert“, wie er während der Embryonalentwicklung auftritt, einschließlich der Fingerbildung und der Resorption des Kaulquappenschwanzes, klassifiziert.
Zellverletzung und Zelltod sind daher sowohl in der Physiologie als auch in der Pathophysiologie wichtig. Der physiologische Zelltod ist während der Embryogenese und embryonalen Entwicklung äußerst wichtig. Die Untersuchung des Zelltods während der Entwicklung hat zu wichtigen und neuen Informationen über die beteiligte Molekulargenetik geführt, insbesondere durch die Untersuchung der Entwicklung bei wirbellosen Tieren. Bei diesen Tieren wurden der genaue Ort und die Bedeutung von Zellen, die zum Zelltod bestimmt sind, sorgfältig untersucht, und mithilfe klassischer Mutagenesetechniken wurden nun mehrere beteiligte Gene identifiziert. In erwachsenen Organen steuert das Gleichgewicht zwischen Zelltod und Zellproliferation die Organgröße. In manchen Organen, wie der Haut und dem Darm, findet ein ständiger Zellumsatz statt. In der Haut beispielsweise differenzieren sich Zellen, wenn sie die Oberfläche erreichen, und unterliegen schließlich einer endgültigen Differenzierung und einem Zelltod, wenn die Keratinisierung mit der Bildung von vernetzten Hüllen fortschreitet.
Viele Klassen toxischer Chemikalien sind in der Lage, eine akute Zellschädigung mit nachfolgendem Zelltod hervorzurufen. Dazu gehören Anoxie und Ischämie und ihre chemischen Analoga wie Kaliumcyanid; chemische Karzinogene, die Elektrophile bilden, die sich kovalent an Proteine in Nukleinsäuren binden; oxidierende Chemikalien, die zur Bildung freier Radikale und oxidativer Schädigung führen; Aktivierung des Komplements; und eine Vielzahl von Calciumionophoren. Der Zelltod ist auch ein wichtiger Bestandteil der chemischen Karzinogenese; Viele vollständige chemische Karzinogene erzeugen in karzinogenen Dosen akute Nekrose und Entzündung, gefolgt von Regeneration und Präneoplasie.
Definitionen
Zellverletzung
Eine Zellschädigung ist definiert als ein Ereignis oder Stimulus, wie z. B. eine toxische Chemikalie, der die normale Homöostase der Zelle stört und somit das Auftreten einer Reihe von Ereignissen verursacht (Abbildung 1). Die dargestellten Hauptziele der tödlichen Verletzung sind die Hemmung der ATP-Synthese, die Störung der Integrität der Plasmamembran oder der Entzug essentieller Wachstumsfaktoren.
Tödliche Verletzungen führen je nach Temperatur, Zelltyp und Stimulus nach unterschiedlicher Zeit zum Absterben einer Zelle; oder sie können subletal oder chronisch sein – das heißt, die Verletzung führt zu einem veränderten homöostatischen Zustand, der, obwohl anormal, nicht zum Zelltod führt (Trump und Arstila 1971; Trump und Berezesky 1992; Trump und Berezesky 1995; Trump, Berezesky und Osornio-Vargas 1981). Bei einer tödlichen Verletzung gibt es eine Phase vor dem Zeitpunkt des Zelltods
während dieser Zeit erholt sich die Zelle; Ab einem bestimmten Zeitpunkt (dem „Point of no return“ oder dem Zelltod) führt die Entfernung der Verletzung jedoch nicht zur Genesung, sondern die Zelle wird degradiert und hydrolysiert, wodurch schließlich ein physikalisch-chemisches Gleichgewicht mit der Zelle erreicht wird Umgebung. Dies ist die Phase, die als Nekrose bekannt ist. Während der präletalen Phase treten abhängig von der Zelle und der Art der Verletzung mehrere Haupttypen von Veränderungen auf. Diese sind als Apoptose und Onkose bekannt.
Apoptosis
Apoptose leitet sich von den griechischen Wörtern ab apo, was weg von und bedeutet Ptosis, bedeutet fallen. Der Begriff abfallen leitet sich aus der Tatsache ab, dass die Zellen während dieser Art von präletaler Veränderung schrumpfen und an der Peripherie eine deutliche Blasenbildung erfahren. Die Bläschen lösen sich dann und schweben weg. Apoptose tritt in einer Vielzahl von Zelltypen nach verschiedenen Arten von toxischer Verletzung auf (Wyllie, Kerr und Currie 1980). Es ist besonders ausgeprägt in Lymphozyten, wo es der vorherrschende Mechanismus für den Turnover von Lymphozytenklonen ist. Die resultierenden Fragmente führen zu den basophilen Körperchen, die innerhalb von Makrophagen in Lymphknoten zu sehen sind. In anderen Organen tritt Apoptose typischerweise in einzelnen Zellen auf, die vor und nach dem Tod schnell durch Phagozytose der Fragmente durch benachbarte Parenchymzellen oder durch Makrophagen beseitigt werden. Die in einzelnen Zellen auftretende Apoptose mit anschließender Phagozytose führt typischerweise nicht zu einer Entzündung. Vor dem Tod zeigen apoptotische Zellen ein sehr dichtes Zytosol mit normalen oder verdichteten Mitochondrien. Das endoplasmatische Retikulum (ER) ist normal oder nur leicht dilatiert. Das Kernchromatin ist entlang der Kernhülle und um den Nukleolus deutlich verklumpt. Auch die Kernkontur ist unregelmäßig und es kommt zur Kernfragmentierung. Die Chromatinkondensation ist mit einer DNA-Fragmentierung verbunden, die in vielen Fällen zwischen Nukleosomen auftritt und bei der Elektrophorese ein charakteristisches Leiterbild ergibt.
Bei Apoptose erhöhte [Ca2+]i kann K stimulieren+ Ausfluss, der zu einer Zellschrumpfung führt, die wahrscheinlich ATP erfordert. Verletzungen, die die ATP-Synthese vollständig hemmen, führen daher eher zu Apoptose. Ein anhaltender Anstieg von [Ca2+]i hat eine Reihe schädlicher Wirkungen, einschließlich der Aktivierung von Proteasen, Endonukleasen und Phospholipasen. Endonuklease-Aktivierung führt zu Einzel- und Doppel-DNA-Strangbrüchen, die wiederum erhöhte Spiegel von p53 und Poly-ADP-Ribosylierung sowie von Kernproteinen stimulieren, die für die DNA-Reparatur wesentlich sind. Die Aktivierung von Proteasen modifiziert eine Reihe von Substraten, einschließlich Aktin und verwandter Proteine, was zur Blasenbildung führt. Ein weiteres wichtiges Substrat ist die Poly(ADP-Ribose)-Polymerase (PARP), die die DNA-Reparatur hemmt. Erhöhte [ca2+]i ist auch mit der Aktivierung einer Reihe von Proteinkinasen wie MAP-Kinase, Calmodulin-Kinase und anderen verbunden. Solche Kinasen sind an der Aktivierung von Transkriptionsfaktoren beteiligt, die die Transkription von Immediate-Early-Genen initiieren, beispielsweise c-fos, c-jun und c-myc, und an der Aktivierung von Phospholipase A2 was zu einer Permeabilisierung der Plasmamembran und von intrazellulären Membranen wie der inneren Membran von Mitochondrien führt.
Onkose
Onkose, abgeleitet vom griechischen Wort Ist s, anschwellen, wird so genannt, weil bei dieser Art von präletaler Veränderung die Zelle fast unmittelbar nach der Verletzung zu schwellen beginnt (Majno und Joris 1995). Der Grund für die Schwellung ist eine Zunahme von Kationen im Wasser innerhalb der Zelle. Das hauptsächlich verantwortliche Kation ist Natrium, das normalerweise reguliert wird, um das Zellvolumen aufrechtzuerhalten. In Abwesenheit von ATP oder wenn die Na-ATPase des Plasmalemmas gehemmt ist, geht jedoch die Volumenkontrolle aufgrund von intrazellulärem Protein verloren, und Natrium im Wasser nimmt weiter zu. Zu den frühen Ereignissen bei Onkosen gehören daher vermehrt [Na+]i was zu Zellschwellung und erhöhtem [Ca2+]i entweder durch Einströmen aus dem extrazellulären Raum oder Freisetzung aus intrazellulären Speichern. Dies führt zu einer Schwellung des Zytosols, einer Schwellung des endoplasmatischen Retikulums und des Golgi-Apparats und zur Bildung wässriger Bläschen um die Zelloberfläche herum. Die Mitochondrien unterliegen zunächst einer Kondensation, zeigen aber später auch eine starke Schwellung aufgrund einer Schädigung der inneren Mitochondrienmembran. Bei dieser Art von präletaler Veränderung wird das Chromatin kondensiert und schließlich abgebaut; das charakteristische Leitermuster der Apoptose ist jedoch nicht zu sehen.
Nekrose
Nekrose bezieht sich auf die Reihe von Veränderungen, die nach dem Zelltod auftreten, wenn die Zelle in Trümmer umgewandelt wird, die typischerweise durch die Entzündungsreaktion entfernt werden. Zwei Typen können unterschieden werden: onkotische Nekrose und apoptotische Nekrose. Onkotische Nekrosen treten typischerweise in großen Zonen auf, zum Beispiel bei einem Myokardinfarkt oder regional in einem Organ nach chemischer Toxizität, wie dem proximalen Nierentubulus nach Verabreichung von HgCl2. Breite Zonen eines Organs sind betroffen und die nekrotischen Zellen lösen schnell eine Entzündungsreaktion aus, zuerst akut und dann chronisch. Falls der Organismus überlebt, folgt in vielen Organen der Nekrose die Abtragung der abgestorbenen Zellen und die Regeneration, beispielsweise in Leber oder Niere nach chemischer Toxizität. Im Gegensatz dazu tritt apoptotische Nekrose typischerweise auf einer Einzelzellbasis auf und die nekrotischen Trümmer werden innerhalb der Fresszellen von Makrophagen oder benachbarten parenchymalen Zellen gebildet. Zu den frühesten Merkmalen nekrotischer Zellen gehören Unterbrechungen in der Kontinuität der Plasmamembran und das Auftreten flockiger Dichten, die denaturierte Proteine innerhalb der mitochondrialen Matrix darstellen. Bei einigen Verletzungsformen, die anfänglich die mitochondriale Kalziumakkumulation nicht stören, können Kalziumphosphatablagerungen innerhalb der Mitochondrien gesehen werden. Andere Membransysteme sind ähnlich fragmentierend, wie das ER, die Lysosomen und der Golgi-Apparat. Letztendlich wird das nukleäre Chromatin einer Lyse unterzogen, die aus dem Angriff durch lysosomale Hydrolasen resultiert. Nach dem Zelltod spielen lysosomale Hydrolasen eine wichtige Rolle bei der Entfernung von Trümmern mit Cathepsinen, Nucleolasen und Lipasen, da diese ein saures pH-Optimum haben und den niedrigen pH-Wert nekrotischer Zellen überleben können, während andere zelluläre Enzyme denaturiert und inaktiviert werden.
Mechanismen
Anfänglicher Reiz
Bei tödlichen Verletzungen sind die häufigsten anfänglichen Wechselwirkungen, die zu einer Verletzung führen, die zum Zelltod führt, Störungen des Energiestoffwechsels, wie Anoxie, Ischämie oder Atemhemmer, und Glykolyse, wie Kaliumcyanid, Kohlenmonoxid, Jodacetat und bald. Wie oben erwähnt, führen hohe Dosen von Verbindungen, die den Energiestoffwechsel hemmen, typischerweise zu einer Onkose. Die andere häufige Art von anfänglicher Verletzung, die zu akutem Zelltod führt, ist die Veränderung der Funktion der Plasmamembran (Trump und Arstila 1971; Trump, Berezesky und Osornio-Vargas 1981). Dies kann entweder eine direkte Schädigung und Permeabilisierung sein, wie im Falle eines Traumas oder einer Aktivierung des C5b-C9-Komplementkomplexes, eine mechanische Schädigung der Zellmembran oder eine Hemmung des Natrium-Kalium (Na+-K+) Pumpe mit Glykosiden wie Ouabain. Calciumionophore wie Ionomycin oder A23187, die schnell [Ca2+] den Gradienten hinunter in die Zelle führen ebenfalls zu akuten tödlichen Verletzungen. In einigen Fällen ist das Muster der präletalen Veränderung Apoptose; in anderen ist es Onkose.
Signalwege
Bei vielen Arten von Verletzungen werden die mitochondriale Atmung und die oxidative Phosphorylierung schnell beeinträchtigt. Dies stimuliert in einigen Zellen die anaerobe Glykolyse, die in der Lage ist, ATP aufrechtzuerhalten, aber bei vielen Verletzungen wird dies gehemmt. Der Mangel an ATP führt dazu, dass eine Reihe wichtiger homöostatischer Prozesse nicht aktiviert werden, insbesondere die Kontrolle der intrazellulären Ionenhomöostase (Trump und Berezesky 1992; Trump, Berezesky und Osornio-Vargas 1981). Dies führt zu schnellen Anstiegen von [Ca2+]i, und erhöhte [Na+] und [Cl-] führt zu einer Zellschwellung. Erhöhungen von [Ca2+]i führen zur Aktivierung einer Reihe anderer unten diskutierter Signalmechanismen, einschließlich einer Reihe von Kinasen, die zu einer erhöhten unmittelbaren frühen Gentranskription führen können. Erhöhte [ca2+]i modifiziert auch die Zytoskelettfunktion, was teilweise zur Bildung von Bläschen und zur Aktivierung von Endonukleasen, Proteasen und Phospholipasen führt. Diese scheinen viele der oben diskutierten wichtigen Wirkungen auszulösen, wie z. B. Membranschäden durch Protease- und Lipaseaktivierung, direkten Abbau von DNA durch Endonukleaseaktivierung und Aktivierung von Kinasen wie MAP-Kinase und Calmodulin-Kinase, die als Transkriptionsfaktoren wirken.
Durch umfangreiche Entwicklungsarbeit bei Wirbellosen C. elegans und Drosophilasowie in menschlichen und tierischen Zellen wurde eine Reihe von Protodesgenen identifiziert. Es wurde festgestellt, dass einige dieser Wirbellosen-Gene Säugetier-Gegenstücke haben. Zum Beispiel das ced-3-Gen, das für den programmierten Zelltod essentiell ist C. elegans, besitzt Protease-Aktivität und eine starke Homologie mit dem Säuger-Interleukin-Converting-Enzym (ICE). Ein nahe verwandtes Gen namens Apopain oder prICE wurde kürzlich mit noch engerer Homologie identifiziert (Nicholson et al. 1995). In Drosophilascheint das Reaper-Gen an einem Signal beteiligt zu sein, das zum programmierten Zelltod führt. Zu den weiteren Protodesgenen gehören das Fas-Membranprotein und das wichtige Tumorsuppressor-Gen p53, das weitgehend konserviert ist. p53 wird nach einer DNA-Schädigung auf Proteinebene induziert und fungiert, wenn es phosphoryliert wird, als Transkriptionsfaktor für andere Gene wie gadd45 und waf-1, die an der Zelltodsignalisierung beteiligt sind. Andere unmittelbar frühe Gene wie c-fos, c-jun und c-myc scheinen ebenfalls an einigen Systemen beteiligt zu sein.
Gleichzeitig gibt es Anti-Todes-Gene, die den Pro-Todes-Genen entgegenzuwirken scheinen. Das erste davon, das identifiziert werden konnte, war ced-9 from C. elegans, das beim Menschen zu bcl-2 homolog ist. Diese Gene wirken auf eine noch unbekannte Weise, um das Abtöten von Zellen durch genetische oder chemische Toxine zu verhindern. Einige neuere Beweise deuten darauf hin, dass bcl-2 als Antioxidans wirken kann. Derzeit wird intensiv daran gearbeitet, ein Verständnis für die beteiligten Gene zu entwickeln und Möglichkeiten zu entwickeln, diese Gene je nach Situation zu aktivieren oder zu hemmen.
Zusammenfassung der Expositionsmaßnahmen im Arbeitsleben
Forscher können sich glücklich schätzen, wenn ihnen eine detaillierte Chronologie der Arbeitserfahrung von Arbeitnehmern zur Verfügung steht, die einen historischen Rückblick auf ihre Jobs im Laufe der Zeit bietet. Für diese Arbeitnehmer a Job-Exposure-Matrix kann dann so eingerichtet werden, dass jeder einzelne Arbeitsplatzwechsel, den ein Arbeitnehmer durchlaufen hat, mit spezifischen Expositionsinformationen verknüpft werden kann.
Detaillierte Expositionsgeschichten müssen zu Analysezwecken zusammengefasst werden, um festzustellen, ob Muster erkennbar sind, die mit Gesundheits- und Sicherheitsproblemen am Arbeitsplatz zusammenhängen könnten. Wir können eine Liste von beispielsweise 20 Stellenwechseln visualisieren, die ein Arbeitnehmer in seinem oder ihrem Arbeitsleben erlebt hat. Es gibt dann mehrere alternative Möglichkeiten, wie die Expositionsdetails (für jeden der 20 Arbeitsplatzwechsel in diesem Beispiel) unter Berücksichtigung von Dauer und/oder Konzentration/Dosis/Grad der Exposition zusammengefasst werden können.
Es ist jedoch zu beachten, dass je nach gewählter Methode unterschiedliche Schlussfolgerungen aus einer Studie gezogen werden können (Suarez-Almazor et al. 1992). Ein Beispiel für fünf zusammenfassende Expositionsmessungen während des Arbeitslebens ist in Tabelle 1 dargestellt.
Tabelle 1. Formeln und Dimensionen oder Einheiten der fünf ausgewählten zusammenfassenden Maße der Exposition während des Arbeitslebens
|
Belichtungsmaß |
Formel |
Abmessungen/Einheiten |
|
Kumulativer Expositionsindex (CEI) |
Σ (Grad x Belichtungszeit) |
Klasse und Zeit |
|
Durchschnittsnote (MG) |
Σ (Grad x Expositionszeit)/Gesamtzeit der Exposition |
Klasse |
|
Bestnote aller Zeiten (HG) |
höchste Klasse, der ≥ 7 Tage ausgesetzt waren |
Klasse |
|
Zeitgewichteter Durchschnitt (TWA) Note |
Σ (Grad x Expositionszeit)/Gesamtbeschäftigungszeit |
Klasse |
|
Gesamtzeit ausgesetzt (TTE) |
Σ Zeit ausgesetzt |
Zeit |
Adaptiert von Suarez-Almazor et al. 1992.
Kumulativer Expositionsindex. Der kumulative Expositionsindex (CEI) entspricht in toxikologischen Studien der „Dosis“ und stellt die Summe der Produkte aus Expositionsgrad und Expositionsdauer für jede aufeinanderfolgende Berufsbezeichnung über ein Arbeitsleben dar. Es enthält die Zeit in seinen Einheiten.
Mittlere Note. Die mittlere Note (MG) kumuliert die Produkte aus Expositionsnote und Expositionsdauer für jede aufeinanderfolgende Berufsbezeichnung (dh den CEI) und dividiert durch die Gesamtzeit, die bei einer Note größer als null verbracht wurde. MG ist in seinen Einheiten zeitunabhängig; Die zusammenfassende Maßnahme für eine Person, die über einen langen Zeitraum einer hohen Konzentration ausgesetzt ist, ist ähnlich wie die für eine Person, die über einen kurzen Zeitraum einer hohen Konzentration ausgesetzt ist. Innerhalb jedes Matched Sets in einem Fall-Kontroll-Design ist MG ein durchschnittlicher Expositionsgrad pro exponierter Zeiteinheit. Es handelt sich um eine Durchschnittsnote für die tatsächliche Expositionszeit gegenüber dem betrachteten Mittel.
Höchste Note aller Zeiten. Die Bestnote aller Zeiten (HG) wird ermittelt, indem der Arbeitsverlauf nach der höchsten Notenaufgabe im Beobachtungszeitraum gescannt wird, der der Arbeitnehmer mindestens sieben Tage lang ausgesetzt war. Das HG könnte die berufliche Exposition einer Person falsch darstellen, da es seiner Formulierung nach auf einem Maximierungs- und nicht auf einem Mittelungsverfahren basiert und daher in seinen Einheiten unabhängig von der Expositionsdauer ist.
Zeitgewichteter Notendurchschnitt. Die zeitgewichtete Durchschnittsnote (TWA) ist der kumulative Expositionsindex (CEI) dividiert durch die Gesamtbeschäftigungszeit. Innerhalb jedes Matched Sets in einem Fall-Kontroll-Design ergibt sich der TWA-Grad als Durchschnitt über die gesamte aufgewendete Zeit. Sie unterscheidet sich von MG, die nur über die tatsächlich exponierte Gesamtzeit mittelt. Somit kann die TWA-Klasse unabhängig von der Exposition als durchschnittliche Exposition pro Zeiteinheit während der gesamten Beschäftigungsdauer angesehen werden an sich.
Gesamtzeit ausgesetzt. Die Total Time Exposure (TTE) summiert alle mit der Exposition verbundenen Zeiträume in Zeiteinheiten. TTE besticht durch seine Einfachheit. Es ist jedoch allgemein anerkannt, dass gesundheitliche Auswirkungen nicht nur von der Dauer der Exposition gegenüber Chemikalien, sondern auch von der Intensität dieser Exposition (dh der Konzentration oder dem Grad) abhängen müssen.
Die Nützlichkeit eines zusammenfassenden Expositionsmaßes wird eindeutig durch das jeweilige Gewicht bestimmt, das es entweder der Dauer oder der Konzentration der Exposition oder beiden beimisst. Daher können unterschiedliche Maßnahmen zu unterschiedlichen Ergebnissen führen (Walker und Blettner 1985). Idealerweise sollte das ausgewählte zusammenfassende Maß auf einer Reihe von vertretbaren Annahmen bezüglich des postulierten biologischen Mechanismus für den untersuchten Erreger oder Krankheitsverband beruhen (Smith 1987). Dieses Verfahren ist jedoch nicht immer möglich. Sehr oft ist die biologische Wirkung der Expositionsdauer oder der Konzentration des untersuchten Agens unbekannt. In diesem Zusammenhang kann die Verwendung verschiedener Expositionsmaße nützlich sein, um einen Mechanismus vorzuschlagen, durch den die Exposition ihre Wirkung entfaltet.
Es wird empfohlen, dass in Ermangelung bewährter Modelle zur Bewertung der Exposition eine Vielzahl von zusammenfassenden Expositionsmessungen im Berufsleben zur Risikoabschätzung verwendet werden. Dieser Ansatz würde den Vergleich von Ergebnissen über Studien hinweg erleichtern.
Körperhaltungen bei der Arbeit
Die Haltung einer Person bei der Arbeit – die gemeinsame Organisation von Rumpf, Kopf und Extremitäten – kann aus mehreren Blickwinkeln analysiert und verstanden werden. Körperhaltungen zielen darauf ab, die Arbeit voranzubringen; daher haben sie eine Endgültigkeit, die ihre Natur, ihre zeitliche Beziehung und ihre (physiologischen oder sonstigen) Kosten für die betreffende Person beeinflusst. Es besteht eine enge Wechselwirkung zwischen den physiologischen Fähigkeiten und Eigenschaften des Körpers und den Anforderungen der Arbeit.
Muskel-Skelett-Belastung ist ein notwendiges Element der Körperfunktionen und unverzichtbar für das Wohlbefinden. Aus gestalterischer Sicht geht es darum, die optimale Balance zwischen Notwendigem und Überflüssigem zu finden.
Körperhaltungen interessieren Forscher und Praktiker zumindest aus den folgenden Gründen:
- Eine Körperhaltung ist die Quelle der muskuloskelettalen Belastung. Außer beim entspannten Stehen, Sitzen und Liegen in der Waagerechten müssen Muskeln Kräfte aufbringen, um die Körperhaltung auszugleichen und/oder Bewegungen zu kontrollieren. Bei klassischen schweren Aufgaben, zum Beispiel in der Bauindustrie oder bei der manuellen Handhabung schwerer Materialien, kommen externe Kräfte, sowohl dynamische als auch statische, zu den inneren Kräften im Körper hinzu und erzeugen manchmal hohe Belastungen, die die Kapazität des Gewebes übersteigen können. (Siehe Abbildung 1) Selbst in entspannter Haltung, wenn die Muskelarbeit gegen Null geht, können Sehnen und Gelenke belastet werden und Ermüdungserscheinungen zeigen. Eine Tätigkeit mit geringer scheinbarer Belastung – beispielsweise die eines Mikroskopikers – kann ermüdend und anstrengend werden, wenn sie über einen längeren Zeitraum ausgeübt wird.
- Die Körperhaltung ist eng mit Gleichgewicht und Stabilität verbunden. Tatsächlich wird die Körperhaltung durch mehrere neurale Reflexe gesteuert, bei denen der Input von taktilen Empfindungen und visuellen Hinweisen aus der Umgebung eine wichtige Rolle spielen. Einige Körperhaltungen, wie das Greifen nach Objekten aus der Ferne, sind von Natur aus instabil. Gleichgewichtsverlust ist eine häufige unmittelbare Ursache für Arbeitsunfälle. Einige Arbeitsaufgaben werden in einer Umgebung ausgeführt, in der die Stabilität nicht immer gewährleistet werden kann, beispielsweise in der Bauindustrie.
- Die Körperhaltung ist die Grundlage für geschickte Bewegungen und visuelle Beobachtung. Viele Aufgaben erfordern feine, geschickte Handbewegungen und eine genaue Beobachtung des Arbeitsgegenstands. In solchen Fällen wird die Körperhaltung zur Plattform dieser Aktionen. Die Aufmerksamkeit wird auf die Aufgabe gelenkt und die Haltungselemente werden zur Unterstützung der Aufgaben herangezogen: Die Haltung wird bewegungslos, die muskuläre Belastung steigt und wird statischer. Eine französische Forschungsgruppe zeigte in ihrer klassischen Studie, dass Immobilität und Muskel-Skelett-Belastung zunahmen, wenn das Arbeitspensum zunahm (Teiger, Laville und Duraffourg 1974).
- Haltung ist eine Informationsquelle über die Ereignisse, die bei der Arbeit stattfinden. Die Beobachtungshaltung kann beabsichtigt oder unbewusst sein. Geschickte Vorgesetzte und Arbeiter sind dafür bekannt, Haltungsbeobachtungen als Indikatoren für den Arbeitsprozess zu verwenden. Oft ist das Beobachten von Haltungsinformationen nicht bewusst. Beispielsweise wurden auf einem Ölbohrturm Haltungshinweise verwendet, um Nachrichten zwischen Teammitgliedern während verschiedener Phasen einer Aufgabe zu kommunizieren. Dies geschieht unter Bedingungen, bei denen andere Kommunikationsmittel nicht möglich sind.
Abbildung 1. Zu hohe Handpositionen oder Vorwärtsbeugen gehören zu den häufigsten Arten, eine „statische“ Belastung zu erzeugen
Sicherheit, Gesundheit und Arbeitshaltung
Aus Sicht der Sicherheit und Gesundheit können alle oben beschriebenen Aspekte der Körperhaltung wichtig sein. Die größte Aufmerksamkeit haben jedoch Körperhaltungen als Ursache für Muskel-Skelett-Erkrankungen wie Erkrankungen des unteren Rückens auf sich gezogen. Muskel-Skelett-Probleme im Zusammenhang mit sich wiederholender Arbeit sind auch mit Körperhaltungen verbunden.
Schmerzen im unteren Rückenbereich (LBP) ist ein Oberbegriff für verschiedene Erkrankungen des unteren Rückens. Es hat viele Ursachen und die Körperhaltung ist ein mögliches ursächliches Element. Epidemiologische Studien haben gezeigt, dass körperlich schwere Arbeit Kreuzschmerzen begünstigt und dass Körperhaltungen ein Element in diesem Prozess sind. Es gibt mehrere mögliche Mechanismen, die erklären, warum bestimmte Körperhaltungen LBP verursachen können. Vorgebeugte Haltungen erhöhen die Belastung der Wirbelsäule und der Bänder, die besonders anfällig für Belastungen in einer verdrehten Haltung sind. Äußere Belastungen, insbesondere dynamische, wie z. B. durch Stöße und Rutschen, können die Belastungen des Rückens um ein Vielfaches erhöhen.
Aus Sicherheits- und Gesundheitsgründen ist es wichtig, Fehlhaltungen und andere Haltungselemente im Rahmen der Sicherheits- und Gesundheitsanalyse der Arbeit im Allgemeinen zu identifizieren.
Erfassung und Messung der Arbeitshaltung
Körperhaltungen können durch visuelle Beobachtung oder mehr oder weniger ausgefeilte Messtechniken erfasst und objektiv gemessen werden. Sie können auch mithilfe von Selbstbewertungsschemata erfasst werden. Die meisten Methoden betrachten die Körperhaltung als eines der Elemente in einem größeren Kontext, beispielsweise als Teil des Arbeitsinhalts – ebenso wie die von AET und Renault Les Profile des Posts (Landau und Rohmert 1981; RNUR 1976) – oder als Ausgangspunkt für biomechanische Berechnungen, die auch andere Komponenten berücksichtigen.
Trotz der Fortschritte in der Messtechnik bleibt die visuelle Beobachtung unter Feldbedingungen das einzig praktikable Mittel zur systematischen Erfassung von Körperhaltungen. Die Genauigkeit solcher Messungen bleibt jedoch gering. Trotzdem können Haltungsbeobachtungen eine reichhaltige Informationsquelle für die Arbeit im Allgemeinen sein.
Die folgende kurze Liste von Messmethoden und -techniken stellt ausgewählte Beispiele vor:
- Fragebögen zur Selbstauskunft und Tagebücher. Fragebögen zur Selbstauskunft und Tagebücher sind ein kostengünstiges Mittel zur Erfassung von Haltungsdaten. Die Selbstauskunft basiert auf der Wahrnehmung des Probanden und weicht meist stark von „objektiv“ beobachteten Körperhaltungen ab, kann aber dennoch wichtige Informationen über die Ermüdung der Arbeit vermitteln.
- Beobachtung von Körperhaltungen. Die Haltungsbeobachtung umfasst die rein visuelle Erfassung der Haltungen und ihrer Bestandteile sowie Methoden, bei denen ein Interview die Informationen vervollständigt. Für diese Methoden steht in der Regel eine Computerunterstützung zur Verfügung. Für visuelle Beobachtungen stehen viele Methoden zur Verfügung. Die Methode kann einfach einen Aktionskatalog enthalten, einschließlich Haltungen des Rumpfes und der Gliedmaßen (z. B. Keyserling 1986; Van der Beek, Van Gaalen und Frings-Dresen 1992). Die OWAS-Methode schlägt ein strukturiertes Schema für die Analyse, Bewertung und Bewertung vor von Rumpf- und Gliedmaßenhaltungen für Feldbedingungen (Karhu, Kansi und Kuorinka 1977). Die Aufzeichnungs- und Analysemethode kann Notationsschemata enthalten, von denen einige sehr detailliert sind (wie bei der Posture Targeting-Methode von Corlett und Bishop 1976), und sie können eine Notation für die Position vieler anatomischer Elemente für jedes Element der Aufgabe bereitstellen ( Drurry 1987).
- Computergestützte Haltungsanalysen. Computer haben Haltungsanalysen in vielerlei Hinsicht unterstützt. Tragbare Computer und spezielle Programme ermöglichen eine einfache Aufzeichnung und schnelle Analyse von Körperhaltungen. Persson und Kilbom (1983) haben das Programm VIRA zur Untersuchung der oberen Extremitäten entwickelt; Kerguelen (1986) hat ein komplettes Aufzeichnungs- und Analysepaket für Arbeitsaufgaben produziert; Kivi und Mattila (1991) haben eine computergestützte OWAS-Version für Aufzeichnung und Analyse entworfen.
Video ist normalerweise ein integraler Bestandteil des Aufnahme- und Analyseprozesses. Das US National Institute for Occupational Safety and Health (NIOSH) hat Richtlinien für den Einsatz von Videomethoden in der Gefahrenanalyse vorgelegt (NIOSH 1990).
Biomechanische und anthropometrische Computerprogramme bieten spezialisierte Werkzeuge zur Analyse einiger posturaler Elemente in der Arbeitstätigkeit und im Labor (z. B. Chaffin 1969).
Faktoren, die die Arbeitshaltung beeinflussen
Arbeitshaltungen dienen einem Ziel, einer Endgültigkeit außerhalb ihrer selbst. Deshalb beziehen sie sich auf äußere Arbeitsbedingungen. Haltungsanalysen, die das Arbeitsumfeld und die Aufgabe selbst nicht berücksichtigen, sind für Ergonomen nur von begrenztem Interesse.
Die dimensionalen Eigenschaften des Arbeitsplatzes bestimmen weitgehend die Haltungen (wie bei einer sitzenden Tätigkeit), auch bei dynamischen Tätigkeiten (z. B. Materialhandhabung auf engstem Raum). Die zu handhabenden Lasten zwingen den Körper ebenso wie das Gewicht und die Beschaffenheit des Arbeitsgerätes in eine bestimmte Körperhaltung. Einige Aufgaben erfordern, dass das Körpergewicht verwendet wird, um ein Werkzeug zu stützen oder Kraft auf das Arbeitsobjekt auszuüben, wie beispielsweise in Abbildung 2 gezeigt.
Abbildung 2. Ergonomische Aspekte des Stehens
Individuelle Unterschiede, Alter und Geschlecht beeinflussen die Körperhaltung. Tatsächlich hat sich herausgestellt, dass eine „typische“ oder „beste“ Körperhaltung, beispielsweise bei der manuellen Handhabung, weitgehend Fiktion ist. Für jede Person und jede Arbeitssituation gibt es eine Reihe alternativer „bester“ Körperhaltungen nach unterschiedlichen Kriterien.
Arbeitshilfen und Stützen für Arbeitshaltungen
Gurte, Lordosenstützen und Orthesen werden für Aufgaben empfohlen, bei denen das Risiko von Rückenschmerzen oder Verletzungen des Bewegungsapparates der oberen Extremitäten besteht. Es wurde angenommen, dass diese Geräte die Muskeln unterstützen, indem sie zum Beispiel den intraabdominalen Druck oder Handbewegungen kontrollieren. Es wird auch erwartet, dass sie den Bewegungsbereich des Ellbogens, des Handgelenks oder der Finger einschränken. Es gibt keine Hinweise darauf, dass die Veränderung von Haltungselementen mit diesen Geräten helfen würde, Muskel-Skelett-Probleme zu vermeiden.
Zur Linderung von Haltungsbelastungen und Schmerzen können Haltungshilfen am Arbeitsplatz und an Maschinen wie Haltegriffe, Stützpolster zum Knien und Sitzhilfen hilfreich sein.
Sicherheits- und Gesundheitsvorschriften für Haltungselemente
Körperhaltungen oder Haltungselemente waren nicht Gegenstand regulatorischer Aktivitäten an sich. Einige Dokumente enthalten jedoch entweder haltungsrelevante Aussagen oder nehmen die Frage der Körperhaltung als integralen Bestandteil einer Verordnung auf. Ein vollständiges Bild des bestehenden Regulierungsmaterials ist nicht verfügbar. Die folgenden Referenzen werden als Beispiele präsentiert.
- Die Internationale Arbeitsorganisation veröffentlichte 1967 eine Empfehlung zu maximal zu handhabenden Lasten. Obwohl die Empfehlung die Haltungselemente als solche nicht regelt, hat sie einen erheblichen Einfluss auf die Haltungsbelastung. Die Empfehlung ist inzwischen veraltet, hat aber einen wichtigen Zweck erfüllt, indem sie die Aufmerksamkeit auf Probleme bei der manuellen Materialhandhabung gelenkt hat.
- Die NIOSH Lifting Guidelines (NIOSH 1981) als solche sind ebenfalls keine Vorschriften, haben aber diesen Status erlangt. Die Richtlinien leiten Gewichtsgrenzen für Belastungen ab, indem sie den Ort der Belastung – ein Haltungselement – zugrunde legen.
- Sowohl in der Internationalen Organisation für Normung als auch in der Europäischen Gemeinschaft existieren Ergonomie-Normen und -Richtlinien, die sich auf Haltungselemente beziehen (CEN 1990 und 1991).
Genetische Toxikologie
Die genetische Toxikologie ist per Definition die Untersuchung, wie chemische oder physikalische Wirkstoffe den komplizierten Prozess der Vererbung beeinflussen. Genotoxische Chemikalien werden als Verbindungen definiert, die in der Lage sind, das Erbmaterial lebender Zellen zu verändern. Die Wahrscheinlichkeit, dass eine bestimmte Chemikalie genetische Schäden verursacht, hängt zwangsläufig von mehreren Variablen ab, einschließlich der Exposition des Organismus gegenüber der Chemikalie, der Verteilung und Retention der Chemikalie, sobald sie in den Körper gelangt, der Effizienz der Stoffwechselaktivierung und/oder der Entgiftungssysteme Zielgewebe und die Reaktivität der Chemikalie oder ihrer Metaboliten mit kritischen Makromolekülen in Zellen. Die Wahrscheinlichkeit, dass ein genetischer Schaden eine Krankheit verursacht, hängt letztendlich von der Art des Schadens, der Fähigkeit der Zelle, den genetischen Schaden zu reparieren oder zu verstärken, der Möglichkeit, die hervorgerufene Veränderung auszudrücken, und der Fähigkeit des Körpers ab, die Vermehrung zu erkennen und zu unterdrücken abweichende Zellen.
In höheren Organismen ist die Erbinformation in Chromosomen organisiert. Chromosomen bestehen aus eng kondensierten Strängen proteinassoziierter DNA. Innerhalb eines einzelnen Chromosoms existiert jedes DNA-Molekül als Paar langer, unverzweigter Ketten von Nukleotid-Untereinheiten, die durch Phosphodiester-Bindungen miteinander verbunden sind, die das 5-Kohlenstoffatom einer Desoxyribose-Einheit mit dem 3-Kohlenstoffatom des nächsten verbinden (Abbildung 1). Außerdem hängt an jeder Desoxyribose-Untereinheit eine von vier verschiedenen Nukleotidbasen (Adenin, Cytosin, Guanin oder Thymin) wie Perlen an einer Schnur. Dreidimensional bildet jedes Paar DNA-Stränge eine Doppelhelix, wobei alle Basen zum Inneren der Spirale ausgerichtet sind. Innerhalb der Helix ist jede Base mit ihrer komplementären Base auf dem gegenüberliegenden DNA-Strang verbunden; Wasserstoffbrückenbindungen diktieren eine starke, nichtkovalente Paarung von Adenin mit Thymin und Guanin mit Cytosin (Abbildung 1). Da die Sequenz der Nukleotidbasen über die gesamte Länge des Duplex-DNA-Moleküls komplementär ist, tragen beide Stränge im Wesentlichen die gleiche genetische Information. Tatsächlich dient während der DNA-Replikation jeder Strang als Matrize für die Produktion eines neuen Partnerstrangs.
Abbildung 1. Die (a) primäre, (b) sekundäre und (c) tertiäre Organisation menschlicher Erbinformationen
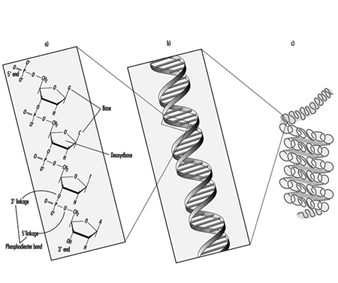 Unter Verwendung von RNA und einer Reihe verschiedener Proteine entschlüsselt die Zelle letztendlich die Informationen, die durch die lineare Abfolge von Basen innerhalb spezifischer DNA-Regionen (Gene) codiert sind, und produziert Proteine, die für das grundlegende Überleben der Zelle sowie für normales Wachstum und Differenzierung unerlässlich sind. Im Wesentlichen funktionieren die Nukleotide wie ein biologisches Alphabet, das zur Codierung von Aminosäuren, den Bausteinen von Proteinen, verwendet wird.
Unter Verwendung von RNA und einer Reihe verschiedener Proteine entschlüsselt die Zelle letztendlich die Informationen, die durch die lineare Abfolge von Basen innerhalb spezifischer DNA-Regionen (Gene) codiert sind, und produziert Proteine, die für das grundlegende Überleben der Zelle sowie für normales Wachstum und Differenzierung unerlässlich sind. Im Wesentlichen funktionieren die Nukleotide wie ein biologisches Alphabet, das zur Codierung von Aminosäuren, den Bausteinen von Proteinen, verwendet wird.
Wenn falsche Nukleotide eingefügt werden oder Nukleotide verloren gehen oder wenn während der DNA-Synthese unnötige Nukleotide hinzugefügt werden, wird der Fehler als Mutation bezeichnet. Es wurde geschätzt, dass weniger als eine Mutation auf 10 auftritt9 Nukleotide, die während der normalen Replikation von Zellen eingebaut werden. Obwohl Mutationen nicht unbedingt schädlich sind, können Veränderungen, die eine Inaktivierung oder Überexpression wichtiger Gene verursachen, zu einer Vielzahl von Erkrankungen führen, darunter Krebs, Erbkrankheiten, Entwicklungsstörungen, Unfruchtbarkeit und embryonaler oder perinataler Tod. Sehr selten kann eine Mutation zu einem verbesserten Überleben führen; Solche Vorkommnisse sind die Grundlage der natürlichen Auslese.
Obwohl einige Chemikalien direkt mit DNA reagieren, erfordern die meisten eine metabolische Aktivierung. Im letzteren Fall sind letztlich elektrophile Zwischenprodukte wie Epoxide oder Carboniumionen für die Induktion von Läsionen an verschiedenen nukleophilen Stellen innerhalb des genetischen Materials verantwortlich (Abbildung 2). In anderen Fällen wird die Genotoxizität durch Nebenprodukte der Wechselwirkung von Verbindungen mit intrazellulären Lipiden, Proteinen oder Sauerstoff vermittelt.
Abbildung 2. Bioaktivierung von: a) Benzo(a)pyren; und b) N-Nitrosodimethylamin
Aufgrund ihrer relativen Häufigkeit in Zellen sind Proteine das häufigste Ziel von toxischen Wechselwirkungen. Die Modifikation der DNA ist jedoch aufgrund der zentralen Rolle dieses Moleküls bei der Regulierung des Wachstums und der Differenzierung über mehrere Generationen von Zellen von größerer Bedeutung.
Auf molekularer Ebene neigen elektrophile Verbindungen dazu, Sauerstoff und Stickstoff in der DNA anzugreifen. Die Stellen, die am anfälligsten für Modifikationen sind, sind in Abbildung 3 dargestellt. Obwohl Sauerstoffatome innerhalb von Phosphatgruppen im DNA-Rückgrat ebenfalls Ziele für chemische Modifikationen sind, wird angenommen, dass eine Schädigung von Basen biologisch relevanter ist, da diese Gruppen als die primäre Informationsquelle angesehen werden Elemente im DNA-Molekül.
Abbildung 3. Primärstellen chemisch induzierter DNA-Schäden
Verbindungen, die eine elektrophile Einheit enthalten, üben typischerweise Genotoxizität aus, indem sie Monoaddukte in DNA erzeugen. In ähnlicher Weise können Verbindungen, die zwei oder mehr reaktive Einheiten enthalten, mit zwei verschiedenen nukleophilen Zentren reagieren und dadurch intra- oder intermolekulare Vernetzungen im genetischen Material erzeugen (Abbildung 4). DNA-DNA- und DNA-Protein-Crosslinks zwischen den Strängen können besonders zytotoxisch sein, da sie vollständige Blöcke für die DNA-Replikation bilden können. Aus offensichtlichen Gründen eliminiert der Tod einer Zelle die Möglichkeit, dass sie mutiert oder neoplastisch transformiert wird. Genotoxische Mittel können auch wirken, indem sie Brüche im Phosphodiester-Rückgrat oder zwischen Basen und Zuckern (die abasische Stellen erzeugen) in der DNA induzieren. Solche Brüche können ein direktes Ergebnis chemischer Reaktivität an der Schadensstelle sein oder können während der Reparatur einer der oben erwähnten Arten von DNA-Läsion auftreten.
Abbildung 4. Verschiedene Arten von Schäden am Protein-DNA-Komplex
In den letzten dreißig bis vierzig Jahren wurde eine Vielzahl von Techniken entwickelt, um die Art der genetischen Schädigung zu überwachen, die durch verschiedene Chemikalien hervorgerufen wird. Solche Assays werden an anderer Stelle in diesem Kapitel und ausführlich beschrieben Enzyklopädie.
Die Fehlreplikation von „Mikroläsionen“ wie Monoaddukten, abasischen Stellen oder Einzelstrangbrüchen kann letztendlich zu Nukleotidbasenpaarsubstitutionen oder der Insertion oder Deletion kurzer Polynukleotidfragmente in chromosomaler DNA führen. Im Gegensatz dazu können „Makroläsionen“ wie sperrige Addukte, Quervernetzungen oder Doppelstrangbrüche den Gewinn, Verlust oder die Neuanordnung relativ großer Chromosomenstücke auslösen. In jedem Fall können die Folgen für den Organismus verheerend sein, da jedes dieser Ereignisse zu Zelltod, Funktionsverlust oder bösartiger Transformation von Zellen führen kann. Wie genau DNA-Schäden Krebs verursachen, ist weitgehend unbekannt. Es wird derzeit angenommen, dass der Prozess eine unangemessene Aktivierung von Proto-Onkogenen beinhalten kann, wie z myc und rasund/oder Inaktivierung kürzlich identifizierter Tumorsuppressorgene wie p53. Eine anormale Expression beider Gentypen setzt normale zelluläre Mechanismen zur Kontrolle der Zellproliferation und/oder -differenzierung außer Kraft.
Die überwiegende Anzahl experimenteller Beweise weist darauf hin, dass die Entwicklung von Krebs nach Exposition gegenüber elektrophilen Verbindungen ein relativ seltenes Ereignis ist. Dies kann teilweise durch die intrinsische Fähigkeit der Zelle erklärt werden, beschädigte DNA zu erkennen und zu reparieren, oder durch das Versagen von Zellen mit beschädigter DNA zu überleben. Während der Reparatur wird die beschädigte Base, das Nukleotid oder der kurze Nukleotidabschnitt, der die beschädigte Stelle umgibt, entfernt und (unter Verwendung des gegenüberliegenden Strangs als Vorlage) wird ein neues DNA-Stück synthetisiert und an Ort und Stelle gespleißt. Um effektiv zu sein, muss die DNA-Reparatur mit großer Genauigkeit vor der Zellteilung erfolgen, bevor Gelegenheiten für die Ausbreitung von Mutationen bestehen.
Klinische Studien haben gezeigt, dass Menschen mit angeborenen Defekten in der Fähigkeit, beschädigte DNA zu reparieren, häufig in einem frühen Alter an Krebs und/oder Entwicklungsanomalien erkranken (Tabelle 1). Solche Beispiele liefern starke Beweise dafür, dass die Akkumulation von DNA-Schäden mit menschlichen Krankheiten in Verbindung gebracht wird. In ähnlicher Weise fördern Wirkstoffe, die die Zellproliferation fördern (wie Tetradecanoylphorbolacetat), häufig die Karzinogenese. Bei diesen Verbindungen kann die erhöhte Wahrscheinlichkeit einer neoplastischen Transformation eine direkte Folge einer Verringerung der Zeit sein, die der Zelle zur Durchführung einer angemessenen DNA-Reparatur zur Verfügung steht.
Tabelle 1. Erbliche, krebsanfällige Erkrankungen, die Defekte in der DNA-Reparatur zu beinhalten scheinen
| Syndrom | Symptome | Zellulärer Phänotyp |
| Ataxie teleangiektasie | Neurologische Verschlechterung Immunschwäche Hohe Inzidenz von Lymphomen |
Überempfindlichkeit gegen ionisierende Strahlung und bestimmte Alkylierungsmittel. Dysregulierte Replikation beschädigter DNA (kann auf eine verkürzte Zeit für die DNA-Reparatur hinweisen) |
| Bloom-Syndrom | Entwicklungsstörungen Läsionen auf exponierter Haut Hohe Inzidenz von Tumoren des Immunsystems und des Magen-Darm-Trakts |
Hohe Häufigkeit von Chromosomenaberrationen Defekte Ligation von Brüchen im Zusammenhang mit der DNA-Reparatur |
| Fanconis Anämie | Wachstumsverzögerung Hohe Inzidenz von Leukämie |
Überempfindlichkeit gegen Vernetzungsmittel Hohe Häufigkeit von Chromosomenaberrationen Defekte Reparatur von Quervernetzungen in DNA |
| Erblicher Dickdarmkrebs ohne Polyposis | Hohe Inzidenz von Dickdarmkrebs | Defekt in der DNA-Mismatch-Reparatur (wenn während der Replikation ein falsches Nukleotid eingefügt wird) |
| Mondscheinkrankheit | Hohe Inzidenz von Epitheliomen auf exponierten Hautbereichen Neurologische Beeinträchtigung (in vielen Fällen) |
Überempfindlichkeit gegen UV-Licht und viele chemische Karzinogene Defekte bei der Exzisionsreparatur und/oder Replikation beschädigter DNA |
Die frühesten Theorien darüber, wie Chemikalien mit DNA interagieren, lassen sich auf Studien zurückführen, die während der Entwicklung von Senfgas für den Einsatz in der Kriegsführung durchgeführt wurden. Weiteres Verständnis erwuchs aus den Bemühungen, Antikrebsmittel zu identifizieren, die selektiv die Replikation von sich schnell teilenden Tumorzellen stoppen würden. Die zunehmende Besorgnis der Öffentlichkeit über Gefahren in unserer Umwelt hat zu zusätzlicher Forschung über die Mechanismen und Folgen der chemischen Wechselwirkung mit dem genetischen Material geführt. Beispiele für verschiedene Arten von Chemikalien, die genotoxisch wirken, sind in Tabelle 2 aufgeführt.
Tabelle 2. Beispiele für Chemikalien, die in menschlichen Zellen Genotoxizität zeigen
| Klasse der Chemikalie | Beispiel | Quelle der Exposition | Wahrscheinlich genotoxische Läsion |
| Aflatoxine | Aflatoxin B1 | Kontaminiertes Essen | Sperrige DNA-Addukte |
| Aromatische Amine | 2-Acetylaminofluoren | Umwelt | Sperrige DNA-Addukte |
| Aziridinchinone | Mitomycin C | Chemotherapie bei Krebs | Monoaddukte, Quervernetzungen zwischen den Strängen und Einzelstrangbrüche in der DNA. |
| Chlorierte Kohlenwasserstoffe | Vinylchlorid | Umwelt | Monoaddukte in DNA |
| Metalle und Metallverbindungen | Cisplatin | Chemotherapie bei Krebs | Sowohl Intra- als auch Interstrang-Crosslinks in DNA |
| Nickelverbindungen | Umwelt | Monoaddukte und Einzelstrangbrüche in der DNA | |
| Stickstoffsenf | Cyclophosphamid | Chemotherapie bei Krebs | Monoaddukte und Quervernetzungen zwischen den Strängen in der DNA |
| Nitrosamine | N-Nitrosodimethylamin | Kontaminiertes Essen | Monoaddukte in DNA |
| Polyzyklische aromatische Kohlenwasserstoffe | Benzo (a) pyren | Umwelt | Sperrige DNA-Addukte |
Mehr...
Messung der Auswirkungen von Expositionen
Die Epidemiologie umfasst die Messung des Auftretens von Krankheiten und die Quantifizierung von Zusammenhängen zwischen Krankheiten und Expositionen.
Maßnahmen zum Auftreten von Krankheiten
Das Auftreten von Krankheiten kann gemessen werden durch Frequenzen (zählt), wird aber besser beschrieben durch Preise, die sich aus drei Elementen zusammensetzen: der Anzahl der Betroffenen (Zähler), der Anzahl der Personen in der Ausgangs- bzw. Grundgesamtheit (d. h. der Risikopopulation), aus der die betroffenen Personen stammen, und dem abgedeckten Zeitraum. Der Nenner der Rate ist die gesamte Personenzeit, die von der Quellpopulation erfahren wird. Raten ermöglichen aussagekräftigere Vergleiche zwischen Populationen unterschiedlicher Größe als Zählungen allein. Risiko, die Wahrscheinlichkeit, dass eine Person innerhalb eines bestimmten Zeitraums eine Krankheit entwickelt, ist ein Anteil zwischen 0 und 1 und keine Rate an sich. Angriffsgeschwindigkeit, der Anteil der Personen in einer Bevölkerung, die innerhalb eines bestimmten Zeitraums betroffen sind, ist technisch gesehen ein Risikomaß, keine Rate.
Krankheitsspezifische Morbidität umfasst Häufigkeit, die sich auf die Anzahl der Personen bezieht, bei denen die betreffende Krankheit neu diagnostiziert wird. Prävalenz bezieht sich auf die Anzahl der bestehenden Fälle. Sterblichkeit bezieht sich auf die Zahl der Verstorbenen.
Häufigkeit ist definiert als die Anzahl neu diagnostizierter Fälle innerhalb eines bestimmten Zeitraums, während die Inzidenzrate ist diese Zahl geteilt durch die gesamte Personenzeit, die von der Quellpopulation erfahren wird (Tabelle 1). Bei Krebs werden die Raten normalerweise als jährliche Raten pro 100,000 Personen ausgedrückt. Die Raten für andere häufigere Krankheiten können für eine kleinere Anzahl von Personen ausgedrückt werden. Beispielsweise werden Geburtsfehlerraten normalerweise pro 1,000 Lebendgeburten ausgedrückt. Kumulative Inzidenz, der Anteil der Personen, die innerhalb eines bestimmten Zeitraums zu Fällen werden, ist ein Maß für das durchschnittliche Risiko für eine Bevölkerung.
Tabelle 1. Maße für das Auftreten der Krankheit: Hypothetische Population, die über einen Zeitraum von fünf Jahren beobachtet wurde
|
Neu diagnostizierte Fälle |
10 |
|
Zuvor diagnostizierte lebende Fälle |
12 |
|
Todesfälle, alle Ursachen* |
5 |
|
Todesfälle, Krankheit von Interesse |
3 |
|
Personen in der Bevölkerung |
100 |
|
Jahre beobachtet |
5 |
|
Häufigkeit |
10 Personen |
|
Jährliche Inzidenzrate |
|
|
Punktprävalenz (am Ende des 5. Jahres) |
(10 + 12 - 3) = 19 Personen |
|
Periodenprävalenz (Fünfjahreszeitraum) |
(10 + 12) = 22 Personen |
|
Jährliche Todesrate |
|
|
Jährliche Sterblichkeitsrate |
|
*Um die Berechnungen zu vereinfachen, wird in diesem Beispiel davon ausgegangen, dass alle Todesfälle am Ende des Fünfjahreszeitraums eingetreten sind, sodass alle 100 Personen in der Bevölkerung die vollen fünf Jahre am Leben waren.
Prävalenz Dazu gehören Punkt Prävalenz, die Anzahl der Krankheitsfälle zu einem bestimmten Zeitpunkt und Periodenprävalenz, die Gesamtzahl der Fälle einer Krankheit, von denen bekannt ist, dass sie irgendwann während eines bestimmten Zeitraums aufgetreten sind.
Sterblichkeit, die sich eher auf Todesfälle als auf neu diagnostizierte Krankheitsfälle bezieht, spiegelt Faktoren wider, die Krankheiten verursachen, sowie Faktoren im Zusammenhang mit der Qualität der medizinischen Versorgung, wie z. B. Screening, Zugang zu medizinischer Versorgung und Verfügbarkeit wirksamer Behandlungen. Folglich können hypothesengenerierende Bemühungen und ätiologische Forschung informativer und leichter zu interpretieren sein, wenn sie auf Inzidenzdaten statt auf Mortalitätsdaten basieren. Allerdings sind Sterblichkeitsdaten für große Populationen oft leichter verfügbar als Inzidenzdaten.
Die Todesrate wird allgemein akzeptiert, um die Rate für Todesfälle aus allen Ursachen zusammen zu bezeichnen, wohingegen Sterblichkeitsrate ist die Todesrate aufgrund einer bestimmten Ursache. Für eine bestimmte Krankheit, die Fallsterblichkeitsrate (technisch gesehen ein Anteil, keine Rate) ist die Anzahl der Personen, die während eines bestimmten Zeitraums an der Krankheit sterben, dividiert durch die Anzahl der Personen mit der Krankheit. Das Komplement der Sterblichkeitsrate ist die Überlebensrate. Die Fünf-Jahres-Überlebensrate ist ein allgemeiner Maßstab für chronische Krankheiten wie Krebs.
Das Auftreten einer Krankheit kann zwischen Untergruppen der Bevölkerung oder im Laufe der Zeit variieren. Ein Krankheitsmaß für eine ganze Bevölkerung ohne Berücksichtigung von Untergruppen wird als a bezeichnet Rohsatz. Beispielsweise ist eine Inzidenzrate für alle Altersgruppen zusammen eine grobe Rate. Die Preise für die einzelnen Altersgruppen sind die altersspezifische Tarife. Um zwei oder mehr Populationen mit unterschiedlichen Altersverteilungen zu vergleichen, altersangepasst (oder, altersstandardisiert) Raten sollten für jede Population berechnet werden, indem jede altersspezifische Rate mit dem Prozentsatz der Standardpopulation (z. B. einer der untersuchten Populationen, der US-Bevölkerung von 1970) in dieser Altersgruppe multipliziert und dann über alle Altersgruppen summiert wird eine altersbereinigte Gesamtrate ergeben. Die Tarife können um andere Faktoren als das Alter, wie Rasse, Geschlecht oder Raucherstatus, angepasst werden, wenn die kategoriespezifischen Tarife bekannt sind.
Die Überwachung und Auswertung von deskriptiven Daten kann Hinweise auf die Krankheitsätiologie liefern, Untergruppen mit hohem Risiko identifizieren, die für Interventions- oder Screening-Programme geeignet sein könnten, und Daten über die Wirksamkeit solcher Programme liefern. Zu den Informationsquellen, die für Überwachungstätigkeiten verwendet wurden, gehören Sterbeurkunden, Krankenakten, Krebsregister, andere Krankheitsregister (z. B. Geburtsfehlerregister, Register für Nierenerkrankungen im Endstadium), Verzeichnisse der beruflichen Exposition, Kranken- oder Berufsunfähigkeitsversicherungsunterlagen und Arbeitnehmerentschädigungen Aufzeichnungen.
Maßnahmen der Assoziation
Die Epidemiologie versucht, Faktoren zu identifizieren und zu quantifizieren, die Krankheiten beeinflussen. Im einfachsten Ansatz wird das Auftreten von Krankheiten bei Personen, die einem verdächtigen Faktor ausgesetzt sind, mit dem Auftreten von Personen verglichen, die nicht exponiert sind. Das Ausmaß eines Zusammenhangs zwischen Exposition und Krankheit kann in beiden ausgedrückt werden Absolute or relativ Bedingungen. (Siehe auch „Fallbeispiel: Maßnahmen“).
Absolute Effekte werden gemessen durch Tarifunterschiede und Risikounterschiede (Tabelle 2). EIN Tarifunterschied ist eine Rate minus einer zweiten Rate. Wenn zum Beispiel die Inzidenzrate von Leukämie unter Benzol-exponierten Arbeitern 72 pro 100,000 Personenjahre und die Rate unter nicht exponierten Arbeitern 12 pro 100,000 Personenjahre beträgt, dann beträgt die Ratendifferenz 60 pro 100,000 Personenjahre. EIN Risiko Unterschied ist ein Unterschied in den Risiken oder der kumulativen Inzidenz und kann von -1 bis 1 reichen.
Tabelle 2. Assoziationsmaße für eine Kohortenstudie
|
Projekte |
Personenjahre gefährdet |
Preis pro 100,000 |
|
|
Ausgesetzt |
100 |
20,000 |
500 |
|
Unbelichtet |
200 |
80,000 |
250 |
|
Gesamt |
300 |
100,000 |
300 |
Ratendifferenz (RD) = 500/100,000 - 250/100,000
= 250/100,000 pro Jahr
(146.06/100,000 - 353.94/100,000)*
Ratenverhältnis (oder relatives Risiko) (RR) = ![]()
Zurechenbares Risiko bei Exponierten (ARe) = 100/20,000 - 200/80,000
= 250/100,000 pro Jahr
Zurechenbares Risiko in Prozent der Exponierten (ARe%) =![]()
Bevölkerungsbezogenes Risiko (PAR) = 300/100,000 - 200/80,000
= 50/100,000 pro Jahr
Bevölkerungsbezogenes Risiko in Prozent (PAR%) =
![]()
* In Klammern 95-%-Konfidenzintervalle, berechnet mit den Formeln in den Kästchen.
Relative Effekte basieren auf Quotenverhältnissen oder Risikomaßen statt auf Differenzen. EIN Ratenverhältnis ist das Verhältnis einer Rate in einer Population zu der Rate in einer anderen. Das Ratenverhältnis wurde auch als das bezeichnet Risikoverhältnis, relatives Risiko, relative Rate und Häufigkeit (oder Sterblichkeit) Ratenverhältnis. Das Maß ist dimensionslos und reicht von 0 bis unendlich. Wenn die Rate in zwei Gruppen ähnlich ist (dh es gibt keine Wirkung von der Exposition), die Ratenverhältnis gleich Eins (1) ist. Eine Exposition, die das Risiko erhöht, würde ein Ratenverhältnis größer als eins ergeben, während ein Schutzfaktor ein Verhältnis zwischen 0 und 1 ergeben würde übermäßiges relatives Risiko ist das relative Risiko minus 1. Beispielsweise kann ein relatives Risiko von 1.4 auch als ein zusätzliches relatives Risiko von 40 % ausgedrückt werden.
In Fall-Kontroll-Studien (auch Fall-Referenz-Studien genannt) werden Personen mit Krankheit identifiziert (Fälle) und Personen ohne Krankheit identifiziert (Kontrollen oder Referenzen). Vergangene Expositionen der beiden Gruppen werden verglichen. Die Wahrscheinlichkeit, ein exponierter Fall zu sein, wird mit der Wahrscheinlichkeit, eine exponierte Kontrolle zu sein, verglichen. Vollständige Zählungen der Quellpopulationen von exponierten und nicht exponierten Personen sind nicht verfügbar, daher können keine Krankheitsraten berechnet werden. Stattdessen können die exponierten Fälle durch Berechnung von mit den exponierten Kontrollen verglichen werden relative ChancenOder das Wahrscheinlichkeit (Tisch 3).
Tabelle 3. Assoziationsmaße für Fall-Kontroll-Studien: Exposition gegenüber Holzstaub und Adenokarzinom der Nasenhöhle und der Nasennebenhöhlen
|
Projekte |
Steuergriffe |
|
|
Ausgesetzt |
18 |
55 |
|
Unbelichtet |
5 |
140 |
|
Gesamt |
23 |
195 |
Relative Quoten (Odds Ratio) (OR) = ![]()
Zurechenbares Risiko in Prozent der exponierten (![]() ) =
) = ![]()
Bevölkerungsbezogenes Risiko in Prozent (PAR%) = ![]()
woher ![]() = Anteil der exponierten Kontrollen = 55/195 = 0.28
= Anteil der exponierten Kontrollen = 55/195 = 0.28
* In Klammern 95-%-Konfidenzintervalle, berechnet mit den Formeln im Kasten auf der Rückseite.
Quelle: Adaptiert von Hayes et al. 1986.
Relative Wirkungsmaße werden häufiger als absolute Maße verwendet, um die Stärke eines Zusammenhangs zu beschreiben. Absolute Maße können jedoch einen besseren Hinweis auf die Auswirkungen einer Assoziation auf die öffentliche Gesundheit geben. Ein kleiner relativer Anstieg bei einer häufigen Krankheit wie Herzerkrankungen kann mehr Personen betreffen (großer Risikounterschied) und stärkere Auswirkungen auf die öffentliche Gesundheit haben als ein großer relativer Anstieg (aber kleiner absoluter Unterschied) bei einer seltenen Krankheit wie z Angiosarkom der Leber.
Signifikanztest
Das Testen auf statistische Signifikanz wird häufig an Wirkungsmaßen durchgeführt, um die Wahrscheinlichkeit zu bewerten, dass die beobachtete Wirkung von der Nullhypothese abweicht (dh keine Wirkung). Während viele Studien, insbesondere in anderen Bereichen der biomedizinischen Forschung, ihre Bedeutung zum Ausdruck bringen können p-Werte, typischerweise epidemiologische Studien vorhanden Vertrauensintervalle (CI) (auch genannt Grenzen des Selbstvertrauens). Ein 95-%-Konfidenzintervall ist beispielsweise ein Bereich von Werten für das Effektmaß, das das aus den Studiendaten erhaltene geschätzte Maß und dasjenige umfasst, das mit 95-%-Wahrscheinlichkeit den wahren Wert enthält. Bei Werten außerhalb des Intervalls ist es unwahrscheinlich, dass sie das wahre Maß der Wirkung enthalten. Wenn das KI für ein Ratenverhältnis Eins enthält, gibt es keinen statistisch signifikanten Unterschied zwischen den verglichenen Gruppen.
Konfidenzintervalle sind aussagekräftiger als p-Werte allein. Die Größe eines p-Werts wird durch einen oder beide von zwei Gründen bestimmt. Entweder ist das Assoziationsmaß (z. B. Rate Ratio, Risikodifferenz) groß oder die untersuchten Populationen sind groß. Beispielsweise kann ein kleiner Unterschied in den Krankheitsraten, der in einer großen Population beobachtet wird, zu einem hochsignifikanten p-Wert führen. Aus dem p-Wert allein lassen sich die Gründe für den großen p-Wert nicht erkennen. Konfidenzintervalle ermöglichen es uns jedoch, die beiden Faktoren voneinander zu trennen. Erstens ist die Größe des Effekts durch die Werte des Effektmaßes und die vom Intervall umfassten Zahlen erkennbar. Größere Risikokennzahlen weisen beispielsweise auf eine stärkere Wirkung hin. Zweitens beeinflusst die Größe der Grundgesamtheit die Breite des Konfidenzintervalls. Kleine Populationen mit statistisch instabilen Schätzungen erzeugen breitere Konfidenzintervalle als größere Populationen.
Das zum Ausdrücken der Variabilität der Ergebnisse gewählte Konfidenzniveau (die „statistische Signifikanz“) ist willkürlich, liegt jedoch traditionell bei 95 %, was einem p-Wert von 0.05 entspricht. Ein Konfidenzintervall von 95 % enthält mit einer Wahrscheinlichkeit von 95 % das wahre Maß des Effekts. Gelegentlich werden auch andere Konfidenzniveaus wie 90 % verwendet.
Expositionen können dichotom sein (z. B. exponiert und nicht exponiert) oder können viele Expositionsniveaus beinhalten. Wirkungsmaße (dh Reaktion) können je nach Expositionsgrad variieren. Auswerten Expositions-Antwort Beziehungen ist ein wichtiger Teil der Interpretation epidemiologischer Daten. Das Analogon zur Expositions-Wirkung im Tierversuch ist die „Dosis-Wirkung“. Wenn die Reaktion mit der Expositionshöhe zunimmt, ist ein kausaler Zusammenhang wahrscheinlicher, als wenn kein Trend beobachtet wird. Zu den statistischen Tests zur Bewertung von Expositions-Wirkungs-Beziehungen gehören der Mantel-Erweiterungstest und der Chi-Quadrat-Trendtest.
Standardisierung
Um andere Faktoren als die interessierende primäre Exposition und die Krankheit zu berücksichtigen, können Assoziationsmaße verwendet werden standardisiert B. durch Schichtungs- oder Regressionstechniken. Schichtung bedeutet die Einteilung der Populationen in homogene Gruppen in Bezug auf den Faktor (z. B. Geschlechtsgruppen, Altersgruppen, Rauchergruppen). Risikokennzahlen oder Quotenverhältnisse werden für jede Schicht berechnet und gewichtete Gesamtdurchschnitte der Risikokennzahlen oder Quotenverhältnisse werden berechnet. Diese Gesamtwerte spiegeln den um den Stratifizierungsfaktor bereinigten Zusammenhang zwischen der primären Exposition und der Erkrankung wider, dh den Zusammenhang mit den Effekten des Stratifizierungsfaktors herausgerechnet.
A standardisiertes Ratenverhältnis (SRR) ist das Verhältnis zweier standardisierter Zinssätze. Mit anderen Worten, ein SRR ist ein gewichteter Durchschnitt von schichtspezifischen Ratenverhältnissen, wobei die Gewichtungen für jede Schicht die Personen-Zeit-Verteilung der nicht exponierten oder Bezugsgruppe sind. SRRs für zwei oder mehr Gruppen können verglichen werden, wenn dieselben Gewichte verwendet werden. Konfidenzintervalle können für SRRs wie für Ratenverhältnisse konstruiert werden.
Das standardisierte Sterblichkeitsrate (SMR) ist ein gewichteter Durchschnitt von altersspezifischen Quotenverhältnissen, wobei die Gewichtungen (z. B. Person-Time-at-Risk) von der untersuchten Gruppe und die Quoten von der Referenzpopulation stammen, das Gegenteil der Situation in einer SRR. Die übliche Bezugspopulation ist die allgemeine Bevölkerung, deren Sterblichkeitsraten möglicherweise leicht verfügbar sind und auf großen Zahlen basieren und daher stabiler sind als die Verwendung von Raten aus einer nicht exponierten Kohorte oder Untergruppe der untersuchten Berufsgruppe. Die Verwendung der Gewichte der Kohorte anstelle der Referenzpopulation wird als indirekte Standardisierung bezeichnet. Die SMR ist das Verhältnis der beobachteten Anzahl von Todesfällen in der Kohorte zur erwarteten Anzahl, basierend auf den Raten der Referenzpopulation (das Verhältnis wird zur Darstellung typischerweise mit 100 multipliziert). Wenn kein Zusammenhang besteht, beträgt die SMR 100. Es sollte beachtet werden, dass zwei oder mehr SMRs tendenziell nicht vergleichbar sind, da die Raten von der Referenzpopulation und die Gewichtungen von der Studiengruppe stammen. Diese Nicht-Vergleichbarkeit wird bei der Interpretation epidemiologischer Daten oft vergessen und es können falsche Schlussfolgerungen gezogen werden.
Healthy-Worker-Effekt
Berufskohorten haben sehr häufig eine niedrigere Gesamtmortalität als die allgemeine Bevölkerung, selbst wenn die Arbeitnehmer einem erhöhten Risiko für ausgewählte Todesursachen aufgrund von Expositionen am Arbeitsplatz ausgesetzt sind. Dieses Phänomen, genannt die gesunder Arbeitereffekt, spiegelt die Tatsache wider, dass jede Gruppe von Erwerbstätigen im Durchschnitt wahrscheinlich gesünder ist als die allgemeine Bevölkerung, zu der Arbeitnehmer und Personen gehören, die aufgrund von Krankheiten und Behinderungen nicht arbeiten können. Die Gesamtsterblichkeitsrate in der Allgemeinbevölkerung ist tendenziell höher als die Rate bei Arbeitnehmern. Die Wirkung ist je nach Todesursache unterschiedlich stark. Beispielsweise scheint es bei Krebs im Allgemeinen weniger wichtig zu sein als bei chronisch obstruktiven Lungenerkrankungen. Ein Grund dafür ist, dass sich die meisten Krebserkrankungen wahrscheinlich nicht aus einer Prädisposition für Krebs entwickelt hätten, die der Berufswahl in einem jüngeren Alter zugrunde liegt. Der Gesunde-Arbeiter-Effekt in einer bestimmten Gruppe von Arbeitnehmern nimmt im Laufe der Zeit tendenziell ab.
Proportionale Sterblichkeit
Manchmal ist eine vollständige tabellarische Aufstellung einer Kohorte (dh gefährdete Personenzeit) nicht verfügbar, und es gibt nur Informationen zu den Todesfällen oder einer Teilmenge von Todesfällen in der Kohorte (z. B. Todesfälle unter Rentnern und aktiven Angestellten, aber nicht unter Arbeitnehmern). die ihre Erwerbstätigkeit aufgegeben haben, bevor sie Anspruch auf eine Rente hatten). Die Berechnung von Personenjahren erfordert spezielle Methoden zur Erfassung der Personenzeit, einschließlich Sterbetafelmethoden. Ohne Angaben zur gesamten Personenzeit aller Kohortenmitglieder, unabhängig vom Krankheitsstatus, können SMRs und SRRs nicht berechnet werden. Stattdessen, proportionale Sterblichkeitsverhältnisse (PMRs) verwendet werden. Ein PMR ist das Verhältnis der beobachteten Anzahl von Todesfällen aufgrund einer bestimmten Ursache im Vergleich zu der erwarteten Anzahl, basierend auf dem Anteil der Gesamttodesfälle aufgrund der spezifischen Ursache in der Referenzpopulation, multipliziert mit der Anzahl der Gesamttodesfälle in der Studie Gruppe, multipliziert mit 100.
Da der Anteil der Todesfälle aus allen Todesursachen zusammen 1 (PMR = 100) betragen muss, scheinen einige PMRs zu hoch zu sein, sind aber tatsächlich künstlich aufgeblasen aufgrund echter Defizite bei anderen Todesursachen. In ähnlicher Weise können einige offensichtliche Defizite lediglich tatsächliche Exzesse bei anderen Todesursachen widerspiegeln. Wenn beispielsweise Pestizidausbringer aus der Luft einen großen realen Überschuss an Todesfällen aufgrund von Unfällen haben, kann die mathematische Anforderung, dass der PMR für alle Ursachen zusammen gleich 100 ist, dazu führen, dass die eine oder andere Todesursache mangelhaft erscheint, selbst wenn die Sterblichkeit zu hoch ist. Um dieses potenzielle Problem zu lindern, können Forscher, die sich hauptsächlich für Krebs interessieren, kalkulieren proportionale Krebssterblichkeitsraten (PCMR). PCMRs vergleichen die beobachtete Zahl der Krebstodesfälle mit der erwarteten Zahl basierend auf dem Anteil der gesamten Krebstodesfälle (anstelle aller Todesfälle) für den interessierenden Krebs in der Referenzpopulation multipliziert mit der Gesamtzahl der Krebstodesfälle in der Studiengruppe, multipliziert mit 100. Somit wird die PCMR nicht durch eine Abweichung (Überschuss oder Mangel) bei einer nicht krebsbedingten Todesursache wie Unfällen, Herzerkrankungen oder nicht bösartigen Lungenerkrankungen beeinflusst.
PMR-Studien können besser analysiert werden mit Sterblichkeit Odds Ratios (MORs), wobei die Daten im Wesentlichen so analysiert werden, als ob sie aus einer Fall-Kontroll-Studie stammen würden. Die „Kontrollen“ sind die Todesfälle aus einer Untergruppe aller Todesfälle, von denen angenommen wird, dass sie in keinem Zusammenhang mit der untersuchten Exposition stehen. Wenn beispielsweise das Hauptinteresse der Studie Krebs war, könnten die Sterblichkeitswahrscheinlichkeitsverhältnisse berechnet werden, indem die Exposition bei den Krebstoten mit der Exposition bei den kardiovaskulären Todesfällen verglichen wird. Dieser Ansatz vermeidet wie die PCMR die Probleme mit der PMR, die entstehen, wenn eine Schwankung bei einer Todesursache das offensichtliche Risiko einer anderen beeinflusst, einfach weil die Gesamt-PMR gleich 100 sein muss. Die Wahl der Kontrolltodesursachen ist jedoch kritisch . Wie oben erwähnt, müssen sie nicht mit der Exposition zusammenhängen, aber die mögliche Beziehung zwischen Exposition und Krankheit ist möglicherweise für viele potenzielle Kontrollkrankheiten nicht bekannt.
Zurechenbares Risiko
Es stehen Maßzahlen zur Verfügung, die das Krankheitsausmaß ausdrücken, das einer Exposition zuzuschreiben wäre, wenn der beobachtete Zusammenhang zwischen der Exposition und der Krankheit kausal wäre. Das zurechenbares Risiko im Exponierten (ARe) ist die Krankheitsrate bei den Exponierten minus der Rate bei den Nicht-Exponierten. Da Krankheitsraten in Fall-Kontroll-Studien nicht direkt gemessen werden können, ist der ARe ist nur für Kohortenstudien berechenbar. Eine verwandte, intuitivere Maßnahme, die zurechenbaren Risikoprozentsatz im Exponierten (ARe%), können aus beiden Studiendesigns gewonnen werden. Die ARe% ist der Anteil der in der exponierten Bevölkerung aufgetretenen Fälle, der auf die Exposition zurückzuführen ist (Formel siehe Tabelle 2 und Tabelle 3). Die ARe% ist das Quotenverhältnis (oder Odds Ratio) minus 1, geteilt durch das Quotenverhältnis (oder Odds Ratio), multipliziert mit 100.
Das der Bevölkerung zuzurechnendes Risiko (PAR) und die der Bevölkerung zuzurechnendes Risiko in Prozent (PAR%) oder ätiologische Fraktion, drücken das Ausmaß der Erkrankung in der Gesamtbevölkerung aus, die sich aus exponierten und nicht exponierten Personen zusammensetzt, die auf die Exposition zurückzuführen ist, wenn der beobachtete Zusammenhang kausal ist. Der PAR kann aus Kohortenstudien erhalten werden (Tabelle 28.3) und der PAR% kann sowohl in Kohorten- als auch in Fall-Kontroll-Studien berechnet werden (Tabelle 2 und Tabelle 3).
Repräsentativität
Es gibt mehrere Risikomaße, die beschrieben wurden. Jeder übernimmt zugrunde liegende Methoden zum Zählen von Ereignissen und in die Repräsentanten dieser Ereignisse zu einer definierten Gruppe. Wenn Ergebnisse studienübergreifend verglichen werden, ist ein Verständnis der verwendeten Methoden unerlässlich, um beobachtete Unterschiede zu erklären.
Biomechanik
Ziele und Grundsätze
Die Biomechanik ist eine Disziplin, die sich dem Studium des Körpers so nähert, als wäre er ein rein mechanisches System: Alle Teile des Körpers werden mit mechanischen Strukturen verglichen und als solche untersucht. Folgende Analogien lassen sich beispielsweise ziehen:
- Knochen: Hebel, Bauteile
- Fleisch: Volumen und Massen
- Gelenke: Lagerflächen und Gelenke
- Gelenkbeläge: Schmiermittel
- Muskeln: Motoren, Federn
- Nerven: Feedback-Kontrollmechanismen
- Organe: Netzteile
- Sehnen: Seile
- Gewebe: Federn
- Körperhöhlen: Luftballons.
Das Hauptziel der Biomechanik ist es, die Art und Weise zu untersuchen, wie der Körper Kraft erzeugt und Bewegung erzeugt. Die Disziplin stützt sich hauptsächlich auf Anatomie, Mathematik und Physik; verwandte Disziplinen sind Anthropometrie (Lehre der menschlichen Körpermaße), Arbeitsphysiologie und Kinesiologie (Lehre der Grundlagen der Mechanik und Anatomie in Bezug auf die menschliche Bewegung).
Bei der Berücksichtigung der Arbeitsgesundheit des Arbeitnehmers hilft die Biomechanik zu verstehen, warum einige Aufgaben zu Verletzungen und Erkrankungen führen. Einige relevante Arten von gesundheitsschädlichen Auswirkungen sind Muskelverspannungen, Gelenkprobleme, Rückenprobleme und Müdigkeit.
Rückenzerrungen und Verstauchungen sowie schwerwiegendere Bandscheibenprobleme sind häufige Beispiele für vermeidbare Arbeitsunfälle. Diese treten häufig aufgrund einer plötzlichen besonderen Überlastung auf, können aber auch die Ausübung übermäßiger Kräfte des Körpers über viele Jahre widerspiegeln: Probleme können plötzlich auftreten oder sich erst nach einiger Zeit entwickeln. Ein Beispiel für ein Problem, das sich im Laufe der Zeit entwickelt, ist der „Finger der Näherin“. Eine neuere Beschreibung beschreibt die Hände einer Frau, die nach 28 Jahren Arbeit in einer Bekleidungsfabrik sowie Nähen in ihrer Freizeit eine verhärtete, verdickte Haut und eine Unfähigkeit, ihre Finger zu beugen, entwickelte (Poole 1993). (Insbesondere litt sie an einer Flexionsdeformität des rechten Zeigefingers, hervorstehenden Heberden-Knoten an Zeigefinger und Daumen der rechten Hand und einer hervorstehenden Schwiele am rechten Mittelfinger aufgrund der ständigen Reibung durch die Schere.) Röntgenbild Filme ihrer Hände zeigten schwere degenerative Veränderungen in den äußersten Gelenken ihres rechten Zeige- und Mittelfingers mit Gelenkspaltverlust, Gelenksklerose (Gewebeverhärtung), Osteophyten (Knochenwucherungen am Gelenk) und Knochenzysten.
Die Kontrolle am Arbeitsplatz ergab, dass diese Probleme auf eine wiederholte Überstreckung (Aufwärtsbeugung) des äußersten Fingergelenks zurückzuführen waren. Mechanische Überlastung und Einschränkung des Blutflusses (sichtbar als Weißfärbung des Fingers) wären an diesen Gelenken maximal. Diese Probleme entwickelten sich als Reaktion auf wiederholte Muskelanstrengung an einer anderen Stelle als dem Muskel.
Die Biomechanik hilft, Wege zur Gestaltung von Aufgaben vorzuschlagen, um diese Art von Verletzungen zu vermeiden oder schlecht gestaltete Aufgaben zu verbessern. Abhilfen für diese speziellen Probleme bestehen darin, die Schere neu zu gestalten und die Nähaufgaben zu ändern, um die Notwendigkeit für die durchgeführten Aktionen zu beseitigen.
Zwei wichtige Prinzipien der Biomechanik sind:
- Muskeln treten paarweise auf. Muskeln können sich nur zusammenziehen, also muss es für jedes Gelenk einen Muskel (oder eine Muskelgruppe) geben, um es in eine Richtung zu bewegen, und einen entsprechenden Muskel (oder eine Muskelgruppe), um es in die entgegengesetzte Richtung zu bewegen. Abbildung 1 zeigt den Punkt für das Ellbogengelenk.
- Muskeln kontrahieren am effizientesten, wenn sich das Muskelpaar in entspannter Balance befindet. Der Muskel wirkt am effizientesten, wenn er sich in der Mitte des Gelenks befindet, das er beugt. Dies aus zwei Gründen: Erstens, wenn der Muskel versucht, sich zusammenzuziehen, während er verkürzt ist, zieht er gegen den verlängerten Gegenmuskel. Da letzterer gedehnt wird, übt er eine elastische Gegenkraft aus, die der kontrahierende Muskel überwinden muss. Abbildung 2 zeigt, wie sich die Muskelkraft mit der Muskellänge ändert.
Abbildung 1. Skelettmuskeln treten paarweise auf, um eine Bewegung einzuleiten oder umzukehren
Abbildung 2. Die Muskelspannung variiert mit der Muskellänge
Zweitens, wenn der Muskel versucht, sich in einem anderen als dem mittleren Bereich der Bewegung des Gelenks zusammenzuziehen, wird er mit einem mechanischen Nachteil arbeiten. Abbildung 3 veranschaulicht die Änderung des mechanischen Vorteils für den Ellbogen in drei verschiedenen Positionen.
Abbildung 3. Optimale Positionen für die Gelenkbewegung
Aus diesen Grundsätzen folgt ein wichtiges Kriterium für die Arbeitsgestaltung: Die Arbeit sollte so gestaltet werden, dass sie mit den gegenüberliegenden Muskeln jedes Gelenks in entspanntem Gleichgewicht erfolgt. Für die meisten Gelenke bedeutet dies, dass sich das Gelenk etwa im mittleren Bewegungsbereich befinden sollte.
Diese Regel bedeutet auch, dass die Muskelspannung während der Ausführung einer Aufgabe auf ein Minimum reduziert wird. Ein Beispiel für die Verletzung der Regel ist das Überbeanspruchungssyndrom (RSI, Repetitive Strain Injury), das die Muskeln des oberen Teils des Unterarms bei Tastaturbedienern betrifft, die gewöhnlich mit nach oben gebeugtem Handgelenk arbeiten. Oft wird diese Gewohnheit dem Bediener durch das Design der Tastatur und der Arbeitsstation aufgezwungen.
Anwendungen
Im Folgenden sind einige Beispiele aufgeführt, die die Anwendung der Biomechanik veranschaulichen.
Der optimale Durchmesser von Werkzeuggriffen
Der Durchmesser eines Griffs beeinflusst die Kraft, die die Handmuskeln auf ein Werkzeug ausüben können. Untersuchungen haben gezeigt, dass der optimale Griffdurchmesser von der Verwendung des Werkzeugs abhängt. Um einen Schub entlang der Grifflinie auszuüben, ist der beste Durchmesser einer, der es den Fingern und dem Daumen ermöglicht, einen leicht überlappenden Griff anzunehmen. Das sind etwa 40 mm. Um ein Drehmoment auszuüben, ist ein Durchmesser von etwa 50–65 mm optimal. (Leider sind die meisten Handles für beide Zwecke kleiner als diese Werte.)
Die Verwendung einer Zange
Als Spezialfall eines Griffs hängt die Kraftausübung mit einer Zange von der Grifftrennung ab, wie in Abbildung 4 dargestellt.
Abbildung 4. Von männlichen und weiblichen Benutzern ausgeübte Greifkraft der Zangenbacken als Funktion der Grifftrennung
Sitzhaltung
Die Elektromyographie ist eine Technik, mit der die Muskelspannung gemessen werden kann. In einer Studie über die Spannung in der Erektor Spinae Muskeln (des Rückens) von sitzenden Probanden wurde festgestellt, dass das Zurücklehnen (mit geneigter Rückenlehne) die Spannung in diesen Muskeln verringerte. Der Effekt lässt sich dadurch erklären, dass die Rückenlehne mehr Gewicht des Oberkörpers aufnimmt.
Röntgenuntersuchungen von Probanden in verschiedenen Haltungen zeigten, dass die Position des entspannten Gleichgewichts der Muskeln, die das Hüftgelenk öffnen und schließen, einem Hüftwinkel von etwa 135º entspricht. Dies kommt der Position (128º) nahe, die dieses Gelenk in der Schwerelosigkeit (im Weltraum) einnimmt. In der sitzenden Haltung, mit einem Winkel von 90º an der Hüfte, neigen die Kniesehnenmuskeln, die sowohl über das Knie- als auch über das Hüftgelenk verlaufen, dazu, das Kreuzbein (den Teil der Wirbelsäule, der mit dem Becken verbunden ist) in eine vertikale Position zu ziehen. Der Effekt besteht darin, die natürliche Lordose (Krümmung) der Lendenwirbelsäule zu beseitigen; Stühle sollten entsprechende Rückenlehnen haben, um diese Anstrengung auszugleichen.
Schrauben
Warum werden Schrauben im Uhrzeigersinn eingesetzt? Die Praxis entstand wahrscheinlich aus der unbewussten Erkenntnis, dass die Muskeln, die den rechten Arm im Uhrzeigersinn drehen (die meisten Menschen sind Rechtshänder), größer (und daher stärker) sind als die Muskeln, die ihn gegen den Uhrzeigersinn drehen.
Beachten Sie, dass Linkshänder beim Schrauben per Hand benachteiligt sind. Etwa 9 % der Bevölkerung sind Linkshänder und benötigen daher in manchen Situationen spezielle Werkzeuge: Scheren und Dosenöffner sind zwei solche Beispiele.
Eine Studie über Menschen, die Schraubendreher bei einer Montagearbeit verwendeten, zeigte eine subtilere Beziehung zwischen einer bestimmten Bewegung und einem bestimmten Gesundheitsproblem. Es wurde festgestellt, dass je größer der Ellbogenwinkel (je gerader der Arm) war, desto mehr Menschen hatten eine Entzündung am Ellbogen. Der Grund für diesen Effekt ist, dass der Muskel, der den Unterarm dreht (Bizeps), auch den Radiusköpfchen (Unterarmknochen) auf das Capitulum (runder Kopf) des Humerus (Oberarmknochen) zieht. Die erhöhte Kraft beim höheren Ellbogenwinkel verursachte eine größere Reibungskraft am Ellbogen mit einer daraus resultierenden Erwärmung des Gelenks, was zu der Entzündung führte. Bei dem höheren Winkel musste der Muskel auch mit größerer Kraft ziehen, um die Schraubbewegung zu bewirken, sodass eine größere Kraft aufgebracht wurde, als es bei einem Ellbogen bei etwa 90° erforderlich gewesen wäre. Die Lösung bestand darin, die Aufgabe näher an die Bediener zu verlagern, um den Ellbogenwinkel auf etwa 90º zu reduzieren.
Die oben genannten Fälle zeigen, dass für die Anwendung der Biomechanik am Arbeitsplatz ein angemessenes Verständnis der Anatomie erforderlich ist. Designer von Aufgaben müssen möglicherweise Experten für funktionelle Anatomie konsultieren, um die besprochenen Problemtypen zu antizipieren. (Der Pocket-Ergonom (Brown und Mitchell 1986), basierend auf elektromyografischer Forschung, schlägt viele Möglichkeiten vor, körperliche Beschwerden bei der Arbeit zu reduzieren.)
Manuelle Materialhandhabung
Die manuelle Handhabung umfasst das Heben, Senken, Schieben, Ziehen, Tragen, Bewegen, Halten und Fesseln und umfasst einen großen Teil der Tätigkeiten des Arbeitslebens.
Die Biomechanik hat offensichtlich eine direkte Relevanz für manuelle Handhabungsarbeiten, da sich Muskeln bewegen müssen, um Aufgaben auszuführen. Die Frage ist: Wie viel körperliche Arbeit ist den Menschen zumutbar? Die Antwort hängt von den Umständen ab; Es gibt wirklich drei Fragen, die gestellt werden müssen. Jeder hat eine Antwort, die auf wissenschaftlich recherchierten Kriterien basiert:
- Wie viel kann ohne Schädigung des Körpers (in Form von z. B. Muskelverspannungen, Bandscheibenschäden oder Gelenkbeschwerden) bewältigt werden? Dies nennt man die biomechanisches Kriterium.
- Wie viel kann bewältigt werden, ohne die Lungen zu überanstrengen (schweres Atmen bis zum Hecheln)? Dies nennt man die physiologisches Kriterium.
- Wie viel fühlen sich die Menschen in der Lage, bequem damit umzugehen? Dies nennt man die psychophysisches Kriterium.
Diese drei unterschiedlichen Kriterien sind notwendig, weil es drei sehr unterschiedliche Reaktionen gibt, die auf Hebeaufgaben auftreten können: Wenn die Arbeit den ganzen Tag dauert, geht es darum, wie die Person arbeitet fühlt sich über die Aufgabe – das psychophysische Kriterium; wenn die aufzuwendende Kraft groß ist, wäre die Sorge, dass Muskeln und Gelenke sind nicht überladen bis zur Schädigung – das biomechanische Kriterium; und wenn die Arbeitsgeschwindigkeit zu groß ist, dann kann es durchaus das physiologische Kriterium oder die aerobe Kapazität der Person überschreiten.
Viele Faktoren bestimmen das Ausmaß der Belastung des Körpers durch eine manuelle Handhabungsaufgabe. Alle schlagen Möglichkeiten der Kontrolle vor.
Haltung und Bewegungen
Wenn die Aufgabe erfordert, dass sich eine Person mit einer Last dreht oder nach vorne greift, ist das Verletzungsrisiko größer. Die Arbeitsstation kann oft umgestaltet werden, um diese Aktionen zu verhindern. Wenn das Heben auf Bodenhöhe beginnt, treten mehr Rückenverletzungen auf als auf der Mitte des Oberschenkels, und dies legt einfache Kontrollmaßnahmen nahe. (Dies gilt auch für das Hochheben.)
Die Ladung.
Die Ladung selbst kann durch ihr Gewicht und ihren Standort das Fahrverhalten beeinflussen. Andere Faktoren wie seine Form, seine Stabilität, seine Größe und seine Gleitfähigkeit können alle die Leichtigkeit einer Handhabungsaufgabe beeinflussen.
Organisation und Umfeld.
Auch die Arbeitsorganisation, sowohl räumlich als auch zeitlich (zeitlich), beeinflusst die Handhabung. Es ist besser, die Last des Entladens eines Lastwagens in einer Lieferbucht für eine Stunde auf mehrere Personen zu verteilen, als einen Arbeiter zu bitten, den ganzen Tag mit dieser Aufgabe zu verbringen. Die Umgebung beeinflusst die Handhabung – schlechtes Licht, unordentliche oder unebene Böden und schlechte Haushaltsführung können alle dazu führen, dass eine Person stolpert.
Persönliche Faktoren.
Persönliche Handhabungsfähigkeiten, das Alter der Person und die getragene Kleidung können ebenfalls die Handhabungsanforderungen beeinflussen. Eine Schulung für Training und Heben ist erforderlich, um sowohl die notwendigen Informationen bereitzustellen als auch Zeit für die Entwicklung der körperlichen Fähigkeiten zur Handhabung zu geben. Jüngere Menschen sind stärker gefährdet; Andererseits haben ältere Menschen weniger Kraft und weniger physiologische Kapazität. Enge Kleidung kann die für eine Aufgabe erforderliche Muskelkraft erhöhen, da sich Menschen gegen das enge Tuch anstrengen. Klassische Beispiele sind die Kitteluniform der Krankenschwester und enge Overalls, wenn Menschen über ihren Köpfen arbeiten.
Empfohlene Gewichtsgrenzen
Die oben genannten Punkte zeigen, dass es unmöglich ist, ein Gewicht anzugeben, das unter allen Umständen „sicher“ ist. (Gewichtsgrenzen sind von Land zu Land tendenziell willkürlich unterschiedlich. So durften indische Hafenarbeiter einst 110 kg heben, während ihre Kollegen in der ehemaligen Volksrepublik Deutschland auf 32 kg “beschränkt” waren .) Gewichtsgrenzen sind auch tendenziell zu hoch. Die in vielen Ländern vorgeschlagenen 55 kg werden aufgrund neuerer wissenschaftlicher Erkenntnisse heute als viel zu hoch angesehen. Das National Institute for Occupational Safety and Health (NIOSH) in den Vereinigten Staaten hat 23 1991 kg als Belastungsgrenze festgelegt (Waters et al. 1993).
Jede Hebeaufgabe muss für sich betrachtet werden. Ein nützlicher Ansatz zur Bestimmung einer Gewichtsgrenze für eine Hebeaufgabe ist die von NIOSH entwickelte Gleichung:
RWL = LC x HM x VM x DM x AM x CM x FM
Wo
RWL = empfohlene Gewichtsgrenze für die betreffende Aufgabe
HM = der horizontale Abstand vom Schwerpunkt der Last zum Mittelpunkt zwischen den Knöcheln (mindestens 15 cm, höchstens 80 cm)
VM = der vertikale Abstand zwischen dem Schwerpunkt der Last und dem Boden am Beginn des Hebevorgangs (maximal 175 cm)
DM = der vertikale Weg des Lifts (mindestens 25 cm, maximal 200 cm)
AM = Asymmetriefaktor – der Winkel, von dem die Aufgabe direkt vor dem Körper abweicht
CM = Kopplungsmultiplikator – die Fähigkeit, das zu hebende Objekt gut zu greifen, was in einer Referenztabelle zu finden ist
FM = Frequenzmultiplikatoren – die Frequenz des Hebens.
Alle Längenvariablen in der Gleichung werden in Zentimetern ausgedrückt. Es sollte beachtet werden, dass 23 kg das maximale Gewicht ist, das NIOSH zum Heben empfiehlt. Dies wurde von 40 kg reduziert, nachdem die Beobachtung vieler Menschen, die viele Hebeaufgaben verrichteten, gezeigt hatte, dass der durchschnittliche Abstand vom Körper zu Beginn des Hebens 25 cm beträgt, nicht die 15 cm, die in einer früheren Version der Gleichung angenommen wurden (NIOSH 1981 ).
Lifting-Index.
Durch den Vergleich des zu hebenden Gewichts in der Aufgabe und der RWL wird ein Hebeindex (LI) kann gemäß der Beziehung erhalten werden:
LI=(zu handhabendes Gewicht)/RWL.
Daher ist eine besonders wertvolle Verwendung der NIOSH-Gleichung die Anordnung von Hebeaufgaben nach Schweregrad, wobei der Hebeindex verwendet wird, um Prioritäten für Maßnahmen festzulegen. (Die Gleichung weist jedoch eine Reihe von Einschränkungen auf, die für eine möglichst effektive Anwendung verstanden werden müssen. Siehe Waters et al. 1993).
Schätzen der durch die Aufgabe auferlegten Kompression der Wirbelsäule
Es ist Computersoftware verfügbar, um die Wirbelsäulenkompression abzuschätzen, die durch eine manuelle Handhabungsaufgabe erzeugt wird. Die statischen 2D- und 3D-Festigkeitsvorhersageprogramme der University of Michigan („Backsoft“) schätzen die Wirbelsäulenkompression. Die für das Programm erforderlichen Eingaben sind:
- die Körperhaltung, in der die Handhabungstätigkeit ausgeführt wird
- die ausgeübte Kraft
- die Richtung der Kraftausübung
- die Anzahl der Hände, die die Kraft ausüben
- das Perzentil der untersuchten Bevölkerung.
Die 2D- und 3D-Programme unterscheiden sich darin, dass die 3D-Software Berechnungen ermöglicht, die sich auf Körperhaltungen in drei Dimensionen beziehen. Die Programmausgabe gibt Wirbelsäulenkompressionsdaten und listet den Prozentsatz der ausgewählten Population auf, der in der Lage wäre, die bestimmte Aufgabe auszuführen, ohne die empfohlenen Grenzen für sechs Gelenke zu überschreiten: Knöchel, Knie, Hüfte, erste Lendenwirbelsäule, Schulter und Ellbogen. Diese Methode hat auch eine Reihe von Einschränkungen, die vollständig verstanden werden müssen, um den maximalen Nutzen aus dem Programm zu ziehen.
Immuntoxikologie
Die Funktionen des Immunsystems bestehen darin, den Körper vor eindringenden Infektionserregern zu schützen und eine Immunüberwachung gegen entstehende Tumorzellen bereitzustellen. Es hat eine erste Verteidigungslinie, die unspezifisch ist und selbst Effektorreaktionen initiieren kann, und einen erworbenen spezifischen Zweig, in dem Lymphozyten und Antikörper die Spezifität der Erkennung und anschließenden Reaktivität gegenüber dem Antigen tragen.
Immuntoxikologie wurde definiert als „die Disziplin, die sich mit der Untersuchung der Ereignisse befasst, die als Folge der Wechselwirkung von Fremdstoffen mit dem Immunsystem zu unerwünschten Wirkungen führen können. Diese unerwünschten Ereignisse können als Folge von (1) einer direkten und/oder indirekten Wirkung des Xenobiotikums (und/oder seines Biotransformationsprodukts) auf das Immunsystem oder (2) einer immunologisch basierten Wirtsantwort auf die Verbindung und/oder resultieren seine Metaboliten oder durch die Verbindung oder seine Metaboliten modifizierte Wirtsantigene“ (Berlin et al. 1987).
Wenn das Immunsystem als passives Ziel chemischer Angriffe fungiert, kann das Ergebnis eine verringerte Resistenz gegen Infektionen und bestimmte Formen von Neoplasien oder eine Fehlregulation/Stimulation des Immunsystems sein, die eine Allergie oder Autoimmunität verschlimmern kann. In dem Fall, dass das Immunsystem auf die antigene Spezifität des Xenobiotikums oder des durch die Verbindung modifizierten Wirtsantigens reagiert, kann sich die Toxizität in Form von Allergien oder Autoimmunerkrankungen manifestieren.
Tiermodelle zur Untersuchung der chemisch induzierten Immunsuppression wurden entwickelt, und eine Reihe dieser Methoden sind validiert (Burleson, Munson und Dean 1995; IPCS 1996). Für Testzwecke wird ein abgestufter Ansatz verfolgt, um eine angemessene Auswahl aus der überwältigenden Anzahl verfügbarer Assays zu treffen. Im Allgemeinen besteht das Ziel der ersten Stufe darin, potenzielle Immunotoxine zu identifizieren. Wenn eine potenzielle Immuntoxizität festgestellt wird, wird eine zweite Teststufe durchgeführt, um die beobachteten Veränderungen zu bestätigen und weiter zu charakterisieren. Untersuchungen der dritten Ebene umfassen spezielle Studien zum Wirkmechanismus der Verbindung. Mehrere Xenobiotika wurden in solchen Studien mit Labortieren als Immunotoxine identifiziert, die eine Immunsuppression verursachen.
Die Datenlage zu Störungen der Immunfunktion beim Menschen durch Umweltchemikalien ist begrenzt (Descotes 1986; NRC Subcommittee on Immunotoxicology 1992). Der Verwendung von Immuntoxizitätsmarkern wurde in klinischen und epidemiologischen Studien zur Untersuchung der Wirkung dieser Chemikalien auf die menschliche Gesundheit wenig Beachtung geschenkt. Solche Studien wurden nicht häufig durchgeführt, und ihre Interpretation lässt häufig keine eindeutigen Schlussfolgerungen zu, beispielsweise aufgrund der unkontrollierten Natur der Exposition. Daher bildet derzeit die Immuntoxizitätsbewertung bei Nagern mit anschließender Extrapolation auf den Menschen die Grundlage für Entscheidungen über Gefährdung und Risiko.
Überempfindlichkeitsreaktionen, insbesondere allergisches Asthma und Kontaktdermatitis, sind wichtige arbeitsbedingte Gesundheitsprobleme in Industrieländern (Vos, Younes und Smith 1995). Das Phänomen der Kontaktsensibilisierung wurde zuerst am Meerschweinchen untersucht (Andersen und Maibach 1985). Bis vor kurzem war dies die Art der Wahl für prädiktive Tests. Es stehen viele Meerschweinchen-Testverfahren zur Verfügung, wobei die am häufigsten angewandten der Meerschweinchen-Maximierungstest und der okkludierte Patch-Test von Buehler sind. Meerschweinchentests und neuere Ansätze, die an Mäusen entwickelt wurden, wie z. B. Ohrschwellungstests und der lokale Lymphknotentest, bieten dem Toxikologen die Werkzeuge, um die Gefahr einer Hautsensibilisierung einzuschätzen. Ganz anders verhält es sich bei der Sensibilisierung der Atemwege. Es gibt noch keine gut validierten oder allgemein anerkannten Methoden zur Identifizierung chemischer Atemwegsallergene, obwohl Fortschritte bei der Entwicklung von Tiermodellen zur Untersuchung chemischer Atemwegsallergien bei Meerschweinchen und Maus erzielt wurden.
Humandaten zeigen, dass chemische Wirkstoffe, insbesondere Medikamente, Autoimmunerkrankungen hervorrufen können (Kammüller, Bloksma und Seinen 1989). Es gibt eine Reihe experimenteller Tiermodelle menschlicher Autoimmunerkrankungen. Solche umfassen sowohl spontane Pathologie (zum Beispiel systemischer Lupus erythematodes bei New Zealand Black-Mäusen) als auch Autoimmunphänomene, die durch experimentelle Immunisierung mit einem kreuzreaktiven Autoantigen induziert werden (zum Beispiel durch das H37Ra-Adjuvans induzierte Arthritis in Ratten vom Lewis-Stamm). Diese Modelle werden in der präklinischen Bewertung von Immunsuppressiva angewendet. Nur sehr wenige Studien haben sich mit dem Potenzial dieser Modelle für die Bewertung befasst, ob ein Fremdstoff die induzierte oder angeborene Autoimmunität verschlimmert. Tiermodelle, die geeignet sind, die Fähigkeit von Chemikalien zur Auslösung von Autoimmunerkrankungen zu untersuchen, fehlen praktisch. Ein Modell, das in begrenztem Umfang verwendet wird, ist der Popliteal-Lymphknoten-Assay bei Mäusen. Wie beim Menschen spielen genetische Faktoren bei der Entwicklung von Autoimmunerkrankungen (AD) bei Labortieren eine entscheidende Rolle, was den Vorhersagewert solcher Tests einschränken wird.
Das Immunsystem
Die Hauptfunktion des Immunsystems ist die Abwehr von Bakterien, Viren, Parasiten, Pilzen und neoplastischen Zellen. Erreicht wird dies durch das fein abgestimmte Zusammenspiel verschiedener Zelltypen und ihrer löslichen Mediatoren. Die Wirtsabwehr kann grob unterteilt werden in unspezifische oder angeborene Resistenz und spezifische oder erworbene, durch Lymphozyten vermittelte Immunität (Roitt, Brostoff und Male 1989).
Komponenten des Immunsystems sind im ganzen Körper vorhanden (Jones et al. 1990). Das Lymphozytenkompartiment befindet sich innerhalb lymphoider Organe (Abbildung 1). Das Knochenmark und der Thymus werden als primäre oder zentrale lymphatische Organe klassifiziert; Zu den sekundären oder peripheren lymphatischen Organen gehören Lymphknoten, Milz und lymphatisches Gewebe entlang sekretorischer Oberflächen wie dem Magen-Darm-Trakt und den Atemwegen, das sogenannte Mukosa-assoziierte lymphatische Gewebe (MALT). Etwa die Hälfte der körpereigenen Lymphozyten befinden sich zu jedem Zeitpunkt in MALT. Außerdem ist die Haut ein wichtiges Organ für die Induktion von Immunantworten auf auf der Haut vorhandene Antigene. Wichtig in diesem Prozess sind epidermale Langerhans-Zellen, die eine Antigen-präsentierende Funktion haben.
Abbildung 1. Primäre und sekundäre lymphatische Organe und Gewebe
Phagozytische Zellen der Monozyten/Makrophagen-Linie, die als mononukleäres Phagozytensystem (MPS) bezeichnet werden, kommen in lymphatischen Organen und auch an extranodalen Stellen vor; Zu den extranodalen Phagozyten gehören Kupffer-Zellen in der Leber, Alveolarmakrophagen in der Lunge, Mesangialmakrophagen in der Niere und Gliazellen im Gehirn. Polymorphkernige Leukozyten (PMNs) sind hauptsächlich im Blut und Knochenmark vorhanden, reichern sich aber an Entzündungsstellen an.
Unspezifische Abwehr
Eine erste Verteidigungslinie gegen Mikroorganismen wird durch eine physikalische und chemische Barriere ausgeführt, beispielsweise an der Haut, den Atemwegen und dem Verdauungstrakt. Diese Barriere wird durch unspezifische Schutzmechanismen unterstützt, darunter Fresszellen wie Makrophagen und polymorphkernige Leukozyten, die Krankheitserreger abtöten können, und natürliche Killerzellen, die Tumorzellen und virusinfizierte Zellen lysieren können. Das Komplementsystem und bestimmte mikrobielle Inhibitoren (z. B. Lysozym) sind ebenfalls an der unspezifischen Reaktion beteiligt.
Spezifische Immunität
Nach dem ersten Kontakt des Wirts mit dem Erreger werden spezifische Immunantworten induziert. Kennzeichen dieser zweiten Verteidigungslinie ist die spezifische Erkennung von Determinanten, sogenannten Antigenen oder Epitopen, der Erreger durch Rezeptoren auf der Zelloberfläche von B- und T-Lymphozyten. Nach der Interaktion mit dem spezifischen Antigen wird die rezeptortragende Zelle stimuliert, sich einer Proliferation und Differenzierung zu unterziehen, wodurch ein Klon von Nachkommenzellen produziert wird, die für das auslösende Antigen spezifisch sind. Die spezifischen Immunantworten helfen der unspezifischen Abwehr, die den Pathogenen präsentiert wird, indem sie die Wirksamkeit der unspezifischen Reaktionen stimulieren. Ein grundlegendes Merkmal der spezifischen Immunität ist, dass sich das Gedächtnis entwickelt. Sekundärer Kontakt mit demselben Antigen provoziert eine schnellere und kräftigere, aber gut regulierte Reaktion.
Das Genom ist nicht in der Lage, die Codes einer Reihe von Antigenrezeptoren zu tragen, die ausreichen, um die Anzahl der Antigene zu erkennen, auf die man stoßen kann. Das Repertoire an Spezifität entwickelt sich durch einen Prozess von Genumordnungen. Dies ist ein zufälliger Prozess, bei dem verschiedene Besonderheiten zustande kommen. Dies schließt Besonderheiten für Eigenkomponenten ein, die unerwünscht sind. Ein Selektionsprozess, der in der Thymusdrüse (T-Zellen) oder im Knochenmark (B-Zellen) stattfindet, dient dazu, diese unerwünschten Spezifitäten zu beseitigen.
Die normale Immuneffektorfunktion und die homöostatische Regulation der Immunantwort hängen von einer Vielzahl löslicher Produkte ab, die zusammenfassend als Cytokine bekannt sind und von Lymphozyten und anderen Zelltypen synthetisiert und ausgeschieden werden. Zytokine haben pleiotrope Wirkungen auf Immun- und Entzündungsreaktionen. Die Zusammenarbeit zwischen verschiedenen Zellpopulationen ist für die Immunantwort erforderlich – die Regulierung von Antikörperantworten, die Akkumulation von Immunzellen und -molekülen an Entzündungsstellen, die Initiierung von Akute-Phase-Antworten, die Kontrolle der zytotoxischen Funktion von Makrophagen und viele andere Prozesse, die für die Wirtsresistenz zentral sind . Diese werden durch einzeln oder gemeinsam wirkende Zytokine beeinflusst und sind in vielen Fällen davon abhängig.
Zwei Arme der spezifischen Immunität werden anerkannt – humorale Immunität und zellvermittelte oder zelluläre Immunität:
Humorale Immunität. Im humoralen Arm werden B-Lymphozyten nach Erkennung des Antigens durch Zelloberflächenrezeptoren stimuliert. Antigenrezeptoren auf B-Lymphozyten sind Immunglobuline (Ig). Reife B-Zellen (Plasmazellen) beginnen mit der Produktion antigenspezifischer Immunglobuline, die als Antikörper im Serum oder an Schleimhautoberflächen wirken. Es gibt fünf Hauptklassen von Immunglobulinen: (1) IgM, pentameres Ig mit optimaler Agglutinationskapazität, das zuerst nach Antigenstimulation produziert wird; (2) IgG, das hauptsächlich im Umlauf befindliche Ig, das die Plazenta passieren kann; (3) IgA, sekretorisches Ig zum Schutz von Schleimhautoberflächen; (4) IgE, Ig-Fixierung an Mastzellen oder basophilen Granulozyten, die an unmittelbaren Überempfindlichkeitsreaktionen beteiligt sind, und (5) IgD, dessen Hauptfunktion als Rezeptor auf B-Lymphozyten besteht.
Zellvermittelte Immunität. Der zelluläre Arm des spezifischen Immunsystems wird durch T-Lymphozyten vermittelt. Diese Zellen haben auch Antigenrezeptoren auf ihren Membranen. Sie erkennen ein Antigen, wenn es von antigenpräsentierenden Zellen im Zusammenhang mit Histokompatibilitätsantigenen präsentiert wird. Daher haben diese Zellen zusätzlich zur Antigenspezifität eine Restriktion. T-Zellen fungieren als Helferzellen für verschiedene (einschließlich humorale) Immunantworten, vermitteln die Rekrutierung von Entzündungszellen und können als zytotoxische T-Zellen Zielzellen nach Antigen-spezifischer Erkennung töten.
Mechanismen der Immuntoxizität
Immunsuppression
Eine wirksame Wirtsresistenz hängt von der funktionellen Integrität des Immunsystems ab, was wiederum erfordert, dass die Komponentenzellen und Moleküle, die die Immunantwort orchestrieren, in ausreichender Zahl und in funktionsfähiger Form verfügbar sind. Angeborene Immundefekte beim Menschen sind häufig durch Defekte in bestimmten Stammzelllinien gekennzeichnet, die zu einer beeinträchtigten oder fehlenden Produktion von Immunzellen führen. In Analogie zu angeborenen und erworbenen Immunschwächekrankheiten des Menschen kann eine chemikalieninduzierte Immunsuppression einfach aus einer reduzierten Anzahl funktionsfähiger Zellen resultieren (IPCS 1996). Das Fehlen oder die verringerte Anzahl von Lymphozyten kann mehr oder weniger tiefgreifende Auswirkungen auf den Immunstatus haben. Einige Immunschwächezustände und schwere Immunsuppression, wie sie bei einer Transplantation oder zytostatischen Therapie auftreten können, wurden insbesondere mit einem erhöhten Auftreten opportunistischer Infektionen und bestimmter neoplastischer Erkrankungen in Verbindung gebracht. Die Infektionen können bakteriell, viral, durch Pilze oder Protozoen sein, und die vorherrschende Art der Infektion hängt von der damit verbundenen Immunschwäche ab. Es ist zu erwarten, dass die Exposition gegenüber immunsuppressiven Umweltchemikalien zu subtileren Formen der Immunsuppression führt, die möglicherweise schwer zu erkennen sind. Diese können beispielsweise zu einem erhöhten Auftreten von Infektionen wie Influenza oder Erkältung führen.
Angesichts der Komplexität des Immunsystems mit der großen Vielfalt an Zellen, Mediatoren und Funktionen, die ein kompliziertes und interaktives Netzwerk bilden, haben immuntoxische Verbindungen zahlreiche Möglichkeiten, ihre Wirkung zu entfalten. Obwohl die Natur der durch viele immuntoxische Chemikalien induzierten anfänglichen Läsionen noch nicht aufgeklärt wurde, gibt es zunehmend Informationen, hauptsächlich aus Studien an Labortieren, bezüglich der immunbiologischen Veränderungen, die zu einer Unterdrückung der Immunfunktion führen (Dean et al. 1994). . Toxische Wirkungen können bei den folgenden kritischen Funktionen auftreten (und einige Beispiele für immunotoxische Verbindungen, die diese Funktionen beeinträchtigen):
- Entwicklung und Ausbreitung verschiedener Stammzellpopulationen (Benzol übt immuntoxische Wirkungen auf Stammzellebene aus und verursacht Lymphozytopenie)
- Proliferation verschiedener lymphatischer und myeloischer Zellen sowie Stützgewebe, in denen diese Zellen reifen und funktionieren (immuntoxische Organozinnverbindungen unterdrücken die proliferative Aktivität von Lymphozyten in der Thymusrinde durch direkte Zytotoxizität; die thymotoxische Wirkung von 2,3,7,8-Tetrachlor -Dibenzo-p-dioxin (TCDD) und verwandte Verbindungen ist wahrscheinlich eher auf eine beeinträchtigte Funktion der Thymusepithelzellen als auf eine direkte Toxizität für Thymozyten zurückzuführen)
- Antigenaufnahme, Verarbeitung und Präsentation durch Makrophagen und andere antigenpräsentierende Zellen (eines der Ziele von 7,12-Dimethylbenz(a)anthracen (DMBA) und von Blei ist die Antigenpräsentation durch Makrophagen; ein Ziel der ultravioletten Strahlung ist das Antigen- präsentiert Langerhans-Zelle)
- regulatorische Funktion von T-Helfer- und T-Suppressorzellen (die Funktion der T-Helferzellen wird durch Organozine, Aldicarb, polychlorierte Biphenyle (PCBs), TCDD und DMBA beeinträchtigt; die Funktion der T-Suppressorzellen wird durch eine niedrig dosierte Behandlung mit Cyclophosphamid reduziert)
- Produktion verschiedener Zytokine oder Interleukine (Benzo(a)pyren (BP) unterdrückt die Interleukin-1-Produktion; ultraviolette Strahlung verändert die Produktion von Zytokinen durch Keratinozyten)
- Die Synthese verschiedener Klassen von Immunglobulinen IgM und IgG wird nach einer Behandlung mit PCB und Tributylzinnoxid (TBT) unterdrückt und nach einer Exposition gegenüber Hexachlorbenzol (HCB) erhöht).
- Komplementregulation und -aktivierung (beeinflusst von TCDD)
- zytotoxische T-Zell-Funktion (3-Methylcholanthren (3-MC), DMBA und TCDD unterdrücken die zytotoxische T-Zell-Aktivität)
- Funktion natürlicher Killerzellen (NK) (die NK-Aktivität der Lunge wird durch Ozon unterdrückt; die NK-Aktivität der Milz wird durch Nickel beeinträchtigt)
- Chemotaxis und zytotoxische Funktionen von Makrophagen und polymorphkernigen Leukozyten (Ozon und Stickstoffdioxid beeinträchtigen die phagozytische Aktivität von Alveolarmakrophagen).
Allergie
Allergie können als nachteilige Auswirkungen auf die Gesundheit definiert werden, die aus der Induktion und Auslösung spezifischer Immunantworten resultieren. Bei Überempfindlichkeitsreaktionen ohne Beteiligung des Immunsystems kommt der Begriff vor Pseudoallergie wird genutzt. Im Kontext der Immuntoxikologie resultieren Allergien aus einer spezifischen Immunantwort auf interessierende Chemikalien und Medikamente. Die Fähigkeit einer Chemikalie, Personen zu sensibilisieren, hängt im Allgemeinen mit ihrer Fähigkeit zusammen, sich kovalent an Körperproteine zu binden. Allergische Reaktionen können verschiedene Formen annehmen und diese unterscheiden sich sowohl hinsichtlich der zugrunde liegenden immunologischen Mechanismen als auch der Geschwindigkeit der Reaktion. Vier Haupttypen von allergischen Reaktionen wurden erkannt: Überempfindlichkeitsreaktionen vom Typ I, die durch IgE-Antikörper bewirkt werden und bei denen sich die Symptome innerhalb von Minuten nach der Exposition der sensibilisierten Person manifestieren. Überempfindlichkeitsreaktionen vom Typ II resultieren aus der Schädigung oder Zerstörung von Wirtszellen durch Antikörper. In diesem Fall treten die Symptome innerhalb von Stunden auf. Typ-III-Überempfindlichkeits- oder Arthus-Reaktionen sind ebenfalls Antikörper-vermittelt, jedoch gegen lösliches Antigen, und resultieren aus der lokalen oder systemischen Wirkung von Immunkomplexen. Typ-IV- oder Überempfindlichkeitsreaktionen vom verzögerten Typ werden durch T-Lymphozyten bewirkt und normalerweise entwickeln sich die Symptome 24 bis 48 Stunden nach der Exposition der sensibilisierten Person.
Die beiden arbeitsmedizinisch relevantesten Arten von Chemikalienallergien sind die Kontakt- oder Hautallergie und die Atemwegsallergie.
Kontaktüberempfindlichkeit. Eine Vielzahl von Chemikalien kann Hautsensibilisierungen hervorrufen. Nach topischer Exposition eines empfindlichen Individuums gegenüber einem chemischen Allergen wird eine T-Lymphozyten-Reaktion in den drainierenden Lymphknoten induziert. In der Haut interagiert das Allergen direkt oder indirekt mit epidermalen Langerhans-Zellen, die die Chemikalie zu den Lymphknoten transportieren und sie in einer immunogenen Form an reagierende T-Lymphozyten präsentieren. Allergen-aktivierte T-Lymphozyten proliferieren, was zu einer klonalen Expansion führt. Die Person ist nun sensibilisiert und reagiert auf eine zweite dermale Exposition gegenüber derselben Chemikalie mit einer aggressiveren Immunantwort, was zu einer allergischen Kontaktdermatitis führt. Die kutane Entzündungsreaktion, die allergische Kontaktdermatitis charakterisiert, ist sekundär zur Erkennung des Allergens in der Haut durch spezifische T-Lymphozyten. Diese Lymphozyten werden aktiviert, setzen Zytokine frei und verursachen die lokale Akkumulation anderer mononukleärer Leukozyten. Die Symptome entwickeln sich etwa 24 bis 48 Stunden nach der Exposition der sensibilisierten Person, und die allergische Kontaktdermatitis stellt daher eine Form der Überempfindlichkeit vom verzögerten Typ dar. Häufige Ursachen für allergische Kontaktdermatitis sind organische Chemikalien (wie 2,4-Dinitrochlorbenzol), Metalle (wie Nickel und Chrom) und Pflanzenprodukte (wie Urushiol aus Poison Ivy).
Überempfindlichkeit der Atemwege. Eine Überempfindlichkeit der Atemwege wird normalerweise als Überempfindlichkeitsreaktion vom Typ I angesehen. Spätphasenreaktionen und die chronischeren Symptome, die mit Asthma verbunden sind, können jedoch zellvermittelte (Typ IV) Immunprozesse umfassen. Die mit einer Atemwegsallergie verbundenen akuten Symptome werden durch IgE-Antikörper bewirkt, deren Produktion ausgelöst wird, nachdem das empfindliche Individuum dem induzierenden chemischen Allergen ausgesetzt wurde. Der IgE-Antikörper verteilt sich systemisch und bindet über Membranrezeptoren an Mastzellen, die in vaskularisierten Geweben einschließlich der Atemwege gefunden werden. Nach Einatmen derselben Chemikalie wird eine Überempfindlichkeitsreaktion der Atemwege ausgelöst. Allergen verbindet sich mit Protein und bindet an und vernetzt IgE-Antikörper, die an Mastzellen gebunden sind. Dies wiederum bewirkt die Degranulation von Mastzellen und die Freisetzung von Entzündungsmediatoren wie Histamin und Leukotrienen. Solche Mediatoren verursachen eine Bronchokonstriktion und Vasodilatation, was zu den Symptomen einer Atemwegsallergie führt; Asthma und/oder Rhinitis. Zu den Chemikalien, von denen bekannt ist, dass sie beim Menschen eine Überempfindlichkeit der Atemwege verursachen, gehören Säureanhydride (wie Trimellitsäureanhydrid), einige Diisocyanate (wie Toluoldiisocyanat), Platinsalze und einige Reaktivfarbstoffe. Es ist auch bekannt, dass eine chronische Exposition gegenüber Beryllium eine Überempfindlichkeits-Lungenerkrankung verursacht.
Autoimmunität
Autoimmunität kann definiert werden als die Stimulierung spezifischer Immunantworten, die gegen endogene „Selbst“-Antigene gerichtet sind. Eine induzierte Autoimmunität kann entweder aus Veränderungen im Gleichgewicht regulatorischer T-Lymphozyten oder aus der Assoziation eines Xenobiotikums mit normalen Gewebekomponenten resultieren, um diese immunogen zu machen („verändertes Selbst“). Medikamente und Chemikalien, von denen bekannt ist, dass sie bei anfälligen Personen zufällig Wirkungen wie die einer Autoimmunerkrankung (AD) hervorrufen oder verschlimmern, sind Verbindungen mit niedrigem Molekulargewicht (Molekulargewicht 100 bis 500), die im Allgemeinen selbst als nicht immunogen angesehen werden. Der Mechanismus der AD durch chemische Exposition ist weitgehend unbekannt. Eine Krankheit kann direkt durch zirkulierende Antikörper, indirekt durch die Bildung von Immunkomplexen oder als Folge einer zellvermittelten Immunität erzeugt werden, tritt aber wahrscheinlich durch eine Kombination von Mechanismen auf. Die Pathogenese ist am besten bei medikamenteninduzierten immunhämolytischen Erkrankungen bekannt:
- Das Medikament kann sich an die Membran der roten Blutkörperchen anheften und mit einem medikamentenspezifischen Antikörper interagieren.
- Das Medikament kann die Membran der roten Blutkörperchen verändern, sodass das Immunsystem die Zelle als fremd betrachtet.
- Das Medikament und sein spezifischer Antikörper bilden Immunkomplexe, die an der Membran der roten Blutkörperchen haften und Verletzungen hervorrufen.
- Eine Erythrozytensensibilisierung tritt aufgrund der Produktion von Erythrozyten-Autoantikörpern auf.
Es wurde festgestellt, dass eine Vielzahl von Chemikalien und Arzneimitteln, insbesondere letztere, autoimmunähnliche Reaktionen hervorrufen (Kamüller, Bloksma und Seinen 1989). Berufliche Exposition gegenüber Chemikalien kann nebenbei zu AD-ähnlichen Syndromen führen. Die Exposition gegenüber monomerem Vinylchlorid, Trichlorethylen, Perchlorethylen, Epoxidharzen und Quarzstaub kann Sklerodermie-ähnliche Syndrome hervorrufen. Nach Exposition gegenüber Hydrazin wurde ein dem systemischen Lupus erythematodes (SLE) ähnliches Syndrom beschrieben. Die Exposition gegenüber Toluoldiisocyanat wurde mit der Induktion von thrombozytopenischer Purpura in Verbindung gebracht. Schwermetalle wie Quecksilber wurden mit einigen Fällen von Immunkomplex-Glomerulonephritis in Verbindung gebracht.
Bewertung des menschlichen Risikos
Die Beurteilung des menschlichen Immunstatus wird hauptsächlich unter Verwendung von peripherem Blut zur Analyse humoraler Substanzen wie Immunglobuline und Komplement und von Blutleukozyten zur Untergruppenzusammensetzung und Funktionalität von Subpopulationen durchgeführt. Diese Methoden sind in der Regel dieselben, die zur Untersuchung der humoralen und zellvermittelten Immunität sowie der unspezifischen Resistenz von Patienten mit Verdacht auf angeborene Immunschwächekrankheit verwendet werden. Für epidemiologische Studien (z. B. von beruflich exponierten Bevölkerungsgruppen) sollten Parameter auf der Grundlage ihres Vorhersagewerts in menschlichen Populationen, validierten Tiermodellen und der zugrunde liegenden Biologie der Marker ausgewählt werden (siehe Tabelle 1). Die Strategie beim Screening auf immuntoxische Wirkungen nach (unbeabsichtigter) Exposition gegenüber Umweltschadstoffen oder anderen Giftstoffen hängt stark von den Umständen ab, wie z. B. Art der zu erwartenden Immunschwäche, Zeit zwischen Exposition und Beurteilung des Immunstatus, Ausmaß der Exposition und Anzahl der exponierten Personen. Der Prozess der Bewertung des immuntoxischen Risikos eines bestimmten Xenobiotikums beim Menschen ist äußerst schwierig und oft unmöglich, hauptsächlich aufgrund des Vorhandenseins verschiedener Störfaktoren endogenen oder exogenen Ursprungs, die die Reaktion von Individuen auf toxische Schäden beeinflussen. Dies gilt insbesondere für Studien, die die Rolle der Chemikalienbelastung bei Autoimmunerkrankungen untersuchen, bei denen genetische Faktoren eine entscheidende Rolle spielen.
Tabelle 1. Klassifizierung von Tests für Immunmarker
| Testkategorie | Eigenschaften | Spezifische Tests |
| Basic-allgemein Sollte in allgemeinen Panels enthalten sein |
Indikatoren für den allgemeinen Gesundheitszustand und den Status des Organsystems | Blutharnstoffstickstoff, Blutzucker usw. |
| Basic-immun Sollte in allgemeinen Panels enthalten sein |
Allgemeine Indikatoren des Immunstatus Relativ niedrige Kosten Assay-Methoden sind unter den Labors standardisiert Ergebnisse außerhalb der Referenzbereiche sind klinisch interpretierbar |
Vollständiges Blutbild Serum-IgG-, IgA-, IgM-Spiegel Oberflächenmarker-Phänotypen für große Lymphozyten-Untergruppen |
| Fokussiert/Reflex Sollte eingeschlossen werden, wenn dies durch klinische Befunde, vermutete Expositionen oder frühere Testergebnisse angezeigt wird |
Indikatoren spezifischer Immunfunktionen/-ereignisse Die Kosten variieren Assay-Methoden sind unter den Labors standardisiert Ergebnisse außerhalb der Referenzbereiche sind klinisch interpretierbar |
Histokompatibilitäts-Genotyp Antikörper gegen Infektionserreger Gesamtserum-IgE Allergenspezifisches IgE Autoantikörper Hauttests auf Überempfindlichkeit Oxidativer Ausbruch von Granulozyten Histopathologie (Gewebebiopsie) |
| Forschung Sollte nur bei Kontrollpopulationen und sorgfältigem Studiendesign eingeschlossen werden |
Indikatoren allgemeiner oder spezifischer Immunfunktionen/-ereignisse Die Kosten variieren; oft teuer Assay-Methoden sind in der Regel nicht unter den Labors standardisiert Ergebnisse außerhalb der Referenzbereiche sind oft klinisch nicht interpretierbar |
In-vitro-Stimulationsassays Oberflächenmarker für die Zellaktivierung Zytokin-Serumkonzentrationen Klonalitätsassays (Antikörper, zellulär, genetisch) Zytotoxizitätstests |
Da nur selten adäquate Humandaten verfügbar sind, basiert die Bewertung des Risikos einer chemisch induzierten Immunsuppression beim Menschen in den meisten Fällen auf Tierversuchen. Die Identifizierung potenziell immuntoxischer Xenobiotika erfolgt hauptsächlich in kontrollierten Studien an Nagern. In-vivo-Expositionsstudien stellen in dieser Hinsicht den optimalen Ansatz dar, um das immuntoxische Potenzial einer Verbindung abzuschätzen. Dies liegt an der multifaktoriellen und komplexen Natur des Immunsystems und der Immunantworten. In-vitro-Studien sind von zunehmendem Wert bei der Aufklärung von Mechanismen der Immuntoxizität. Darüber hinaus können durch die Untersuchung der Wirkung des Wirkstoffs anhand von Zellen tierischen und menschlichen Ursprungs Daten für den Artenvergleich generiert werden, die im „Parallelogramm“-Ansatz zur Verbesserung des Risikobewertungsprozesses verwendet werden können. Wenn Daten für drei Eckpfeiler des Parallelogramms (In-vivo-Tier und In-vitro-Tier und -Mensch) verfügbar sind, kann es einfacher sein, das Ergebnis für den verbleibenden Eckpfeiler, d. h. das Risiko beim Menschen, vorherzusagen.
Wenn sich die Risikobewertung einer chemikalieninduzierten Immunsuppression ausschließlich auf Daten aus Tierversuchen stützen muss, kann bei der Extrapolation auf den Menschen ein Ansatz verfolgt werden, indem Unsicherheitsfaktoren auf das No-Observed-Adverse-Effect-Level (NOAEL) angewendet werden. Dieses Niveau kann auf Parametern basieren, die in relevanten Modellen bestimmt wurden, wie z. B. Wirtsresistenzassays und In-vivo-Beurteilung von Überempfindlichkeitsreaktionen und Antikörperproduktion. Idealerweise muss die Relevanz dieses Ansatzes für die Risikobewertung durch Studien am Menschen bestätigt werden. Solche Studien sollten die Identifizierung und Messung des Giftstoffs, epidemiologische Daten und Bewertungen des Immunstatus kombinieren.
Zur Vorhersage von Kontaktallergien stehen Meerschweinchenmodelle zur Verfügung, die seit den 1970er Jahren in der Risikobewertung eingesetzt werden. Obwohl diese Tests empfindlich und reproduzierbar sind, haben sie Einschränkungen, da sie von einer subjektiven Bewertung abhängen; Dies kann durch neuere und quantitativere Methoden überwunden werden, die in der Maus entwickelt wurden. In Bezug auf die durch Inhalation oder Einnahme von Allergenen induzierte chemikalieninduzierte Überempfindlichkeit sollten Tests entwickelt und im Hinblick auf ihren Vorhersagewert beim Menschen bewertet werden. Wenn es darum geht, sichere Arbeitsplatzkonzentrationen potenzieller Allergene festzulegen, muss die zweiphasige Natur der Allergie berücksichtigt werden: die Sensibilisierungsphase und die Auslösephase. Die Konzentration, die erforderlich ist, um eine allergische Reaktion bei einer zuvor sensibilisierten Person hervorzurufen, ist erheblich niedriger als die Konzentration, die erforderlich ist, um eine Sensibilisierung bei einer immunologisch naiven, aber anfälligen Person auszulösen.
Da es praktisch an Tiermodellen zur Vorhersage einer durch Chemikalien induzierten Autoimmunität mangelt, sollte der Entwicklung solcher Modelle besondere Aufmerksamkeit geschenkt werden. Für die Entwicklung solcher Modelle sollte unser Wissen über chemisch induzierte Autoimmunität beim Menschen erweitert werden, einschließlich der Untersuchung von genetischen Markern und Markern des Immunsystems, um anfällige Personen zu identifizieren. Menschen, die Medikamenten ausgesetzt sind, die Autoimmunität induzieren, bieten eine solche Gelegenheit.
Optionen im Studiendesign
Der Epidemiologe interessiert sich für Beziehungen zwischen Variablen, hauptsächlich Expositions- und Ergebnisvariablen. Typischerweise möchten Epidemiologen feststellen, ob das Auftreten einer Krankheit mit dem Vorhandensein eines bestimmten Erregers (Exposition) in der Bevölkerung zusammenhängt. Die Art und Weise, wie diese Beziehungen untersucht werden, kann sehr unterschiedlich sein. Man kann alle Personen identifizieren, die diesem Agens ausgesetzt sind, und sie nachverfolgen, um das Auftreten der Krankheit zu messen, indem man dieses Auftreten mit dem Auftreten der Krankheit in einer geeigneten, nicht exponierten Population vergleicht. Alternativ kann man einfach unter den Belichteten und Unbelichteten Proben nehmen, ohne eine vollständige Aufzählung von ihnen zu haben. Oder man kann als dritte Alternative alle Personen identifizieren, die in einem definierten Zeitraum eine interessierende Krankheit entwickeln („Fälle“) und eine geeignete Gruppe von krankheitsfreien Personen (eine Stichprobe der Quellpopulation von Fällen) und ermitteln ob sich die Expositionsmuster zwischen den beiden Gruppen unterscheiden. Eine Möglichkeit ist die Nachbeobachtung der Studienteilnehmer (in sogenannten Längsschnittstudien): In dieser Situation besteht eine zeitliche Verzögerung zwischen dem Auftreten der Exposition und dem Ausbruch der Erkrankung. Eine alternative Möglichkeit ist ein Bevölkerungsquerschnitt, bei dem sowohl die Exposition als auch die Erkrankung zum gleichen Zeitpunkt gemessen werden.
In diesem Artikel wird auf die gängigen Studiendesigns – Kohorte, Fall-Referent (Fall-Kontrolle) und Querschnitt – eingegangen. Betrachten Sie als Grundlage für diese Diskussion eine große Viskosefabrik in einer kleinen Stadt. Eine Untersuchung, ob eine Schwefelkohlenstoffbelastung das Risiko für Herz-Kreislauf-Erkrankungen erhöht, wird eingeleitet. Die Untersuchung hat mehrere Gestaltungsmöglichkeiten, einige mehr und andere weniger offensichtlich. Eine erste Strategie besteht darin, alle Arbeiter zu identifizieren, die Schwefelkohlenstoff ausgesetzt waren, und sie auf kardiovaskuläre Mortalität zu verfolgen.
Kohortenstudien
Eine Kohortenstudie umfasst Forschungsteilnehmer, die ein gemeinsames Ereignis teilen, die Exposition. Eine klassische Kohortenstudie identifiziert eine definierte Gruppe von exponierten Personen, und dann werden alle weiterverfolgt und ihre Morbiditäts- und/oder Mortalitätserfahrungen registriert. Neben einer gemeinsamen qualitativen Exposition sollte die Kohorte auch auf andere Weise definiert werden AuswahlkriterienB. Altersgruppe, Geschlecht (männlich oder weiblich oder beides), Mindestdauer und -intensität der Exposition, Freiheit von anderen Expositionen und dergleichen, um die Aussagekraft und Effizienz der Studie zu verbessern. Bei der Aufnahme sollten alle Kohortenmitglieder frei von der zu untersuchenden Krankheit sein, gemäß dem empirischen Kriterienkatalog, der zur Messung der Krankheit verwendet wird.
Wird beispielsweise in der Kohortenstudie zu den Auswirkungen von Schwefelkohlenstoff auf die koronare Morbidität eine koronare Herzkrankheit empirisch als klinischer Infarkt gemessen, müssen diejenigen, die zu Studienbeginn einen Koronarinfarkt in der Vorgeschichte hatten, aus der Kohorte ausgeschlossen werden. Im Gegensatz dazu können elektrokardiographische Anomalien ohne Infarktanamnese akzeptiert werden. Wenn jedoch das Auftreten neuer elektrokardiographischer Veränderungen das empirische Ergebnismaß ist, sollten die Kohortenmitglieder auch normale Elektrokardiogramme zu Studienbeginn haben.
Die Morbidität (in Bezug auf die Inzidenz) oder die Mortalität einer exponierten Kohorte sollte mit einer Referenzkohorte verglichen werden, die der exponierten Kohorte idealerweise in allen relevanten Aspekten, mit Ausnahme der Exposition, so ähnlich wie möglich sein sollte, um das relative Risiko zu bestimmen Krankheit oder Tod durch Exposition. Die Verwendung einer ähnlichen, aber nicht exponierten Kohorte als Anbieter der Referenzerfahrung ist der üblichen (Fehl-)Praxis vorzuziehen, die Morbidität oder Mortalität der exponierten Kohorte mit altersstandardisierten nationalen Zahlen zu vergleichen, da die allgemeine Bevölkerung selbst die meisten nicht erfüllt elementare Anforderungen an die Vergleichsvalidität. Das standardisierte Morbiditäts- (oder Mortalitäts-)Verhältnis (SMR), das sich aus einem solchen Vergleich ergibt, führt normalerweise zu einer Unterschätzung des wahren Risikoverhältnisses, da in der exponierten Kohorte eine Verzerrung auftritt, was zu einer mangelnden Vergleichbarkeit zwischen den beiden Populationen führt. Diese Vergleichsverzerrung wird als „Healthy Worker Effect“ bezeichnet. Es handelt sich jedoch nicht wirklich um einen echten „Effekt“, sondern um eine Verzerrung durch negatives Confounding, das wiederum durch gesundheitsselektive Fluktuation in einer erwerbstätigen Bevölkerung entstanden ist. (Menschen mit schlechter Gesundheit neigen dazu, „exponierte“ Kohorten zu verlassen oder nie in sie einzutreten, da ihr Endziel oft der arbeitslose Teil der Allgemeinbevölkerung ist.)
Denn eine „exponierte“ Kohorte ist nur definiert als eine bestimmte Exposition Wirkungen, die durch diese einzelne Exposition verursacht wurden (oder Mischung von Expositionen) können gleichzeitig studiert werden. Andererseits erlaubt das Kohortendesign die Untersuchung von mehrere Krankheiten gleichzeitig. Man kann auch gleichzeitig verschiedene Manifestationen derselben Krankheit untersuchen – zum Beispiel Angina pectoris, EKG-Veränderungen, klinische Myokardinfarkte und koronare Mortalität. Eine Kohortenstudie ist zwar gut geeignet, um spezifische Hypothesen zu testen (z. B. „Einwirkung von Schwefelkohlenstoff verursacht koronare Herzkrankheit“), liefert aber auch Antworten auf die allgemeinere Frage: „Welche Krankheiten werden durch diese Einwirkung verursacht?“
Beispielsweise werden in einer Kohortenstudie, die das Risiko von Gießereiarbeitern untersucht, an Lungenkrebs zu sterben, die Mortalitätsdaten aus dem nationalen Todesursachenregister bezogen. Obwohl die Studie klären sollte, ob Gießereistaub Lungenkrebs verursacht, gibt die Datenquelle bei gleichem Aufwand auch Auskunft über alle anderen Todesursachen. Daher können gleichzeitig andere mögliche Gesundheitsrisiken untersucht werden.
Der Zeitpunkt einer Kohortenstudie kann entweder retrospektiv (historisch) oder prospektiv (gleichzeitig) sein. In beiden Fällen ist die Designstruktur dieselbe. Eine vollständige Zählung der exponierten Personen erfolgt zu einem bestimmten Zeitpunkt oder Zeitraum, und das Ergebnis wird für alle Personen bis zu einem definierten Endpunkt gemessen. Der Unterschied zwischen prospektiv und retrospektiv liegt im Zeitpunkt der Studie. Wenn rückwirkend, ist der Endpunkt bereits eingetreten; wenn Interessent, muss man darauf warten.
Beim retrospektiven Design wird die Kohorte zu einem bestimmten Zeitpunkt in der Vergangenheit definiert (z. B. diejenigen, die am 1. Januar 1961 exponiert waren oder zwischen 1961 und 1970 eine exponierte Arbeit übernommen haben). Die Morbidität und/oder Mortalität von alle Kohortenmitglieder wird dann bis in die Gegenwart verfolgt. Obwohl „alle“ bedeutet, dass auch die Ausgeschiedenen erfasst werden müssen, ist eine 100-prozentige Erfassung in der Praxis selten zu erreichen. Je vollständiger jedoch das Follow-up ist, desto aussagekräftiger ist die Studie.
Beim prospektiven Design wird die Kohorte zum gegenwärtigen Zeitpunkt oder während eines zukünftigen Zeitraums definiert, und die Morbidität wird dann in die Zukunft verfolgt.
Bei der Durchführung von Kohortenstudien muss genügend Zeit für die Nachverfolgung eingeplant werden, damit die Endpunkte der Bedenken genügend Zeit haben, sich zu manifestieren. Da historische Aufzeichnungen möglicherweise nur für einen kurzen Zeitraum in der Vergangenheit verfügbar sind, ist es manchmal dennoch wünschenswert, diese Datenquelle zu nutzen, da dies bedeutet, dass ein kürzerer Zeitraum der prospektiven Nachverfolgung erforderlich wäre, bevor Ergebnisse aus der Studie vorliegen könnten erhältlich. In diesen Situationen kann eine Kombination aus retrospektivem und prospektivem Kohortenstudiendesign effizient sein. Das allgemeine Layout von Häufigkeitstabellen mit Kohortendaten ist in Tabelle 1 dargestellt.
Tabelle 1. Das allgemeine Layout von Häufigkeitstabellen mit Kohortendaten
|
Komponente der Krankheitsrate |
Exponierte Kohorte |
Nicht exponierte Kohorte |
|
Krankheits- oder Todesfälle |
c1 |
c0 |
|
Anzahl der Personen in der Kohorte |
N1 |
N0 |
Der beobachtete Anteil an Erkrankten in der exponierten Kohorte wird berechnet als:
![]()
und die der Referenzkohorte als:
![]()
Das Ratenverhältnis wird dann ausgedrückt als:

N0 und N1 werden in der Regel in Personen-Zeit-Einheiten und nicht als Anzahl der Personen ausgedrückt die Bevölkerungen. Personenjahre werden für jede Person separat berechnet. Verschiedene Personen treten oft während eines bestimmten Zeitraums in die Kohorte ein, nicht zum selben Zeitpunkt. Daher beginnen ihre Nachverfolgungszeiten zu unterschiedlichen Zeitpunkten. Ebenso sind sie nach ihrem Tod oder nach Eintreten des interessierenden Ereignisses nicht mehr „gefährdet“ und sollten nicht weiterhin Personenjahre zum Nenner beitragen.
Wenn die RR größer als 1 ist, ist die Morbidität der exponierten Kohorte höher als die der Referenzkohorte und umgekehrt. Die RR ist eine Punktschätzung, für die ein Konfidenzintervall (KI) berechnet werden sollte. Je größer die Studie, desto schmaler wird das Konfidenzintervall. Wenn RR = 1 nicht im Konfidenzintervall enthalten ist (z. B. das 95 %-KI 1.4 bis 5.8 beträgt), kann das Ergebnis auf dem gewählten Wahrscheinlichkeitsniveau (in diesem Beispiel α = 0.05) als „statistisch signifikant“ angesehen werden.
Wird die allgemeine Bevölkerung als Referenzbevölkerung verwendet, c0 wird durch die „erwartete“ Zahl ersetzt, E (c1 ), abgeleitet von den altersstandardisierten Morbiditäts- oder Mortalitätsraten dieser Population (dh der Anzahl der Fälle, die in der Kohorte aufgetreten wären, wenn die interessierende Exposition nicht stattgefunden hätte). Dies ergibt das standardisierte Mortalitäts- (oder Morbiditäts-) Verhältnis, SMR. Daher,
![]()
Auch für die SMR sollte ein Konfidenzintervall berechnet werden. Es ist besser, dieses Maß in einer Veröffentlichung anzugeben als einen p-Wert, da statistische Signifikanztests bedeutungslos sind, wenn die allgemeine Bevölkerung die Referenzkategorie ist. Ein solcher Vergleich bringt eine beträchtliche Verzerrung mit sich (die gesunder Arbeitereffekt oben erwähnt) und statistische Signifikanztests, die ursprünglich für die experimentelle Forschung entwickelt wurden, sind bei Vorliegen systematischer Fehler irreführend.
Angenommen, die Frage lautet, ob Quarzstaub Lungenkrebs verursacht. Üblicherweise tritt Quarzstaub zusammen mit anderen Karzinogenen auf – etwa Radon-Tochterprodukte und Dieselabgase in Bergwerken oder polyaromatische Kohlenwasserstoffe in Gießereien. Granitsteinbrüche setzen die Steinarbeiter diesen anderen Karzinogenen nicht aus. Daher wird das Problem am besten unter Steinarbeitern untersucht, die in Granitsteinbrüchen beschäftigt sind.
Nehmen wir dann an, dass alle 2,000 Arbeiter, die zwischen 20 und 1951 in 1960 Steinbrüchen beschäftigt waren, in die Kohorte aufgenommen werden und ihre Krebsinzidenz (alternativ nur Mortalität) ab zehn Jahren nach der ersten Exposition verfolgt wird (um eine Induktionszeit zu ermöglichen) und bis 1990. Dies ist eine 20- bis 30-jährige (je nach Eintrittsjahr) oder, sagen wir, durchschnittlich 25-jährige Nachbeobachtung der Krebsmortalität (oder -morbidität) unter 1,000 der Steinbrucharbeiter, die waren speziell Granitarbeiter. Die Expositionsgeschichte jedes Kohortenmitglieds muss aufgezeichnet werden. Diejenigen, die die Steinbrüche verlassen haben, müssen aufgespürt und ihre spätere Expositionsgeschichte aufgezeichnet werden. In Ländern, in denen alle Einwohner eindeutige Registrierungsnummern haben, ist dies ein einfaches Verfahren, das hauptsächlich durch nationale Datenschutzgesetze geregelt wird. Wo kein solches System existiert, kann es äußerst schwierig sein, Mitarbeiter zu Nachverfolgungszwecken aufzuspüren. Wo entsprechende Todes- oder Krankheitsregister existieren, kann die Sterblichkeit aus allen Ursachen, allen Krebsarten und spezifischen Krebsherden aus dem nationalen Register der Todesursachen abgerufen werden. (Für die Krebssterblichkeit ist das nationale Krebsregister eine bessere Quelle, da es genauere Diagnosen enthält. Außerdem können auch Inzidenz- (oder Morbiditäts-) Daten abgerufen werden.) Die Todesraten (oder Krebsinzidenzraten) können verglichen werden mit „ erwartete Zahlen“, berechnet aus nationalen Raten unter Zugrundelegung der Personenjahre der exponierten Kohorte.
Nehmen wir an, dass 70 tödliche Fälle von Lungenkrebs in der Kohorte gefunden werden, während die erwartete Zahl (die Zahl, die aufgetreten wäre, wenn es keine Exposition gegeben hätte) 35 ist. Dann:
c1 = 70, E (c1) = 35
![]()
Somit ist die SMR = 200, was auf eine zweifache Erhöhung des Risikos, an Lungenkrebs zu sterben, unter den Exponierten hinweist. Wenn detaillierte Expositionsdaten verfügbar sind, kann die Krebssterblichkeit in Abhängigkeit von verschiedenen Latenzzeiten (z. B. 10, 15, 20 Jahre), Arbeit in verschiedenen Arten von Steinbrüchen (verschiedene Granitsorten), verschiedenen historischen Perioden und verschiedenen Expositionen untersucht werden Intensitäten und so weiter. Allerdings lassen sich 70 Fälle nicht in zu viele Kategorien unterteilen, da die Zahl der Fälle für eine statistische Auswertung schnell zu gering wird.
Beide Arten von Kohortendesigns haben Vor- und Nachteile. Eine retrospektive Studie kann in der Regel nur die Mortalität messen, da Daten für mildere Manifestationen meist fehlen. Eine Ausnahme bilden Krebsregister und vielleicht einige andere, wie Schlaganfallregister und Krankenhausentlassungsregister, in denen auch Inzidenzdaten verfügbar sind. Die Bewertung früherer Expositionen ist immer ein Problem, und die Expositionsdaten sind in retrospektiven Studien normalerweise eher schwach. Dies kann zu einer Effektmaskierung führen. Andererseits liegen die Ergebnisse der Studie viel früher vor, da die Fälle bereits aufgetreten sind; in, sagen wir, zwei bis drei Jahren.
Eine prospektive Kohortenstudie kann besser geplant werden, um den Bedürfnissen des Forschers gerecht zu werden, und Expositionsdaten können genau und systematisch gesammelt werden. Es können mehrere unterschiedliche Manifestationen einer Krankheit gemessen werden. Sowohl Expositions- als auch Ergebnismessungen können wiederholt werden, und alle Messungen können standardisiert und ihre Gültigkeit überprüft werden. Wenn die Krankheit jedoch eine lange Latenz hat (wie Krebs), wird viel Zeit – sogar 20 bis 30 Jahre – vergehen müssen, bevor die Ergebnisse der Studie vorliegen können. In dieser Zeit kann viel passieren. Zum Beispiel Fluktuation von Forschern, Verbesserungen der Techniken zur Messung der Exposition, Umbau oder Schließung der für die Untersuchung ausgewählten Anlagen und so weiter. All diese Umstände gefährden den Studienerfolg. Auch die Kosten einer prospektiven Studie sind in der Regel höher als die einer retrospektiven Studie, dies liegt aber meist an der deutlich höheren Anzahl an Messungen (wiederholte Expositionsüberwachung, klinische Untersuchungen etc.) und nicht an der teureren Sterberegistrierung. Deshalb, die Kosten pro Informationseinheit nicht notwendigerweise über die einer retrospektiven Studie hinausgehen. Vor diesem Hintergrund eignen sich prospektive Studien eher für Erkrankungen mit eher kurzer Latenz, die ein kurzes Follow-up erfordern, während retrospektive Studien besser für Erkrankungen mit langer Latenz geeignet sind.
Fallkontrollstudien (oder fallbezogene Studien).
Kommen wir zurück zur Viskosefabrik. Eine retrospektive Kohortenstudie ist möglicherweise nicht durchführbar, wenn die Dienstpläne der exponierten Arbeiter verloren gegangen sind, während eine prospektive Kohortenstudie erst nach sehr langer Zeit solide Ergebnisse liefern würde. Eine Alternative wäre dann der Vergleich zwischen den in der Stadt im Laufe eines definierten Zeitraums an koronarer Herzkrankheit Verstorbenen und einer Stichprobe der Gesamtbevölkerung in der gleichen Altersgruppe.
Das klassische fallkontrollierte (oder fallbezogene) Design basiert auf der Stichprobenziehung aus einer dynamischen (offenen, durch einen Mitgliederwechsel gekennzeichneten) Population. Diese Bevölkerung kann die eines ganzen Landes, eines Bezirks oder einer Gemeinde sein (wie in unserem Beispiel), oder es kann die administrativ definierte Bevölkerung sein, aus der Patienten in ein Krankenhaus aufgenommen werden. Die definierte Population stellt sowohl die Fälle als auch die Kontrollen (oder Referenzen) bereit.
Die Technik besteht darin, alle Fälle der fraglichen Krankheit zu sammeln, die bei a existieren Punkt in der Zeit (häufige Fälle) oder während eines definierten Zeitraums aufgetreten sind Zeit der Zeit (Ereignisfälle). Die Fälle können somit Morbiditäts- oder Mortalitätsregistern entnommen werden oder direkt von Krankenhäusern oder anderen Quellen mit gültiger Diagnostik gesammelt werden. Die Steuerelemente werden als gezeichnet Sample aus derselben Population, entweder aus Nicht-Fällen oder aus der Gesamtpopulation. Eine andere Möglichkeit ist wählen Patienten mit einer anderen Krankheit als Kontrollen, aber dann müssen diese Patienten repräsentativ für die Bevölkerung sein, aus der die Fälle stammen. Für jeden Fall kann es eine oder mehrere Kontrollen (dh Referenten) geben. Der Stichprobenansatz unterscheidet sich von Kohortenstudien, die die gesamte Bevölkerung untersuchen. Es versteht sich von selbst, dass die Vorteile in Bezug auf die geringeren Kosten von Fall-Kontroll-Designs beträchtlich sind, aber es ist wichtig, dass die Stichprobe es ist Vertreter der gesamten Population, aus der die Fälle stammen (dh die „Studienbasis“) – andernfalls kann die Studie verzerrt sein.
Wenn Fälle und Kontrollen identifiziert wurden, werden ihre Expositionsgeschichten durch Fragebögen, Interviews oder in einigen Fällen aus bestehenden Aufzeichnungen (z. B. Gehaltslisten, aus denen Arbeitsverläufe abgeleitet werden können) gesammelt. Die Daten können entweder von den Teilnehmern selbst oder, falls sie verstorben sind, von nahen Angehörigen erhoben werden. Um einen symmetrischen Rückruf zu gewährleisten, ist es wichtig, dass der Anteil von toten und lebenden Fällen und Referenten gleich ist, da nahe Verwandte normalerweise eine weniger detaillierte Expositionsgeschichte als die Teilnehmer selbst angeben. Informationen über das Expositionsmuster bei den Fällen werden mit denen bei den Kontrollen verglichen, was eine Schätzung der Wahrscheinlichkeit (OR), ein indirektes Maß für die Risiko unter den Exponierten, an der Krankheit zu erkranken relativ zu dem der Unbelichteten.
Da das Fall-Kontroll-Design auf den Expositionsinformationen beruht, die von Patienten mit einer bestimmten Krankheit (dh Fällen) zusammen mit einer Stichprobe von nicht erkrankten Personen (dh Kontrollen) aus der Population, aus der die Fälle stammten, erhalten wurden, ist die Verbindung mit Expositionen gegeben kann nur recherchiert werden eine Krankheit. Im Gegensatz dazu ermöglicht dieses Design die gleichzeitige Untersuchung der Wirkung von mehrere unterschiedliche Belichtungen. Die fallbezogene Studie ist gut geeignet, um spezifische Forschungsfragen zu beantworten (z. B. „Wird eine koronare Herzkrankheit durch die Exposition gegenüber Schwefelkohlenstoff verursacht?“), aber sie kann auch helfen, die allgemeinere Frage zu beantworten: „Welche Expositionen können diese Krankheit verursachen? ?”
Die Frage, ob die Exposition gegenüber organischen Lösungsmitteln primären Leberkrebs verursacht, wird (als Beispiel) in Europa aufgeworfen. Fälle von primärem Leberkrebs, einer vergleichsweise seltenen Erkrankung in Europa, werden am besten aus einem nationalen Krebsregister erfasst. Angenommen, alle Krebsfälle, die während drei Jahren auftreten, bilden die Fallserie. Die Bevölkerungsbasis für die Studie ist dann ein dreijähriges Follow-up der gesamten Bevölkerung in dem betreffenden europäischen Land. Die Kontrollen werden als Stichprobe von Personen ohne Leberkrebs aus der gleichen Population gezogen. Aus Gründen der Bequemlichkeit (d. h. dass dieselbe Quelle für die Probenahme der Kontrollen verwendet werden kann) können Patienten mit einer anderen Krebsart, die nicht mit Lösungsmittelexposition in Verbindung steht, als Kontrollen verwendet werden. Dickdarmkrebs hat keinen bekannten Zusammenhang mit Lösungsmittelexposition; daher kann dieser Krebstyp zu den Kontrollen gezählt werden. (Die Verwendung von Krebskontrollen minimiert Erinnerungsverzerrungen, da die Genauigkeit der Anamnese von Fällen und Kontrollen im Durchschnitt symmetrisch ist. Wenn jedoch später ein derzeit unbekannter Zusammenhang zwischen Dickdarmkrebs und Lösungsmittelexposition aufgedeckt würde, würde diese Art der Kontrolle zu Problemen führen eine Unterschätzung des wahren Risikos – keine Übertreibung davon.)
Für jeden Fall von Leberkrebs werden zwei Kontrollen gezogen, um eine größere statistische Aussagekraft zu erreichen. (Man könnte noch mehr Kontrollen ziehen, aber verfügbare Mittel können ein limitierender Faktor sein. Wenn die Mittel nicht begrenzt wären, wären vielleicht bis zu vier Kontrollen optimal. Über vier hinaus gilt das Gesetz des abnehmenden Ertrags.) Nach Einholung einer entsprechenden Erlaubnis von Daten Schutzbehörden, die Fälle und Kontrollen oder ihre nahen Angehörigen werden kontaktiert, in der Regel mittels eines per Post zugesandten Fragebogens, in dem um eine detaillierte Berufsgeschichte mit besonderem Schwerpunkt auf einer chronologischen Liste der Namen aller Arbeitgeber, der Arbeitsabteilungen, der Arbeitsaufgaben in unterschiedlichen Beschäftigungen und die Dauer der Beschäftigung in der jeweiligen Tätigkeit. Diese Daten sind nur schwer von Verwandten zu bekommen; An bestimmte Chemikalien oder Handelsnamen erinnern sich Verwandte jedoch normalerweise nicht gut. Der Fragebogen sollte auch Fragen zu möglichen Stördaten wie Alkoholkonsum, Kontakt mit aflatoxinhaltigen Lebensmitteln und Hepatitis-B- und -C-Infektionen enthalten. Um eine ausreichend hohe Responsequote zu erreichen, werden zwei Reminder im Abstand von drei Wochen an Nicht-Responder versendet. Dies führt in der Regel zu einer endgültigen Rücklaufquote von über 70 %. Die berufliche Vorgeschichte wird dann von einem Arbeitshygieniker überprüft, ohne Kenntnis des Falls oder des Kontrollstatus des Befragten, und die Exposition wird in hohe, mittlere, niedrige, keine und unbekannte Exposition gegenüber Lösungsmitteln eingeteilt. Die zehnjährige Exposition unmittelbar vor der Krebsdiagnose werden nicht berücksichtigt, da es biologisch nicht plausibel ist, dass Karzinogene vom Initiatortyp bei einer so kurzen Latenzzeit die Ursache des Krebses sein können (obwohl Promotoren dies tatsächlich könnten). In diesem Stadium ist es auch möglich, zwischen verschiedenen Arten der Lösungsmittelbelastung zu unterscheiden. Da eine vollständige Erwerbshistorie vorgelegt wurde, ist es auch möglich, andere Expositionen zu untersuchen, obwohl diese in der ursprünglichen Studienhypothese nicht enthalten waren. Odds Ratios können dann für die Exposition gegenüber einem beliebigen Lösungsmittel, bestimmten Lösungsmitteln, Lösungsmittelgemischen, verschiedenen Kategorien der Expositionsintensität und für verschiedene Zeitfenster in Bezug auf die Krebsdiagnose berechnet werden. Es ist ratsam, Personen mit unbekannter Exposition von der Analyse auszuschließen.
Die Fälle und Kontrollen können als Proben entnommen und analysiert werden eigenständige Serie or passende Gruppen. Matching bedeutet, dass Kontrollen für jeden Fall basierend auf bestimmten Merkmalen oder Attributen ausgewählt werden, um Paare (oder Sätze, wenn mehr als eine Kontrolle für jeden Fall ausgewählt wird) zu bilden. Der Abgleich erfolgt normalerweise auf der Grundlage eines oder mehrerer solcher Faktoren, wie Alter, Vitalzustand, Rauchergeschichte, Kalenderzeit der Falldiagnose und dergleichen. In unserem Beispiel werden Fälle und Kontrollen dann nach Alter und Vitalstatus abgeglichen. (Vitalstatus ist wichtig, da Patienten selbst in der Regel eine genauere Expositionsgeschichte angeben als nahe Verwandte, und Symmetrie aus Validitätsgründen unerlässlich ist.) Heute wird empfohlen, beim Matching restriktiv vorzugehen, da dieses Verfahren negative (Effektmaskierung) einführen kann ) verwirrend.
Wenn ein Steuerelement einem Fall zugeordnet ist, wird das Design a genannt Matched-Pair-Design. Vorausgesetzt, die Kosten für die Untersuchung weiterer Kontrollen sind nicht unerschwinglich, verbessert mehr als ein Referent pro Fall die Stabilität der Schätzung des OR, wodurch die Studie größeneffizienter wird.
Die Aufteilung der Ergebnisse einer ungepaarten Fall-Kontroll-Studie ist in Tabelle 2 dargestellt.
Tabelle 2. Musterlayout von Fallkontrolldaten
|
Expositionsklassifizierung |
||
|
Ausgesetzt |
Unbelichtet |
|
|
Projekte |
c1 |
c0 |
|
Nicht-Fälle |
n1 |
n0 |
Aus dieser Tabelle können die Expositionswahrscheinlichkeiten unter den Fällen und die Expositionswahrscheinlichkeiten unter der Population (den Kontrollen) berechnet und geteilt werden, um das Expositionswahrscheinlichkeitsverhältnis OR zu erhalten. Für die Fälle ist die Expositionswahrscheinlichkeit c1 / c0, und für die Kontrollen ist es n1 / n0. Die Abschätzung des OR ist dann:
![]()
Wenn relativ mehr Fälle als Kontrollen exponiert wurden, liegt das OR über 1 und umgekehrt. Konfidenzintervalle müssen für das OR auf die gleiche Weise wie für das RR berechnet und bereitgestellt werden.
Als weiteres Beispiel dient ein arbeitsmedizinisches Zentrum eines großen Unternehmens für 8,000 Mitarbeiter, die einer Vielzahl von Stäuben und anderen chemischen Arbeitsstoffen ausgesetzt sind. Uns interessiert der Zusammenhang zwischen Mischstaubbelastung und chronischer Bronchitis. Die Studie umfasst eine einjährige Nachbeobachtung dieser Population. Als diagnostisches Kriterium für eine chronische Bronchitis haben wir „Morgenhusten und Schleimproduktion für drei Monate in zwei aufeinanderfolgenden Jahren“ festgelegt. Kriterien für eine „positive“ Staubexposition werden vor Studienbeginn festgelegt. Jeder Patient, der das Gesundheitszentrum besucht und diese Kriterien während eines Zeitraums von einem Jahr erfüllt, ist ein Fall, und der nächste Patient, der wegen nicht pulmonaler Probleme ärztlichen Rat einholt, wird als Kontrolle definiert. Angenommen, während des Studienzeitraums werden 100 Fälle und 100 Kontrollen aufgenommen. Es seien 40 Fälle und 15 Kontrollen als staubexponiert einzustufen. Dann
c1 = 40, c0 = 60, n1 = 15 und n0 = 85.
Folglich
![]()
Im vorstehenden Beispiel wurde die Möglichkeit einer Verwechslung nicht berücksichtigt, die aufgrund systematischer Unterschiede zwischen Fällen und Kontrollen in einer Variablen wie dem Alter zu einer Verzerrung des OR führen kann. Eine Möglichkeit, diese Verzerrung zu reduzieren, besteht darin, die Kontrollen den Fällen nach Alter oder anderen verdächtigen Faktoren zuzuordnen. Daraus ergibt sich ein in Tabelle 3 dargestelltes Datenlayout.
Tabelle 3. Layout der Fallkontrolldaten, wenn jedem Fall eine Kontrolle zugeordnet wird
|
Referenten |
||
|
Projekte |
Belichtung (+) |
Belichtung (-) |
|
Belichtung (+) |
f+ + |
f+ - |
|
Belichtung (-) |
f- + |
f- - |
Die Analyse konzentriert sich auf die diskordanten Paare: „Fall exponiert, Kontrolle nicht exponiert“ (f+–); und „Fall unbelichtet, Kontrolle belichtet“ (f–+). Wenn beide Mitglieder eines Paares exponiert oder nicht exponiert sind, wird das Paar nicht berücksichtigt. Das OR in einem Matched-Pair-Studiendesign ist definiert als
![]()
In einer Studie zum Zusammenhang zwischen Nasenkrebs und Holzstaubbelastung gab es insgesamt 164 Fall-Kontroll-Paare. Bei nur einem Paar waren sowohl der Fall als auch die Kontrolle exponiert worden, und bei 150 Paaren waren weder der Fall noch die Kontrolle exponiert worden. Diese Paare werden nicht weiter betrachtet. Das Gehäuse, aber nicht die Kontrolle, wurde in 12 Paaren exponiert, und die Kontrolle, aber nicht das Gehäuse, in einem Paar. Somit,
![]()
und da die Einheit in diesem Intervall nicht enthalten ist, ist das Ergebnis statistisch signifikant – das heißt, es besteht ein statistisch signifikanter Zusammenhang zwischen Nasenkrebs und Holzstaubbelastung.
Fall-Kontroll-Studien sind effizienter als Kohortenstudien, wenn die Krankheit ist selten; sie können tatsächlich die einzige Option bieten. Aber auch Volkskrankheiten können mit dieser Methode untersucht werden. Wenn die Exposition ist selten, eine expositionsbasierte Kohorte ist das bevorzugte oder einzig mögliche epidemiologische Design. Selbstverständlich können auch Kohortenstudien zu gemeinsamen Expositionen durchgeführt werden. Die Wahl zwischen Kohorten- und Fall-Kontroll-Designs, wenn sowohl die Exposition als auch die Erkrankung häufig sind, wird normalerweise unter Berücksichtigung von Validitätserwägungen entschieden.
Da sich Fall-Kontroll-Studien auf retrospektive Expositionsdaten stützen, die normalerweise auf der Erinnerung der Teilnehmer beruhen, ist ihre Schwachstelle die Ungenauigkeit und Rohheit der Expositionsinformationen, was zu einer Effektmaskierung führt nicht differenziell (symmetrische) Fehlklassifizierung des Expositionsstatus. Darüber hinaus kann der Rückruf manchmal zwischen Fällen und Kontrollen asymmetrisch sein, Fälle, von denen normalerweise angenommen wird, dass sie sich „besser“ erinnern (dh Rückrufverzerrung).
Selektive Rückrufe können eine effektverstärkende Verzerrung bewirken Differential (asymmetrische) Fehlklassifizierung des Expositionsstatus. Die Vorteile von Fall-Kontroll-Studien liegen in ihrer Kosteneffektivität und ihrer Fähigkeit, relativ schnell eine Problemlösung zu liefern. Aufgrund der Stichprobenstrategie ermöglichen sie die Untersuchung sehr großer Zielpopulationen (z. B. durch nationale Krebsregister) und erhöhen damit die statistische Aussagekraft der Studie. In Ländern, in denen Datenschutzgesetze oder das Fehlen guter Bevölkerungs- und Morbiditätsregister die Durchführung von Kohortenstudien behindern, können krankenhausbasierte Fall-Kontroll-Studien die einzige praktische Möglichkeit sein, epidemiologische Forschung durchzuführen.
Fall-Kontroll-Stichprobe innerhalb einer Kohorte (verschachtelte Fall-Kontroll-Studiendesigns)
Eine Kohortenstudie kann auch für Stichproben anstelle einer vollständigen Nachverfolgung konzipiert werden. Dieses Design wurde früher als „verschachtelte“ Fall-Kontroll-Studie bezeichnet. Ein Stichprobenansatz innerhalb der Kohorte stellt andere Anforderungen an die Kohorteneignung, da die Vergleiche nun innerhalb derselben Kohorte erfolgen. Dies sollte daher nicht nur stark exponierte Arbeitnehmer, sondern auch weniger exponierte und sogar nicht exponierte Arbeitnehmer umfassen, um eine Versorgung zu gewährleisten Belichtungskontraste in sich. Es ist wichtig, diesen Unterschied in den Zulassungsvoraussetzungen bei der Zusammenstellung der Kohorte zu berücksichtigen. Wenn zuerst eine vollständige Kohortenanalyse an einer Kohorte durchgeführt wird, deren Eignungskriterien auf einer „hohen“ Exposition lagen, und später eine „verschachtelte“ Fall-Kontroll-Studie an derselben Kohorte durchgeführt wird, wird die Studie unempfindlich. Dies führt zu einer Effektmaskierung, da die Belichtungskontraste aufgrund einer fehlenden Variabilität in der Belichtungserfahrung unter den Mitgliedern der Kohorte „absichtlich“ unzureichend sind.
Vorausgesetzt, die Kohorte verfügt über ein breites Spektrum an Expositionserfahrung, ist der verschachtelte Fall-Kontroll-Ansatz jedoch sehr attraktiv. Man fasst alle in der Kohorte auftretenden Fälle über den Nachbeobachtungszeitraum zur Fallserie zusammen, während nur a Sample der Nicht-Fälle wird für die Kontrollreihe gezogen. Die Forscher sammeln dann, wie beim traditionellen Fall-Kontroll-Design, detaillierte Informationen über die Expositionserfahrung, indem sie Fälle und Kontrollen (oder ihre nahen Verwandten) befragen, die Personallisten der Arbeitgeber prüfen, indem sie a Job-Exposure-Matrix, oder durch Kombinieren von zwei oder mehr dieser Ansätze. Die Kontrollen können entweder den Fällen zugeordnet oder als eigenständige Serie behandelt werden.
Der Stichprobenansatz kann im Vergleich zur umfassenden Informationsbeschaffung über jedes Mitglied der Kohorte weniger kostspielig sein. Da insbesondere nur eine Stichprobe von Kontrollen untersucht wird, können mehr Ressourcen für eine detaillierte und genaue Expositionsbewertung für jeden Fall und jede Kontrolle aufgewendet werden. Allerdings herrschen die gleichen statistischen Power-Probleme wie in klassischen Kohortenstudien. Um eine ausreichende statistische Aussagekraft zu erreichen, muss die Kohorte je nach Größe des zu erfassenden Risikos immer eine „ausreichende“ Anzahl exponierter Fälle umfassen.
Querschnittsstudiendesigns
Im wissenschaftlichen Sinne ist ein Querschnittsdesign ein Querschnitt der Studienpopulation ohne zeitliche Berücksichtigung. Sowohl Exposition als auch Morbidität (Prävalenz) werden zum gleichen Zeitpunkt gemessen.
Aus ätiologischer Sicht ist dieses Studiendesign schwach, auch weil es sich nicht um die Inzidenz, sondern um die Prävalenz handelt. Die Prävalenz ist ein zusammengesetztes Maß, das sowohl von der Inzidenz als auch von der Dauer der Krankheit abhängt. Dies schränkt auch den Einsatz von Querschnittsstudien auf lang andauernde Erkrankungen ein. Noch gravierender ist die starke negative Verzerrung, die durch die gesundheitsbedingte Eliminierung der gegenüber Expositionswirkungen empfindlicheren Personen aus der exponierten Gruppe verursacht wird. Daher werden ätiologische Probleme am besten durch Längsschnittdesigns gelöst. Tatsächlich lassen Querschnittsstudien keine Rückschlüsse darauf zu, ob eine Exposition einer Erkrankung vorausging oder umgekehrt. Der Wirkungsquerschnitt ist nur dann ätiologisch aussagekräftig, wenn zwischen der Exposition und dem Ergebnis ein echter zeitlicher Zusammenhang besteht, das heißt, dass die aktuelle Exposition unmittelbare Auswirkungen haben muss. Die Exposition kann jedoch querschnittlich gemessen werden, so dass sie einen längeren vergangenen Zeitraum darstellt (z. B. der Blutbleispiegel), während das Ergebnismaß eine Prävalenz ist (z. B. Nervenleitungsgeschwindigkeiten). Die Studie ist dann eher eine Mischung aus einem Längsschnitt- und einem Querschnittsdesign als ein bloßer Querschnitt der Studienpopulation.
Deskriptive Querschnittsbefragungen
Querschnittserhebungen sind oft eher für praktische und administrative als für wissenschaftliche Zwecke nützlich. Epidemiologische Prinzipien können auf systematische Überwachungsaktivitäten im arbeitsmedizinischen Umfeld angewendet werden, wie zum Beispiel:
- Beobachtung der Morbidität in Bezug auf Beruf, Arbeitsbereich oder bestimmte Expositionen
- regelmäßige Befragungen von Arbeitnehmern, die bekannten Berufsgefahren ausgesetzt sind
- Untersuchung von Arbeitnehmern, die mit neuen Gesundheitsgefahren in Kontakt kommen
- biologische Überwachungsprogramme
- Expositionserhebungen zur Identifizierung und Quantifizierung von Gefahren
- Screening-Programme verschiedener Arbeitnehmergruppen
- Bewertung des Anteils der Arbeitnehmer, die einer Vorbeugung oder regelmäßigen Kontrolle bedürfen (z. B. Blutdruck, koronare Herzkrankheit).
Es ist wichtig, repräsentative, gültige und spezifische Morbiditätsindikatoren für alle Arten von Erhebungen auszuwählen. Eine Befragung oder ein Screening-Programm kann im Gegensatz zur klinischen Diagnostik nur wenige Tests verwenden, daher ist der Vorhersagewert des Screening-Tests wichtig. Unempfindliche Methoden können die interessierende Krankheit nicht nachweisen, während hochempfindliche Methoden zu viele falsch positive Ergebnisse liefern. Ein Screening auf seltene Erkrankungen ist im beruflichen Umfeld nicht sinnvoll. Alle Aktivitäten zur Fallfindung (dh Screening) erfordern auch einen Mechanismus zur Betreuung von Personen mit „positiven“ Befunden, sowohl in Bezug auf Diagnostik als auch Therapie. Andernfalls wird nur Frustration resultieren, bei der möglicherweise mehr Schaden als Nutzen entsteht.
HAFTUNGSAUSSCHLUSS: Die ILO übernimmt keine Verantwortung für auf diesem Webportal präsentierte Inhalte, die in einer anderen Sprache als Englisch präsentiert werden, der Sprache, die für die Erstproduktion und Peer-Review von Originalinhalten verwendet wird. Bestimmte Statistiken wurden seitdem nicht aktualisiert die Produktion der 4. Auflage der Encyclopaedia (1998)."