bambini categorie

1. Sangue (3)

1. Sangue
Editor del capitolo: Bernard D.Goldstein
Sommario
tavoli
Sistema Ematopoietico e Linfatico
Bernard D.Goldstein
Leucemia, linfomi maligni e mieloma multiplo
Timo Partanen, Paolo Boffetta, Elisabete Weiderpass
Agenti o condizioni di lavoro che influenzano il sangue
Bernard D.Goldstein
tavoli
Fare clic su un collegamento sottostante per visualizzare la tabella nel contesto dell'articolo.

2. Cancro (4)

2. Cancro
Editor del capitolo: Paolo Boffetta
Table di contenuti
tavoli
Introduzione
Neil Pearce, Paolo Boffetta e Manolis Kogevinas
Agenti cancerogeni occupazionali
Paolo Boffetta, Rodolfo Saracci, Manolis Kogevinas, Julian Wilbourn e Harri Vainio
Cancro ambientale
Bruce K. Armstrong e Paolo Boffetta
Frodi
Per Gustavson
tavoli
Fare clic su un collegamento sottostante per visualizzare la tabella nel contesto dell'articolo.
- Tumori professionali: fatti chiave
- Proporzioni stimate di cancro (PAR) attribuibili alle occupazioni
- Valutazione delle prove di cancerogenicità nelle Monografie IARC
- Gruppi di classificazione del programma della monografia IARC
- Gruppo 1-Sostanze chimiche cancerogene per l'uomo
- Gruppo 2A: sostanze chimiche probabilmente cancerogene per l'uomo
- Gruppo 2B—Sostanze chimiche possibilmente cancerogene per l'uomo
- Pesticidi valutati nelle monografie IARC, volumi 1-63 (1972-1995)
- Farmaci valutati nelle monografie IARC, volumi 1-63 (1972-1995)
- Agenti ambientali/esposizioni note o sospette di cancro umano
- Industrie, occupazioni, esposizioni che presentano un rischio cancerogeno
- Industrie, occs., esp. con eccesso di cancro non cancerogeni definitivi
- Variazioni di popolazione registrate dell'incidenza di alcuni tumori comuni

3. Sistema cardiovascolare (7)

3. Sistema cardiovascolare
Redattori di capitoli: Lothar Heinemann e Gerd Heuchert
Sommario
Tabelle e figure
Introduzione
Lothar Heinemann e Gerd Heuchert
Morbilità e mortalità cardiovascolare nella forza lavoro
Gottfried Enderlein e Lothar Heinemann
Il concetto di fattore di rischio nelle malattie cardiovascolari
Lothar Heinemann, Gottfried Enderlein e Heide Stark
Programmi di riabilitazione e prevenzione
Lothar Heinemann e Gottfried Enderlein
Pericoli fisici, chimici e biologici
Fattori fisici
Heide Stark e Gerd Heuchert
Materiali chimici pericolosi
Ulrike Tittelbach e Wolfram Dietmar Schneider
Rischi biologici
Regina Jäckel, Ulrike Tittelbach e Wolfram Dietmar Schneider
tavoli
Fare clic su un collegamento sottostante per visualizzare la tabella nel contesto dell'articolo
- Mortalità da malattie cardiovascolari
- Tassi di mortalità, gruppi speciali di diagnosi cardiovascolare
- Tasso di malattia e ridotta capacità lavorativa
- Lavoro associato a rischi cardiovascolari
- Infezioni e malattie professionali
Cifre
Punta su una miniatura per vedere la didascalia della figura, fai clic per vedere la figura nel contesto dell'articolo.

4. Apparato digerente (6)

4. Apparato digerente
Editor del capitolo: Heikki Savolainen
Sommario
Cifre
Apparato digerente
G.Frada
Bocca e denti
F.Gabbato
Fegato
Giorgio Kazantzis
Ulcera peptica
KS Cho
Cancro al fegato
Timo Partanen, Timo Kauppinen, Paolo Boffetta e Elisabete Weiderpass
Cancro al pancreas
Timo Partanen, Timo Kauppinen, Paolo Boffetta e Elisabete Weiderpass
Cifre
Punta su una miniatura per vedere la didascalia della figura, fai clic per vedere la figura nel contesto dell'articolo.

5. Salute mentale (8)

5. Salute mentale
Redattori del capitolo: Joseph J. Hurrell, Lawrence R. Murphy, Steven L. Sauter e Lennart Levi
Sommario
Tabelle e figure
Lavoro e salute mentale
Irene LD Houtman e Michiel AJ Kompier
Psicosi lavoro-correlata
Craig Stenberg, Judith Holder e Krishna Tallur
Umore e affetto
Depressione
Jay Lasser e Jeffrey P.Kahn
Ansia correlata al lavoro
Randal D. Beaton
Disturbo da stress post-traumatico e sua relazione con la salute sul lavoro e la prevenzione degli infortuni
Marco Bravermann
Stress e burnout e loro implicazione nell'ambiente di lavoro
Herbert J.Freudenberger
Disturbi cognitivi
Catherine A.Heaney
Karoshi: Morte per eccesso di lavoro
Takashi Haratani
tavoli
Fare clic su un collegamento sottostante per visualizzare la tabella nel contesto dell'articolo.
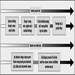
1. Panoramica schematica delle strategie di gestione ed esempi
Cifre
Punta su una miniatura per vedere la didascalia della figura, fai clic per vedere la figura nel contesto dell'articolo.

6. Sistema muscoloscheletrico (14)

6. Sistema muscoloscheletrico
Redattori del capitolo: Hilkka Riihimäki e Eira Viikari-Juntura
Sommario
Tabelle e figure
Panoramica
Hilkka Riihimäki
Muscoli
Gisela Sjogaard
tendini
Thomas J.Armstrong
Ossa e articolazioni
David Hamman
Dischi intervertebrali
Sally Roberts e Jill PG Urban
Regione lombare
Hilkka Riihimäki
Regione della colonna vertebrale toracica
Jarl-Erik Michelsson
Collo
Åsa Kilbom
Spalla
Mats Hagberg
Gomito
Eira Viikari-Juntura
Avambraccio, polso e mano
Eira Viikari-Juntura
Anca e ginocchio
Eva Vingård
Gamba, caviglia e piede
Jarl-Erik Michelsson
Altre malattie
Marjatta Leirisalo-Repo
tavoli
Fare clic su un collegamento sottostante per visualizzare la tabella nel contesto dell'articolo.
- Struttura-funzione dei componenti articolari
- Prevalenza di disturbi alla schiena, nei finlandesi oltre i 30 anni
- Ridurre i rischi di mal di schiena sul lavoro
- Classificazione dei disturbi lombari (Quebec Task Force)
- Movimenti consentiti per la testa nella guida prolungata
- Incidenza di epicondilite in varie popolazioni
- Incidenza di tenosinovite/peritendinite
- Osteoartrosi primaria dell'anca a Malmö, Svezia
- Linee guida per il trattamento dell'artrite reumatoide
- Infezioni note per scatenare l'artrite reattiva
Cifre
Punta su una miniatura per vedere la didascalia della figura, fai clic per vedere la figura nel contesto dell'articolo.

7. Sistema nervoso (9)

7. Sistema nervoso
Editor del capitolo: Donna Merger
Sommario
Tabelle e figure
Sistema nervoso: panoramica
Donna Mergler e José A. Valciukas
Anatomia e fisiologia
Josè A. Valciukas
Agenti Chimici Neurotossici
Peter Arlien-Søborg e Leif Simonsen
Manifestazioni di avvelenamento acuto e precoce cronico
Donna Merger
Prevenire la neurotossicità sul lavoro
Barry Johnson
Sindromi cliniche associate a neurotossicità
Robert G. Feldmann
Misurazione dei deficit neurotossici
Donna Merger
Diagnosi
Anna Maria Seppäläinen
Neuroepidemiologia occupazionale
Olav Axelson
tavoli
Fare clic su un collegamento sottostante per visualizzare la tabella nel contesto dell'articolo.
- Nomi e funzioni principali di ciascuna coppia di nervi cranici
- Raggruppamento degli effetti neurotossici per quanto riguarda la neurotossicità
- Gas associati ad effetti neurotossici
- Metalli neurotossici e loro composti inorganici
- Monomeri neurotossici
- Solventi organici associati a neurotossicità
- Classi di comuni pesticidi neurotossici
- Altre sostanze chimiche associate alla neurotossicità
- Lista di controllo dei sintomi cronici
- Effetti neurofunzionali dell'esposizione ad alcune neurotossine
- Esposizioni chimiche e sindromi neurotossiche associate
- Alcune batterie "core" per valutare i primi effetti neurotossici
- Albero decisionale per la malattia neurotossica
- Effetti neurofunzionali coerenti dell'esposizione in cantiere ad alcune delle principali sostanze neurotossiche
Cifre
Punta su una miniatura per vedere la didascalia della figura, fai clic per vedere la figura nel contesto dell'articolo.

8. Apparato renale-urinario (2)

8. Sistema renale-urinario
Editor del capitolo: George P.Hemstreet
Sommario
Tabelle e figure
Sistemi renale-urinario
George P.Hemstreet
Tumori renali-urinari
Timo Partanen, Harri Vainio, Paolo Boffetta e Elisabete Weiderpass
tavoli
Fare clic su un collegamento sottostante per visualizzare la tabella nel contesto dell'articolo.
- Enzimi del metabolismo dei farmaci nel rene
- Le cause più comuni di ematuria, per età e sesso
- Criteri per la selezione dei biomarcatori
- Potenziali biomarcatori legati al danno cellulare
- Insufficienza renale acuta e occupazione
- Segmenti del nefrone interessati da sostanze tossiche selezionate
- Applicazioni della citologia urinaria
Cifre
Punta su una miniatura per vedere la didascalia della figura, fai clic per vedere la figura nel contesto dell'articolo.

9. Sistema riproduttivo (9)

9. Sistema riproduttivo
Editor del capitolo: Grace Kawas Lemasters
Sommario
Tabelle e figure
Sistema riproduttivo: introduzione
Lowell E. Sever
Introduzione alla funzione riproduttiva maschile e femminile
Donald R. Mattison
Sistema riproduttivo maschile e tossicologia
Steven Schrader e Grace Kawas Lemasters
Struttura del sistema riproduttivo femminile e vulnerabilità dell'organo bersaglio
Donald R. Mattison
Esposizioni occupazionali materne ed esiti avversi della gravidanza
Grace Kawas Lemasters
Parto pretermine e lavoro
Nicola Mamelle
Esposizioni occupazionali e ambientali del neonato
Mary S. Wolff e Patrisha M. Woolard
Protezione della maternità nella legislazione
Marie-Claire Séguret
Raccomandazioni per la gravidanza e il lavoro negli Stati Uniti
Leon J.Warshaw
tavoli
Fare clic su un collegamento sottostante per visualizzare la tabella nel contesto dell'articolo.
1. Esposizioni con endpoint avversi multipli
2. Studi epidemiologici degli effetti paterni sull'esito della gravidanza
3. Potenziali sostanze tossiche per la riproduzione femminile
4. Definizione di perdita fetale e morte infantile
5. Fattori per piccoli per età gestazionale e perdita fetale
6. Fonti identificate di affaticamento professionale
7. Rischi relativi e indici di affaticamento per il parto pretermine
8. Rischio di prematurità per numero di indici di affaticamento professionale
9. Rischi relativi e cambiamenti delle condizioni di lavoro
10 Fonti e livelli di esposizione neonatale
Cifre
Punta su una miniatura per vedere la didascalia della figura, fai clic per vedere la figura nel contesto dell'articolo.

10. Sistema respiratorio (18)

10. Sistema respiratorio
Editor di capitoli: Alois David e Gregory R.Wagner
Sommario
Tabelle e figure
Struttura e funzione
Morton Lipmann
Esame della funzionalità polmonare
Ulf Ulfvarson e Monica Dahlqvist
Malattie causate da irritanti respiratori e sostanze chimiche tossiche
David LS Ryon e William N. Rom
Asma professionale
George Friedman-Jimenez e Edward L. Petsonk
Malattie causate da polveri organiche
Ragnar Rylander e Richard SF Schilling
Malattia del berillio
Homayun Kazemi
Pneumoconiosi: definizione
Alois David
Classificazione internazionale ILO delle radiografie delle pneumoconiosi
Michele Lesage
Eziopatogenesi delle pneumoconiosi
Patrick Sébastien e Raymond Bégin
Silicosi
John E. Parker e Gregory R. Wagner
Malattie polmonari dei lavoratori del carbone
Michael D. Attfield, Edward L. Petsonk e Gregory R. Wagner
Malattie correlate all'amianto
Margaret R. Becklake
Malattia dei metalli duri
Gerolamo Chiappino
Sistema respiratorio: la varietà di pneumoconiosi
Steven R. Short e Edward L. Petsonk
Broncopneumopatia cronica ostruttiva
Kazimierz Marek e Jan E. Zejda
Effetti sulla salute delle fibre sintetiche
James E. Lockey e Clara S. Ross
Cancro respiratorio
Paolo Boffetta e Elisabete Weiderpass
Infezioni professionali acquisite del polmone
Anthony A. Marfin, Ann F. Hubbs, Karl J. Musgrave e John E. Parker
tavoli
Fare clic su un collegamento sottostante per visualizzare la tabella nel contesto dell'articolo.
1. Regioni del tratto respiratorio e modelli di deposizione di particelle
2. Criteri per la polvere inalabile, toracica e respirabile
3. Riepilogo degli irritanti respiratori
4. Meccanismi di danno polmonare da sostanze inalate
5. Composti capaci di tossicità polmonare
6. Definizione di caso medico di asma professionale
7. Passi nella valutazione diagnostica dell'asma sul posto di lavoro
8. Agenti sensibilizzanti che possono causare asma professionale
9. Esempi di sorgenti di pericoli di esposizione a polveri organiche
10 Agenti nelle polveri organiche con potenziale attività biologica
11 Malattie indotte da polveri organiche e loro codici ICD
12 Criteri diagnostici per la bissinosi
13 Proprietà del berillio e dei suoi composti
14 Descrizione delle radiografie standard
15 Classificazione ILO 1980: radiografie di pneumoconiosi
16 Malattie e condizioni legate all'amianto
17 Principali fonti commerciali, prodotti e usi dell'amianto
18 Prevalenza della BPCO
19 Fattori di rischio implicati nella BPCO
20 Perdita della funzione ventilatoria
21 Classificazione diagnostica, bronchite cronica ed enfisema
22 Test di funzionalità polmonare nella BPCO
23 Fibre sintetiche
24 Carcinogeni respiratori umani accertati (IARC)
25 Probabili cancerogeni respiratori umani (IARC)
26 Malattie infettive respiratorie professionali acquisite
Cifre
Punta su una miniatura per vedere la didascalia della figura, fai clic per vedere la figura nel contesto dell'articolo.

11. Sistemi sensoriali (8)

11. Sistemi sensoriali
Editor del capitolo: Heikki Savolainen
Sommario
Tabelle e figure
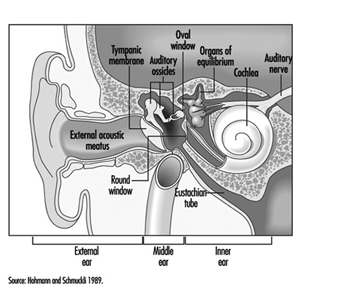
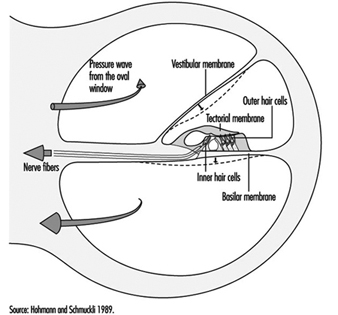
L'orecchio
Marcel-André Boillat
Disturbi dell'udito indotti chimicamente
Pietro Jacobsen
Disturbi dell'udito di origine fisica
Peter L. Pelmear
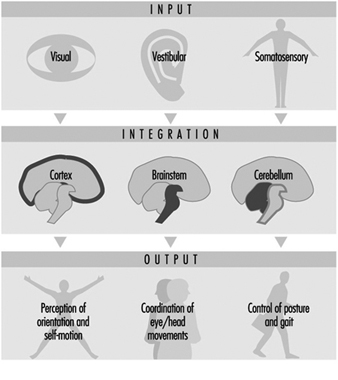
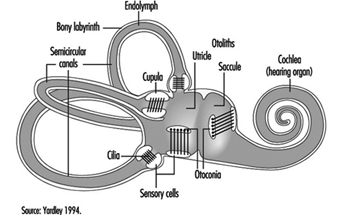
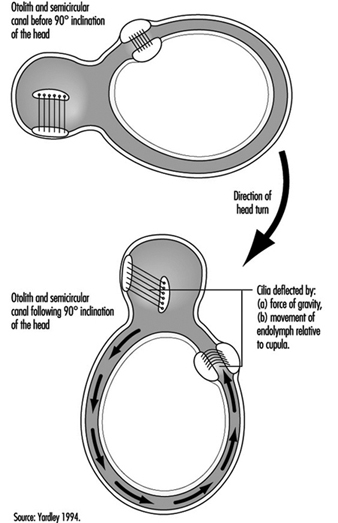
equilibrio
Lucia Yardley
Visione e lavoro
Paule Rey e Jean-Jacques Meyer
Gusto
Aprile E. Mott e Norman Mann
Odore
Aprile E. Mott
Recettori Cutanei
Robert Dykes e Daniel McBain
tavoli
Fare clic su un collegamento sottostante per visualizzare la tabella nel contesto dell'articolo.
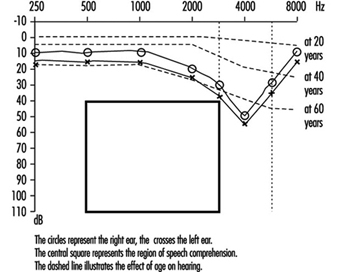
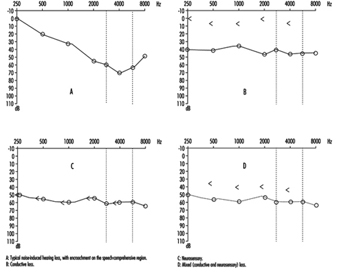
1. Tipico calcolo della perdita funzionale da un audiogramma
2. Requisiti visivi per diverse attività
3. Valori di illuminamento consigliati per la progettazione illuminotecnica
4. Requisiti visivi per una patente di guida in Francia
5. Agenti/processi segnalati per alterare il sistema del gusto
6. Agenti/processi associati ad anomalie olfattive
Cifre
Punta su una miniatura per vedere la didascalia della figura, fai clic per vedere la figura nel contesto dell'articolo.

12. Malattie della pelle (7)

12. Malattie della pelle
Editor del capitolo: Luigi Filippo Durocher
Sommario
Tabelle e figure
Panoramica: Malattie professionali della pelle
Donald J.Birmingham
Cancro della pelle non melanocitico
Elisabete Weiderpass, Timo Partanen, Paolo Boffetta
Melanoma maligno
Timo Partanen, Paolo Boffetta, Elisabete Weiderpass
Dermatite professionale da contatto
Denis Sasseville
Prevenzione delle dermatosi professionali
Luigi Filippo Durocher
Distrofia professionale delle unghie
CD Calnan
Stigmata
H.Mierzecki
tavoli
Fare clic su un collegamento sottostante per visualizzare la tabella nel contesto dell'articolo.
1. Occupazioni a rischio
2. Tipi di dermatite da contatto
3. Irritanti comuni
4. Allergeni cutanei comuni
5. Fattori predisponenti per la dermatite professionale
6. Esempi di irritanti e sensibilizzanti della pelle con occupazioni
7. Dermatosi occupazionali in Quebec nel 1989
8. Fattori di rischio e loro effetti sulla pelle
9. Misure collettive (approccio di gruppo) alla prevenzione
Cifre
Punta su una miniatura per vedere la didascalia della figura, fai clic per vedere la figura nel contesto dell'articolo.

13. Condizioni sistemiche (3)

13. Condizioni sistemiche
Editor del capitolo: Howard M. Kipen
Sommario
Cifre
Condizioni sistemiche: un'introduzione
Howard M. Kipen
Sindrome da costruzione malata
Michael J.Hodgson
Sensibilità chimiche multiple
Mark R. Cullen
Cifre
Punta su una miniatura per vedere la didascalia della figura, fai clic per vedere la figura nel contesto dell'articolo.
Eziopatogenesi delle pneumoconiosi
Le pneumoconiosi sono da tempo riconosciute come malattie professionali. Notevoli sforzi sono stati rivolti alla ricerca, alla prevenzione primaria e alla gestione medica. Ma medici e igienisti riferiscono che il problema è ancora presente sia nei paesi industrializzati che in quelli in via di industrializzazione (Valiante, Richards e Kinsley 1992; Markowitz 1992). Poiché vi è una forte evidenza che i tre principali minerali industriali responsabili delle pneumoconiosi (amianto, carbone e silice) continueranno ad avere una certa importanza economica, comportando quindi un'ulteriore possibile esposizione, si prevede che il problema continuerà ad essere di una certa entità per tutto il mondo, in particolare tra le popolazioni svantaggiate nelle piccole industrie e nelle piccole attività minerarie. Difficoltà pratiche nella prevenzione primaria, o insufficiente comprensione dei meccanismi responsabili dell'induzione e della progressione della malattia sono tutti fattori che potrebbero eventualmente spiegare la persistenza del problema.
L'eziopatogenesi delle pneumoconiosi può essere definita come la valutazione e la comprensione di tutti i fenomeni che si verificano nel polmone in seguito all'inalazione di particelle di polvere fibrogena. L'espressione cascata di eventi si trova spesso nella letteratura sull'argomento. La cascata è una serie di eventi che prima l'esposizione e nella sua massima estensione progredisce verso la malattia nelle sue forme più gravi. Se si escludono le rare forme di silicosi accelerata, che possono svilupparsi dopo solo pochi mesi di esposizione, la maggior parte delle pneumoconiosi si sviluppano dopo periodi di esposizione misurati in decenni anziché in anni. Ciò è particolarmente vero oggigiorno nei luoghi di lavoro che adottano moderni standard di prevenzione. I fenomeni di eziopatogenesi dovrebbero quindi essere analizzati in termini della sua dinamica a lungo termine.
Negli ultimi 20 anni si è resa disponibile una grande quantità di informazioni sulle numerose e complesse reazioni polmonari coinvolte nella fibrosi polmonare interstiziale indotta da diversi agenti, comprese le polveri minerali. Queste reazioni sono state descritte a livello biochimico e cellulare (Richards, Masek e Brown 1991). I contributi sono stati forniti non solo da fisici e patologi sperimentali, ma anche da medici che hanno utilizzato ampiamente il lavaggio broncoalveolare come nuova tecnica di indagine polmonare. Questi studi hanno raffigurato l'eziopatogenesi come un'entità molto complessa, che può tuttavia essere scomposta per rivelare diversi aspetti: (1) l'inalazione stessa di particelle di polvere e la conseguente costituzione e significato del carico polmonare (relazioni esposizione-dose-risposta), ( 2) le caratteristiche fisico-chimiche delle particelle fibrogeniche, (3) le reazioni biochimiche e cellulari che inducono le lesioni fondamentali delle pneumoconiosi e (4) i determinanti della progressione e delle complicanze. L'ultimo aspetto non deve essere ignorato, poiché le forme più gravi di pneumoconiosi sono quelle che comportano menomazione e disabilità.
Un'analisi dettagliata dell'eziopatogenesi delle pneumoconiosi esula dagli scopi di questo articolo. Bisognerebbe distinguere i vari tipi di polvere e approfondire numerosi ambiti specialistici, alcuni dei quali sono tuttora oggetto di attiva ricerca. Ma interessanti nozioni generali emergono dalla mole di conoscenze attualmente disponibili sull'argomento. Saranno qui presentati attraverso le quattro “sfaccettature” precedentemente menzionate e la bibliografia rimanderà il lettore interessato a testi più specialistici. Verranno forniti esempi essenzialmente per le tre principali e più documentate pneumoconiosi: l'asbestosi, la pneumoconiosi dei lavoratori del carbone (CWP) e la silicosi. Verranno discussi i possibili impatti sulla prevenzione.
Relazioni esposizione-dose-risposta
Le pneumoconiosi derivano dall'inalazione di alcune particelle di polvere fibrogena. Nella fisica degli aerosol, il termine polvere ha un significato molto preciso (Hinds 1982). Si riferisce a particelle sospese nell'aria ottenute per sminuzzamento meccanico di un materiale base allo stato solido. Le particelle generate da altri processi non dovrebbero essere chiamate polvere. Le nuvole di polvere in vari ambienti industriali (ad es. miniere, tunnel, sabbiatura e produzione) generalmente contengono una miscela di diversi tipi di polvere. Le particelle di polvere aerodisperse non hanno una dimensione uniforme. Presentano una distribuzione dimensionale. Le dimensioni e altri parametri fisici (densità, forma e carica superficiale) determinano il comportamento aerodinamico delle particelle e la probabilità della loro penetrazione e deposizione nei vari compartimenti dell'apparato respiratorio.
Nel campo delle pneumoconiosi, il compartimento sito di interesse è il compartimento alveolare. Le particelle sospese nell'aria abbastanza piccole da raggiungere questi compartimenti sono indicate come particelle respirabili. Tutte le particelle che raggiungono i compartimenti alveolari non vengono sistematicamente depositate, alcune sono ancora presenti nell'aria espirata. I meccanismi fisici responsabili della deposizione sono ora ben compresi per le particelle isometriche (Raabe 1984) così come per le particelle fibrose (Sébastien 1991). Sono state stabilite le funzioni che mettono in relazione la probabilità di deposizione ai parametri fisici. Le particelle respirabili e le particelle depositate nel compartimento alveolare hanno caratteristiche dimensionali leggermente diverse. Per le particelle non fibrose, vengono utilizzati strumenti di campionamento dell'aria selettivi per dimensione e strumenti a lettura diretta per misurare le concentrazioni di massa delle particelle respirabili. Per le particelle fibrose, l'approccio è diverso. La tecnica di misurazione si basa sulla raccolta del filtro della "polvere totale" e sul conteggio delle fibre al microscopio ottico. In questo caso la selezione dimensionale viene effettuata escludendo dal conteggio le fibre “non respirabili” con dimensioni eccedenti criteri prefissati.
In seguito alla deposizione di particelle sulle superfici alveolari inizia il cosiddetto processo di clearance alveolare. Il reclutamento chemiotattico dei macrofagi e la fagocitosi costituiscono le sue prime fasi. Sono state descritte diverse vie di clearance: rimozione dei macrofagi carichi di polvere verso le vie aeree ciliate, interazione con le cellule epiteliali e trasferimento di particelle libere attraverso la membrana alveolare, fagocitosi da parte dei macrofagi interstiziali, sequestro nell'area interstiziale e trasporto ai linfonodi ( Lauweryns e Baert 1977). I percorsi di clearance hanno una cinetica specifica. Non solo il regime di esposizione, ma anche le caratteristiche fisico-chimiche delle particelle depositate, innescano l'attivazione delle diverse vie responsabili della ritenzione polmonare di tali contaminanti.
La nozione di un modello di ritenzione specifico per ogni tipo di polvere è piuttosto nuova, ma è ormai sufficientemente consolidata per essere integrata negli schemi eziopatogenetici. Ad esempio, questo autore ha scoperto che dopo un'esposizione a lungo termine all'amianto, le fibre si accumuleranno nei polmoni se sono del tipo anfibolo, ma non se sono del tipo crisotilo (Sébastien 1991). È stato dimostrato che le fibre corte vengono eliminate più rapidamente di quelle più lunghe. È noto che il quarzo mostra un certo tropismo linfatico e penetra facilmente nel sistema linfatico. È stato dimostrato che la modifica della chimica superficiale delle particelle di quarzo influisce sulla clearance alveolare (Hemenway et al. 1994; Dubois et al. 1988). L'esposizione concomitante a diversi tipi di polvere può anche influenzare la clearance alveolare (Davis, Jones e Miller 1991).
Durante la clearance alveolare, le particelle di polvere possono subire alcuni cambiamenti chimici e fisici. Esempi di questi cambiamenti includono il rivestimento con materiale ferruginoso, la lisciviazione di alcuni costituenti elementari e l'adsorbimento di alcune molecole biologiche.
Un'altra nozione recentemente derivata da esperimenti su animali è quella di “sovraccarico polmonare” (Mermelstein et al. 1994). I ratti fortemente esposti per inalazione a una varietà di polveri insolubili hanno sviluppato risposte simili: infiammazione cronica, aumento del numero di macrofagi carichi di particelle, aumento del numero di particelle nell'interstizio, ispessimento del setto, lipoproteinosi e fibrosi. Questi risultati non sono stati attribuiti alla reattività delle polveri testate (biossido di titanio, ceneri vulcaniche, ceneri volanti, coke di petrolio, cloruro di polivinile, toner, nerofumo e particolato di scarico diesel), ma a un'eccessiva esposizione del polmone. Non è noto se il sovraccarico polmonare debba essere considerato in caso di esposizione umana a polveri fibrogeniche.
Tra le vie di clearance, il trasferimento verso l'interstizio sarebbe di particolare importanza per le pneumoconiosi. L'eliminazione delle particelle che hanno subito il sequestro nell'interstizio è molto meno efficace dell'eliminazione delle particelle inghiottite dai macrofagi nello spazio alveolare e rimosse dalle vie aeree ciliate (Vincent e Donaldson 1990). Negli esseri umani, è stato riscontrato che dopo un'esposizione a lungo termine a una varietà di contaminanti inorganici trasportati dall'aria, lo stoccaggio era molto maggiore nei macrofagi interstiziali rispetto a quelli alveolari (Sébastien et al. 1994). È stata anche espressa l'opinione che la fibrosi polmonare indotta dalla silice implichi la reazione di particelle con macrofagi interstiziali piuttosto che alveolari (Bowden, Hedgecock e Adamson 1989). La ritenzione è responsabile della “dose”, una misura del contatto tra le particelle di polvere e il loro ambiente biologico. Una corretta descrizione della dose richiederebbe di conoscere in ogni momento la quantità di polvere immagazzinata nelle diverse strutture e cellule polmonari, gli stati fisico-chimici delle particelle (inclusi gli stati superficiali) e le interazioni tra le particelle e il cellule e fluidi polmonari. La valutazione diretta della dose negli esseri umani è ovviamente un compito impossibile, anche se fossero disponibili metodi per misurare le particelle di polvere in diversi campioni biologici di origine polmonare come espettorato, fluido di lavaggio broncoalveolare o tessuto prelevato alla biopsia o all'autopsia (Bignon, Sébastien e Bientz 1979) . Questi metodi sono stati utilizzati per una varietà di scopi: fornire informazioni sui meccanismi di ritenzione, convalidare determinate informazioni sull'esposizione, studiare il ruolo di diversi tipi di polvere negli sviluppi patogeni (ad esempio, anfiboli rispetto all'esposizione al crisotilo nell'asbestosi o quarzo rispetto al carbone nella CWP) e per aiutare nella diagnosi.
Ma queste misurazioni dirette forniscono solo un'istantanea della ritenzione al momento del campionamento e non consentono allo sperimentatore di ricostituire i dati sulla dose. Nuovi modelli dosimetrici offrono prospettive interessanti a tale riguardo (Katsnelson et al. 1994; Smith 1991; Vincent e Donaldson 1990). Questi modelli mirano a valutare la dose dalle informazioni sull'esposizione considerando la probabilità di deposito e la cinetica dei diversi percorsi di eliminazione. Recentemente è stata introdotta in questi modelli l'interessante nozione di “consegna dannosa” (Vincent e Donaldson 1990). Questa nozione tiene conto della reattività specifica delle particelle immagazzinate, ogni particella essendo considerata come una fonte che libera alcune entità tossiche nell'ambiente polmonare. Nel caso delle particelle di quarzo, ad esempio, si potrebbe ipotizzare che alcuni siti superficiali possano essere fonte di specie di ossigeno attivo. I modelli sviluppati lungo tali linee potrebbero anche essere perfezionati per tener conto della grande variazione interindividuale generalmente osservata con la clearance alveolare. Ciò è stato documentato sperimentalmente con l'amianto, gli "animali ad alto mantenimento" sono a maggior rischio di sviluppare l'asbestosi (Bégin e Sébastien 1989).
Finora, questi modelli sono stati utilizzati esclusivamente da patologi sperimentali. Ma potrebbero anche essere utili agli epidemiologi (Smith 1991). La maggior parte degli studi epidemiologici che esaminavano le relazioni di risposta all'esposizione si basava sull'"esposizione cumulativa", un indice di esposizione ottenuto integrando nel tempo le concentrazioni stimate di polvere aerodispersa a cui i lavoratori erano stati esposti (prodotto di intensità e durata). L'uso dell'esposizione cumulativa ha alcune limitazioni. Le analisi basate su questo indice assumono implicitamente che la durata e l'intensità abbiano effetti equivalenti sul rischio (Vacek e McDonald 1991).
Forse l'uso di questi sofisticati modelli dosimetrici potrebbe fornire qualche spiegazione per un'osservazione comune nell'epidemiologia delle pneumoconiosi: "le notevoli differenze tra le forze di lavoro" e questo fenomeno è stato chiaramente osservato per l'asbestosi (Becklake 1991) e per CWP (Attfield e Morring 1992). Nel mettere in relazione la prevalenza della malattia con l'esposizione cumulativa, sono state osservate grandi differenze, fino a 50 volte, nel rischio tra alcuni gruppi professionali. L'origine geologica del carbone (grado di carbone) ha fornito una spiegazione parziale per CWP, giacimenti minerari di carbone di alto rango (un carbone con un alto contenuto di carbonio, come l'antracite) che comportano un rischio maggiore. Il fenomeno resta da spiegare nel caso dell'asbestosi. Le incertezze sulla corretta curva di risposta all'esposizione influiscono, almeno teoricamente, sul risultato, anche con gli attuali standard di esposizione.
Più in generale, le metriche di esposizione sono essenziali nel processo di valutazione del rischio e nella definizione dei limiti di controllo. L'utilizzo dei nuovi modelli dosimetrici può migliorare il processo di valutazione del rischio per pneumoconiosi con l'obiettivo finale di aumentare il grado di protezione offerto dai limiti di controllo (Kriebel 1994).
Caratteristiche fisico-chimiche delle particelle di polvere fibrogeniche
Una tossicità specifica per ogni tipo di polvere, correlata alle caratteristiche fisico-chimiche delle particelle (comprese quelle più sottili come le caratteristiche superficiali), costituisce probabilmente la nozione più importante emersa progressivamente negli ultimi 20 anni. Nelle primissime fasi della ricerca non si faceva alcuna distinzione tra “polveri minerali”. Poi sono state introdotte le categorie generiche: amianto, carbone, fibre inorganiche artificiali, fillosilicati e silice. Ma questa classificazione si è rivelata non abbastanza precisa da spiegare la varietà degli effetti biologici osservati. Al giorno d'oggi viene utilizzata una classificazione mineralogica. Ad esempio, si distinguono i vari tipi mineralogici di amianto: crisotilo serpentino, anfibolo amosite, anfibolo crocidolite e anfibolo tremolite. Per la silice viene generalmente fatta una distinzione tra quarzo (di gran lunga il più diffuso), altri polimorfi cristallini e varietà amorfe. Nel campo del carbone, i carboni di alto rango e di basso rango dovrebbero essere trattati separatamente, poiché vi sono prove evidenti che il rischio di CWP e in particolare il rischio di fibrosi massiva progressiva è molto maggiore dopo l'esposizione alla polvere prodotta nelle miniere di carbone di alto rango.
Ma anche la classificazione mineralogica ha dei limiti. Esistono prove, sia sperimentali che epidemiologiche (tenendo conto delle "differenze tra le forze di lavoro"), che la tossicità intrinseca di un singolo tipo mineralogico di polvere può essere modulata agendo sulle caratteristiche fisico-chimiche delle particelle. Ciò ha sollevato la difficile questione del significato tossicologico di ciascuno dei numerosi parametri che possono essere utilizzati per descrivere una particella di polvere e una nuvola di polvere. A livello di singola particella, possono essere considerati diversi parametri: chimica di massa, struttura cristallina, forma, densità, dimensione, area superficiale, chimica superficiale e carica superficiale. Trattare con le nuvole di polvere aggiunge un altro livello di complessità a causa della distribuzione di questi parametri (ad esempio, la distribuzione delle dimensioni e la composizione della polvere mista).
La dimensione delle particelle e la loro chimica superficiale sono stati i due parametri più studiati per spiegare l'effetto di modulazione. Come visto in precedenza, i meccanismi di ritenzione sono correlati alle dimensioni. Ma le dimensioni possono anche modulare la tossicità on-site, come dimostrato da numerosi animali e in vitro studi.
Nel campo delle fibre minerali, la dimensione era ritenuta di tale importanza da costituire la base di una teoria patogenetica. Questa teoria attribuiva la tossicità delle particelle fibrose (naturali e artificiali) alla forma e alle dimensioni delle particelle, senza lasciare alcun ruolo alla composizione chimica. Quando si tratta di fibre, la dimensione deve essere suddivisa in lunghezza e diametro. Dovrebbe essere utilizzata una matrice bidimensionale per riportare le distribuzioni delle dimensioni, gli intervalli utili sono da 0.03 a 3.0 mm per il diametro e da 0.3 a 300 mm per la lunghezza (Sébastien 1991). Integrando i risultati dei numerosi studi, Lippman (1988) ha assegnato un indice di tossicità a diverse cellule della matrice. C'è una tendenza generale a credere che le fibre lunghe e sottili siano le più pericolose. Poiché le norme attualmente utilizzate nell'igiene industriale si basano sull'uso del microscopio ottico, ignorano le fibre più sottili. Se valutare la tossicità specifica di ogni cellula all'interno della matrice ha un certo interesse accademico, il suo interesse pratico è limitato dal fatto che ogni tipo di fibra è associato a una distribuzione dimensionale specifica che è relativamente uniforme. Per le particelle compatte, come il carbone e la silice, non ci sono evidenze chiare su un possibile ruolo specifico per le diverse sottofrazioni dimensionali delle particelle depositate nella regione alveolare del polmone.
Più recenti teorie di patogenesi nel campo delle polveri minerali implicano siti (o funzionalità) chimici attivi presenti sulla superficie delle particelle. Quando la particella "nasce" per separazione dal suo materiale genitore, alcuni legami chimici vengono rotti in modo eterolitico o omolitico. Ciò che si verifica durante la rottura e le successive ricombinazioni o reazioni con molecole di aria ambiente o molecole biologiche costituisce la chimica superficiale delle particelle. Per quanto riguarda le particelle di quarzo, ad esempio, sono state descritte diverse funzionalità chimiche di particolare interesse: ponti silossanici, gruppi silanolo, gruppi parzialmente ionizzati e radicali a base di silicio.
Queste funzionalità possono avviare sia reazioni acido-base che redox. Solo di recente è stata attirata l'attenzione su quest'ultimo (Dalal, Shi e Vallyathan 1990; Fubini et al. 1990; Pézerat et al. 1989; Kamp et al. 1992; Kennedy et al. 1989; Bronwyn, Razzaboni e Bolsaitis 1990). Ora ci sono buone prove che le particelle con radicali superficiali possono produrre specie reattive dell'ossigeno, anche in un ambiente cellulare. Non è certo se tutta la produzione di specie ossigenate debba essere attribuita ai radicali di superficie. Si ipotizza che questi siti possano innescare l'attivazione delle cellule polmonari (Hemenway et al. 1994). Altri siti possono essere coinvolti nell'attività membranolitica delle particelle citotossiche con reazioni quali attrazione ionica, legame idrogeno e legame idrofobico (Nolan et al. 1981; Heppleston 1991).
In seguito al riconoscimento della chimica superficiale come importante determinante della tossicità della polvere, sono stati fatti diversi tentativi per modificare le superfici naturali delle particelle di polvere minerale per ridurne la tossicità, come valutato in modelli sperimentali.
È stato riscontrato che l'adsorbimento di alluminio su particelle di quarzo riduce la loro fibrogenicità e favorisce la clearance alveolare (Dubois et al. 1988). Il trattamento con polivinilpiridina-N-ossido (PVPNO) ha avuto anche qualche effetto profilattico (Goldstein e Rendall 1987; Heppleston 1991). Sono stati utilizzati diversi altri processi di modifica: macinazione, trattamento termico, incisione con acido e adsorbimento di molecole organiche (Wiessner et al. 1990). Le particelle di quarzo appena fratturate hanno mostrato la massima attività superficiale (Kuhn e Demers 1992; Vallyathan et al. 1988). Abbastanza interessante, ogni allontanamento da questa "superficie fondamentale" ha portato a una diminuzione della tossicità del quarzo (Sébastien 1990). La purezza della superficie di diverse varietà di quarzo presenti in natura potrebbe essere responsabile di alcune differenze osservate nella tossicità (Wallace et al. 1994). Alcuni dati supportano l'idea che la quantità di superficie di quarzo incontaminata sia un parametro importante (Kriegseis, Scharman e Serafin 1987).
La molteplicità dei parametri, insieme alla loro distribuzione nella nube di polvere, produce una varietà di modi possibili per riportare le concentrazioni nell'aria: concentrazione di massa, concentrazione numerica, concentrazione dell'area superficiale e concentrazione in varie categorie dimensionali. Pertanto, possono essere costruiti numerosi indici di esposizione e deve essere valutato il significato tossicologico di ciascuno. Gli standard attuali in materia di igiene del lavoro riflettono questa molteplicità. Per l'amianto, gli standard si basano sulla concentrazione numerica di particelle fibrose in una determinata categoria di dimensioni geometriche. Per la silice e il carbone, gli standard si basano sulla concentrazione di massa delle particelle respirabili. Alcuni standard sono stati sviluppati anche per l'esposizione a miscele di particelle contenenti quarzo. Nessuno standard si basa sulle caratteristiche della superficie.
Meccanismi biologici che inducono le lesioni fondamentali
Le pneumoconiosi sono malattie polmonari fibrose interstiziali, la fibrosi è diffusa o nodulare. La reazione fibrotica comporta l'attivazione del fibroblasto polmonare (Goldstein e Fine 1986) e la produzione e il metabolismo dei componenti del tessuto connettivo (collagene, elastina e glicosaminoglicani). Si ritiene che rappresenti una fase tardiva di guarigione dopo un danno polmonare (Niewoehner e Hoidal 1982). Anche se diversi fattori, essenzialmente legati alle caratteristiche dell'esposizione, possono modulare la risposta patologica, è interessante notare che ogni tipo di pneumoconiosi è caratterizzato da quella che potrebbe essere definita una lesione fondamentale. L'alveolite fibrosante intorno alle vie aeree periferiche costituisce la lesione fondamentale dell'esposizione all'amianto (Bégin et al. 1992). Il nodulo silicotico è la lesione fondamentale della silicosi (Ziskind, Jones e Weil 1976). Il CWP semplice è composto da macule e noduli di polvere (Seaton 1983).
La patogenesi delle pneumoconiosi si presenta generalmente come una cascata di eventi la cui sequenza è la seguente: alveolite dei macrofagi alveolari, signaling da parte delle citochine cellulari infiammatorie, danno ossidativo, proliferazione e attivazione dei fibroblasti e del metabolismo del collagene e dell'elastina. L'alveolite dei macrofagi alveolari è una caratteristica reazione alla ritenzione di polvere minerale fibrosante (Rom 1991). L'alveolite è definita da un numero maggiore di macrofagi alveolari attivati che rilasciano quantità eccessive di mediatori tra cui ossidanti, chemiotassine, fattori di crescita dei fibroblasti e proteasi. Le chemiotassine attraggono i neutrofili e, insieme ai macrofagi, possono rilasciare ossidanti in grado di danneggiare le cellule epiteliali alveolari. I fattori di crescita dei fibroblasti ottengono l'accesso all'interstizio, dove segnalano ai fibroblasti di replicarsi e aumentare la produzione di collagene.
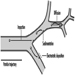
La cascata inizia al primo incontro di particelle depositate negli alveoli. Con l'amianto, ad esempio, la lesione polmonare iniziale si verifica quasi immediatamente dopo l'esposizione alle biforcazioni del dotto alveolare. Dopo solo 1 ora di esposizione negli esperimenti sugli animali, c'è un assorbimento attivo delle fibre da parte delle cellule epiteliali di tipo I (Brody et al. 1981). Entro 48 ore, nei siti di deposizione si accumula un numero maggiore di macrofagi alveolari. Con l'esposizione cronica, questo processo può portare ad alveolite fibrosante peribronchiolare.
L'esatto meccanismo mediante il quale le particelle depositate producono un danno biochimico primario al rivestimento alveolare, a una cellula specifica oa uno qualsiasi dei suoi organelli, è sconosciuto. Può darsi che reazioni biochimiche estremamente rapide e complesse portino alla formazione di radicali liberi, alla perossidazione lipidica o all'esaurimento di alcune specie di molecole protettive cellulari vitali. E' stato dimostrato che le particelle minerali possono agire come substrati catalitici per la generazione di radicali idrossilici e superossidi (Guilianelli et al. 1993).
A livello cellulare, ci sono leggermente più informazioni. Dopo la deposizione a livello alveolare, la sottilissima cellula epiteliale di tipo I viene prontamente danneggiata (Adamson, Young e Bowden 1988). I macrofagi e altre cellule infiammatorie sono attratte dal sito danneggiato e la risposta infiammatoria è amplificata dal rilascio di metaboliti dell'acido arachidonico come prostaglandine e leucotrieni insieme all'esposizione della membrana basale (Holtzman 1991; Kuhn et al. 1990; Engelen et al. 1989). In questa fase del danno primario, l'architettura polmonare diventa disorganizzata, mostrando un edema interstiziale.
Durante il processo infiammatorio cronico, sia la superficie delle particelle di polvere che le cellule infiammatorie attivate rilasciano maggiori quantità di specie reattive dell'ossigeno nel tratto respiratorio inferiore. Lo stress ossidativo nel polmone ha alcuni effetti rilevabili sul sistema di difesa antiossidante (Heffner e Repine 1989), con espressione di enzimi antiossidanti come superossido dismutasi, glutatione perossidasi e catalasi (Engelen et al. 1990). Questi fattori sono localizzati nel tessuto polmonare, nel liquido interstiziale e negli eritrociti circolanti. I profili degli enzimi antiossidanti possono dipendere dal tipo di polvere fibrogenica (Janssen et al. 1992). I radicali liberi sono noti mediatori di lesioni e malattie dei tessuti (Kehrer 1993).
La fibrosi interstiziale deriva da un processo di riparazione. Ci sono numerose teorie per spiegare come avviene il processo di riparazione. L'interazione macrofagi/fibroblasti ha ricevuto la massima attenzione. I macrofagi attivati secernono una rete di citochine fibrogeniche proinfiammatorie: TNF, IL-1, fattore di crescita trasformante e fattore di crescita derivato dalle piastrine. Producono anche fibronectina, una glicoproteina della superficie cellulare che agisce come attrattivo chimico e, in alcune condizioni, come stimolante della crescita delle cellule mesenchimali. Alcuni autori ritengono che alcuni fattori siano più importanti di altri. Ad esempio, particolare importanza è stata attribuita al TNF nella patogenesi della silicosi. Negli animali da esperimento, è stato dimostrato che la deposizione di collagene dopo l'instillazione di silice nei topi era quasi completamente prevenuta dall'anticorpo anti-TNF (Piguet et al. 1990). Il rilascio del fattore di crescita derivato dalle piastrine e del fattore di crescita trasformante è stato presentato come un ruolo importante nella patogenesi dell'asbestosi (Brody 1993).
Sfortunatamente, molte delle teorie sui macrofagi/fibroblasti tendono a ignorare il potenziale equilibrio tra le citochine fibrogeniche ei loro inibitori (Kelley 1990). Infatti, il conseguente squilibrio tra agenti ossidanti e antiossidanti, proteasi e antiproteasi, metaboliti dell'acido arachidonico, elastasi e collagenasi, nonché gli squilibri tra le varie citochine e fattori di crescita, determinerebbero il rimodellamento anomalo della componente interstiziale verso i vari forme di pneumoconiosi (Porcher et al. 1993). Nelle pneumoconiosi, l'equilibrio è chiaramente diretto verso un effetto schiacciante delle attività dannose delle citochine.
Poiché le cellule di tipo I non sono in grado di dividersi, dopo l'insulto primario, la barriera epiteliale viene sostituita con cellule di tipo II (Lesur et al. 1992). C'è qualche indicazione che se questo processo di riparazione epiteliale ha successo e che le cellule di tipo II in rigenerazione non vengono ulteriormente danneggiate, è probabile che la fibrogenesi non proceda. In alcune condizioni, la riparazione da parte delle cellule di tipo II è portata all'eccesso, con conseguente proteinosi alveolare. Questo processo è stato chiaramente dimostrato dopo l'esposizione alla silice (Heppleston 1991). Non è chiaro fino a che punto le alterazioni nelle cellule epiteliali influenzino i fibroblasti. Pertanto, sembrerebbe che la fibrogenesi sia iniziata in aree di esteso danno epiteliale, poiché i fibroblasti si replicano, quindi si differenziano e producono più collagene, fibronectina e altri componenti della matrice extracellulare.
Esiste un'abbondante letteratura sulla biochimica dei diversi tipi di collagene che si formano nelle pneumoconiosi (Richards, Masek e Brown 1991). Il metabolismo di tale collagene e la sua stabilità nel polmone sono elementi importanti del processo di fibrogenesi. Lo stesso probabilmente vale per gli altri componenti del tessuto connettivo danneggiato. Il metabolismo del collagene e dell'elastina è di particolare interesse nella fase di guarigione poiché queste proteine sono così importanti per la struttura e la funzione polmonare. È stato molto ben dimostrato che le alterazioni nella sintesi di queste proteine potrebbero determinare se l'enfisema o la fibrosi si evolvono dopo il danno polmonare (Niewoehner e Hoidal 1982). Nello stato di malattia, meccanismi come un aumento dell'attività della transglutaminasi potrebbero favorire la formazione di masse proteiche stabili. In alcune lesioni fibrotiche CWP, i componenti proteici rappresentano un terzo della lesione, il resto è costituito da polvere e fosfato di calcio.
Considerando solo il metabolismo del collagene, sono possibili diversi stadi di fibrosi, alcuni dei quali sono potenzialmente reversibili mentre altri sono progressivi. Esistono prove sperimentali che, a meno che non venga superata un'esposizione critica, le lesioni precoci possono regredire e la fibrosi irreversibile è un risultato improbabile. Nell'asbestosi, ad esempio, sono stati descritti diversi tipi di reazioni polmonari (Bégin, Cantin e Massé 1989): una reazione infiammatoria transitoria senza lesione, una reazione a bassa ritenzione con cicatrice fibrotica limitata alle vie aeree distali, una reazione infiammatoria elevata sostenuta dalla continua esposizione e la debole clearance delle fibre più lunghe.
Da questi studi si può concludere che l'esposizione a particelle di polvere fibrotica è in grado di innescare diversi percorsi biochimici e cellulari complessi coinvolti nel danno polmonare e nella riparazione. Il regime di esposizione, le caratteristiche fisico-chimiche delle particelle di polvere e forse i fattori di suscettibilità individuale sembrano essere i fattori determinanti del sottile equilibrio tra i diversi percorsi. Le caratteristiche fisico-chimiche determineranno il tipo di lesione fondamentale definitiva. Il regime di esposizione sembra determinare il corso temporale degli eventi. C'è qualche indicazione che regimi di esposizione sufficientemente bassi possono nella maggior parte dei casi limitare la reazione polmonare a lesioni non progressive senza disabilità o menomazione.
La sorveglianza medica e lo screening hanno sempre fatto parte delle strategie di prevenzione delle pneumoconiosi. In tale contesto, la possibilità di rilevare alcune lesioni precoci è vantaggiosa. Una maggiore conoscenza della patogenesi ha aperto la strada allo sviluppo di diversi biomarcatori (Borm 1994) e al perfezionamento e all'uso di tecniche di indagine polmonare "non classiche" come la misurazione del tasso di clearance del 99 tecnezio dietilentriamina-penta-acetato depositato ( 99 Tc-DTPA) per valutare l'integrità epiteliale polmonare (O'Brodovich e Coates 1987) e scintigrafia polmonare quantitativa con gallio-67 per valutare l'attività infiammatoria (Bisson, Lamoureux e Bégin 1987).
Diversi biomarcatori sono stati presi in considerazione nel campo delle pneumoconiosi: macrofagi dell'espettorato, fattori di crescita sierica, peptide procollagene sierico di tipo III, antiossidanti dei globuli rossi, fibronectina, elastasi leucocitaria, metalloendopeptidasi neutra e peptidi di elastina nel plasma, idrocarburi volatili nell'aria espirata e rilascio di TNF da parte di monociti del sangue periferico. I biomarcatori sono concettualmente piuttosto interessanti, ma sono necessari molti altri studi per valutarne con precisione il significato. Questo sforzo di convalida sarà piuttosto impegnativo, poiché richiederà agli investigatori di condurre studi epidemiologici prospettici. Tale sforzo è stato effettuato di recente per il rilascio di TNF da parte dei monociti del sangue periferico in CWP. Il TNF è risultato essere un marcatore interessante della progressione del CWP (Borm 1994). Oltre agli aspetti scientifici del significato dei biomarcatori nella patogenesi delle pneumoconiosi, devono essere esaminate attentamente altre questioni relative all'uso dei biomarcatori (Schulte 1993), vale a dire le opportunità di prevenzione, l'impatto sulla medicina del lavoro ei problemi etici e legali.
Progressione e complicazione delle pneumoconiosi
Nei primi decenni di questo secolo, la pneumoconiosi era considerata una malattia che invalidava i giovani e uccideva prematuramente. Nei paesi industrializzati, ora è generalmente considerata nient'altro che un'anomalia radiologica, senza compromissione o disabilità (Sadoul 1983). Tuttavia, due osservazioni dovrebbero essere contrassegnate contro questa affermazione ottimistica. In primo luogo, anche se in condizioni di esposizione limitata, la pneumoconiosi rimane una malattia relativamente silente e asintomatica, dovrebbe essere noto che la malattia può progredire verso forme più gravi e invalidanti. I fattori che influenzano questa progressione sono decisamente importanti da considerare come parte dell'eziopatogenesi della condizione. In secondo luogo, ora ci sono prove che alcune pneumoconiosi possono influenzare l'esito generale della salute e possono essere un fattore che contribuisce al cancro del polmone.
La natura cronica e progressiva dell'asbestosi è stata documentata dalla lesione subclinica iniziale all'asbestosi clinica (Bégin, Cantin e Massé 1989). Le moderne tecniche di indagine polmonare (BAL, TAC, assorbimento polmonare di gallio-67) hanno rivelato che l'infiammazione e la lesione erano continue dal momento dell'esposizione, attraverso la fase latente o subclinica, allo sviluppo della malattia clinica. È stato riportato (Bégin et al. 1985) che il 75% dei soggetti che inizialmente avevano una scintigrafia al gallio-67 positiva ma che a quel tempo non presentavano asbestosi clinica, sono progrediti verso l'asbestosi clinica "conclamata" in un periodo di quattro anni. periodo. Sia negli esseri umani che negli animali da esperimento, l'asbestosi può progredire dopo il riconoscimento della malattia e la cessazione dell'esposizione. È altamente probabile che la storia dell'esposizione prima del riconoscimento sia un importante determinante della progressione. Alcuni dati sperimentali supportano la nozione di asbestosi non progressiva associata all'esposizione all'induzione della luce e alla cessazione dell'esposizione al riconoscimento (Sébastien, Dufresne e Bégin 1994). Supponendo che la stessa nozione si applichi agli esseri umani, sarebbe di primaria importanza stabilire con precisione le metriche di "esposizione per induzione della luce". Nonostante tutti gli sforzi per controllare la popolazione attiva esposta all'amianto, queste informazioni mancano ancora.
È ben noto che l'esposizione all'amianto può comportare un rischio eccessivo di cancro ai polmoni. Anche se si ammette che l'amianto è cancerogeno di per sé, è stato a lungo dibattuto se il rischio di cancro al polmone tra i lavoratori dell'amianto fosse correlato all'esposizione all'amianto o alla fibrosi polmonare (Hughes e Weil 1991). Questo problema non è stato ancora risolto.
A causa del continuo miglioramento delle condizioni di lavoro nelle moderne strutture minerarie, al giorno d'oggi, il CWP è una malattia che colpisce essenzialmente i minatori in pensione. Se la CWP semplice è una condizione senza sintomi e senza effetti dimostrabili sulla funzione polmonare, la fibrosi massiva progressiva (PMF) è una condizione molto più grave, con importanti alterazioni strutturali del polmone, deficit della funzione polmonare e ridotta aspettativa di vita. Molti studi hanno mirato a identificare i determinanti della progressione verso la PMF (forte ritenzione di polvere nel polmone, rango di carbone, infezione micobatterica o stimolazione immunologica). È stata proposta una teoria unificante (Vanhee et al. 1994), basata su una continua e grave infiammazione alveolare con attivazione dei macrofagi alveolari e produzione sostanziale di specie reattive dell'ossigeno, fattori chemiotattici e fibronectina. Altre complicanze della CWP comprendono l'infezione da micobatteri, la sindrome di Caplan e la sclerodermia. Non ci sono prove di un rischio elevato di cancro ai polmoni tra i minatori di carbone.
La forma cronica di silicosi segue l'esposizione, misurata in decenni anziché in anni, a polvere respirabile contenente generalmente meno del 30% di quarzo. Ma in caso di esposizione incontrollata a polveri ricche di quarzo (esposizioni storiche con sabbiatura, ad esempio), si possono riscontrare forme acute e accelerate solo dopo diversi mesi. I casi di malattia acuta e accelerata sono particolarmente a rischio di complicanze dovute alla tubercolosi (Ziskind, Jones e Weil 1976). Può anche verificarsi una progressione, con lo sviluppo di grandi lesioni che obliterano la struttura polmonare, chiamate entrambe silicosi complicata or PMF.
Alcuni studi hanno esaminato la progressione della silicosi in relazione all'esposizione e hanno prodotto risultati divergenti sulle relazioni tra progressione ed esposizione, prima e dopo l'insorgenza (Hessel et al. 1988). Recentemente, Infante-Rivard et al. (1991) hanno studiato i fattori prognostici che influenzano la sopravvivenza dei pazienti silicotici compensati. I pazienti con piccole opacità solo sulla radiografia del torace e che non presentavano dispnea, espettorazione o rumori respiratori anomali hanno avuto una sopravvivenza simile a quella dei referenti. Altri pazienti hanno avuto una sopravvivenza inferiore. Infine, si dovrebbe menzionare la recente preoccupazione per la silice, la silicosi e il cancro ai polmoni. Ci sono alcune prove a favore e contro l'affermazione che la silice di per sé è cancerogeno (Agius 1992). La silice può creare sinergie con potenti agenti cancerogeni ambientali, come quelli presenti nel fumo di tabacco, attraverso un effetto di promozione relativamente debole sulla carcinogenesi o compromettendone l'eliminazione. Inoltre, il processo patologico associato o che porta alla silicosi potrebbe comportare un aumento del rischio di cancro ai polmoni.
Al giorno d'oggi, la progressione e la complicazione delle pneumoconiosi potrebbero essere considerate una questione chiave per la gestione medica. L'uso delle classiche tecniche di indagine polmonare è stato perfezionato per il riconoscimento precoce della malattia (Bégin et al. 1992), in una fase in cui la pneumoconiosi è limitata alla sua manifestazione radiologica, senza compromissione o disabilità. Nel prossimo futuro, è probabile che sarà disponibile una batteria di biomarcatori per documentare anche stadi precoci della malattia. La questione se un lavoratore con diagnosi di pneumoconiosi - o documentato per essere nelle sue fasi iniziali - debba essere autorizzato a continuare con il suo lavoro ha lasciato perplessi i responsabili delle decisioni in materia di salute sul lavoro per qualche tempo. È una questione piuttosto difficile che comporta considerazioni etiche, sociali e scientifiche. Se è disponibile una letteratura scientifica schiacciante sull'induzione della pneumoconiosi, le informazioni sulla progressione utilizzabili dai decisori sono piuttosto scarse e alquanto confuse. Sono stati fatti alcuni tentativi per studiare i ruoli di variabili come la storia dell'esposizione, la ritenzione di polvere e le condizioni mediche all'inizio. Le relazioni tra tutte queste variabili complicano la questione. Vengono formulate raccomandazioni per lo screening sanitario e la sorveglianza dei lavoratori esposti a polveri minerali (Wagner 1996). I programmi sono già o saranno messi in atto di conseguenza. Tali programmi trarrebbero sicuramente vantaggio da una migliore conoscenza scientifica sulla progressione, e in particolare sulla relazione tra esposizione e caratteristiche di ritenzione.
Discussione
Le informazioni portate da molte discipline scientifiche sull'eziopatogenesi delle pneumoconiosi sono schiaccianti. La difficoltà maggiore ora è ricomporre gli elementi sparsi del puzzle in percorsi meccanicistici unificanti che portano alle lesioni fondamentali delle pneumoconiosi. Senza questa necessaria integrazione, rimarrebbe il contrasto tra poche lesioni fondamentali e numerosissime reazioni biochimiche e cellulari.
La nostra conoscenza dell'eziopatogenesi ha sinora influenzato solo in misura limitata le pratiche di igiene del lavoro, nonostante la forte intenzione degli igienisti di operare secondo norme aventi un certo significato biologico. Due nozioni principali sono state incorporate nelle loro pratiche: la selezione delle dimensioni delle particelle di polvere respirabile e la dipendenza dalla tossicità del tipo di polvere. Quest'ultimo ha fornito alcuni limiti specifici per ogni tipo di polvere. La valutazione quantitativa del rischio, passaggio necessario nella definizione dei limiti di esposizione, costituisce un esercizio complicato per diversi motivi, quali la varietà dei possibili indici di esposizione, la scarsa informazione sulle esposizioni pregresse, la difficoltà che si ha con i modelli epidemiologici nel trattare indici multipli di esposizione e la difficoltà di stimare la dose dalle informazioni sull'esposizione. Gli attuali limiti di esposizione, che talvolta comportano notevoli incertezze, sono probabilmente sufficientemente bassi da offrire una buona protezione. Le differenze tra la forza lavoro osservate nelle relazioni esposizione-risposta, tuttavia, riflettono il nostro controllo incompleto del fenomeno.
L'impatto della nuova comprensione della cascata di eventi nella patogenesi delle pneumoconiosi non ha modificato l'approccio tradizionale alla sorveglianza dei lavoratori, ma ha aiutato significativamente i medici nella loro capacità di riconoscere precocemente la malattia (pneumoconiosi), in un momento in cui la malattia ha avuto solo un impatto limitato sulla funzione polmonare. Sono infatti i soggetti allo stadio iniziale della malattia che dovrebbero essere riconosciuti e ritirati da un'ulteriore esposizione significativa se si vuole ottenere la prevenzione della disabilità mediante la sorveglianza medica.
Silicosi
La silicosi è una malattia fibrotica dei polmoni causata dall'inalazione, dalla ritenzione e dalla reazione polmonare alla silice cristallina. Nonostante la conoscenza della causa di questo disturbo - esposizioni respiratorie a polveri contenenti silice - questa malattia polmonare professionale grave e potenzialmente fatale rimane prevalente in tutto il mondo. La silice, o biossido di silicio, è il componente predominante della crosta terrestre. L'esposizione professionale a particelle di silice di dimensioni respirabili (diametro aerodinamico da 0.5 a 5 μm) è associata a attività di estrazione, estrazione, perforazione, tunneling e sabbiatura abrasiva con materiali contenenti quarzo (sabbiatura). L'esposizione alla silice rappresenta anche un pericolo per i tagliapietre e i lavoratori della ceramica, della fonderia, della silice macinata e dei refrattari. Poiché l'esposizione alla silice cristallina è così diffusa e la sabbia silicea è un componente economico e versatile di molti processi di produzione, milioni di lavoratori in tutto il mondo sono a rischio di malattia. La vera prevalenza della malattia non è nota.
Definizione
La silicosi è una malattia polmonare occupazionale attribuibile all'inalazione di biossido di silicio, comunemente noto come silice, in forme cristalline, solitamente come quarzo, ma anche come altre importanti forme cristalline di silice, ad esempio cristobalite e tridimite. Queste forme sono chiamate anche “silice libera” per distinguerle dai silicati. Il contenuto di silice in diverse formazioni rocciose, come arenaria, granito e ardesia, varia dal 20 a quasi il 100%.
Lavoratori in professioni e industrie ad alto rischio
Sebbene la silicosi sia una malattia antica, sono ancora segnalati nuovi casi sia nel mondo sviluppato che in quello in via di sviluppo. Nella prima parte di questo secolo, la silicosi era una delle principali cause di morbilità e mortalità. I lavoratori contemporanei sono ancora esposti alla polvere di silice in una varietà di occupazioni e quando la nuova tecnologia manca di un adeguato controllo della polvere, l'esposizione può essere a livelli di polvere e particelle più pericolosi che in ambienti di lavoro non meccanizzati. Ogni volta che la crosta terrestre viene disturbata e vengono utilizzate o lavorate rocce o sabbie contenenti silice, esistono potenziali rischi respiratori per i lavoratori. Continuano le segnalazioni di silicosi da industrie e ambienti di lavoro non precedentemente riconosciuti come a rischio, che riflettono la presenza quasi onnipresente di silice. Infatti, a causa della latenza e della cronicità di questo disturbo, compreso lo sviluppo e la progressione della silicosi dopo che l'esposizione è cessata, alcuni lavoratori con esposizioni attuali potrebbero non manifestare la malattia fino al prossimo secolo. In molti paesi in tutto il mondo, i lavori di estrazione, estrazione, tunneling, sabbiatura abrasiva e fonderia continuano a presentare grandi rischi per l'esposizione alla silice e continuano a verificarsi epidemie di silicosi, anche nelle nazioni sviluppate.
Forme di silicosi: storia dell'esposizione e descrizioni clinicopatologiche
Sono comunemente descritte forme croniche, accelerate e acute di silicosi. Queste espressioni cliniche e patologiche della malattia riflettono diverse intensità di esposizione, periodi di latenza e storie naturali. La forma cronica o classica di solito segue uno o più decenni di esposizione a polvere respirabile contenente quarzo, e questa può progredire verso la fibrosi massiva progressiva (PMF). La forma accelerata segue esposizioni più brevi e più pesanti e progredisce più rapidamente. La forma acuta può manifestarsi dopo esposizioni intense e di breve durata ad alti livelli di polvere respirabile con alto contenuto di silice per periodi che possono essere misurati in mesi anziché in anni.
Silicosi cronica (o classica). può essere asintomatica o causare dispnea da sforzo insidiosamente progressiva o tosse (spesso erroneamente attribuita al processo di invecchiamento). Si presenta come un'anomalia radiografica con piccole opacità arrotondate (<10 mm) prevalentemente nei lobi superiori. È comune una storia di 15 anni o più dall'inizio dell'esposizione. Il segno patologico della forma cronica è il nodulo silicotico. La lesione è caratterizzata da un'area centrale priva di cellule di fibre collagene ialinizzate a spirale disposte concentricamente, circondate da tessuto connettivo cellulare con fibre reticoliniche. La silicosi cronica può progredire in PMF (a volte indicata come silicosi complicata), anche dopo che l'esposizione alla polvere contenente silice è cessata.
Fibrosi massiva progressiva è più probabile che si presenti con dispnea da sforzo. Questa forma di malattia è caratterizzata da opacità nodulari superiori a 1 cm alla radiografia del torace e comunemente comporterà una ridotta capacità di diffusione del monossido di carbonio, una ridotta tensione arteriosa dell'ossigeno a riposo o durante l'esercizio e una marcata restrizione della spirometria o della misurazione del volume polmonare. La distorsione dell'albero bronchiale può anche portare all'ostruzione delle vie aeree e alla tosse produttiva. Può verificarsi un'infezione batterica ricorrente non dissimile da quella osservata nelle bronchiectasie. La perdita di peso e la cavitazione delle grandi opacità dovrebbero indurre a temere la tubercolosi o altre infezioni micobatteriche. Il pneumotorace può essere una complicanza pericolosa per la vita, dal momento che il polmone fibrotico può essere difficile da ri-espandere. L'insufficienza respiratoria ipossiemica con cuore polmonare è un evento terminale comune.
Silicosi accelerata può comparire dopo esposizioni più intense di durata più breve (da 5 a 10 anni). Sintomi, reperti radiografici e misurazioni fisiologiche sono simili a quelli osservati nella forma cronica. Il deterioramento della funzione polmonare è più rapido e molti lavoratori con malattia accelerata possono sviluppare un'infezione da micobatteri. La malattia autoimmune, inclusa la sclerodermia o la sclerosi sistemica, è osservata con la silicosi, spesso di tipo accelerato. La progressione delle anomalie radiografiche e della compromissione funzionale può essere molto rapida quando la malattia autoimmune è associata alla silicosi.
Silicosi acuta può svilupparsi da pochi mesi a 2 anni di massiccia esposizione alla silice. Dispnea drammatica, debolezza e perdita di peso sono spesso sintomi di presentazione. I reperti radiografici del riempimento alveolare diffuso differiscono da quelli delle forme più croniche di silicosi. Sono stati descritti reperti istologici simili alla proteinosi alveolare polmonare e occasionalmente sono riportate anomalie extrapolmonari (renali ed epatiche). Il decorso abituale è la rapida progressione verso una grave insufficienza ventilatoria ipossiemica.
La tubercolosi può complicare tutte le forme di silicosi, ma le persone con malattia acuta e accelerata possono essere maggiormente a rischio. Anche l'esposizione alla silice da sola, anche senza silicosi, può predisporre a questa infezione. M. tuberculosis è l'organismo abituale, ma si osservano anche micobatteri atipici.
Anche in assenza di silicosi radiografica, i lavoratori esposti alla silice possono anche avere altre malattie associate all'esposizione professionale alla polvere, come la bronchite cronica e l'enfisema associato. Queste anomalie sono associate a molte esposizioni professionali alla polvere minerale, comprese le polveri contenenti silice.
Patogenesi e l'associazione con la tubercolosi
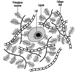
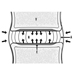
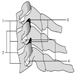
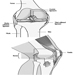
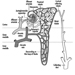
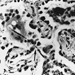
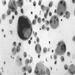
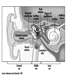
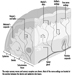
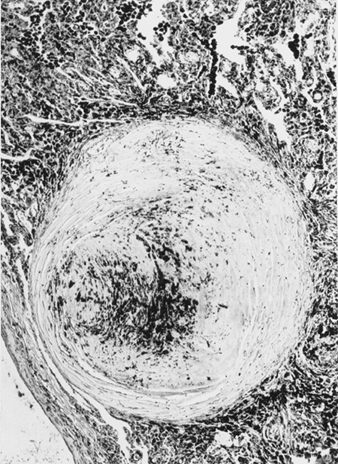
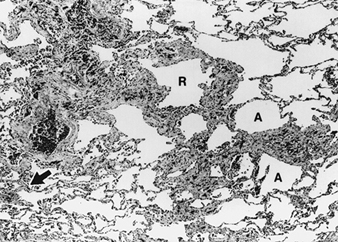
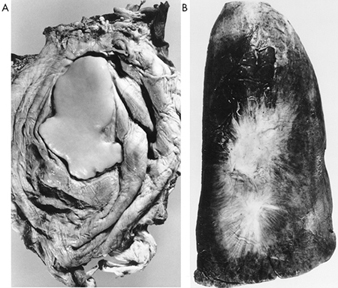
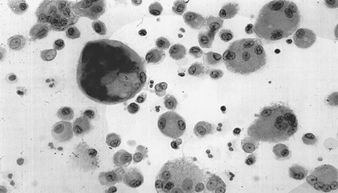
La precisa patogenesi della silicosi è incerta, ma un'abbondanza di prove implica l'interazione tra il macrofago alveolare polmonare e le particelle di silice depositate nel polmone. Le proprietà superficiali della particella di silice sembrano promuovere l'attivazione dei macrofagi. Queste cellule rilasciano quindi fattori chemiotattici e mediatori infiammatori che determinano un'ulteriore risposta cellulare da parte di leucociti polimorfonucleati, linfociti e altri macrofagi. Vengono rilasciati fattori stimolanti i fibroblasti che promuovono la ialinizzazione e la deposizione di collagene. La risultante lesione silicotica patologica è il nodulo ialino, contenente una zona acellulare centrale con silice libera circondata da vortici di collagene e fibroblasti, e una zona periferica attiva composta da macrofagi, fibroblasti, plasmacellule e ulteriore silice libera come mostrato nella figura 1.
Figura 1. Tipico nodulo silicotico, sezione microscopica. Per gentile concessione del dottor V. Vallyathan.
Le proprietà precise delle particelle di silice che evocano la risposta polmonare sopra descritta non sono note, ma le caratteristiche superficiali possono essere importanti. La natura e l'entità della risposta biologica sono in generale legate all'intensità dell'esposizione; tuttavia, vi sono prove crescenti che la silice appena fratturata possa essere più tossica della polvere invecchiata contenente silice, un effetto forse correlato ai gruppi radicalici reattivi sui piani di scissione della silice appena fratturata. Ciò può offrire una spiegazione patogena per l'osservazione di casi di malattia avanzata sia nelle sabbiatrici che nelle perforatrici di roccia dove le esposizioni alla silice fratturata di recente sono particolarmente intense.
L'insulto tossico iniziale può verificarsi con una reazione immunologica minima; tuttavia, una risposta immunologica prolungata all'insulto può essere importante in alcune delle manifestazioni croniche della silicosi. Ad esempio, gli anticorpi antinucleari possono verificarsi nella silicosi accelerata e nella sclerodermia, così come in altre malattie del collagene nei lavoratori che sono stati esposti alla silice. La suscettibilità dei lavoratori silicotici alle infezioni, come la tubercolosi e Nocardia asteroidi, è probabilmente correlato all'effetto tossico della silice sui macrofagi polmonari.
Il legame tra silicosi e tubercolosi è riconosciuto da quasi un secolo. La tubercolosi attiva nei lavoratori silicotici può superare il 20% quando la prevalenza comunitaria della tubercolosi è elevata. Ancora una volta, le persone con silicosi acuta sembrano essere a rischio considerevolmente più elevato.
Quadro clinico della silicosi
Il sintomo principale è di solito la dispnea, che si nota dapprima durante l'attività o l'esercizio e successivamente a riposo quando si perde la riserva polmonare del polmone. Tuttavia, in assenza di altre malattie respiratorie, la mancanza di respiro può essere assente e la presentazione può essere un lavoratore asintomatico con una radiografia del torace anomala. La radiografia a volte può mostrare una malattia abbastanza avanzata con solo sintomi minimi. La comparsa o la progressione della dispnea può preannunciare lo sviluppo di complicanze tra cui tubercolosi, ostruzione delle vie aeree o PMF. La tosse è spesso presente in seguito a bronchite cronica da esposizione professionale alla polvere, uso di tabacco o entrambi. La tosse a volte può anche essere attribuita alla pressione di grandi masse di linfonodi silicotici sulla trachea o sui bronchi principali.
Altri sintomi al torace sono meno comuni della dispnea e della tosse. L'emottisi è rara e dovrebbe destare preoccupazione per i disturbi complicanti. Il respiro sibilante e la costrizione toracica possono verificarsi di solito come parte di una malattia ostruttiva delle vie aeree o di una bronchite associate. Dolore toracico e bastonatura delle dita non sono caratteristiche della silicosi. Sintomi sistemici, come febbre e perdita di peso, suggeriscono un'infezione complicante o una malattia neoplastica. Forme avanzate di silicosi sono associate a insufficienza respiratoria progressiva con o senza cuore polmonare. Pochi segni fisici possono essere notati a meno che non siano presenti complicazioni.
Schemi radiografici e anomalie polmonari funzionali
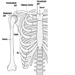
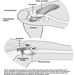
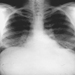
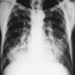
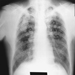
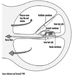
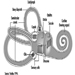
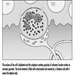
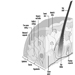
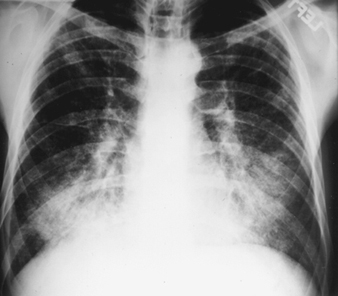
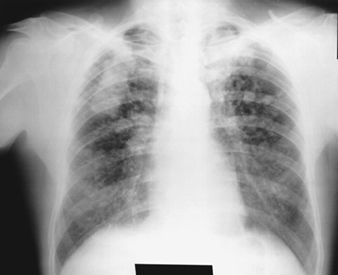
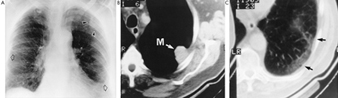
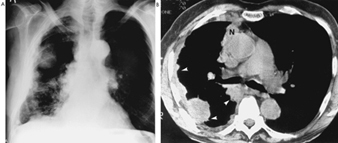
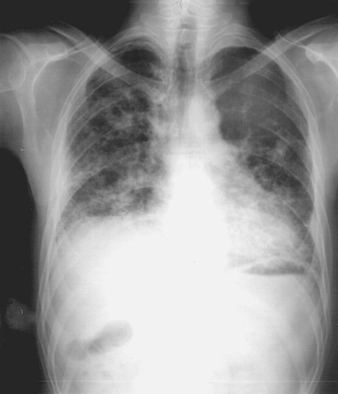
I primi segni radiografici di silicosi non complicata sono generalmente piccole opacità arrotondate. Questi possono essere descritti dalla classificazione internazionale ILO delle radiografie delle pneumoconiosi per dimensione, forma e categoria di profusione. Nella silicosi dominano le opacità di tipo “q” e “r”. Sono stati descritti anche altri modelli che includono ombre lineari o irregolari. Le opacità viste sulla radiografia rappresentano la somma dei noduli silicotici patologici. Di solito si trovano prevalentemente nelle zone superiori e possono successivamente progredire fino a coinvolgere altre zone. Talvolta si nota anche linfoadenopatia ilare prima delle ombre parenchimali nodulari. La calcificazione del guscio d'uovo è fortemente indicativa di silicosi, sebbene questa caratteristica sia osservata raramente. PMF è caratterizzato dalla formazione di grandi opacità. Queste grandi lesioni possono essere descritte in base alle dimensioni utilizzando la classificazione ILO come categorie A, B o C. Le grandi opacità o lesioni PMF tendono a contrarsi, solitamente ai lobi superiori, lasciando aree di enfisema compensatorio ai loro margini e spesso nelle basi polmonari. Di conseguenza, piccole opacità arrotondate precedentemente evidenti possono a volte scomparire o essere meno evidenti. Possono verificarsi anomalie pleuriche, ma non sono una caratteristica radiografica frequente nella silicosi. Grandi opacità possono anche destare preoccupazione per quanto riguarda la neoplasia e la distinzione radiografica in assenza di vecchi film può essere difficile. Tutte le lesioni che cavitano o cambiano rapidamente devono essere valutate per la tubercolosi attiva. La silicosi acuta può presentarsi con un pattern di riempimento alveolare radiologico con rapido sviluppo di PMF o complicate lesioni di massa. Vedere le figure 2 e 3.
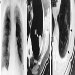
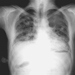
Figura 2. Radiografia del torace, silico-proteinosi acuta in una perforatrice di una miniera di carbone di superficie. Per gentile concessione del Dr. NL Lapp e del Dr. DE Banks.
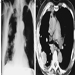
Figura 3. Radiografia del torace, silicosi complicata che mostra fibrosi massiva progressiva.
I test di funzionalità polmonare, come la spirometria e la capacità di diffusione, sono utili per la valutazione clinica delle persone con sospetta silicosi. La spirometria può anche essere utile nel riconoscimento precoce degli effetti sulla salute derivanti dall'esposizione professionale alla polvere, in quanto può rilevare anomalie fisiologiche che possono precedere i cambiamenti radiologici. Nella silicosi non è presente un modello esclusivamente caratteristico di compromissione della ventilazione. La spirometria può essere normale o, quando anormale, i tracciati possono mostrare ostruzione, restrizione o un pattern misto. L'ostruzione può effettivamente essere la scoperta più comune. Questi cambiamenti tendono ad essere più marcati con le categorie radiologiche avanzate. Tuttavia, esiste una scarsa correlazione tra anomalie radiografiche e compromissione della ventilazione. Nella silicosi acuta e accelerata, i cambiamenti funzionali sono più marcati e la progressione è più rapida. Nella silicosi acuta, la progressione radiologica è accompagnata da un aumento della compromissione della ventilazione e delle anomalie degli scambi gassosi, che portano all'insufficienza respiratoria e infine alla morte per ipossiemia intrattabile.
Complicanze e problemi diagnostici speciali
Con una storia di esposizione e una radiografia caratteristica, la diagnosi di silicosi non è generalmente difficile da stabilire. Le sfide sorgono solo quando le caratteristiche radiologiche sono insolite o la storia dell'esposizione non è riconosciuta. La biopsia polmonare è raramente necessaria per stabilire la diagnosi. Tuttavia, i campioni di tessuto sono utili in alcuni contesti clinici quando sono presenti complicanze o la diagnosi differenziale include tubercolosi, neoplasia o PMF. Il materiale della biopsia dovrebbe essere inviato per la coltura e, nei contesti di ricerca, l'analisi della polvere può essere un'utile misura aggiuntiva. Quando è richiesto il tessuto, la biopsia polmonare aperta è generalmente necessaria per materiale adeguato per l'esame.
La vigilanza per le complicanze infettive, in particolare la tubercolosi, non può essere sottovalutata e i sintomi di cambiamento nella tosse o nell'emottisi, e la febbre o la perdita di peso dovrebbero innescare un work-up per escludere questo problema curabile.
La sostanziale preoccupazione e l'interesse per la relazione tra esposizione alla silice, silicosi e cancro del polmone continua a stimolare il dibattito e ulteriori ricerche. Nell'ottobre del 1996, un comitato dell'Agenzia internazionale per la ricerca sul cancro (IARC) classificò la silice cristallina come cancerogeno di gruppo I, giungendo a questa conclusione sulla base di "prove sufficienti di cancerogenicità nell'uomo". Esiste incertezza sui meccanismi patogenetici per lo sviluppo del cancro del polmone nelle popolazioni esposte alla silice e la possibile relazione tra silicosi (o fibrosi polmonare) e cancro nei lavoratori esposti continua ad essere studiata. Indipendentemente dal meccanismo che può essere responsabile degli eventi neoplastici, la nota associazione tra esposizioni alla silice e silicosi impone il controllo e la riduzione dell'esposizione dei lavoratori a rischio per questa malattia.
Prevenzione della silicosi
La prevenzione rimane la pietra angolare per eliminare questa malattia polmonare professionale. L'uso di una migliore ventilazione e scarico locale, recinzione di processo, tecniche umide, protezione personale inclusa la corretta selezione di respiratori e, ove possibile, sostituzione industriale di agenti meno pericolosi della silice, tutti riducono l'esposizione. Anche l'educazione dei lavoratori e dei datori di lavoro riguardo ai pericoli dell'esposizione alla polvere di silice e alle misure per controllare l'esposizione è importante.
Se si riconosce la silicosi in un lavoratore, è consigliabile allontanarlo dall'esposizione continua. Sfortunatamente, la malattia può progredire anche senza un'ulteriore esposizione alla silice. Inoltre, il riscontro di un caso di silicosi, in particolare la forma acuta o accelerata, dovrebbe richiedere una valutazione sul posto di lavoro per proteggere altri lavoratori anch'essi a rischio.
Screening e sorveglianza
I lavoratori esposti alla silice e ad altre polveri minerali dovrebbero sottoporsi a screening periodici per gli effetti avversi sulla salute in aggiunta, ma non in sostituzione, al controllo dell'esposizione alla polvere. Tale screening include comunemente valutazioni per sintomi respiratori, anomalie della funzione polmonare e malattie neoplastiche. Dovrebbero essere eseguite anche valutazioni per l'infezione da tubercolosi. Oltre allo screening dei singoli lavoratori, dovrebbero essere raccolti dati da gruppi di lavoratori per attività di sorveglianza e prevenzione. La guida per questi tipi di studi è inclusa nell'elenco delle letture suggerite.
Terapia, gestione delle complicanze e controllo della silicosi
Quando la prevenzione non ha avuto successo e si è sviluppata la silicosi, la terapia è diretta principalmente alle complicanze della malattia. Le misure terapeutiche sono simili a quelle comunemente utilizzate nella gestione dell'ostruzione delle vie aeree, delle infezioni, del pneumotorace, dell'ipossiemia e dell'insufficienza respiratoria che complicano altre malattie polmonari. Storicamente, l'inalazione di alluminio aerosol non ha avuto successo come terapia specifica per la silicosi. Il polivinil piridina-N-ossido, un polimero che ha protetto gli animali da esperimento, non è disponibile per l'uso nell'uomo. Il recente lavoro di laboratorio con la tetrandrina ha dimostrato in vivo riduzione della fibrosi e della sintesi del collagene negli animali esposti alla silice trattati con questo farmaco. Tuttavia, al momento mancano prove evidenti dell'efficacia sull'uomo e vi sono preoccupazioni circa la potenziale tossicità, inclusa la mutagenicità, di questo farmaco. A causa dell'elevata prevalenza della malattia in alcuni paesi, continuano le indagini sulle combinazioni di farmaci e altri interventi. Attualmente non è emerso alcun approccio di successo e la ricerca di una terapia specifica per la silicosi fino ad oggi non è stata gratificante.
Un'ulteriore esposizione è indesiderabile e dovrebbero essere forniti consigli su come lasciare o cambiare il lavoro attuale con informazioni sulle condizioni di esposizione passate e presenti.
Nella gestione medica della silicosi, la vigilanza per complicare le infezioni, in particolare la tubercolosi, è fondamentale. L'uso di BCG nel paziente silicotico tubercolino-negativo non è raccomandato, ma l'uso della terapia preventiva con isoniazide (INH) nel soggetto silicotico tubercolino-positivo è consigliato nei paesi in cui la prevalenza della tubercolosi è bassa. La diagnosi di infezione tubercolare attiva nei pazienti con silicosi può essere difficile. Sintomi clinici di perdita di peso, febbre, sudorazione e malessere devono richiedere una valutazione radiografica e colture e ceppi di bacilli acido-resistenti dell'espettorato. Destano particolare preoccupazione i cambiamenti radiografici, tra cui l'allargamento o la cavitazione nelle lesioni conglomerate o nelle opacità nodulari. Gli studi batteriologici sull'espettorato possono non essere sempre affidabili nella silicotubercolosi. La broncoscopia a fibre ottiche per ulteriori campioni per la coltura e lo studio può spesso essere utile per stabilire una diagnosi di malattia attiva. L'uso della terapia multifarmaco per sospetta malattia attiva nei silicotici è giustificato a un livello di sospetto inferiore rispetto al soggetto non silicotico, a causa della difficoltà di stabilire con certezza l'evidenza di infezione attiva. La terapia con rifampicina sembra aver migliorato il tasso di successo del trattamento della silicosi complicata dalla tubercolosi e in alcuni studi recenti la risposta alla terapia a breve termine è stata paragonabile nei casi di silicotubercolosi a quella nei casi corrispondenti di tubercolosi primaria.
Il supporto ventilatorio per insufficienza respiratoria è indicato quando precipitato da una complicanza trattabile. Il pneumotorace, spontaneo e correlato al ventilatore, viene solitamente trattato con l'inserimento di un tubo toracico. Si può sviluppare una fistola broncopleurica e si deve prendere in considerazione la consultazione e la gestione chirurgica.
La silicosi acuta può progredire rapidamente verso l'insufficienza respiratoria. Quando questa malattia assomiglia alla proteinosi alveolare polmonare ed è presente una grave ipossiemia, la terapia aggressiva ha incluso un massiccio lavaggio dell'intero polmone con il paziente in anestesia generale nel tentativo di migliorare lo scambio gassoso e rimuovere i detriti alveolari. Sebbene attraente nel concetto, l'efficacia del lavaggio polmonare intero non è stata stabilita. La terapia con glucocorticoidi è stata utilizzata anche per la silicosi acuta; tuttavia, è ancora di beneficio non dimostrato.
Alcuni giovani pazienti con silicosi allo stadio terminale possono essere considerati candidati al trapianto di polmone o cuore-polmone da centri esperti in questa procedura costosa e ad alto rischio. Il rinvio e la valutazione anticipati per questo intervento possono essere offerti a pazienti selezionati.
La discussione di un intervento terapeutico aggressivo e ad alta tecnologia come il trapianto serve drammaticamente a sottolineare la natura grave e potenzialmente fatale della silicosi, nonché a sottolineare il ruolo cruciale della prevenzione primaria. Il controllo della silicosi dipende in ultima analisi dalla riduzione e dal controllo dell'esposizione alla polvere sul posto di lavoro. Ciò si ottiene mediante l'applicazione rigorosa e coscienziosa dei principi fondamentali dell'ingegneria e dell'igiene del lavoro, con l'impegno a preservare la salute dei lavoratori.
Malattie polmonari dei lavoratori del carbone
I minatori di carbone sono soggetti a una serie di malattie polmonari e disturbi derivanti dalla loro esposizione alla polvere di miniera di carbone. Questi includono pneumoconiosi, bronchite cronica e malattia polmonare ostruttiva. L'insorgenza e la gravità della malattia dipendono dall'intensità e dalla durata dell'esposizione alla polvere. Anche la composizione specifica della polvere della miniera di carbone influisce su alcuni effetti sulla salute.
Nei paesi sviluppati, dove in passato esistevano alte prevalenze di malattie polmonari, la riduzione dei livelli di polvere determinata dalla regolamentazione ha portato a sostanziali riduzioni della prevalenza della malattia dagli anni '1970. Inoltre, le importanti riduzioni della forza lavoro mineraria nella maggior parte di questi paesi negli ultimi decenni, in parte causate dai cambiamenti tecnologici e dai conseguenti miglioramenti della produttività, si tradurranno in ulteriori riduzioni dei livelli complessivi di malattia. I minatori di altri paesi, dove l'estrazione del carbone è un fenomeno più recente ei controlli delle polveri sono meno aggressivi, non sono stati così fortunati. Questo problema è esacerbato dall'alto costo della moderna tecnologia mineraria, che costringe all'impiego di un gran numero di lavoratori, molti dei quali sono ad alto rischio di sviluppare malattie.
Nel testo che segue, ogni malattia o disturbo è considerato a sua volta. Quelli specifici dell'estrazione del carbone, come la pneumoconiosi dei lavoratori del carbone, sono descritti in dettaglio; la descrizione di altri, come la malattia polmonare ostruttiva, è limitata a quegli aspetti che riguardano i minatori di carbone e l'esposizione alla polvere.
Pneumoconiosi dei lavoratori del carbone
La pneumoconiosi dei lavoratori del carbone (CWP) è la malattia più comunemente associata all'estrazione del carbone. Non è una malattia a rapido sviluppo, di solito ci vogliono almeno dieci anni per manifestarsi, e spesso molto di più quando le esposizioni sono basse. Nelle sue fasi iniziali è un indicatore di eccessiva ritenzione di polvere polmonare e può essere associato a pochi sintomi o segni di per sé. Tuttavia, man mano che avanza, espone il minatore a un rischio crescente di sviluppare la fibrosi massiva progressiva (PMF) molto più grave.
Patologia
La classica lesione della CWP è la macula di carbone, una raccolta di polvere e macrofagi carichi di polvere attorno alla periferia dei bronchioli respiratori. Le macule contengono collagene minimo e quindi di solito non sono palpabili. Hanno una dimensione da 1 a 5 mm circa e sono spesso accompagnati da un allargamento degli spazi aerei adiacenti, chiamato enfisema focale. Sebbene spesso molto numerosi, di solito non sono evidenti su una radiografia del torace.
Un'altra lesione associata alla CWP è il nodulo di carbone. Queste lesioni più grandi sono palpabili e contengono una miscela di macrofagi carichi di polvere, collagene e reticolina. La presenza di noduli di carbone, con o senza noduli silicotici (vedi sotto), indica fibrosi polmonare ed è in gran parte responsabile delle opacità osservate nelle radiografie del torace. I macronoduli (da 7 a 20 mm) di dimensioni possono fondersi per formare una fibrosi massiva progressiva (vedi sotto), oppure la PMF può svilupparsi da un singolo macronodulo.
Noduli silicotici (descritti sotto silicosi) sono stati trovati in una significativa minoranza di minatori di carbone sotterranei. Per la maggior parte, la causa può risiedere semplicemente nella silice presente nella polvere di carbone, sebbene l'esposizione alla silice pura in alcuni lavori sia certamente un fattore importante (ad esempio, tra perforatori di superficie, automobilisti sotterranei e chiodatori di tetti).
Radiografia
L'indicatore più utile di CWP nei minatori durante la vita si ottiene utilizzando la radiografia del torace di routine. I depositi di polvere e le reazioni del tessuto nodulare attenuano il raggio di raggi X e provocano opacità sulla pellicola. La profusione di queste opacità può essere valutata sistematicamente utilizzando un metodo standardizzato di descrizione radiografica come quello diffuso dall'ILO e descritto in questo capitolo. In questo metodo, i singoli film postero-anteriore vengono confrontati con radiografie standard che mostrano una crescente profusione di piccole opacità e il film viene classificato in una delle quattro categorie principali (0, 1, 2, 3) in base alla sua somiglianza con lo standard. Viene inoltre effettuata una classificazione secondaria, a seconda della valutazione del lettore sulla somiglianza del film con le categorie ILO adiacenti. Si notano anche altri aspetti delle opacità, come la dimensione, la forma e la regione di occorrenza nel polmone. Alcuni paesi, come la Cina e il Giappone, hanno sviluppato sistemi simili per la descrizione o l'interpretazione sistematica delle radiografie, particolarmente adatti alle proprie esigenze.
Tradizionalmente, piccolo arrotondato tipi di opacità sono stati associati all'estrazione del carbone. Tuttavia, dati più recenti lo indicano irregolare i tipi possono anche derivare dall'esposizione alla polvere di miniera di carbone. Le opacità di CWP e silicosi sono spesso indistinguibili sulla radiografia. Tuttavia, ci sono alcune prove che opacità di dimensioni maggiori (tipo r) indicano più spesso silicosi.
È importante notare che una quantità sostanziale di anomalie patologiche correlate alla pneumoconiosi può essere presente nel polmone prima che possa essere rilevata sulla radiografia del torace di routine. Ciò è particolarmente vero per la deposizione maculare, ma diventa progressivamente meno vero con una maggiore profusione e dimensione dei noduli. L'enfisema concomitante può anche ridurre la visibilità delle lesioni alla radiografia del torace. La tomografia computerizzata (TC), in particolare la tomografia computerizzata ad alta risoluzione (HRCT), può consentire la visualizzazione di anomalie non chiaramente evidenti nelle normali radiografie del torace, sebbene la TC non sia necessaria per la diagnosi clinica di routine delle malattie polmonari dei minatori e non sia indicata per esami medici. sorveglianza dei minatori.
Aspetti clinici
Lo sviluppo di CWP, sebbene sia un marker di eccessiva ritenzione di polvere polmonare, di per sé spesso non è accompagnato da alcun segno clinico evidente. Questo non dovrebbe, tuttavia, essere interpretato nel senso che l'inalazione di polvere di miniera di carbone è senza rischi, poiché è ormai ben noto che altre malattie polmonari possono derivare dall'esposizione alla polvere. L'ipertensione polmonare è più spesso osservata nei minatori che sviluppano ostruzione del flusso aereo in associazione con CWP. Inoltre, una volta che il CWP si è sviluppato, di solito progredisce a meno che l'esposizione alla polvere non cessi e può progredire successivamente. Inoltre espone il minatore a un rischio notevolmente aumentato di sviluppare la PMF clinicamente minacciosa, con la probabilità di successiva menomazione, disabilità e mortalità prematura.
Meccanismi di malattia
Lo sviluppo del primo cambiamento di CWP, la macula di polvere, rappresenta gli effetti della deposizione e dell'accumulo di polvere. Lo stadio successivo, cioè lo sviluppo dei noduli, deriva dalla reazione infiammatoria e fibrotica del polmone alla polvere. In questo, i ruoli della polvere di silice e non silice sono stati a lungo dibattuti. Da un lato, la polvere di silice è nota per essere notevolmente più tossica della polvere di carbone. Tuttavia, d'altra parte, gli studi epidemiologici non hanno mostrato prove evidenti che implichino l'esposizione alla silice nella prevalenza o incidenza di CWP. In effetti, sembra che esista quasi una relazione inversa, in quanto i livelli di malattia tendono ad essere elevati laddove i livelli di silice sono inferiori (ad esempio, nelle aree in cui si estrae l'antracite). Recentemente, una certa comprensione di questo paradosso è stata acquisita attraverso studi sulle caratteristiche delle particelle. Questi studi indicano che non solo la quantità di silice presente nella polvere (misurata convenzionalmente mediante spettrometria infrarossa o diffrazione di raggi X), ma anche la biodisponibilità della superficie delle particelle di silice può essere correlata alla tossicità. Ad esempio, il rivestimento di argilla (occlusione) può svolgere un importante ruolo di modifica. Un altro fattore importante attualmente oggetto di indagine riguarda la carica superficiale sotto forma di radicali liberi e gli effetti delle polveri contenenti silice "appena fratturate" rispetto a quelle "invecchiate".
Sorveglianza ed epidemiologia
La prevalenza di CWP tra i minatori sotterranei varia a seconda del tipo di lavoro, del mandato e dell'età. Un recente studio sui minatori di carbone statunitensi ha rivelato che dal 1970 al 1972 circa il 25-40% dei minatori di carbone che lavoravano aveva opacità arrotondate di categoria 1 o superiore dopo 30 o più anni di attività mineraria. Questa prevalenza riflette l'esposizione a livelli di 6 mg/mXNUMX3 o più di polvere respirabile tra i lavoratori del carbone prima di quel momento. L'introduzione di un limite di polvere di 3 mg/m3 nel 1969, con una riduzione a 2 mg/m3 nel 1972 ha portato a un calo della prevalenza della malattia a circa la metà dei livelli precedenti. Diminuzioni relative al controllo delle polveri sono state notate altrove, ad esempio nel Regno Unito e in Australia. Sfortunatamente, questi guadagni sono stati controbilanciati da aumenti temporali della prevalenza altrove.
Una serie di studi ha dimostrato una relazione esposizione-risposta per la prevalenza o l'incidenza di CWP e l'esposizione alla polvere. Questi hanno dimostrato che la principale variabile significativa di esposizione alla polvere è l'esposizione alla polvere di miniera mista. Studi intensivi condotti da ricercatori britannici non sono riusciti a rivelare alcuna influenza importante dell'esposizione alla silice, purché la percentuale di silice fosse inferiore a circa il 5%. Il rango del carbone (percentuale di carbonio) è un altro importante fattore predittivo dello sviluppo del CWP. Studi negli Stati Uniti, nel Regno Unito, in Germania e altrove hanno fornito chiare indicazioni che la prevalenza e l'incidenza del CWP aumenta notevolmente con il rango del carbone, essendo sostanzialmente maggiore dove viene estratto il carbone antracite (alto rango). Non è stato riscontrato che altre variabili ambientali esercitino effetti importanti sullo sviluppo del CWP. L'età dei minatori sembra avere una certa influenza sullo sviluppo della malattia, poiché i minatori più anziani sembrano essere maggiormente a rischio. Tuttavia, non è del tutto chiaro se ciò implichi che i minatori più anziani siano più suscettibili, se si tratti di un effetto del tempo di residenza o semplicemente di un artefatto (l'effetto dell'età potrebbe riflettere una sottostima delle stime di esposizione per i minatori più anziani, ad esempio). Il fumo di sigaretta non sembra aumentare il rischio di sviluppo di CWP.
La ricerca in cui i minatori sono stati seguiti con radiografie del torace ogni cinque anni mostra che il rischio di sviluppare PMF nel corso dei cinque anni è chiaramente correlato alla categoria di CWP come rivelato sulla radiografia del torace iniziale. Poiché il rischio alla categoria 2 è molto maggiore di quello alla categoria 1, la saggezza convenzionale una volta era che ai minatori dovrebbe essere impedito di raggiungere la categoria 2, se possibile. Tuttavia, nella maggior parte delle miniere di solito ci sono molti più minatori con CWP di categoria 1 rispetto alla categoria 2. Pertanto, il minor rischio per la categoria 1 rispetto alla categoria 2 è in qualche modo compensato dal maggior numero di minatori con categoria 1. è diventato chiaro che tutte le pneumoconiosi dovrebbero essere prevenute.
Mortalità
È stato osservato che i minatori come gruppo hanno un aumentato rischio di morte per malattie respiratorie non maligne e ci sono prove che la mortalità tra i minatori con CWP è in qualche modo aumentata rispetto a quelli di età simile senza la malattia. Tuttavia, l'effetto è inferiore all'eccesso osservato per i minatori con PMF (vedi sotto).
Frodi
L'unica protezione contro il CWP è la riduzione al minimo dell'esposizione alla polvere. Se possibile, ciò dovrebbe essere ottenuto mediante metodi di abbattimento delle polveri, come ventilazione e spruzzi d'acqua, piuttosto che mediante l'uso di respiratori o controlli amministrativi, ad esempio la rotazione dei lavoratori. A questo proposito, ora ci sono buone prove che le azioni normative in alcuni paesi per ridurre il livello di polvere, intraprese intorno agli anni '1970, hanno portato a livelli di malattia notevolmente ridotti. Il trasferimento di lavoratori con segni precoci di CWP a lavori meno polverosi è un'azione prudente, sebbene ci siano poche prove pratiche che tali programmi siano riusciti a prevenire la progressione della malattia. Per questo motivo, l'abbattimento delle polveri deve rimanere il metodo principale di prevenzione delle malattie.
Il monitoraggio continuo e aggressivo dell'esposizione alla polvere e l'esercizio consapevole degli sforzi di controllo possono essere integrati dalla sorveglianza sanitaria dei minatori. Se si scopre che i minatori sviluppano malattie legate alla polvere, gli sforzi per il controllo dell'esposizione dovrebbero essere intensificati in tutto il posto di lavoro e ai minatori con effetti di polvere dovrebbe essere offerto lavoro in aree a bassa polvere dell'ambiente minerario.
Trattamento
Sebbene siano state provate diverse forme di trattamento, tra cui l'inalazione di polvere di alluminio e la somministrazione di tetrandine, non è noto alcun trattamento che inverta o rallenti efficacemente il processo fibrotico nel polmone. Attualmente, principalmente in Cina, ma anche altrove, si sta sperimentando il lavaggio dell'intero polmone con l'intento di ridurre il carico totale di polvere polmonare. Sebbene la procedura possa comportare la rimozione di una notevole quantità di polvere, i suoi rischi, benefici e ruolo nella gestione della salute dei minatori non sono chiari.
Per altri aspetti, il trattamento dovrebbe essere diretto alla prevenzione delle complicanze, massimizzando lo stato funzionale dei minatori e alleviando i loro sintomi, siano essi dovuti a CWP o ad altre malattie respiratorie concomitanti. In generale, i minatori che sviluppano malattie polmonari indotte dalla polvere dovrebbero valutare le loro attuali esposizioni alla polvere e utilizzare le risorse del governo e delle organizzazioni sindacali per trovare le strade disponibili per ridurre tutte le esposizioni respiratorie avverse. Per i minatori che fumano, smettere di fumare è un primo passo nella gestione dell'esposizione personale. Si suggerisce di prevenire le complicanze infettive delle malattie polmonari croniche con i vaccini pneumococcici e antinfluenzali annuali disponibili. Si raccomanda inoltre un'indagine precoce dei sintomi di infezione polmonare, con particolare attenzione alla malattia micobatterica. I trattamenti per la bronchite acuta, il broncospasmo e l'insufficienza cardiaca congestizia tra i minatori sono simili a quelli per i pazienti senza malattie legate alla polvere.
Fibrosi massiva progressiva
La PMF, a volte indicata come pneumoconiosi complicata, viene diagnosticata quando una o più grandi lesioni fibrotiche (la cui definizione dipende dalla modalità di rilevazione) sono presenti in uno o entrambi i polmoni. Come suggerisce il nome, il PMF diventa spesso più grave nel tempo, anche in assenza di ulteriore esposizione alla polvere. Può anche svilupparsi dopo che l'esposizione alla polvere è cessata e spesso può causare disabilità e mortalità prematura.
Patologia
Le lesioni da PMF possono essere unilaterali o bilaterali e si trovano più spesso nei lobi superiori o medi del polmone. Le lesioni sono formate da collagene, reticolina, polvere di miniera di carbone e macrofagi carichi di polvere, mentre il centro può contenere un liquido nero che occasionalmente cavita. Gli standard patologici statunitensi richiedono che le lesioni abbiano una dimensione di 2 cm o superiore per essere identificate come entità PMF nei campioni chirurgici o autoptici.
Radiologia
Grandi opacità >>1 cm) sulla radiografia, insieme a una storia di estesa esposizione alla polvere di miniera di carbone, sono considerate implicare la presenza di PMF. Tuttavia, è importante considerare altre malattie come il cancro ai polmoni, la tubercolosi e i granulomi. Di solito si osservano grandi opacità su uno sfondo di piccole opacità, ma lo sviluppo di PMF da una profusione di categoria 0 è stato notato in un periodo di cinque anni.
Aspetti clinici
Le possibilità diagnostiche per ogni singolo minatore con grandi opacità toraciche devono essere opportunamente valutate. I minatori clinicamente stabili con lesioni bilaterali nella tipica distribuzione del polmone superiore e con CWP semplice preesistente possono presentare una piccola sfida diagnostica. Tuttavia, i minatori con sintomi progressivi, fattori di rischio per altri disturbi (p. es., tubercolosi) o caratteristiche cliniche atipiche dovrebbero essere sottoposti a un esame approfondito e appropriato prima che il diagnostico attribuisca le lesioni alla PMF.
La dispnea e altri sintomi respiratori spesso accompagnano la PMF, ma potrebbero non essere necessariamente dovuti alla malattia stessa. L'insufficienza cardiaca congestizia (dovuta a ipertensione polmonare e cuore polmonare) è una complicanza non infrequente.
Meccanismi di malattia
Nonostante le ricerche approfondite, la vera causa dello sviluppo della PMF rimane poco chiara. Nel corso degli anni sono state proposte varie ipotesi, ma nessuna è pienamente soddisfacente. Una teoria importante era che la tubercolosi avesse un ruolo. Infatti, la tubercolosi è spesso presente nei minatori con PMF, in particolare nei paesi in via di sviluppo. Tuttavia, è stato riscontrato che la PMF si sviluppa nei minatori in cui non vi era alcun segno di tubercolosi e la reattività alla tubercolina non è risultata elevata nei minatori con pneumoconiosi. Nonostante le indagini, mancano prove coerenti del ruolo del sistema immunitario nello sviluppo della PMF.
Sorveglianza ed epidemiologia
Come per il CWP, i livelli di PMF sono in calo nei paesi che hanno rigide normative e programmi di controllo delle polveri. Un recente studio sui minatori statunitensi ha rivelato che circa il 2% dei minatori di carbone che lavorano sottoterra aveva PMF dopo 30 o più anni di attività mineraria (sebbene questa cifra possa essere stata distorta dai minatori colpiti che hanno lasciato la forza lavoro).
Le indagini sull'esposizione-risposta del PMF hanno dimostrato che l'esposizione alla polvere di miniera di carbone, la categoria di CWP, il rango del carbone e l'età sono i principali determinanti dello sviluppo della malattia. Come con CWP, gli studi epidemiologici non hanno rilevato effetti importanti della polvere di silice. Anche se un tempo si pensava che la PMF si sviluppasse solo sullo sfondo delle piccole opacità della CWP, recentemente si è scoperto che non era così. È stato dimostrato che i minatori con una radiografia del torace iniziale che mostra CWP di categoria 0 sviluppano PMF nell'arco di cinque anni, con un rischio che aumenta con la loro esposizione cumulativa alla polvere. Inoltre, i minatori possono sviluppare PMF dopo la cessazione dell'esposizione alla polvere.
Mortalità
La PMF porta a mortalità prematura, la prognosi peggiora con l'aumentare dello stadio della malattia. Uno studio recente ha mostrato che i minatori con PMF di categoria C avevano solo un quarto del tasso di sopravvivenza in 22 anni rispetto ai minatori senza pneumoconiosi. Questo effetto si è manifestato su tutti i gruppi di età.
Frodi
Evitare l'esposizione alla polvere è l'unico modo per prevenire il PMF. Poiché il rischio del suo sviluppo aumenta notevolmente con l'aumentare della categoria di CWP semplice, una strategia per la prevenzione secondaria della PMF è che i minatori si sottopongano periodicamente a radiografie del torace e interrompano o riducano la loro esposizione se viene rilevata CWP semplice. Anche se questo approccio sembra valido ed è stato adottato in alcune giurisdizioni, la sua efficacia non è stata valutata sistematicamente.
Trattamento
Non esiste un trattamento noto per la PMF. L'assistenza medica dovrebbe essere organizzata per migliorare la condizione e le malattie polmonari associate, proteggendo al tempo stesso dalle complicanze infettive. Sebbene il mantenimento della stabilità funzionale possa essere più difficile nei pazienti con PMF, per altri aspetti la gestione è simile alla CWP semplice.
Malattia polmonare ostruttiva
Ora ci sono prove coerenti e convincenti di una relazione tra la perdita della funzione polmonare e l'esposizione alla polvere. Vari studi in diversi paesi hanno esaminato l'influenza dell'esposizione alla polvere sui valori assoluti e sui cambiamenti temporali nelle misurazioni della funzione ventilatoria, come il volume espiratorio forzato in un secondo (FEV1), capacità vitale forzata (FVC) e portate. Tutti hanno trovato prove che l'esposizione alla polvere porta a una riduzione della funzione polmonare, ei risultati sono stati sorprendentemente simili per diverse recenti indagini britanniche e statunitensi. Questi indicano che nel corso di un anno, l'esposizione alla polvere sul fronte del carbone provoca, in media, una riduzione della funzionalità polmonare equivalente al fumo di mezzo pacchetto di sigarette al giorno. Gli studi dimostrano anche che gli effetti variano e un dato minatore può sviluppare effetti uguali o peggiori di quelli attesi dal fumo di sigaretta, in particolare se l'individuo ha subito esposizioni alla polvere più elevate.
Gli effetti dell'esposizione alla polvere sono stati riscontrati sia in coloro che non hanno mai fumato sia nei fumatori attuali. Inoltre, non ci sono prove che il fumo aggravi l'effetto dell'esposizione alla polvere. Piuttosto, gli studi hanno generalmente mostrato un effetto leggermente inferiore nei fumatori attuali, un risultato che potrebbe essere dovuto alla selezione di lavoratori sani. È importante notare che la relazione tra l'esposizione alla polvere e il declino della ventilazione sembra esistere indipendentemente dalla pneumoconiosi. Cioè, non è un requisito che la pneumoconiosi sia presente perché ci sia una ridotta funzionalità polmonare. Al contrario, sembra piuttosto che la polvere inalata possa agire lungo più percorsi, portando a pneumoconiosi in alcuni minatori, a ostruzione in altri ea molteplici esiti in altri ancora. A differenza dei minatori con CWP da solo, i minatori con sintomi respiratori hanno una funzione polmonare significativamente inferiore, dopo la standardizzazione per età, fumo, esposizione alla polvere e altri fattori.
Il recente lavoro sui cambiamenti della funzione ventilatoria ha comportato l'esplorazione dei cambiamenti longitudinali. I risultati indicano che potrebbe esserci una tendenza non lineare di declino nel tempo nei nuovi minatori, un alto tasso di perdita iniziale seguito da un calo più moderato con esposizione continua. Inoltre, ci sono prove che i minatori che reagiscono alla polvere possono scegliere, se possibile, di allontanarsi dalle esposizioni più pesanti.
Bronchite cronica
I sintomi respiratori, come la tosse cronica e la produzione di catarro, sono una conseguenza frequente del lavoro nell'estrazione del carbone, la maggior parte degli studi mostra una prevalenza eccessiva rispetto ai gruppi di controllo non esposti. Inoltre, è stato dimostrato che la prevalenza e l'incidenza dei sintomi respiratori aumentano con l'esposizione cumulativa alla polvere, tenendo conto dell'età e del fumo. La presenza di sintomi sembra essere associata a una riduzione della funzionalità polmonare oltre a quella dovuta all'esposizione alla polvere e ad altre cause presunte. Ciò suggerisce che l'esposizione alla polvere può essere determinante nell'iniziare determinati processi patologici che poi progrediscono indipendentemente da un'ulteriore esposizione. È stata dimostrata patologicamente una relazione tra le dimensioni delle ghiandole bronchiali e l'esposizione alla polvere ed è stato riscontrato che la mortalità per bronchite ed enfisema aumenta con l'aumentare dell'esposizione cumulativa alla polvere.
Enfisema
Studi patologici hanno ripetutamente riscontrato un eccesso di enfisema nei minatori di carbone rispetto ai gruppi di controllo. Inoltre, il grado di enfisema è risultato essere correlato sia alla quantità di polvere nei polmoni che a valutazioni patologiche di pneumoconiosi. Inoltre, è importante riconoscere che esistono prove che la presenza di enfisema è correlata all'esposizione alla polvere e alla percentuale del FEVXNUMX previsto1. Quindi, questi risultati sono coerenti con l'idea che l'esposizione alla polvere può portare alla disabilità causando enfisema.
La forma di enfisema più chiaramente associata all'estrazione del carbone è l'enfisema focale. Consiste in zone di spazi aerei allargati, di dimensioni da 1 a 2 mm, adiacenti a macule di polvere che circondano i bronchioli respiratori. Il pensiero corrente è che l'enfisema sia formato dalla distruzione dei tessuti, piuttosto che dalla distensione o dilatazione. A parte l'enfisema focale, ci sono prove che l'enfisema centriacinare ha un'origine occupazionale, e che l'enfisema totale (cioè l'estensione di tutti i tipi) è correlato con la permanenza nell'attività mineraria, in coloro che non hanno mai fumato così come nei fumatori. Non ci sono prove che il fumo potenzi la relazione esposizione alla polvere/enfisema. Tuttavia, vi sono indicazioni di una relazione inversa tra il contenuto di silice nei polmoni e la presenza di enfisema.
La questione dell'enfisema è stata a lungo controversa, con alcuni che affermano che il bias di selezione e il fumo rendono difficile l'interpretazione degli studi patologici. Inoltre, alcuni ritengono che l'enfisema focale abbia solo effetti banali sulla funzione polmonare. Tuttavia, gli studi patologici intrapresi dagli anni '1980 hanno risposto alle critiche precedenti e indicano che l'effetto dell'esposizione alla polvere potrebbe essere più significativo per la salute dei minatori di quanto si pensasse in precedenza. Questo punto di vista è supportato da recenti scoperte secondo cui la mortalità per bronchite ed enfisema è correlata all'esposizione cumulativa alla polvere.
Silicosi
La silicosi, sebbene associata maggiormente a industrie diverse dall'estrazione del carbone, può verificarsi nei minatori di carbone. Nelle miniere sotterranee, si trova più frequentemente nei lavoratori in determinati lavori in cui si verifica tipicamente l'esposizione alla silice pura. Tali lavoratori includono i bullonatori del tetto, che perforano la roccia del soffitto, che spesso può essere arenaria o altra roccia con un alto contenuto di silice; i motormen, conducenti di trasporti ferroviari che sono esposti alla polvere generata dalla sabbia depositata sui binari per dare trazione; e perforatori di roccia, che sono coinvolti nello sviluppo della miniera. È stato dimostrato che i perforatori di roccia nelle miniere di carbone di superficie sono particolarmente a rischio negli Stati Uniti, con alcuni che sviluppano silicosi acuta dopo solo pochi anni di esposizione. Sulla base di prove patologiche, come indicato di seguito, un certo grado di silicosi può affliggere molti più minatori di carbone rispetto a quelli che svolgono i lavori sopra indicati.
I noduli silicotici nei minatori di carbone sono di natura simile a quelli osservati altrove e consistono in uno schema a spirale di collagene e reticolina. Un ampio studio autoptico ha rivelato che circa il 13% dei minatori di carbone aveva noduli silicotici nei polmoni. Sebbene un lavoro, (quello del macchinista) fosse notevole per avere una prevalenza molto più alta di noduli silicotici (25%), c'era poca variazione nella prevalenza tra i minatori in altri lavori, suggerendo che la silice nella polvere mista della miniera fosse responsabile.
La silicosi non può essere differenziata in modo affidabile dalla pneumoconiosi dei lavoratori del carbone su una radiografia. Tuttavia, ci sono alcune prove che il tipo più grande di piccole opacità (tipo r) sia indicativo di silicosi.
Pneumoconiosi reumatoide
Pneumoconiosi reumatoide, una variante del quale è chiamata La sindrome di Caplan, è il termine usato per una condizione che colpisce i lavoratori esposti alla polvere che sviluppano molteplici ombre radiografiche di grandi dimensioni. Dal punto di vista patologico, queste lesioni assomigliano a noduli reumatoidi piuttosto che a lesioni da PMF e spesso insorgono in un breve intervallo di tempo. Generalmente si riscontrano artrite attiva o la presenza di fattore reumatoide circolante, ma occasionalmente sono assenti.
Lung Cancer
Tra le esposizioni professionali subite dai minatori di carbone vi è una serie di sostanze potenzialmente cancerogene. Alcuni di questi sono silice e benzo(a)pireni. Tuttavia, non vi è alcuna chiara evidenza di un eccesso di decessi per cancro ai polmoni nei minatori di carbone. Una spiegazione ovvia di ciò è che ai minatori di carbone è vietato fumare sotto terra a causa del pericolo di incendi ed esplosioni. Tuttavia, il fatto che non sia stata rilevata alcuna relazione esposizione-risposta tra il cancro ai polmoni e l'esposizione alla polvere suggerisce che la polvere di miniera di carbone non è una delle principali cause di cancro ai polmoni nel settore.
Limiti normativi sull'esposizione alla polvere
L'Organizzazione mondiale della sanità (OMS) ha raccomandato un "limite di esposizione provvisorio basato sulla salute" per la polvere di miniera di carbone respirabile (con meno del 6% di quarzo respirabile) compreso tra 0.5 e 4 mg/m3. L'OMS suggerisce un rischio di 2 su 1,000 di PMF nel corso della vita lavorativa come criterio e raccomanda che i fattori ambientali basati sulle miniere, tra cui il grado di carbone, la percentuale di quarzo e la dimensione delle particelle, dovrebbero essere presi in considerazione quando si fissano i limiti.
Attualmente, tra i maggiori paesi produttori di carbone, i limiti si basano sulla regolamentazione della sola polvere di carbone (ad esempio, 3.8 mg/m3 nel Regno Unito, 5 mg/m3 in Australia e Canada) o sulla regolamentazione di una miscela di carbone e silice come negli Stati Uniti (2 mg/m3 quando la percentuale di quarzo è pari o inferiore a 5, o (10 mg/m3)/per cento SiO2), o in Germania (4 mg/m3 quando la percentuale di quarzo è pari o inferiore a 5, o 0.15 mg/m3 altrimenti), o sulla regolazione del quarzo puro (es. Polonia, con 0.05 mg/m3 limite).
Malattie correlate all'amianto
Prospettiva storica
Amianto è un termine usato per descrivere un gruppo di minerali fibrosi presenti in natura che sono ampiamente distribuiti negli affioramenti rocciosi e nei depositi di tutto il mondo. Lo sfruttamento delle proprietà di resistenza alla trazione e al calore dell'amianto per uso umano risale a tempi antichissimi. Ad esempio, nel III secolo aC l'amianto veniva usato per rinforzare vasi di terracotta in Finlandia. In epoca classica, per conservare le ceneri dei defunti famosi si usavano sudari intessuti di amianto. Marco Polo tornò dai suoi viaggi in Cina con descrizioni di un materiale magico che poteva essere fabbricato in un tessuto ignifugo. Nei primi anni del diciannovesimo secolo si conosceva l'esistenza di giacimenti in diverse parti del mondo, inclusi i monti Urali, l'Italia settentrionale e altre aree del Mediterraneo, in Sud Africa e in Canada, ma lo sfruttamento commerciale iniziò solo nella seconda metà del il XIX secolo. A questo punto, la rivoluzione industriale ha creato non solo la domanda (come quella dell'isolamento del motore a vapore), ma ha anche facilitato la produzione, con la meccanizzazione che ha sostituito la cobnatura manuale della fibra dalla roccia madre. L'industria moderna iniziò in Italia e nel Regno Unito dopo il 1860 e fu potenziata dallo sviluppo e dallo sfruttamento degli estesi giacimenti di amianto crisotilo (bianco) in Quebec (Canada) negli anni Ottanta dell'Ottocento. Lo sfruttamento degli anche estesi depositi di crisotilo negli Urali fu modesto fino agli anni '1880. Le fibre lunghe e sottili del crisotilo erano particolarmente adatte per la filatura in tessuti e feltri, uno dei primi usi commerciali del minerale. Lo sfruttamento dei giacimenti di amianto crocidolite (blu) del Capo Nord-Ovest, Sudafrica, fibra più resistente all'acqua del crisotilo e più adatta all'uso marino, e dei giacimenti di amianto amosite (bruno), anch'esso presente in Sudafrica, iniziato nei primi anni di questo secolo. Lo sfruttamento dei giacimenti finlandesi di amianto antofillite, unica importante fonte commerciale di questa fibra, è avvenuto tra il 1920 e il 1918, mentre i giacimenti di crocidolite a Wittenoom, nell'Australia occidentale, sono stati estratti dal 1966 al 1937.
Tipi di fibre
I minerali di amianto si dividono in due gruppi, il gruppo serpentino che comprende il crisotilo, e gli anfiboli, che comprendono crocidolite, tremolite, amosite e antofillite (figura 1). La maggior parte dei depositi di minerale sono eterogenei dal punto di vista mineralogico, così come la maggior parte delle forme commerciali del minerale (Skinner, Roos e Frondel 1988). Il crisotilo ei vari minerali di amianto anfibolo differiscono nella struttura cristallina, nelle caratteristiche chimiche e superficiali e nelle caratteristiche fisiche delle loro fibre, solitamente descritte in termini di rapporto lunghezza-diametro (o aspetto). Differiscono anche per le caratteristiche che ne distinguono l'uso commerciale e il grado. Pertinente alla discussione in corso è l'evidenza che le diverse fibre differiscono nella loro potenza biologica (come considerato di seguito nelle sezioni sulle varie malattie).
Figura 1. Tipi di fibre di amianto.
Visto su microscopia elettorale insieme a spettri di raggi X a dispersione di energia che consentono l'identificazione delle singole fibre. Per gentile concessione di A. Dufresne e M. Harrigan, McGill University.
Produzione commerciale
La crescita della produzione commerciale, illustrata nella figura 2, è stata lenta nei primi anni di questo secolo. Ad esempio, la produzione canadese superò per la prima volta le 100,000 tonnellate corte all'anno nel 1911 e le 200,000 tonnellate nel 1923. comprese quelle della guerra fredda) per raggiungere un picco nel 1976 di 5,708,000 tonnellate corte (Selikoff e Lee 1978). Successivamente, la produzione ha vacillato poiché gli effetti sulla salute dell'esposizione sono diventati motivo di crescente preoccupazione pubblica in Nord America ed Europa e sono rimasti a circa 4,000,000 di tonnellate corte all'anno fino al 1986, ma sono diminuiti ulteriormente negli anni '1990. C'è stato anche un cambiamento negli usi e nelle fonti di fibra negli anni '1980; in Europa e Nord America la domanda è diminuita per l'introduzione di sostituti per molte applicazioni, mentre nei continenti africano, asiatico e sudamericano è aumentata la domanda di amianto per soddisfare le esigenze di un materiale durevole ed economico per l'uso nelle costruzioni e nella reticolazione delle acque. Nel 1981, la Russia era diventata il principale produttore mondiale, con un aumento dello sfruttamento commerciale di grandi giacimenti in Cina e Brasile. Nel 1980, è stato stimato che in tutto il mondo fossero state estratte oltre 100 milioni di tonnellate di amianto, il 90% delle quali era crisotilo, di cui circa il 75% proveniva da 4 aree minerarie di crisotilo, situate in Quebec (Canada), Africa meridionale e gli Urali centrali e meridionali. Il 2-3% della produzione totale mondiale era di crocidolite, proveniente dal Capo Settentrionale, in Sudafrica, e dall'Australia occidentale, e un altro 1988-XNUMX% era di amosite, proveniente dal Transvaal orientale, in Sudafrica (Skinner, Ross e Frondel XNUMX). .
Figura 2. Produzione mondiale di amianto in migliaia di tonnellate 1900-92
Malattie e condizioni correlate all'amianto
Come la silice, l'amianto ha la capacità di provocare reazioni cicatriziali in tutti i tessuti biologici, umani e animali. Inoltre, l'amianto evoca reazioni maligne, aggiungendo un ulteriore elemento alla preoccupazione per la salute umana, nonché una sfida alla scienza su come l'amianto eserciti i suoi effetti negativi. La prima malattia correlata all'amianto ad essere riconosciuta, la fibrosi o cicatrizzazione polmonare interstiziale diffusa, in seguito chiamata asbestosi, è stata oggetto di segnalazioni di casi nel Regno Unito all'inizio del 1900. Successivamente, negli anni '1930, nella letteratura medica apparvero segnalazioni di casi di cancro ai polmoni in associazione con l'asbestosi, anche se fu solo nei decenni successivi che furono raccolte le prove scientifiche che stabilivano che l'amianto era il fattore cancerogeno. Nel 1960, l'associazione tra l'esposizione all'amianto e un altro tumore molto meno comune, il mesotelioma maligno, che coinvolge la pleura (una membrana che ricopre il polmone e riveste la parete toracica) fu drammaticamente portata all'attenzione dalla segnalazione di un gruppo di questi tumori in 33 persone, tutte lavoratrici o vissute nell'area mineraria di amianto del Capo Nordoccidentale (Wagner 1996). L'asbestosi è stata l'obiettivo dei livelli di controllo delle polveri introdotti e implementati con crescente rigore negli anni '1960 e '1970, e in molti paesi industrializzati, con la diminuzione della frequenza di questa malattia, la malattia pleurica correlata all'amianto è emersa come la manifestazione più frequente di esposizione e la condizione che più frequentemente ha portato i soggetti esposti all'attenzione medica. La tabella 1 elenca le malattie e le condizioni attualmente riconosciute come correlate all'amianto. Le malattie in grassetto sono quelle più frequentemente riscontrate e per le quali è ben accertato un nesso causale diretto, mentre per completezza sono elencate anche alcune altre condizioni, per le quali il nesso è meno accertato (vedi nota alla Tabella 16 ) e le sezioni che seguono nel testo sottostante che ampliano i vari titoli delle malattie).
Tabella 1. Malattie e condizioni correlate all'amianto
| Patologia | Organo(i) interessato(i). | Malattia/condizione1 |
| Non maligno | Polmoni Pleura Pelle | asbestosi (fibrosi interstiziale diffusa) Malattia delle piccole vie aeree2 (fibrosi limitata al regione peri-bronchiolare) Malattia cronica delle vie aeree3 Placche pleuriche Reazioni viscero-parietali, compreso pleurico benigno versamento, fibrosi pleurica diffusa e arrotondata atelettasia Calli di amianto4 |
| Maligno | Polmoni Pleura Altre cavità rivestite di mesotelio Tratto gastrointestinale5 Altro5 | Cancro ai polmoni (tutti i tipi di cellule) Cancro della laringe Mesotelioma della pleura Mesotelioma del peritoneo, pericardio e scroto (con frequenza decrescente di occorrenza) Cancro di stomaco, esofago, colon, retto Ovaio, cistifellea, dotti biliari, pancreas, rene |
1 Le malattie o le condizioni indicate in grassetto sono quelle più frequentemente riscontrate e quelle per le quali è ben accertato e/o generalmente riconosciuto un nesso causale.
2 Si ritiene che la fibrosi nelle pareti delle piccole vie aeree del polmone (compresi i bronchioli membranosi e respiratori) rappresenti la risposta precoce del parenchima polmonare all'amianto trattenuto (Wright et al. 1992) che progredirà verso l'asbestosi se l'esposizione continua e/o è pesante, ma se l'esposizione è limitata o leggera, la risposta polmonare può essere limitata a queste aree (Becklake in Liddell & Miller 1991).
3 Sono inclusi la bronchite, la broncopneumopatia cronica ostruttiva (BPCO) e l'enfisema. È stato dimostrato che tutti sono associati al lavoro in ambienti polverosi. Le prove di causalità sono esaminate nella sezione Malattie croniche delle vie aeree e Becklake (1992).
4 Relativo alla gestione diretta dell'amianto e di interesse storico piuttosto che attuale.
5 Dati non coerenti da tutti gli studi (Doll e Peto 1987); alcuni dei rischi più elevati sono stati segnalati in una coorte di oltre 17,000 lavoratori dell'isolamento dell'amianto americani e canadesi (Selikoff 1990), seguiti dal 1 gennaio 1967 al 31 dicembre 1986 in cui l'esposizione era stata particolarmente pesante.
Fonti: Becklake 1994; Liddell e Miller 1992; Selikoff 1990; Doll e Peto in Antman e Aisner 1987; Wright et al. 1992.
si utilizza
La tabella 2 elenca le principali fonti, prodotti e usi dei minerali di amianto.
Tabella 2. Principali fonti commerciali, prodotti e usi dell'amianto
| Tipo di fibra | Posizione dei principali depositi | Prodotti e/o usi commerciali |
| crisotilo (bianca) |
Russia, Canada (Québec, anche British Columbia, Terranova), Cina (provincia di Szechwan); Paesi del Mediterraneo (Italia, Grecia, Corsica, Cipro); Africa meridionale (Sud Africa, Zimbabwe, Swaziland); Brasile; depositi minori negli Stati Uniti (Vermont, Arizona, California) e in Giappone | Materiali da costruzione (tegole, scandole, grondaie e cisterne; coperture, rivestimenti e rivestimenti) Pressione e altri tubi Ignifugo (marino e altro) Isolamento e insonorizzazione Prodotti in plastica rinforzata (pale di ventole, interruttori) Materiali di attrito solitamente in combinazione con resine in freni, frizioni, altro Tessili (utilizzati in cinture, abbigliamento, involucri, barriere antincendio, autoclavi, filati e imballaggi) Prodotti di carta (utilizzati in cartone, isolanti, guarnizioni, feltro per tetti, rivestimenti murali, ecc.) Galleggia in vernici, rivestimenti e bacchette per saldatura |
| crocidolite (blu) |
Sudafrica (Northwest Cape, Transvaal orientale), Australia occidentale1 | Utilizzato principalmente in combinazione nei prodotti cementizi (in particolare tubi in pressione) ma anche in molti degli altri prodotti sopra elencati |
| Amosite (Marrone) |
Sudafrica (Transvaal settentrionale)1 | Utilizzato principalmente in cemento, isolamento termico e prodotti per coperture, in particolare negli Stati Uniti2 , ma anche in combinazione in molti dei prodotti elencati sotto crisotilo |
| Antofillite | Finlandia1 | Filler nell'industria della gomma, plastica e chimica |
| tremolite | Italia, Corea e alcune isole del Pacifico; estratto su piccola scala in Turchia, Cina e altrove; contamina la roccia minerale in alcune miniere di amianto, ferro, talco e vermiculite; trovato anche in terreni agricoli nella penisola balcanica e in Turchia | Utilizzato come riempitivo nel talco; può o non può essere rimosso durante la lavorazione del minerale in modo che possa apparire nei prodotti finali |
| actinolite | Contamina i depositi di amosite e, meno spesso, di crisotilo, talco e vermiculite | Di solito non sfruttato commercialmente |
1 Un elenco come questo ovviamente non è completo e i lettori dovrebbero consultare le fonti citate e altri capitoli in questo Enciclopedia per informazioni più complete.
2 Non più in funzione.
Fonti: Istituto dell'amianto (1995); Browne (1994); Liddell e Miller (1991); Selikoff e Lee (1978); Skinner e altri (1988).
Sebbene necessariamente incompleta, questa tabella sottolinea che:
- I giacimenti si trovano in molte parti del mondo, la maggior parte dei quali sono stati sfruttati a fini non commerciali o commerciali in passato, e alcuni dei quali sono attualmente sfruttati commercialmente.
- Ci sono molti manufatti in uso attuale o passato che contengono amianto, in particolare nei settori dell'edilizia e dei trasporti.
- La disintegrazione di questi prodotti o la loro rimozione comporta il rischio della risospensione delle fibre e di una nuova esposizione umana.
Una cifra di oltre 3,000 è stata comunemente citata per il numero di usi dell'amianto e senza dubbio ha portato l'amianto a essere soprannominato il "minerale magico" negli anni '1960. Un elenco industriale del 1953 contiene ben 50 usi dell'amianto grezzo, oltre al suo uso nella fabbricazione dei prodotti elencati nella Tabella 17, ciascuno dei quali ha molte altre applicazioni industriali. Nel 1972, il consumo di amianto in un paese industrializzato come gli Stati Uniti era attribuito alle seguenti categorie merceologiche: edilizia (42%); materiali d'attrito, feltri, baderne e guarnizioni (20%); piastrelle per pavimenti (11%); carta (9%); isolamento e tessili (3%) e altri usi (15%) (Selikoff e Lee 1978). Al contrario, un elenco industriale del 1995 delle principali categorie di prodotti mostra un'importante ridistribuzione su base mondiale come segue: cemento-amianto (84%); materiali di attrito (10%); tessili (3%); tenute e guarnizioni (2%); e altri usi (1%) (Asbestos Institute 1995).
Esposizioni occupazionali, passate e attuali
L'esposizione professionale, certamente nei paesi industrializzati, è sempre stata ed è tuttora la fonte più probabile di esposizione umana (vedi Tabella 17 e i riferimenti citati nella sua nota a piè di pagina; altre sezioni di questo Enciclopedia contenere ulteriori informazioni). Ci sono stati, tuttavia, importanti cambiamenti nei processi e nelle procedure industriali volti a diminuire il rilascio di polvere nell'ambiente di lavoro (Browne 1994; Selikoff e Lee 1978). Nei paesi con operazioni minerarie, la fresatura avviene solitamente presso la testa della miniera. La maggior parte delle miniere di crisotilo sono a cielo aperto, mentre le miniere di anfiboli di solito comportano metodi sotterranei che generano più polvere. La macinazione comporta la separazione della fibra dalla roccia mediante frantumazione e vagliatura meccanizzate, che erano processi polverosi fino all'introduzione dei metodi a umido e/o della recinzione nella maggior parte dei mulini durante gli anni '1950 e '1960. Anche la movimentazione dei rifiuti era una fonte di esposizione umana, così come il trasporto di amianto in sacchi, sia che si trattasse di caricare e scaricare camion e vagoni ferroviari o di lavorare in banchina. Queste esposizioni sono diminuite dall'introduzione di sacchetti a tenuta stagna e dall'uso di contenitori sigillati.
I lavoratori hanno dovuto utilizzare l'amianto grezzo direttamente nell'imballaggio e nel rivestimento, in particolare nelle locomotive, e nella spruzzatura di pareti, soffitti e condotti dell'aria, e nell'industria marittima, ponti e paratie. Alcuni di questi usi sono stati eliminati volontariamente o sono stati vietati. Nella fabbricazione di prodotti in cemento-amianto, l'esposizione avviene durante la ricezione e l'apertura di sacchi contenenti amianto grezzo, nella preparazione della fibra per la miscelazione nell'impasto liquido, nella lavorazione dei prodotti finali e nella gestione dei rifiuti. Nella produzione di piastrelle e pavimenti in vinile, l'amianto è stato utilizzato come agente rinforzante e riempitivo da miscelare con resine organiche, ma ora è stato ampiamente sostituito da fibre organiche in Europa e Nord America. Nella produzione di filati e tessuti, l'esposizione alla fibra avviene durante la ricezione, la preparazione, la miscelazione, la cardatura, la filatura, la tessitura e la calandratura della fibra, processi che fino a poco tempo fa erano secchi e potenzialmente molto polverosi. L'esposizione alla polvere è stata notevolmente ridotta negli impianti moderni grazie all'uso di una sospensione colloidale di fibre estruse attraverso un coagulante per formare fili bagnati per gli ultimi tre processi. Nella fabbricazione di prodotti di carta a base di amianto, l'esposizione umana alla polvere di amianto è anche molto probabile che si verifichi nella ricezione e preparazione della miscela di scorta e nel taglio dei prodotti finali che negli anni '1970 contenevano dal 30 al 90% di amianto. Nella fabbricazione di prodotti di attrito dell'amianto (stampati a secco, laminati, tessuti o avvolti senza fine) è molto probabile che l'esposizione umana alla polvere di amianto si verifichi anche durante i processi iniziali di manipolazione e miscelazione, nonché nella finitura del prodotto finale, che negli anni '1970 conteneva dal 30 all'80% di amianto. Nell'industria delle costruzioni, prima dell'uso regolare di un'adeguata ventilazione di scarico (introdotta negli anni '1960), la segatura, la foratura e la levigatura ad alta velocità di pannelli o piastrelle contenenti amianto portavano al rilascio di polvere contenente fibre vicino al zona di respirazione dell'operatore, in particolare quando tali operazioni sono state condotte in ambienti chiusi (ad esempio in grattacieli in costruzione). Nel periodo successivo alla seconda guerra mondiale, una delle principali fonti di esposizione umana era l'uso, la rimozione o la sostituzione di materiali contenenti amianto nella demolizione o ristrutturazione di edifici o navi. Uno dei motivi principali di questo stato di cose era la mancanza di consapevolezza, sia della composizione di questi materiali (cioè che contenessero amianto) sia che l'esposizione all'amianto potesse essere dannosa per la salute. Una migliore istruzione dei lavoratori, migliori pratiche di lavoro e protezione personale hanno ridotto il rischio negli anni '1990 in alcuni paesi. Nel settore dei trasporti, le fonti di esposizione sono state la rimozione e la sostituzione della gommatura nei motori delle locomotive e del materiale frenante negli autocarri e nelle autovetture nel settore delle riparazioni automobilistiche.
Altre fonti di esposizione
L'esposizione di persone impegnate in attività commerciali che non comportano direttamente l'uso o la manipolazione dell'amianto ma che lavorano nella stessa area di coloro che lo trattano direttamente è chiamata para-occupazionale (spettatore) esposizione. Questa è stata un'importante fonte di esposizione non solo in passato, ma anche per i casi presentati per la diagnosi negli anni '1990. I lavoratori coinvolti includono elettricisti, saldatori e carpentieri nell'edilizia e nelle industrie di costruzione o riparazione navale; personale di manutenzione nelle fabbriche di amianto; installatori, fuochisti e altri in centrali elettriche, navi e caldaie in cui è presente rivestimento in amianto o altro isolamento e personale di manutenzione in grattacieli del dopoguerra che incorporano vari materiali contenenti amianto. Nel passato, esposizione domestica si è verificato principalmente da indumenti da lavoro carichi di polvere che venivano scossi o lavati a casa, la polvere così rilasciata rimaneva intrappolata in tappeti o arredi e risospesa nell'aria con le attività della vita quotidiana. Non solo i livelli di fibre disperse nell'aria potevano raggiungere livelli fino a 10 fibre per millilitro (f/ml), cioè dieci volte il limite di esposizione professionale proposto da una consultazione dell'OMS (1989) di 1.0 f/ml, ma le fibre tendevano a rimanere in volo per diversi giorni. Dagli anni '1970, la pratica di conservare tutti gli indumenti da lavoro in cantiere per il riciclaggio è stata ampiamente ma non universalmente adottata. In passato, inoltre, l'esposizione residenziale si verificava a causa della contaminazione dell'aria da fonti industriali. Ad esempio, sono stati documentati livelli aumentati di amianto nell'aria nelle vicinanze di miniere e impianti di amianto e sono determinati dai livelli di produzione, dai controlli delle emissioni e dalle condizioni meteorologiche. Dato il lungo lasso di tempo per, in particolare, le malattie pleuriche correlate all'amianto, è probabile che tali esposizioni siano ancora responsabili di alcuni casi che si presentano per la diagnosi negli anni '1990. Negli anni '1970 e '1980, con l'aumento della consapevolezza pubblica sia delle conseguenze per la salute dell'esposizione all'amianto sia del fatto che i materiali contenenti amianto sono ampiamente utilizzati nelle costruzioni moderne (in particolare nella forma friabile utilizzata per applicazioni a spruzzo su pareti , soffitti e condotti di ventilazione), una delle principali preoccupazioni è stata incentrata sul fatto che, poiché tali edifici invecchiano e sono soggetti all'usura quotidiana, le fibre di amianto possono essere rilasciate nell'aria in numero sufficiente a diventare una minaccia per la salute di coloro che lavorano in grattacieli moderni (vedi sotto per le stime del rischio). Altre fonti di contaminazione dell'aria nelle aree urbane includono il rilascio di fibre dai freni dei veicoli e la ridispersione delle fibre rilasciate dai veicoli in transito (Bignon, Peto e Saracci 1989).
Le fonti non industriali di esposizione ambientale includono fibre presenti naturalmente nei suoli, ad esempio nell'Europa orientale, e negli affioramenti rocciosi nella regione mediterranea, tra cui Corsica, Cipro, Grecia e Turchia (Bignon, Peto e Saracci 1989). Un'ulteriore fonte di esposizione umana deriva dall'uso di tremolite per intonaci e stucchi in Grecia e Turchia e, secondo rapporti più recenti, in Nuova Caledonia nel Pacifico meridionale (Luce et al. 1994). Inoltre, in diversi villaggi rurali in Turchia, una fibra di zeolite, l'erionite, è stata trovata utilizzata sia nello stucco che nell'edilizia domestica ed è stata implicata nella produzione di mesotelioma (Bignon, Peto e Saracci 1991). Infine, l'esposizione umana può avvenire attraverso l'acqua potabile, principalmente per contaminazione naturale, e data l'ampia distribuzione naturale della fibra negli affioramenti, la maggior parte delle fonti d'acqua contiene fibre, i cui livelli sono più alti nelle aree minerarie (Skinner, Roos e Frondel 1988).
Eziopatologia delle malattie correlate all'amianto
Destino delle fibre inalate
Le fibre inalate si allineano con il flusso d'aria e la loro capacità di penetrare negli spazi polmonari più profondi dipende dalla loro dimensione, fibre di diametro aerodinamico pari o inferiore a 5 mm che mostrano una penetrazione superiore all'80%, ma anche una ritenzione inferiore al 10-20%. Le particelle più grandi possono colpire il naso e le principali vie aeree in corrispondenza delle biforcazioni, dove tendono a raccogliersi. Le particelle depositate nelle principali vie aeree vengono eliminate dall'azione delle cellule ciliate e vengono trasportate lungo la scala mobile del muco. Le differenze individuali associate a quella che sembra essere la stessa esposizione sono dovute, almeno in parte, a differenze tra individui nella penetrazione e ritenzione delle fibre inalate (Bégin, Cantin e Massé 1989). Piccole particelle depositate oltre le principali vie aeree vengono fagocitate dai macrofagi alveolari, cellule scavenger che ingeriscono materiale estraneo. Le fibre più lunghe, cioè quelle oltre i 10 mm, spesso attaccate da più di un macrofago, hanno maggiori probabilità di rivestirsi e formare il nucleo di un corpo di amianto, una struttura caratteristica riconosciuta fin dai primi del 1900 come marker di esposizione ( vedi figura 3). Il rivestimento di una fibra è considerato parte della difesa dei polmoni per renderla inerte e non immunogenica. È più probabile che i corpi di amianto si formino sull'anfibolo che sulle fibre di crisotilo e la loro densità nel materiale biologico (espettorato, lavaggio broncoalveolare, tessuto polmonare) è un indicatore indiretto del carico polmonare. Le fibre rivestite possono persistere nel polmone per lunghi periodi, per essere recuperate dall'espettorato o dal fluido di lavaggio broncoalveolare fino a 30 anni dopo l'ultima esposizione. La clearance delle fibre non rivestite depositate nel parenchima del polmone è verso la periferia del polmone e le regioni subpleuriche, e quindi verso i linfonodi alla radice del polmone.
Figura 3. Corpo in amianto
Ingrandimento x 400, visto su sezione microscopica del polmone come una struttura allungata leggermente curva con un rivestimento proteico di ferro finemente perlato. La fibra di amianto stessa può essere identificata come la linea sottile vicino a un'estremità del corpo di amianto (freccia). Fonte: Fraser et al. 1990
Le teorie per spiegare come le fibre evocano le varie reazioni pleuriche associate all'esposizione all'amianto includono:
- penetrazione diretta nello spazio pleurico e drenaggio con il liquido pleurico nei pori della pleura che rivestono la parete toracica
- rilascio di mediatori nello spazio pleurico da raccolte linfatiche subpleuriche
- flusso retrogrado dai linfonodi alla radice del polmone alla pleura parietale (Browne 1994)
Potrebbe anche esserci un flusso retrogrado attraverso il dotto toracico ai linfonodi addominali per spiegare l'insorgenza del mesotelioma peritoneale.
Effetti cellulari delle fibre inalate
Gli studi sugli animali indicano che gli eventi iniziali che seguono la ritenzione di amianto nei polmoni includono:
- una reazione infiammatoria, con accumulo di globuli bianchi seguito da alveolite macrofagica con rilascio di fibronectina, fattore di crescita e vari fattori chemiotattici dei neutrofili e, nel tempo, rilascio di ione superossido e
- proliferazione delle cellule alveolari, epiteliali, interstiziali ed endoteliali (Bignon, Peto e Saracci 1989).
Questi eventi si riflettono nel materiale recuperato dal lavaggio broncoalveolare negli animali e nell'uomo (Bégin, Cantin e Massé 1989). Sia le dimensioni delle fibre che le loro caratteristiche chimiche sembrano determinare la potenza biologica per la fibrogenesi e queste caratteristiche, oltre alle proprietà superficiali, sono ritenute importanti anche per la carcinogenesi. Le fibre lunghe e sottili sono più attive di quelle corte, anche se l'attività di queste ultime non può essere ignorata, e gli anfiboli sono più attivi del crisotilo, proprietà attribuita alla loro maggiore biopersistenza (Bégin, Cantin e Massé 1989). Le fibre di amianto possono anche influenzare il sistema immunitario umano e modificare la popolazione circolante di linfociti del sangue. Ad esempio, l'immunità mediata da cellule umane agli antigeni cellulari (come quella mostrata in un test cutaneo alla tubercolina) può essere compromessa (Browne 1994). Inoltre, poiché le fibre di amianto sembrano essere in grado di indurre anomalie cromosomiche, è stato espresso l'opinione che esse possano anche essere considerate in grado di indurre oltre che promuovere il cancro (Jaurand in Bignon, Peto e Saracci 1989).
Relazioni tra dose e risposta all'esposizione
Nelle scienze biologiche come la farmacologia o la tossicologia in cui le relazioni dose-risposta sono utilizzate per stimare la probabilità degli effetti desiderati o il rischio di effetti indesiderati, una dose è concettualizzata come la quantità di agente erogato e che rimane in contatto con l'organo bersaglio per tempo sufficiente per provocare una reazione. Nella medicina del lavoro, i surrogati della dose, come varie misure di esposizione, sono solitamente la base per le stime del rischio. Tuttavia, le relazioni esposizione-risposta possono solitamente essere dimostrate in studi basati sulla forza lavoro; la misura di esposizione più appropriata può, tuttavia, differire tra le malattie. Alquanto sconcertante è il fatto che, sebbene le relazioni esposizione-risposta differiscano tra le forze lavoro, queste differenze possono essere spiegate solo in parte dalla fibra, dalla dimensione delle particelle e dal processo industriale. Tuttavia, tali relazioni esposizione-risposta hanno costituito la base scientifica per la valutazione del rischio e per la definizione dei livelli di esposizione ammissibili, originariamente incentrati sul controllo dell'asbestosi (Selikoff e Lee 1978). Poiché la prevalenza e/o l'incidenza di questa condizione è diminuita, si è spostata la preoccupazione per garantire la protezione della salute umana contro i tumori correlati all'amianto. Nell'ultimo decennio sono state sviluppate tecniche per la misurazione quantitativa del carico di polvere polmonare o della dose biologica direttamente in termini di fibre per grammo di tessuto polmonare secco. Inoltre, l'analisi a raggi X che eroga energia (EDXA) consente una caratterizzazione precisa di ciascuna fibra per tipo di fibra (Churg 1991). Sebbene la standardizzazione dei risultati tra i laboratori non sia stata ancora raggiunta, i confronti dei risultati ottenuti all'interno di un determinato laboratorio sono utili e le misurazioni del carico polmonare hanno aggiunto un nuovo strumento per la valutazione dei casi. Inoltre, l'applicazione di queste tecniche negli studi epidemiologici ha
- ha confermato la biopersistenza delle fibre di anfibolo nel polmone rispetto alle fibre di crisotilo
- carico di fibre identificato nei polmoni di alcuni individui in cui l'esposizione è stata dimenticata, remota o ritenuta non importante
- dimostrato un gradiente di carico polmonare associato alla residenza rurale e urbana e all'esposizione professionale e
- confermato un gradiente di fibre nel carico di polvere polmonare associato alle principali malattie correlate all'amianto (Becklake e Caso 1994).
asbestosi
Definizione e storia
asbestosi è il nome dato alla pneumoconiosi conseguente all'esposizione alla polvere di amianto. Il termine pneumoconiosi è usato qui come definito nell'articolo “Pneumoconiosi: definizioni”, di questo Enciclopedia come una condizione in cui vi è “accumulo di polvere nei polmoni e risposte dei tessuti alla polvere”. Nel caso dell'asbestosi, la reazione tissutale è collagenica, e determina un'alterazione permanente dell'architettura alveolare con cicatrizzazione. Già nel 1898 il Rapporto annuale dell'ispettore capo delle fabbriche di Sua Maestà conteneva un riferimento al rapporto di un ispettore di fabbrica sulle conseguenze negative per la salute dell'esposizione all'amianto, e il 1899 Relazione conteneva i dettagli di uno di questi casi in un uomo che aveva lavorato per 12 anni in una delle fabbriche tessili di recente costituzione a Londra, in Inghilterra. L'autopsia ha rivelato una fibrosi grave diffusa del polmone e quelli che successivamente sono diventati noti come corpi di amianto sono stati osservati al successivo riesame istologico dei vetrini. Poiché la fibrosi del polmone è una condizione non comune, si ritenne che l'associazione fosse causale e il caso fu presentato come prova a un comitato sul risarcimento per malattia industriale nel 1907 (Browne 1994). Nonostante la comparsa di rapporti di natura simile presentati da ispettori del Regno Unito, dell'Europa e del Canada nel decennio successivo, il ruolo dell'esposizione all'amianto nella genesi della condizione non è stato generalmente riconosciuto fino a quando non è stato pubblicato un caso clinico nel British Medical Journal nel 1927. In questo rapporto, il termine asbestosi polmonare fu usato per la prima volta per descrivere questa particolare pneumoconiosi, e fu fatto un commento sulla preminenza delle reazioni pleuriche associate, in contrasto, per esempio, con la silicosi, la principale pneumoconiosi riconosciuta all'epoca (Selikoff e Lee 1978). Negli anni '1930, due importanti studi basati sulla forza lavoro condotti tra i lavoratori tessili, uno nel Regno Unito e uno negli Stati Uniti, hanno fornito prove di una relazione esposizione-risposta (e quindi probabile causalità) tra livello e durata dell'esposizione e radiografia alterazioni indicative di asbestosi. Questi rapporti costituirono la base dei primi regolamenti di controllo nel Regno Unito, promulgati nel 1930, e dei primi valori limite di soglia per l'amianto pubblicati dalla Conferenza americana degli igienisti governativi e industriali nel 1938 (Selikoff e Lee 1978).
Patologia
Le alterazioni fibrotiche che caratterizzano l'asbestosi sono la conseguenza di un processo infiammatorio innescato dalle fibre trattenute nel polmone. La fibrosi da asbestosi è interstiziale, diffusa, tende a interessare preferenzialmente i lobi inferiori e le zone periferiche e, nel caso avanzato, si associa ad obliterazione della normale architettura polmonare. La fibrosi della pleura adiacente è comune. Nulla nelle caratteristiche istologiche dell'asbestosi la distingue dalla fibrosi interstiziale dovuta ad altre cause, eccetto la presenza di amianto nei polmoni sia sotto forma di corpi di amianto, visibili al microscopio ottico, sia come fibre non rivestite, la maggior parte delle quali sono troppo sottili per essere visto se non per mezzo di microscopia elettronica. Pertanto, l'assenza di corpi di amianto nelle immagini derivate dalla microscopia ottica non esclude né l'esposizione né la diagnosi di asbestosi. All'estremo opposto dello spettro della gravità della malattia, la fibrosi può essere limitata a relativamente poche zone e interessare principalmente le regioni peribronchiolari (vedi figura 4), dando origine a quella che è stata chiamata malattia delle piccole vie aeree correlata all'amianto. Di nuovo, tranne forse per un interessamento più esteso delle piccole vie aeree membranose, nulla nei cambiamenti istologici di questa condizione la distingue dalla malattia delle piccole vie aeree dovuta ad altre cause (come il fumo di sigaretta o l'esposizione ad altre polveri minerali) diverse dalla presenza di amianto nelle il polmone. La malattia delle piccole vie aeree può essere l'unica manifestazione di fibrosi polmonare correlata all'amianto o può coesistere con vari gradi di fibrosi interstiziale, cioè asbestosi (Wright et al. 1992). Criteri attentamente considerati sono stati pubblicati per la classificazione patologica dell'asbestosi (Craighead et al. 1982). In generale, l'estensione e l'intensità della fibrosi polmonare si riferiscono al carico di polvere polmonare misurato (Liddell e Miller 1991).
Figura 4. Malattia delle piccole vie aeree correlata all'amianto
La fibrosi peribronchiolare e l'infiltrazione di cellule infiammatorie sono visibili su una sezione istologica di un bronchiolo respiratorio (R) e delle sue divisioni distali o dotti alveolari (A). Il polmone circostante è per lo più normale ma con ispessimento focale del tessuto interstiziale (freccia), che rappresenta l'asbestosi precoce. Fonte: Fraser et al. 1990
Caratteristiche cliniche
La mancanza di respiro, il disturbo più precoce, più costantemente riportato e più doloroso, ha portato l'asbestosi a essere definita una malattia monosintomatica (Selikoff e Lee 1978). La mancanza di respiro precede altri sintomi che includono una tosse secca, spesso fastidiosa, e senso di costrizione toracica, che si ritiene siano associati a reazioni pleuriche. Si sentono rantoli inspiratori tardivi o crepitii che persistono dopo la tosse, prima nell'ascella e sopra le basi polmonari, prima di diventare più generalizzati con l'avanzare della condizione, e si pensa che siano dovuti all'apertura esplosiva delle vie aeree che si chiudono all'espirazione. Si pensa che rantoli grossolani e ronchi, se presenti, riflettano la bronchite sia in risposta al lavoro in un ambiente polveroso, sia a causa del fumo.
Imaging del torace
Tradizionalmente, la radiografia del torace è stata il singolo strumento diagnostico più importante per stabilire la presenza di asbestosi. Ciò è stato facilitato dall'uso della classificazione radiologica dell'ILO (1980), che classifica le piccole opacità irregolari che sono caratteristiche dell'asbestosi su un continuum dall'assenza di malattia alla malattia più avanzata, sia per gravità (descritta come profusione su un 12- scala in punti da –/0 a 3/+) ed estensione (descritta come il numero di zone interessate). Nonostante le differenze tra i lettori, anche tra coloro che hanno completato corsi di formazione alla lettura, questa classificazione si è rivelata particolarmente utile negli studi epidemiologici, ed è stata utilizzata anche clinicamente. Tuttavia, i cambiamenti patologici dell'asbestosi possono essere presenti alla biopsia polmonare fino al 20% dei soggetti con una normale radiografia del torace. Inoltre, piccole opacità irregolari di bassa profusione (ad esempio, 1/0 sulla scala ILO) non sono specifiche per l'asbestosi ma possono essere viste in relazione ad altre esposizioni, per esempio al fumo di sigaretta (Browne 1994). La tomografia computerizzata (TC) ha rivoluzionato l'imaging delle malattie polmonari interstiziali, compresa l'asbestosi, con la tomografia computerizzata ad alta risoluzione (HRCT) aggiungendo una maggiore sensibilità alla rilevazione delle malattie interstiziali e pleuriche (Fraser et al. 1990). Le caratteristiche dell'asbestosi che possono essere identificate dall'HRCT includono linee centrali interlobulari (settali) e intralobulari ispessite, bande parenchimali, linee subpleuriche curvilinee e densità subpleuriche dipendenti, le prime due sono le più distintive per l'asbestosi (Fraser et al. 1990). HRCT può anche identificare questi cambiamenti nei casi con deficit della funzione polmonare in cui la radiografia del torace non è conclusiva. Sulla base dell'HRCT post mortem, è stato dimostrato che le linee intralobulari ispessite sono correlate con la fibrosi peribronchiolare e le linee interlobulari ispessite con la fibrosi interstiziale (Fraser et al. 1990). Finora, non è stato sviluppato alcun metodo di lettura standardizzato per l'uso dell'HRCT nelle malattie correlate all'amianto. Oltre al suo costo, il fatto che un dispositivo CT sia un'installazione ospedaliera rende improbabile che possa sostituire la radiografia del torace per la sorveglianza e gli studi epidemiologici; il suo ruolo rimarrà probabilmente limitato all'indagine di casi individuali oa studi pianificati destinati ad affrontare questioni specifiche. La Figura 21 illustra l'uso dell'imaging del torace nella diagnosi delle malattie polmonari correlate all'amianto; il caso mostrato presenta asbestosi, malattia pleurica correlata all'amianto e cancro ai polmoni. Le grandi opacità, una complicazione di altre pneumoconiosi, in particolare la silicosi, sono insolite nell'asbestosi e di solito sono dovute ad altre condizioni come il cancro del polmone (vedi il caso descritto nella figura 5) o l'atelettasia arrotondata.
Figura 5. Imaging del torace nella malattia polmonare correlata all'amianto.
Una radiografia del torace postero-anteriore (A) mostra asbestosi coinvolgente entrambi i polmoni e valutata come categoria ILO 1/1, associata a ispessimento pleurico bilaterale (frecce aperte) e opacità vagamente definita (punte di freccia) nel lobo superiore sinistro. Alla scansione HRCT (B), è stato dimostrato che si trattava di una massa densa (M) a ridosso della pleura e la biopsia con ago transtoracico ha rivelato un adenocarcinoma del polmone. Sempre alla TC (C), ad alta attenuazione si notano placche pleuriche (punte di freccia) e una sottile opacità curvilinea nel parenchima sottostante le placche con anomalia interstiziale nel polmone tra l'opacità e la pleura. Fonte: Fraser et al. 1990
Test di funzionalità polmonare
La fibrosi polmonare interstiziale accertata dovuta all'esposizione all'amianto, come la fibrosi polmonare accertata dovuta ad altre cause, è solitamente ma non invariabilmente associata a un profilo di funzionalità polmonare restrittivo (Becklake 1994). Le sue caratteristiche includono volumi polmonari ridotti, in particolare capacità vitale (VC) con conservazione del rapporto tra volume espiratorio forzato in 1 secondo e capacità vitale forzata (FEV1/FVC%), riduzione della compliance polmonare e compromissione dello scambio gassoso. Limitazione del flusso d'aria con FEV ridotto1/FVC può, tuttavia, essere presente anche come risposta ad un ambiente di lavoro polveroso o al fumo di sigaretta. Nelle prime fasi dell'asbestosi, quando i cambiamenti patologici sono limitati alla fibrosi peribronchiolare e anche prima che piccole opacità irregolari siano evidenti sulla radiografia del torace, l'alterazione dei test che riflettono la disfunzione delle piccole vie aeree come la portata massima medio-espiratoria può essere l'unico segno di disfunzione respiratoria. Le risposte allo stress dell'esercizio possono anche essere compromesse all'inizio della malattia, con una maggiore ventilazione in relazione al fabbisogno di ossigeno dell'esercizio (a causa di una maggiore frequenza respiratoria e respirazione superficiale) e O ridotta2 scambio. Con il progredire della malattia, è richiesto sempre meno esercizio fisico per compromettere l'O2 scambio. Dato che il lavoratore esposto all'amianto può presentare caratteristiche di un profilo di funzione polmonare sia restrittivo che ostruttivo, il medico saggio interpreta il profilo di funzione polmonare nel lavoratore dell'amianto per quello che è, come una misura di menomazione, piuttosto che come un aiuto per diagnosi. Le funzioni polmonari, in particolare la capacità vitale, forniscono uno strumento utile per il follow-up dei soggetti individualmente o in studi epidemiologici, ad esempio dopo la cessazione dell'esposizione, per monitorare la storia naturale dell'asbestosi o della malattia pleurica correlata all'amianto.
Altri esami di laboratorio
Il lavaggio broncoalveolare è sempre più utilizzato come strumento clinico nelle indagini sulle malattie polmonari correlate all'amianto:
- escludere altre diagnosi
- per valutare l'attività delle reazioni polmonari in studio come la fibrosi o
- identificare l'agente sotto forma di corpi o fibre di amianto.
Viene anche utilizzato per studiare i meccanismi delle malattie negli esseri umani e negli animali (Bégin, Cantin e Massé 1989). L'assorbimento di Gallio-67 viene utilizzato come misura dell'attività del processo polmonare e anche gli anticorpi antinucleari sierici (ANA) e i fattori reumatoidi (RF), che riflettono entrambi lo stato immunologico dell'individuo, sono stati studiati come fattori influenzare la progressione della malattia e/o tenere conto delle differenze individuali in risposta a quello che sembra essere lo stesso livello e la stessa dose di esposizione.
Epidemiologia compresa la storia naturale
La prevalenza dell'asbestosi radiologica documentata nelle indagini basate sulla forza lavoro varia considerevolmente e, come ci si potrebbe aspettare, queste differenze si riferiscono a differenze nella durata e nell'intensità dell'esposizione piuttosto che a differenze tra i luoghi di lavoro. Tuttavia, anche quando questi vengono presi in considerazione restringendo il confronto delle relazioni di risposta all'esposizione a quegli studi in cui le stime dell'esposizione sono state individualizzate per ciascun membro della coorte e basate sulla storia lavorativa e sulle misurazioni dell'igiene industriale, sono evidenti gradienti marcati relativi alle fibre e al processo (Liddell e Miller 1991). Ad esempio, una prevalenza del 5% di piccole opacità irregolari (1/0 o più sulla classificazione ILO) è risultata da un'esposizione cumulativa a circa 1,000 anni di fibra nei minatori di crisotilo del Quebec, a circa 400 anni di fibra nei minatori di crisotilo della Corsica e a meno di 10 anni di fibra nei minatori di crocidolite sudafricani e australiani. Al contrario, per i lavoratori tessili esposti al crisotilo del Quebec, una prevalenza del 5% di piccole opacità irregolari risultava da un'esposizione cumulativa a meno di 20 anni di fibra. Anche gli studi sul carico di polvere polmonare sono coerenti con un gradiente di fibre per evocare l'asbestosi: in 29 uomini nei cantieri navali del Pacifico con asbestosi associata principalmente all'esposizione all'amosite, il carico polmonare medio trovato nel materiale dell'autopsia era di 10 milioni di fibre di amosite per grammo di tessuto polmonare secco rispetto a un carico medio di crisotilo di 30 milioni di fibre per grammo di tessuto polmonare secco in 23 minatori e mugnai di crisotilo del Quebec (Becklake e Caso 1994). La distribuzione delle dimensioni delle fibre contribuisce ma non spiega completamente queste differenze, suggerendo che altri fattori specifici della pianta, inclusi altri contaminanti sul posto di lavoro, possono svolgere un ruolo.
L'asbestosi può rimanere stabile o progredire, ma probabilmente non regredisce. I tassi di progressione aumentano con l'età, con l'esposizione cumulativa e con l'estensione della malattia esistente, ed è più probabile che si verifichi se l'esposizione è stata alla crocidolite. L'asbestosi radiologica può sia progredire che apparire molto tempo dopo la cessazione dell'esposizione. Il deterioramento delle funzioni polmonari può verificarsi anche dopo che l'esposizione è cessata (Liddell e Miller 1991). Una questione importante (e su cui l'evidenza epidemiologica non è coerente) è se l'esposizione continua aumenta la possibilità di progressione una volta che si sono sviluppate alterazioni radiologiche (Browne 1994; Liddell e Miller 1991). In alcune giurisdizioni, ad esempio nel Regno Unito, il numero di casi di asbestosi presentati per il risarcimento del lavoratore è diminuito negli ultimi decenni, riflettendo i controlli sul posto di lavoro messi in atto negli anni '1970 (Meredith e McDonald 1994). In altri paesi, per esempio in Germania (Gibbs, Valic e Browne 1994), i tassi di asbestosi continuano ad aumentare. Negli Stati Uniti, i tassi di mortalità correlata all'amianto aggiustati per l'età (basati sulla menzione dell'asbestosi nel certificato di morte come causa di morte o come ruolo contribuente) per l'età 1+ sono aumentati da meno di 1 per milione nel 1960 a oltre 2.5 nel 1986 e 3 nel 1990 (Dipartimento della salute e dei servizi umani degli Stati Uniti, 1994).
Diagnosi e gestione dei casi
La diagnosi clinica dipende da:
- stabilire la presenza della malattia
- stabilire se l'esposizione si è verificata e
- valutare se l'esposizione potesse aver causato la malattia.
La radiografia del torace rimane lo strumento chiave per stabilire la presenza di malattia, integrata da HRCT se disponibile nei casi in cui vi è dubbio. Altre caratteristiche oggettive sono la presenza di crepitii basali, mentre il livello di funzionalità polmonare, inclusa la sfida dell'esercizio, è utile per stabilire la compromissione, passaggio necessario per la valutazione della compensazione. Poiché né la patologia, i cambiamenti radiologici, né i sintomi e i cambiamenti della funzionalità polmonare associati all'asbestosi sono diversi da quelli associati alla fibrosi polmonare interstiziale dovuta ad altre cause, stabilire l'esposizione è fondamentale per la diagnosi. Inoltre, i numerosi usi dei prodotti a base di amianto, il cui contenuto spesso non è noto all'utente, rendono la cronologia delle esposizioni un esercizio di interrogatorio molto più scoraggiante di quanto si pensasse in precedenza. Se la storia dell'esposizione appare inadeguata, l'identificazione dell'agente nei campioni biologici (espettorato, lavaggio broncoalveolare e quando indicato, biopsia) può corroborare l'esposizione; la dose sotto forma di carico polmonare può essere valutata quantitativamente mediante autopsia o nei polmoni rimossi chirurgicamente. L'evidenza dell'attività della malattia (da una scintigrafia al gallio-67 o da un lavaggio broncoalveolare) può aiutare a stimare la prognosi, un problema chiave in questa condizione irreversibile. Anche in assenza di prove epidemiologiche coerenti che la progressione sia rallentata una volta cessata l'esposizione, un tale corso può essere prudente e certamente desiderabile. Non è, tuttavia, una decisione facile da prendere o raccomandare, in particolare per i lavoratori più anziani con scarse possibilità di riqualificazione professionale. Certamente l'esposizione non dovrebbe continuare in qualsiasi luogo di lavoro non conforme agli attuali livelli di esposizione consentiti. I criteri per la diagnosi di asbestosi ai fini epidemiologici sono meno impegnativi, in particolare per gli studi trasversali basati sulla forza lavoro che includono coloro che stanno abbastanza bene per essere al lavoro. Questi di solito affrontano questioni di causalità e spesso utilizzano marcatori che indicano una malattia minima, in base al livello di funzionalità polmonare o ai cambiamenti nella radiografia del torace. Al contrario, i criteri per la diagnosi a fini medico-legali sono notevolmente più rigorosi e variano a seconda dei sistemi amministrativi legali in cui operano, variando tra gli stati all'interno dei paesi e tra i paesi.
Malattia pleurica correlata all'amianto
Prospettiva storica
Le prime descrizioni dell'asbestosi menzionano la fibrosi della pleura viscerale come parte del processo patologico (vedi “Patologia”, pagina 10.55). Negli anni '1930 sono stati segnalati anche placche pleuriche circoscritte, spesso calcificate, nella pleura parietale (che riveste la parete toracica e ricopre la superficie del diaframma), e che si verificano in quelli con esposizione ambientale, non occupazionale. Uno studio del 1955 basato sulla forza lavoro di una fabbrica tedesca ha riportato una prevalenza del 5% di alterazioni pleuriche sulla radiografia del torace, attirando così l'attenzione sul fatto che la malattia pleurica potrebbe essere la principale se non l'unica manifestazione di esposizione. Le reazioni pleuriche visceroparietali, tra cui la fibrosi pleurica diffusa, il versamento pleurico benigno (riportato per la prima volta negli anni '1960) e l'atelettasia arrotondata (riportata per la prima volta negli anni '1980) sono ora tutte considerate reazioni correlate che sono utilmente distinte dalle placche pleuriche sulla base della patologia e probabilmente della patogenesi , così come le caratteristiche cliniche e la presentazione. Nelle giurisdizioni in cui i tassi di prevalenza e/o incidenza dell'asbestosi sono in diminuzione, le manifestazioni pleuriche, sempre più comuni nelle indagini, sono sempre più la base per il rilevamento di un'esposizione passata e sempre più la ragione per cui un individuo cerca assistenza medica.
Placche pleuriche
Le placche pleuriche sono lesioni irregolari lisce, rilevate, bianche ricoperte di mesotelio e che si trovano sulla pleura parietale o sul diaframma (figura 6). Hanno dimensioni variabili, sono spesso multiple e tendono a calcificarsi con l'aumentare dell'età (Browne 1994). Solo una piccola percentuale di quelli rilevati all'autopsia è visibile sulla radiografia del torace, sebbene la maggior parte possa essere rilevata dall'HRCT. In assenza di fibrosi polmonare, le placche pleuriche possono non causare sintomi e possono essere rilevate solo nelle indagini di screening mediante radiografia del torace. Tuttavia, nelle indagini sulla forza lavoro, sono costantemente associati a compromissione della funzione polmonare modesta ma misurabile, principalmente in VC e FVC (Ernst e Zejda 1991). Nelle indagini radiologiche negli Stati Uniti, sono riportati tassi dell'1% negli uomini senza esposizione nota e del 2.3% negli uomini che includono quelli nelle popolazioni urbane, con esposizione professionale. I tassi sono più alti anche nelle comunità con industrie di amianto o tassi di utilizzo elevati, mentre in alcune forze lavoro, come lavoratori della lamiera, isolatori, idraulici e ferrovieri, i tassi possono superare il 50%. In un'indagine autoptica finlandese del 1994 su 288 uomini di età compresa tra 35 e 69 anni che morirono improvvisamente, le placche pleuriche furono rilevate nel 58% e mostrarono la tendenza ad aumentare con l'età, con la probabilità di esposizione (basata sulla storia), con la concentrazione di fibre di amianto nel tessuto polmonare e con il fumo (Karjalainen et al. 1994). La frazione eziologica delle placche attribuibili a un carico di polvere polmonare di 0.1 milioni di fibre per grammo di tessuto polmonare è stata stimata al 24%, (questo valore è considerato una sottostima). Anche gli studi sul carico di polvere polmonare sono coerenti con il gradiente di fibre nella potenza per evocare reazioni pleuriche; in 103 uomini con esposizione all'amosite nei cantieri navali del Pacifico, tutti con placche pleuriche, il carico polmonare medio dell'autopsia era di 1.4 milioni di fibre per grammo di tessuto polmonare, rispetto a 15.5 e 75 milioni di fibre per grammo di tessuto polmonare rispettivamente per crisotilo e tremolite in 63 I minatori e i mugnai di crisotilo del Quebec esaminati allo stesso modo (Becklake e Caso 1994).
Figura 6. Malattia pleurica correlata all'amianto
Una placca pleurica diaframmatica (A) è visibile in un campione autoptico come un focolaio liscio e ben definito di fibrosi sul diaframma di un operaio edile con esposizione accidentale ad amianto e corpi di amianto nel polmone. La fibrosi pleurica viscerale (B) è osservata su un campione di polmone autoptico gonfiato e si irradia da due fuochi centrali sulla pleura viscerale del polmone di un operaio edile con esposizione all'amianto che presentava anche diverse placche pleuriche parietali. Fonte: Fraser et al. 1990.
Reazioni pleuriche visceroparietali
Sebbene la patologia e la patogenesi delle diverse forme di reazione visceroparietale all'esposizione all'amianto siano quasi certamente correlate, le loro manifestazioni cliniche e il modo in cui vengono rilevate differiscono. Reazioni pleuriche essudative acute possono manifestarsi sotto forma di versamenti in soggetti i cui polmoni non manifestano altre malattie correlate all'amianto o come esacerbazione della gravità e dell'estensione delle reazioni pleuriche esistenti. Tali versamenti pleurici sono chiamati benigni per distinguerli dai versamenti associati al mesotelioma maligno. I versamenti pleurici benigni si verificano tipicamente da 10 a 15 anni dopo la prima esposizione (o dopo un'esposizione passata limitata) in individui di 20 e 30 anni. Di solito sono transitori ma possono ripresentarsi, possono coinvolgere uno o entrambi i lati del torace simultaneamente o in sequenza e possono essere silenti o associati a sintomi tra cui oppressione toracica e/o dolore pleurico e dispnea. Il liquido pleurico contiene leucociti, spesso sangue, ed è ricco di albumina; solo raramente contiene corpi o fibre di amianto che si possono però trovare nel materiale bioptico della pleura o del polmone sottostante. La maggior parte dei versamenti pleurici benigni si risolve spontaneamente, sebbene in una piccola percentuale di soggetti (dell'ordine del 10% in una serie) questi versamenti possano evolvere in fibrosi pleurica diffusa (vedi figura 6), con o senza lo sviluppo di fibrosi polmonare. Le reazioni pleuriche locali possono anche ripiegarsi su se stesse, intrappolando il tessuto polmonare e causando lesioni ben definite chiamate atelettasia arrotondata or pseudotumore perché possono avere l'aspetto radiologico del cancro ai polmoni. Contrariamente alle placche pleuriche, che raramente causano sintomi, le reazioni pleuriche visceroparietali sono solitamente associate a una certa mancanza di respiro e compromissione della funzione polmonare, in particolare quando c'è obliterazione dell'angolo costofrenico. In uno studio, per esempio, il deficit medio di FVC era di 0.07 l quando era coinvolta la parete toracica e di 0.50 l quando era coinvolto l'angolo costofrenico (Ernst e Zejda in Liddell e Miller 1991). Come già indicato, la distribuzione e i determinanti delle reazioni pleuriche variano considerevolmente tra le forze lavoro, con tassi di prevalenza che aumentano con:
- tempo di permanenza stimato della fibra nel polmone (misurato come tempo dalla prima esposizione)
- esposizioni principalmente ad anfibolo o incluso e
- possibile intermittenza dell'esposizione, dati gli alti tassi di contaminazione nelle occupazioni in cui l'uso di materiali di amianto è intermittente, ma l'esposizione probabilmente pesante.
Lung Cancer
Prospettiva storica
Gli anni '1930 videro la pubblicazione di una serie di casi clinici negli Stati Uniti, nel Regno Unito e in Germania di cancro ai polmoni (una condizione molto meno comune allora di quanto lo sia oggi) nei lavoratori dell'amianto, la maggior parte dei quali soffriva anche di asbestosi di vario grado di severità. Ulteriori prove dell'associazione tra le due condizioni furono fornite nel Rapporto annuale del 1947 dell'ispettore capo delle fabbriche di Sua Maestà, che notava che il cancro ai polmoni era stato segnalato nel 13.2% dei decessi maschili attribuiti all'asbestosi nel periodo dal 1924 al 1946 e solo in 1.3% dei decessi maschili attribuiti alla silicosi. Il primo studio ad affrontare l'ipotesi causale è stato uno studio sulla mortalità di coorte di un grande impianto tessile di amianto del Regno Unito (Doll 1955), uno dei primi studi di questo tipo basati sulla forza lavoro, e nel 1980, dopo almeno otto studi di questo tipo su altrettante forze lavoro aveva confermato una relazione esposizione-risposta, l'associazione era generalmente accettata come causale (McDonald e McDonald in Antman e Aisner 1987).
Caratteristiche cliniche e patologia
In assenza di altre malattie associate all'amianto, le caratteristiche cliniche ei criteri per la diagnosi del cancro del polmone associato all'amianto non sono diversi da quelli del cancro del polmone non associato all'esposizione all'amianto. In origine, i tumori polmonari associati all'amianto erano considerati tumori cicatriziali, simili al cancro polmonare osservato in altre forme di fibrosi polmonare diffusa come la sclerodermia. Le caratteristiche che favorivano questa visione erano la loro localizzazione nei lobi polmonari inferiori (dove l'asbestosi è di solito più marcata), la loro origine a volte multicentrica e una preponderanza di adenocarcinoma in alcune casistiche. Tuttavia, nella maggior parte degli studi basati sulla forza lavoro riportati, la distribuzione dei tipi di cellule non era diversa da quella osservata negli studi su popolazioni non esposte all'amianto, a sostegno dell'opinione che l'amianto stesso possa essere cancerogeno per l'uomo, una conclusione raggiunta dall'Agenzia internazionale per la ricerca sul cancro (Organizzazione mondiale della sanità: Agenzia internazionale per la ricerca sul cancro 1982). La maggior parte, ma non tutti, i tumori polmonari correlati all'amianto si verificano in associazione con l'asbestosi radiologica (vedi sotto).
Epidemiologia
Studi di coorte confermano che il rischio di cancro al polmone aumenta con l'esposizione, anche se il tasso frazionario di aumento per ogni fibra per millilitro per anno esposto varia ed è correlato sia al tipo di fibra che al processo industriale (Health Effects Institute—Asbestos Research 1991). Ad esempio, per le esposizioni principalmente al crisotilo nella produzione di prodotti minerari, molitori e di attrito, l'aumento variava dallo 0.01 allo 0.17% circa e nella produzione tessile dall'1.1 al 2.8%, mentre per l'esposizione ai prodotti isolanti amosite e ad alcuni prodotti cementizi che comportano esposizioni miste fibra, sono stati registrati tassi fino al 4.3 e 6.7% (Nicholson 1991). Studi di coorte sui lavoratori dell'amianto confermano anche che il rischio di cancro è dimostrabile per i non fumatori e che il rischio è aumentato (più vicino al moltiplicativo che additivo) dal fumo di sigaretta (McDonald e McDonald in Antman e Aisner 1987). Il rischio relativo di cancro al polmone diminuisce dopo la cessazione dell'esposizione, sebbene il declino appaia più lento di quello che si verifica dopo aver smesso di fumare. Anche gli studi sul carico di polvere polmonare sono coerenti con un gradiente di fibre nella produzione di cancro ai polmoni; 32 uomini nei cantieri navali del Pacifico con esposizione principalmente all'amosite avevano un carico di polvere polmonare di 1.1 milioni di fibre di amosite per grammo di tessuto polmonare secco rispetto a 36 minatori di crisotilo del Quebec con un carico medio di polvere polmonare di 13 milioni di fibre di crisotilo per grammo di tessuto polmonare (Becklake e Caso 1994).
Relazione con l'asbestosi
Nello studio autoptico del 1955 sulle cause di morte in 102 lavoratori impiegati nella fabbrica tessile di amianto del Regno Unito di cui sopra (Doll 1955), il cancro ai polmoni è stato riscontrato in 18 individui, 15 dei quali avevano anche l'asbestosi. Tutti i soggetti in cui sono state riscontrate entrambe le condizioni avevano lavorato per almeno 9 anni prima del 1931, quando furono introdotte le normative nazionali per il controllo delle polveri di amianto. Queste osservazioni hanno suggerito che con la diminuzione dei livelli di esposizione, diminuiva anche il rischio concorrente di morte per asbestosi ei lavoratori vivevano abbastanza a lungo da mostrare lo sviluppo del cancro. Nella maggior parte degli studi basati sulla forza lavoro, i lavoratori più anziani con un lungo servizio hanno alcune prove patologiche di asbestosi (o malattia delle piccole vie aeree correlata all'amianto) all'autopsia, anche se questo può essere minimo e non rilevabile sulla radiografia del torace in vita (McDonald e McDonald in Antman e Aisner 1987). Diversi studi di coorte, ma non tutti, sono coerenti con l'idea che non tutti i tumori polmonari in eccesso nelle popolazioni esposte all'amianto siano correlati all'asbestosi. Più di un meccanismo patogenetico può infatti essere responsabile dei tumori polmonari nei soggetti esposti all'amianto a seconda della sede e della deposizione delle fibre. Ad esempio, si ritiene che le fibre lunghe e sottili, che si depositano preferenzialmente in corrispondenza delle biforcazioni delle vie aeree, si concentrino e agiscano come induttori del processo di cancerogenesi attraverso il danno cromosomico. I promotori di questo processo possono includere la continua esposizione alle fibre di amianto o al fumo di tabacco (Lippman 1995). È più probabile che tali tumori siano di tipo a cellule squamose. Al contrario, nei polmoni che sono la sede della fibrosi, la cancerogenesi può derivare dal processo fibrotico: è più probabile che tali tumori siano adenocarcinomi.
Implicazioni e imputabilità
Mentre i determinanti dell'eccesso di rischio di cancro possono essere ricavati per le popolazioni esposte, l'attribuibilità nel singolo caso no. Ovviamente, l'attribuibilità all'esposizione all'amianto è più probabile e credibile in un soggetto esposto con asbestosi che non ha mai fumato che in un soggetto esposto senza asbestosi che fuma. Né questa probabilità può essere modellata ragionevolmente. Le misurazioni del carico di polvere polmonare possono integrare un'attenta valutazione clinica, ma ogni caso deve essere valutato nel merito (Becklake 1994).
Mesotelioma maligno
Patologia, diagnosi, accertamento e caratteristiche cliniche
I mesoteliomi maligni derivano dalle cavità sierose del corpo. Circa due terzi insorgono nella pleura, circa un quinto nel peritoneo, mentre il pericardio e la tunica vaginale sono colpiti molto meno frequentemente (McDonald e McDonald in Lidell e Miller 1991). Poiché le cellule mesoteliali sono pluripotenti, le caratteristiche istologiche dei tumori mesoteliali possono variare; nella maggior parte delle serie, le forme epiteliali, sarcomatose e miste rappresentano rispettivamente circa il 50, 30 e 10% dei casi. La diagnosi di questo raro tumore, anche nelle mani di patologi esperti, non è facile, e i patologi del panel del mesotelioma spesso confermano solo una piccola percentuale, in alcuni studi meno del 50% dei casi sottoposti a revisione. È stata sviluppata una varietà di tecniche citologiche e immunoistochimiche per aiutare a differenziare il mesotelioma maligno dalle principali diagnosi cliniche alternative, vale a dire cancro secondario o iperplasia mesoteliale reattiva; questo rimane un campo di ricerca attivo in cui le aspettative sono alte ma i risultati inconcludenti (Jaurand, Bignon e Brochard 1993). Per tutti questi motivi, l'accertamento dei casi per le indagini epidemiologiche non è semplice e, anche se basato sui registri tumori, può risultare incompleto. Inoltre, è necessaria la conferma da parte di gruppi di esperti che utilizzino criteri patologici specifici per garantire la comparabilità dei criteri di registrazione.
Caratteristiche cliniche
Il dolore è solitamente la caratteristica di presentazione. Per i tumori pleurici, questo inizia nel torace e/o nelle spalle e può essere grave. Segue dispnea, associata a versamento pleurico e/o progressivo rivestimento del polmone da parte del tumore, e perdita di peso. Con i tumori peritoneali, il dolore addominale è solitamente accompagnato da gonfiore. Le caratteristiche di imaging sono illustrate nella figura 7. Il decorso clinico è generalmente rapido e i tempi di sopravvivenza mediani, sei mesi in un rapporto del 1973 e otto mesi in un rapporto del 1993, sono cambiati poco negli ultimi due decenni, nonostante la maggiore consapevolezza pubblica e medica che spesso porta a una diagnosi precoce e nonostante i progressi nelle tecniche diagnostiche e un aumento del numero di opzioni terapeutiche per il cancro.
Figura 7. Mesotelioma maligno
Visto su un roetngenogram toracico eccessivamente penetrato (A) come una grande massa nella regione ascellare. Si noti la associata riduzione di volume dell'emotorace destro con marcato ispessimento nodulare irregolare della pleura di tutto il polmone destro. La TC (B) conferma l'ampio ispessimento pleurico che coinvolge la pleura parietale e mediastinica (frecce chiuse) all'interno e attorno alle costole. Fonte: Fraser et al. 1990
Epidemiologia
Nei 15 anni che seguirono la segnalazione del 1960 della serie di casi di mesotelioma del Capo Nordoccidentale, Sud Africa (Wagner 1996), la conferma internazionale dell'associazione venne da segnalazioni di altre serie di casi dall'Europa (Regno Unito, Francia, Germania, Olanda) , Stati Uniti (Illinois, Pennsylvania e New Jersey) e Australia, e di studi caso controllo provenienti da Regno Unito (4 città), Europa (Italia, Svezia, Olanda) e Stati Uniti e Canada. Gli odds ratio in questi studi variavano da 2 a 9. In Europa in particolare, l'associazione con le occupazioni nei cantieri navali era forte. Inoltre, studi sulla mortalità proporzionale in coorti esposte all'amianto hanno suggerito che il rischio era associato sia al tipo di fibra che al processo industriale, con tassi attribuibili al mesotelioma che andavano dallo 0.3% nell'estrazione di crisotilo all'1% nella produzione di crisotilo, rispetto al 3.4% nell'anfibolo minerario e manifatturiero e fino all'8.6% per l'esposizione a fibre miste nell'isolamento (McDonald e McDonald in Liddell e Miller 1991). Simili gradienti di fibre sono mostrati negli studi sulla mortalità di coorte che, dati i brevi tempi di sopravvivenza di questi tumori, sono un ragionevole riflesso dell'incidenza. Questi studi mostrano anche periodi di latenza più lunghi quando l'esposizione era al crisotilo rispetto agli anfiboli. La variazione geografica dell'incidenza è stata documentata utilizzando tassi canadesi specifici per età e sesso dal 1966 al 1972 per calcolare i tassi attesi (McDonald e McDonald in Liddell e Miller 1991); i rapporti tra i tassi (valori effettivamente osservati rispetto alle attese) erano 0.8 per gli Stati Uniti (1972), 1.1 per la Svezia (dal 1958 al 1967), 1.3 per la Finlandia (dal 1965 al 1969), 1.7 per il Regno Unito (dal 1967 al 1968) e 2.1 per Paesi Bassi (dal 1969 al 1971). Sebbene i fattori tecnici, incluso l'accertamento, possano ovviamente contribuire alla variazione registrata, i risultati suggeriscono tassi più elevati in Europa rispetto al Nord America.
Le tendenze temporali e le differenze di genere nell'incidenza del mesotelioma sono state utilizzate come misura dell'impatto sulla salute dell'esposizione all'amianto sulle popolazioni. Le migliori stime per i tassi complessivi nei paesi industrializzati prima del 1950 sono inferiori a 1.0 per milione per uomini e donne (McDonald e McDonald in Jaurand e Bignon 1993). Successivamente, i tassi sono aumentati costantemente negli uomini e per niente o meno nelle donne. Ad esempio, i tassi complessivi in uomini e donne per milione sono stati riportati a 11.0 e meno di 2.0 negli Stati Uniti nel 1982, 14.7 e 7.0 in Danimarca per il 1975-80, 15.3 e 3.2 nel Regno Unito per il 1980-83, e 20.9 e 3.6 nei Paesi Bassi per il 1978-87. Tassi più elevati negli uomini e nelle donne, ma escludendo i soggetti più giovani, sono stati riportati per i paesi minerari di crocidolite: 28.9 e 4.7 rispettivamente in Australia (età 2+) per il 1986, e 32.9 e 8.9 rispettivamente nei bianchi sudafricani (età 1+) per il 1988 ( Health Effects Institute—Ricerca sull'amianto 1991). È probabile che i tassi di aumento negli uomini riflettano l'esposizione professionale e, in tal caso, dovrebbero stabilizzarsi o diminuire entro il periodo di "incubazione" di 20-30 anni successivo all'introduzione dei controlli sul posto di lavoro e alla riduzione dei livelli di esposizione nella maggior parte dei luoghi di lavoro nella maggior parte dei luoghi di lavoro. Paesi industrializzati negli anni '1970. Nei paesi in cui i tassi di donne sono in aumento, questo aumento può riflettere il loro crescente impegno in occupazioni con esposizione al rischio, o la crescente contaminazione ambientale o interna dell'aria urbana (McDonald 1985).
Eziologia
I fattori ambientali sono chiaramente i principali determinanti del rischio di mesotelioma, l'esposizione all'amianto è il più importante, sebbene la presenza di gruppi familiari mantenga l'interesse per il ruolo potenziale dei fattori genetici. Tutti i tipi di fibre di amianto sono stati implicati nella produzione di mesotelioma, compresa l'antofillite per la prima volta in un recente rapporto dalla Finlandia (Meurman, Pukkala e Hakama 1994). Tuttavia, vi è un corpo sostanziale di prove, da studi sulla mortalità proporzionale e di coorte e studi sul carico polmonare, che suggeriscono il ruolo di un gradiente di fibre nella produzione di mesotelioma, il rischio è maggiore per le esposizioni a principalmente anfiboli o miscele di crisotilo anfibolo, rispetto a principalmente crisotilo esposizioni. Inoltre, ci sono differenze di velocità tra la forza lavoro per la stessa fibra a quello che sembra essere lo stesso livello di esposizione; questi rimangono da spiegare, sebbene la distribuzione delle dimensioni delle fibre sia un probabile fattore che contribuisce.
Il ruolo della tremolite è stato ampiamente dibattuto, dibattito acceso dall'evidenza della sua biopersistenza nel tessuto polmonare, animale e umano, rispetto a quella del crisotilo. Un'ipotesi plausibile è che le numerose fibre corte che raggiungono e si depositano nelle vie aeree polmonari periferiche e negli alveoli vengano scaricate nei vasi linfatici subpleurici dove si raccolgono; la loro potenza nella produzione di mesotelioma dipende dalla loro biopersistenza a contatto con le superfici pleuriche (Lippmann 1995). Negli studi sull'uomo, i tassi di mesotelioma sono inferiori per le popolazioni esposte sul posto di lavoro a crisotilo relativamente incontaminato da tremolite (ad esempio, nelle miniere dello Zimbabwe) rispetto a quelle esposte a crisotilo così contaminato (ad esempio, nelle miniere del Quebec), e questi risultati hanno stato replicato in studi su animali (Lippmann 1995). Inoltre, in un'analisi multivariata del carico di fibre polmonari nel materiale di uno studio caso controllo sul mesotelioma in tutto il Canada (McDonald et al. 1989), i risultati hanno suggerito che la maggior parte, se non tutti i mesoteliomi, potrebbero essere spiegati dal carico di fibre polmonari tremolite. Infine, una recente analisi della mortalità nella coorte di oltre 10,000 minatori e mugnai di crisotilo del Quebec nati tra il 1890 e il 1920, e seguiti fino al 1988 (McDonald e McDonald 1995), supporta questa visione: in quasi 7,300 decessi, i 37 decessi per mesotelioma erano concentrati in alcune miniere dell'area di Thetford, tuttavia il carico polmonare di 88 membri della coorte delle miniere implicate non differiva da quello dei minatori di altre miniere in termini di carico di fibre di crisotilo, solo in termini di carico di tremolite (McDonald et al. 1993 ).
Quella che è stata chiamata la questione del tremolite è forse la più importante delle questioni scientifiche attualmente dibattute, e ha anche implicazioni per la salute pubblica. Si deve anche notare l'importante fatto che in tutte le serie e giurisdizioni, una certa percentuale di casi si verifica senza che sia stata segnalata un'esposizione all'amianto e che solo in alcuni di questi casi gli studi sul carico di polvere polmonare indicano una precedente esposizione ambientale o professionale. Altre esposizioni professionali sono state implicate nella produzione di mesotelioma, ad esempio nell'estrazione di talco, vermiculite e possibilmente mica, ma in queste il minerale conteneva o tremolite o altre fibre (Bignon, Peto e Saracci 1989). Dovrebbe proseguire la ricerca aperta di altre esposizioni, professionali o non professionali, a fibre, inorganiche e organiche, e ad altri agenti che possono essere associati alla produzione di mesotelioma.
Altre malattie correlate all'amianto
Malattia cronica delle vie aeree
Solitamente inclusi in questa rubrica sono la bronchite cronica e la broncopneumopatia cronica ostruttiva (BPCO), entrambe diagnosticabili clinicamente, e l'enfisema, fino a poco tempo fa diagnosticato solo mediante esame patologico dei polmoni rimossi durante l'autopsia o altro (Becklake 1992). Una delle cause principali è il fumo e, negli ultimi decenni, la mortalità e la morbilità dovute a malattie croniche delle vie aeree sono aumentate nella maggior parte dei paesi industrializzati. Tuttavia, con il declino della pneumoconiosi in molte forze lavoro, sono emerse prove che implicano esposizioni professionali nella genesi della malattia cronica delle vie aeree, dopo aver preso in considerazione il ruolo dominante del fumo. È stato dimostrato che tutte le forme di malattia cronica delle vie aeree sono associate al lavoro in una varietà di occupazioni polverose, comprese quelle occupazioni in cui una componente importante della polvere che contaminava il posto di lavoro era l'amianto (Ernst e Zejda in Liddell e Miller 1991). Si pensa che sia implicato il carico totale di inquinanti, piuttosto che l'esposizione a uno qualsiasi dei suoi componenti particolari, in questo caso la polvere di amianto, più o meno allo stesso modo in cui viene visto l'effetto dell'esposizione al fumo sulle malattie croniche delle vie respiratorie, cioè in termini di onere totale dell'esposizione (ad esempio, come pacchetto-anno), nessuna esposizione a nessuno degli oltre 4,000 componenti del fumo di tabacco. (vedi altrove in questo volume per un'ulteriore discussione della relazione tra esposizioni professionali e malattie croniche delle vie aeree).
Altri tumori
In molti dei precedenti studi di coorte sui lavoratori esposti all'amianto, la mortalità attribuibile a tutti i tumori ha superato quella prevista, sulla base delle statistiche vitali nazionali o regionali. Mentre il cancro del polmone rappresentava la maggior parte dell'eccesso, altri tumori implicati erano tumori gastrointestinali, cancro della laringe e cancro delle ovaie, in questo ordine di frequenza. Per i tumori gastrointestinali (inclusi quelli che colpiscono l'esofago, lo stomaco, il colon e il retto), si presume che l'esposizione rilevante nelle coorti occupazionali avvenga tramite l'ingestione di espettorato carico di amianto sollevato dalle principali vie aeree del polmone e in tempi precedenti (prima che venissero prese misure di protezione contro l'esposizione nei luoghi di pranzo) contaminazione diretta del cibo nei luoghi di lavoro che non avevano aree di pranzo separate dalle aree di lavoro di stabilimenti e fabbriche. Potrebbe anche verificarsi un flusso retrogrado attraverso il dotto toracico dai linfonodi che drenano il polmone (vedere “Il destino delle fibre inalate”, pagina 10.54). Poiché l'associazione era incoerente nelle diverse coorti studiate e poiché le relazioni di risposta all'esposizione non erano sempre osservate, c'è stata una riluttanza ad accettare l'evidenza dell'associazione tra esposizione professionale ed esposizione all'amianto come causale (Doll e Peto 1987; Liddell e Miller 1991).
Il cancro della laringe è molto meno comune del cancro gastrointestinale o del polmone. Già negli anni '1970, ci sono state segnalazioni di un'associazione tra il cancro della laringe e l'esposizione all'amianto. Come il cancro ai polmoni, il fumo è uno dei principali fattori di rischio e causa del cancro della laringe. Anche il cancro della laringe è fortemente associato al consumo di alcol. Data la localizzazione della laringe (organo esposto a tutti gli inquinanti inalati a cui sono esposti i polmoni) e dato che è rivestita dallo stesso epitelio che riveste i bronchi maggiori, è certamente biologicamente plausibile che il cancro della laringe si verifica a causa dell'esposizione all'amianto. Tuttavia, le prove complessive disponibili fino ad oggi sono incoerenti, anche da ampi studi di coorte come i minatori di crisotilo del Quebec e Balangero (Italia), forse perché si tratta di un cancro raro e c'è ancora riluttanza a considerare l'associazione come causale (Liddell e Miller 1991) nonostante la sua plausibilità biologica. Il cancro delle ovaie è stato registrato in eccesso rispetto al previsto in tre studi di coorte (WHO 1989). Una diagnosi errata, in particolare come mesotelioma peritoneale, può spiegare la maggior parte dei casi (Doll e Peto 1987).
Prevenzione, Sorveglianza e Valutazione
Approcci storici e attuali
La prevenzione di qualsiasi pneumoconiosi, compresa l'asbestosi, è stata tradizionalmente attraverso:
- pratiche ingegneristiche e di lavoro per mantenere i livelli di fibre nell'aria il più basso possibile, o almeno in conformità con i livelli di esposizione consentiti generalmente stabiliti dalla legge o dalla normativa
- sorveglianza, condotta per registrare le tendenze dei marcatori di malattia nelle popolazioni esposte e monitorare i risultati delle misure di controllo
- istruzione ed etichettatura dei prodotti volti ad assistere i lavoratori e il pubblico in generale nell'evitare l'esposizione non professionale.
I livelli di esposizione ammissibili erano originariamente diretti al controllo dell'asbestosi e si basavano su misurazioni di igiene industriale in milioni di particelle per piede cubo, raccolte utilizzando gli stessi metodi utilizzati per il controllo della silicosi. Con lo spostamento del focus biologico sulle fibre, in particolare quelle lunghe e sottili, come causa di asbestosi, sono stati sviluppati metodi più appropriati per la loro identificazione e misurazione in aria e, dati questi metodi, il focus sulle fibre corte più abbondanti che contaminano maggiormente posti di lavoro è stato ridotto al minimo. I rapporti di aspetto (lunghezza/diametro) per la maggior parte delle particelle di amianto crisotilo macinato rientrano nell'intervallo da 5:1 a 20:1, salendo fino a 50:1, in contrasto con la maggior parte delle particelle di amianto anfibolo macinato (compresi i frammenti di scissione) i cui valori scendono inferiore a 3:1. L'introduzione del filtro a membrana per il conteggio delle fibre dei campioni d'aria ha portato a un'arbitraria definizione igienica industriale e medica di una fibra come una particella lunga almeno 5 μm, spessa 3 μm o inferiore e con un rapporto lunghezza/larghezza di almeno 3:1 . Questa definizione, utilizzata per molti degli studi sulle relazioni esposizione-risposta, costituisce la base scientifica per la definizione di standard ambientali.
Ad esempio, è stato utilizzato in un incontro sponsorizzato dall'Organizzazione Mondiale della Sanità (1989) per proporre limiti di esposizione professionale ed è stato adottato da agenzie come la US Occupational Safety and Health Administration; viene mantenuto principalmente per ragioni di comparabilità. La riunione dell'OMS, presieduta da Sir Richard Doll, pur riconoscendo che il limite di esposizione professionale in qualsiasi paese può essere stabilito solo dall'organismo nazionale appropriato, ha raccomandato ai paesi con limiti elevati di adottare misure urgenti per ridurre l'esposizione professionale di un singolo lavoratore a 2 f/ml (media ponderata nel tempo di otto ore) e che tutti i paesi dovrebbero passare il più rapidamente possibile a 1 f/ml (media ponderata nel tempo di otto ore) se non l'hanno già fatto. Con la diminuzione dei tassi di asbestosi in alcuni paesi industrializzati e la preoccupazione per i tumori correlati all'amianto in tutti, l'attenzione si è ora spostata sulla determinazione se gli stessi parametri delle fibre, cioè lunghe almeno 5 mm, spesse 3 mm o meno e con una lunghezza rapporto larghezza/larghezza di almeno 3:1, sono anche appropriati per il controllo della carcinogenesi (Browne 1994). Un'attuale teoria sulla carcinogenesi dell'amianto implica sia fibre corte che lunghe (Lippmann 1995). Inoltre, data l'evidenza di un gradiente di fibre nella produzione di mesotelioma e cancro del polmone, e in misura minore, per la produzione di asbestosi, si potrebbe argomentare a favore dei livelli di esposizione ammissibili tenendo conto del tipo di fibra. Alcuni paesi hanno affrontato il problema vietando l'uso (e quindi l'importazione) di crocidolite e fissando livelli di esposizione più stringenti per l'amosite, ovvero 0.1 f/l (McDonald e McDonald 1987).
Livelli di esposizione sul posto di lavoro
I livelli di esposizione ammissibili incarnano l'ipotesi, basata su tutte le prove disponibili, che la salute umana sarà preservata se l'esposizione viene mantenuta entro tali limiti. La revisione dei livelli di esposizione ammissibili, quando si verifica, è invariabilmente verso una maggiore severità (come descritto nel paragrafo precedente). Tuttavia, nonostante il buon rispetto dei controlli sul posto di lavoro, continuano a verificarsi casi di malattia, per motivi di suscettibilità personale (ad esempio, tassi di ritenzione di fibre superiori alla media) o per il fallimento dei controlli sul posto di lavoro per determinati lavori o processi. I controlli ingegneristici, il miglioramento delle pratiche sul posto di lavoro e l'uso di sostituti, descritti altrove nel capitolo, sono stati implementati a livello internazionale (Gibbs, Valic e Browne 1994) in stabilimenti più grandi attraverso l'industria, i sindacati e altre iniziative. Ad esempio, secondo una revisione mondiale del settore del 1986, la conformità con l'attuale standard raccomandato di 1 f/ml era stata raggiunta nell'83% dei siti di produzione (miniere e mulini) coprendo 13,499 lavoratori in 6 paesi; nel 96% delle 167 cementerie operanti in 23 paesi; nel 71% di 40 fabbriche tessili che coprono oltre 2,000 lavoratori operanti in 7 paesi; e nel 97% delle 64 fabbriche che producono materiali di attrito, coprendo 10,190 lavoratori in 10 paesi (Bouige 1990). Tuttavia, una percentuale non trascurabile di tali luoghi di lavoro non è ancora conforme alle normative, non tutti i paesi produttori hanno partecipato a questa indagine e i benefici per la salute previsti sono evidenti solo in alcune statistiche nazionali, non in altre (“Diagnosi e gestione dei casi”, pag. 10.57). Il controllo nei processi di demolizione e nelle piccole imprese che utilizzano l'amianto continua ad avere scarso successo, anche in molti paesi industrializzati.
Sorveglianza
La radiografia del torace è lo strumento principale per la sorveglianza dell'asbestosi, i registri dei tumori e le statistiche nazionali per i tumori correlati all'amianto. Un'encomiabile iniziativa di sorveglianza internazionale delle attività minerarie, di tunneling e di estrazione, intrapresa dall'ILO attraverso segnalazioni volontarie da parte di fonti governative, si concentra sull'estrazione di carbone e roccia dura, ma potrebbe includere l'amianto. Sfortunatamente, il follow-through è stato scarso, con l'ultimo rapporto, basato sui dati per il 1973-77, pubblicato nel 1985 (ILO 1985). Numerosi paesi pubblicano dati nazionali sulla mortalità e sulla morbilità, un esempio eccellente è il Rapporto sulla sorveglianza delle malattie polmonari legate al lavoro per gli Stati Uniti, un rapporto citato sopra (USDHSS 1994). Tali rapporti forniscono informazioni per interpretare le tendenze e valutare l'impatto dei livelli di controllo a livello nazionale. Le industrie più grandi dovrebbero (e molte lo fanno) mantenere le proprie statistiche di sorveglianza, così come fanno alcuni sindacati. La sorveglianza delle industrie più piccole può richiedere studi specifici a intervalli appropriati. Altre fonti di informazione includono programmi come il Surveillance of Work-related Respiratory Diseases (SWORD) nel Regno Unito, che raccoglie rapporti regolari da un campione di medici del torace e del lavoro del paese (Meredith e McDonald 1994) e rapporti da commissioni di compensazione (che spesso però non forniscono informazioni sui lavoratori a rischio).
Etichettatura dei prodotti, istruzione e autostrada dell'informazione
L'etichettatura obbligatoria dei prodotti insieme all'educazione dei lavoratori e dell'opinione pubblica sono potenti strumenti di prevenzione. Mentre in passato ciò avveniva nell'ambito delle organizzazioni dei lavoratori, dei comitati di gestione dei lavoratori e dei programmi di formazione sindacale, gli approcci futuri potrebbero sfruttare le autostrade elettroniche per rendere disponibili i database sulla salute e la sicurezza in tossicologia e medicina.
Esposizione in edifici e da fonti idriche
Nel 1988, il Congresso degli Stati Uniti ha commissionato una revisione dei potenziali rischi per la salute associati al lavoro in edifici costruiti utilizzando materiali contenenti amianto (Health Effects Institute—Asbestos Research 1991). I risultati di un gran numero di studi di campionamento indoor in Europa, Stati Uniti e Canada sono stati utilizzati nelle stime del rischio. Il rischio di morte prematura per cancro nel corso della vita è stato stimato pari a 1 per milione per coloro che sono stati esposti per 15 anni nelle scuole (per livelli di esposizione stimati compresi tra 0005 e 005 f/ml) e 4 per milione per coloro che sono stati esposti per 20 anni a lavorare in edifici per uffici (per livelli di esposizione stimati compresi tra 0002 e 002 f/ml). A titolo di confronto, il rischio per l'esposizione professionale a 0.1 f/ml (ossia, in conformità con il limite di esposizione consentito proposto dalla US Occupational Safety and Health Administration) per 20 anni è stato stimato a 2,000 per milione di esposti. Le misurazioni dell'acqua potabile nelle comunità urbane mostrano notevoli variazioni, da livelli non rilevabili a livelli elevati che vanno da 0.7 milioni di f/l nel Connecticut, USA, a livelli che vanno da 1.1 milioni a 1.3 miliardi di f/l nelle aree minerarie del Quebec (Bignon, Peto e Saracci 1989). Una certa contaminazione può verificarsi anche dai tubi di cemento-amianto che devono servire la maggior parte dei servizi di rete idrica urbana nel mondo. Tuttavia, un gruppo di lavoro che ha riesaminato le prove nel 1987 non ha ignorato il potenziale pericolo associato, ma non ha considerato i rischi per la salute associati all'ingestione di amianto come "uno dei rischi più urgenti per la salute pubblica" (USDHHS 1987), una visione concordante con le osservazioni conclusive di una monografia IARC (WHO) sull'esposizione non professionale alle fibre minerali (Bignon, Peto e Saracci 1989).
Amianto e altre fibre nel 21° secolo
La prima metà del ventesimo secolo è stata caratterizzata da ciò che potrebbe essere descritto come un grave abbandono dei problemi di salute legati all'amianto. Prima della seconda guerra mondiale, le ragioni di ciò non sono chiare; la base scientifica del controllo c'era ma forse non la volontà e nemmeno la militanza operaia. Durante la guerra, c'erano altre priorità nazionali e internazionali, e dopo la guerra, le pressioni dell'urbanizzazione da parte di una popolazione mondiale in rapido aumento ebbero la precedenza, e forse il fascino in un'era industriale per la versatilità del minerale "magico" distolse l'attenzione dai suoi pericoli . In seguito alla prima conferenza internazionale sugli effetti biologici dell'amianto nel 1964 (Selikoff e Churg 1965), le malattie correlate all'amianto divennero una cause célèbre, non solo per conto proprio, ma anche perché ha segnato un periodo di confronto sindacale sui diritti del lavoratore alla conoscenza dei rischi sul lavoro, alla tutela della salute e all'equo risarcimento per infortunio o malattia. Nei paesi con indennizzo dei lavoratori senza colpa, le malattie legate all'amianto nel complesso hanno ricevuto un giusto riconoscimento e trattamento. Nei paesi in cui la responsabilità per danno da prodotti difettosi e le azioni collettive erano più comuni, sono stati concessi grandi premi ad alcuni lavoratori interessati (e ai loro avvocati) mentre altri sono rimasti indigenti e senza sostegno. Mentre è improbabile che la necessità di fibre nelle società moderne diminuisca, il ruolo delle fibre minerali rispetto ad altre fibre potrebbe cambiare. C'è già stato uno spostamento negli usi sia all'interno che tra paesi (vedere “Altre fonti di esposizione”, pagina 10.53). Sebbene esista la tecnologia per ridurre le esposizioni sul posto di lavoro, rimangono luoghi di lavoro in cui non è stata applicata. Date le attuali conoscenze, data la comunicazione internazionale e l'etichettatura dei prodotti, e data l'istruzione dei lavoratori e l'impegno dell'industria, dovrebbe essere possibile utilizzare questo minerale per fornire prodotti economici e durevoli da utilizzare nell'edilizia e nella reticolazione dell'acqua su base internazionale senza rischi per l'utente, lavoratore, produttore o minatore, o al pubblico in generale.
Malattia dei metalli duri
Poco dopo la fine della prima guerra mondiale, mentre svolgeva ricerche per trovare un materiale in grado di sostituire il diamante negli ugelli di trafilatura dei metalli, Karl Schoeter brevettò a Berlino un processo di sinterizzazione (pressurizzazione più riscaldamento a 1,500°C) di una miscela di tungsteno fine polvere di carburo (WC) con il 10% di cobalto per produrre “metallo duro”. Le caratteristiche principali di questo agglomerato sono l'estrema durezza, solo di poco inferiore a quella del diamante, e il mantenimento delle sue proprietà meccaniche alle alte temperature; queste caratteristiche lo rendono idoneo all'impiego nella trafilatura dei metalli, per inserti saldati, e per utensili ad alta velocità per la lavorazione di metalli, pietra, legno e materiali con elevata resistenza all'usura o al calore, in campo meccanico, aeronautico e balistico. L'uso del metallo duro è in continua espansione in tutto il mondo. Nel 1927 Krupp estese l'uso del metallo duro nel campo degli utensili da taglio, chiamandolo “Widia” (come Diamant—come diamante), un nome ancora in uso oggi.
La sinterizzazione rimane la base di tutta la produzione di metallo duro: le tecniche sono migliorate dall'introduzione di altri carburi metallici - carburo di titanio (TiC) e carburo di tantalio (TaC) - e dal trattamento di parti in metallo duro per inserti da taglio mobili con uno o più strati di nitruro di titanio o ossido di alluminio e di altri composti molto duri applicati con deposizione chimica da fase vapore (CVD) o deposizione fisica da fase vapore (PVD). Gli inserti fissi saldati agli utensili non possono essere placcati, ma vengono ripetutamente affilati da una mola diamantata (figure 1 e 2).
Figura 1. (A) Esempi di alcuni inserti mobili trafilati in metallo duro, rivestiti con nitruro di tungsteno giallo oro; (B) inserto saldato all'utensile e lavorante in trafilato di acciaio.
Figura 2. Inserti fissi saldati a (A) punta per pietra e (B) disco per sega.
Il metallo duro sinterizzato è formato da particelle di carburi metallici inglobate in una matrice formata da cobalto, che fonde durante la sinterizzazione, interagendo e occupando gli interstizi. Il cobalto è quindi il materiale collante della struttura, che assume caratteristiche metallo-ceramiche (figure 3, 4 e 5).
Figura 3. Microstruttura di una sinterizzazione WC/Co; Le particelle di WC sono incorporate nella matrice Co light (1,500x).
Figura 4. Microstruttura di una sinterizzazione WC + TiC + TaC + Co. Insieme alle particelle prismatiche WC, si osservano particelle globulari formate da una soluzione solida di TiC + TaC. La matrice di luce è formata da Co (1,500x).
Figura 5. Microstruttura di sinterizzazione placcata da più strati molto duri (2,000x).
Il processo di sinterizzazione utilizza polveri finissime di carburo metallico (diametri medi da 1 a 9μm) e polveri di cobalto (diametro medio da 1 a 4μm) che vengono miscelate, trattate con soluzione di paraffina, pressate in stampo, decerate a bassa temperatura, pre- sinterizzato a 700-750°C e sinterizzato a 1,500°C (Brookes 1992).
Quando la sinterizzazione viene effettuata con metodi inadeguati, tecniche improprie e scarsa igiene industriale, le polveri possono inquinare l'atmosfera dell'ambiente di lavoro: i lavoratori sono quindi esposti al rischio di inalazione di polveri di carburi metallici e polveri di cobalto. Oltre al processo primario esistono altre attività che possono esporre i lavoratori al rischio di inalazione di aerosol di metallo duro. L'affilatura degli inserti fissi saldati agli utensili viene normalmente effettuata mediante molatura diamantata a secco o, più frequentemente, raffreddata con liquidi di varia natura, producendo polveri o nebbie formate da piccolissime gocce contenenti particelle metalliche. Particelle di metallo duro sono utilizzate anche nella produzione di uno strato ad alta resistenza su superfici in acciaio soggette ad usura, applicate attraverso metodi (processo di rivestimento al plasma e altri) basati sulla combinazione di uno spruzzo di polvere con un arco elettrico o un'esplosione controllata di una miscela di gas ad alta temperatura. L'arco elettrico o il flusso esplosivo del gas determina la fusione delle particelle metalliche e il loro impatto sulla superficie da placcare.
Le prime osservazioni sulle "malattie da metalli duri" furono descritte in Germania negli anni '1940. Hanno riportato una fibrosi polmonare diffusa e progressiva, chiamata Hartmetallungenfibrose. Durante i successivi 20 anni sono stati osservati e descritti casi paralleli in tutti i paesi industriali. I lavoratori interessati erano nella maggior parte dei casi responsabili della sinterizzazione. Dal 1970 ad oggi, diversi studi indicano che la patologia all'apparato respiratorio è causata dall'inalazione di particelle di metallo duro. Colpisce solo i soggetti predisposti, e si compone dei seguenti sintomi:
- acuto: rinite, asma
- subacuta: alveolite fibrosa
- cronico: fibrosi interstiziale diffusa e progressiva.
Colpisce non solo gli addetti alla sinterizzazione, ma chiunque inali aerosol contenenti metalli duri e in particolare cobalto. È causato principalmente e forse esclusivamente dal cobalto.
La definizione di malattia da metalli duri comprende oggi un gruppo di patologie dell'apparato respiratorio, diverse tra loro per gravità clinica e prognosi, ma accomunate da una variabile reattività individuale al fattore eziologico cobalto.
Più recenti informazioni epidemiologiche e sperimentali concordano sul ruolo causale del cobalto per i sintomi acuti delle prime vie respiratorie (riniti, asma) e per i sintomi subacuti e cronici del parenchima bronchiale (alveolite fibrosante e fibrosi interstiziale cronica).
Il meccanismo patogenetico si basa sull'induzione da parte del Co di una immunoreazione ipersensibile: infatti solo alcuni dei soggetti presentano patologie dopo brevi esposizioni a concentrazioni relativamente basse, o anche dopo esposizioni più lunghe e intense. Le concentrazioni di co nei campioni biologici (sangue, urine, pelle) non sono significativamente differenti in chi ha la patologia e chi no; non c'è correlazione tra dose e risposta a livello tissutale; sono stati individuati anticorpi specifici (immunoglobine IgE e IgG) contro un composto della Co-albumina negli asmatici, e il patch test del Co è positivo nei soggetti con alveolite o fibrosi; gli aspetti citologici dell'alveolite a cellule giganti sono compatibili con l'immunoreazione ei sintomi acuti o subacuti tendono a regredire quando i soggetti vengono allontanati dall'esposizione al Co (Parkes 1994).
La base immunologica dell'ipersensibilità al Co non è stata ancora spiegata in modo soddisfacente; non è possibile, quindi, identificare un marcatore affidabile di suscettibilità individuale.
Patologie identiche a quelle riscontrate nei soggetti esposti a metalli duri sono state osservate anche nei tagliatori di diamanti, che utilizzano dischi formati da microdiamanti cementati con Co e che quindi inalano solo Co e particelle di diamante.
Non è ancora del tutto dimostrato che il Co puro (escluse tutte le altre particelle inalate) sia in grado da solo di produrre le patologie e soprattutto la fibrosi interstiziale diffusa: le particelle inalate con il Co potrebbero avere un effetto sinergico oltre che modulante. Studi sperimentali sembrano dimostrare che la reattività biologica ad una miscela di particelle di Co e di tungsteno è maggiore di quella provocata dal solo Co, e non si riscontrano patologie significative negli addetti alla produzione di polvere di Co puro (Science of Ambiente totale 1994).
I sintomi clinici della malattia da metalli duri, che, sulla base delle attuali conoscenze eziopatogenetiche, dovrebbero più precisamente essere definiti “malattia del cobalto”, sono, come accennato in precedenza, acuti, subacuti e cronici.
I sintomi acuti comprendono una specifica irritazione respiratoria (rinite, laringo-tracheite, edema polmonare) causata dall'esposizione ad alte concentrazioni di polvere di Co o fumo di Co; sono osservabili solo in casi eccezionali. L'asma è osservato più frequentemente. Compare dal 5 al 10% dei lavoratori esposti a concentrazioni di cobalto di 0.05 mg/m3, l'attuale valore limite di soglia (TLV) statunitense. I sintomi di costrizione toracica con dispnea e tosse tendono a comparire alla fine del turno di lavoro o durante la notte. La diagnosi di asma bronchiale allergico professionale da cobalto può essere sospettata sulla base di criteri anamnestici, ma è confermata da uno specifico test di stimolazione bronchiale che determina la comparsa di una risposta broncospastica immediata, ritardata o duale. Anche i test di capacità respiratoria effettuati all'inizio e alla fine del turno di lavoro possono aiutare la diagnosi. I sintomi asmatici dovuti al cobalto tendono a scomparire quando il soggetto viene allontanato dall'esposizione, ma, analogamente a tutte le altre forme di asma allergico professionale, i sintomi possono diventare cronici e irreversibili quando l'esposizione si protrae per lungo tempo (anni), nonostante la presenza di disturbi respiratori. I soggetti fortemente broncoreattivi possono presentare sintomi asmatici eziologici non allergici, con risposta aspecifica all'inalazione di cobalto e altre polveri irritanti. In un'alta percentuale di casi con asma bronchiale allergico, è stata riscontrata nel siero IgE una reazione specifica verso un composto di Co-sieroalbumina umana. Il reperto radiologico non varia: solo in rari casi si possono riscontrare forme miste di asma più alveolite con alterazione radiologica specificatamente causata da alveolite. La terapia broncodilatatoria, insieme ad un'immediata esposizione al termine dell'attività lavorativa, porta alla completa guarigione per i casi di recente insorgenza, non ancora cronici.
I sintomi subacuti e cronici comprendono l'alveolite fibrosa e la fibrosi interstiziale cronica diffusa e progressiva (DIPF). L'esperienza clinica sembra indicare che il passaggio dall'alveolite alla fibrosi interstiziale è un processo che evolve gradualmente e lentamente nel tempo: si possono riscontrare casi di alveolite iniziale pura reversibili con sospensione dall'esposizione più terapia con corticosteroidi; oppure casi con componente fibrotica già presente, che possono migliorare ma non raggiungere la completa guarigione togliendo il soggetto dall'esposizione, anche con terapia aggiuntiva; e, infine, i casi in cui la situazione predominante è quella di un DIPF irreversibile. L'incidenza di tali casi è bassa nei lavoratori esposti, molto inferiore alla percentuale di casi di asma allergico.
L'alveolite è oggi facilmente studiabile nelle sue componenti citologiche attraverso il lavaggio bronco-alveolare (BAL); è caratterizzato da un forte aumento del numero totale di cellule, formate principalmente da macrofagi, con numerose cellule giganti multinucleari e dal tipico aspetto di cellule giganti da corpo estraneo contenenti a volte cellule citoplasmatiche (figura 6); è frequente anche un aumento assoluto o relativo dei linfociti, con diminuzione del rapporto CD4/CD8, associato ad un forte aumento degli eosinofili e dei mastociti. Raramente l'alveolite è prevalentemente linfocitaria, con rapporto CD4/CD8 invertito, come avviene nelle pneumopatie da ipersensibilità.
Figura 6. BAL citologico in un caso di alveolite cellulare gigante mononucleare macrofagica causata da metallo duro. Tra i macrofagi mononucleari e il linfocita si osserva un tipo di cellula gigante da corpo estraneo (400x).
I soggetti con alveolite riferiscono dispnea associata a stanchezza, perdita di peso e tosse secca. Crepitazione è presente nel polmone inferiore con alterazione funzionale di tipo restrittivo e diffusa opacità radiologica rotonda o irregolare. Il patch test per il cobalto è positivo nella maggior parte dei casi. Nei soggetti predisposti l'alveolite si manifesta dopo un periodo relativamente breve di esposizione lavorativa, di uno o pochi anni. Nelle sue fasi iniziali questa forma è reversibile fino alla completa guarigione con la semplice rimozione dall'esposizione, con risultati migliori se abbinata alla terapia con cortisone.
Lo sviluppo della fibrosi interstiziale diffusa aggrava la sintomatologia clinica con un peggioramento della dispnea, che compare anche dopo minimo sforzo e poi anche a riposo, con peggioramento della compromissione ventilatoria restrittiva che è legata ad una riduzione della diffusione capillare-alveolare, e con comparsa di opacità radiografiche di tipo lineare ea nido d'ape (figura 7). Il quadro istologico è quello di un'alveolite fibrosante di tipo “murale”.
Figura 7. Radiografia toracica di un soggetto affetto da fibrosi interstiziale da metallo duro. Si osservano opacità lineari e diffuse e aspetti a nido d'ape.
L'evoluzione è rapidamente progressiva; le terapie sono inefficaci e la prognosi dubbia. Uno dei casi diagnosticati dall'autore alla fine ha richiesto un trapianto di polmone.
La diagnosi occupazionale si basa sull'anamnesi, sul pattern citologico del BAL e sul patch test al cobalto.
La prevenzione della malattia da metalli duri, o, più precisamente, da cobalto, è oggi principalmente tecnica: proteggere i lavoratori attraverso l'eliminazione di polveri, fumi o nebbie con un'adeguata ventilazione delle aree di lavoro. Infatti, la mancanza di conoscenza dei fattori che determinano l'ipersensibilità individuale al cobalto rende impossibile l'identificazione delle persone suscettibili e deve essere fatto il massimo sforzo per ridurre le concentrazioni atmosferiche.
Il numero di persone a rischio è sottostimato perché molte attività di affilatura vengono svolte in piccole industrie o da artigiani. In tali luoghi di lavoro, il TLV statunitense di 0.05 mg/m3 viene spesso superato. C'è anche qualche dubbio sull'adeguatezza del TLV per proteggere i lavoratori contro la malattia da cobalto poiché le relazioni dose-effetto per i meccanismi patologici che coinvolgono l'ipersensibilità non sono completamente comprese.
La sorveglianza di routine deve essere sufficientemente accurata da identificare le patologie da cobalto nelle loro prime fasi. Deve essere somministrato un questionario annuale mirato principalmente ai sintomi temporanei, insieme a una visita medica che comprende test di funzionalità polmonare e altri esami medici appropriati. Poiché è stato dimostrato che esiste una buona correlazione tra le concentrazioni di cobalto nell'ambiente di lavoro e l'escrezione urinaria del metallo, è opportuno effettuare la misurazione semestrale del cobalto nelle urine (CoU) su campioni prelevati alla fine del la settimana lavorativa. Quando l'esposizione è al livello del TLV, l'indice di esposizione biologica (BEI) è stimato pari a 30μg Co/litro urina.
Le visite mediche pre-esposizione per la presenza di malattie respiratorie preesistenti e ipersensibilità bronchiale possono essere utili nella consulenza e nel collocamento dei lavoratori. I test della metacolina sono un utile indicatore di iperreattività bronchiale aspecifica e possono essere utili in alcuni contesti.
Si raccomanda vivamente la standardizzazione internazionale dei metodi di sorveglianza ambientale e medica per i lavoratori esposti al cobalto.
Sistema respiratorio: la varietà di pneumoconiosi
Questo articolo è dedicato alla discussione delle pneumoconiosi correlate a una varietà di specifiche sostanze non fibrose; le esposizioni a queste polveri non sono trattate altrove in questo volume. Per ogni materiale in grado di generare una pneumoconiosi per esposizione, una breve trattazione della mineralogia e dell'importanza commerciale è seguita da informazioni relative alla salute polmonare dei lavoratori esposti.
Alluminio
L'alluminio è un metallo leggero con molti usi commerciali sia nel suo stato metallico che in quello combinato. (Abramson et al. 1989; Kilburn e Warshaw 1992; Kongerud et al. 1994.) I minerali contenenti alluminio, principalmente bauxite e criolite, sono costituiti da combinazioni del metallo con ossigeno, fluoro e ferro. La contaminazione da silice dei minerali è comune. Allumina (Al2O3) viene estratta dalla bauxite e può essere lavorata per essere utilizzata come abrasivo o come catalizzatore. L'alluminio metallico è ottenuto dall'allumina mediante riduzione elettrolitica in presenza di fluoruro. L'elettrolisi della miscela viene effettuata utilizzando elettrodi di carbone ad una temperatura di circa 1,000°C in celle dette pentole. L'alluminio metallico viene quindi estratto per la fusione. L'esposizione a polvere, fumi e gas nelle pentole, inclusi carbonio, allumina, fluoruri, anidride solforosa, monossido di carbonio e idrocarburi aromatici, è accentuata durante la rottura della crosta e altre operazioni di manutenzione. Numerosi prodotti sono fabbricati da lastre, scaglie, granuli e fusioni di alluminio, con un ampio potenziale di esposizione professionale. L'alluminio metallico e le sue leghe trovano impiego nell'industria aeronautica, nautica e automobilistica, nella fabbricazione di contenitori e di dispositivi elettrici e meccanici, nonché in svariate applicazioni edili e strutturali. Piccole particelle di alluminio sono utilizzate in vernici, esplosivi e dispositivi incendiari. Per mantenere la separazione delle particelle, vengono aggiunti oli minerali o stearina; l'aumento della tossicità polmonare dei fiocchi di alluminio è stato associato all'uso di olio minerale.
Salute polmonare
L'inalazione di polveri e fumi contenenti alluminio può verificarsi nei lavoratori coinvolti nell'estrazione, estrazione, lavorazione, fabbricazione e utilizzo finale di materiali contenenti alluminio. La fibrosi polmonare, che si manifesta con sintomi e riscontri radiografici, è stata descritta in lavoratori con esposizioni diverse a sostanze contenenti alluminio. La malattia di Shaver è una grave pneumoconiosi descritta tra i lavoratori coinvolti nella produzione di abrasivi di allumina. Sono stati segnalati numerosi decessi per questa condizione. I lobi superiori del polmone sono più spesso colpiti e l'insorgenza di pneumotorace è una complicanza frequente. Alti livelli di biossido di silicio sono stati trovati nell'ambiente della pentola così come nei polmoni dei lavoratori durante l'autopsia, suggerendo che la silice può contribuire al quadro clinico della malattia di Shaver. Sono state osservate anche alte concentrazioni di particolato di ossido di alluminio. La patologia polmonare può mostrare vesciche e bolle e occasionalmente si osserva ispessimento pleurico. La fibrosi è diffusa, con aree di infiammazione nei polmoni e nei linfonodi associati.
Le polveri di alluminio sono utilizzate nella produzione di esplosivi e sono stati segnalati numerosi casi di fibrosi grave e progressiva nei lavoratori coinvolti in questo processo. Il coinvolgimento polmonare è stato occasionalmente descritto anche in lavoratori impiegati nella saldatura o nella lucidatura dell'alluminio e nell'insacco di lettiere per gatti contenenti silicato di alluminio (alunite). Tuttavia, vi è stata una notevole variazione nella segnalazione di malattie polmonari in relazione all'esposizione all'alluminio. Gli studi epidemiologici sui lavoratori esposti alla riduzione dell'alluminio hanno generalmente mostrato una bassa prevalenza di alterazioni pneumoconiotiche e lievi riduzioni medie della funzione ventilatoria polmonare. In vari ambienti di lavoro, i composti di allumina possono presentarsi in diverse forme e negli studi sugli animali queste forme sembrano avere diverse tossicità polmonari. Anche la silice e altre polveri miste possono contribuire a questa tossicità variabile, così come i materiali utilizzati per rivestire le particelle di alluminio. Un lavoratore, che ha sviluppato una malattia polmonare granulomatosa dopo l'esposizione a ossidi e alluminio metallico, ha mostrato la trasformazione dei suoi linfociti del sangue in seguito all'esposizione a sali di alluminio, suggerendo che i fattori immunologici potrebbero svolgere un ruolo.
Una sindrome asmatica è stata frequentemente osservata tra i lavoratori esposti ai fumi nelle stanze dei vasi di riduzione dell'alluminio. I fluoruri trovati nell'ambiente della pentola sono stati implicati, sebbene l'agente o gli agenti specifici associati alla sindrome asmatica non siano stati determinati. Come con altri tipi di asma professionale, i sintomi sono spesso ritardati da 4 a 12 ore dopo l'esposizione e comprendono tosse, dispnea, costrizione toracica e respiro sibilante. Si può anche notare una reazione immediata. L'atopia e una storia familiare di asma non sembrano essere fattori di rischio per lo sviluppo dell'asma da vaso. Dopo la cessazione dell'esposizione, nella maggior parte dei casi ci si può aspettare che i sintomi scompaiano, sebbene due terzi dei lavoratori interessati mostrino una persistente risposta bronchiale aspecifica e, in alcuni lavoratori, i sintomi e l'iperreattività delle vie aeree continuino per anni anche dopo la fine dell'esposizione. La prognosi per l'asma da vaso sembra essere migliore in coloro che vengono immediatamente rimossi dall'esposizione quando i sintomi asmatici si manifestano. Anche l'ostruzione fissa del flusso d'aria è stata associata al lavoro nella stanza dei vasi.
Gli elettrodi di carbonio vengono utilizzati nel processo di riduzione dell'alluminio e nell'ambiente della pentola sono stati identificati noti cancerogeni per l'uomo. Diversi studi sulla mortalità hanno rivelato eccessi di cancro ai polmoni tra i lavoratori esposti in questo settore.
Terra di diatomea
I depositi di farina fossile derivano dall'accrescimento di scheletri di organismi microscopici. (Cooper e Jacobson 1977; Checkoway et al. 1993.) La farina fossile può essere utilizzata nelle fonderie e nella manutenzione di filtri, abrasivi, lubrificanti ed esplosivi. Alcuni depositi contengono fino al 90% di silice libera. I lavoratori esposti possono sviluppare alterazioni polmonari che comportano pneumoconiosi semplice o complicata. Il rischio di morte sia per malattie respiratorie non maligne che per cancro ai polmoni è stato correlato alla permanenza dei lavoratori in lavori polverosi, nonché alle esposizioni cumulative di silice cristallina durante l'estrazione e la lavorazione della farina fossile.
Carbonio elementare
A parte il carbone, le due forme comuni di carbonio elementare sono la grafite (carbonio cristallino) e il nerofumo. (Hanoa 1983; Petsonk et al. 1988.) La grafite viene utilizzata nella produzione di matite di piombo, rivestimenti per fonderia, vernici, elettrodi, batterie a secco e crogioli per scopi metallurgici. La grafite finemente macinata ha proprietà lubrificanti. Il nerofumo è una forma parzialmente decomposta utilizzata in pneumatici per autoveicoli, pigmenti, plastica, inchiostri e altri prodotti. Il nerofumo è prodotto da combustibili fossili attraverso una varietà di processi che coinvolgono la combustione parziale e la decomposizione termica.
Durante l'estrazione e la macinazione di grafite naturale e durante la produzione di grafite artificiale, può verificarsi l'inalazione di carbonio e polveri associate. La grafite artificiale è prodotta dal riscaldamento di carbone o coke di petrolio e generalmente non contiene silice libera.
Salute polmonare
La pneumoconiosi deriva dall'esposizione dei lavoratori alla grafite sia naturale che artificiale. Clinicamente, i lavoratori con pneumoconiosi da carbonio o grafite mostrano risultati radiografici simili a quelli dei lavoratori del carbone. In passato sono stati segnalati gravi casi sintomatici con fibrosi polmonare massiccia, in particolare legati alla produzione di elettrodi di carbonio per la metallurgia, anche se rapporti recenti sottolineano che i materiali implicati nelle esposizioni che portano a questo tipo di condizione sono probabilmente polveri miste.
Gilsonite
La gilsonite, nota anche come uintaite, è un idrocarburo solidificato. (Keimig et al. 1987.) Si verifica nelle vene negli Stati Uniti occidentali. Gli usi attuali includono la produzione di sigillanti, inchiostri, vernici e smalti per carrozzerie automobilistiche. È un ingrediente di fluidi e cementi per la perforazione di pozzi petroliferi; è un additivo negli stampi in sabbia nell'industria della fonderia; si trova come componente di asfalto, pannelli da costruzione ed esplosivi; ed è impiegato nella produzione di grafite di grado nucleare. I lavoratori esposti alla polvere di gilsonite hanno riportato sintomi di tosse e produzione di catarro. Cinque dei novantanove lavoratori intervistati hanno mostrato prove radiografiche di pneumoconiosi. Non sono state definite anomalie nella funzione polmonare in relazione all'esposizione alla polvere di gilsonite.
Gesso
Il gesso è solfato di calcio idrato (CaSO4· 2H2O) (Oakes et al. 1982). Viene utilizzato come componente di cartongesso, gesso di Parigi e cemento Portland. I depositi si trovano in diverse forme e sono spesso associati ad altri minerali come il quarzo. La pneumoconiosi è stata osservata nei minatori di gesso ed è stata attribuita alla contaminazione da silice. Le anomalie ventilatorie non sono state associate all'esposizione alla polvere di gesso.
Oli e lubrificanti
I liquidi contenenti oli idrocarburici sono usati come refrigeranti, oli da taglio e lubrificanti (Cullen et al. 1981). Gli oli vegetali si trovano in alcuni prodotti commerciali e in una varietà di alimenti. Questi oli possono essere aerosolizzati e inalati quando i metalli rivestiti con oli vengono fresati o lavorati a macchina o se vengono utilizzati spray contenenti olio per scopi di pulizia o lubrificazione. Le misurazioni ambientali nelle officine meccaniche e negli stabilimenti hanno documentato livelli di olio nell'aria fino a 9 mg/m3. Un rapporto ha implicato l'esposizione a olio disperso nell'aria dalla combustione di grassi animali e vegetali in un edificio chiuso.
Salute polmonare
È stato occasionalmente segnalato che i lavoratori esposti a questi aerosol sviluppano prove di a polmonite lipoide, simile a quello osservato nei pazienti che hanno aspirato gocce nasali di olio minerale o altri materiali oleosi. La condizione è associata a sintomi di tosse e dispnea, crepitii polmonari inspiratori e compromissione della funzione polmonare, generalmente di gravità lieve. Sono stati segnalati alcuni casi con alterazioni radiografiche più estese e gravi compromissioni polmonari. L'esposizione agli oli minerali è stata anche associata in diversi studi ad un aumentato rischio di tumori del tratto respiratorio.
Cemento Portland
Il cemento Portland è costituito da silicati di calcio idrati, ossido di alluminio, ossido di magnesio, ossido di ferro, solfato di calcio, argilla, scisto e sabbia (Abrons et al. 1988; Yan et al. 1993). L'impasto viene frantumato e calcinato ad alte temperature con l'aggiunta di gesso. Il cemento trova numerosi usi nella costruzione di strade e di edifici.
Salute polmonare
La silicosi sembra essere il rischio maggiore nei lavoratori del cemento, seguita da una pneumoconiosi mista a polvere. (In passato, l'amianto veniva aggiunto al cemento per migliorarne le caratteristiche.) Sono stati osservati reperti radiografici del torace anomali, tra cui piccole opacità arrotondate e irregolari e alterazioni pleuriche. È stato occasionalmente segnalato che i lavoratori hanno sviluppato proteinosi alveolare polmonare dopo l'inalazione di polvere di cemento. I cambiamenti ostruttivi del flusso d'aria sono stati notati in alcuni, ma non in tutti, i sondaggi sui lavoratori del cemento.
Metalli delle terre rare
I metalli delle terre rare o "lantanidi" hanno numeri atomici compresi tra 57 e 71. Il lantanio (numero atomico 57), il cerio (58) e il neodimio (60) sono i più comuni del gruppo. Gli altri elementi di questo gruppo includono praseodimio (59), promezio (61), samario (62), europio (63), gadolinio (64), terbio (65), disprosio (66), olmio (67), erbio (68 ), tulio (69), itterbio (70) e lutezio (71). (Hussain, Dick e Kaplan 1980; Sabbioni, Pietra e Gaglione 1982; Vocaturo, Colombo e Zanoni 1983; Sulotto, Romano e Berra 1986; Waring e Watling 1990; Deng et al. 1991.) Gli elementi delle terre rare si trovano naturalmente nella monazite sabbia, da cui vengono estratti. Sono utilizzati in una varietà di leghe metalliche, come abrasivi per la lucidatura di specchi e lenti, per ceramiche ad alta temperatura, nei fuochi d'artificio e nelle pietre focaie per accendisigari. Nell'industria elettronica sono utilizzati nell'elettrosaldatura e si trovano in vari componenti elettronici, inclusi fosfori televisivi, schermi radiografici, laser, dispositivi a microonde, isolanti, condensatori e semiconduttori.
Le lampade ad arco di carbonio sono ampiamente utilizzate nei settori della stampa, della fotoincisione e della litografia e sono state utilizzate per l'illuminazione di riflettori, riflettori e proiezioni cinematografiche prima dell'adozione su larga scala delle lampade ad argon e allo xeno. Gli ossidi metallici delle terre rare sono stati incorporati nel nucleo centrale delle aste ad arco in carbonio, dove stabilizzano il flusso dell'arco. I fumi emessi dalle lampade sono una miscela di materiale gassoso e particolato composto da circa il 65% di ossidi di terre rare, il 10% di fluoruri e carbonio incombusto e impurità.
Salute polmonare
La pneumoconiosi nei lavoratori esposti a terre rare è stata evidenziata principalmente come infiltrati radiografici del torace nodulari bilaterali. La patologia polmonare nei casi di pneumoconiosi delle terre rare è stata descritta come una fibrosi interstiziale accompagnata da un accumulo di particelle di polvere granulare fine o alterazioni granulomatose.
Sono state descritte alterazioni funzionali polmonari variabili, da restrittive a miste restrittive-ostruttive. Tuttavia, lo spettro delle malattie polmonari correlate all'inalazione di elementi delle terre rare deve ancora essere definito e i dati relativi al modello e alla progressione della malattia e ai cambiamenti istologici sono disponibili principalmente solo da pochi casi clinici.
Un potenziale neoplastico degli isotopi delle terre rare è stato suggerito da un caso clinico di cancro ai polmoni, probabilmente correlato alle radiazioni ionizzanti dei radioisotopi delle terre rare presenti in natura.
Composti Sedimentari
I depositi rocciosi sedimentari si formano attraverso i processi di alterazione fisica e chimica, erosione, trasporto, deposizione e diagenesi. Questi possono essere caratterizzati in due grandi classi: Clastici, che includono detriti di erosione depositati meccanicamente, e precipitati chimici, che comprendono carbonati, gusci di scheletri organici e depositi salini. I carbonati, i solfati e gli alogenuri sedimentari forniscono minerali relativamente puri che si sono cristallizzati da soluzioni concentrate. A causa dell'elevata solubilità di molti dei composti sedimentari, vengono rapidamente eliminati dai polmoni e sono generalmente associati a piccole patologie polmonari. Al contrario, i lavoratori esposti a determinati composti sedimentari, principalmente clastici, hanno mostrato alterazioni pneumoconiotiche.
fosfati
Minerale di fosfato, Ca5(F,Cl)(PO4)3, è utilizzato nella produzione di fertilizzanti, integratori alimentari, dentifrici, conservanti, detergenti, pesticidi, veleni per roditori e munizioni (Dutton et al. 1993). L'estrazione e la lavorazione del minerale possono comportare una varietà di esposizioni irritanti. Le indagini sui lavoratori nell'estrazione e nell'estrazione di fosfati hanno documentato un aumento dei sintomi di tosse e produzione di catarro, nonché prove radiografiche di pneumoconiosi, ma poche prove di funzionalità polmonare anormale.
roccia scistosa
Lo scisto è una miscela di materiale organico composta principalmente da carbonio, idrogeno, ossigeno, zolfo e azoto (Rom, Lee e Craft 1981; Seaton et al. 1981). La componente minerale (cherogeno) si trova nella roccia sedimentaria chiamata marna, che è di colore grigio-marrone e di consistenza stratificata. Lo scisto bituminoso è stato utilizzato come fonte di energia sin dal 1850 in Scozia. I principali giacimenti esistono negli Stati Uniti, in Scozia e in Estonia. La polvere nell'atmosfera delle miniere sotterranee di scisto bituminoso ha una dispersione relativamente fine, con fino all'80% delle particelle di polvere di dimensioni inferiori a 2 mm.
Salute polmonare
Viene definita pneumoconiosi correlata alla deposizione di polvere di scisto nei polmoni shalosis. La polvere crea una reazione granulomatosa e fibrotica nei polmoni. Questa pneumoconiosi è clinicamente simile alla pneumoconiosi e alla silicosi dei lavoratori del carbone e può progredire in una fibrosi massiccia anche dopo che il lavoratore ha lasciato l'industria.
Le alterazioni patologiche identificate nei polmoni con shalosi sono caratterizzate da deformazione vascolare e bronchiale, con ispessimento irregolare dei setti interalveolari e interlobulari. Oltre alla fibrosi interstiziale, i campioni polmonari con pneumoconiosi da scisto hanno mostrato ombre ilari ingrandite, correlate al trasporto di polvere di scisto e successivo sviluppo di cambiamenti sclerotici ben definiti nei linfonodi ilari.
È stato riscontrato che i lavoratori dello scisto hanno una prevalenza di bronchite cronica due volte e mezzo quella dei controlli di pari età. L'effetto dell'esposizione alla polvere di scisto sulla funzione polmonare non è stato studiato sistematicamente.
Ardesia
L'ardesia è una roccia metamorfica, costituita da vari minerali, argille e materia carboniosa (McDermott et al. 1978). I principali costituenti dell'ardesia includono muscovite, clorite, calcite e quarzo, insieme a grafite, magnetite e rutilo. Questi hanno subito metamorfosi per formare una densa roccia cristallina che possiede forza ma si spacca facilmente, caratteristiche che spiegano la sua importanza economica. L'ardesia viene utilizzata in coperture, pietre dimensionali, piastrelle per pavimenti, lastricature, forme strutturali come pannelli e davanzali, lavagne, matite, tavoli da biliardo e banchi da laboratorio. L'ardesia frantumata viene utilizzata nella costruzione di autostrade, superfici di campi da tennis e granuli leggeri per coperture.
Salute polmonare
La pneumoconiosi è stata riscontrata in un terzo dei lavoratori studiati nell'industria dell'ardesia nel nord del Galles e nel 54% dei produttori di matite in ardesia in India. Vari cambiamenti radiografici polmonari sono stati identificati nei lavoratori di lavagna. A causa dell'alto contenuto di quarzo di alcune ardesie e degli strati rocciosi adiacenti, la pneumoconiosi dei lavoratori dell'ardesia può avere caratteristiche di silicosi. La prevalenza dei sintomi respiratori nei lavoratori di turno è elevata e la percentuale di lavoratori con sintomi aumenta con la categoria di pneumoconiosi, indipendentemente dallo stato di fumatore. Valori ridotti del volume espiratorio forzato in un secondo (FEV1) e la capacità vitale forzata (FVC) sono associate all'aumento della categoria di pneumoconiosi.
I polmoni dei minatori esposti alla polvere di ardesia rivelano aree localizzate di fibrosi perivascolare e peribronchiale, che si estendono alla formazione di macule e ad un'estesa fibrosi interstiziale. Le lesioni tipiche sono macule fibrotiche di configurazione variabile intimamente associate a piccoli vasi sanguigni polmonari.
Talco
Il talco è composto da silicati di magnesio e si trova in una varietà di forme. (Vallyathan e Craighead 1981; Wegman et al. 1982; Stille e Tabershaw 1982; Wergeland, Andersen e Baerheim 1990; Gibbs, Pooley e Griffith 1992.)
I depositi di talco sono spesso contaminati da altri minerali, tra cui tremolite fibrosa e non fibrosa e quarzo. Gli effetti sulla salute polmonare dei lavoratori esposti al talco possono essere correlati sia al talco stesso che agli altri minerali associati.
La produzione di talco avviene principalmente in Australia, Austria, Cina, Francia e Stati Uniti. Il talco è utilizzato come componente in centinaia di prodotti e viene utilizzato nella produzione di vernici, prodotti farmaceutici, cosmetici, ceramiche, pneumatici per automobili e carta.
Salute polmonare
Sulle radiografie del torace dei lavoratori del talco si osservano opacità polmonari parenchimali diffuse arrotondate e irregolari e anomalie pleuriche in associazione con l'esposizione al talco. A seconda delle esposizioni specifiche sperimentate, le ombre radiografiche possono essere attribuite al talco stesso oa contaminanti nel talco. L'esposizione al talco è stata associata a sintomi di tosse, dispnea e produzione di catarro e con evidenza di ostruzione delle vie aeree negli studi sulla funzionalità polmonare. La patologia polmonare ha rivelato varie forme di fibrosi polmonare: sono stati segnalati cambiamenti granulomatosi e corpi ferruginosi e macrofagi carichi di polvere raccolti attorno ai bronchioli respiratori mescolati a fasci di collagene. Anche l'esame mineralogico del tessuto polmonare dei lavoratori del talco è variabile e può mostrare silice, mica o silicati misti.
Poiché i depositi di talco possono essere associati all'amianto e ad altre fibre, non sorprende che sia stato riportato un aumento del rischio di carcinoma broncogeno nei minatori di talco e nei mugnai. Recenti indagini su lavoratori esposti a talco senza fibre di amianto associate hanno rivelato tendenze per una maggiore mortalità per malattie respiratorie non maligne (silicosi, silico-tubercolosi, enfisema e polmonite), ma il rischio di cancro broncogeno non è risultato elevato.
Hairspray
L'esposizione alle lacche per capelli si verifica sia nell'ambiente domestico che negli stabilimenti commerciali per parrucchieri (Rom 1992b). Le misurazioni ambientali nei saloni di bellezza hanno indicato il potenziale di esposizione all'aerosol respirabile. Diversi case report hanno implicato l'esposizione alla lacca per capelli nel verificarsi di una polmonite, thesaurosi, in soggetti fortemente esposti. I sintomi clinici nei casi erano generalmente lievi e si sono risolti con la cessazione dell'esposizione. L'istologia di solito mostrava un processo granulomatoso nel polmone e ingrossamento dei linfonodi ilari, con ispessimento delle pareti alveolari e numerosi macrofagi granulari negli spazi aerei. Le macromolecole nelle lacche per capelli, tra cui gommalacca e polivinilpirrolidone, sono state suggerite come potenziali agenti. Contrariamente alle segnalazioni di casi clinici, l'aumento delle ombre radiografiche del parenchima polmonare osservato nelle indagini radiologiche dei parrucchieri commerciali non è stato correlato in modo definitivo all'esposizione alla lacca per capelli. Sebbene i risultati di questi studi non consentano di trarre conclusioni definitive, le malattie polmonari clinicamente importanti dovute alle tipiche esposizioni alla lacca per capelli sembrano essere un evento insolito.
Broncopneumopatia cronica ostruttiva
I disturbi respiratori cronici caratterizzati da diversi gradi di dispnea, tosse, espettorazione flemma e insufficienza respiratoria funzionale sono inclusi nella categoria generale delle malattie polmonari croniche non specifiche (CNSLD). La definizione originale di CNSLD, accettata al Ciba Symposium nel 1959, copriva la bronchite cronica, l'enfisema e l'asma. Successivamente, la terminologia diagnostica della bronchite cronica è stata ridefinita secondo il concetto che la limitazione invalidante del flusso aereo rappresenta lo stadio finale del processo in continua progressione che inizia come espettorazione benigna causata dall'inalazione prolungata o ricorrente di sostanze irritanti bronchiali (la "British Hypothesis") . Il concetto è stato messo in discussione nel 1977 e da allora l'ipersecrezione e l'ostruzione delle vie aeree sono considerate processi non correlati. L'ipotesi alternativa, nota come "ipotesi olandese", pur accettando il ruolo del fumo e dell'inquinamento atmosferico nell'eziologia della limitazione cronica del flusso aereo, indica il ruolo chiave e possibilmente causale della suscettibilità dell'ospite, che si manifesta come, ad esempio, una tendenza asmatica. Studi successivi hanno dimostrato che entrambe le ipotesi possono contribuire alla comprensione della storia naturale della malattia cronica delle vie aeree. Sebbene la conclusione sul valore prognostico insignificante della sindrome ipersecretoria sia stata generalmente accettata come fondata, studi recenti hanno mostrato una significativa associazione tra disturbo ipersecretorio e aumento del rischio di sviluppo di limitazione del flusso aereo e mortalità respiratoria.
Attualmente, il termine CNSLD combina due grandi categorie di disturbi respiratori cronici, l'asma (discussa in un articolo separato di questo capitolo) e la broncopneumopatia cronica ostruttiva (BPCO).
Definizione
In un documento pubblicato dall'American Thoracic Society (ATS) (1987), la BPCO è definita come un disturbo caratterizzato da test anormali del flusso espiratorio che non cambiano in modo marcato per periodi di osservazione di diversi mesi. Prendendo in considerazione le cause funzionali e strutturali della limitazione del flusso aereo, la definizione include i seguenti disturbi delle vie aeree non asmatici: bronchite cronica, enfisema e malattia delle vie aeree periferiche. Le importanti caratteristiche comuni della BPCO sono pronunciate anomalie fisiopatologiche per lo più esibite come un grado variabile di limitazione cronica del flusso aereo (CAL). La limitazione cronica del flusso aereo può essere riscontrata in un soggetto con qualsiasi malattia inclusa nella rubrica della BPCO.
La bronchite cronica è definita come una condizione anomala delle vie respiratorie, caratterizzata da tosse produttiva persistente ed eccessiva, che riflette l'ipersecrezione mucosa all'interno delle vie aeree. Ai fini epidemiologici, la diagnosi di bronchite cronica si è basata sulle risposte al set di domande standard incluse nel questionario del Medical Research Council (MRC) o ATS sui sintomi respiratori. Il disturbo è definito come tosse ed espettorazione catarro che si verificano nella maggior parte dei giorni per almeno tre mesi all'anno, durante almeno due anni consecutivi.
L'enfisema è definito come un'alterazione anatomica del polmone caratterizzata da un abnorme allargamento degli spazi aerei distali al bronchiolo terminale, accompagnato dalla distruzione dell'architettura acinare. L'enfisema spesso coesiste con la bronchite cronica.
Il termine vie aeree periferiche malattia or malattia delle piccole vie aeree è usato per descrivere la condizione anomala delle vie aeree di diametro inferiore a 2-3 mm. L'infiammazione, l'ostruzione e la produzione eccessiva di muco in questa parte dell'albero bronchiale sono state osservate in una varietà di entità cliniche, tra cui la bronchite cronica e l'enfisema. L'evidenza patologica di anomalie strutturali locali e il concetto che i cambiamenti osservati possano rappresentare uno stadio precoce nella storia naturale della malattia cronica delle vie aeree, hanno stimolato alla fine degli anni '1960 e '1970 un rapido sviluppo di test funzionali progettati per esaminare le proprietà fisiologiche delle vie aeree periferiche. Di conseguenza, il termine malattia delle vie aeree periferiche è generalmente inteso riferirsi ad anomalie strutturali o difetto funzionale.
CAL è un segno distintivo funzionale della BPCO. Il termine si riferisce a una maggiore resistenza al flusso d'aria, con conseguente rallentamento persistente durante l'espirazione forzata. La sua definizione e le conoscenze cliniche e fisiopatologiche sottostanti implicano due importanti indizi diagnostici. In primo luogo, si deve dimostrare che la condizione ha un decorso cronico e la prima raccomandazione del 1958 richiedeva la presenza di CAL per più di un anno per soddisfare i criteri diagnostici. La tempistica suggerita di recente è meno rigorosa e si riferisce alla manifestazione di un difetto nell'arco di tre mesi. Nella sorveglianza della CAL correlata al lavoro, la valutazione spirometrica standard fornisce mezzi sufficienti per identificare la CAL, basata sulla riduzione del volume espiratorio forzato in un secondo (FEV1) e/o nel rapporto del FEV1 alla capacità vitale forzata (FVC).
Di solito, CAL viene diagnosticato quando il FEV1 APPREZZIAMO si riduce al di sotto dell'80% del valore previsto. Secondo la classificazione funzionale della CAL raccomandata dall'American Thoracic Society:
- lieve compromissione si verifica quando il valore del FEV1 è inferiore all'80% e superiore al 60% del valore previsto
- moderata compromissione si verifica quando FEV1 è compreso tra il 40% e il 59% del valore previsto
- grave compromissione si verifica quando FEV1 è inferiore al 40% del valore previsto.
Quando il grado di menomazione è valutato dal valore del FEV1rapporto /FVC, viene diagnosticato un difetto lieve se il rapporto scende tra il 60% e il 74%; compromissione moderata se il rapporto è compreso tra il 41% e il 59%; e grave compromissione se il rapporto è pari o inferiore al 40%.
Prevalenza della BPCO
Le prove accumulate indicano che la BPCO è un problema comune in molti paesi. La sua prevalenza è più alta negli uomini che nelle donne e aumenta con l'età. La bronchite cronica, una forma diagnostica ben standardizzata di BPCO, è da due a tre volte più diffusa negli uomini che nelle donne. Ampi sondaggi documentano che solitamente tra il 10% e il 20% degli uomini adulti nella popolazione generale soddisfano i criteri diagnostici di bronchite cronica (Tabella 18). La malattia è molto più frequente tra i fumatori, sia negli uomini che nelle donne. L'incidenza della BPCO nelle popolazioni occupate è discussa di seguito.
Tabella 1. Prevalenza della BPCO in paesi selezionati: risultati di ampie indagini
| Paese | Anno | Profilo demografico | Maschi | Le femmine | ||||
| SMK (%) | CB (%) | BPCO/CAL (%) | SMK (%) | CB (%) | BPCO/CAL (%) | |||
| USA | 1978 | 4,699 | 56.6 | 16.5 | nr | 36.2 | 5.9 | nr |
| USA | 1982 | 2,540 | 52.8 | 13.0 | 5.2 | 32.2 | 4.1 | 2.5 |
| UK | 1961 | 1,569 | 17.0 | nr | nr | 8.0 | nr | |
| Italia | 1988 | 3,289 | 49.2 | 13.1 | nr | 26.9 | 2.8 | nr |
| Polonia | 1986 | 4,335 | 59.6 | 24.2 | 8.5 | 26.7 | 10.4 | 4.9 |
| Nepal | 1984 | 2,826 | 78.3 | 17.6 | nr | 58.9 | 18.9 | nr |
| Giappone | 1977 | 22,590 | nr | 5.8 | nr | nr | 3.1 | nr |
| Australia | 1968 | 3,331 | nr | 6.3 | nr | nr | 2.4 | nr |
Legenda: SMK = abitudine al fumo; CB = bronchite cronica; BPCO/CAL = broncopneumopatia cronica ostruttiva/limitazione cronica delle vie aeree; nr = non segnalato.
Modificato con il permesso di: Woolcock 1989.
Fattori di rischio di BPCO, compreso l'effetto delle esposizioni professionali
La BPCO è un disturbo ad eziologia multifattoriale. Numerosi studi hanno fornito prove di una dipendenza causale della BPCO da molti fattori di rischio, classificati come ospite e fattori ambientali. Il ruolo delle esposizioni professionali tra i fattori di rischio ambientale nella genesi della BPCO è stato riconosciuto in seguito all'accumulo di evidenze epidemiologiche pubblicate nel periodo 1984-1988. Recentemente sono stati confermati effetti indipendenti del fumo e delle esposizioni professionali, sulla base dei risultati degli studi pubblicati dal 1966 al 1991. La tabella 2 riassume lo stato attuale delle conoscenze sull'eziologia multifattoriale della BPCO.
Tabella 2. Fattori di rischio implicati nella BPCO
| Fattore correlate a |
Reti | putativo |
| ospite | Deficit di antitripsina per età sessuale | Atopia Fattori familiari Aumento della reattività delle vie aeree Salute pregressa |
| Ambiente | Fumo di tabacco (personale) | Fumo di tabacco (ambientale) Inquinamento atmosferico Esposizione professionale |
Riprodotto con il permesso di: Becklake et al. 1988.
L'insorgenza di bronchite cronica nelle popolazioni occupazionali è un potenziale marker di esposizione significativa a sostanze irritanti professionali. Un effetto significativo dell'esposizione alla polvere industriale sullo sviluppo della bronchite cronica è stato documentato nei lavoratori impiegati nell'estrazione del carbone, nell'industria siderurgica, nonché nell'industria tessile, edile e agricola. In generale, gli ambienti più polverosi sono associati a una maggiore prevalenza dei sintomi dell'espettorazione cronica. Gli studi di prevalenza, tuttavia, sono soggetti a "effetto lavoratore sano", un pregiudizio che si traduce in una sottostima dell'impatto sulla salute delle esposizioni professionali dannose. Più conclusivi, ma meno disponibili, sono i dati sull'incidenza della malattia. In alcune professioni il tasso di incidenza della bronchite cronica è elevato e va da 197-276/10,000 negli agricoltori a 380/10,000 negli operai metalmeccanici e 724/10,000 nei minatori e cavatori, contro i 108/10,000 negli impiegati.
Questo modello, e anche l'effetto causale del fumo, sono in linea con il concetto che la bronchite cronica presenta una risposta comune all'inalazione cronica di irritanti respiratori.
Si ritiene che un effetto deleterio del carico di polvere polmonare provochi un'infiammazione cronica aspecifica della parete bronchiale. Questo tipo di risposta infiammatoria è stata documentata in lavoratori esposti a polveri organiche e suoi costituenti, come ad esempio cereali ed endotossine, entrambi responsabili dell'infiammazione neutrofila. Il ruolo della suscettibilità individuale non può essere escluso e i fattori noti correlati all'ospite includono infezioni respiratorie pregresse, l'efficienza dei meccanismi di clearance e fattori genetici scarsamente determinati, mentre il fumo di sigaretta rimane una singola causa ambientale più potente di bronchite cronica.
Il contributo delle esposizioni professionali all'eziologia dell'enfisema non è chiaramente compreso. I presunti fattori causali includono ossido di azoto, ozono e cadmio, come suggerito da osservazioni sperimentali. I dati forniti dall'epidemiologia occupazionale sono meno convincenti e possono essere difficili da ottenere a causa dei livelli generalmente bassi di esposizione professionale e dell'effetto predominante del fumo. Questo è particolarmente importante in caso di cd enfisema centriacinare. L'altra forma patologica della malattia, l'enfisema panacinare, è considerata ereditaria e correlata all'alfa1-deficit di antitripsina.
L'infiammazione bronchiolare e peribronchiolare, accompagnata da un progressivo restringimento del segmento interessato dell'albero bronchiale (malattia delle vie aeree periferiche o bronchiolite costrittiva) può essere osservata in una varietà di condizioni alla base dei sintomi della BPCO, in diversi stadi della storia naturale. In ambito lavorativo, la malattia di solito segue un danno polmonare acuto dovuto all'inalazione di fumi tossici, come anidride solforosa, ammoniaca, cloro e ossidi di azoto. Tuttavia, l'epidemiologia occupazionale della bronchiolite costrittiva rimane in gran parte poco chiara. Evidentemente, i suoi primi stadi sono difficili da identificare a causa della sintomatologia non specifica e della limitazione della procedura diagnostica. Si sa di più sui casi successivi agli incidenti sul lavoro. In caso contrario, la malattia può passare inosservata fino allo sviluppo di una sintomatologia conclamata e di un'obiettiva compromissione respiratoria (ossia, limitazione cronica del flusso aereo).
La CAL non è infrequente in diversi gruppi professionali e, come documentato da studi controllati, la sua prevalenza negli operai può superare quella degli impiegati. A causa della complessa eziologia della CAL, compreso l'effetto del fumo e dei fattori di rischio correlati all'ospite, i primi studi sull'associazione tra limitazione cronica del flusso aereo ed esposizione professionale erano inconcludenti. La moderna epidemiologia occupazionale, impiegando la progettazione orientata agli obiettivi e la modellizzazione delle relazioni esposizione-risposta, ha fornito prove sull'associazione della capacità del flusso d'aria con l'esposizione a polveri, fumi e gas sia minerali che organici.
Studi longitudinali basati sulla forza lavoro condotti su lavoratori esposti a polveri minerali e organiche ea fumi e gas mostrano che la perdita di funzionalità polmonare è associata a esposizioni professionali. I risultati riassunti nella tabella 3 dimostrano un effetto significativo dell'esposizione alla polvere nelle miniere di carbone e ferro, nell'industria del cemento-amianto, nei lavoratori dell'acciaio e delle fonderie e nei lavoratori delle cartiere. Una serie di esposizioni analizzate è composta da esposizione a polveri e fumi (come idrocarburi non alogenati, pitture, resine o vernici) e gas (come anidride solforosa o ossidi di azoto). Secondo i risultati di una revisione completa, limitata agli articoli più validi e sistematicamente analizzati sulla BPCO e l'esposizione professionale alla polvere, si può stimare che 80 su 1,000 minatori di carbone non fumatori potrebbero sviluppare almeno il 20% di perdita di FEVXNUMX.1 dopo 35 anni di lavoro con una concentrazione media di polvere respirabile di 2 mg/m3, e per i cercatori d'oro non fumatori il rispettivo rischio potrebbe essere tre volte maggiore.
Tabella 3. Perdita della funzione ventilatoria in relazione alle esposizioni professionali: risultati di studi longitudinali selezionati basati sulla forza lavoro
| Paese (anno) | Soggetti ed esposizioni | Prova utilizzata | Perdita annuale di funzionalità* | |||
| NE | E | NS | S | |||
| UK (1982) | 1,677 minatori di carbone | FEVXNUMX ml | 37 | 41 (av) 57 (max) |
37 | 48 |
| USA (1985) | 1,072 minatori di carbone | FEVXNUMX ml | 40 | 47 | 40 | 49 |
| Italia (1984) | 65 lavoratori del cemento amianto | FEVXNUMX ml | 9 | 49 | Non data | Non data |
| Svezia (1985) | 70 lavoratori del cemento amianto | FEV% | 4.2 | 9.2 | 3.7 | 9.4 |
| Francia (1986) | 871 minatori di ferro | FEV% | 6 | 8 | 5 | 7 |
| Francia (1979) | 159 operai siderurgici | FEV% | 0.6 | 7.4 | Non data | Non data |
| Canada (1984) | 179 lavoratori delle miniere e delle fonderie | FEVXNUMX/FVC% | 1.6 | 3.1 | 2.0 | 3.4 |
| Francia (1982) | 556 lavoratori nelle fabbriche | FEVXNUMX ml | 42 | 50 52 (polvere) 47 (gas) 55 (calore) |
40 | 48 |
| Finlandia (1982) | 659 lavoratori della cartiera | FEVXNUMX ml | Nessun effetto | Nessun effetto | 37 | 49 |
| Canada (1987) | 972 lavoratori delle miniere e delle fonderie | FEVXNUMX ml | 69 (torrefazione) 49 (forno) 33 (estrazione mineraria) |
41 | 54 | |
* La tabella mostra la perdita media annua di funzionalità polmonare negli esposti (E) rispetto ai non esposti (NE), e nei fumatori (S) rispetto ai non fumatori (NS). Effetti indipendenti del fumo (S) e/o dell'esposizione (E) si sono rivelati significativi nelle analisi effettuate dagli autori in tutti gli studi ad eccezione dello studio finlandese.
Modificato con il permesso di: Becklake 1989.
Studi selezionati eseguiti con i lavoratori del grano mostrano l'effetto dell'esposizione professionale alla polvere organica sui cambiamenti longitudinali nella funzione polmonare. Sebbene limitati nel numero e nella durata del follow-up, i risultati documentano una relazione indipendente del fumo con la perdita annuale della funzione polmonare (rispetto all'esposizione alla polvere di grano).
patogenesi
Il disturbo fisiopatologico centrale della BPCO è la limitazione cronica del flusso aereo. Il disturbo deriva dal restringimento delle vie aeree - una condizione che ha un meccanismo complesso nella bronchite cronica - mentre nell'enfisema l'ostruzione delle vie aeree deriva principalmente dal basso ritorno elastico del tessuto polmonare. Entrambi i meccanismi spesso coesistono.
Le anomalie strutturali e funzionali osservate nella bronchite cronica comprendono l'ipertrofia e l'iperplasia delle ghiandole sottomucose associate all'ipersecrezione mucosa. I cambiamenti infiammatori portano a iperplasia della muscolatura liscia e gonfiore della mucosa. L'ipersecrezione mucosa e il restringimento delle vie aeree favoriscono infezioni batteriche e virali delle vie respiratorie, che possono ulteriormente aumentare l'ostruzione delle vie aeree.
La limitazione del flusso aereo nell'enfisema riflette la perdita del ritorno elastico come conseguenza della distruzione delle fibre di elastina e del collasso della parete bronchiolare a causa dell'elevata compliance polmonare. Si ritiene che la distruzione delle fibre di elastina derivi da uno squilibrio nel sistema proteolitico-antiproteolitico, in un processo noto anche come carenza di inibitore della proteasi. Alfa1-antitripsina è la proteasi più potente che inibisce l'effetto dell'elastasi sugli alveoli nell'uomo. I neutrofili e i macrofagi che rilasciano elastasi si accumulano in risposta ai mediatori dell'infiammazione locale e all'inalazione di vari irritanti respiratori, compreso il fumo di tabacco. Gli altri inibitori meno potenti sono a2-macroglobulina e inibitore dell'elastasi a basso peso, rilasciato dalle ghiandole sottomucose.
Recentemente, l'ipotesi della carenza di antiossidanti è stata esaminata per il suo ruolo nei meccanismi patogenetici dell'enfisema. L'ipotesi sostiene che gli ossidanti, se non inibiti dagli antiossidanti, causino danni al tessuto polmonare, portando all'enfisema. Gli ossidanti noti includono fattori esogeni (ozono, cloro, ossidi di azoto e fumo di tabacco) e fattori endogeni come i radicali liberi. I fattori antiossidanti più importanti includono antiossidanti naturali come le vitamine E e C, catalasi, superossido dismutasi, glutatione, ceruloplasmina e antiossidanti sintetici come N-acetilcisteina e allopurinolo. C'è un numero crescente di prove sul sinergismo per quanto riguarda i meccanismi di carenza di antiossidanti e di inibitori della proteasi nella patogenesi dell'enfisema.
Patologia
Dal punto di vista patologico, la bronchite cronica è caratterizzata da ipertrofia e iperplasia delle ghiandole nella sottomucosa delle grandi vie aeree. Di conseguenza, il rapporto tra lo spessore della ghiandola bronchiale e lo spessore della parete bronchiale (il cosiddetto Indice Reid) aumenta. Altre anomalie patologiche comprendono la metaplasia dell'epitelio ciliare, l'iperplasia della muscolatura liscia e le infiltrazioni neutrofile e linfocitarie. I cambiamenti nelle grandi vie aeree sono spesso accompagnati da anomalie patologiche nei piccoli bronchioli.
I cambiamenti patologici nei piccoli bronchioli sono stati costantemente documentati come vari gradi del processo infiammatorio delle pareti delle vie aeree. Dopo l'introduzione del concetto di malattia delle piccole vie aeree, l'attenzione si è concentrata sulla morfologia dei segmenti separati dei bronchioli. L'esame istologico dei bronchioli membranosi, espansi successivamente ai bronchioli respiratori, evidenzia infiammazione parietale, fibrosi, ipertrofia muscolare, deposizione di pigmento, metaplasia epiteliale calice e squamosa e macrofagi intraluminali. Le anomalie patologiche del tipo sopra descritto sono state denominate "malattia delle vie aeree indotta da polvere minerale". Una condizione associata dimostrata in questo segmento del tratto respiratorio è l'alveolite fibrosante peribronchiolare, che si ritiene rappresenti la reazione precoce del tessuto polmonare all'inalazione di polvere minerale.
I cambiamenti patologici nell'enfisema possono essere classificati come enfisema centriacinare or enfisema panacinare. La prima entità è in gran parte limitata al centro dell'acino, mentre la seconda forma comporta cambiamenti in tutte le strutture dell'acino. Sebbene si ritenga che l'enfisema panacinare rifletta un deficit ereditario di un inibitore della proteasi, entrambe le forme possono coesistere. Nell'enfisema, i bronchioli terminali mostrano segni di infiammazione e gli spazi aerei distali sono ingranditi in modo anomalo. La distruzione strutturale coinvolge alveoli, capillari e può portare alla formazione di ampi spazi aerei anomali (enfisema bolloso). L'enfisema centriacinare tende a localizzarsi nei lobi polmonari superiori mentre l'enfisema panacinare si trova solitamente nei lobi polmonari inferiori.
Sintomi clinici
La tosse cronica e l'espettorazione del catarro sono due sintomi principali della bronchite cronica, mentre la dispnea (respiro corto) è una caratteristica clinica dell'enfisema. Nei casi avanzati, i sintomi di espettorazione cronica e dispnea di solito coesistono. L'insorgenza e la progressione della dispnea suggeriscono lo sviluppo di una limitazione cronica del flusso aereo. Secondo i sintomi e lo stato fisiologico, la presentazione clinica della bronchite cronica comprende tre forme della malattia: bronchite semplice, mucopurulenta e ostruttiva.
Nella bronchite cronica, i risultati dell'auscultazione del torace possono rivelare suoni respiratori normali. Nei casi avanzati ci può essere un tempo espiratorio prolungato, sibili e rantoli, uditi durante l'espirazione. La cianosi è comune nella bronchite ostruttiva avanzata.
La diagnosi clinica di enfisema è difficile nella sua fase iniziale. La dispnea può essere un singolo reperto. Il paziente con enfisema avanzato può avere il torace a botte e segni di iperventilazione. Come risultato dell'iperinflazione polmonare, altri risultati includono iperrisonanza, diminuzione dell'escursione diaframmatica e diminuzione dei suoni respiratori. La cianosi è rara.
A causa di fattori causali simili (prevalentemente l'effetto del fumo di tabacco) e di presentazione simile, la diagnosi di bronchite cronica nei confronti dell'enfisema può essere difficile, specialmente se la limitazione cronica del flusso aereo domina il quadro. La tabella 4 fornisce alcuni indizi utili per la diagnosi. La forma avanzata di BPCO può assumere due tipi estremi: bronchite predominante ("bloater blu") o enfisema predominante ("puffer rosa").
Tabella 4. Classificazione diagnostica di due tipi clinici di BPCO, bronchite cronica ed enfisema
| Segni/sintomi | Bronchite predominante ("Gonfiore blu") |
Enfisema predominante ("Puffo rosa") |
| Massa corporea | Maggiori prenotazioni | Diminuzione |
| cianosi | Frequente | Infrequente |
| Tosse | Sintomo predominante | Intermittente |
| sputo | Grossa quantità | Raro |
| Dispnea | Solitamente contrassegnato durante l'esercizio | Sintomo predominante |
| Suoni del respiro | Normale o leggermente diminuito, suoni polmonari avventizi |
Diminuzione |
| Cuore polmonare | Frequente | Infrequente |
| Infezioni respiratorie | Frequente | Infrequente |
La radiologia del torace ha un valore diagnostico limitato nella bronchite cronica e nelle prime fasi dell'enfisema. L'enfisema avanzato mostra un pattern radiologico di aumentata radiotrasparenza (iperinflazione). La tomografia computerizzata fornisce una migliore comprensione della posizione e dell'entità dei cambiamenti enfisematosi, inclusa la differenziazione tra enfisema centriacinare e panacinare.
I test di funzionalità polmonare hanno una posizione consolidata nella valutazione diagnostica della BPCO (tabella 5). La batteria di test di importanza pratica nella valutazione funzionale della bronchite cronica e dell'enfisema comprende capacità funzionale residua (FRC), volume residuo (RV), capacità polmonare totale (TLC), FEV1 e FEV1/VC, resistenza delle vie aeree (Raw), conformità statica (Cst), rinculo elastico (PL, el), emogas (PaO2, Pa CO2) e capacità di diffusione (DLCO).
Tabella 5. Test di funzionalità polmonare nella diagnosi differenziale di due tipi clinici di BPCO, bronchite cronica ed enfisema
| Test di funzionalità polmonare | Bronchite predominante ("Gonfiore blu") |
Enfisema predominante ("Puffo rosa") |
| Camper, FRC, TLC | Normale o leggermente aumentato | Notevolmente aumentato |
| FEV1 , FEV1 /VC | Diminuzione | Diminuzione |
| Raw | Notevolmente aumentato | Leggermente aumentato |
| Cst | Normale | Notevolmente aumentato |
| PL, el | Normale | Notevolmente aumentato |
| PaO2 | Notevolmente aumentato | Leggermente diminuito |
| PaCO2 | Maggiori prenotazioni | Normale |
| DLCO | Normale o leggermente diminuito | Diminuzione |
RV = volume residuo; FRC = capacità residua funzionale; TLC = capacità polmonare totale; FEV1 = volume espiratorio forzato nel primo secondo e VC = capacità vitale; Raw = resistenza delle vie aeree; Cst = conformità statica; PL, el = rinculo elastico; PaO2 e PaCO2 = gas nel sangue; DLCO = capacità di diffusione.
La diagnosi clinica della malattia delle vie aeree periferiche non è possibile. Molto spesso la malattia accompagna la bronchite cronica o l'enfisema o addirittura precede la presentazione clinica di entrambe le ultime forme o della BPCO. La forma isolata di malattia delle vie aeree periferiche può essere studiata mediante test di funzionalità polmonare, sebbene lo stato funzionale delle vie aeree periferiche sia difficile da valutare. Questa parte dell'albero bronchiale contribuisce a meno del 20% della resistenza totale al flusso aereo e le anomalie isolate e lievi nelle piccole vie aeree sono considerate inferiori al livello di rilevabilità della spirometria convenzionale. I metodi più sensibili progettati per misurare la funzione delle vie aeree periferiche includono una serie di test, tra i quali i seguenti sono quelli di uso più frequente: flusso medio espiratorio massimo (FEF25-75), portate a bassi volumi polmonari (MEF50, MEF25), indice di azoto in un singolo respiro (SBN2/l), capacità di chiusura (CC), conduttanza del flusso d'aria a monte (Gus) e la compliance dipendente dalla frequenza (Cfd). In generale, si ritiene che questi test abbiano una bassa specificità. Su basi teoriche FEF25-75 e MEF50,25 dovrebbe riflettere innanzitutto i meccanismi di limitazione del calibro, mentre SBN2/l è pensato per essere più specifico per le proprietà meccaniche degli spazi aerei. I primi indici sono usati più frequentemente nell'epidemiologia occupazionale.
Diagnosi differenziale
Le differenze fondamentali tra bronchite cronica ed enfisema sono mostrate nelle tabelle 4 e 5. Tuttavia, in singoli casi la diagnosi differenziale è difficile e talvolta impossibile da condurre con un discreto grado di sicurezza. In alcuni casi è anche difficile distinguere tra BPCO e asma. In pratica, l'asma e la BPCO non sono entità ben definite e vi è un ampio grado di sovrapposizione tra le due malattie. Nell'asma, l'ostruzione delle vie aeree è solitamente intermittente, mentre nella BPCO è costante. Il decorso della limitazione del flusso aereo è più variabile nell'asma che nella BPCO.
Gestione del caso
La gestione clinica della BPCO comporta la cessazione dell'abitudine al fumo, l'unica misura più efficace. L'esposizione professionale a sostanze irritanti per le vie respiratorie deve essere interrotta o evitata. La gestione clinica dovrebbe concentrarsi sul corretto trattamento delle infezioni respiratorie e dovrebbe comportare regolari vaccinazioni antinfluenzali. La terapia con broncodilatatori è giustificata nei pazienti con limitazione del flusso aereo e dovrebbe comprendere b2-agonisti adrenergici e anticolinergici, somministrati in monoterapia o in associazione, preferibilmente per aerosol. La teofillina è ancora in uso sebbene il suo ruolo nella gestione della BPCO sia controverso. La terapia a lungo termine con corticosteroidi può essere efficace in alcuni casi. L'ipersecrezione bronchiale è spesso trattata con farmaci mucoattivi che influenzano la produzione di muco, la struttura del muco o la clearance mucociliare. La valutazione degli effetti della terapia mucolitica è difficile perché questi farmaci non sono usati come monoterapia della BPCO. Pazienti con ipossiemia (PaO2 pari o inferiore a 55 mm Hg) qualificano per l'ossigenoterapia a lungo termine, un trattamento facilitato dall'accesso agli ossigenatori portatili. Terapia di aumento con alfa1-antitripsina può essere considerata nell'enfisema con alfa confermata1-deficit di antitripsina (fenotipo PiZZ). L'effetto dei farmaci antiossidanti (come la vitamina E e C) sul decorso dell'enfisema è in fase di studio.
Frodi
La prevenzione della BPCO dovrebbe iniziare con campagne antifumo rivolte sia alla popolazione generale che ai gruppi professionali a rischio. In ambito lavorativo, il controllo e la prevenzione delle esposizioni ad irritanti respiratori sono essenziali e costituiscono sempre una priorità. Queste attività dovrebbero mirare a un'effettiva riduzione dell'inquinamento atmosferico a livelli di sicurezza, solitamente definiti dai cosiddetti livelli di esposizione ammissibili. Poiché il numero di inquinanti atmosferici non è regolamentato o non è adeguatamente regolamentato, ogni sforzo per ridurre l'esposizione è giustificato. In circostanze in cui tale riduzione è impossibile da ottenere, è necessaria una protezione respiratoria personale per ridurre il rischio di esposizione individuale ad agenti nocivi.
La prevenzione medica della BPCO in ambiente lavorativo comprende due passaggi importanti: un programma di sorveglianza della salute respiratoria e un programma di formazione dei dipendenti.
Il programma di sorveglianza della salute respiratoria prevede una valutazione regolare della salute respiratoria; inizia con la valutazione iniziale (anamnesi, esame fisico, radiografia del torace e test di funzionalità polmonare standard) e continua ad essere eseguito periodicamente durante il periodo di impiego. Il programma ha lo scopo di valutare la salute respiratoria di base dei lavoratori (e di identificare i lavoratori con compromissione respiratoria soggettiva e/o oggettiva) prima dell'inizio del lavoro e di rilevare i primi segni di compromissione respiratoria durante la sorveglianza continua dei lavoratori. I lavoratori con risultati positivi devono essere ritirati dall'esposizione e inviati per un'ulteriore valutazione diagnostica.
Il programma di formazione dei dipendenti dovrebbe essere basato sul riconoscimento affidabile dei rischi respiratori presenti nell'ambiente di lavoro e dovrebbe essere progettato da professionisti della salute, igienisti industriali, ingegneri della sicurezza e la direzione. Il programma dovrebbe fornire ai lavoratori informazioni adeguate sui rischi respiratori sul posto di lavoro, sui potenziali effetti respiratori delle esposizioni e sulle normative pertinenti. Dovrebbe anche comportare la promozione di pratiche di lavoro sicure e di uno stile di vita sano.
Effetti sulla salute delle fibre sintetiche
L'uso industriale di vari tipi di fibre sintetiche è in aumento, in particolare da quando sono state poste restrizioni sull'uso dell'amianto in considerazione dei suoi noti rischi per la salute. Il potenziale di effetti negativi sulla salute legati alla produzione e all'uso di fibre sintetiche è ancora in fase di studio. Questo articolo fornirà una panoramica dei principi generali relativi al potenziale di tossicità correlato a tali fibre, una panoramica dei vari tipi di fibre in produzione (come elencato nella tabella 1) e un aggiornamento sugli studi esistenti e in corso sui loro potenziali effetti sulla salute .
Tabella 1. Fibre sintetiche
| Fibre sintetiche |
Ossido di alluminio Carbonio/grafite Kevlar® para-aramidiche Fibre di carburo di silicio e |
|
| Fibre vetrose artificiali |
Fibra di vetro
Lana minerale
Fibra ceramica refrattaria |
Lana di vetro Lana di roccia |
Determinanti di tossicità
I principali fattori correlati alla potenziale tossicità dovuta all'esposizione alle fibre sono:
- dimensione della fibra
- durata della fibra e
- dose all'organo bersaglio.
In generale, le fibre lunghe e sottili (ma di dimensioni respirabili) e durevoli hanno il maggior potenziale di causare effetti avversi se rilasciate nei polmoni in concentrazione sufficiente. La tossicità delle fibre è stata correlata in studi di inalazione su animali a breve termine con infiammazione, citotossicità, funzione alterata dei macrociti e biopersistenza. Il potenziale cancerogeno è molto probabilmente correlato al danno del DNA cellulare attraverso la formazione di radicali liberi dell'ossigeno, la formazione di fattori clastogenici o la missegregazione dei cromosomi nelle cellule in mitosi, da soli o in combinazione. Le fibre di dimensione respirabile sono quelle di diametro inferiore a 3.0-3.5 mm e di lunghezza inferiore a 200 μm. Secondo l'"ipotesi di Stanton", il potenziale cancerogeno delle fibre (come determinato da studi di impianto pleurico animale) è correlato alla loro dimensione (il rischio maggiore è associato a fibre di diametro inferiore a 0.25 μm e lunghezza superiore a 8 mm) e alla durata (Stanton et al. 1981). Le fibre minerali presenti in natura, come l'amianto, esistono in una struttura policristallina che ha la propensione a fendersi lungo i piani longitudinali, creando fibre più sottili con rapporti lunghezza-larghezza più elevati, che hanno un maggiore potenziale di tossicità. La stragrande maggioranza delle fibre artificiali sono non cristalline o amorfe e si fratturano perpendicolarmente al loro piano longitudinale in fibre più corte. Questa è una differenza importante tra silicati fibrosi di amianto e non-amianto e fibre sintetiche. La durata delle fibre depositate nel polmone dipende dalla capacità del polmone di eliminare le fibre, nonché dalle proprietà fisiche e chimiche delle fibre. La durabilità delle fibre sintetiche può essere modificata nel processo di produzione, in base ai requisiti dell'uso finale, attraverso l'aggiunta di alcuni stabilizzanti come Al2O3. A causa di questa variabilità dei costituenti chimici e delle dimensioni delle fibre sintetiche, la loro potenziale tossicità deve essere valutata in base al tipo di fibra.
Fibre sintetiche
Fibre di ossido di alluminio
La tossicità della fibra di ossido di alluminio cristallino è stata suggerita da un caso clinico di fibrosi polmonare in un lavoratore impiegato nella fusione dell'alluminio per 19 anni (Jederlinic et al. 1990). La sua radiografia del torace ha rivelato una fibrosi interstiziale. L'analisi del tessuto polmonare mediante tecniche di microscopia elettronica ha dimostrato 1.3 × 109 fibre cristalline per grammo di tessuto polmonare secco, o dieci volte più fibre del numero di fibre di amianto trovate nel tessuto polmonare da minatori di amianto crisotilo con asbestosi. Sono necessari ulteriori studi per determinare il ruolo delle fibre di ossido di alluminio cristallino (figura 1) e della fibrosi polmonare. Questo case report, tuttavia, suggerisce la possibilità che si verifichi la fibrizzazione quando coesistono condizioni ambientali adeguate, come un aumento del flusso d'aria attraverso i materiali fusi. Sia la microscopia ottica a contrasto di fase che la microscopia elettronica con analisi a raggi X a dispersione di energia dovrebbero essere utilizzate per identificare potenziali fibre aerodisperse nell'ambiente di lavoro e nei campioni di tessuto polmonare nei casi in cui vi siano risultati clinici compatibili con pneumoconiosi indotta da fibre.
Figura 1. Micrografia elettronica a scansione (SEM) di fibre di ossido di alluminio.
Per gentile concessione di T. Hesterberg.
Fibre di carbonio/grafite
Fibre di pece carbonacea, rayon o poliacrilonitrile riscaldate a 1,200°C formano fibre di carbonio amorfo, e quando riscaldate oltre 2,20°C formano fibre di grafite cristallina (figura 2). Possono essere aggiunti leganti di resina per aumentare la resistenza e per consentire lo stampaggio e la lavorazione del materiale. Generalmente, queste fibre hanno un diametro compreso tra 7 e 10 μm, ma si verificano variazioni di dimensioni dovute al processo di fabbricazione e alla manipolazione meccanica. I compositi carbonio/grafite sono utilizzati nell'industria aeronautica, automobilistica e degli articoli sportivi. L'esposizione a particelle di carbonio/grafite di dimensioni respirabili può verificarsi durante il processo di produzione e con manipolazione meccanica. Inoltre, è possibile produrre piccole quantità di fibre di dimensioni respirabili quando i compositi vengono riscaldati a una temperatura compresa tra 900 e 1,10 °C. Le conoscenze esistenti su queste fibre sono inadeguate per fornire risposte certe sul loro potenziale di causare effetti nocivi sulla salute. Gli studi che hanno coinvolto l'iniezione intratracheale di diverse polveri composite di fibre di grafite nei ratti hanno prodotto risultati eterogenei. Tre dei campioni di polvere testati hanno prodotto una tossicità minima e due dei campioni hanno prodotto una tossicità costante come manifestato dalla citotossicità per i macrofagi alveolari e dalle differenze nel numero totale di cellule recuperate dal polmone (Martin, Meyer e Luchtel 1989). Effetti clastogenici sono stati osservati in studi di mutagenicità di fibre a base di pece, ma non di fibre di carbonio a base di poliacrilonitrile. Uno studio decennale sugli addetti alla produzione di fibre di carbonio, che fabbricavano fibre da 8 a 10 mm di diametro, non ha rivelato alcuna anomalia (Jones, Jones e Lyle 1982). Fino a quando non saranno disponibili ulteriori studi, si raccomanda che l'esposizione a fibre di carbonio/grafite di dimensioni respirabili sia pari o inferiore a 1 fibra/ml (f/ml) e che l'esposizione a particelle composite di dimensioni respirabili sia mantenuta al di sotto dell'attuale standard di polvere respirabile per polvere fastidiosa.
Figura 2. SEM di fibre di carbonio.
Fibre para-aramidiche di kevlar
Kevlar le fibre di para-aramide hanno un diametro di circa 12 μm e le fibrille ricurve a forma di nastro sulla superficie delle fibre hanno una larghezza inferiore a 1 mm (figura 3). Le fibrille si staccano parzialmente dalle fibre e si incastrano con altre fibrille per formare grumi di dimensioni non respirabili. Le proprietà fisiche di Kevlar le fibre includono una notevole resistenza al calore e resistenza alla trazione. Hanno molti usi diversi, fungendo da agente rinforzante in plastica, tessuti e gomma e come materiale di attrito per i freni delle automobili. La media ponderata nel tempo (TWA) di otto ore dei livelli di fibrille durante la produzione e le applicazioni finali varia da 0.01 a 0.4 f/ml (Merriman 1989). Livelli molto bassi di Kevlar le fibre di aramide vengono generate nella polvere quando vengono utilizzate nei materiali di attrito. Gli unici dati disponibili sugli effetti sulla salute provengono da studi sugli animali. Gli studi sull'inalazione nel ratto che hanno coinvolto periodi di tempo da uno a due anni e l'esposizione a fibrille a 25, 100 e 400 f/ml hanno rivelato una bronchiolarizzazione alveolare correlata alla dose. A livelli di esposizione più elevati sono state notate anche lievi fibrosi e alterazioni fibrotiche del dotto alveolare. La fibrosi potrebbe essere stata correlata al sovraccarico dei meccanismi di clearance polmonare. Un tipo di tumore unico nei ratti, il tumore a cellule squamose cheratinizzante cistico, si è sviluppato in alcuni degli animali dello studio (Lee et al. 1988). Studi di inalazione a breve termine sui ratti indicano che le fibrille hanno una bassa durata nel tessuto polmonare e vengono eliminate rapidamente (Warheit et al. 1992). Non sono disponibili studi sugli effetti sulla salute umana dell'esposizione a Kevlar fibra para-aramidica. Tuttavia, alla luce dell'evidenza di una ridotta biopersistenza e data la struttura fisica di Kevlar, i rischi per la salute dovrebbero essere minimi se le esposizioni alle fibrille vengono mantenute a 0.5 f/ml o meno, come avviene ora nelle applicazioni commerciali.
Figura 3. SEM di fibre para-aramidiche di Kevlar.
Fibre e baffi di carburo di silicio
Il carburo di silicio (carborundum) è un materiale abrasivo e refrattario ampiamente utilizzato che viene prodotto combinando silice e carbonio a 2,400°C. Fibre e baffi di carburo di silicio - figura 4 (Harper et al. 1995) - possono essere generati come sottoprodotti della fabbricazione di cristalli di carburo di silicio o possono essere appositamente prodotti come fibre policristalline o baffi monocristallini. Le fibre generalmente hanno un diametro inferiore a 1-2 μm e una lunghezza compresa tra 3 e 30 μm. I baffi hanno un diametro medio di 0.5 μm e una lunghezza di 10 μm. L'incorporazione di fibre e baffi di carburo di silicio aggiunge forza a prodotti come compositi a matrice metallica, ceramiche e componenti ceramici. L'esposizione a fibre e baffi può verificarsi durante i processi di produzione e lavorazione e potenzialmente durante i processi di lavorazione e finitura. Ad esempio, è stato dimostrato che l'esposizione a breve termine durante la manipolazione di materiali riciclati raggiunge livelli fino a 5 f/ml. La lavorazione di compositi a matrice metallica e ceramica ha portato a concentrazioni di esposizione TWA di otto ore di 0.031 f/ml e fino a 0.76 f/ml, rispettivamente (Scansetti, Piolatto e Botta 1992; Bye 1985).
Figura 4. SEM di fibre di carburo di silicio (A) e baffi (B).
A.
I dati esistenti provenienti da studi su animali e umani indicano un potenziale fibrogenico definito e possibile cancerogeno. In vitro studi su colture di cellule di topo che coinvolgono baffi di carburo di silicio hanno rivelato una citotossicità uguale o superiore a quella risultante dall'amianto crocidolite (Johnson et al. 1992; Vaughan et al. 1991). L'iperplasia adenomatosa persistente dei polmoni di ratto è stata dimostrata in uno studio di inalazione subacuta (Lapin et al. 1991). Studi sull'inalazione di pecore che coinvolgono polvere di carburo di silicio hanno rivelato che le particelle erano inerti. Tuttavia, l'esposizione alle fibre di carburo di silicio ha provocato alveolite fibrosante e aumento dell'attività di crescita dei fibroblasti (Bégin et al. 1989). Gli studi sui campioni di tessuto polmonare dei lavoratori della produzione di carburo di silicio hanno rivelato noduli silicotici e corpi ferruginosi e hanno indicato che le fibre di carburo di silicio sono durevoli e possono esistere in alte concentrazioni nel parenchima polmonare. Anche le radiografie del torace sono state coerenti con alterazioni interstiziali nodulari e irregolari e placche pleuriche.
Le fibre e i baffi di carburo di silicio sono di dimensioni respirabili, durevoli e hanno un potenziale fibrogenico definito nel tessuto polmonare. Un produttore di baffi in carburo di silicio ha fissato uno standard interno a 0.2 f/ml come TWA di otto ore (Beaumont 1991). Si tratta di una raccomandazione prudente basata sulle informazioni sanitarie attualmente disponibili.
Fibre vetrose artificiali
Le fibre vetrose artificiali (MMVF) sono generalmente classificate come:
- fibra di vetro (lana di vetro o fibra di vetro, filamento di vetro continuo e fibra di vetro per usi speciali)
- lana minerale (lana di roccia e lana di scoria) e
- fibra ceramica (fibra tessile ceramica e fibra ceramica refrattaria).
Il processo di fabbricazione inizia con la fusione delle materie prime con successivo rapido raffreddamento, con conseguente produzione di fibre non cristalline (o vetrose). Alcuni processi di produzione consentono grandi variazioni in termini di dimensioni delle fibre, il limite inferiore è di 1 mm o meno di diametro (figura 5). Stabilizzatori (come Al2O3, TiO2 e ZnO) e modificatori (come MgO, Li2O, BaO, CaO, Na2O e K2O) può essere aggiunto per alterare le proprietà fisiche e chimiche come la resistenza alla trazione, l'elasticità, la durabilità e il non trasferimento termico.
Figura 5. SEM di lana di scoria.
Lana di roccia, fibre di vetro e fibre ceramiche refrattarie sono identiche nell'aspetto.
La fibra di vetro è prodotta da biossido di silicio e varie concentrazioni di stabilizzanti e modificatori. La maggior parte della lana di vetro viene prodotta attraverso l'uso di un processo rotativo che produce fibre discontinue di diametro medio da 3 a 15 μm con variazioni di diametro fino a 1 μm o meno. Le fibre di lana di vetro sono legate insieme, più comunemente con resine fenoliche di formaldeide, e quindi sottoposte a un processo di polimerizzazione a caldo. Possono essere aggiunti anche altri agenti, inclusi lubrificanti e agenti bagnanti, a seconda del processo di produzione. Il processo di produzione del filamento di vetro continuo comporta una minore variazione dal diametro medio della fibra rispetto alla lana di vetro e alla fibra di vetro per usi speciali. Le fibre a filamento di vetro continuo hanno un diametro compreso tra 3 e 25 μm. La produzione di fibre di vetro per scopi speciali comporta un processo di fibrizzazione con attenuazione della fiamma che produce fibre con un diametro medio inferiore a 3 μm.
La produzione di lana di scoria e lana di roccia comporta rispettivamente la fusione e la fibrificazione di scorie di minerali metallici e rocce ignee. Il processo di produzione comprende un processo di ruota a forma di disco e centrifuga a ruota. Produce fibre discontinue di diametro medio da 3.5 a 7 μm la cui dimensione può variare bene nella gamma respirabile. La lana minerale può essere prodotta con o senza legante, a seconda delle applicazioni di utilizzo finale.
La fibra ceramica refrattaria viene prodotta attraverso una centrifuga a ruota o un processo di fibrizzazione a getto di vapore utilizzando caolino fuso, allumina/silice o allumina/silice/ossido di zirconio. I diametri medi delle fibre vanno da 1 a 5μm. Se riscaldate a temperature superiori a 1,000°C, le fibre ceramiche refrattarie possono subire la conversione in cristobalite (una silice cristallina).
MMVF con diversi diametri di fibra e composizione chimica sono utilizzati in oltre 35,000 applicazioni. La lana di vetro viene utilizzata in applicazioni di isolamento acustico e termico residenziali e commerciali, nonché nei sistemi di trattamento dell'aria. Il filamento continuo di vetro viene utilizzato nei tessuti e come agenti di rinforzo nelle materie plastiche come quelle impiegate nelle parti di automobili. La fibra di vetro per scopi speciali viene utilizzata in applicazioni speciali, ad esempio negli aerei, che richiedono elevate proprietà di isolamento termico e acustico. La lana di roccia e di scoria senza legante viene utilizzata come isolante soffiato e nei pannelli del controsoffitto. La lana di roccia e di scoria con un legante di resina fenolica viene utilizzata nei materiali isolanti, come coperte isolanti e materassini. La fibra ceramica refrattaria costituisce dall'1 al 2% della produzione mondiale di MMVF. La fibra ceramica refrattaria viene utilizzata in applicazioni industriali specializzate ad alta temperatura, come fornaci e forni. Lana di vetro, filamento di vetro continuo e lana di roccia vengono prodotti in grandi quantità.
Si ritiene che gli MMVF abbiano un potenziale minore rispetto ai silicati fibrosi presenti in natura (come l'amianto) per produrre effetti negativi sulla salute a causa del loro stato non cristallino e della loro propensione a fratturarsi in fibre più corte. I dati esistenti suggeriscono che l'MMVF più comunemente utilizzato, la lana di vetro, ha il minor rischio di produrre effetti nocivi per la salute, seguita dalla lana di roccia e di scoria, e quindi sia dalla fibra di vetro per usi speciali con una maggiore durata che dalla fibra ceramica refrattaria. La fibra di vetro per usi speciali e la fibra ceramica refrattaria hanno il maggior potenziale di esistere come fibre di dimensioni respirabili poiché hanno generalmente un diametro inferiore a 3 mm. Fibra di vetro per usi speciali (con maggiore concentrazione di stabilizzanti come Al2O3) e la fibra ceramica refrattaria sono anche durevoli nei fluidi fisiologici. I filamenti continui di vetro non sono di dimensioni respirabili e pertanto non rappresentano un potenziale rischio per la salute polmonare.
I dati sulla salute disponibili sono raccolti da studi sull'inalazione negli animali e studi sulla morbilità e sulla mortalità dei lavoratori coinvolti nella produzione di MMVF. Gli studi sull'inalazione che hanno comportato l'esposizione di ratti a due materiali isolanti in lana di vetro commerciali con un diametro medio di 1 μm e una lunghezza di 20 μm hanno rivelato una lieve risposta cellulare polmonare che si è parzialmente invertita dopo l'interruzione dell'esposizione. Risultati simili sono il risultato di uno studio sull'inalazione animale di un tipo di lana di scorie. La fibrosi minima è stata dimostrata con l'esposizione per inalazione di animali alla lana di roccia. Studi sull'inalazione di fibre ceramiche refrattarie hanno provocato cancro ai polmoni, mesotelioma e fibrosi pleurica e polmonare nei ratti e mesotelioma e fibrosi pleurica e polmonare nei criceti a una dose massima tollerata di 250 f/ml. A 75 f/ml e 120 f/ml, nei ratti è stato dimostrato un mesotelioma e una fibrosi minima, ea 25 f/ml, c'era una risposta cellulare polmonare (Bunn et al. 1993).
Può verificarsi irritazione della pelle, degli occhi e del tratto respiratorio superiore e inferiore e dipende dai livelli di esposizione e dalle mansioni lavorative. L'irritazione cutanea è stato l'effetto sulla salute più comune notato e può indurre fino al 5% dei nuovi lavoratori degli impianti di produzione di MMVF a lasciare il lavoro entro poche settimane. È causato da un trauma meccanico alla pelle causato da fibre di diametro superiore a 4-5 μm. Può essere prevenuto con adeguate misure di controllo ambientale, incluso evitare il contatto diretto della pelle con le fibre, indossare indumenti larghi e con maniche lunghe e lavare separatamente gli indumenti da lavoro. I sintomi delle vie respiratorie superiori e inferiori possono verificarsi in situazioni insolitamente polverose, in particolare nella fabbricazione di prodotti MMVF e nelle applicazioni di uso finale e in ambienti residenziali quando gli MMVF non vengono maneggiati, installati o riparati correttamente.
Gli studi sulla morbilità respiratoria, misurata dai sintomi, dalle radiografie del torace e dai test di funzionalità polmonare tra i lavoratori degli impianti di produzione in genere non hanno riscontrato effetti avversi. Tuttavia, uno studio in corso sui lavoratori degli impianti di produzione di fibre ceramiche refrattarie ha rivelato un'aumentata prevalenza di placche pleuriche (Lemasters et al. 1994). Gli studi sui lavoratori della produzione secondaria e sugli utenti finali di MMVF sono limitati e sono stati ostacolati dalla probabilità del fattore di confusione delle precedenti esposizioni all'amianto.
Proseguono in Europa e negli Stati Uniti gli studi sulla mortalità dei lavoratori negli impianti di produzione di fibre di vetro e lana minerale. I dati dello studio in Europa hanno rivelato un aumento complessivo della mortalità per cancro al polmone basato sui tassi di mortalità nazionali, ma non locali. C'è stata una tendenza all'aumento del cancro ai polmoni nelle coorti di vetro e lana minerale con il tempo dal primo impiego ma non con la durata dell'impiego. Usando i tassi di mortalità locale, c'è stato un aumento della mortalità per cancro al polmone per la prima fase della produzione di lana minerale (Simonato, Fletcher e Cherrie 1987; Boffetta et al. 1992). I dati dello studio negli Stati Uniti hanno dimostrato un aumento statisticamente significativo del rischio di cancro respiratorio, ma non sono riusciti a trovare un'associazione tra lo sviluppo del cancro e vari indici di esposizione alle fibre (Marsh et al. 1990). Ciò è in accordo con altri studi caso-controllo su lavoratori di impianti di produzione di lana di scorie e fibre di vetro che hanno rivelato un aumento del rischio di cancro ai polmoni associato al fumo di sigaretta, ma non nella misura dell'esposizione MMVF (Wong, Foliart e Trent 1991; Chiazze, Watkins e Fryar 1992). Uno studio sulla mortalità dei lavoratori della produzione di filamenti di vetro continui non ha rivelato un aumento del rischio di mortalità (Shannon et al. 1990). Negli Stati Uniti è in corso uno studio sulla mortalità che coinvolge i lavoratori della fibra ceramica refrattaria. Gli studi sulla mortalità dei lavoratori coinvolti nella fabbricazione dei prodotti e degli utenti finali di MMVF sono molto limitati.
Nel 1987, l'Agenzia internazionale per la ricerca sul cancro (IARC) ha classificato la lana di vetro, la lana di roccia, la lana di scoria e le fibre ceramiche come possibili agenti cancerogeni per l'uomo (gruppo 2B). Gli studi sugli animali in corso e gli studi sulla morbilità e mortalità dei lavoratori coinvolti con MMVF contribuiranno a definire ulteriormente qualsiasi potenziale rischio per la salute umana. Sulla base dei dati disponibili, il rischio per la salute derivante dall'esposizione a MMVF è sostanzialmente inferiore a quello che è stato associato all'esposizione all'amianto sia dal punto di vista della morbilità che della mortalità. La stragrande maggioranza degli studi sull'uomo, tuttavia, proviene da impianti di produzione di MMVF in cui i livelli di esposizione sono stati generalmente mantenuti al di sotto di un livello compreso tra 0.5 e 1 f/ml per una giornata lavorativa di otto ore. La mancanza di dati sulla morbilità e sulla mortalità degli utilizzatori secondari e finali di MMVF rende prudente controllare l'esposizione alla fibra respirabile a questi livelli o al di sotto attraverso misure di controllo ambientale, pratiche lavorative, formazione dei lavoratori e programmi di protezione respiratoria. Ciò è particolarmente applicabile con l'esposizione a ceramica refrattaria durevole e vetro MMVF per scopi speciali e qualsiasi altro tipo di fibra artificiale respirabile che sia durevole nei mezzi biologici e che possa quindi essere depositata e trattenuta nel parenchima polmonare.
Cancro respiratorio
Lung Cancer
Il cancro del polmone è il cancro più comune in tutto il mondo. Nel 1985, si stima che in tutto il mondo si siano verificati 676,500 casi nei maschi e 219,300 casi nelle femmine, pari all'11.8% di tutti i nuovi tumori, e questa cifra sta aumentando a un tasso di circa lo 0.5% all'anno (Parkin, Pisani e Ferlay 1993). . Circa il 60% di questi casi si verifica nei paesi industrializzati, in molti dei quali il cancro ai polmoni è la principale causa di morte per cancro tra i maschi. Sia nei paesi industrializzati che in quelli in via di sviluppo, i maschi hanno un'incidenza maggiore rispetto alle femmine, il rapporto tra i sessi va da due a dieci volte. Le variazioni intergender internazionali nell'incidenza del cancro del polmone sono in gran parte spiegate dalla variazione dei modelli di fumo attuali e passati.
Un più alto rischio di cancro al polmone è stato costantemente osservato nelle aree urbane rispetto alle zone rurali. Nei paesi industrializzati, una chiara relazione inversa è evidente nei maschi nell'incidenza del cancro del polmone e nella mortalità per classe sociale, mentre le donne mostrano modelli meno chiari e coerenti. Le differenze di classe sociale nei maschi riflettono principalmente un diverso modello di fumo. Nei paesi in via di sviluppo, tuttavia, sembra esserci un rischio maggiore negli uomini della classe sociale superiore rispetto agli altri uomini: questo modello riflette probabilmente la precedente adozione delle abitudini occidentali da parte dei gruppi benestanti della popolazione.
I dati di incidenza del programma SEER del National Cancer Institute degli Stati Uniti per il periodo 1980-86 indicano, analogamente agli anni precedenti, che i maschi neri hanno un'incidenza maggiore rispetto ai maschi bianchi, mentre l'incidenza per le femmine non differisce in base alla razza. Queste differenze tra i gruppi etnici negli Stati Uniti possono effettivamente essere attribuite a differenze socio-economiche tra neri e bianchi (Baquet et al. 1991).
L'incidenza del cancro al polmone aumenta quasi linearmente con l'età, se tracciata in una scala log-log; solo nelle fasce di età più anziane si può osservare una curva discendente. L'incidenza e la mortalità del cancro al polmone sono aumentate rapidamente durante questo secolo e continuano ad aumentare nella maggior parte dei paesi.
Esistono quattro principali tipi istologici di cancro del polmone: carcinoma a cellule squamose, adenocarcinoma, carcinoma a grandi cellule e carcinoma a piccole cellule (SCLC). I primi tre sono anche indicati come carcinoma polmonare non a piccole cellule (NSCLC). Le proporzioni di ciascun tipo istologico cambiano a seconda del sesso e dell'età.
Il carcinoma a cellule squamose è fortemente associato al fumo e rappresenta il tipo più comune di cancro ai polmoni in molte popolazioni. Sorge più frequentemente nei bronchi prossimali.
L'adenocarcinoma è meno fortemente associato al fumo. Questo tumore è di origine periferica e può presentarsi come un nodulo periferico solitario, una malattia multifocale o una forma polmonare rapidamente progressiva, che si diffonde da lobo a lobo.
Il carcinoma a grandi cellule rappresenta una percentuale minore di tutti i tumori polmonari e ha un comportamento simile all'adenocarcinoma.
SCLC rappresenta una piccola percentuale (dal 10 al 15%) di tutti i tumori polmonari; insorge tipicamente nella sede endobronchiale centrale e tende a sviluppare metastasi precoci.
I segni e i sintomi del cancro del polmone dipendono dalla localizzazione del tumore, dalla diffusione e dagli effetti della crescita metastatica. Molti pazienti presentano una lesione asintomatica scoperta casualmente alla radiografia. Tra i pazienti con NSCLC, sono comuni affaticamento, diminuzione dell'attività, tosse persistente, dispnea, diminuzione dell'appetito e perdita di peso. Il respiro sibilante o lo stridore possono anche svilupparsi in stadi avanzati. La crescita continua può causare atelectasia, polmonite e formazione di ascessi. I segni clinici tra i pazienti con SCLC sono meno pronunciati rispetto a quelli con NSCLC e sono generalmente correlati alla localizzazione endobronchiale.
Il cancro del polmone può metastatizzare praticamente in qualsiasi organo. Le sedi più comuni delle lesioni metastatiche sono la pleura, i linfonodi, le ossa, il cervello, le ghiandole surrenali, il pericardio e il fegato. Al momento della diagnosi, la maggior parte dei pazienti con carcinoma polmonare presenta metastasi.
La prognosi varia con lo stadio della malattia. La sopravvivenza complessiva a cinque anni per i malati di cancro al polmone in Europa (nel 1983-85) era compresa tra il 7% e il 9% (Berrino et al. 1995).
Nessun metodo di screening della popolazione è attualmente disponibile per il cancro del polmone.
Cancro nasofaringeo
Il cancro rinofaringeo è raro nella maggior parte delle popolazioni, ma è frequente in entrambi i sessi in aree come il sud-est asiatico, la Cina meridionale e il nord Africa. I migranti dalla Cina meridionale mantengono in larga misura il rischio elevato, ma i migranti cinesi di seconda e terza generazione negli Stati Uniti hanno meno della metà del rischio dei migranti di prima generazione.
I tumori del rinofaringe sono prevalentemente di origine epiteliale squamosa. Secondo l'OMS, questi tumori sono classificati come: tipo 1, carcinoma a cellule squamose cheratinizzanti; tipo 2, carcinoma non cheratinizzante; e il tipo 3, carcinoma indifferenziato, che è il tipo istologico più frequente. Il tipo 1 ha una crescita locale incontrollata e la diffusione metastatica si trova nel 60% dei pazienti. I tipi 2 e 3 hanno una diffusione metastatica nell'80-90% dei pazienti.
Una massa nel collo si nota in circa il 90% dei pazienti con carcinoma nasofaringeo. Si possono notare alterazioni dell'udito, otite media sierosa, tinnito, ostruzione nasale, dolore e sintomi legati alla crescita del tumore nelle strutture anatomiche adiacenti.
La sopravvivenza complessiva a cinque anni per i malati di cancro nasofaringeo in Europa tra il 1983 e il 1985 è stata di circa il 35%, variabile a seconda dello stadio del tumore e della sua localizzazione (Berrino et al. 1995).
Il consumo di pesce salato alla cinese è un fattore di rischio di cancro nasofaringeo; il ruolo di altri fattori nutrizionali e di virus, in particolare il virus di Epstein-Barr, sebbene sospetto, non è stato confermato. Non è noto che fattori professionali causino il cancro nasofaringeo. Attualmente non sono disponibili misure preventive (Higginson, Muir e Muñoz 1992).
Cancro sinusale
Le neoplasie del naso e delle cavità nasali sono relativamente rare. Insieme, il cancro del naso e del seno nasale, compresi i seni mascellari, etmoidali, sfenoidali e frontali, rappresentano meno dell'1% di tutti i tumori. Nella maggior parte dei casi questi tumori sono classificati come carcinomi squamosi. Nei paesi occidentali, i tumori del naso sono più comuni dei tumori del seno nasale (Higginson, Muir e Muñoz 1992).
Si verificano più frequentemente negli uomini e tra le popolazioni nere. L'incidenza più alta si registra in Kuwait, Martinica e India. Il picco di sviluppo della malattia si verifica durante la sesta decade di vita. La principale causa nota di cancro sinonasale è l'esposizione alla polvere di legno, in particolare da specie di legno duro. Il fumo di tabacco non sembra essere associato a questo tipo di cancro.
La maggior parte dei tumori della cavità nasale e del seno paranasale sono ben differenziati e a crescita lenta. I sintomi possono includere ulcera che non guarisce, sanguinamento, ostruzione nasale e sintomi correlati alla crescita nella cavità orale, nell'orbita e nella fossa pterigoidea. La malattia è generalmente avanzata al momento della diagnosi.
La sopravvivenza complessiva a cinque anni per i pazienti con cancro del naso e dei seni nasali in Europa tra il 1983 e il 1985 è stata di circa il 35%, variabile a seconda delle dimensioni della lesione alla diagnosi (Berrino et al. 1995).
Cancro alla laringe
La più alta incidenza di cancro della laringe è segnalata a San Paolo (Brasile), Navarra (Spagna) e Varese (Italia). Elevata mortalità è stata segnalata anche in Francia, Uruguay, Ungheria, Jugoslavia, Cuba, Medio Oriente e Nord Africa. Il cancro della laringe è prevalentemente un cancro maschile: si stima che nel 120,500 si siano verificati 20,700 casi tra i maschi e 1985 casi tra le femmine (Parkin, Pisani e Ferlay 1993). In generale, l'incidenza è maggiore tra le popolazioni nere rispetto ai bianchi e nelle aree urbane rispetto a quelle rurali.
Quasi tutti i tumori della laringe sono carcinomi squamosi. La maggior parte si trova nella glottide, ma possono svilupparsi anche nella sovraglottide o, raramente, nella sottoglottide.
I sintomi possono non verificarsi o essere molto sottili. Possono essere presenti dolore, sensazione di graffio, alterazione della tolleranza ai cibi caldi o freddi, tendenza ad aspirare liquidi, alterazione delle vie aeree, lieve alterazione della voce per diverse settimane e adenopatia cervicale, a seconda della sede e dello stadio della lesione.
La maggior parte dei tumori della laringe sono visibili con l'ispezione laringea o l'endoscopia. Lesioni pre-neoplastiche possono essere identificate nella laringe dei fumatori (Higginson, Muir e Muñoz 1992).
La sopravvivenza complessiva a cinque anni per i malati di cancro laringeo in Europa tra il 1983 e il 1985 era di circa il 55% (Berrino et al. 1995).
Mesotelioma pleurico
I mesoteliomi possono derivare dalla pleura, dal peritoneo e dal pericardio. Il mesotelioma maligno rappresenta il tumore pleurico più importante; si manifesta principalmente tra la quinta e la settima decade di vita.
Il mesotelioma pleurico era una volta un tumore raro e rimane tale nella maggior parte delle popolazioni femminili, mentre negli uomini nei paesi industrializzati è aumentato dal 5 al 10% all'anno negli ultimi decenni. In generale, gli uomini sono colpiti cinque volte tanto quanto le donne. Stime precise di incidenza e mortalità sono problematiche a causa delle difficoltà nella diagnosi istologica e dei cambiamenti nella Classificazione Internazionale delle Malattie (ICD) (Higginson, Muir e Muñoz 1992). Tuttavia, i tassi di incidenza sembrano presentare variazioni locali molto importanti: sono molto elevati nelle aree in cui è presente l'estrazione di amianto (ad esempio, la provincia del Capo nord-occidentale del Sud Africa), nelle principali città di cantieri navali e nelle regioni con contaminazione di fibre ambientali, come come alcune zone della Turchia centrale.
I pazienti possono essere asintomatici e avere la loro malattia diagnosticata incidentalmente sulle radiografie del torace, oppure possono avere dispnea e dolore toracico.
I mesoteliomi tendono ad essere invasivi. La sopravvivenza mediana è di 4-18 mesi in varie serie.
Fattori di rischio occupazionale del cancro respiratorio
Oltre al fumo di tabacco, secondo l'Agenzia internazionale per la ricerca sul cancro (IARC) è stata dimostrata un'associazione causale con il cancro respiratorio per 13 agenti o miscele e nove circostanze di esposizione (vedere tabella 1). Inoltre, ci sono otto agenti, miscele o circostanze di esposizione che secondo IARC sono probabilmente cancerogeni per uno o più organi delle vie respiratorie (tabella 2). Tutti tranne l'azatioprina, un farmaco immunosoppressore, sono principalmente esposizioni professionali (IARC 1971-94).
Tabella 1. Cancerogeni respiratori umani accertati secondo IARC
| Agenti Singoli agenti | Siti di destinazione |
| Amianto | Polmone, laringe, pleura |
| Arsenico e composti dell'arsenico | Polmone |
| Berillio e composti del berillio | Polmone |
| Bis (clorometil) etere | Polmone |
| Cadmio e composti di cadmio | Polmone |
| Clorometil metil etere (grado tecnico) | Polmone |
| Composti di cromo (VI). | Naso, polmone |
| Senape gas | Polmone, laringe |
| Composti di nichel | Naso, polmone |
| Talco contenente fibre asbestiformi | Polmone, pleura |
| Miscele complesse | |
| Catrami di carbone | Polmone |
| Piazzole di catrame di carbone | Polmone |
| Fuliggine | Polmone |
| Fumo di tabacco | Naso, polmone, laringe |
| Circostanze di esposizione | |
| Produzione di alluminio | Polmone |
| Fabbricazione e riparazione di stivali e scarpe | Naso |
| Gassificazione del carbone | Polmone |
| Produzione di coke | Polmone |
| Fondazioni siderurgiche | Polmone |
| Mobili ed ebanisteria | Naso |
| Forti nebbie di acidi inorganici contenenti acido solforico (esposizioni professionali a) | Laringe |
| Pittori (esposizione professionale come) | Polmone |
| Radon e suoi prodotti di decadimento | Polmone |
| Estrazione sotterranea di ematite (con esposizione al radon) | Polmone |
Fonte: IARC, 1971-1994.
Tabella 2. Probabili carcinogeni respiratori umani secondo IARC
| Agenti Singoli agenti | Siti bersaglio sospetti |
| acrilonitrile | Polmone |
| Azatioprina | Polmone |
| Formaldehyde | Naso, laringe |
| Silice (cristallina) | Polmone |
| Miscele complesse | |
| Scarico del motore diesel | Polmone |
| Fumi di saldatura | Polmone |
| Circostanze di esposizione | |
| Industria della gomma | Polmone |
| Spruzzatura e applicazione di insetticidi (esposizioni professionali in) | Polmone |
Fonte: IARC, 1971-1994.
I gruppi professionali che dimostrano un aumento del rischio di cancro ai polmoni in seguito all'esposizione a composti dell'arsenico includono lavoratori di fonderie di metalli non ferrosi, allevatori di pellicce, produttori di composti per salse di pecora e lavoratori del vigneto (IARC 1987).
Sono stati condotti numerosi studi epidemiologici sull'associazione tra i composti del cromo (VI) e l'insorgenza di cancro ai polmoni e al naso nelle industrie dei cromati, dei pigmenti cromati e della cromatura (IARC 1990a). La coerenza dei risultati e l'entità degli eccessi hanno dimostrato il potenziale cancerogeno dei composti del cromo (VI).
I lavoratori delle raffinerie di nichel di molti paesi hanno mostrato un aumento sostanziale dei rischi di tumori polmonari e nasali; altri gruppi professionali esposti al nichel tra i quali è stato rilevato un aumento del rischio di cancro ai polmoni includono minatori di minerale di nichel solfuro e lavoratori della produzione di leghe ad alto contenuto di nichel (IARC 1990b).
I lavoratori esposti al berillio sono a rischio elevato di cancro ai polmoni (IARC 1994a). I dati più informativi sono quelli derivati dal registro dei casi di berillio degli Stati Uniti, in cui sono stati raccolti casi di malattie polmonari correlate al berillio da diverse industrie.
Un aumento dell'insorgenza di cancro al polmone è stato riscontrato nelle coorti di fonderie di cadmio e lavoratori di batterie al nichel-cadmio (IARC 1994b). L'esposizione concomitante all'arsenico tra i fonditori e al nichel tra i lavoratori delle batterie non può spiegare un tale aumento.
L'amianto è un importante cancerogeno professionale. Il cancro del polmone e il mesotelioma sono le principali neoplasie correlate all'amianto, ma nei lavoratori dell'amianto sono stati segnalati tumori in altri siti, come il tratto gastrointestinale, la laringe e il rene. Tutte le forme di amianto sono state causalmente correlate al cancro del polmone e al mesotelioma. Inoltre, è stato dimostrato che le fibre asbestiformi contenenti talco sono cancerogene per il polmone umano (IARC 1987). Una caratteristica distintiva del cancro del polmone indotto dall'amianto è la sua relazione sinergica con il fumo di sigaretta.
Numerosi studi tra minatori, cavatori, fonditori, ceramisti, granitisti e tagliapietre hanno dimostrato che gli individui con diagnosi di silicosi dopo l'esposizione a polvere contenente silice cristallina hanno un aumentato rischio di cancro ai polmoni (IARC 1987).
Gli idrocarburi aromatici polinucleari (IPA) si formano principalmente a seguito di processi pirolitici, in particolare la combustione incompleta di materiali organici. Tuttavia, gli esseri umani sono esposti esclusivamente a miscele di IPA, come fuliggine, catrame di carbone e pece di catrame di carbone. Studi di coorte sulla mortalità tra gli spazzacamini hanno mostrato un aumento del rischio di cancro ai polmoni, che è stato attribuito all'esposizione alla fuliggine. Diversi studi epidemiologici hanno mostrato eccessi di cancro respiratorio tra i lavoratori esposti ai fumi di pece nella produzione di alluminio, nella produzione di carburo di calcio e nelle coperture. In queste industrie si verifica anche l'esposizione al catrame, e in particolare al catrame di carbone. Altre industrie in cui un eccesso di cancro respiratorio è dovuto all'esposizione ai fumi di catrame di carbone sono la gassificazione del carbone e la produzione di coke (IARC 1987). In alcuni è stato riscontrato un aumento del rischio di cancro respiratorio (principalmente ai polmoni), ma non tutti gli studi hanno cercato di analizzare l'esposizione ai gas di scarico dei motori diesel separatamente da altri prodotti di combustione; i gruppi professionali studiati includono ferrovieri, lavoratori portuali, addetti alle officine di autobus, impiegati di compagnie di autobus e autotrasportatori professionisti (IARC 1989a). Altre miscele di IPA che sono state studiate per la loro cancerogenicità per l'uomo includono nerofumo, gas di scarico dei motori a benzina, oli minerali, oli di scisto e bitumi. Gli oli di scisto e gli oli minerali non trattati e leggermente trattati sono cancerogeni per l'uomo, mentre i gas di scarico dei motori a benzina sono probabilmente cancerogeni e gli oli minerali altamente raffinati, i bitumi e il nerofumo non sono classificabili per quanto riguarda la loro cancerogenicità per l'uomo (IARC 1987, 1989a). Sebbene queste miscele contengano IPA, per nessuno di essi è stato dimostrato un effetto cancerogeno sul polmone umano e l'evidenza di cancerogenicità per gli oli minerali non trattati e leggermente trattati e per gli oli di scisto si basa sull'aumento del rischio di tumori da siti diversi organi respiratori (principalmente pelle e scroto) tra i lavoratori esposti.
Il bis(b-cloroetil)solfuro, noto come iprite, fu ampiamente utilizzato durante la prima guerra mondiale, e gli studi sui soldati esposti all'iprite e sugli operai impiegati nella sua fabbricazione hanno rivelato un successivo sviluppo di cancro ai polmoni e al naso (IARC 1987).
Numerosi studi epidemiologici hanno dimostrato che i lavoratori esposti a clorometil metil etere e/o bis(clorometil)-etere hanno un aumentato rischio di cancro ai polmoni, principalmente di SCLC (IARC 1987).
I lavoratori esposti all'acrilonitrile sono risultati a più alto rischio di cancro ai polmoni in alcuni ma non in tutti gli studi che sono stati condotti tra i lavoratori della produzione di fibre tessili, della polimerizzazione dell'acrilonitrile e dell'industria della gomma (IARC 1987).
È stato segnalato un eccesso di occorrenza per i lavoratori esposti alla formaldeide, compresi i lavoratori chimici, i lavoratori del legno, i produttori e gli utilizzatori di formaldeide (IARC 1987). L'evidenza è più forte per il cancro nasale e rinofaringeo: l'insorgenza di questi tumori ha mostrato un gradiente dose-risposta in più di uno studio, sebbene il numero di casi esposti fosse spesso ridotto. Altre neoplasie a possibile maggior rischio sono il cancro del polmone e del cervello e la leucemia.
Un aumento del rischio di cancro alla laringe è stato riscontrato in diversi studi su lavoratori esposti a nebbie e vapori di acidi solforici e altri acidi inorganici forti, come i lavoratori nelle operazioni di decapaggio dell'acciaio, nella produzione di saponi e nei lavoratori petrolchimici (IARC 1992). Anche il rischio di cancro al polmone è aumentato in alcuni, ma non in tutti, questi studi. Inoltre, un eccesso di cancro sinonasale è stato riscontrato in una coorte di lavoratori nella produzione di isopropanolo utilizzando il processo dell'acido forte.
I lavoratori del legno sono a maggior rischio di cancro nasale, in particolare adenocarcinoma (IARC 1987). Il rischio è confermato per mobili ed ebanisti; studi su lavoratori di falegnameria e falegnameria hanno suggerito un simile eccesso di rischio, ma alcuni studi hanno prodotto risultati negativi. Altre industrie del legno, come le segherie e la produzione di cellulosa e carta, non erano classificabili per quanto riguarda il loro rischio cancerogeno. Sebbene la cancerogenicità della polvere di legno non sia stata valutata dall'IARC, è plausibile ritenere che la polvere di legno sia responsabile di almeno una parte dell'aumento del rischio di adenocarcinoma nasale tra i lavoratori del legno. I falegnami non sembrano essere maggiormente a rischio di cancro in altri organi respiratori.
L'adenocarcinoma nasale è stato causato anche dall'impiego nella produzione e riparazione di stivali e calzature (IARC 1987). Non è invece disponibile alcuna chiara evidenza che i lavoratori impiegati nella fabbricazione di prodotti in pelle e nella concia e lavorazione delle pelli siano a maggior rischio di cancro respiratorio. Non è noto al momento se l'eccesso di adenocarcinoma nasale nell'industria degli stivali e delle calzature sia dovuto alla polvere di cuoio o ad altre esposizioni. La cancerogenicità della polvere di cuoio non è stata valutata dalla IARC.
Il cancro ai polmoni è stato comune tra i minatori di uranio, i minatori di ematite sotterranei e molti altri gruppi di minatori di metalli (IARC 1988; BEIR IV Committee on the Biological Effects of Ionizing Radiation 1988). Un fattore comune a ciascuno di questi gruppi professionali è l'esposizione alle radiazioni a emesse dalle particelle di radon inalate. La principale fonte di dati sul cancro in seguito all'esposizione a radiazioni ionizzanti deriva dal follow-up dei sopravvissuti alla bomba atomica (Preston et al. 1986; Shimizu et al. 1987). Il rischio di cancro ai polmoni è elevato tra i sopravvissuti alla bomba atomica così come tra le persone che hanno ricevuto radioterapia (Smith e Doll 1982). Nessuna prova convincente, tuttavia, è attualmente disponibile sull'esistenza di un elevato rischio di cancro al polmone tra i lavoratori esposti a radiazioni ionizzanti di basso livello, come quelle che si verificano nell'industria nucleare (Beral et al. 1987; BEIR V, Comitato sugli effetti biologici delle radiazioni ionizzanti 1990). La cancerogenicità delle radiazioni ionizzanti non è stata valutata dalla IARC.
Un rischio elevato di cancro ai polmoni tra i pittori è stato riscontrato in tre ampi studi di coorte e in otto piccoli studi di coorte e basati su censimenti, nonché in undici studi caso-controllo di vari paesi. D'altra parte, sono state trovate poche prove di un aumento del rischio di cancro ai polmoni tra i lavoratori coinvolti nella produzione di vernici (IARC 1989b).
Un certo numero di altre sostanze chimiche, miscele, occupazioni e industrie che sono state valutate dall'IARC come cancerogene per l'uomo (IARC Gruppo 1) non hanno il polmone come organo bersaglio primario. Tuttavia, la possibilità di un aumento del rischio di cancro ai polmoni è stata sollevata per alcune di queste sostanze chimiche, come il cloruro di vinile (IARC 1987), e occupazioni, come l'irrorazione e l'applicazione di insetticidi (IARC 1991a), ma l'evidenza non è coerente .
Inoltre, diversi agenti che hanno il polmone come uno dei bersagli principali, sono stati considerati possibili cancerogeni per l'uomo (IARC Gruppo 2B), sulla base dell'attività cancerogena negli animali da esperimento e/o di limitate prove epidemiologiche. Includono composti inorganici di piombo (IARC 1987), cobalto (IARC 1991b), fibre vetrose artificiali (lana di roccia, lana di scoria e lana di vetro) (IARC 1988b) e fumi di saldatura (IARC 1990c).
Infezioni professionali acquisite del polmone
Sebbene gli studi epidemiologici sulla polmonite acquisita sul lavoro (OAP) siano limitati, si ritiene che le infezioni polmonari correlate al lavoro stiano diminuendo in tutto il mondo. Al contrario, gli OAP nelle nazioni sviluppate potrebbero essere in aumento nelle occupazioni associate alla ricerca biomedica o all'assistenza sanitaria. L'OAP nei lavoratori ospedalieri riflette in gran parte i patogeni prevalenti acquisiti in comunità, ma la ricomparsa di tubercolosi, morbillo e pertosse nelle strutture sanitarie presenta un rischio aggiuntivo per le occupazioni basate sulla salute. Nelle nazioni in via di sviluppo e in specifiche occupazioni nelle nazioni sviluppate, agenti patogeni infettivi unici che non circolano comunemente nella comunità causano molti OAP.
Attribuire l'infezione all'esposizione professionale piuttosto che alla comunità può essere difficile, soprattutto per i lavoratori ospedalieri. In passato il rischio occupazionale era documentato con certezza solo nelle situazioni in cui i lavoratori erano contagiati da agenti avvenuti sul posto di lavoro ma non presenti nella comunità. In futuro, l'uso di tecniche molecolari per tracciare cloni microbici specifici attraverso il posto di lavoro e le comunità renderà più chiare le determinazioni del rischio.
Come la polmonite acquisita in comunità, l'OAP deriva dalla microaspirazione di batteri che colonizzano l'orofaringe, dall'inalazione di particelle infettive respirabili o dalla semina ematogena dei polmoni. La maggior parte delle polmoniti acquisite in comunità deriva dalla microaspirazione, ma l'OAP è solitamente dovuta all'inalazione di particelle aerodisperse infette da 0.5 a 10 μm sul posto di lavoro. Le particelle più grandi non riescono a raggiungere gli alveoli a causa dell'impatto o della sedimentazione sulle pareti delle grandi vie aeree e vengono successivamente eliminate. Le particelle più piccole rimangono sospese durante il flusso inspiratorio ed espiratorio e raramente si depositano negli alveoli. Per alcune malattie, come la febbre emorragica con sindrome renale associata a infezione da hantavirus, la principale modalità di trasmissione è l'inalazione, ma l'obiettivo principale della malattia potrebbe non essere i polmoni. Gli agenti patogeni acquisiti professionalmente che non vengono trasmessi per inalazione possono coinvolgere secondariamente i polmoni, ma non saranno discussi qui.
Questa recensione discute brevemente alcuni dei più importanti agenti patogeni acquisiti professionalmente. Un elenco più ampio di malattie polmonari acquisite professionalmente, classificate per eziologie specifiche, è presentato nella tabella 1.
Tabella 1. Malattie infettive acquisite sul lavoro contratte tramite microaspirazione o inalazione di particelle infettive
|
Malattia (agente patogeno) |
Serbatoio |
Popolazioni a rischio |
|
Batteri, clamidie, micoplasmi e rickettsie |
||
|
brucellosi (Brucelle spp.) |
Bestiame (bovini, caprini, suini) |
Addetti alle cure veterinarie, operai agricoli, addetti ai laboratori, addetti ai mattatoi |
|
Antrace da inalazione (Bacillus anthracis) |
Prodotti animali (lane, pelli) |
Lavoratori agricoli, conciatori, macellai, tessili, laboratoristi |
|
Peste polmonare (Yersinia pestis) |
Roditori selvatici |
Addetti alle cure veterinarie, cacciatori/trappers, addetti ai laboratori |
|
Pertosse (Bordatella pertosse) |
Gli esseri umani |
Dipendenti delle case di cura, operatori sanitari |
|
Legionellosi (Legionella spp.) |
Fonti di acqua contaminata (p. es., torri di raffreddamento, condensatori dell'evaporatore) |
Operatori sanitari, addetti ai laboratori, addetti ai laboratori industriali, escavatori per pozzi d'acqua |
|
Melioidosi (Pseudomonas pseudomallei) |
Suolo, acqua stagnante, risaie |
Personale militare, lavoratori agricoli |
|
Streptococcus pneumoniae |
Gli esseri umani |
Operatori sanitari, lavoratori agricoli, minatori sotterranei |
|
Neisseria meningitidis |
Gli esseri umani |
Operatori sanitari, addetti ai laboratori, personale militare |
|
Pasteurellosi (Pasteurella multocida) |
Varietà di animali domestici (gatti, cani) e selvatici |
Lavoratori agricoli, addetti alle cure veterinarie |
|
Tularemia respiratoria (Francisella tularensis) |
Roditori selvatici e conigli |
Operai manuali, militari, operai di laboratorio, cacciatori/trappers, lavoratori agricoli |
|
Ornitosi (Chlamydia psittaci) |
Uccelli |
Addetti ai negozi di animali, addetti alla produzione di pollame, addetti alle cure veterinarie, addetti ai laboratori |
|
polmonite TWAR (Chlamydia pneumoniae) |
Gli esseri umani |
Operatori sanitari, personale militare |
|
Febbre Q (Coxiella burnetii) |
Animali domestici (bovini, ovini, caprini) |
Lavoratori di laboratorio, operai tessili, addetti ai mattatoi, addetti alle bovine da latte, addetti alle cure veterinarie |
|
Polmonite atipica (Mycoplasma pneumoniae) |
Gli esseri umani |
Personale militare, operatori sanitari, operatori istituzionali |
|
Funghi/micobatteri |
||
|
istoplasmosi (Capsulatum Histoplasma) |
Suolo; escrementi di uccelli o pipistrelli (endemici del Nord America orientale) |
Lavoratori agricoli, operai di laboratorio, manovali |
|
Coccidioidomicosi (Coccidioides immitis) |
Suolo (endemico del Nord America occidentale) |
Militari, operai agricoli, operai, operai tessili, operai di laboratorio |
|
Blastomicosi (Blastomyces dermatitidis) |
Suolo (endemico del Nord America orientale) |
Laboratori, operai agricoli, operai, operai forestali |
|
Paracoccidioidomicosi (Paracoccidioides brasiliensis) |
Suolo (endemico in Venezuela, Colombia, Brasile) |
Lavoratori agricoli |
|
Sporotricosi (Sporotrix schenkii) |
Detriti vegetali, cortecce di alberi e piante da giardino |
Giardinieri, fioristi, minatori |
|
Tubercolosi (Mycobacterium tuberculosis, M. bovis, M. africanum) |
Primati umani e non umani, bovini |
Minatori di roccia dura, operai di fonderia, operatori sanitari e di laboratorio, addetti ai mattatoi, addetti alle cure veterinarie, personale militare, addetti alle taverne |
|
Micobatteriosi diverse dalla tubercolosi (Micobatterio spp..) |
Suolo |
Lavoratori esposti alla silice, comprese le sabbiatrici |
|
I virus |
||
|
hantavirus |
Roditore |
Lavoratori agricoli, pastori, addetti alla derattizzazione |
|
Morbillo |
Gli esseri umani |
Operatori sanitari e di laboratorio |
|
Rosolia |
Gli esseri umani |
Operatori sanitari e di laboratorio |
|
Influenza |
Gli esseri umani |
Operatori sanitari e di laboratorio |
|
Varicella zoster |
Gli esseri umani |
Operatori sanitari e di laboratorio, personale militare |
|
Virus respiratorio sinciziale |
Gli esseri umani |
Operatori sanitari e di laboratorio |
|
adenovirus |
Gli esseri umani |
Operatori sanitari e di laboratorio, personale militare |
|
virus parainfluenzale |
Gli esseri umani |
Operatori sanitari e di laboratorio |
|
Virus della coriomeningite linfocitaria (arenavirus) |
Roditore |
Lavoratori di laboratorio, addetti alle cure veterinarie |
|
Febbre di Lassa (arenavirus) |
Roditore |
Operatore sanitario |
|
Virus Marburg ed Ebola (filovirus) |
Primati umani e non umani, possibilmente pipistrelli |
Lavoratori di laboratorio, operatori veterinari, operatori sanitari, operai di cotonifici |
Infezioni acquisite sul lavoro nei lavoratori agricoli
Oltre ai gas e alle polveri organiche che colpiscono le vie respiratorie e imitano le malattie infettive, diverse malattie zoonotiche (patogeni comuni agli animali e all'uomo) e altre malattie infettive associate alla vita rurale colpiscono in modo univoco i lavoratori agricoli. Queste malattie vengono acquisite per inalazione di aerosol infettivi e raramente vengono trasmesse da una persona all'altra. Tali malattie che si verificano nei lavoratori agricoli includono antrace, brucellosi, febbre Q, ornitosi, tubercolosi e peste (tabella 1). I patogeni fungini includono istoplasmosi, blastomicosi, coccidioidomicosi, paracoccidioidomicosi e criptococcosi (tabella 1). Fatta eccezione per le malattie hantavirali, le malattie virali non sono una causa importante di malattie polmonari professionali nei lavoratori agricoli.
Si ritiene che alcune di queste infezioni siano più comuni, ma la loro incidenza è difficile da determinare perché: (1) la maggior parte delle infezioni è subclinica, (2) la malattia clinica è lieve o difficile da diagnosticare a causa di sintomi non specifici, (3) malattie mediche e i servizi diagnostici sono raramente disponibili per la maggior parte dei lavoratori agricoli, (4) non esiste un sistema organizzato per la segnalazione di molte di queste malattie e (5) molte di queste sono malattie rare nella comunità in generale e non sono riconosciute dal personale medico. Ad esempio, sebbene la nefrite epidemica dovuta al virus Puumala, un hantavirus, sia raramente segnalata nell'Europa occidentale, le indagini sierologiche sui lavoratori agricoli hanno mostrato una prevalenza dal 2 al 7% di anticorpi contro gli hantavirus.
Le infezioni zoonotiche nelle nazioni sviluppate stanno diminuendo grazie ai programmi attivi di controllo delle malattie diretti alle popolazioni animali. Nonostante questi controlli, i lavoratori agricoli e le persone che lavorano in settori correlati all'agricoltura (come veterinari, confezionatori di carne, addetti alla lavorazione del pollame e lavoratori di peli e pelli) rimangono a rischio di molte malattie.
Infezione da Hantavirus
Infezione da Hantavirus che causa febbre emorragica con sindrome renale (HFRS) o nefrite epidemica (EN) è stata clinicamente descritta tra i lavoratori agricoli, il personale militare e gli addetti ai laboratori nelle aree endemiche dell'Asia e dell'Europa per più di 50 anni. L'infezione deriva dall'inalazione di aerosol di urina, saliva e feci di roditori infetti. La malattia emorragica e la ridotta funzionalità renale si sviluppano durante la maggior parte delle malattie da hantavirus piuttosto che nella polmonite, ma è stato riportato edema polmonare dovuto all'aumentata permeabilità vascolare in HFRS e EN. Le profonde conseguenze polmonari delle infezioni da hantavirus non sono state pienamente apprezzate fino a un recente focolaio di sindrome polmonare da hantavirus (HPS) associata all'infezione con un hantavirus recentemente isolato negli Stati Uniti occidentali (virus Muerto Canyon, virus Four Corners o virus Sin Nombre).
Gli hantavirus sono membri del Bunyaviridae, una famiglia di virus a RNA. Cinque hantavirus sono stati associati a malattie umane. L'HFRS è stato associato al virus Hantaan nell'Asia orientale, al virus Dobrava nei Balcani e al virus Seoul, che ha una distribuzione mondiale. EN è stata associata al virus Puumala nell'Europa occidentale. L'HPS è stato associato a un hantavirus recentemente isolato negli Stati Uniti occidentali. Dal 1951 al 1983, nella Repubblica di Corea sono stati segnalati 12,000 casi di HFRS. Si dice che l'incidenza della malattia in Cina sia in aumento con le epidemie nei centri rurali e urbani e nel 1980, 30,500 casi con 2,000 decessi sono stati attribuiti all'HFRS.
Presentazione clinica
Con i virus che causano HFRS o EN, l'infezione di solito provoca lo sviluppo asintomatico di anticorpi anti-hantavirus. Nelle persone che si ammalano, i segni ei sintomi della fase iniziale non sono specifici e l'infezione da hantavirus può essere diagnosticata solo con test sierologici. Il recupero lento è comune, ma alcune persone progrediscono verso l'HFRS o la EN sviluppando proteinuria, ematuria microscopica, azotemia e oliguria. Le persone con HFRS sviluppano anche emorragie profonde dovute a coagulazione intravascolare disseminata, aumento della permeabilità vascolare e shock. La mortalità nelle persone con la sindrome HFRS completa varia dal 5 al 20%.
L'HPS è caratterizzata da diffusi infiltrati polmonari interstiziali e dall'improvvisa insorgenza di distress respiratorio acuto e shock. Una marcata leucocitosi può verificarsi come conseguenza dell'aumento delle citochine che caratterizzano le malattie da hantavirus. In HPS, la mortalità può essere superiore al 50%. L'incidenza di infezione asintomatica o di HPS non riconosciuta è studiata in modo incompleto.
Test diagnostici
La diagnosi viene effettuata dimostrando la presenza di immunoglobulina M o l'aumento del titolo di immunoglobulina G mediante immunofluorescenza indiretta altamente specifica e sensibile e test anticorpali neutralizzanti. Altri metodi diagnostici includono la reazione a catena della polimerasi per l'acido ribonucleico virale e l'immunoistochimica per l'antigene virale.
Epidemiologia
L'infezione deriva dall'inalazione di aerosol di urina, saliva e feci di roditori infetti. I roditori infetti non hanno alcuna malattia apparente. La trasmissione può avvenire per inoculazione percutanea di urina, saliva o feci di roditori infetti, ma non vi è evidenza di trasmissione interumana.
Indagini sieroepidemiologiche su esseri umani e roditori hanno dimostrato che gli hantavirus sono endemici con una distribuzione mondiale in ambienti rurali e urbani. Negli ambienti rurali endemici, le interazioni uomo-roditore aumentano quando i roditori invadono stagionalmente le case o l'attività umana aumenta nelle aree ad alta densità di roditori. Le persone nelle occupazioni rurali sono a maggior rischio di infezione. Nelle indagini sulle popolazioni rurali asintomatiche in Italia, dal 4 al 7% dei lavoratori forestali, ranger, agricoltori e cacciatori presentavano anticorpi anti-hantavirus, rispetto allo 0.7% dei soldati. Nei lavoratori agricoli asintomatici in Irlanda e Cecoslovacchia, la prevalenza dell'anticorpo anti-hantavirus era rispettivamente dell'1-2% e del 20-30%. La semina, la raccolta, la trebbiatura, la pastorizia e la silvicoltura sono fattori di rischio per l'infezione da virus. Sono in corso indagini sierologiche negli Stati Uniti occidentali per determinare il rischio professionale di infezione da hantavirus, ma in uno studio sugli operatori sanitari (operatori sanitari) che si prendono cura dei pazienti affetti da HPS, non sono state identificate infezioni. Dalle prime 68 persone con HPS, sembra che le attività agricole negli habitat di roditori infetti siano fattori di rischio per l'infezione. I pazienti avevano maggiori probabilità di arare a mano, pulire le aree di stoccaggio del cibo, piantare, pulire le stalle degli animali ed essere pastori. Il principale serbatoio di HPS è il topo cervo, Peromiscus maniculatus.
Altre professioni interessate
Negli ambienti urbani, il serbatoio dei roditori per il virus Seoul è il topo domestico. I lavoratori urbani, come i lavoratori portuali, i lavoratori delle strutture di stoccaggio del grano, i lavoratori degli zoo e gli addetti al controllo dei roditori possono essere a rischio di infezione da hantavirus. I laboratori di ricerca che utilizzano roditori per ricerche diverse dalla ricerca sugli hantavirus sono stati occasionalmente fonti insospettate di infezioni da hantavirus degli addetti ai laboratori. Altre professioni, come il personale militare e i biologi sul campo, sono a rischio di infezione da hantavirus.
Trattamento
Ribavirina ha dimostrato in vitro attività contro diversi hantavirus ed efficacia clinica contro l'infezione da virus Hantaan ed è stato utilizzato per il trattamento di persone con HPS.
Controlli di sanità pubblica
Nessun vaccino è disponibile per l'uso, sebbene siano in corso sforzi per sviluppare vaccini vivi e uccisi. Ridurre al minimo il contatto umano con i roditori e ridurre le popolazioni di roditori negli ambienti umani riduce il rischio di malattia. Nei laboratori di ricerca sugli hantavirus, le strutture di biosicurezza di alto livello limitano il rischio di propagazione del virus nelle colture cellulari o la manipolazione di materiali con alte concentrazioni di virus. In altri laboratori di ricerca che utilizzano roditori, può essere presa in considerazione la sorveglianza sierologica periodica per l'infezione da hantavirus delle colonie di roditori.
Coriomeningite linfocitica (LCM)
La LCM, come le infezioni da hantavirus, è naturalmente un'infezione di roditori selvatici che occasionalmente si diffonde all'uomo. Il virus LCM è un arenavirus, ma la trasmissione di solito avviene per aerosolizzazione. Gli ospiti naturali includono topi selvatici, ma l'infezione persistente dei criceti siriani domestici è ben documentata. L'infezione è, quindi, possibile nella maggior parte delle occupazioni che comportano l'aerosol di urina di roditore. Il più recente focolaio professionale documentato di questa malattia si è verificato nel personale di laboratorio esposto a topi nudi carenti di cellule T persistentemente infetti a seguito dell'inoculazione di linee cellulari tumorali contaminate.
Presentazione clinica
La maggior parte dei casi di LCM sono asintomatici o associati a malattie simil-influenzali aspecifiche e, pertanto, non sono riconosciuti. Sebbene il tratto respiratorio sia il sito di ingresso, i sintomi respiratori tendono ad essere aspecifici e autolimitanti. Meningite o meningoencefalite si sviluppa in una piccola percentuale di pazienti e può portare a una diagnosi specifica.
Test diagnostici
La diagnosi si basa solitamente sulla dimostrazione sierologica di un aumento del titolo del virus in presenza di segni clinici appropriati. Occasionalmente vengono utilizzati anche l'isolamento del virus e l'immunofluorescenza tissutale.
Epidemiologia
Circa il 20% dei topi selvatici è infetto da questo virus. La trasmissione transplacentare del virus nei roditori suscettibili porta alla tolleranza delle cellule T e topi (o criceti) con infezione congenita che rimangono costantemente infetti per tutta la vita. Allo stesso modo, i topi carenti di cellule T, come i topi nudi, possono essere infettati in modo persistente dal virus. Gli esseri umani sono infettati dalla trasmissione di aerosol. Inoltre, le linee cellulari di roditori possono essere contaminate e propagare il virus. Gli esseri umani di solito vengono infettati dagli aerosol, sebbene la trasmissione possa essere diretta o tramite insetti vettori.
Altre professioni interessate
Qualsiasi occupazione che comporti l'esposizione a polveri contaminate dagli escrementi di roditori selvatici conferisce il rischio di infezione da LCM. I custodi di animali nelle strutture per animali da laboratorio, i lavoratori nel settore dei negozi di animali e gli addetti ai laboratori che lavorano con linee cellulari di roditori possono essere infettati.
Trattamento
L'infezione da LCM è solitamente autolimitante. Nei casi più gravi può essere necessario un trattamento di supporto.
Controlli di sanità pubblica
Nessun vaccino è disponibile. Lo screening di topi, criceti e linee cellulari di ricerca ha limitato la maggior parte delle infezioni acquisite in laboratorio. Per i topi carenti di cellule T, i test sierologici richiedono l'uso di topi sentinella immunocompetenti. È appropriato l'uso delle normali precauzioni di sicurezza di laboratorio come guanti, protezione per gli occhi e camici da laboratorio. La riduzione del numero di roditori selvatici nell'ambiente umano è importante per il controllo di LCM, hantavirus e peste.
Clamidiosi respiratoria
Clamidiosi respiratoria dovuta a Chlamydia psittaci è la causa più frequentemente segnalata di OAP associata alla macellazione di animali (pollame) e alla lavorazione della carne. La clamidiosi e altre malattie sono spesso associate all'esposizione ad animali malati, che possono essere l'unico indizio sulla fonte e sul tipo di infezione. La lavorazione di animali infetti crea aerosol che infettano le persone lontane dalla lavorazione della carne e lavorare vicino agli impianti di lavorazione della carne può essere un indizio del tipo di infezione. La clamidiosi respiratoria può essere associata all'esposizione a pappagalli (psittacosi) o uccelli non psittacidi (ornitosi). Fonti non aviarie di Chlamydia psittaci di solito non sono considerate potenziali zoonosi, sebbene siano stati segnalati aborto spontaneo e congiuntivite negli esseri umani esposti a ceppi ovini e caprini. Polmonite dovuta a C.pneumoniae è una causa comune recentemente descritta di polmonite acquisita in comunità distinta da C. psittacci infezioni. A causa della sua recente scoperta, il ruolo di C.pneumoniae negli OAP è indagato in modo incompleto e non sarà ulteriormente discusso in questa recensione.
Presentazione clinica
L'ornitosi varia da una lieve malattia simil-influenzale a una grave polmonite con encefalite che, nell'era preantibiotica, aveva un tasso di mortalità per caso (CFR) superiore al 20%. Febbre prodromica, brividi, mialgia, mal di testa e tosse non produttiva possono durare fino a tre settimane prima della diagnosi di polmonite. Sono comuni alterazioni neurologiche, epatiche e renali. I reperti radiografici comprendono il consolidamento del lobo inferiore con linfoadenopatia ilare. Il sospetto clinico dopo aver determinato l'esposizione al lavoro o altre esposizioni agli uccelli è cruciale per la diagnosi perché non ci sono risultati patognomonici.
Test diagnostici
L'ornitosi di solito determina un titolo elevato di anticorpi di fissazione del complemento (CF), sebbene un trattamento precoce con tetracicline possa sopprimere la formazione di anticorpi. Per formulare la diagnosi può essere utilizzata una singola diluizione del titolo sierico acuto ³1:16 dell'anticorpo CF con una presentazione clinica compatibile o una variazione quadrupla del titolo anticorpale CF. I campioni di siero accoppiati in modo inappropriato e l'elevato livello di anticorpi contro la clamidia nei gruppi a rischio minano l'utilità dei test anticorpali per diagnosticare la maggior parte delle malattie da clamidia.
Epidemiologia
C. psittacci è presente praticamente in tutte le specie aviarie ed è comune nei mammiferi. L'infezione di solito deriva dalla trasmissione zoonotica, ma è stata segnalata la trasmissione da persona a persona. L'infezione asintomatica è comune e fino all'11% dei lavoratori agricoli senza una storia di malattia ha anticorpi contro C. psittacci. Focolai limitati rimangono intermittenti, ma le pandemie associate al commercio di uccelli esotici si sono verificate più di recente nel 1930. Negli Stati Uniti, ogni anno vengono segnalati da 70 a 100 casi di ornitosi e quasi un terzo di queste malattie sono acquisite sul lavoro. La maggior parte delle infezioni acquisite sul lavoro si verificano nei lavoratori delle industrie di lavorazione degli uccelli da compagnia o del pollame e sono correlate all'aerosol di tessuto o feci aviari. Nei paesi in cui gli uccelli sono comunemente tenuti come animali domestici e le quarantene per l'importazione sono scarsamente applicate, i focolai sono più comuni ma l'occupazione è meno un fattore di rischio.
Altre professioni interessate
La malattia si verifica più frequentemente nei lavoratori della lavorazione del pollame, ma sono a rischio i lavoratori nelle strutture di distribuzione di uccelli esotici e di quarantena degli uccelli, nelle voliere di allevamento e nelle cliniche veterinarie.
Trattamento
La tetraciclina o l'eritromicina per 10-14 giorni dovrebbero essere un trattamento adeguato, ma la recidiva clinica è comune quando il trattamento viene somministrato per una durata inadeguata.
Controlli di sanità pubblica
Negli Stati Uniti gli uccelli esotici vengono messi in quarantena per la chemioprofilassi con le tetracicline. Metodi simili sono usati in altri paesi dove esiste un commercio di uccelli esotici. Nessun vaccino è stato sviluppato per l'ornitosi. Sono stati istituiti programmi per aumentare la ventilazione per diluire la concentrazione di aerosol, ridurre l'aerosol o l'inalazione di particelle infettive o curare uccelli malati negli impianti di trasformazione commerciale, ma la loro efficacia non è stata dimostrata.
brucellosi
Ogni anno si verificano circa 500,000 casi di brucellosi in tutto il mondo, causati da diverse specie di Brucella. La patogenicità della Brucella dipende dalle specie infettanti, che tendono ad avere diversi ospiti serbatoio. I serbatoi per Brucella abortus, B. suis, B. melitensis, B. ovis, B. canis, ed B. neotomæ tendono ad essere rispettivamente bovini, suini, capre, pecore, cani e ratti.
La brucellosi può derivare dall'infezione per vie diverse, inclusa l'aerosol. Tuttavia, la maggior parte delle malattie deriva dall'ingestione di latticini non pastorizzati di capre. La conseguente malattia sistemica è causata da B. melitensis ma non associato a occupazioni specifiche. La polmonite si verifica nell'1% dei casi, sebbene la tosse sia un reperto frequente.
Nei paesi sviluppati, la brucellosi professionale è solitamente causata da Brucella aborto e risulta dall'ingestione o dall'inalazione di aerosol infettivi associati alla placenta di suini e bovini. L'infezione subclinica è comune; fino all'1% dei lavoratori agricoli ha anticorpi contro B. aborto. La malattia si sviluppa in circa il 10% delle persone infette. A differenza della malattia dovuta a B. melitensis, malattia associata a B. aborto di solito è acquisita professionalmente ed è meno grave. Le persone con brucellosi acuta sviluppano febbri giornaliere elevate, artralgia ed epatosplenomegalia. Nella polmonite brucellare primaria, il consolidamento polmonare è in realtà raro e i reperti polmonari possono includere raucedine o respiro sibilante, adenopatia ilare, infiltrati peribronchiali, noduli parenchimali o un pattern miliare. L'isolamento può essere effettuato dal midollo osseo nel 90% dei casi acuti e dal sangue nel 50-80% dei casi. La diagnosi può essere fatta sierologicamente con una varietà di test anticorpali. Le tetracicline dovrebbero essere utilizzate per XNUMX-XNUMX settimane e la rifampicina può essere aggiunta per la sinergia. Allevatori di bovini, caprini, ovini e suini, lavoratori lattiero-caseari, addetti ai macelli, veterinari e macellai sono le principali popolazioni a rischio. I programmi di test e di eradicazione della brucella hanno notevolmente ridotto il numero di animali infetti e hanno identificato gli allevamenti che presentano il maggior rischio di trasmissione della malattia. Quando si lavora con animali infetti da Brucella, l'evitamento o la protezione personale, soprattutto dopo l'aborto o il parto, sono gli unici metodi efficaci di controllo della malattia.
Antrace da inalazione
L'antrace da inalazione si verifica in tutto il mondo ma è meno comune dell'antrace cutaneo. L'antrace è una malattia sistemica in molti animali e di solito viene trasmessa all'uomo per infezione percutanea dalla lavorazione o dal consumo di carne contaminata. L'antrace da inalazione è causato dall'inalazione di spore di Bacillus anthracis dall'osso, dal pelo o dalla pelle di pecore, capre o bovini ("malattia del selezionatore di lana") o raramente durante la lavorazione di carne infetta. Le spore subiscono la fagocitosi da parte dei macrofagi alveolari e vengono trasportate ai linfonodi mediastinici, dove germinano. Ciò si traduce in una mediastinite emorragica ma raramente si presenta come polmonite primaria. La malattia è caratterizzata da mediastino allargato, edema polmonare, versamenti pleurici, splenomegalia e rapida progressione verso l'insufficienza respiratoria. Il tasso di mortalità è del 50% o superiore nonostante gli antibiotici e il supporto ventilatorio. Le emocolture positive sono comuni, ma possono essere utilizzati test sierologici che utilizzano un immunodosaggio per blotting. Le persone malate sono trattate con penicillina ad alto dosaggio o ciprofloxacina per via endovenosa come alternativa nelle persone allergiche alla penicillina. Gli allevatori di animali, i veterinari, gli addetti alle cure veterinarie, i trasformatori di peli e pelli e i lavoratori dei macelli sono maggiormente a rischio. La vaccinazione annuale è disponibile per gli animali nelle aree endemiche e per gli esseri umani ad alto rischio di malattia. Le misure di controllo specifiche contro l'antrace da inalazione comprendono la decontaminazione con formaldeide, la sterilizzazione a vapore o l'irradiazione di peli e pelli; proibire l'importazione di pelli dalle aree endemiche; e protezione respiratoria personale per i lavoratori.
Peste polmonare
Peste, causata da Yersinia pestis, è prevalentemente una malattia enzootica trasmessa dalle pulci nei roditori selvatici. Gli esseri umani di solito si infettano quando vengono morsi da una pulce infetta e spesso sviluppano setticemia. Negli Stati Uniti dal 1970 al 1988, la polmonite secondaria da diffusione ematogena si è sviluppata in circa il 10% delle persone setticemiche. Gli animali e gli esseri umani con peste polmonare producono aerosol infettivi. La polmonite primaria negli esseri umani può verificarsi per inalazione di un aerosol infettivo creato attorno ad animali morenti con polmonite secondaria. Nonostante il potenziale di diffusione polmonare, la trasmissione da persona a persona è rara e non si verifica negli Stati Uniti da quasi 50 anni. I controlli delle malattie includono l'isolamento delle persone affette da peste polmonare e l'uso di protezioni respiratorie personali da parte del personale sanitario. La trasmissione per aerosol agli operatori ospedalieri è possibile e la profilassi con tetracicline dovrebbe essere presa in considerazione per chiunque entri in contatto con esseri umani o animali con peste polmonare. Numerose professioni sono a rischio di trasmissione di aerosol, compresi gli addetti ai laboratori biomedici e ospedalieri e, nelle aree endemiche, numerose occupazioni rurali, tra cui veterinari, addetti al controllo dei roditori, cacciatori/trapper, mammologi, biologi della fauna selvatica e lavoratori agricoli. Un vaccino ucciso è raccomandato per le persone con occupazioni ad alto rischio.
Febbre Q
Causato dall'inalazione di Coxiella burnetiiLa febbre Q è una malattia sistemica che si presenta come polmonite atipica nel 10-60% delle persone infette. Molti diversi isolati di C. burnetii producono malattie e le teorie sulla virulenza plasmide-dipendente sono controverse. C. burnetii infetta molti animali domestici (p. es., pecore, bovini, capre, gatti) in tutto il mondo; è aerosolizzato da urina, feci, latte, placenta o tessuti uterini; forma un'endospora altamente resistente che rimane infettiva per anni; ed è estremamente contagioso.
Presentazione clinica
Dopo un periodo di incubazione da 4 a 40 giorni, la febbre Q acuta si presenta come una malattia simil-influenzale che progredisce in una polmonite atipica simile a Mycoplasma. La malattia acuta dura circa due settimane ma può persistere fino a nove settimane. Malattie croniche, prevalentemente un'endocardite e un'epatite, possono svilupparsi fino a 20 anni dopo la malattia acuta.
Test diagnostici
Isolamento primario di C. burnetii viene eseguito raramente perché richiede un alto livello di contenimento della biosicurezza. La diagnosi viene fatta sierologicamente dimostrando un titolo anticorpale CF di 1:8 o superiore in un contesto clinico appropriato o un cambiamento di quattro volte nel titolo CF.
Altre professioni interessate
I lavoratori agricoli (soprattutto lattiero-caseari e della lana), i laboratori ospedalieri e la ricerca biomedica sono a rischio di infezione.
Trattamento
Non esiste un vaccino efficace per C. burnetii. Un ciclo di due settimane di tetracicline o ciprofloxacina viene utilizzato per trattare la malattia acuta.
Controlli di sanità pubblica
A causa della sua ampia distribuzione geografica, dei numerosi serbatoi animali e della resistenza all'inattivazione, la protezione respiratoria personale e i controlli tecnici per contenere gli aerosol infettivi sono le uniche misure preventive efficaci. Tuttavia, questi metodi di controllo sono difficili da implementare in molti contesti agricoli (ad esempio, allevamento di ovini e bovini). La diagnosi precoce della febbre Q da parte del personale medico può essere facilitata dall'educazione dei lavoratori ad alto rischio di contrarre questa malattia rara. Può verificarsi la trasmissione al personale ospedaliero e l'isolamento può limitare la diffusione della polmonite da febbre Q negli ospedali.
Varie OAPS batteriche dei lavoratori agricoli
Pseudomonas pseudomallei è un organismo associato al suolo e ai roditori principalmente del sud-est asiatico che causa la melioidosi. La malattia è associata all'esposizione al suolo ea una latenza potenzialmente lunga. Il personale militare durante e dopo la guerra del Vietnam è stato le principali vittime della melioidosi negli Stati Uniti. La polmonite multifocale, nodulare, suppurativa o granulomatosa caratterizza la forma polmonare della melioidosi.
Francisella tularensis, l'agente eziologico della tularemia, è una zoonosi associata a roditori selvatici e lagomorfi. Questa è una potenziale malattia professionale di biologi della fauna selvatica, mammologi, addetti al controllo dei roditori, cacciatori, cacciatori e veterinari. La tularemia può derivare da inalazione, inoculazione diretta, contatto cutaneo o ingestione, oppure può essere trasmessa da vettori. La malattia polmonare deriva dall'esposizione diretta per inalazione o dalla diffusione ematogena della malattia setticemica. Le lesioni polmonari della tularemia sono acute, multifocali, suppurative e necrotizzanti.
Istoplasmosi
Istoplasmosi è causato da Capsulatum Histoplasma, una muffa vivente nel terreno associata alle feci di uccelli o pipistrelli. L'istoplasmosi è la causa più importante di OAP fungine nei lavoratori agricoli. Le varie polmoniti fungine dei lavoratori agricoli sono descritte nella sezione successiva.
Presentazione clinica
Dopo l'esposizione, i tassi di attacco e la gravità dell'istoplasmosi variano a causa dell'inoculo infettante e dei livelli anticorpali dell'ospite conferiti dall'infezione precedente. A seguito di una forte esposizione, fino al 50% delle persone sviluppa malattie respiratorie autolimitanti, mentre altre rimangono asintomatiche. La meno grave delle sindromi sintomatiche include sintomi "simil-influenzali", tosse non produttiva e dolore toracico. L'esame obiettivo può essere notevole per l'eritema nodoso o l'eritema multiforme. Le radiografie del torace mostrano infiltrati irregolari e segmentali, ma nessun riscontro radiografico può differenziare in modo specifico l'istoplasmosi da altre infezioni polmonari. La linfoadenopatia ilare o mediastinica è comune in tutti gli stadi dell'istoplasmosi primaria.
L'istoplasmosi polmonare primaria progressiva è caratterizzata da profondi disturbi sistemici, tosse con espettorato purulento ed emottisi. I cambiamenti radiografici progressivi includono noduli multipli, consolidamento lobare e infiltrati interstiziali densi e multilobari. Esposizioni maggiori aumentano la gravità della malattia e provocano una grave malattia respiratoria, la sindrome da distress respiratorio acuto (ARDS) o l'atelettasia dovuta all'ostruzione da parte della linfoadenopatia mediastinica.
Circa il 20% dei malati sviluppa altre sindromi istoplasmosiche sono idiosincratiche e non il risultato di una maggiore esposizione o progressione della malattia primaria. Le sindromi comprendono l'artrite-eritema nodoso, la pericardite e l'istoplasmosi polmonare cronica (infiltrati polmonari apicali fibrotici con cavitazione). L'istoplasmosi disseminata si sviluppa in una piccola percentuale di pazienti, in particolare gli immunodepressi.
Test diagnostici
La diagnosi definitiva viene effettuata isolando o dimostrando istopatologicamente l'organismo in un campione clinico appropriato. Sfortunatamente, l'organismo è presente in basse concentrazioni e la sensibilità di questi metodi è bassa. Le diagnosi presunte sono spesso fatte sulla base della posizione geografica, della storia dell'esposizione e dei reperti radiografici dei polmoni o delle calcificazioni nella milza.
Epidemiologia
H. capsulato si trova in tutto il mondo associato a specifiche condizioni del suolo, ma la malattia è segnalata principalmente dalle valli del fiume Ohio e Mississippi degli Stati Uniti. Elevate concentrazioni di spore si trovano nei posatoi degli uccelli, nei vecchi edifici, nei pollai, nelle grotte o nei cortili delle scuole; sono interrotti dall'attività lavorativa. La concentrazione di microconidi è maggiore nelle aree chiuse e disgregate (p. es., demolizione di edifici) e determina un inoculo più elevato per i lavoratori rispetto alla maggior parte dei siti all'aperto. Nelle aree endemiche, le persone che puliscono i posatoi degli uccelli, demoliscono vecchi edifici contaminati o eseguono scavi per la costruzione di strade o edifici corrono un rischio maggiore rispetto alla popolazione generale. Negli Stati Uniti, da 15,000 a 20,000 persone vengono ricoverate ogni anno con istoplasmosi e circa il 3% di loro muore.
Altre professioni interessate
Attribuzione del rischio professionale per Histoplasm l'infezione è difficile perché l'organismo vive libero nel suolo e la concentrazione di spore aerosolizzate è aumentata dal vento e dalle condizioni polverose. L'infezione è principalmente dovuta alla posizione geografica. Nelle aree endemiche, le persone rurali, indipendentemente dall'occupazione, hanno una prevalenza dal 60 all'80% di test cutanei positivi per H. capsulato antigeni. La malattia effettiva deriva da un grande inoculo infettante e di solito è limitata ai lavoratori coinvolti nella distruzione del suolo o nella distruzione di edifici contaminati.
Trattamento
Il trattamento antimicotico per l'istoplasmosi e altre infezioni fungine acquisite professionalmente non è indicato per la malattia polmonare acuta autolimitante. La terapia con amfotericina B (dose totale da 30 a 35 mg/kg) o ketoconazolo (400 mg/die per sei mesi) o regimi di trattamento che utilizzano entrambi gli agenti è indicata per istoplasmosi disseminata, istoplasmosi polmonare cronica, istoplasmosi polmonare acuta con ARDS o granuloma mediastinico con ostruzione sintomatica e può essere utile per una malattia primaria prolungata e moderatamente grave. Il trattamento determina un tasso di risposta dell'80-100%, ma le ricadute sono comuni e possono raggiungere il 20% con l'amfotericina B e il 50% con il ketoconazolo. L'efficacia dei nuovi farmaci azolici (ossia, itraconazolo e fluconazolo) per le infezioni fungine occupazionali non è stata definita.
Controlli di sanità pubblica
Non è stato sviluppato alcun vaccino efficace. La decontaminazione chimica con formaldeide al 3%, la pre-bagnatura del terreno o delle superfici contaminate per ridurre l'aerosol e la protezione respiratoria personale per ridurre l'inalazione di spore aerosol possono ridurre l'infezione, ma l'efficacia di questi metodi non è stata determinata.
Varie polmoniti fungine
Le varie polmoniti fungine dei lavoratori agricoli includono aspergillosi, blastomicosi, criptococcosi, coccidioidomicosi e paracoccidioidomicosi (tabella 1). Queste malattie sono causate da Aspergillus spp., Blastomyces dermatitidis, Cryptococcus neoformans, Coccidioides immitis ed Paracoccidioides brasiliensis, rispettivamente. Sebbene questi funghi abbiano un'ampia distribuzione geografica, la malattia viene solitamente segnalata da aree endemiche. Rispetto alle cause virali e batteriche di polmonite, questi disturbi sono rari e spesso inizialmente non sospettati. I disordini delle cellule T aumentano la suscettibilità all'istoplasmosi, alla blastomicosi, alla criptococcosi, alla coccidioidomicosi e alla paracoccidioidomicosi. Tuttavia, una grande esposizione iniziale può causare malattie nel lavoratore immunocompetente. Infezioni da Aspergillus e funghi correlati tendono a manifestarsi nei pazienti neutropenici. L'aspergillosi è più frequentemente un OAP degli immunodepressi e sarà discussa nella sezione sulle infezioni negli immunodepressi.
Cr. neoformans, piace H. capsulato, è un comune abitante del suolo contaminato da feci aviarie e l'esposizione professionale a tali polveri o altre polveri contaminate da Cr. neoformans può provocare malattie. La blastomicosi professionale è associata a occupazioni esterne, specialmente negli Stati Uniti orientali e centrali. La coccidioidomicosi deriva dall'esposizione a polveri contaminate nelle aree endemiche degli Stati Uniti sudoccidentali (da cui il sinonimo febbre della valle di San Joaquin). L'esposizione professionale a suoli contaminati dell'America meridionale e centrale è spesso associata alla paracoccidioidomicosi. A causa della latenza potenzialmente lunga della paracoccidioidomicosi, questa esposizione può precedere di molto la comparsa dei sintomi.
Presentazione clinica
La presentazione clinica di coccidioidomicosi, blastomicosi o paracoccidioidomicosi è simile all'istoplasmosi. L'esposizione all'aerosol a questi funghi può produrre OAP se l'inoculo iniziale è sufficientemente alto. Tuttavia, i fattori dell'ospite, come l'esposizione precedente, limitano la malattia nella maggior parte degli individui. Nella coccidioidomicosi, i segni polmonari e sistemici della malattia sono evidenti in una piccola percentuale di persone infette; la malattia progressiva con disseminazione a più organi è rara in assenza di immunosoppressione. Sebbene la fonte dell'infezione sia solitamente il polmone, la blastomicosi può presentarsi come malattia polmonare, malattia cutanea o malattia sistemica. La presentazione clinica più comune della blastomicosi è una tosse cronica con polmonite indistinguibile dalla tubercolosi. Tuttavia, la maggior parte dei pazienti con blastomicosi clinicamente evidente presenterà lesioni extrapolmonari che coinvolgono la pelle, le ossa o il sistema genito-urinario. La paracoccidioidomicosi è una malattia del Messico, Centro e Sud America che si presenta più frequentemente come riattivazione di una precedente infezione dopo un lungo ma variabile periodo di latenza. La malattia può essere associata all'invecchiamento degli individui infetti e la riattivazione può essere indotta dall'immunosoppressione. La presentazione polmonare è simile ad altre polmoniti fungine, ma la malattia extrapolmonare, in particolare delle membrane mucose, è comune nella paracoccidioidomicosi.
Il polmone è il sito abituale per l'infezione primaria con Criptococco neoformans. Come per i funghi discussi in precedenza, le infezioni polmonari possono essere asintomatiche, autolimitanti o progressive. Tuttavia, la disseminazione del microrganismo, in particolare alle meningi e al cervello, può avvenire senza malattia respiratoria sintomatica. La meningoencefalite criptococcica senza evidenza di criptococcosi polmonare, sebbene rara, è la manifestazione clinica più comune di Cr. neoformans infezione.
Test diagnostici
La dimostrazione diretta della forma tissutale dell'organismo consente una diagnosi definitiva nelle biopsie e nei preparati citologici. L'immunofluorescenza può essere un'utile procedura di conferma se i dettagli morfologici sono insufficienti per stabilire l'agente eziologico. Questi microrganismi possono anche essere coltivati da lesioni sospette. Un test positivo per l'agglutinina criptococcica al lattice nel liquido cerebrospinale è coerente con la meningoencefalite criptococcica. Tuttavia, la dimostrazione dei microrganismi potrebbe non essere sufficiente per la diagnosi della malattia. Ad esempio, la crescita saprofitica di cr. neoformans è possibile nelle vie aeree.
Altre professioni interessate
I lavoratori di laboratorio che isolano questi funghi sono a rischio di infezione.
Trattamento
La terapia antimicotica è simile a quella per l'istoplasmosi.
Controlli di sanità pubblica
I controlli tecnici sono indicati per ridurre il rischio per gli operatori di laboratorio. La protezione delle vie respiratorie quando si lavora con suoli fortemente contaminati da feci aviarie ridurrà l'esposizione a Cr. neoformans.
Infezioni acquisite sul lavoro negli operatori sanitari e di laboratorio
L'inalazione di aerosol infetti è la fonte più comune di infezione nei lavoratori ospedalieri e molti tipi di polmonite virale e batterica sono stati attribuiti alla trasmissione correlata al lavoro (Tabella 26). La maggior parte delle infezioni è virale e autolimitante. Tuttavia, nel personale ospedaliero sono stati segnalati focolai potenzialmente gravi di tubercolosi, morbillo, pertosse e polmonite pneumococcica. Le infezioni nei lavoratori immunocompromessi sono discusse alla fine di questa sezione.
I lavoratori dei laboratori diagnostici sono a rischio di infezioni acquisite sul lavoro derivanti dalla trasmissione per via aerea. La trasmissione si verifica quando gli agenti patogeni vengono aerosolizzati durante l'elaborazione iniziale di campioni clinici da pazienti con malattie infettive incerte ed è raramente riconosciuta. Ad esempio, in un recente focolaio comunitario di brucellosi, un terzo dei tecnici di laboratorio ha sviluppato la brucellosi. L'impiego in laboratorio è stato l'unico fattore di rischio identificato. Non è stato possibile dimostrare che la trasmissione da persona a persona tra dipendenti di laboratorio, la trasmissione per via alimentare o idrica o il contatto con un particolare campione clinico sono fattori di rischio. Rosolia, tubercolosi, varicella-zoster e virus respiratorio sinciziale sono malattie professionali parimenti acquisite in laboratorio dai tecnici.
Nonostante le rigorose cure veterinarie, le procedure di contenimento della biosicurezza e l'uso di animali da laboratorio allevati commercialmente e privi di agenti patogeni, l'inalazione rimane la principale modalità di trasmissione di malattie infettive associata ai ricercatori biomedici. Inoltre, è possibile incontrare microrganismi scoperti di recente o serbatoi zoonotici precedentemente non riconosciuti che compromettono queste strategie di controllo delle malattie.
Morbillo
Morbillo, come malattia professionale acquisita, è diventato un problema crescente tra i lavoratori ospedalieri nei paesi sviluppati. Dal 1989, c'è stata una recrudescenza del morbillo negli Stati Uniti a causa della scarsa osservanza delle raccomandazioni sui vaccini e del fallimento dell'immunizzazione primaria nei destinatari del vaccino. A causa dell'elevata morbilità e mortalità potenziale associata al morbillo nei lavoratori suscettibili, si dovrebbe prestare particolare attenzione al morbillo in qualsiasi programma di salute sul lavoro. Dal 1985 al 1989, negli Stati Uniti sono stati segnalati più di 350 casi di morbillo acquisito professionalmente, che rappresentano l'1% di tutti i casi segnalati. Quasi il 30% dei lavoratori ospedalieri con morbillo acquisito professionalmente è stato ricoverato. I gruppi più numerosi di lavoratori ospedalieri con morbillo erano infermieri e medici e il 90% di loro ha contratto il morbillo dai pazienti. Sebbene il 50% di questi malati fosse idoneo alla vaccinazione, nessuno era stato vaccinato. L'aumento della morbilità e mortalità del morbillo negli adulti ha aumentato la preoccupazione che i lavoratori infetti possano infettare pazienti e colleghi.
Nel 1989, il comitato consultivo per le pratiche di immunizzazione ha raccomandato due dosi di vaccino contro il morbillo o prove di immunità al morbillo al momento dell'impiego in un ambiente sanitario. Lo stato sierologico e vaccinale dei lavoratori dovrebbe essere documentato. Inoltre, quando sono presenti pazienti con morbillo, è appropriata una rivalutazione dello stato immunitario del personale sanitario. L'attuazione di queste raccomandazioni e l'isolamento appropriato dei pazienti con morbillo noto e sospetto riduce la trasmissione del morbillo in ambito medico.
Presentazione clinica
Oltre alla presentazione comune del morbillo osservata negli adulti non immuni, devono essere prese in considerazione le presentazioni atipiche e modificate del morbillo perché molti operatori ospedalieri avevano precedentemente ricevuto vaccini uccisi o avevano un'immunità parziale. Nel morbillo classico, un periodo di incubazione di due settimane con lievi sintomi delle vie respiratorie superiori segue l'infezione. Durante questo periodo, il lavoratore è viremico e contagioso. Questo è seguito da un decorso di sette-dieci giorni di tosse, corizza e congiuntivite e lo sviluppo di un'eruzione morbilliforme e macchie di Koplik (lesioni bianche in rilievo sulla mucosa buccale), che sono patognomoniche per il morbillo. Alla radiografia si notano infiltrati reticolonodulari diffusi con linfoadenopatia ilare bilaterale, spesso con broncopolmonite batterica sovrapposta. Questi segni si verificano ben dopo che la persona ha avuto l'opportunità di infettare altre persone suscettibili. Le complicanze polmonari rappresentano il 90% dei decessi per morbillo negli adulti. Nessun trattamento antivirale specifico è efficace per nessuna forma di morbillo, sebbene le immunoglobuline anti-morbillo ad alto titolo possano migliorare alcuni sintomi negli adulti.
Nel morbillo atipico, che si verifica in persone vaccinate con un vaccino ucciso sviluppato negli anni '1960, è comune un grave coinvolgimento polmonare. L'eruzione cutanea è atipica e le macchie di Koplik sono rare. Nel morbillo modificato, che si verifica in persone che hanno ricevuto in precedenza un vaccino vivo ma sviluppano un'immunità parziale, segni e sintomi sono simili al morbillo classico ma più lievi e spesso passano inosservati. Le persone con morbillo atipico e modificato sono viremiche e possono diffondere il virus del morbillo.
Diagnosi
Il morbillo nei lavoratori ospedalieri è spesso modificato o atipico ed è raramente sospettato. Il morbillo dovrebbe essere preso in considerazione in una persona con un rash eritematoso maculopapulare preceduto da un prodromo febbrile di tre o quattro giorni. Nelle persone con una prima infezione e senza precedente immunizzazione, l'isolamento virale o il rilevamento dell'antigene è difficile, ma per una diagnosi rapida possono essere utilizzati immunosorbenti legati all'enzima o test di anticorpi fluorescenti. Nelle persone con precedenti vaccinazioni, l'interpretazione di questi test è difficile, ma possono essere utili le colorazioni anticorpali immunofluorescenti delle cellule esfoliate.
Epidemiologia
Infermieri e medici suscettibili hanno quasi nove volte più probabilità di contrarre il morbillo rispetto alle persone della stessa età che non sono operatori sanitari. Come per tutte le infezioni da morbillo, la trasmissione da persona a persona avviene per inalazione di un aerosol infettivo. Gli operatori ospedalieri acquisiscono il morbillo da pazienti e colleghi e, a loro volta, trasmettono il morbillo a pazienti, colleghi e familiari suscettibili.
Altre professioni interessate
Il morbillo epidemico si è verificato nelle istituzioni accademiche delle nazioni sviluppate e tra i lavoratori agricoli limitati agli alloggi collettivi nelle piantagioni.
Controlli di sanità pubblica
Le strategie di intervento della sanità pubblica includono programmi di immunizzazione e programmi di controllo delle infezioni per monitorare la malattia del morbillo e lo stato anticorpale dei lavoratori. Se non è possibile documentare un'infezione naturale o un'appropriata vaccinazione a due dosi, devono essere eseguiti i test anticorpali. La vaccinazione delle lavoratrici gestanti è controindicata. La vaccinazione di altri lavoratori a rischio è un aiuto importante nella prevenzione delle malattie. Dopo l'esposizione al morbillo, l'allontanamento dei lavoratori suscettibili dal contatto con il paziente per 21 giorni può ridurre la diffusione della malattia. Anche l'attività limitata dei lavoratori con morbillo per 7 giorni dopo la comparsa dell'eruzione cutanea può ridurre la trasmissione della malattia. Sfortunatamente, i lavoratori opportunamente vaccinati hanno sviluppato il morbillo nonostante i livelli di anticorpi protettivi documentati prima della malattia. Di conseguenza, molti raccomandano la protezione respiratoria personale quando si prendono cura dei pazienti con morbillo.
Varie infezioni virali delle vie respiratorie
Una varietà di virus che non sono esclusivi dell'ambiente sanitario sono la causa più comune di OAP negli operatori sanitari. Gli agenti eziologici sono quelli che causano OAP acquisiti in comunità, inclusi adenovirus, citomegalovirus, virus dell'influenza, virus della parainfluenza e virus respiratorio sinciziale. Poiché questi microrganismi sono presenti anche nella comunità, è difficile stabilirli come causa di un singolo OAP. Tuttavia, gli studi sierologici suggeriscono che gli operatori sanitari e diurni sono a maggior rischio di esposizione a questi agenti patogeni respiratori. Questi virus sono anche responsabili di epidemie in molte situazioni in cui i lavoratori sono riuniti in uno spazio ristretto. Ad esempio, i focolai di infezione adenovirale sono comuni nelle reclute militari.
Pertosse
La pertosse, come il morbillo, è stata sempre più segnalata nei lavoratori ospedalieri nelle nazioni sviluppate. Nel 1993, negli Stati Uniti sono stati segnalati quasi 6,000 casi di pertosse, un aumento dell'80% rispetto al 1992. A differenza degli anni precedenti, il 25% dei casi segnalati si è verificato in persone di età superiore ai dieci anni. Il numero di malattie professionali acquisite nei lavoratori ospedalieri non è noto, ma si ritiene che sia sottostimato nelle nazioni sviluppate. A causa della diminuzione dell'immunità negli adulti e della possibilità per il personale ospedaliero di infettare i bambini suscettibili, c'è una maggiore enfasi sulla diagnosi e la sorveglianza della pertosse.
Presentazione clinica
La pertosse può persistere da sei a dieci settimane senza intervento. Nella prima settimana, quando il malato è più contagioso, si sviluppano tosse secca, corizza, congiuntivite e febbre. Negli adulti precedentemente vaccinati, la tosse persistente e produttiva può durare diverse settimane e la pertosse viene raramente presa in considerazione. La diagnosi clinica è difficile e il sospetto clinico dovrebbe essere suscitato quando si incontra un lavoratore con una tosse che dura da più di sette giorni. Una conta bianca superiore a 20,000 con una predominanza di linfociti può essere l'unica anomalia di laboratorio, ma questa si nota raramente negli adulti. Le radiografie del torace mostrano broncopolmonite confluente nei lobi inferiori che si irradiano dal cuore per dare il caratteristico segno del "cuore irsuto" e l'atelettasia è presente nel 50% dei casi. A causa dell'estrema infettività di questo agente, è necessario un rigoroso isolamento respiratorio fino a quando il trattamento con eritromicina o trimetoprim/sulfametossazolo non è continuato per cinque giorni. I contatti stretti di persone infette e operatori ospedalieri che non utilizzavano precauzioni respiratorie dovrebbero ricevere 14 giorni di profilassi antibiotica indipendentemente dallo stato di immunizzazione.
Diagnosi
Isolamento di Bordetella pertussis, colorazione immunofluorescente diretta delle secrezioni nasali o sviluppo di a B. pertosse la risposta anticorpale viene utilizzata per formulare una diagnosi definitiva.
Epidemiologia
B. pertosse è altamente contagioso, trasmesso da persona a persona tramite inalazione di aerosol infettivi e ha un tasso di attacco dal 70 al 100%. In passato non è stata una malattia degli adulti e non è stata apprezzata come OAP. Durante un'epidemia di pertosse nella comunità degli Stati Uniti occidentali, molti operatori ospedalieri sono stati esposti al lavoro e hanno sviluppato la pertosse nonostante la profilassi antibiotica. A causa della diminuzione dei livelli di anticorpi protettivi negli adulti che non hanno mai avuto una malattia clinica ma hanno ricevuto il vaccino cellulare dopo il 1940, c'è una crescente popolazione di lavoratori ospedalieri sensibili alla pertosse nelle nazioni sviluppate.
Controlli di sanità pubblica
L'identificazione, l'isolamento e il trattamento sono le principali strategie di controllo delle malattie negli ospedali. Il ruolo del vaccino contro la pertosse acellulare per il personale ospedaliero senza livelli adeguati di anticorpi protettivi non è chiaro. Durante la recente epidemia negli Stati Uniti occidentali, un terzo degli operatori ospedalieri vaccinati ha riportato effetti collaterali da lievi a moderati al vaccino, ma l'1% ha avuto sintomi sistemici "gravi". Sebbene questi lavoratori più gravemente colpiti abbiano perso giorni di lavoro, non sono stati riportati sintomi neurologici.
Tubercolosi
Durante gli anni '1950, era generalmente riconosciuto che gli operatori sanitari nelle nazioni sviluppate erano maggiormente a rischio di tubercolosi (TBC, malattia granulomatosa dovuta a Mycobacterium tuberculosis o organismi strettamente correlati M. bovis) rispetto alla popolazione generale. Dagli anni '1970 fino all'inizio degli anni '1980, i sondaggi hanno suggerito che questo era diventato solo un rischio leggermente aumentato. Alla fine degli anni '1980, un marcato aumento del numero di casi di tubercolosi ricoverati negli ospedali statunitensi ha provocato la trasmissione insospettata di M. tuberculosis agli operatori ospedalieri. L'elevata prevalenza di fondo di positività al test cutaneo alla tubercolina (TST) in alcuni gruppi socio-economici o di immigrati da cui provenivano molti operatori ospedalieri, e la scarsa associazione della conversione del TST con l'esposizione alla tubercolosi correlata al lavoro, hanno reso difficile quantificare il rischio di Trasmissione professionale della tubercolosi ai lavoratori. Nel 1993 negli Stati Uniti, circa il 3.2% delle persone segnalate con tubercolosi erano operatori sanitari. Nonostante i problemi nella definizione del rischio, l'infezione correlata al lavoro dovrebbe essere presa in considerazione quando i lavoratori ospedalieri sviluppano la tubercolosi o convertono il loro TST.
M. tuberculosis si diffonde quasi esclusivamente da persona a persona su particelle infettive con un diametro da 1 a 5 mm che derivano da tosse, parole o starnuti. Il rischio di infezione è direttamente correlato all'intensità dell'esposizione agli aerosol infettivi: piccoli spazi condivisi, maggiore densità di particelle infettive, scarsa eliminazione di particelle infettive, ricircolo di aria contenente particelle infettive e tempo di contatto prolungato. Nelle strutture sanitarie, procedure come la broncoscopia, l'intubazione endotracheale e il trattamento con aerosol nebulizzato aumentano la densità degli aerosol infettivi. Circa il 30% dei contatti stretti, persone che condividono uno spazio comune con una persona infetta, si infettano e si sottopongono al test cutaneo. Dopo l'infezione, dal 3 al 10% delle persone svilupperà la tubercolosi entro 12 mesi (cioè malattia primaria) e un ulteriore 5-10% svilupperà la tubercolosi nel corso della vita (cioè malattia di riattivazione). Questi tassi più elevati si verificano nelle nazioni in via di sviluppo e nelle situazioni in cui la malnutrizione è più diffusa. Le persone con infezione da HIV riattivano la tubercolosi a tassi più elevati, circa dal 3 all'8% all'anno. CFR varia; nei paesi sviluppati è compresa tra il 5 e il 10%, ma nei paesi in via di sviluppo questi tassi vanno dal 15 al 40%.
Presentazione clinica
Prima dell'epidemia di HIV, l'85-90% delle persone affette da tubercolosi presentava coinvolgimento polmonare. Tosse cronica, produzione di espettorato, febbre e perdita di peso rimangono i sintomi più frequentemente riportati di tubercolosi polmonare. Fatta eccezione per rari respiri anforici o crepitii post-tossici sui lobi superiori, l'esame obiettivo non è utile. Una radiografia del torace anormale si trova in quasi tutti i casi e di solito è il primo reperto che suggerisce la tubercolosi. Nella tubercolosi primitiva è comune un infiltrato del lobo inferiore o medio con linfoadenopatia ilare omolaterale con atelettasia. La riattivazione della tubercolosi di solito provoca un infiltrato e una cavitazione nei lobi superiori dei polmoni. Sebbene sensibili, le radiografie del torace mancano di specificità e non forniranno una diagnosi definitiva di tubercolosi.
Diagnosi
La diagnosi definitiva di tubercolosi polmonare può essere effettuata solo mediante isolamento M. tuberculosis dall'espettorato o dal tessuto polmonare, sebbene sia possibile una diagnosi presuntiva se i bacilli acido-resistenti (AFB) vengono trovati nell'espettorato di persone con presentazioni cliniche compatibili. La diagnosi di tubercolosi dovrebbe essere considerata sulla base dei segni e dei sintomi clinici; l'isolamento e il trattamento di persone con malattie compatibili non dovrebbero essere ritardati per il risultato di un TST. Nelle nazioni in via di sviluppo in cui i reagenti TST e le radiografie del torace non sono disponibili, l'OMS suggerisce di valutare le persone con qualsiasi sintomo respiratorio della durata di tre settimane, emottisi di qualsiasi durata o significativa perdita di peso per la tubercolosi. Queste persone dovrebbero sottoporsi a un esame microscopico del loro espettorato per AFB.
Altre professioni interessate
Trasmissione aerea da lavoratore a lavoratore e da cliente a lavoratore di M. tuberculosis è stato documentato tra i lavoratori ospedalieri, gli equipaggi di volo delle compagnie aeree, i minatori, i lavoratori delle strutture penitenziarie, i custodi degli animali, i lavoratori dei cantieri navali, i dipendenti delle scuole e gli operai delle fabbriche di compensato. Particolare attenzione deve essere prestata a determinate occupazioni come braccianti agricoli, custodi di animali, lavoratori manuali, governanti, bidelli e addetti alla preparazione del cibo, sebbene la maggior parte del rischio possa essere dovuta allo stato socio-economico o di immigrazione dei lavoratori.
Particolare attenzione dovrebbe essere data alla tubercolosi polmonare tra i minatori e altri gruppi con esposizione alla silice. Oltre a un aumento del rischio di infezione primaria da parte dei colleghi minatori, le persone con silicosi hanno maggiori probabilità di progredire verso la tubercolosi e hanno una mortalità specifica per tubercolosi maggiore rispetto ai lavoratori non silicotici. Come nella maggior parte delle persone, la tubercolosi si riattiva nelle persone silicotiche da lungo tempo M. tuberculosis infezioni che precedono l'esposizione alla silice. Nei sistemi sperimentali, è stato dimostrato che l'esposizione alla silice peggiora il decorso dell'infezione in modo dose-dipendente, ma non è chiaro se i lavoratori non silicotici esposti alla silice siano a maggior rischio di sviluppare la tubercolosi. I lavoratori di fonderia esposti alla silice senza silicosi radiografica corrono un rischio tre volte maggiore di mortalità specifica per tubercolosi rispetto ai lavoratori simili senza esposizione alla silice. Nessun'altra esposizione professionale alla polvere è stata associata a una maggiore progressione della tubercolosi.
I lavoratori agricoli migranti hanno maggiori probabilità di sviluppare la tubercolosi da riattivazione rispetto alla popolazione generale. Le stime di TST positivi nei lavoratori agricoli migranti vanno da circa il 45% nelle persone di età compresa tra 15 e 34 anni a quasi il 70% nei lavoratori di età superiore ai 34 anni.
I lavoratori dei laboratori clinici sono a maggior rischio di tubercolosi acquisita professionalmente attraverso la trasmissione per via aerea. In una recente indagine decennale su ospedali selezionati in Giappone, lo 0.8% degli addetti ai laboratori ha sviluppato la tubercolosi. Non sono state identificate fonti comunitarie e le esposizioni correlate al lavoro sono state identificate solo nel 20% dei casi. La maggior parte dei casi si è verificata tra gli addetti ai laboratori di patologia e batteriologia e alle sale autoptiche.
Trattamento
Diversi regimi di trattamento si sono dimostrati efficaci in diversi contesti ambulatoriali. Tra i pazienti conformi nelle nazioni sviluppate, le dosi giornaliere di quattro farmaci (inclusi isoniazide e rifampicina) per due mesi seguite da dosi giornaliere di isoniazide e rifampicina per i successivi quattro mesi sono diventate un regime di trattamento standard. Osservata direttamente, la somministrazione bisettimanale degli stessi farmaci è un'alternativa efficace nei pazienti meno compiacenti. Nei paesi in via di sviluppo e in situazioni in cui i farmaci antitubercolari non sono prontamente disponibili, sono stati utilizzati da 9 a 12 mesi di somministrazione giornaliera di isoniazide e rifampicina. Un regime di trattamento dovrebbe essere coerente con la politica nazionale e prendere in considerazione la suscettibilità dell'organismo ai farmaci antitubercolari standard disponibili e la durata della terapia. A causa delle risorse limitate per controllare la tubercolosi nei paesi in via di sviluppo, gli sforzi possono concentrarsi sulle principali fonti di infezione: i pazienti con strisci di espettorato che dimostrano AFB.
Nelle strutture sanitarie, le restrizioni sul lavoro sono indicate per i lavoratori infetti con tubercolosi polmonare. In altri contesti, i lavoratori infettivi possono semplicemente essere isolati dagli altri lavoratori. In generale, le persone sono considerate non infettive dopo due settimane di farmaci antitubercolari appropriati se vi è un miglioramento sintomatico e una diminuzione della densità di AFB nello striscio dell'espettorato.
Controlli di sanità pubblica
Il principale controllo di sanità pubblica della trasmissione della tubercolosi professionale o acquisita in comunità rimane l'identificazione, l'isolamento e il trattamento delle persone affette da tubercolosi polmonare. Ventilazione per diluire aerosol infettivi; filtrazione e raggi ultravioletti per decontaminare l'aria contenente l'aerosol; o la protezione respiratoria personale può essere utilizzata laddove è noto che il rischio di trasmissione è eccezionalmente elevato, ma l'efficacia di questi metodi è ancora sconosciuta. L'utilità del BCG nella protezione dei lavoratori rimane controversa.
Infezioni batteriche varie in ambito sanitario
Le comuni infezioni batteriche del polmone possono essere acquisite dai pazienti o all'interno della comunità. Trasmissione aerea correlata al lavoro di agenti patogeni batterici come Streptococcus pneumoniae, Haemophilus influenzae, Neisseria meningitidis, Mycoplasma pneumoniae ed Legionella spp (Tabella 26) e le malattie che ne derivano sono incluse in molti programmi di sorveglianza ospedaliera. Anche le infezioni batteriche professionali delle vie respiratorie non sono limitate agli operatori sanitari. Infezioni da Streptococco spp sono, ad esempio, una causa consolidata di epidemie tra le reclute militari. Tuttavia, per un lavoratore specifico, la prevalenza di questi disturbi al di fuori del posto di lavoro complica la distinzione tra infezioni professionali e acquisite in comunità. La presentazione clinica, i test diagnostici, l'epidemiologia e il trattamento di questi disturbi sono descritti nei manuali di medicina standard.
Le infezioni nel lavoratore immunodepresso
I lavoratori immunosoppressi sono maggiormente a rischio di molti OAP. Inoltre, un certo numero di microrganismi che non causano malattie negli individui normali produrranno malattie negli immunodepressi. Il tipo di immunosoppressione influenzerà anche la suscettibilità alla malattia. Ad esempio, l'aspergillosi polmonare invasiva è una complicanza più frequente della chemioterapia rispetto alla sindrome da immunodeficienza acquisita (AIDS).
L'aspergillosi polmonare invasiva si osserva di solito negli immunodepressi, in particolare negli individui con neutropenia. Tuttavia, l'aspergillosi polmonare invasiva è occasionalmente riportata in individui senza un'apparente predisposizione alla malattia. L'aspergillosi polmonare invasiva si presenta normalmente come una grave polmonite necrotizzante con o senza coinvolgimento sistemico in un paziente neutropenico. Mentre l'aspergillosi invasiva è vista più frequentemente come un'infezione nosocomiale nei pazienti chemioterapici, questa è una malattia altamente fatale in qualsiasi lavoratore neutropenico. Le tecniche che riducono l'aspergillosi nosocomiale, ad esempio il controllo delle polveri dei progetti di costruzione, possono anche proteggere i lavoratori sensibili.
Una varietà di agenti patogeni animali diventa potenziale zoonosi solo nel paziente immunodepresso. Le zoonosi trasmesse dall'esposizione all'aerosol osservate solo negli immunodepressi includono l'encefalitozoonosi (dovuta a Encefalitozoo cuniculi), tubercolosi aviaria (dovuta a Mycobacterium avium) e Rhodococcus equi infezioni. Tali malattie destano particolare preoccupazione in agricoltura. I metodi per la protezione dei lavoratori immunodepressi sono studiati in modo incompleto.
Nel lavoratore immunodepresso, molti potenziali agenti patogeni causano malattie invasive e gravi non osservate nei pazienti normali. Ad esempio, gravi infezioni da Candida albicans ed Pneumocystis carinii sono manifestazioni classiche dell'AIDS. Lo spettro dei patogeni occupazionali nel lavoratore immunodepresso, quindi, comporta potenzialmente disturbi non presenti nei lavoratori immunologicamente normali. Le malattie degli individui immunosoppressi sono state esaminate a fondo altrove e non saranno ulteriormente discusse in questa revisione.
Controlli di sanità pubblica: panoramica
Gli OAP si verificano prevalentemente in cinque gruppi di lavoratori: operatori ospedalieri, lavoratori agricoli, addetti alla produzione di carne, personale militare e addetti ai laboratori biomedici (tabella 1). Evitare gli aerosol infettivi è il modo più efficace per ridurre l'infezione nella maggior parte delle situazioni, ma spesso è difficile. Per esempio, Coxiella burnetii, l'agente eziologico della febbre Q, può essere presente in qualsiasi ambiente precedentemente contaminato con fluidi biologici di animali infetti, ma evitare tutti gli aerosol potenzialmente infetti sarebbe impraticabile in molte situazioni a basso rischio come l'allevamento di pecore o i rodei. Il controllo delle malattie concomitanti può anche ridurre il rischio di OAP. La silicosi, ad esempio, aumenta il rischio di riattivazione della tubercolosi e la riduzione dell'esposizione alla silice può ridurre il rischio di tubercolosi nei minatori. Per gli OAP che presentano mortalità e morbilità significative nella popolazione generale, l'immunizzazione può essere l'intervento di sanità pubblica più importante. L'educazione dei lavoratori sul loro rischio di OAP aiuta i lavoratori a conformarsi ai programmi di controllo delle malattie professionali e aiuta anche nella diagnosi precoce di questi disturbi.
Tra gli operatori ospedalieri e il personale militare, la trasmissione da uomo a uomo è solitamente la principale via di infezione. L'immunizzazione dei lavoratori può prevenire le malattie e può essere utile nel controllo dei patogeni ad alta morbilità e/o mortalità. Perché c'è un rischio per le persone che potrebbero non essere state adeguatamente immunizzate; identificare, isolare e curare le persone malate rimane una parte del controllo delle malattie. Quando l'immunizzazione e l'isolamento respiratorio falliscono o la morbilità e la mortalità associate sono intollerabili, si può prendere in considerazione la protezione personale o controlli tecnici per ridurre la densità o l'infettività degli aerosol.
Per gli addetti all'agricoltura, alla produzione di carne e ai laboratori biomedici, la trasmissione da animale a uomo è un modello di trasmissione comune. Oltre all'immunizzazione delle persone suscettibili, quando possibile, altre strategie di controllo delle malattie possono includere l'immunizzazione degli animali, la profilassi antibiotica controllata dal veterinario di animali in buona salute, la quarantena degli animali appena arrivati, l'isolamento e il trattamento di animali malati e l'acquisto di agenti patogeni. animali liberi. Quando queste strategie hanno fallito o c'è un'elevata morbilità e mortalità, possono essere prese in considerazione strategie come la protezione personale o controlli tecnici.
La trasmissione dall'ambiente all'uomo di agenti infettivi è comune tra i lavoratori agricoli, inclusi molti braccianti. L'immunizzazione dei lavoratori è possibile quando è disponibile un vaccino, ma per molti di questi agenti patogeni l'incidenza della malattia nella popolazione generale è bassa ei vaccini sono raramente fattibili. Negli ambienti agricoli, le fonti di infezione sono diffuse. Di conseguenza, i controlli ingegneristici per ridurre la densità o l'infettività degli aerosol sono raramente realizzabili. In questi contesti possono essere presi in considerazione agenti umettanti o altri metodi per ridurre la polvere, agenti decontaminanti e protezione respiratoria personale. Poiché il controllo dell'OAP nei lavoratori agricoli è spesso difficile e queste malattie sono raramente osservate dal personale medico, l'istruzione dei lavoratori e la comunicazione tra lavoratori e personale medico sono essenziali.
Di Più...
L'orecchio
Anatomia
L'orecchio è l'organo sensoriale responsabile dell'udito e del mantenimento dell'equilibrio, attraverso il rilevamento della posizione del corpo e del movimento della testa. È composto da tre parti: l'orecchio esterno, medio e interno; l'orecchio esterno si trova all'esterno del cranio, mentre le altre due parti sono incorporate nell'osso temporale (figura 1).
Figura 1. Schema dell'orecchio.
L'orecchio esterno è costituito dal padiglione auricolare, una struttura cartilaginea rivestita di pelle, e dal condotto uditivo esterno, un cilindro di forma irregolare lungo circa 25 mm, rivestito da ghiandole che secernono cera.
L'orecchio medio è costituito dalla cavità timpanica, una cavità piena d'aria le cui pareti esterne formano la membrana timpanica (timpano) e comunica prossimalmente con il rinofaringe dalle trombe di Eustachio, che mantengono l'equilibrio di pressione su entrambi i lati della membrana timpanica. Ad esempio, questa comunicazione spiega come la deglutizione consenta l'equalizzazione della pressione e il ripristino dell'acuità uditiva perduta causata da un rapido cambiamento della pressione barometrica (p. es., aeroplani in atterraggio, ascensori veloci). La cavità timpanica contiene anche gli ossicini - il martello, l'incudine e la staffa - che sono controllati dai muscoli stapedio e tensore del timpano. La membrana timpanica è collegata all'orecchio interno dagli ossicini, precisamente dal piede mobile della staffa, che si appoggia alla finestra ovale.
L'orecchio interno contiene l'apparato sensoriale di per sé. Consiste in un guscio osseo (il labirinto osseo) all'interno del quale si trova il labirinto membranoso, una serie di cavità che formano un sistema chiuso riempito di endolinfa, un liquido ricco di potassio. Il labirinto membranoso è separato dal labirinto osseo dalla perilinfa, un liquido ricco di sodio.
Il labirinto osseo stesso è composto da due parti. La porzione anteriore è nota come coclea ed è l'organo vero e proprio dell'udito. Ha una forma a spirale che ricorda il guscio di una lumaca ed è appuntito in direzione anteriore. La porzione posteriore del labirinto osseo contiene il vestibolo ei canali semicircolari ed è responsabile dell'equilibrio. Nel labirinto membranoso sono localizzate le strutture neurosensoriali coinvolte nell'udito e nell'equilibrio: l'organo del Corti si trova nel canale cocleare, mentre le macule dell'utricolo e del sacculo e le ampolle dei canali semicircolari si trovano nella sezione posteriore.
Organi uditivi
Il canale cocleare è un tubo triangolare a spirale, comprendente due giri e mezzo, che separa la scala vestibuli dalla scala tympani. Un'estremità termina nel legamento a spirale, un processo della colonna centrale della coclea, mentre l'altra è collegata alla parete ossea della coclea.
La scala vestibuli e i timpani terminano rispettivamente nella finestra ovale (il piede della staffa) e nella finestra rotonda. Le due camere comunicano attraverso l'elicotrema, la punta della coclea. La membrana basilare forma la superficie inferiore del canale cocleare e sostiene l'organo del Corti, responsabile della trasduzione degli stimoli acustici. Tutte le informazioni uditive sono trasdotte da sole 15,000 cellule ciliate (organo del Corti), di cui le cosiddette cellule ciliate interne, che sono 3,500, sono di fondamentale importanza, poiché formano sinapsi con circa il 90% dei 30,000 neuroni uditivi primari (figura 2 ). Le cellule ciliate interne ed esterne sono separate l'una dall'altra da un abbondante strato di cellule di supporto. Attraversando una membrana straordinariamente sottile, le ciglia delle cellule ciliate sono incorporate nella membrana tettoria, la cui estremità libera si trova sopra le cellule. La superficie superiore del canale cocleare è formata dalla membrana di Reissner.
Figura 2. Sezione trasversale di un'ansa della coclea. Diametro: circa 1.5 mm.
I corpi delle cellule sensoriali cocleari che poggiano sulla membrana basilare sono circondati da terminazioni nervose e i loro circa 30,000 assoni formano il nervo cocleare. Il nervo cocleare attraversa il condotto uditivo interno e si estende alle strutture centrali del tronco encefalico, la parte più antica del cervello. Le fibre uditive terminano il loro tortuoso percorso nel lobo temporale, la parte della corteccia cerebrale deputata alla percezione degli stimoli acustici.
Organi di equilibrio
Le cellule sensoriali si trovano nelle ampolle dei canali semicircolari e nelle macule dell'utricolo e del sacculo, e sono stimolate dalla pressione trasmessa attraverso l'endolinfa a seguito dei movimenti della testa o del corpo. Le cellule si connettono con cellule bipolari i cui processi periferici formano due tratti, uno dai canali semicircolari anteriore ed esterno, l'altro dal canale semicircolare posteriore. Questi due tratti entrano nel condotto uditivo interno e si uniscono per formare il nervo vestibolare, che si estende ai nuclei vestibolari nel tronco encefalico. Le fibre dei nuclei vestibolari, a loro volta, si estendono ai centri cerebellari che controllano i movimenti oculari e al midollo spinale.
L'unione dei nervi vestibolare e cocleare forma l'ottavo nervo cranico, noto anche come nervo vestibolococleare.
Fisiologia dell'udito
Conduzione del suono attraverso l'aria
L'orecchio è composto da un conduttore del suono (l'orecchio esterno e medio) e da un recettore del suono (l'orecchio interno).
Le onde sonore che passano attraverso il condotto uditivo esterno colpiscono la membrana timpanica, facendola vibrare. Questa vibrazione viene trasmessa alle staffe attraverso il martello e l'incudine. La superficie della membrana timpanica è quasi 16 volte quella del piede della staffa (55 mm2/3.5 mm2), e questo, in combinazione con il meccanismo a leva degli ossicini, si traduce in un'amplificazione di 22 volte della pressione sonora. A causa della frequenza di risonanza dell'orecchio medio, il rapporto di trasmissione è ottimale tra 1,000 e 2,000 Hz. Quando il piede della staffa si muove, provoca la formazione di onde nel liquido all'interno del canale vestibolare. Poiché il liquido è incomprimibile, ogni movimento verso l'interno del piede della staffa provoca un equivalente movimento verso l'esterno della finestrella rotonda, verso l'orecchio medio.
Se esposto a livelli sonori elevati, il muscolo della staffa si contrae, proteggendo l'orecchio interno (riflesso di attenuazione). Oltre a questa funzione, i muscoli dell'orecchio medio estendono anche la gamma dinamica dell'orecchio, migliorano la localizzazione del suono, riducono la risonanza nell'orecchio medio e controllano la pressione dell'aria nell'orecchio medio e la pressione del liquido nell'orecchio interno.
Tra 250 e 4,000 Hz, la soglia del riflesso di attenuazione è di circa 80 decibel (dB) al di sopra della soglia uditiva e aumenta di circa 0.6 dB/dB all'aumentare dell'intensità di stimolazione. La sua latenza è di 150 ms alla soglia e di 24-35 ms in presenza di stimoli intensi. A frequenze inferiori alla risonanza naturale dell'orecchio medio, la contrazione dei muscoli dell'orecchio medio attenua la trasmissione del suono di circa 10 dB. A causa della sua latenza, il riflesso di attenuazione fornisce una protezione adeguata dal rumore generato a velocità superiori a due o tre al secondo, ma non dal rumore impulsivo discreto.
La velocità con cui le onde sonore si propagano attraverso l'orecchio dipende dall'elasticità della membrana basilare. L'elasticità aumenta, e quindi la velocità dell'onda diminuisce, dalla base della coclea alla punta. Il trasferimento dell'energia di vibrazione alla membrana di Reissner e alla membrana basilare dipende dalla frequenza. Alle alte frequenze, l'ampiezza dell'onda è massima alla base, mentre per le frequenze più basse è massima alla punta. Pertanto, il punto di massima eccitazione meccanica nella coclea dipende dalla frequenza. Questo fenomeno è alla base della capacità di rilevare le differenze di frequenza. Il movimento della membrana basilare induce forze di taglio nella stereocilia delle cellule ciliate e innesca una serie di eventi meccanici, elettrici e biochimici responsabili della trasduzione meccanico-sensoriale e dell'elaborazione del segnale acustico iniziale. Le forze di taglio sulla stereocilia provocano l'apertura dei canali ionici nelle membrane cellulari, modificando la permeabilità delle membrane e consentendo l'ingresso di ioni potassio nelle cellule. Questo afflusso di ioni di potassio provoca la depolarizzazione e la generazione di un potenziale d'azione.
I neurotrasmettitori liberati alla giunzione sinaptica delle cellule ciliate interne a seguito della depolarizzazione innescano impulsi neuronali che viaggiano lungo le fibre afferenti del nervo uditivo verso i centri superiori. L'intensità della stimolazione uditiva dipende dal numero di potenziali d'azione per unità di tempo e dal numero di cellule stimolate, mentre la frequenza percepita del suono dipende dalle specifiche popolazioni di fibre nervose attivate. Esiste una mappatura spaziale specifica tra la frequenza dello stimolo sonoro e la sezione della corteccia cerebrale stimolata.
Le cellule ciliate interne sono meccanorecettori che trasformano i segnali generati in risposta alla vibrazione acustica in messaggi elettrici inviati al sistema nervoso centrale. Non sono però responsabili della sensibilità di soglia dell'orecchio e della sua straordinaria selettività in frequenza.
Le cellule ciliate esterne, invece, non inviano segnali uditivi al cervello. Piuttosto, la loro funzione è quella di amplificare selettivamente la vibrazione meccano-acustica a livelli vicini alla soglia di un fattore di circa 100 (cioè 40 dB), e quindi facilitare la stimolazione delle cellule ciliate interne. Si ritiene che questa amplificazione funzioni attraverso l'accoppiamento micromeccanico che coinvolge la membrana tettoria. Le cellule ciliate esterne possono produrre più energia di quella che ricevono dagli stimoli esterni e, contraendosi attivamente a frequenze molto alte, possono funzionare come amplificatori cocleari.
Nell'orecchio interno, l'interferenza tra le cellule ciliate esterne e interne crea un circuito di feedback che consente il controllo della ricezione uditiva, in particolare della sensibilità di soglia e della selettività di frequenza. Le fibre cocleari efferenti possono quindi aiutare a ridurre il danno cocleare causato dall'esposizione a intensi stimoli acustici. Le cellule ciliate esterne possono anche subire una contrazione riflessa in presenza di stimoli intensi. Il riflesso di attenuazione dell'orecchio medio, attivo principalmente alle basse frequenze, e il riflesso di contrazione dell'orecchio interno, attivo alle alte frequenze, sono quindi complementari.
Conduzione ossea del suono
Le onde sonore possono anche essere trasmesse attraverso il cranio. Sono possibili due meccanismi:
Nella prima, le onde di compressione che colpiscono il cranio fanno sì che il perilinfa incomprimibile deformi la finestra rotonda o ovale. Poiché le due finestre hanno elasticità differenti, il movimento dell'endolinfa determina il movimento della membrana basilare.
Il secondo meccanismo si basa sul fatto che il movimento degli ossicini induce movimento solo nella scala vestibuli. In questo meccanismo, il movimento della membrana basilare risulta dal movimento traslatorio prodotto dall'inerzia.
La conduzione ossea è normalmente inferiore di 30-50 dB rispetto alla conduzione aerea, come è evidente quando entrambe le orecchie sono bloccate. Ciò è vero, tuttavia, solo per gli stimoli mediati dall'aria, poiché la stimolazione ossea diretta viene attenuata in misura diversa.
Intervallo di sensibilità
La vibrazione meccanica induce potenziali cambiamenti nelle cellule dell'orecchio interno, nelle vie di conduzione e nei centri superiori. Solo frequenze di 16 Hz–25,000 Hz e pressioni sonore (queste possono essere espresse in pascal, Pa) da 20 μPa a 20 Pa. La gamma di pressioni sonore che possono essere percepite è notevole: una gamma di 1 milione di volte! Le soglie di rilevamento della pressione sonora dipendono dalla frequenza, più basse a 1,000-6,000 Hz e in aumento sia alle frequenze più alte che a quelle più basse.
Ai fini pratici, il livello di pressione sonora è espresso in decibel (dB), scala di misura logaritmica corrispondente all'intensità sonora percepita rispetto alla soglia uditiva. Pertanto, 20 μPa equivalgono a 0 dB. Quando la pressione sonora aumenta di dieci volte, il livello di decibel aumenta di 20 dB, secondo la seguente formula:
Lx = 20 registri Px/P0
dove:
Lx = pressione sonora in dB
Px = pressione sonora in pascal
P0 = pressione sonora di riferimento (2×10-5 Pa, la soglia uditiva)
La soglia di discriminazione in frequenza, che è la minima differenza di frequenza rilevabile, è di 1.5 Hz fino a 500 Hz e dello 0.3% della frequenza di stimolo a frequenze più alte. A pressioni sonore vicine alla soglia uditiva, la soglia di discriminazione della pressione sonora è di circa il 20%, sebbene si possano rilevare differenze anche solo del 2% a pressioni sonore elevate.
Se due suoni differiscono in frequenza di una quantità sufficientemente piccola, si sentirà solo un tono. La frequenza percepita del tono sarà a metà strada tra i due toni sorgente, ma il suo livello di pressione sonora è variabile. Se due stimoli acustici hanno frequenze simili ma intensità diverse, si verifica un effetto di mascheramento. Se la differenza nella pressione sonora è abbastanza grande, il mascheramento sarà completo, con solo il suono più forte percepito.
La localizzazione degli stimoli acustici dipende dal rilevamento dell'intervallo di tempo tra l'arrivo dello stimolo a ciascun orecchio e, come tale, richiede un udito bilaterale intatto. Il più piccolo ritardo rilevabile è 3 x 10-5 secondi. La localizzazione è facilitata dall'effetto schermante della testa, che si traduce in differenze nell'intensità dello stimolo in ciascun orecchio.
La notevole capacità degli esseri umani di risolvere gli stimoli acustici è il risultato della scomposizione della frequenza da parte dell'orecchio interno e dell'analisi della frequenza da parte del cervello. Questi sono i meccanismi che consentono di rilevare e identificare singole sorgenti sonore come singoli strumenti musicali nei complessi segnali acustici che compongono la musica di un'intera orchestra sinfonica.
Fisiopatologia
Danno ciliare
Il movimento ciliare indotto da intensi stimoli acustici può superare la resistenza meccanica delle ciglia e causare la distruzione meccanica delle cellule ciliate. Poiché queste cellule sono in numero limitato e incapaci di rigenerarsi, qualsiasi perdita cellulare è permanente e, se l'esposizione allo stimolo sonoro dannoso continua, progressiva. In generale, l'effetto finale del danno ciliare è lo sviluppo di un deficit uditivo.
Le cellule ciliate esterne sono le cellule più sensibili agli agenti sani e tossici come anossia, farmaci ototossici e sostanze chimiche (p. es., derivati del chinino, streptomicina e alcuni altri antibiotici, alcuni preparati antitumorali) e sono quindi le prime ad essere perse. Solo i fenomeni idromeccanici passivi rimangono operativi nelle cellule ciliate esterne che sono danneggiate o hanno stereocilia danneggiata. In queste condizioni, è possibile solo un'analisi grossolana delle vibrazioni acustiche. In termini molto approssimativi, la distruzione delle ciglia nelle cellule ciliate esterne si traduce in un aumento di 40 dB della soglia uditiva.
Danno cellulare
L'esposizione al rumore, soprattutto se ripetitiva o prolungata, può influenzare anche il metabolismo delle cellule dell'organo del Corti e delle sinapsi afferenti situate al di sotto delle cellule ciliate interne. Gli effetti extraciliari riportati includono la modifica dell'ultrastruttura cellulare (reticolo, mitocondri, lisosomi) e, postsinapticamente, il rigonfiamento dei dendriti afferenti. Il gonfiore dendritico è probabilmente dovuto all'accumulo tossico di neurotrasmettitori a seguito dell'eccessiva attività delle cellule ciliate interne. Tuttavia, l'entità del danno stereociliare sembra determinare se la perdita dell'udito è temporanea o permanente.
Perdita dell'udito indotta dal rumore
Il rumore è un serio pericolo per l'udito nelle società industriali sempre più complesse di oggi. Ad esempio, l'esposizione al rumore rappresenta circa un terzo dei 28 milioni di casi di perdita dell'udito negli Stati Uniti e il NIOSH (l'Istituto nazionale per la sicurezza e la salute sul lavoro) riferisce che il 14% dei lavoratori americani è esposto a livelli sonori potenzialmente pericolosi , cioè livelli superiori a 90 dB. L'esposizione al rumore è l'esposizione professionale nociva più diffusa ed è la seconda causa, dopo gli effetti legati all'età, di perdita dell'udito. Non va dimenticato, infine, il contributo dell'esposizione extraprofessionale al rumore, come i laboratori domestici, la musica sovraamplificata soprattutto con l'uso di auricolari, l'uso di armi da fuoco, ecc.
Danni acuti da rumore. Gli effetti immediati dell'esposizione a stimoli sonori ad alta intensità (ad esempio, esplosioni) includono l'innalzamento della soglia uditiva, la rottura del timpano e danni traumatici all'orecchio medio e interno (lussazione degli ossicini, lesioni cocleari o fistole).
Spostamento temporaneo della soglia. L'esposizione al rumore provoca una diminuzione della sensibilità delle cellule sensoriali uditive che è proporzionale alla durata e all'intensità dell'esposizione. Nelle sue fasi iniziali, questo aumento della soglia uditiva, noto come affaticamento uditivo or spostamento temporaneo della soglia (TTS), è completamente reversibile ma persiste per qualche tempo dopo la cessazione dell'esposizione.
Gli studi sul recupero della sensibilità uditiva hanno identificato diversi tipi di affaticamento uditivo. La fatica a breve termine si dissipa in meno di due minuti e si traduce in uno spostamento della soglia massima alla frequenza di esposizione. La fatica a lungo termine è caratterizzata dal recupero in più di due minuti ma meno di 16 ore, un limite arbitrario derivato da studi sull'esposizione al rumore industriale. In generale, l'affaticamento uditivo è una funzione dell'intensità, della durata, della frequenza e della continuità dello stimolo. Pertanto, per una data dose di rumore, ottenuta integrando intensità e durata, i modelli di esposizione intermittente sono meno dannosi di quelli continui.
La gravità del TTS aumenta di circa 6 dB per ogni raddoppio dell'intensità dello stimolo. Al di sopra di un'intensità di esposizione specifica (il livello critico), questo tasso aumenta, in particolare se l'esposizione è al rumore impulsivo. Il TTS aumenta asintoticamente con la durata dell'esposizione; l'asintoto stesso aumenta con l'intensità dello stimolo. A causa delle caratteristiche della funzione di trasferimento dell'orecchio esterno e medio, le basse frequenze sono tollerate al meglio.
Gli studi sull'esposizione a toni puri indicano che all'aumentare dell'intensità dello stimolo, la frequenza alla quale il TTS è massimo si sposta progressivamente verso frequenze superiori a quella dello stimolo. I soggetti esposti a un tono puro di 2,000 Hz sviluppano TTS che è massimo a circa 3,000 Hz (uno spostamento di una semiottava). Si ritiene che l'effetto del rumore sulle cellule ciliate esterne sia responsabile di questo fenomeno.
Il lavoratore che mostra TTS recupera i valori uditivi di base entro poche ore dalla rimozione dal rumore. Tuttavia, esposizioni ripetute al rumore comportano un minore recupero dell'udito e una conseguente perdita permanente dell'udito.
Spostamento della soglia permanente. L'esposizione a stimoli sonori ad alta intensità per diversi anni può portare alla perdita permanente dell'udito. Questo è indicato come spostamento permanente della soglia (PTS). Anatomicamente, la PTS è caratterizzata dalla degenerazione delle cellule ciliate, che inizia con lievi modificazioni istologiche ma alla fine culmina nella completa distruzione cellulare. È molto probabile che la perdita dell'udito coinvolga le frequenze a cui l'orecchio è più sensibile, poiché è a queste frequenze che la trasmissione dell'energia acustica dall'ambiente esterno all'orecchio interno è ottimale. Questo spiega perché la perdita dell'udito a 4,000 Hz è il primo segno di perdita dell'udito indotta dal lavoro (figura 3). È stata osservata l'interazione tra l'intensità e la durata dello stimolo e gli standard internazionali assumono il grado di perdita dell'udito in funzione dell'energia acustica totale ricevuta dall'orecchio (dose di rumore).
Figura 3. Audiogramma che mostra l'ipoacusia bilaterale indotta dal rumore.
Lo sviluppo della perdita dell'udito indotta dal rumore mostra suscettibilità individuale. Varie variabili potenzialmente importanti sono state esaminate per spiegare questa suscettibilità, come l'età, il sesso, la razza, le malattie cardiovascolari, il fumo, ecc. I dati erano inconcludenti.
Una domanda interessante è se la quantità di TTS possa essere utilizzata per prevedere il rischio di PTS. Come notato sopra, c'è un progressivo spostamento del TTS a frequenze superiori a quella della frequenza di stimolazione. D'altra parte, la maggior parte del danno ciliare che si verifica ad alte intensità di stimolo coinvolge cellule sensibili alla frequenza dello stimolo. Se l'esposizione persiste, la differenza tra la frequenza alla quale il PTS è massimo e la frequenza di stimolazione diminuisce progressivamente. Il danno ciliare e la perdita cellulare si verificano di conseguenza nelle cellule più sensibili alle frequenze dello stimolo. Sembra quindi che TTS e PTS coinvolgano meccanismi diversi e che sia quindi impossibile prevedere il PTS di un individuo sulla base del TTS osservato.
Gli individui con PTS di solito sono inizialmente asintomatici. Con il progredire della perdita dell'udito, iniziano ad avere difficoltà a seguire le conversazioni in ambienti rumorosi come feste o ristoranti. La progressione, che di solito influisce sulla capacità di percepire prima i suoni acuti, è solitamente indolore e relativamente lenta.
Esame delle persone che soffrono di ipoacusia
Esame clinico
Oltre alla cronologia della data in cui l'ipoacusia è stata rilevata per la prima volta (se presente) e di come si è evoluta, inclusa qualsiasi asimmetria dell'udito, il questionario medico dovrebbe raccogliere informazioni sull'età del paziente, la storia familiare, l'uso di farmaci ototossici o esposizione ad altre sostanze chimiche ototossiche, presenza di tinnito (ossia, ronzio, fischio o ronzio in una o entrambe le orecchie), vertigini o eventuali problemi di equilibrio e qualsiasi storia di infezioni dell'orecchio con dolore o secrezione dal condotto uditivo esterno. Di fondamentale importanza è una storia dettagliata di esposizione a livelli elevati per tutta la vita suono livelli (si noti che, per i non addetti ai lavori, non tutti i suoni sono "rumore") sul lavoro, nei lavori precedenti e fuori dal lavoro. Una storia di episodi di TTS confermerebbe precedenti esposizioni tossiche al rumore.
L'esame fisico dovrebbe includere la valutazione della funzione degli altri nervi cranici, test di equilibrio e oftalmoscopia per rilevare qualsiasi evidenza di aumento della pressione cranica. L'esame visivo del canale uditivo esterno rileverà qualsiasi cerume incluso e, dopo che è stato rimosso con cautela (nessun oggetto appuntito!), qualsiasi evidenza di cicatrizzazione o perforazione della membrana timpanica. La perdita dell'udito può essere determinata in modo molto approssimativo testando la capacità del paziente di ripetere parole e frasi pronunciate a bassa voce o sussurrate dall'esaminatore quando si trova dietro e fuori dalla vista del paziente. Il test di Weber (posizionando un diapason vibrante al centro della fronte per determinare se questo suono viene “udito” in una o entrambe le orecchie) e il test del tono di Rinné (posizionando un diapason vibrante sul processo mastoideo finché il paziente non non riesce più a sentire il suono, quindi posizionare rapidamente la forchetta vicino al condotto uditivo; normalmente il suono può essere udito più a lungo attraverso l'aria che attraverso l'osso) consentirà di classificare la perdita dell'udito come trasmissione o neurosensoriale.
L'audiogramma è il test standard per rilevare e valutare la perdita dell'udito (vedi sotto). In alcuni pazienti possono essere necessari studi specialistici per completare l'audiogramma. Questi includono: timpanometria, test di discriminazione delle parole, valutazione del riflesso di attenuazione, studi elettrofisici (elettrococleogramma, potenziali evocati uditivi) e studi radiologici (radiografie craniche di routine integrate da TAC, risonanza magnetica).
audiometria
Questa componente cruciale della valutazione medica utilizza un dispositivo noto come audiometro per determinare la soglia uditiva degli individui a toni puri di 250-8,000 Hz e livelli sonori compresi tra –10 dB (la soglia uditiva delle orecchie intatte) e 110 dB (danno massimo ). Per eliminare gli effetti dei TTS, i pazienti non dovrebbero essere stati esposti al rumore durante le 16 ore precedenti. La conduzione aerea viene misurata mediante auricolari posizionati sulle orecchie, mentre la conduzione ossea viene misurata ponendo un vibratore a contatto con il cranio dietro l'orecchio. L'udito di ciascun orecchio viene misurato separatamente ei risultati del test vengono riportati su un grafico noto come audiogramma (Figura 3). La soglia dell'intelligibilità, cioè. l'intensità sonora alla quale il parlato diventa intelligibile, è determinata da un metodo di prova complementare noto come audiometria vocale, basato sulla capacità di comprendere parole composte da due sillabe di uguale intensità (ad esempio, pastore, cena, stordimento).
Il confronto tra conduzione aerea e ossea consente di classificare le perdite uditive come trasmissione (che coinvolge il canale uditivo esterno o l'orecchio medio) o perdita neurosensoriale (che coinvolge l'orecchio interno o il nervo uditivo) (figure 3 e 4). L'audiogramma osservato nei casi di perdita dell'udito indotta dal rumore è caratterizzato da un inizio di perdita dell'udito a 4,000 Hz, visibile come un calo nell'audiogramma (figura 3). Man mano che l'esposizione a livelli di rumore eccessivi continua, le frequenze vicine vengono progressivamente influenzate e il calo si amplia, invadendo, a circa 3,000 Hz, frequenze essenziali per la comprensione della conversazione. L'ipoacusia indotta dal rumore è solitamente bilaterale e mostra uno schema simile in entrambe le orecchie, cioè la differenza tra le due orecchie non supera i 15 dB a 500 Hz, a 1,000 dB e a 2,000 Hz, e 30 dB a 3,000, a 4,000 e a 6,000 Hz. Il danno asimmetrico può tuttavia essere presente nei casi di esposizione non uniforme, ad esempio con tiratori scelti, nei quali la perdita uditiva è maggiore dal lato opposto al dito del grilletto (lato sinistro, in un destro). Nella perdita dell'udito non correlata all'esposizione al rumore, l'audiogramma non mostra il caratteristico calo di 4,000 Hz (figura 4).
Figura 4. Esempi di audiogrammi dell'orecchio destro. I cerchi rappresentano la perdita dell'udito per conduzione aerea, la "" conduzione ossea.
Esistono due tipi di esami audiometrici: di screening e diagnostici. L'audiometria di screening viene utilizzata per il rapido esame di gruppi di individui sul posto di lavoro, nelle scuole o altrove nella comunità per identificare coloro che apparire avere una certa perdita dell'udito. Spesso vengono utilizzati audiometri elettronici che consentono l'autotest e, di norma, gli audiogrammi di screening vengono ottenuti in un'area tranquilla ma non necessariamente in una camera insonorizzata e priva di vibrazioni. Quest'ultimo è considerato un prerequisito per l'audiometria diagnostica che ha lo scopo di misurare la perdita dell'udito con precisione e accuratezza riproducibili. L'esame diagnostico viene eseguito correttamente da un audiologo qualificato (in alcune circostanze è richiesta una certificazione formale della competenza dell'audiologo). L'accuratezza di entrambi i tipi di audiometria dipende dai test periodici e dalla ricalibrazione dell'apparecchiatura utilizzata.
In molte giurisdizioni, le persone con perdita dell'udito causata dal rumore legata al lavoro hanno diritto a prestazioni di compensazione per i lavoratori. Di conseguenza, molti datori di lavoro stanno includendo l'audiometria nelle loro visite mediche prima del collocamento per rilevare eventuali perdite uditive esistenti che potrebbero essere responsabilità di un precedente datore di lavoro o rappresentare un'esposizione non professionale.
Le soglie uditive aumentano progressivamente con l'età, con frequenze più alte che sono più colpite (figura 3). Il caratteristico calo di 4,000 Hz osservato nell'ipoacusia indotta dal rumore non si osserva con questo tipo di ipoacusia.
Calcolo della perdita dell'udito
Negli Stati Uniti la formula più ampiamente accettata per il calcolo della limitazione funzionale correlata alla perdita dell'udito è quella proposta nel 1979 dall'American Academy of Otolaryngology (AAO) e adottata dall'American Medical Association. Si basa sulla media dei valori ottenuti a 500, a 1,000, a 2,000 ea 3,000 Hz (tabella 1), con il limite inferiore per la limitazione funzionale fissato a 25 dB.
Tabella 1. Calcolo tipico della perdita funzionale da un audiogramma
| Frequenza | |||||||
| 500 Hz |
1,000 Hz |
2,000 Hz |
3,000 Hz |
4,000 Hz |
6,000 Hz |
8,000 Hz |
|
| Orecchio destro (dB) | 25 | 35 | 35 | 45 | 50 | 60 | 45 |
| Orecchio sinistro (dB) | 25 | 35 | 40 | 50 | 60 | 70 | 50 |
| Perdita unilaterale |
| Percentuale perdita unilaterale = (media a 500, 1,000, 2,000 e 3,000 Hz) – 25dB (limite inferiore) x1.5 |
| Esempio: Orecchio destro: [([25 + 35 + 35 + 45]/4) – 25) x 1.5 = 15 (per cento) Orecchio sinistro: [([25 + 35 + 40 + 50]/4) – 25) x 1.5 = 18.8 (per cento) |
| Perdita bilaterale |
| Percentuale di perdita bilaterale = {(percentuale di perdita unilaterale dell'orecchio migliore x 5) + (percentuale di perdita unilaterale dell'orecchio peggiore)}/6 |
| Esempio: {(15 x 5) + 18.8}/6 = 15.6 (per cento) |
Fonte: Rees e Duckert 1994.
Presbiacusia
La presbiacusia o perdita dell'udito legata all'età generalmente inizia intorno ai 40 anni e progredisce gradualmente con l'aumentare dell'età. Di solito è bilaterale. Il caratteristico calo di 4,000 Hz osservato nell'ipoacusia indotta dal rumore non si osserva con la presbiacusia. Tuttavia, è possibile che gli effetti dell'invecchiamento si sovrappongano alla perdita dell'udito dovuta al rumore.
Trattamento
Il primo elemento essenziale del trattamento è evitare qualsiasi ulteriore esposizione a livelli di rumore potenzialmente tossici (vedere "Prevenzione" di seguito). Si ritiene generalmente che dopo la rimozione dall'esposizione al rumore non si verifichi più perdita dell'udito di quanto ci si aspetterebbe dal normale processo di invecchiamento.
Mentre le perdite di conduzione, ad esempio quelle correlate a danni traumatici acuti indotti dal rumore, sono suscettibili di cure mediche o interventi chirurgici, l'ipoacusia cronica indotta dal rumore non può essere corretta dal trattamento. L'uso di un apparecchio acustico è l'unico “rimedio” possibile ed è indicato solo quando l'ipoacusia interessa le frequenze critiche per la comprensione del parlato (da 500 a 3,000 Hz). Altri tipi di supporto, ad esempio la lettura labiale e l'amplificazione del suono (sui telefoni, ad esempio), possono tuttavia essere possibili.
Frodi
Poiché la perdita dell'udito indotta dal rumore è permanente, è essenziale applicare qualsiasi misura in grado di ridurre l'esposizione. Ciò include la riduzione alla fonte (macchine e apparecchiature più silenziose o il loro inserimento in involucri insonorizzati) o l'uso di dispositivi di protezione individuale come tappi per le orecchie e/o cuffie. Se ci si affida a questi ultimi, è imperativo verificare che le dichiarazioni di efficacia dei loro produttori siano valide e che i lavoratori esposti li utilizzino correttamente in ogni momento.
La designazione di 85 dB (A) come limite di esposizione professionale massimo consentito era per proteggere il maggior numero di persone. Tuttavia, poiché esiste una variazione interpersonale significativa, sono indicati sforzi strenui per mantenere le esposizioni ben al di sotto di tale livello. L'audiometria periodica dovrebbe essere istituita come parte del programma di sorveglianza medica per rilevare il prima possibile qualsiasi effetto che possa indicare tossicità da rumore.
Disturbi dell'udito indotti chimicamente
La compromissione dell'udito dovuta alla tossicità cocleare di diversi farmaci è ben documentata (Ryback 1993). Ma fino all'ultimo decennio è stata prestata solo poca attenzione agli effetti audiologici dei prodotti chimici industriali. La recente ricerca sui disturbi dell'udito indotti da sostanze chimiche si è concentrata su solventi, metalli pesanti e sostanze chimiche che inducono anossia.
Solventi. Negli studi sui roditori, è stata dimostrata una diminuzione permanente della sensibilità uditiva ai toni ad alta frequenza dopo settimane di esposizione ad alto livello al toluene. Gli studi sulla risposta istopatologica e uditiva del tronco encefalico hanno indicato un effetto importante sulla coclea con danni alle cellule ciliate esterne. Effetti simili sono stati riscontrati nell'esposizione a stirene, xileni o tricloroetilene. Solfuro di carbonio e n-esano può anche influenzare le funzioni uditive mentre il loro effetto principale sembra essere sulle vie più centrali (Johnson e Nylén 1995).
Diversi casi umani con danni al sistema uditivo insieme a gravi anomalie neurologiche sono stati segnalati a seguito di sniffing di solventi. In caso di serie di persone con esposizione professionale a miscele di solventi, a n-esano o al disolfuro di carbonio, sono stati segnalati effetti sia cocleari che centrali sulle funzioni uditive. L'esposizione al rumore era prevalente in questi gruppi, ma l'effetto sull'udito è stato considerato maggiore del previsto dal rumore.
Finora solo pochi studi controllati hanno affrontato il problema dell'ipoacusia negli esseri umani esposti a solventi senza una significativa esposizione al rumore. In uno studio danese, è stato riscontrato un rischio elevato statisticamente significativo di ipoacusia auto-riferita pari a 1.4 (IC 95%: 1.1-1.9) dopo l'esposizione a solventi per cinque anni o più. In un gruppo esposto sia ai solventi che al rumore, non è stato riscontrato alcun effetto aggiuntivo dall'esposizione ai solventi. Un buon accordo tra la segnalazione di problemi uditivi ei criteri audiometrici per l'ipoacusia è stato trovato in un sottocampione della popolazione in studio (Jacobsen et al. 1993).
In uno studio olandese su lavoratori esposti allo stirene, è stata rilevata mediante audiometria una differenza dose-dipendente nelle soglie uditive (Muijser et al. 1988).
In un altro studio condotto in Brasile, l'effetto audiologico dell'esposizione al rumore, al toluene combinato con il rumore ea solventi misti è stato esaminato nei lavoratori delle industrie di stampa e produzione di vernici. Rispetto a un gruppo di controllo non esposto, sono stati riscontrati rischi significativamente elevati di ipoacusia audiometrica ad alta frequenza per tutti e tre i gruppi di esposizione. Per le esposizioni al rumore e ai solventi misti i rischi relativi erano rispettivamente 4 e 5. Nel gruppo con esposizione combinata a toluene e rumore è stato trovato un rischio relativo di 11, suggerendo un'interazione tra le due esposizioni (Morata et al. 1993).
Metalli. L'effetto del piombo sull'udito è stato studiato in sondaggi su bambini e adolescenti degli Stati Uniti. Una significativa associazione dose-risposta tra piombo nel sangue e soglie uditive a frequenze da 0.5 a 4 kHz è stata trovata dopo aver controllato diversi potenziali fattori confondenti. L'effetto del piombo era presente nell'intero intervallo di esposizione e poteva essere rilevato a livelli di piombo nel sangue inferiori a 10 μg/100 ml. Nei bambini senza segni clinici di tossicità da piombo è stata trovata una relazione lineare tra piombo nel sangue e latenze delle onde III e V nei potenziali uditivi del tronco encefalico (BAEP), indicando un sito di azione centrale rispetto al nucleo cocleare (Otto et al. 1985).
La perdita dell'udito è descritta come una parte comune del quadro clinico nell'avvelenamento acuto e cronico da metilmercurio. Sono state coinvolte sia lesioni cocleari che postcocleari (Oyanagi et al. 1989). Il mercurio inorganico può anche influenzare il sistema uditivo, probabilmente attraverso danni alle strutture cocleari.
L'esposizione all'arsenico inorganico è stata implicata nei disturbi dell'udito nei bambini. È stata osservata un'alta frequenza di ipoacusia grave (>30 dB) in bambini nutriti con latte in polvere contaminato da arsenico inorganico V. In uno studio condotto in Cecoslovacchia, l'esposizione ambientale all'arsenico proveniente da una centrale elettrica a carbone è stata associata a ipoacusia audiometrica nei bambini di dieci anni. Negli esperimenti sugli animali, i composti inorganici dell'arsenico hanno prodotto danni cocleari estesi (WHO 1981).
Nell'avvelenamento acuto da trimetilstagno, la perdita dell'udito e l'acufene sono stati i primi sintomi. L'audiometria ha mostrato una perdita dell'udito pancocleare tra 15 e 30 dB alla presentazione. Non è chiaro se le anomalie siano state reversibili (Besser et al. 1987). Negli esperimenti sugli animali, i composti di trimetilstagno e trietilstagno hanno prodotto danni cocleari parzialmente reversibili (Clerisi et al. 1991).
Asfissianti. Nei rapporti sull'avvelenamento umano acuto da monossido di carbonio o idrogeno solforato, sono stati spesso notati disturbi dell'udito insieme a malattie del sistema nervoso centrale (Ryback 1992).
Negli esperimenti con roditori, l'esposizione al monossido di carbonio ha avuto un effetto sinergico con il rumore sulle soglie uditive e sulle strutture cocleari. Nessun effetto è stato osservato dopo l'esposizione al solo monossido di carbonio (Fechter et al. 1988).
In breve
Studi sperimentali hanno documentato che diversi solventi possono produrre disturbi dell'udito in determinate circostanze di esposizione. Studi sull'uomo hanno indicato che l'effetto può essere presente a seguito di esposizioni comuni nell'ambiente lavorativo. Effetti sinergici tra rumore e sostanze chimiche sono stati osservati in alcuni studi sugli animali umani e sperimentali. Alcuni metalli pesanti possono influenzare l'udito, la maggior parte solo a livelli di esposizione che producono tossicità sistemica evidente. Per il piombo, sono stati osservati effetti minori sulle soglie uditive a esposizioni molto al di sotto dei livelli di esposizione professionale. Uno specifico effetto ototossico degli asfissianti non è stato attualmente documentato, sebbene il monossido di carbonio possa potenziare l'effetto audiologico del rumore.
Disturbi dell'udito di origine fisica
In virtù della sua posizione all'interno del cranio, il sistema uditivo è generalmente ben protetto contro le lesioni causate da forze fisiche esterne. Ci sono, tuttavia, una serie di rischi fisici sul posto di lavoro che possono influenzarlo. Loro includono:
Barotrauma. Improvvise variazioni della pressione barometrica (dovute a una rapida discesa o risalita sottomarina o improvvisa discesa di un aereo) associate al malfunzionamento della tromba di Eustachio (mancata equalizzazione della pressione) possono portare alla rottura della membrana timpanica con dolore ed emorragia nell'orecchio medio ed esterno . Nei casi meno gravi lo stiramento della membrana causerà dolore da lieve a grave. Ci sarà una temporanea menomazione dell'udito (perdita conduttiva), ma generalmente il trauma ha un decorso benigno con completo recupero funzionale.
Vibrazione. L'esposizione simultanea a vibrazioni e rumore (continua o impatto) non aumenta il rischio o la gravità dell'ipoacusia neurosensoriale; tuttavia, il tasso di insorgenza sembra essere aumentato nei lavoratori con sindrome da vibrazione mano-braccio (HAVS). Si presume che la circolazione cocleare sia influenzata dallo spasmo simpatico riflesso, quando tali lavoratori hanno attacchi di vasospasmo (fenomeno di Raynaud) nelle dita delle mani o dei piedi.
Infrasuoni ed ultrasuoni. L'energia acustica proveniente da entrambe queste fonti è normalmente impercettibile per l'uomo. Le fonti comuni di ultrasuoni, ad esempio i motori a reazione, i trapani dentali ad alta velocità, i pulitori e i miscelatori a ultrasuoni emettono tutti un suono udibile, quindi gli effetti degli ultrasuoni sui soggetti esposti non sono facilmente distinguibili. Si presume che sia innocuo al di sotto di 120 dB e quindi improbabile che causi NIHL. Allo stesso modo, il rumore a bassa frequenza è relativamente sicuro, ma con un'intensità elevata (119-144 dB) può verificarsi la perdita dell'udito.
"L'orecchio del saldatore". Le scintille calde possono penetrare nel canale uditivo esterno fino al livello della membrana timpanica, bruciandola. Ciò provoca dolore acuto all'orecchio e talvolta paralisi del nervo facciale. Con ustioni minori, la condizione non richiede alcun trattamento, mentre nei casi più gravi può essere necessaria la riparazione chirurgica della membrana. Il rischio può essere evitato posizionando correttamente l'elmetto del saldatore o indossando tappi per le orecchie.
equilibrio
Funzione del sistema di equilibrio
Ingresso
La percezione e il controllo dell'orientamento e del movimento del corpo nello spazio sono raggiunti da un sistema che coinvolge input simultanei da tre fonti: la visione, l'organo vestibolare nell'orecchio interno e i sensori nei muscoli, nelle articolazioni e nella pelle che forniscono sensori somatosensoriali o "propriocettivi" informazioni sul movimento del corpo e sul contatto fisico con l'ambiente (figura 1). L'input combinato è integrato nel sistema nervoso centrale che genera azioni appropriate per ripristinare e mantenere l'equilibrio, la coordinazione e il benessere. La mancata compensazione in qualsiasi parte del sistema può produrre malessere, vertigini e instabilità che possono produrre sintomi e/o cadute.
Figura 1. Uno schema dei principali elementi del sistema di equilibrio
Il sistema vestibolare registra direttamente l'orientamento e il movimento della testa. Il labirinto vestibolare è una minuscola struttura ossea situata nell'orecchio interno e comprende il canali semicircolari pieno di fluido (endolinfa) e il otoliti (Figura 6). I tre canali semicircolari sono posizionati ad angolo retto in modo da poter rilevare l'accelerazione in ciascuno dei tre possibili piani di moto angolare. Durante i giri della testa, il movimento relativo dell'endolinfa all'interno dei canali (causato dall'inerzia) determina la deflessione del ciglia proiettando dalle cellule sensoriali, inducendo un cambiamento nel segnale neurale da queste cellule (figura 2). Gli otoliti contengono cristalli pesanti (otoconia) che rispondono ai cambiamenti nella posizione della testa rispetto alla forza di gravità e all'accelerazione o decelerazione lineare, piegando nuovamente le ciglia e alterando così il segnale dalle cellule sensoriali a cui sono attaccate.
Figura 2. Diagramma schematico del labirinto vestibolare.
Figura 3. Rappresentazione schematica degli effetti biomeccanici di un'inclinazione della testa di novanta gradi (in avanti).
integrazione
Le interconnessioni centrali all'interno del sistema di equilibrio sono estremamente complesse; le informazioni provenienti dagli organi vestibolari di entrambe le orecchie sono combinate con le informazioni derivate dalla visione e dal sistema somatosensoriale a vari livelli all'interno del tronco encefalico, del cervelletto e della corteccia (Luxon 1984).
Uscita
Questa informazione integrata fornisce la base non solo per la percezione cosciente dell'orientamento e del movimento personale, ma anche per il controllo preconscio dei movimenti oculari e della postura, per mezzo dei cosiddetti riflessi vestibolooculari e vestibolospinali. Lo scopo del riflesso vestibolooculare è mantenere un punto stabile di fissazione visiva durante il movimento della testa compensando automaticamente il movimento della testa con un movimento oculare equivalente nella direzione opposta (Howard 1982). I riflessi vestibolospinali contribuiscono alla stabilità posturale e all'equilibrio (Pompeiano e Allum 1988).
Disfunzione del sistema di equilibrio
In circostanze normali, l'input dai sistemi vestibolare, visivo e somatosensoriale è congruente, ma se si verifica un'apparente discrepanza tra i diversi input sensoriali al sistema dell'equilibrio, il risultato è una sensazione soggettiva di vertigine, disorientamento o senso di movimento illusorio. Se le vertigini sono prolungate o gravi, saranno accompagnate da sintomi secondari come nausea, sudorazione fredda, pallore, stanchezza e persino vomito. L'interruzione del controllo riflesso dei movimenti oculari e della postura può provocare un'immagine visiva sfocata o tremolante, una tendenza a virare su un lato quando si cammina o barcollare e cadere. Il termine medico per il disorientamento causato dalla disfunzione del sistema di equilibrio è "vertigini", che può essere causato da un disturbo di uno qualsiasi dei sistemi sensoriali che contribuiscono all'equilibrio o da un'integrazione centrale difettosa. Solo l'1 o il 2% della popolazione consulta il proprio medico ogni anno a causa delle vertigini, ma l'incidenza di vertigini e squilibri aumenta notevolmente con l'età. La “cinetosi” è una forma di disorientamento indotta da condizioni ambientali artificiali alle quali il nostro sistema di equilibrio non è stato attrezzato dall'evoluzione per far fronte, come il trasporto passivo in auto o in barca (Crampton 1990).
Cause vestibolari di vertigine
Le cause più comuni di disfunzione vestibolare sono l'infezione (vestibolare labirintite or neuronite), E vertigine parossistica posizionale benigna (BPPV) che si attiva principalmente sdraiandosi su un fianco. Attacchi ricorrenti di vertigini gravi accompagnati da perdita dell'udito e rumori (tinnito) in un orecchio sono tipici di una sindrome nota come La malattia di Meniere. Il danno vestibolare può anche derivare da disturbi dell'orecchio medio (incluse malattie batteriche, traumi e colesteatoma), farmaci ototossici (che dovrebbero essere usati solo in caso di emergenza medica) e trauma cranico.
Cause periferiche non vestibolari di vertigine
I disturbi del collo, che possono alterare le informazioni somatosensoriali relative al movimento della testa o interferire con l'afflusso di sangue al sistema vestibolare, sono ritenuti da molti medici una causa di vertigine. Le eziologie comuni includono lesioni da colpo di frusta e artrite. A volte l'instabilità è correlata a una perdita di sensibilità nei piedi e nelle gambe, che può essere causata da diabete, abuso di alcol, carenza di vitamine, danni al midollo spinale o una serie di altri disturbi. Occasionalmente l'origine di sensazioni di vertigine o movimento illusorio dell'ambiente può essere ricondotta a qualche distorsione dell'input visivo. Un input visivo anormale può essere causato dalla debolezza dei muscoli oculari o può essere sperimentato quando ci si adatta a lenti potenti o occhiali bifocali.
Cause centrali di vertigine
Sebbene la maggior parte dei casi di vertigine sia attribuibile a patologia periferica (principalmente vestibolare), i sintomi di disorientamento possono essere causati da danni al tronco encefalico, al cervelletto o alla corteccia. La vertigine dovuta a disfunzione centrale è quasi sempre accompagnata da qualche altro sintomo di disturbo neurologico centrale, come sensazioni di dolore, formicolio o intorpidimento del viso o degli arti, difficoltà a parlare o deglutire, mal di testa, disturbi visivi e perdita o perdita del controllo motorio di coscienza. Le cause centrali più comuni di vertigini includono disturbi dell'afflusso di sangue al cervello (che vanno dall'emicrania all'ictus), epilessia, sclerosi multipla, alcolismo e occasionalmente tumori. Vertigini e squilibri temporanei sono un potenziale effetto collaterale di una vasta gamma di farmaci, inclusi analgesici, contraccettivi e farmaci ampiamente utilizzati per il controllo delle malattie cardiovascolari, del diabete e del morbo di Parkinson, e in particolare dei farmaci ad azione centrale come stimolanti, sedativi, anticonvulsivanti, antidepressivi e tranquillanti (Ballantyne e Ajodhia 1984).
Diagnosi e trattamento
Tutti i casi di vertigine richiedono cure mediche per garantire che le condizioni pericolose (relativamente non comuni) che possono causare vertigini vengano rilevate e venga somministrato un trattamento appropriato. I farmaci possono essere somministrati per alleviare i sintomi della vertigine acuta a breve termine e, in rari casi, può essere necessario un intervento chirurgico. Tuttavia, se la vertigine è causata da un disturbo vestibolare, i sintomi generalmente si attenuano nel tempo man mano che gli integratori centrali si adattano allo schema alterato dell'input vestibolare, allo stesso modo in cui i marinai continuamente esposti al moto delle onde acquisiscono gradualmente le loro "gambe di mare". ”. Perché ciò avvenga, è essenziale continuare a fare movimenti vigorosi che stimolino il sistema dell'equilibrio, anche se questi inizialmente causeranno vertigini e disagio. Poiché i sintomi della vertigine sono spaventosi e imbarazzanti, i malati possono aver bisogno di fisioterapia e supporto psicologico per combattere la naturale tendenza a limitare le loro attività (Beyts 1987; Yardley 1994).
Vertigini sul posto di lavoro
Fattori di rischio
Vertigini e disorientamento, che possono diventare cronici, sono un sintomo comune nei lavoratori esposti a solventi organici; inoltre, l'esposizione a lungo termine può provocare segni oggettivi di disfunzione del sistema di equilibrio (ad esempio, controllo del riflesso vestibolare-oculare anormale) anche in persone che non presentano vertigini soggettive (Gyntelberg et al. 1986; Möller et al. 1990). I cambiamenti di pressione incontrati durante il volo o le immersioni possono causare danni all'organo vestibolare che si traduce in improvvise vertigini e perdita dell'udito che richiedono un trattamento immediato (Head 1984). Ci sono alcune prove che la perdita dell'udito indotta dal rumore può essere accompagnata da danni agli organi vestibolari (van Dijk 1986). Le persone che lavorano per lunghi periodi davanti agli schermi dei computer a volte lamentano vertigini; la causa di ciò rimane poco chiara, sebbene possa essere correlata alla combinazione di torcicollo e input visivo in movimento.
Difficoltà occupazionali
Attacchi inaspettati di vertigini, come quelli che si verificano nella malattia di Menière, possono causare problemi alle persone il cui lavoro comporta altezze, guida, manipolazione di macchinari pericolosi o responsabilità per la sicurezza degli altri. Una maggiore suscettibilità alla cinetosi è un effetto comune della disfunzione del sistema di equilibrio e può interferire con il viaggio.
Conclusione
L'equilibrio è mantenuto da un complesso sistema multisensoriale, e quindi il disorientamento e lo squilibrio possono derivare da un'ampia varietà di eziologie, in particolare qualsiasi condizione che colpisce il sistema vestibolare o l'integrazione centrale delle informazioni percettive per l'orientamento. In assenza di danno neurologico centrale, la plasticità del sistema di equilibrio consentirà normalmente all'individuo di adattarsi a cause periferiche di disorientamento, sia che si tratti di disturbi dell'orecchio interno che alterano la funzione vestibolare, sia di ambienti che provocano cinetosi. Tuttavia, gli attacchi di vertigini sono spesso imprevedibili, allarmanti e invalidanti e può essere necessaria la riabilitazione per ripristinare la fiducia e aiutare la funzione dell'equilibrio.
" DISCLAIMER: L'ILO non si assume alcuna responsabilità per i contenuti presentati su questo portale Web presentati in una lingua diversa dall'inglese, che è la lingua utilizzata per la produzione iniziale e la revisione tra pari del contenuto originale. Alcune statistiche non sono state aggiornate da allora la produzione della 4a edizione dell'Enciclopedia (1998)."