Kinder Kategorien

1. Blut (3)

1. Blut
Kapitel-Editor: Bernhard D. Goldstein
Inhaltsverzeichnis
Tische
Hämatopoetisches und lymphatisches System
Bernhard D. Goldstein
Leukämie, maligne Lymphome und multiples Myelom
Timo Partanen, Paolo Boffetta, Elisabete Weiderpass
Agenten oder Arbeitsbedingungen, die das Blut beeinflussen
Bernhard D. Goldstein
Tische
Klicken Sie unten auf einen Link, um die Tabelle im Artikelkontext anzuzeigen.

2. Krebs (4)

2. Krebs
Kapitel-Editor: Paolo Bofetta
Tisch des Inhalts
Tische
Einleitung
Neil Pearce, Paolo Boffetta und Manolis Kogevinas
Berufliche Karzinogene
Paolo Boffetta, Rodolfo Saracci, Manolis Kogevinas, Julian Wilbourn und Harri Vainio
Umweltkrebs
Bruce K. Armstrong und Paolo Boffetta
abwehr
Per Gustavsson
Tische
Klicken Sie unten auf einen Link, um die Tabelle im Artikelkontext anzuzeigen.
- Berufsbedingter Krebs: Wichtige Fakten
- Geschätzte Anteile von Krebserkrankungen (PAR), die auf Berufe zurückzuführen sind
- Bewertung von Hinweisen auf Karzinogenität in den IARC-Monographien
- Klassifikationsgruppen des IARC-Monographieprogramms
- Gruppe 1-Chemikalien krebserzeugend für den Menschen
- Gruppe 2A – Chemikalien, die wahrscheinlich krebserzeugend für den Menschen sind
- Gruppe 2B – Chemikalien, die für Menschen möglicherweise krebserregend sind
- In IARC-Monographien, Bände 1-63 (1972-1995) bewertete Pestizide
- Arzneimittel, die in den IARC-Monographien, Bände 1-63 (1972-1995) bewertet wurden
- Umwelteinflüsse/Expositionen, von denen bekannt ist oder vermutet wird, dass sie Krebs beim Menschen verursachen
- Branchen, Berufe, Expositionen, die ein krebserzeugendes Risiko darstellen
- Branchen, Berufe, exp. mit Krebsüberschuss nicht definitive Karzinogene
- Registrierte Bevölkerungsvariationen der Inzidenz einiger häufiger Krebsarten

3. Herz-Kreislauf-System (7)

3. Herz-Kreislauf-System
Kapitel-Editoren: Lothar Heinemann und Gerd Heuchert
Inhaltsverzeichnis
Tabellen und Abbildungen
Einleitung
Lothar Heinemann und Gerd Heuchert
Kardiovaskuläre Morbidität und Mortalität in der Belegschaft
Gottfried Enderlein und Lothar Heinemann
Das Risikofaktorkonzept bei Herz-Kreislauf-Erkrankungen
Lothar Heinemann, Gottfried Enderlein und Heide Stark
Rehabilitations- und Präventionsprogramme
Lothar Heinemann und Gottfried Enderlein
Physikalische, chemische und biologische Gefahren
Physische Faktoren
Heide Stark und Gerd Heuchert
Chemische Gefahrstoffe
Ulrike Tittelbach und Wolfram Dietmar Schneider
Biologische Gefahren
Regina Jäckel, Ulrike Tittelbach und Wolfram Dietmar Schneider
Tische
Klicken Sie unten auf einen Link, um die Tabelle im Artikelkontext anzuzeigen
- Sterblichkeit durch Herz-Kreislauf-Erkrankungen
- Sterblichkeitsraten, spezielle kardiovaskuläre Diagnosegruppen
- Krankheitsrate und verminderte Arbeitsfähigkeit
- Arbeiten im Zusammenhang mit Herz-Kreislauf-Gefahren
- Berufsbedingte Infektionen und Krankheiten
Zahlen
Zeigen Sie auf eine Miniaturansicht, um die Bildunterschrift anzuzeigen, klicken Sie, um die Abbildung im Artikelkontext anzuzeigen.

4. Verdauungssystem (6)

4. Verdauungssystem
Kapitel-Editor: Heikki Savolainen
Inhaltsverzeichnis
Zahlen
Verdauungssystem
G. Frada
Mund und Zähne
F. Gobbato
Leber
Georg Kazantzis
Magengeschwür
KS Cho
Leberkrebs
Timo Partanen, Timo Kauppinen, Paolo Boffetta und Elisabete Weiderpass
Bauchspeicheldrüsenkrebs
Timo Partanen, Timo Kauppinen, Paolo Boffetta und Elisabete Weiderpass
Zahlen
Zeigen Sie auf eine Miniaturansicht, um die Bildunterschrift anzuzeigen, klicken Sie, um die Abbildung im Artikelkontext anzuzeigen.

5. Psychische Gesundheit (8)

5. Psychische Gesundheit
Herausgeber des Kapitels: Joseph J. Hurrell, Lawrence R. Murphy, Steven L. Sauter und Lennart Levi
Inhaltsverzeichnis
Tabellen und Abbildungen
Arbeit und psychische Gesundheit
Irene LD Houtman und Michiel AJ Kompier
Arbeitsbedingte Psychose
Craig Stenberg, Judith Holder und Krishna Tallur
Stimmung und Affekt
Reduzierung des Depressionsrisikos
Jay Lasser und Jeffrey P. Kahn
Arbeitsbedingte Angst
Randal D. Beaton
Posttraumatische Belastungsstörung und ihre Beziehung zur Arbeitsmedizin und Verletzungsprävention
Markus Braverman
Stress und Burnout und ihre Auswirkungen auf die Arbeitsumgebung
Herbert J. Freudenberger
Kognitive Störungen
Catherine A. Heaney
Karoshi: Tod durch Überarbeitung
Takashi Haratani
Tische
Klicken Sie unten auf einen Link, um die Tabelle im Artikelkontext anzuzeigen.
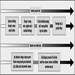
1. Schematischer Überblick über Managementstrategien & Beispiele
Zahlen
Zeigen Sie auf eine Miniaturansicht, um die Bildunterschrift anzuzeigen, klicken Sie, um die Abbildung im Artikelkontext anzuzeigen.

6. Bewegungsapparat (14)

6. Bewegungsapparat
Herausgeber des Kapitels: Hilkka Riihimäki und Eira Viikari-Juntura
Inhaltsverzeichnis
Tabellen und Abbildungen
Überblick
Hilkka Riihimäki
Muskeln
Gisela Sjögaard
Sehnen
Thomas J. Armstrong
Knochen und Gelenke
David Hammermann
Bandscheiben
Sally Roberts und Jill PG Urban
Region des unteren Rückens
Hilkka Riihimäki
Region der Brustwirbelsäule
Jarl-Erik Michelsson
Hals
Asa Kilbom
Ansatzscheiben
Mats Hagberg
Elbow
Eira Viikari-Juntura
Unterarm, Handgelenk und Hand
Eira Viikari-Juntura
Hüfte und Knie
Eva Vingård
Bein, Knöchel und Fuß
Jarl-Erik Michelsson
Andere Krankheiten
Marjatta Leirisalo-Repo
Tische
Klicken Sie unten auf einen Link, um die Tabelle im Artikelkontext anzuzeigen.
- Struktur-Funktion von Gelenkkomponenten
- Prävalenz von Rückenerkrankungen bei Finnen über 30 Jahren
- Verringerung des Risikos für Rückenschmerzen bei der Arbeit
- Klassifikation von Erkrankungen des unteren Rückens (Quebec Task Force)
- Zulässige Kopfbewegungen bei längerem Fahren
- Inzidenz von Epicondylitis in verschiedenen Populationen
- Auftreten von Tenosynovitis/Peritendinitis
- Primäre Osteoarthrose der Hüfte in Malmö, Schweden
- Richtlinien für die Behandlung von rheumatoider Arthritis
- Infektionen, von denen bekannt ist, dass sie reaktive Arthritis auslösen
Zahlen
Zeigen Sie auf eine Miniaturansicht, um die Bildunterschrift anzuzeigen, klicken Sie, um die Abbildung im Artikelkontext anzuzeigen.

7. Nervensystem (9)

7. Nervensystem
Kapitel-Editor: Donna Mergler
Inhaltsverzeichnis
Tabellen und Abbildungen
Nervensystem: Überblick
Donna Mergler und José A. Valciukas
Anatomie und Physiologie
José A. Valciukas
Chemische neurotoxische Mittel
Peter Arlien-Søborg und Leif Simonsen
Manifestationen akuter und früher chronischer Vergiftungen
Donna Mergler
Neurotoxizität am Arbeitsplatz verhindern
Barry Johnson
Klinische Syndrome im Zusammenhang mit Neurotoxizität
Robert G. Feldmann
Messung neurotoxischer Defizite
Donna Mergler
Diagnose
Anna Maria Seppäläinen
Berufliche Neuroepidemiologie
Olaf Axelson
Tische
Klicken Sie unten auf einen Link, um die Tabelle im Artikelkontext anzuzeigen.
- Namen und Hauptfunktionen der einzelnen Hirnnervenpaare
- Gruppierung neurotoxischer Wirkungen nach Neurotoxizität
- Gase, die mit neurotoxischen Wirkungen in Verbindung gebracht werden
- Neurotoxische Metalle und ihre anorganischen Verbindungen
- Neurotoxische Monomere
- Organische Lösungsmittel im Zusammenhang mit Neurotoxizität
- Klassen gängiger neurotoxischer Pestizide
- Andere Chemikalien, die mit Neurotoxizität in Verbindung gebracht werden
- Checkliste für chronische Symptome
- Neurofunktionelle Wirkungen der Exposition gegenüber einigen Neurotoxinen
- Chemische Belastungen und damit verbundene neurotoxische Syndrome
- Einige „Core“-Batterien zur Bewertung früher neurotoxischer Wirkungen
- Entscheidungsbaum für neurotoxische Erkrankungen
- Konsistente neurofunktionelle Wirkungen von Expositionen am Arbeitsplatz gegenüber einigen führenden neurotoxischen Substanzen
Zahlen
Zeigen Sie auf eine Miniaturansicht, um die Bildunterschrift anzuzeigen, klicken Sie, um die Abbildung im Artikelkontext anzuzeigen.

8. Nieren-Harn-System (2)

8. Nieren-Harn-System
Kapitel-Editor: George P. Hemstreet
Inhaltsverzeichnis
Tabellen und Abbildungen
Nieren-Harn-Systeme
George P. Hemstreet
Nieren-Harnkrebs
Timo Partanen, Harri Vainio, Paolo Boffetta und Elisabete Weiderpass
Tische
Klicken Sie unten auf einen Link, um die Tabelle im Artikelkontext anzuzeigen.
- Enzyme des Arzneimittelstoffwechsels in der Niere
- Die häufigsten Ursachen für Hämaturie, nach Alter und Geschlecht
- Kriterien für die Auswahl von Biomarkern
- Potenzielle Biomarker im Zusammenhang mit Zellverletzungen
- Akute Niereninsuffizienz & Beruf
- Segmente des Nephrons, die von ausgewählten Giftstoffen betroffen sind
- Anwendungen der Harnzytologie
Zahlen
Zeigen Sie auf eine Miniaturansicht, um die Bildunterschrift anzuzeigen, klicken Sie, um die Abbildung im Artikelkontext anzuzeigen.

9. Fortpflanzungssystem (9)

9. Fortpflanzungssystem
Kapitel-Editor: Grace Kawas Lemasters
Inhaltsverzeichnis
Tabellen und Abbildungen
Fortpflanzungssystem: Einführung
Lowell E. Sever
Einführung in die männliche und weibliche Fortpflanzungsfunktion
Donald R. Mattison
Männliches Fortpflanzungssystem und Toxikologie
Steven Schrader und Grace Kawas Lemasters
Struktur des weiblichen Fortpflanzungssystems und Anfälligkeit für Zielorgane
Donald R. Mattison
Berufsbedingte Expositionen von Müttern und unerwünschte Schwangerschaftsergebnisse
Grace Kawas Lemasters
Frühgeburt und Arbeit
Nicole Mamelle
Berufliche und umweltbedingte Belastungen des Neugeborenen
Mary S. Wolff und Patrisha M. Woolard
Mutterschutz in der Gesetzgebung
Marie-Claire Séguret
Schwangerschaft und US-Arbeitsempfehlungen
Leon J. Warschau
Tische
Klicken Sie unten auf einen Link, um die Tabelle im Artikelkontext anzuzeigen.
1. Expositionen mit mehreren unerwünschten Endpunkten
2. Epidemiologische Studien zu väterlichen Auswirkungen auf den Schwangerschaftsausgang
3. Potenzielle Giftstoffe für die weibliche Fortpflanzung
4. Definition von fetalem Verlust und Kindstod
5. Faktoren für klein für Gestationsalter und fetalen Verlust
6. Identifizierte Ursachen für Ermüdung am Arbeitsplatz
7. Relative Risiken und Ermüdungsindizes für Frühgeburten
8. Frühgeburtlichkeitsrisiko nach Anzahl der Berufsmüdigkeitsindizes
9. Relative Risiken und Änderungen der Arbeitsbedingungen
10 Expositionsquellen und -niveaus für Neugeborene
Zahlen
Zeigen Sie auf eine Miniaturansicht, um die Bildunterschrift anzuzeigen, klicken Sie, um die Abbildung im Artikelkontext anzuzeigen.

10. Atmungssystem (18)

10. Atmungssystem
Kapitel-Editoren: Alois David und Gregory R. Wagner
Inhaltsverzeichnis
Tabellen und Abbildungen
Struktur und Funktion
Morton Lippmann
Lungenfunktionsuntersuchung
Ulf Ulfvarson und Monica Dahlqvist
Krankheiten, die durch Reizstoffe der Atemwege und giftige Chemikalien verursacht werden
David LS Ryon und William N. Rom
Berufsbedingtes Asthma
George Friedman-Jimenez und Edward L. Petsonk
Krankheiten durch organische Stäube
Ragnar Rylander und Richard SF Schilling
Beryllium-Krankheit
Homayoun Kazemi
Pneumokoniose: Definition
Alois David
Internationale ILO-Klassifikation von Röntgenbildern von Pneumokoniosen
Michel Leage
Ätiopathogenese von Pneumokoniosen
Patrick Sébastien und Raymond Bégin
Silikose
John E. Parker und Gregory R. Wagner
Lungenerkrankungen der Kohlenarbeiter
Michael D. Attfield, Edward L. Petsonk und Gregory R. Wagner
Asbestbedingte Krankheiten
Margaret R. Becklake
Hartmetallkrankheit
Gerolamo Chiappino
Atmungssystem: Die Vielfalt der Pneumokoniosen
Steven R. Short und Edward L. Petsonk
Chronisch obstruktive Lungenerkrankung
Kazimierz Marek und Jan E. Zejda
Gesundheitliche Auswirkungen von Chemiefasern
James E. Lockey und Clara S. Ross
Atemwegskrebs
Paolo Boffetta und Elisabete Weiderpass
Berufsbedingt erworbene Lungeninfektionen
Anthony A. Marfin, Ann F. Hubbs, Karl J. Musgrave und John E. Parker
Tische
Klicken Sie unten auf einen Link, um die Tabelle im Artikelkontext anzuzeigen.
1. Atemwegsregionen und Partikelablagerungsmodelle
2. Kriterien für einatembaren, thorakalen und lungengängigen Staub
3. Zusammenfassung der Atemwegsreizstoffe
4. Mechanismen der Lungenschädigung durch eingeatmete Substanzen
5. Lungentoxische Verbindungen
6. Medizinische Falldefinition von Berufsasthma
7. Schritte zur Diagnostik von Asthma am Arbeitsplatz
8. Allergene, die Berufsasthma verursachen können
9. Beispiele für Gefahrenquellen bei der Exposition gegenüber organischem Staub
10 Wirkstoffe in organischen Stäuben mit potenzieller biologischer Aktivität
11 Durch organische Stäube verursachte Krankheiten und ihre ICD-Codes
12 Diagnostische Kriterien für Byssinose
13 Eigenschaften von Beryllium und seinen Verbindungen
14 Beschreibung von Standard-Röntgenbildern
15 ILO 1980-Klassifikation: Röntgenaufnahmen von Pneumokoniosen
16 Asbestbedingte Krankheiten und Zustände
17 Wichtigste kommerzielle Quellen, Produkte und Verwendungen von Asbest
18 Prävalenz von COPD
19 Risikofaktoren bei COPD
20 Verlust der Atemfunktion
21 Diagnostische Klassifikation, chronische Bronchitis & Emphysem
22 Lungenfunktionstest bei COPD
23 Synthetische Fasern
24 Etablierte humane respiratorische Karzinogene (IARC)
25 Wahrscheinliche Karzinogene der menschlichen Atemwege (IARC)
26 Beruflich erworbene respiratorische Infektionskrankheiten
Zahlen
Zeigen Sie auf eine Miniaturansicht, um die Bildunterschrift anzuzeigen, klicken Sie, um die Abbildung im Artikelkontext anzuzeigen.

11. Sensorische Systeme (8)

11. Sensorische Systeme
Kapitel-Editor: Heikki Savolainen
Inhaltsverzeichnis
Tabellen und Abbildungen
Das Ohr
Marcel-André Boillat
Chemisch induzierte Hörstörungen
Peter Jakobsen
Körperlich bedingte Hörstörungen
Peter L. Pelmear
Gleichgewicht
Lucy Yardley
Vision und Arbeit
Paule Rey und Jean-Jacques Meyer
Genieße
April E. Mott und Norman Mann
Geruch
April E. Mott
Kutane Rezeptoren
Robert Dykes und Daniel McBain
Tische
Klicken Sie unten auf einen Link, um die Tabelle im Artikelkontext anzuzeigen.
1. Typische Berechnung des Funktionsverlustes aus einem Audiogramm
2. Visuelle Anforderungen für verschiedene Aktivitäten
3. Empfohlene Beleuchtungsstärkewerte für die Lichtplanung
4. Sehanforderungen für einen Führerschein in Frankreich
5. Wirkstoffe/Prozesse, von denen berichtet wird, dass sie das Geschmackssystem verändern
6. Agenten/Prozesse im Zusammenhang mit olfaktorischen Anomalien
Zahlen
Zeigen Sie auf eine Miniaturansicht, um die Bildunterschrift anzuzeigen, klicken Sie, um die Abbildung im Artikelkontext anzuzeigen.

12. Hautkrankheiten (7)

12. Hautkrankheiten
Kapitel-Editor: Louis-Philippe Durocher
Inhaltsverzeichnis
Tabellen und Abbildungen
Überblick: Berufsbedingte Hautkrankheiten
Donald J. Birmingham
Nicht-melanozytärer Hautkrebs
Elisabete Weiderpass, Timo Partanen, Paolo Boffetta
Malignes Melanom
Timo Partanen, Paolo Boffetta, Elisabete Weiderpass
Kontaktdermatitis am Arbeitsplatz
Denis Sasseville
Prävention von Berufsdermatosen
Louis-Phillipe Durocher
Berufsbedingte Nageldystrophie
CD Calnan
Stigmata
H. Mierzecki
Tische
Klicken Sie unten auf einen Link, um die Tabelle im Artikelkontext anzuzeigen.
1. Gefährdete Berufe
2. Arten von Kontaktdermatitis
3. Häufige Reizstoffe
4. Häufige Hautallergene
5. Prädisponierende Faktoren für Berufsdermatitis
6. Beispiele für Hautreizstoffe und -sensibilisatoren mit Berufen
7. Berufliche Dermatosen in Quebec im Jahr 1989
8. Risikofaktoren & ihre Auswirkungen auf die Haut
9. Kollektive Maßnahmen (Gruppenansatz) zur Prävention
Zahlen
Zeigen Sie auf eine Miniaturansicht, um die Bildunterschrift anzuzeigen, klicken Sie, um die Abbildung im Artikelkontext anzuzeigen.

13. Systemische Bedingungen (3)

13. Systemische Bedingungen
Kapitel-Editor: Howard M. Kipen
Inhaltsverzeichnis
Zahlen
Systemische Bedingungen: Eine Einführung
Howard M. Kipen
Krankheitsbildendes Syndrom
Michael J. Hodgson
Mehrere chemische Empfindlichkeiten
Mark R. Cullen
Zahlen
Zeigen Sie auf eine Miniaturansicht, um die Bildunterschrift anzuzeigen, klicken Sie, um die Abbildung im Artikelkontext anzuzeigen.
Nervensystem: Überblick
Kenntnisse des Nervensystems im Allgemeinen und des Gehirns und des menschlichen Verhaltens im Besonderen sind von größter Bedeutung für diejenigen, die sich für eine sichere und gesunde Umwelt einsetzen. Arbeitsbedingungen und Expositionen, die sich direkt auf die Gehirnfunktionen auswirken, beeinflussen den Geist und das Verhalten. Um Informationen auszuwerten, Entscheidungen zu treffen und konsequent und angemessen auf Wahrnehmungen der Welt zu reagieren, ist es erforderlich, dass das Nervensystem ordnungsgemäß funktioniert und dass das Verhalten nicht durch gefährliche Umstände wie Unfälle (z Leiter) oder Exposition gegenüber gefährlichen Mengen an neurotoxischen Chemikalien.
Eine Schädigung des Nervensystems kann zu Veränderungen des sensorischen Inputs führen (Verlust des Sehvermögens, des Gehörs, des Geruchssinns usw.), die Fähigkeit zur Steuerung von Bewegungen und Körperfunktionen beeinträchtigen und/oder die Fähigkeit des Gehirns, Informationen zu verarbeiten oder zu speichern, beeinträchtigen. Darüber hinaus kann eine veränderte Funktion des Nervensystems Verhaltens- oder psychische Störungen verursachen. Stimmungs- und Persönlichkeitsveränderungen treten häufig nach körperlichen oder organischen Schädigungen des Gehirns auf. Während sich unser Wissen entwickelt, erfahren wir mehr darüber, wie Prozesse des Nervensystems modifiziert werden. Neurotoxische Substanzen können die natürliche Barriere des Gehirns überwinden und direkt in seine komplizierten Funktionen eingreifen. Obwohl einige Substanzen eine besondere Affinität zu bestimmten Bereichen des Nervensystems haben, haben die meisten Neurotoxine weitreichende Wirkungen und zielen auf Zellprozesse ab, die am Membrantransport, internen zellulären chemischen Reaktionen, der Freisetzung sekretorischer Substanzen usw. beteiligt sind.
Schäden an den verschiedenen Komponenten des Nervensystems können auf unterschiedliche Weise auftreten:
- direkte Körperverletzung durch herabfallende Gegenstände, Kollisionen, Schläge oder übermäßigen Druck auf die Nerven
- Veränderungen in der inneren Umgebung, wie z. B. unzureichender Sauerstoff aufgrund von Erstickungsanfällen und Hitzeeinwirkung
- Eingriff in die zellulären Prozesse durch chemische Einwirkung von Substanzen wie Metallen, organischen Lösungsmitteln und Pestiziden
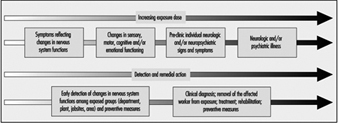
Die schleichende und facettenreiche Entwicklung vieler Erkrankungen des Nervensystems erfordert von Personen, die auf dem Gebiet der Arbeitsmedizin arbeiten, unterschiedliche, aber komplementäre Ansätze für das Studium, das Verständnis, die Prävention und die Behandlung des Problems. Frühe Veränderungen können in Gruppen von aktiven, exponierten Arbeitern mit sensitiven Maßen der Beeinträchtigung festgestellt werden. Die Identifizierung einer anfänglichen Funktionsstörung kann zu vorbeugenden Maßnahmen führen. In den letzten Stadien sind gute klinische Kenntnisse erforderlich, und die Differentialdiagnose ist für die angemessene Behandlung und Betreuung behinderter Arbeitnehmer unerlässlich.
Obwohl chemische Substanzen meistens einzeln untersucht werden, sollte nicht vergessen werden, dass an vielen Arbeitsplätzen Mischungen potenziell neurotoxischer Chemikalien verwendet werden, wodurch die Arbeitnehmer einem sogenannten „Cocktail“ ausgesetzt werden. Bei Prozessen wie Drucken, Lackieren, Reinigen, in schlecht belüfteten Büros, in Labors, beim Ausbringen von Pestiziden, in der Mikroelektronik und vielen anderen Bereichen sind Arbeiter chemischen Gemischen ausgesetzt. Obwohl möglicherweise Informationen über jede der Substanzen separat vorliegen, müssen wir die kombinierte Nozitivität und mögliche additive oder sogar synergistische Wirkungen auf das Nervensystem berücksichtigen. In einigen Fällen von Mehrfachexposition kann jede einzelne Chemikalie in sehr geringer Menge vorhanden sein, sogar unterhalb der Nachweisgrenze von Techniken zur Expositionsbewertung; Wenn jedoch alle zusammenaddiert werden, kann die Gesamtkonzentration sehr hoch sein.
Der Leser sollte sich dreier Hauptschwierigkeiten bei der Überprüfung von Fakten über das Nervensystem in diesem Rahmen bewusst sein Enzyklopädie.
Erstens hat sich das Verständnis von Berufskrankheiten, die das Nervensystem und das Verhalten beeinträchtigen, wesentlich verändert, da neue Ansätze zur Betrachtung von Gehirn-Verhaltens-Beziehungen entwickelt wurden. Dem Hauptinteresse der Charakterisierung grober morphologischer Veränderungen, die aufgrund mechanischer Traumata des Nervensystems – insbesondere, aber nicht ausschließlich des Gehirns – auftreten, folgte ein Interesse an der Absorption neurotoxischer Mittel durch das Nervensystem; Interesse am Studium zellulärer Mechanismen der Pathologie des Nervensystems; und schließlich begann die Suche nach den molekularen Grundlagen dieser pathologischen Prozesse zu wachsen. Diese Ansätze existieren heute nebeneinander und alle tragen Informationen zur Bewertung der Arbeitsbedingungen bei, die sich auf das Gehirn, den Geist und das Verhalten auswirken.
Zweitens sind die von Neurowissenschaftlern generierten Informationen überwältigend. Die dritte Auflage des Buches Prinzipien der Neurowissenschaften herausgegeben von Kandel, Schwartz und Kessell, das 1991 erschien – eine der wertvollsten Übersichten auf diesem Gebiet – wiegt 3.5 kg und ist mehr als 1,000 Seiten lang.
Drittens ist es sehr schwierig, das Wissen über die funktionelle Organisation des Nervensystems zu überprüfen, da es für alle Nischen des Arbeitsschutzes gilt. Bis vor etwa 25 Jahren überschnitten sich die theoretischen Ansichten, die die betroffenen Gesundheitsexperten unterstützten, die sich auf die Erkennung, Überwachung, Vorbeugung und klinische Behandlung eines Arbeitnehmers spezialisiert haben, der ein neurotoxisches Mittel aufgenommen hat, manchmal nicht mit den theoretischen Ansichten über die Hirntrauma und die Verhaltensmanifestationen minimaler Hirnschäden. Verhaltensmanifestationen, die angeblich die Folge der Störung spezifischer chemischer Bahnen im Gehirn waren, waren das ausschließliche Gebiet des Neurotoxikologen; Sowohl strukturelle Gewebeschäden bestimmter Regionen des Gehirns als auch entfernte neurale Strukturen, die mit dem Bereich verbunden sind, in dem die Läsionen auftraten, waren Erklärungen, die von Neurologen angeführt wurden. Erst in den letzten Jahren tauchen konvergierende Ansichten auf.
Vor diesem Hintergrund befasst sich dieses Kapitel mit Fragen, die für das Verständnis des Nervensystems und der Auswirkungen der Arbeitsplatzbedingungen auf seine Funktion wichtig sind. Es beginnt mit einer Beschreibung der Anatomie und Physiologie, gefolgt von einem Abschnitt über Neurotoxizität, der Exposition, Folgen und Prävention behandelt.
Da das Nervensystem für das Wohlbefinden des Körpers von zentraler Bedeutung ist, können viele nicht-chemische Gefahren ebenfalls seine normale Funktion beeinträchtigen. Viele davon werden in verschiedenen Kapiteln behandelt, die sich mit diesen Gefahren befassen. Traumatische Kopfverletzungen gehören dazu Erste Hilfe, Hitzestress wird im Artikel „Auswirkungen von Hitzestress und Arbeit in der Hitze“ behandelt, und die Dekompressionskrankheit wird im Artikel „Schwerkraftstress“ behandelt. Hand-Arm-Vibration („Von der Hand übertragene Vibration“) und sich wiederholende Bewegungen („Chronische Folgen, Bewegungsapparat“) im Kapitel Bewegungsapparat, die Risikofaktoren für periphere Neuropathien sind, werden in diesen Abschnitten ebenfalls berücksichtigt Enzyklopädie.
Das Kapitel endet mit einem Rückblick auf spezielle Fragestellungen und einem Ausblick auf zukünftige Forschungsansätze.
Anatomie und Physiologie
Nervenzellen sind die funktionellen Einheiten des Nervensystems. Es wird angenommen, dass das Nervensystem über zehn Milliarden solcher Zellen verfügt, die sog Neuronen und Glia, wobei die Glia in größerer Zahl als Neuronen vorhanden ist.
Das Neuron
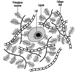
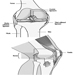
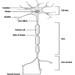
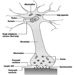
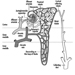
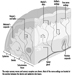
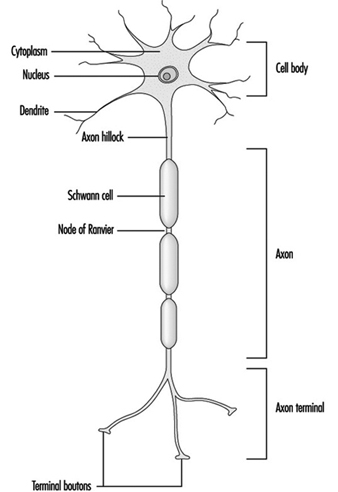
Abbildung 1 ist ein idealisiertes Diagramm eines Neurons mit seinen drei wichtigsten Strukturmerkmalen: dem Zellkörper, den Dendriten und dem Axonterminal.
Abbildung 1. Die Anatomie des Neurons
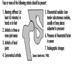
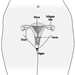
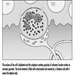
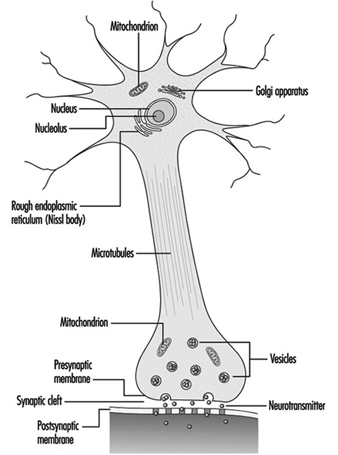
Die Dendriten sind fein verzweigte Fortsätze, die in der Nähe des Zellkörpers eines Neurons entstehen. Über chemische Botenstoffe, sogenannte Neurotransmitter, erhalten die Dendriten erregende oder hemmende Wirkungen. Das Zytoplasma ist das Material des Zellkörpers, in dem sich die Organellen – einschließlich des Zellkerns – und andere Einschlüsse befinden Abbildung 2. Der Zellkern enthält das Chromatin oder genetisches Material der Zelle.
Abbildung 2. Die Organellen
Der Zellkern der Nervenzelle ist im Vergleich zu anderen lebenden Zellen insofern untypisch, als er zwar die Erbsubstanz Desoxyribonukleinsäure (DNA) enthält, die DNA aber nicht am Prozess der Zellteilung beteiligt ist; das heißt, nach Erreichen der Reife teilen sich Nervenzellen nicht. (Eine Ausnahme von dieser Regel sind die Neuronen in der Nasenschleimhaut (olfaktorisches Epithel).) Der Zellkern ist reich an Ribonukleinsäure (RNA), die für die Proteinsynthese notwendig ist. Drei Arten von Proteinen wurden identifiziert: zytosolische Proteine, die die fibrillären Elemente der Nervenzelle bilden; intrakondriale Proteine, die Energie für die Zellaktivität erzeugen; und Proteine, die Membranen und sekretorische Produkte bilden. Neuronen werden heute als modifizierte sekretorische Zellen betrachtet. Es werden sekretorische Granula gebildet, in synaptischen Vesikeln gespeichert und später als Neurotransmittersubstanzen, die chemischen Botenstoffe zwischen Nervenzellen, freigesetzt.
Die fibrillären Elemente, die das Skelett des Neurons bilden, nehmen an der trophischen Funktion des Neurons teil, indem sie als Übertragungsvehikel fungieren. Der axonale Transport kann anterograd (Zellkörper zum Axonterminal) und retrograd (Axonterminal zum Zellkörper) erfolgen. Von den dicksten bis zu den dünnsten werden drei Arten von fibrillären Elementen erkannt: Mikrotubuli, Neurofilamente und Mikrofilamente.
Gliazellen
Im Gegensatz zu Neuronen übertragen Gliazellen selbst keine elektrischen Nachrichten. Es gibt zwei Arten von Gliazellen: die Makroglia und für microglia. Die Makroglia ist ein Name, der mindestens drei Arten von Zellen gegeben wird: Astrozyten, Oligodendrozyten und Ependymzellen. Mikrogliazellen sind in erster Linie Fresszellen zum Entfernen von Trümmern, nachdem Nervenschäden oder Infektionen aufgetreten sind.
Die Gliazellen haben auch charakteristische mikroskopische und ultramikroskopische Merkmale. Gliazellen unterstützen Neuronen physisch, aber auch eine Reihe physiologischer Eigenschaften beginnt man jetzt zu verstehen. Zu den wichtigsten Neuron-Glia-Wechselwirkungen gehört die Rolle der Gliazelle bei der Versorgung der Neuronen mit Nährstoffen, der Entfernung von Fragmenten von Neuronen nach ihrem Tod und, was am wichtigsten ist, ihrem Beitrag zum Prozess der chemischen Kommunikation. Gliazellen können sich im Gegensatz zu Neuronen teilen und sich somit selbst reproduzieren. Tumore des Nervensystems beispielsweise resultieren aus einer abnormalen Vermehrung von Gliazellen.
Myelin
Was bei der makroskopischen Betrachtung von Nervengewebe als „graue Substanz“ und „weiße Substanz“ erscheint, hat eine mikroskopische und biochemische Grundlage. Mikroskopisch gesehen enthält die graue Substanz die neuronalen Zellkörper, während sich in der weißen Substanz Nervenfasern oder Axone befinden. Das „weiße“ Aussehen ist auf eine Hülle zurückzuführen, die aus einer Fettsubstanz namens Myelin besteht, die diese Fasern bedeckt. Das Myelin der peripheren Nerven stammt von der Membran der Schwann-Zelle, die das Axon umhüllt. Das Myelin der Fasern im Zentralnervensystem wird von den Membranen der Oligodendrozyten (einer Vielzahl von Gliazellen) bereitgestellt. Oligodendrozyten myelinisieren normalerweise mehrere Axone, während die Schwann-Zelle nur mit einem Axon assoziiert ist. Zwischen kontinuierlichen Schwann-Zellen oder Oligodendrozyten besteht eine Diskontinuität der Myelinscheide, die als Ranvier-Knoten bezeichnet wird. Es wird geschätzt, dass in der längsten zentralen motorischen Bahn bis zu 2,000 Schwann-Zellen die Myelinhülle bilden. Myelin, dessen Rolle darin besteht, die Ausbreitung des Aktionspotentials zu erleichtern, kann ein spezifisches Ziel für neurotoxische Mittel sein. Eine morphologische Klassifikation neurotoxischer Substanzen beschreibt charakteristische neuropathologische Veränderungen des Myelins als Myelinopathien.
Trophische Funktion des Neurons
Zu den normalen Funktionen des Neurons gehören die Proteinsynthese, der axonale Transport, die Erzeugung und Weiterleitung des Aktionspotentials, die synaptische Übertragung sowie die Bildung und Aufrechterhaltung des Myelins. Einige der grundlegenden trophischen Funktionen des Neurons wurden bereits im 19. Jahrhundert durch Schneiden der Axone (Axotomie) beschrieben. Unter den aufgedeckten Prozessen war einer der wichtigsten die Wallersche Degeneration – nach Waller, dem englischen Physiologen, der sie beschrieb.
Die Wallersche Degeneration bietet eine gute Gelegenheit, bekannte Veränderungen in Organellen als Folge von entweder traumatischen oder toxischen Schäden zu beschreiben. Übrigens sind die Begriffe, die verwendet werden, um die Wallersche Degeneration zu beschreiben, die durch traumatische Axotomie hervorgerufen wird, die gleichen, die verwendet werden, um Veränderungen zu beschreiben, die von neurotoxischen Mitteln herrühren. Auf zellulärer Ebene sind neuropathologische Veränderungen, die aus einer toxischen Schädigung von Nervengewebe resultieren, weitaus komplexer als diejenigen, die als Folge einer traumatischen Schädigung auftreten. Erst vor kurzem wurden Veränderungen in Neuronen beobachtet, die von neurotoxischen Mitteln beeinflusst wurden.
1 Stunden nach dem Schneiden des Axons ist das auffälligste Merkmal das Anschwellen beider Seiten des mechanischen Traumas. Schwellungen resultieren aus der Ansammlung von Flüssigkeiten und membranösen Elementen auf beiden Seiten der Verletzungsstelle. Diese Veränderungen sind denen nicht unähnlich, die auf einer regenüberfluteten Einbahnstraße beobachtet werden, wenn Fahrzeuge auf beiden Seiten des überfluteten Gebiets anhalten. In dieser Analogie sind ins Stocken geratene Fahrzeuge die Schwellung. Nach einigen Tagen kommt es zur Regeneration der umhüllten Axone, dh der mit Myelin bedeckten Axone. Sprossen wachsen aus dem proximalen Stumpf und bewegen sich mit einer Geschwindigkeit von 3 bis XNUMX mm pro Tag. Unter günstigen Bedingungen erreichen Sprossen den distalen (vom Zellkörper entfernten) Stumpf. Wenn die Renervation – das Zusammenfügen der Stümpfe – abgeschlossen ist, sind die grundlegenden Merkmale der normalen Übertragung wiederhergestellt. Der Zellkörper des verletzten Neurons erfährt tiefgreifende strukturelle Veränderungen bei der Proteinsynthese und dem axonalen Transport.
Wenn man sagt, dass die molekulare Neurobiologie eine junge Disziplin ist, ist die Neurobiologie der neurotoxischen Prozesse noch jünger und steckt noch in den Kinderschuhen. Zwar sind die molekularen Wirkungsgrundlagen vieler Neurotoxine und pharmakologischer Wirkstoffe heute gut verstanden. Aber mit einigen bemerkenswerten Ausnahmen (z. B. Blei, Methylquecksilber, Acrylamid) ist die molekulare Grundlage der Toxizität der überwiegenden Mehrheit der umwelt- und neurotoxischen Stoffe unbekannt. Anstatt die molekulare Neurobiologie einer ausgewählten Gruppe von berufs- und umweltbedingten Neurotoxika zu beschreiben, müssen wir daher immer noch auf die vergleichsweise zahlreichen Strategien und Beispiele aus der klassischen Neuropharmakologie oder aus der Arbeit in der modernen Arzneimittelherstellung verweisen.
Neurotransmitter
Ein Neurotransmitter ist eine chemische Substanz, die, wenn sie durch das Aktionspotential aus den Axonenden freigesetzt wird, die momentane Änderung des elektrischen Potentials erzeugt, wenn eine andere Nervenfaser stimuliert wird. Neurotransmitter stimulieren oder hemmen benachbarte Neuronen oder Effektororgane wie Muskeln und Drüsen. Bekannte Neurotransmitter und ihre neuronalen Bahnen werden jetzt intensiv untersucht, und ständig werden neue entdeckt. Einige neurologische und psychiatrische Erkrankungen werden heute als durch chemische Veränderungen in der Neurotransmission verursacht angesehen – zum Beispiel Myasthenia gravis, Parkinson-Krankheit, bestimmte Formen affektiver Störungen wie Depressionen, schwere Verzerrungen von Denkprozessen wie bei Schizophrenie und Alzheimer-Krankheit. Obwohl ausgezeichnete isolierte Berichte über die Wirkung mehrerer umweltbedingter und berufsbedingter neurotoxischer Mittel auf die Neurotransmission veröffentlicht wurden, ist der Wissensbestand im Vergleich zu dem über neuropsychiatrische Erkrankungen dürftig. Pharmakologische Studien von hergestellten Arzneimitteln erfordern ein Verständnis dafür, wie Arzneimittel die Neurotransmission beeinflussen. Arzneimittelherstellung und Neurotransmissionsforschung sind daher eng miteinander verbunden. Die wechselnden Ansichten über die Wirkung von Drogen wurden von Feldman und Quenzer (1984) zusammengefasst.
Die Wirkungen von neurotoxischen Mitteln auf die Neurotransmission werden dadurch gekennzeichnet, wo im Nervensystem sie wirken, ihre chemischen Rezeptoren, den zeitlichen Verlauf ihrer Wirkungen, ob neurotoxische Mittel die Neurotransmission erleichtern, blockieren oder hemmen oder ob neurotoxische Mittel die Beendigung oder Entfernung der Neurotransmission verändern Die pharmakologische Wirkung von Neurotransmittern.
Eine Schwierigkeit, auf die Neurowissenschaftler stoßen, ist die Notwendigkeit, bekannte Prozesse, die auf molekularer Ebene im Neuron ablaufen, mit Ereignissen auf zellulärer Ebene zu verknüpfen, die wiederum erklären können, wie normale und pathologische neuropsychologische Veränderungen auftreten, wie im Folgenden klar dargelegt wird weitgehend noch gilt: „Auf molekularer Ebene ist oft eine Erklärung der Wirkung eines Arzneimittels möglich; Auf zellulärer Ebene ist manchmal eine Erklärung möglich, aber auf Verhaltensebene ist unsere Unwissenheit erschreckend“ (Cooper, Bloom und Roth 1986).
Die Hauptbestandteile des Nervensystems
Die Kenntnis der Hauptkomponenten des Nervensystems ist wesentlich für das Verständnis der groben neuropsychologischen Manifestationen einer neurotoxischen Erkrankung, die Begründung für die Verwendung spezifischer Techniken zur Bewertung von Funktionen des Nervensystems und das Verständnis der pharmakologischen Mechanismen der neurotoxischen Wirkung. Aus funktioneller Sicht kann das Nervensystem in zwei große Kompartimente unterteilt werden: Das somatisches Nervensystem übermittelt sensorische Informationen (Berührung, Temperatur, Schmerz und Position der Gliedmaßen – selbst bei geschlossenen Augen) von den Körpersegmenten und trägt die Nervenbahnen, die die Bewegung der Skelettmuskulatur innervieren und steuern, wie z. B. die der Arme, Finger, Beine und Zehen. Das viszerales Nervensystem steuert innere Organe, die normalerweise nicht unter dem Einfluss von Blutgefäßen stehen, die Erweiterung und Verengung der Pupillen der Augen und so weiter.
Aus anatomischer Sicht müssen vier Hauptkomponenten identifiziert werden: die Zentralnervensystems, der Periphäres Nervensystem einschließlich Hirnnerven, die autonomes System und für neuroendokrines System.
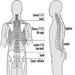
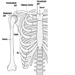
Das zentrale Nervensystem
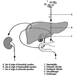
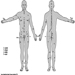
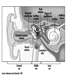
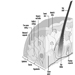
Das Zentralnervensystem enthält das Gehirn und das Rückenmark Abbildung 3. Das Gehirn liegt in der Schädelhöhle und wird durch die Hirnhäute geschützt. Es ist in drei Hauptkomponenten unterteilt; in aufsteigender Reihenfolge – das heißt, vom kaudalen (Schwanz) zum zervikalen (Kopf) Teil des Nervensystems – sind dies das Hinterhirn (auch Rhombencephalon genannt), das Mittelhirn (das Meszenzphalon) und das Vorderhirn (das Proscencephalon).
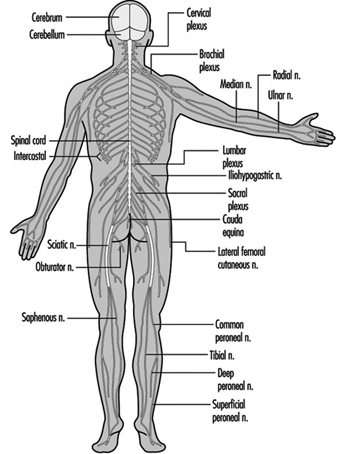
Abbildung 3. Die zentralen und peripheren Bereiche des Nervensystems
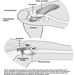
Das Hinterhirn
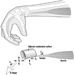
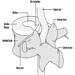
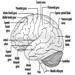
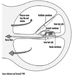
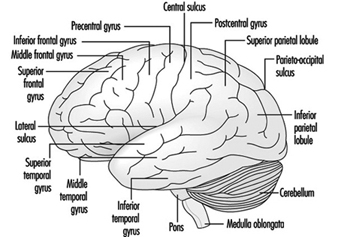
Die drei Hauptbestandteile des Hinterhirns sind die Medulla oblongata, die Brücke und das Kleinhirn Abbildung 4.
Abbildung 4. Das Gehirn von einer lateralen Seite.
Die Medulla oblongata enthält neurale Strukturen, die die Herzfrequenz und Atmung steuern, manchmal das Ziel von neurotoxischen Mitteln und Medikamenten, die zum Tod führen. Die zwischen der Medulla oblongata und dem Mittelhirn gelegene Pons (Brücke) leitet ihren Namen von der großen Anzahl von Fasern ab, die ihre vordere Seite auf dem Weg zu den Kleinhirnhemisphären durchqueren. Das Kleinhirn – auf Lateinisch „kleines Gehirn“ – ist charakteristisch gewellt. Das Kleinhirn empfängt sensorische Informationen und sendet motorische Botschaften, die für die motorische Koordination unerlässlich sind. Es ist (neben anderen Funktionen) für die Ausführung feiner Bewegungen zuständig. Diese Planung – oder Programmierung – erfordert ein angemessenes Timing von sensorischen Eingaben und motorischen Reaktionen. Das Kleinhirn ist oft das Ziel zahlreicher neurotoxischer Mittel – zum Beispiel alkoholischer Getränke, vieler industrieller Lösungsmittel, Blei – die die motorischen Reaktionen beeinflussen.
Das Mittelhirn
Das Mittelhirn ist ein schmaler Teil des Gehirns, der das Hinterhirn mit dem Vorderhirn verbindet. Strukturen des Mittelhirns sind das zerebrale Aquädukt, das Tectum, die Hirnstiele, die Substantia nigra und der rote Kern. Das zerebrale Aquädukt ist ein Kanal, der den dritten mit dem vierten Ventrikel (flüssigkeitsgefüllte Hohlräume des Gehirns) verbindet; Durch diese Öffnung fließt der Liquor cerebrospinalis (CSF).
Das Vorderhirn
Dieser Teil des Gehirns ist unterteilt in Zwischenhirn („Zwischenhirn“) und Großhirn. Die Hauptregionen des Zwischenhirns sind der Thalamus und der Hypothalamus. „Thalamus“ bedeutet „innerer Raum“. Die Thalami bestehen aus neuronalen Gruppierungen, sogenannten Kernen, die fünf Hauptfunktionen haben:
- Empfängt sensorische Informationen und sendet sie an primäre Bereiche der Großhirnrinde
- Senden von Informationen über laufende Bewegungen an motorische Bereiche der Großhirnrinde
- Senden von Informationen über die Aktivität des limbischen Systems an Bereiche der Großhirnrinde, die mit diesem System in Verbindung stehen
- Senden von Informationen über intrathalamische Aktivität an Assoziationsbereiche der Großhirnrinde
- Senden von Informationen über die Aktivität der retikulären Formation im Hirnstamm an weite Bereiche der Großhirnrinde.
Der Name Hypothalamus bedeutet „unter dem Thalamus“. Er bildet die Basis des dritten Ventrikels, ein wichtiger Bezugspunkt für die Bildgebung des Gehirns. Der Hypothalamus ist eine komplexe, winzige neurale Struktur, die für viele Aspekte des Verhaltens wie grundlegende biologische Antriebe, Motivation und Emotionen verantwortlich ist. Es ist das Bindeglied zwischen dem Nervensystem und dem neuroendokrinen System, das weiter unten beschrieben wird. Die Hypophyse (auch Hypophyse genannt) ist durch Neuronen mit den Kernen des Hypothalamus verbunden. Es ist allgemein bekannt, dass die Nervenzellen des Hypothalamus viele neurosekretorische Funktionen erfüllen. Der Hypothalamus ist mit vielen anderen wichtigen Regionen des Gehirns verbunden, einschließlich des Rheinzephalons – der primitiven Hirnrinde, die ursprünglich mit dem Riechen verbunden war – und dem limbischen System, einschließlich des Hippocampus.
Die Großhirnrinde ist der größte Bestandteil des Gehirns und besteht aus zwei Großhirnhemisphären, die durch eine Masse weißer Substanz, den so genannten Corpus callosum, verbunden sind. Die Großhirnrinde ist die Oberflächenschicht jeder Großhirnhemisphäre. Tiefe Sulci in der Großhirnrinde – die zentralen und lateralen Sulci Abbildung 4 – werden als Referenzpunkte genommen, um anatomische Regionen des Gehirns zu trennen. Der Frontallappen liegt vor dem Sulcus centralis. Der Parietallappen beginnt an der Rückseite des Sulcus centralis und liegt neben dem Okzipitallappen, der den hinteren Teil des Gehirns einnimmt. Der Temporallappen beginnt gut innerhalb der Faltung des lateralen Sulcus und erstreckt sich in die ventralen Aspekte der Gehirnhälften. Zwei wichtige Bestandteile des Großhirns sind die Basalganglien und das limbische System.
Die Basalganglien sind Zellkerne, also Ansammlungen von Nervenzellen, die sich in der Mitte des Gehirns befinden. Die Basalganglien umfassen Hauptzentren des extrapyramidalen motorischen Systems. (Das Pyramidensystem, dem der Begriff gegenübergestellt wird, ist an der freiwilligen Steuerung der Bewegung beteiligt.) Das extrapyramidale System wird selektiv von vielen neurotoxischen Wirkstoffen (z. B. Mangan) beeinflusst. In den letzten zwei Jahrzehnten wurden wichtige Entdeckungen hinsichtlich der Rolle gemacht, die diese Zellkerne bei mehreren neuralen degenerativen Erkrankungen (z. B. Parkinson-Krankheit, Chorea Huntington) spielen.
Das limbische System besteht aus verschlungenen neuralen Strukturen, die sich in viele Richtungen verzweigen und Verbindungen zu vielen „alten“ Regionen des Gehirns herstellen, insbesondere zum Hypothalamus. Es ist an der Kontrolle des emotionalen Ausdrucks beteiligt. Es wird angenommen, dass der Hippocampus eine Struktur ist, in der viele Gedächtnisprozesse ablaufen.
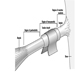
Das Rückenmark
Das Rückenmark ist eine weißliche Struktur, die sich im Wirbelkanal befindet. Es ist in vier Regionen unterteilt: zervikal, thorakal, lumbal und sakral-steißbein. Die beiden am leichtesten erkennbaren Merkmale des Rückenmarks sind die graue Substanz, die die Zellkörper der Neuronen enthält, und die weiße Substanz, die die myelinisierten Axone der Neuronen enthält. Die ventrale Region der grauen Substanz des Rückenmarks enthält Nervenzellen, die die Motorik regulieren; Der mittlere Bereich des Brustrückenmarks ist mit autonomen Funktionen verbunden. Der dorsale Teil erhält sensorische Informationen von den Spinalnerven.
Das periphere Nervensystem
Das periphere Nervensystem umfasst jene Neuronen, die außerhalb des zentralen Nervensystems liegen. Der Begriff peripher beschreibt die anatomische Verteilung dieses Systems, aber funktionell ist es künstlich. Die Zellkörper der peripheren motorischen Fasern befinden sich beispielsweise innerhalb des zentralen Nervensystems. In der experimentellen, klinischen und epidemiologischen Neurotoxikologie wird der Begriff Periphäres Nervensystem (PNS) beschreibt ein System, das selektiv anfällig für die Wirkung toxischer Stoffe ist und sich regenerieren kann.
Die Spinalnerven
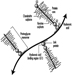
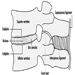
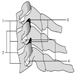
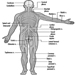
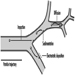
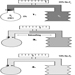
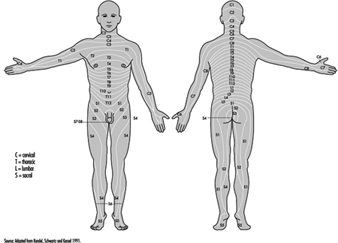
Die ventralen und dorsalen Wurzeln sind dort, wo die peripheren Nerven in das Rückenmark eintreten und es entlang seiner Länge verlassen. Angrenzende Wirbel enthalten Öffnungen, damit Wurzelfasern, die die Spinalnerven bilden, den Spinalkanal verlassen können. Es gibt 31 Paare von Spinalnerven, die nach der Region der Wirbelsäule benannt sind, mit der sie verbunden sind: 8 zervikale, 12 thorakale, 5 lumbale, 5 sakrale und 1 Steißbein. Eine Metamera ist eine Körperregion, die von einem Spinalnerv innerviert wird Abbildung 5.
Abbildung 5. Die segmentale Verteilung der Spinalnerven (die Metamera).
Durch die sorgfältige Untersuchung der motorischen und sensorischen Funktionen von Metameren können Neurologen auf die Stelle von Läsionen schließen, an denen Schäden aufgetreten sind.
Tabelle 1. Namen und Hauptfunktionen der einzelnen Hirnnervenpaare
| Nerv1 | Leitet Impulse | Funktionen |
| I. Olfaktorisch | Von der Nase zum Gehirn | Geruchssinn |
| II. Optik | Vom Auge zum Gehirn | Vision |
| III. Okulomotorik | Vom Gehirn bis zu den Augenmuskeln | Augenbewegungen |
| IV. Trochlea | Vom Gehirn bis zu den äußeren Augenmuskeln | Augenbewegungen |
| V. Trigeminus (oder trifacial) |
Von Haut und Schleimhaut des Kopfes und von den Zähnen bis zum Gehirn; auch vom Gehirn bis zu den Kaumuskeln | Empfindungen von Gesicht, Kopfhaut und Zähnen; Kaubewegungen |
| VI. Abducens | Vom Gehirn bis zu den äußeren Augenmuskeln | Augen nach außen richten |
| VII. Gesichts | Von den Geschmacksknospen der Zunge bis zum Gehirn; vom Gehirn bis zu den Gesichtsmuskeln | Geschmackssinn; Kontraktion der Gesichtsmuskeln |
| VIII. Akustisch | Vom Ohr bis zum Gehirn | Hören; Gefühl von Gleichgewicht |
| IX. Glossopharynx | Von der Kehle und den Geschmacksknospen der Zunge bis zum Gehirn; auch vom Gehirn zu Halsmuskeln und Speicheldrüsen | Rachen-, Geschmacks-, Schluckbewegungen, Speichelsekretion |
| X. Vagus | Von Rachen, Kehlkopf und Organen in Brust- und Bauchhöhle bis zum Gehirn; auch vom Gehirn zu den Halsmuskeln und zu den Organen in der Brust- und Bauchhöhle | Empfindungen von Hals, Kehlkopf und für Brust- und Bauchorgane; Schlucken, Stimmbildung, Verlangsamung des Herzschlags, Beschleunigung der Peristaltik |
| XI. Zubehör für die Wirbelsäule | Vom Gehirn bis zu bestimmten Schulter- und Nackenmuskeln | Schulterbewegungen; Drehbewegungen des Kopfes |
| XII. Hypoglossus | Vom Gehirn bis zu den Zungenmuskeln | Zungenbewegungen |
1 Die Anfangsbuchstaben der Wörter des folgenden Satzes sind die Anfangsbuchstaben der Namen von Hirnnerven: „Auf den winzigen Kreiseln des alten Olymp sahen ein Finne und ein Deutscher etwas Hopfen“. Viele Generationen von Schülern haben diesen oder einen ähnlichen Satz verwendet, um sich die Namen der Hirnnerven zu merken.
Die Hirnnerven
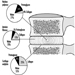
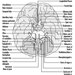
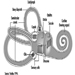
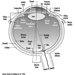
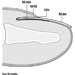
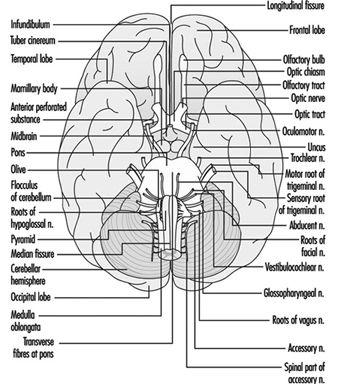
Hirnstamm ist ein umfassender Begriff, der die Region des Nervensystems bezeichnet, die das Medulla, die Pons und das Mittelhirn umfasst. Der Hirnstamm ist eine Fortsetzung des Rückenmarks nach oben und vorne (ventral). In dieser Region treten die meisten Hirnnerven aus und ein. Es gibt 12 Hirnnervenpaare; Tabelle 1 beschreibt den Namen und die Hauptfunktion jedes Paares und Abbildung 6 zeigt den Eingang und Ausgang einiger Hirnnerven im Gehirn.
Abbildung 6. Das von unten gezeigte Gehirn mit den Ein- und Ausgängen vieler Hirnnerven.
Das autonome Nervensystem
Das vegetative Nervensystem ist der Teil des Nervensystems, der die Aktivität der viszeralen Komponenten des menschlichen Körpers steuert. Es wird als „autonom“ bezeichnet, weil es seine Funktionen automatisch ausführt, was bedeutet, dass seine Funktion nicht einfach nach Belieben gesteuert werden kann. Aus anatomischer Sicht besteht das vegetative System aus zwei Hauptkomponenten: dem sympathischen und dem parasympathischen Nervensystem. Die sympathischen Nerven, die die viszerale Aktivität steuern, entspringen den thorakalen und lumbalen Teilen des Rückenmarks; parasympathische Nerven entspringen dem Hirnstamm und dem sakralen Teil des Rückenmarks.
Aus physiologischer Sicht kann keine allgemeingültige Aussage getroffen werden, wie das sympathische und das parasympathische Nervensystem verschiedene Körperorgane steuern. In den meisten Fällen werden viszerale Organe von beiden Systemen innerviert, und jeder Typ hat einen gegensätzlichen Effekt in einem System von Checks and Balances. Das Herz beispielsweise wird von Sympathikusnerven innerviert, deren Erregung eine Beschleunigung des Herzschlags bewirkt, und von Parasympathikusnerven, deren Erregung eine Verlangsamung des Herzschlags bewirkt. Jedes System kann die Organe, die es innerviert, stimulieren oder hemmen. In anderen Fällen werden Organe überwiegend oder ausschließlich von dem einen oder anderen System kontrolliert. Eine lebenswichtige Funktion des vegetativen Nervensystems ist die Aufrechterhaltung der Homöostase (stabiler Gleichgewichtszustand) und die Anpassung des tierischen Körpers an seine äußere Umgebung. Homöostase ist der Gleichgewichtszustand der Körperfunktionen, der durch einen aktiven Prozess erreicht wird; die Kontrolle von Körpertemperatur, Wasser und Elektrolyten sind Beispiele für homöostatische Prozesse.
Aus pharmakologischer Sicht gibt es keinen einzigen Neurotransmitter, der mit sympathischen oder parasympathischen Funktionen assoziiert ist, wie früher angenommen wurde. Die alte Ansicht, Acetylcholin sei der vorherrschende Botenstoff des autonomen Systems, musste aufgegeben werden, als neue Klassen von Neurotransmittern und Neuromodulatoren gefunden wurden (z. B. Dopamin, Serotonin, Purine und verschiedene Neuropeptide).
Neurowissenschaftler haben kürzlich die Verhaltenssicht des autonomen Nervensystems wiederbelebt. Das vegetative Nervensystem ist an der beim Menschen noch vorhandenen Kampf-oder-Flucht-Instinktreaktion beteiligt, die zum größten Teil die Grundlage für die physiologischen Stressreaktionen ist. Über das vegetative Nervensystem sind Wechselwirkungen zwischen dem Nervensystem und immunologischen Funktionen möglich. Emotionen, die aus dem vegetativen Nervensystem stammen, können über die Skelettmuskulatur ausgedrückt werden.
Die autonome Steuerung der glatten Muskulatur
Die Muskeln der Eingeweide – mit Ausnahme des Herzens – sind die glatten Muskeln. Der Herzmuskel hat Eigenschaften sowohl der Skelett- als auch der glatten Muskulatur. Wie die Skelettmuskulatur enthält auch die glatte Muskulatur die beiden Proteine Aktin und in kleineren Anteilen Myosin. Im Gegensatz zu Skelettmuskeln weisen sie nicht die reguläre Organisation von Sarkolemen auf, der kontraktilen Einheit der Muskelfaser. Das Herz ist insofern einzigartig, als es myogene Aktivität erzeugen kann – selbst nachdem seine neuralen Innervationen durchtrennt wurden, kann es sich selbst kontrahieren und mehrere Stunden lang entspannen.
Die neuromuskuläre Kopplung in der glatten Muskulatur unterscheidet sich von der der Skelettmuskulatur. In der Skelettmuskulatur ist die neuromuskuläre Synapse die Verbindung zwischen dem Nerv und den Muskelfasern. In der glatten Muskulatur gibt es keine neuromuskuläre Verbindung; Die Nervenenden dringen in den Muskel ein und breiten sich in alle Richtungen aus. Elektrische Ereignisse innerhalb der glatten Muskulatur sind daher viel langsamer als die in der Skelettmuskulatur. Schließlich hat die glatte Muskulatur die einzigartige Eigenschaft, spontane Kontraktionen zu zeigen, wie sie der Darm zeigt. Das vegetative Nervensystem reguliert weitgehend die spontane Aktivität der glatten Muskulatur.
Die zentralen Komponenten des vegetativen Nervensystems
Die Hauptaufgabe des autonomen Nervensystems besteht darin, die Aktivität der glatten Muskulatur, des Herzens, der Drüsen im Verdauungstrakt, der Schweißdrüsen sowie der Nebennieren und anderer endokriner Drüsen zu regulieren. Das autonome Nervensystem hat eine zentrale Komponente – den Hypothalamus, der sich an der Basis des Gehirns befindet – wo viele autonome Funktionen integriert sind. Vor allem sind die zentralen Komponenten des vegetativen Systems direkt an der Regulation biologischer Triebe (Temperaturregulation, Hunger, Durst, Sex, Wasserlassen, Stuhlgang usw.), Motivation, Emotion und in hohem Maße an „psychologischen“ Funktionen beteiligt wie Stimmungen, Affekte und Gefühle.
Neuroendokrines System
Drüsen sind die Organe des endokrinen Systems. Sie werden als endokrine Drüsen bezeichnet, weil ihre chemischen Botschaften im Inneren des Körpers direkt in den Blutkreislauf abgegeben werden (im Gegensatz zu exokrinen Drüsen wie Schweißdrüsen, deren Sekrete an der äußeren Oberfläche des Körpers erscheinen). Das endokrine System sorgt durch chemische Botenstoffe, die als Hormone bezeichnet werden, für eine langsame, aber lang anhaltende Kontrolle über Organe und Gewebe. Hormone sind die wichtigsten Regulatoren des Körperstoffwechsels. Aber aufgrund enger Verbindungen zwischen dem zentralen, peripheren und autonomen Nervensystem, dem neuroendokrines System– ein Begriff, der solch komplexe Verbindungen erfasst – wird heute als starker Modifikator der Struktur und Funktion des menschlichen Körpers und Verhaltens angesehen.
Hormone wurden als chemische Botenstoffe definiert, die von Zellen in den Blutkreislauf freigesetzt werden, um ihre Wirkung auf entfernte Zielzellen auszuüben. Bis vor kurzem wurden Hormone von den oben diskutierten Neurotransmittern unterschieden. Letztere sind chemische Botenstoffe, die von Neuronen auf eine Synapse zwischen den Nervenenden und einem anderen Neuron oder einem Effektor (dh einem Muskel oder einer Drüse) freigesetzt werden. Mit der Entdeckung, dass klassische Neurotransmitter wie Dopamin auch als Hormone wirken können, ist die Unterscheidung zwischen Neurotransmittern und Hormonen jedoch immer weniger klar. Aus rein anatomischen Überlegungen können daher Hormone, die von Nervenzellen stammen, als Neurohormone bezeichnet werden. Aus funktioneller Sicht kann das Nervensystem als ein echtes neurosekretorisches System betrachtet werden.
Der Hypothalamus steuert endokrine Funktionen durch eine Verbindung mit der Hypophyse (auch Hypophyse genannt, eine winzige Drüse an der Basis des Gehirns). Bis Mitte der 1950er Jahre wurden die endokrinen Drüsen als separates System angesehen, das von der Hypophyse gesteuert wird, die oft als „Meisterdrüse“ bezeichnet wird. Zu dieser Zeit wurde eine neurovaskuläre Hypothese aufgestellt, die die funktionelle Rolle der hypothalamischen/hypophysären Faktoren bei der Kontrolle der endokrinen Funktion feststellte. Aus dieser Sicht stellt der endokrine Hypothalamus den letzten gemeinsamen neuroendokrinen Weg bei der Kontrolle des endokrinen Systems bereit. Es ist nun fest etabliert, dass das endokrine System selbst durch das zentrale Nervensystem sowie die endokrinen Inputs reguliert wird. Daher, Neuroendokrinologie ist nun ein geeigneter Begriff, um die Disziplin zu beschreiben, die die wechselseitige integrierte Rolle des Nervensystems und des endokrinen Systems bei der Kontrolle physiologischer Prozesse untersucht.
Mit zunehmendem Verständnis der Neuroendokrinologie lösen sich ursprüngliche Trennungen auf. Der Hypothalamus, der sich über der Hypophyse befindet und mit ihr verbunden ist, ist das Bindeglied zwischen dem Nerven- und dem endokrinen System, und viele seiner Nervenzellen erfüllen sekretorische Funktionen. Es ist auch mit anderen wichtigen Regionen des Gehirns verbunden, darunter das Rheinzephalon – der primitive Cortex, der ursprünglich mit dem Geruchssinn oder dem Geruchssinn verbunden war – und dem limbischen System, das mit Emotionen verbunden ist. Im Hypothalamus werden Hormone produziert, die von der hinteren Hypophyse freigesetzt werden. Der Hypothalamus produziert auch Substanzen, die als freisetzende und hemmende Hormone bezeichnet werden. Diese wirken auf die Adenohypophyse und bewirken, dass sie die Produktion von Hypophysenvorderlappenhormonen verstärkt oder hemmt, die auf anderswo gelegene Drüsen wirken (Schilddrüse, Nebennierenrinde, Eierstöcke, Hoden und andere).
Chemische neurotoxische Mittel
Definition von Neurotoxizität
Neurotoxizität bezieht sich auf die Fähigkeit, schädliche Wirkungen im Zentralnervensystem, peripheren Nerven oder Sinnesorganen hervorzurufen. Eine Chemikalie gilt als neurotoxisch, wenn sie in der Lage ist, ein konsistentes Muster neuraler Dysfunktion oder eine Veränderung der Chemie oder Struktur des Nervensystems zu induzieren.
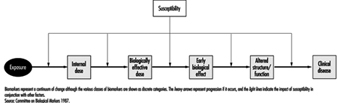
Neurotoxizität manifestiert sich im Allgemeinen als ein Kontinuum von Symptomen und Wirkungen, die von der Art der Chemikalie, der Dosis, der Expositionsdauer und den Eigenschaften der exponierten Person abhängen. Der Schweregrad der beobachteten Wirkungen sowie die Hinweise auf Neurotoxizität nehmen durch die Stufen 1 bis 6 zu, wie in Tabelle 1 gezeigt. Kurzfristige oder niedrig dosierte Exposition gegenüber einer neurotoxischen Chemikalie kann zu subjektiven Symptomen wie Kopfschmerzen und Schwindel führen. aber die Wirkung ist normalerweise reversibel. Mit zunehmender Dosis können neurologische Veränderungen auftreten und schließlich irreversible morphologische Veränderungen erzeugt werden. Der Grad der Anomalie, der erforderlich ist, um auf die Neurotoxizität eines chemischen Wirkstoffs hinzuweisen, ist umstritten. Gemäß der Definition wird ein konsistentes Muster einer neuralen Dysfunktion oder Veränderung in der Chemie oder Struktur des Nervensystems in Betracht gezogen, wenn es gut dokumentierte Beweise für anhaltende Auswirkungen auf Stufe 3, 4, 5 oder 6 in Tabelle 1 gibt. Diese Stufen spiegeln wider die Gewichtung der Beweise durch verschiedene Anzeichen von Neurotoxizität. Zu den neurotoxischen Substanzen gehören natürlich vorkommende Elemente wie Blei, Quecksilber und Mangan; biologische Verbindungen wie Tetrodotoxin (aus dem Kugelfisch, einer japanischen Delikatesse) und Domoinsäure (aus kontaminierten Muscheln); und synthetische Verbindungen, darunter viele Pestizide, industrielle Lösungsmittel und Monomere.
Tabelle 1. Gruppierung neurotoxischer Wirkungen, um ihre relative Stärke für die Feststellung von Neurotoxizität widerzuspiegeln
|
Niveau |
Gruppierung |
Erklärung/Beispiele |
|
6 |
Morphologische Veränderungen |
Morphologische Veränderungen umfassen Zelltod und Axonopathie sowie subzelluläre morphologische Veränderungen. |
|
5 |
Neurologische Veränderungen |
Neurologische Veränderungen umfassen auffällige Befunde bei neurologischen Untersuchungen einzelner Personen. |
|
4 |
Physiologische/Verhaltensänderungen |
Physiologische/Verhaltensänderungen umfassen experimentelle Befunde an Gruppen von Tieren oder Menschen, wie beispielsweise Änderungen der evozierten Potenziale und des EEG oder Änderungen in psychologischen und Verhaltenstests. |
|
3 |
Biochemische Veränderungen |
Biochemische Veränderungen umfassen Veränderungen relevanter biochemischer Parameter (z. B. Transmitterspiegel, GFA-Proteingehalt (glial fibrillary acidic protein) oder Enzymaktivitäten). |
|
21 |
Irreversible, subjektive Symptome |
Subjektive Symptome. Keine Hinweise auf Anomalien bei neurologischen, psychologischen oder anderen medizinischen Untersuchungen. |
|
11 |
Reversible, subjektive Symptome |
Subjektive Symptome. Keine Hinweise auf Anomalien bei neurologischen, psychologischen oder anderen medizinischen Untersuchungen. |
1 Nur Menschen
Quelle: Modifiziert nach Simonsen et al. 1994.
In den Vereinigten Staaten sind zwischen 50,000 und 100,000 Chemikalien im Handel, und jedes Jahr werden 1,000 bis 1,600 neue Chemikalien zur Bewertung eingereicht. Mehr als 750 Chemikalien und mehrere Klassen oder Gruppen chemischer Verbindungen stehen im Verdacht, neurotoxisch zu sein (O'Donoghue 1985), aber die meisten Chemikalien wurden nie auf neurotoxische Eigenschaften getestet. Die meisten der heute verfügbaren bekannten neurotoxischen Chemikalien wurden durch Fallberichte oder durch Unfälle identifiziert.
Obwohl neurotoxische Chemikalien häufig für bestimmte Verwendungszwecke hergestellt werden, kann die Exposition aus mehreren Quellen stammen – Verwendung in Privathaushalten, in der Landwirtschaft und in der Industrie oder durch verschmutztes Trinkwasser und so weiter. A priori feststehende Vorurteile darüber, welche neurotoxischen Verbindungen in welchen Berufen zu erwarten sind, sollten daher mit Vorsicht betrachtet werden, und die folgenden Zitate sollten als mögliche Beispiele angesehen werden, darunter einige der häufigsten neurotoxischen Chemikalien (Arlien-Søborg 1992; O 'Donoghue 1985; Spencer und Schaumburg 1980; WHO 1978).
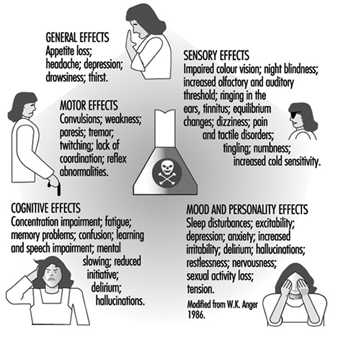
Symptome der Neurotoxizität
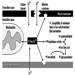
Das Nervensystem reagiert im Allgemeinen ziemlich stereotyp auf die Exposition gegenüber neurotoxischen Substanzen Abbildung 1. Einige typische Syndrome sind unten angegeben.
Abbildung 1. Neurologische und Verhaltenseffekte der Exposition gegenüber neurotoxischen Chemikalien.
Polyneuropathie
Dies wird durch eine Beeinträchtigung der motorischen und sensorischen Nervenfunktion verursacht, die zu einer Schwäche der Muskulatur führt, wobei die Paresen normalerweise peripher in den oberen und unteren Extremitäten (Hände und Füße) am ausgeprägtesten sind. Vorangehende oder gleichzeitige Parästhesien (Kribbeln oder Taubheitsgefühl in den Fingern und Zehen) können auftreten. Dies kann zu Schwierigkeiten beim Gehen oder bei der Feinkoordination von Händen und Fingern führen. Schwermetalle, Lösungsmittel und Pestizide können neben anderen Chemikalien zu einer solchen Behinderung führen, auch wenn der toxische Mechanismus dieser Verbindungen völlig anders sein kann.
Enzephalopathie
Dies wird durch eine diffuse Beeinträchtigung des Gehirns verursacht und kann zu Müdigkeit führen; Beeinträchtigung des Lernens, des Gedächtnisses und der Konzentrationsfähigkeit; Angst, Depression, erhöhte Reizbarkeit und emotionale Instabilität. Solche Symptome können sowohl auf eine frühe diffuse degenerative Hirnerkrankung als auch auf eine berufsbedingte chronische toxische Enzephalopathie hinweisen. Oft können auch eine erhöhte Häufigkeit von Kopfschmerzen, Schwindel, Veränderungen des Schlafmusters und eine verminderte sexuelle Aktivität in den frühen Stadien der Krankheit vorhanden sein. Solche Symptome können sich nach längerer, geringer Exposition gegenüber verschiedenen Chemikalien wie Lösungsmitteln, Schwermetallen oder Schwefelwasserstoff entwickeln und werden auch bei mehreren Demenzerkrankungen beobachtet, die nicht mit der Arbeit zusammenhängen. In einigen Fällen können spezifischere neurologische Symptome beobachtet werden (z. B. Parkinsonismus mit Zittern, Muskelsteifheit und Verlangsamung der Bewegungen oder zerebelläre Symptome wie Zittern und verminderte Koordination von Handbewegungen und Gang). Solche Krankheitsbilder können nach Exposition gegenüber bestimmten Chemikalien wie Mangan oder MPTP (1-Methyl-4-Phenyl-1,2,3,6-Tetrahydropyridin) im ersteren Zustand und Toluol oder Quecksilber im letzteren Zustand beobachtet werden.
Gase
Eine Vielzahl von Chemikalien mit völlig unterschiedlichen chemischen Strukturen sind bei Normaltemperatur Gase und haben sich als neurotoxisch erwiesen Tabelle 3. Einige von ihnen sind selbst in sehr geringen Dosen extrem giftig und wurden sogar als Kampfgase verwendet (Phosgen und Cyanid); andere erfordern hohe Dosen über längere Zeiträume, um Symptome hervorzurufen (z. B. Kohlendioxid). Einige werden zur Vollnarkose verwendet (z. B. Lachgas); andere werden in großem Umfang in der Industrie und in Desinfektionsmitteln (z. B. Formaldehyd) verwendet. Erstere können nach wiederholter geringer Exposition irreversible Veränderungen im Nervensystem hervorrufen, letztere offenbar nur akute Symptome hervorrufen. Die Exposition in kleinen Räumen mit schlechter Belüftung ist besonders gefährlich. Einige der Gase sind geruchlos, was sie besonders gefährlich macht (z. B. Kohlenmonoxid). Wie in Tabelle 2 gezeigt, sind einige Gase wichtige Bestandteile in der industriellen Produktion, während andere das Ergebnis einer unvollständigen oder vollständigen Verbrennung sind (z. B. CO und CO2 beziehungsweise). Dies ist in Bergbau, Stahlwerken, Kraftwerken usw. zu beobachten, kann aber auch in Privathäusern mit unzureichender Belüftung auftreten. Wesentlich für die Behandlung ist es, die weitere Exposition zu stoppen und frische Luft oder Sauerstoff und in schweren Fällen künstliche Beatmung bereitzustellen.
Tabelle 2. Mit neurotoxischen Wirkungen assoziierte Gase
|
Chemical |
Beispiele für Expositionsquellen |
Ausgewählte Branchen in Gefahr |
Effekte1 |
|
Kohlendioxid (CO2 ) |
Schweißen; Fermentation; Herstellung, Lagerung und Verwendung von Trockeneis |
Metallindustrie; Bergbau; Brauereien |
M: Gefäße erweitern A: Kopfschmerzen; Dyspnoe; Tremor; Bewusstseinsverlust C: Kaum etwas |
|
Kohlenmonoxid (CO) |
Autoreparatur; Schweißen; Metallschmelzen; Treiber; Feuerwehrleute |
Metallindustrie; Bergbau; Transport; Kraftwerk |
M: Sauerstoffentzug A: Kopfschmerzen; Schläfrigkeit; Bewusstseinsverlust |
|
Schwefelwasserstoff (H2S) |
Begasung von Gewächshäusern; düngen; Fischer; Entladen von Fischen; Abwasserbehandlung |
Landwirtschaft; Angeln; Kanalarbeiten |
M: Blockieren des oxidativen Stoffwechsels A: Bewusstlosigkeit C: Enzephalopathie |
|
Cyanid (HCN) |
Elektroschweißen; galvanische Oberflächenbehandlung mit Nickel; Kupfer und Silber; Begasung von Schiffen, Häusern, Lebensmitteln und Erde in Gewächshäusern |
Metallindustrie; Chemieindustrie; Kindergarten; Bergbau; Gaswerk |
M: Blockierung von Atmungsenzymen A: Dyspnoe; fallender Blutdruck; Krämpfe; Bewusstseinsverlust; Tod C: Enzephalopathie; Ataxia; Neuropathie (z. B. nach dem Verzehr von Cavasava) Berufsunfähigkeit ungewiss |
|
Lachgas (N2O) |
Vollnarkose während der Operation; leichte Narkose bei Zahnpflege und Entbindung |
Krankenhäuser (Anästhesie); Zahnärzte; Hebamme |
M: Akute Veränderung der Nervenzellmembran; Degeneration von Nervenzellen nach Langzeitexposition A: Benommenheit; Schläfrigkeit; Bewusstseinsverlust C: Taubheit von Fingern und Zehen; reduzierte Koordination; Enzephalopathie |
1 M: Mechanismus; A: akute Wirkungen; C: chronische Wirkungen.
Neuropathie: Funktionsstörung motorischer und sensorischer peripherer Nervenfasern.
Enzephalopathie: Funktionsstörung des Gehirns aufgrund einer generalisierten Beeinträchtigung des Gehirns.
Ataxie: beeinträchtigte motorische Koordination.
Metallindustrie
In der Regel steigt die Toxizität von Metallen mit zunehmendem Atomgewicht, wobei Blei und Quecksilber besonders giftig sind. Metalle kommen in der Natur normalerweise in geringen Konzentrationen vor, aber in bestimmten Branchen werden sie in großen Mengen verwendet (siehe Tabelle 3) und können ein Berufsrisiko für die Arbeitnehmer darstellen. Darüber hinaus werden erhebliche Mengen an Metallen im Abwasser gefunden und können zu Umweltrisiken für die Anwohner in der Nähe der Anlagen, aber auch in größerer Entfernung führen. Oft werden die Metalle (oder zum Beispiel organische Quecksilberverbindungen) in die Nahrungskette aufgenommen und reichern sich in Fischen, Vögeln und Tieren an, was ein Risiko für Verbraucher darstellt. Die Toxizität und die Art und Weise, wie die Metalle vom Organismus verarbeitet werden, können von der chemischen Struktur abhängen. Reine Metalle können durch Einatmen oder Hautkontakt von Dämpfen (Quecksilber) und/oder kleinen Partikeln (Blei) oder oral (Blei) aufgenommen werden. Anorganische Quecksilberverbindungen (zB HgCl2) werden hauptsächlich durch den Mund aufgenommen, während organische Metallverbindungen (z. B. Tetraethylblei) hauptsächlich durch Einatmen oder durch Hautkontakt aufgenommen werden. Die Körperbelastung kann sich bis zu einem gewissen Grad in der Metallkonzentration im Blut oder Urin widerspiegeln. Dies ist die Grundlage für das biologische Monitoring. Bei der Behandlung ist zu beachten, dass insbesondere Blei nur sehr langsam aus Ablagerungen im Körper freigesetzt wird. Die Menge an Blei in Knochen wird normalerweise über 50 Jahre nur um 10 % reduziert. Diese Freisetzung kann durch die Verwendung von Chelatbildnern beschleunigt werden: BAL (Dimercapto-1-propanol), Ca-EDTA oder Penicillamin.
Tabelle 3. Mit Neurotoxizität assoziierte Metalle und ihre anorganischen Verbindungen
|
Chemical |
Beispiele für Expositionsquellen |
Ausgewählte Branchen in Gefahr |
Effekte1 |
|
Führen (Lead) |
Schmelzen; Löten; Schleif; Reparatur; Verglasung; Weichmacher |
Metallarbeiten; Bergbau; Speicheranlagen; Autoreparatur; Werften; Glasarbeiter; Keramik; Keramik; Plastik |
M: Beeinträchtigung des oxidativen Stoffwechsels von Nervenzellen und Glia A: Bauchschmerzen; Kopfschmerzen; Enzephalopathie; Anfälle C: Enzephalopathie; Polyneuropathie, einschließlich Fallhand |
|
Quecksilber-Elementar |
Elektrolyse; elektrische Instrumente (Gyroskop; Manometer; Thermometer; Batterie; Glühbirne; Röhren usw.); Amalgamfüllung |
Chloralkali-Pflanzen; Bergbau; Elektronik; Zahnheilkunde; Polymerherstellung; Papier- und Zellstoffindustrie |
M: Beeinträchtigung an mehreren Stellen in Nervenzellen A: Lungenentzündung; Kopfschmerzen; beeinträchtigte Sprache C: Zahnfleischentzündung; Appetitlosigkeit; Enzephalopathie; einschließlich Zittern; Reizbarkeit |
|
Kalomel Hg2Cl2 |
Laboratories |
A: Niedrige akute Toxizität, chronisch toxische Wirkungen, siehe oben |
|
|
HgCl sublimieren2 |
Desinfektion |
Krankenhäuser; Kliniken; Labore |
M: Akute tubuläre und glomeruläre Nierendegeneration. Sehr giftig selbst in kleinen oralen Dosen, tödlich bis zu 30 mg/kg Gewicht C: Siehe oben. |
|
Mangan |
Schmelzen (Stahllegierung); Schneiden; Schweißen in Stahl; trockene Batterien |
Manganabbau; Stahl- und Aluminiumproduktion; Metallindustrie; Batterieproduktion; Chemieindustrie; Ziegelei |
M: Nicht bekannt, mögliche Veränderungen von Dopamin und Katecholamin in den Basalganglien im Zentrum des Gehirns A: Dysphorie C: Enzephalopathie einschließlich Parkinsonismus; Psychose; Appetitlosigkeit; Reizbarkeit; Kopfschmerzen; die Schwäche |
|
Aluminium |
Metallurgie; Schleif; Polieren |
Metallindustrie |
M: Unbekannt C: Möglicherweise Enzephalopathie |
1 M: Mechanismus; A: akute Wirkungen; C: chronische Wirkungen.
Neuropathie: Funktionsstörung motorischer und sensorischer peripherer Nervenfasern.
Enzephalopathie: Funktionsstörung des Gehirns aufgrund einer generalisierten Beeinträchtigung des Gehirns.
Monomere
Monomere bilden eine große, heterogene Gruppe reaktiver Chemikalien, die für die chemische Synthese und Herstellung von Polymeren, Harzen und Kunststoffen verwendet werden. Monomere umfassen polyhalogenierte aromatische Verbindungen wie z p-Chlorbenzol und 1,2,4-Trichlorbenzol; ungesättigte organische Lösungsmittel wie Styrol und Vinyltoluol, Acrylamid und verwandte Verbindungen, Phenole, ɛ-Caprolactam und ζ-Aminobutyrolactam. Einige der weit verbreiteten neurotoxischen Monomere und ihre Wirkung auf das Nervensystem sind in Tabelle 3 aufgeführt. Eine berufliche Exposition gegenüber neurotoxischen Monomeren kann in Industrien stattfinden, die chemische Produkte und Kunststoffprodukte herstellen, transportieren und verwenden. Beim Umgang mit Polymeren, die Restmonomere enthalten, und beim Formen in Werften und Zahnkliniken findet eine erhebliche Exposition gegenüber neurotoxischen Monomeren statt. Bei Kontakt mit diesen Monomeren kann eine Aufnahme während der Inhalation (z. B. Schwefelkohlenstoff und Styrol) oder durch Hautkontakt (z. B. Acrylamid) erfolgen. Da Monomere eine heterogene Gruppe von Chemikalien sind, sind mehrere unterschiedliche Toxizitätsmechanismen wahrscheinlich. Dies spiegelt sich in Unterschieden in den Symptomen wider (Tabelle 4).
Tabelle 4. Neurotoxische Monomere
|
Compounds |
Beispiele für Expositionsquellen |
Ausgewählte Branchen in Gefahr |
Effekte1 |
|
Acrylamid |
Mitarbeiter, die dem Monomer ausgesetzt sind |
Polymerherstellung; Tunnel- und Bohrarbeiten |
M: Beeinträchtigter axonaler Transport C: Polyneuropathie; Schwindel; Zittern und Ataxie |
|
Acrylnitril |
Unfälle in Labors und Industrien; Hausbegasung |
Polymer- und Gummiherstellung; chemische Synthese |
A: Übererregbarkeit; Speichelfluss; Erbrechen; Zyanose; Ataxia; Schwierigkeiten beim Atmen |
|
Schwefelkohlenstoff |
Herstellung von Gummi und Viskose |
Gummi- und Viskoseindustrie |
M: Eine Beeinträchtigung des axonalen Transports und der Enzymaktivität ist wahrscheinlich C: Periphere Neuropathie; Enzephalopathie; Kopfschmerzen; Schwindel; Magen-Darm-Störungen |
|
Styrol |
Herstellung von glasfaserverstärkten Kunststoffen; Monomerherstellung und -transport; Verwendung von styrolhaltigen Harzen und Beschichtungen |
Chemieindustrie; Glasfaser-Produktion; Polymerindustrie |
M: Unbekannt A: Depression des zentralen Nervensystems; Kopfschmerzen C: Polyneuropathie; Enzephalopathie; Schwerhörigkeit |
|
Vinyltoluol |
Harzproduktion; Insektizide Verbindungen |
Chemie- und Polymerindustrie |
C: Polyneuropathie; reduzierte motorische Nervenleitgeschwindigkeit |
1 M: Mechanismus; A: akute Wirkungen; C: chronische Wirkungen.
Neuropathie: Funktionsstörung motorischer und sensorischer peripherer Nervenfasern.
Enzephalopathie: Funktionsstörung des Gehirns aufgrund einer generalisierten Beeinträchtigung des Gehirns.
Ataxie: beeinträchtigte motorische Koordination.
Organische Lösungsmittel
Organische Lösungsmittel ist eine gebräuchliche Bezeichnung für eine große Gruppe von mehr als 200 lipophilen chemischen Verbindungen, die in der Lage sind, Fette, Öle, Wachse, Harze, Gummi, Asphalt, Zellulosefäden und Kunststoffe zu lösen. Sie sind bei Raumtemperatur normalerweise Flüssigkeiten mit Siedepunkten unter 200 bis 250 °C und verdampfen leicht. Sie werden hauptsächlich über die Lunge aufgenommen, einige können aber auch die Haut durchdringen. Aufgrund ihrer Lipophilie werden sie in fettreiche Organe verteilt. So finden sich hohe Konzentrationen in Körperfett, Knochenmark, Leber und Gehirn, die ebenfalls als Lösungsmittelreservoirs fungieren können. Der Verteilungskoeffizient Oktanol/Wasser kann Aufschluss darüber geben, ob mit hohen Hirnkonzentrationen zu rechnen ist. Der Mechanismus der Toxizität ist noch nicht bekannt, aber es wurden mehrere Möglichkeiten ins Auge gefasst: Blockierung wichtiger Enzyme beim metabolischen Abbau von Glukose und damit Verringerung der für die neuronale Verarbeitung verfügbaren Energie; Verringerung der Energiebildung in den Mitochondrien; Veränderung neuronaler Membranen, was zu einer Beeinträchtigung der Ionenkanalfunktion führt; Verlangsamung des axonalen Flusses. Methylenchlorid wird zu CO verstoffwechselt, das den Sauerstofftransport im Blut blockiert. Große Gruppen von Arbeitnehmern in den unterschiedlichsten Berufen sind täglich oder zumindest häufig exponiert (siehe Tabelle 5). In einigen Ländern ist der Verbrauch von organischen Lösungsmitteln in einigen Berufen aufgrund hygienischer Verbesserungen und Substitution zurückgegangen (z. B. Anstreicher, Arbeiter in der grafischen Industrie, Metallarbeiter), während sich in anderen Berufen das Expositionsmuster geändert hat, aber die Gesamtmenge an organischen Lösungsmitteln ist unverändert geblieben. Beispielsweise wurde Trichlorethylen durch 1,1,1-Trichlorethan und Freon ersetzt. So sind Lösemittel an vielen Arbeitsplätzen noch immer ein großes hygienisches Problem. Menschen sind besonders gefährdet, wenn sie in kleinen Räumen mit schlechter Belüftung und hohen Temperaturen exponiert sind, was die Verdunstung erhöht. Körperliche Arbeit erhöht die pulmonale Aufnahme von Lösungsmitteln. In mehreren Ländern (insbesondere in den nordischen Ländern) wurde Arbeitnehmern, die nach längerer Exposition gegenüber Lösungsmitteln in geringer Konzentration eine chronische toxische Enzephalopathie entwickelt haben, eine Entschädigung gewährt.
Tabelle 5. Mit Neurotoxizität assoziierte organische Lösungsmittel
|
Chemical |
Beispiele für Expositionsquellen |
Ausgewählte Branchen in Gefahr |
Effekte1 |
|
Chlorierte Kohlenwasserstoffe: Trichlorethylen; 1,1,1-Trichlorethan; Tetrachlorethylen |
Entfetten; Galvanik; malen; Drucken; Reinigung; Vollnarkose und leichte Anästhesie |
Metallindustrie; grafische Industrie; elektronische Industrie; chemische Reinigungen; Anästhesisten |
M: Unbekannt A: Pränarkotische Symptome C: Enzephalopathie; Polyneuropathie; Trigeminusaffektion (TRI); Schwerhörigkeit |
|
Methylenchlorid |
Extraktion, einschließlich Extraktion von Koffein; Farbentferner |
Nahrungsmittelindustrie; Maler; grafische Industrie |
M: Stoffwechsel ® CO A: Pränarkotische Symptome; Koma C: Enzephalopathie |
|
Methylchlorid |
Herstellung und Reparatur von Kühlschränken |
Kühlschrank-Produktion; Gummiindustrie; Kunststoffindustrie |
M: Unbekannt A: Pränarkotische Symptome; Bewusstseinsverlust; Tod C: Enzephalopathie |
|
Toluol |
Drucken; Reinigung; Entfetten; Galvanik; malen; Spritzlackierung |
Grafische Industrie; elektronische Industrie |
M: Unbekannt A: Pränarkotische Symptome C: Enzephalopathie; zerebelläre Dysfunktion; Polyneuropathie; Schwerhörigkeit; visuelle Störung |
|
Xylen |
Drucken; Synthese von Phthalsäureanhydrid; malen; histologische Laborverfahren |
Grafische Industrie; Kunststoffindustrie; Histologische Laboratorien |
M: Unbekannt A: Pränarkotische Symptome C: Enzephalopathie; visuelle Störung; Schwerhörigkeit |
|
Styrol |
Polymerisation; Formteil |
Kunststoffindustrie; Glasfaserproduktion |
M: Unbekannt A: Pränarkotische Symptome C: Enzephalopathie; Polyneuropathie; Schwerhörigkeit |
|
Hexacarbone: n-Hexan; Methylbutylketon (MBK); Methylethylketon (MEK) |
Kleben; Drucken; Kunststoffbeschichtung; malen; Extraktion |
Leder- und Schuhindustrie; grafische Industrie; Maler; Labore |
M: Beeinträchtigung des axonalen Transports A: Pränarkotisch C: Polyneuropathie; Enzephalopathie |
|
Verschiedene Lösungsmittel: Freon 113 |
Herstellung und Reparatur von Kühlschränken; chemische Reinigung; Entfetten |
Kühlschrank-Produktion; Metallindustrie; elektronische Industrie; chemische Reinigung |
M: Unbekannt A: Leichte pränarkotische Symptome C: Enzephalopathie |
|
Diethylether; Halothan |
Allgemeinanästhesie (Krankenschwestern; Ärzte) |
Krankenhäuser; Kliniken |
M: Unbekannt A: Pränarkotische Symptome C: Enzephalopathie |
|
Schwefelkohlenstoff |
Siehe Monomere |
Siehe Monomere |
Siehe Monomere |
|
Mischungen: Testbenzin und Verdünnung |
Malen; Entfetten; Reinigung; Drucken; Imprägnierung; Oberflächenbehandlung |
Metallindustrie; grafische Industrie; Holzindustrie; Maler |
M: Unbekannt A: Pränarkotische Symptome C: Enzephalopathie |
1 M: Mechanismus; A: akute Wirkungen; C: chronische Wirkungen.
Neuropathie: Funktionsstörung motorischer und sensorischer peripherer Nervenfasern.
Enzephalopathie: Funktionsstörung des Gehirns aufgrund einer generalisierten Beeinträchtigung des Gehirns
Pestizide
Pestizide wird als Oberbegriff für jede Chemikalie verwendet, die dazu bestimmt ist, Gruppen von Pflanzen oder Tieren zu töten, die eine Gefahr für die menschliche Gesundheit darstellen oder wirtschaftliche Verluste verursachen können. Es umfasst Insektizide, Fungizide, Rodentizide, Begasungsmittel und Herbizide. Ungefähr 5 Milliarden Pfund Pestizidprodukte, die aus mehr als 600 Pestizidwirkstoffen bestehen, werden jährlich weltweit in der Landwirtschaft verwendet. Organophosphor-, Carbamat- und Organochlor-Pestizide haben zusammen mit Pyrethroiden, Chlorphenoxy-Herbiziden und organischen Metallverbindungen, die als Fungizide verwendet werden, neurotoxische Eigenschaften (Tabelle 6). Unter den vielen verschiedenen Chemikalien, die als Rodentizide verwendet werden, sind einige (z. B. Strychnin, Zinkphosphid und Thallium) auch neurotoxisch. Die berufliche Exposition gegenüber neurotoxischen Pestiziden ist hauptsächlich mit landwirtschaftlichen Arbeiten wie dem Umgang mit Pestiziden und der Arbeit mit behandelten Pflanzen verbunden, aber Kammerjäger, Mitarbeiter in der Pestizidherstellung und -formulierung, Straßen- und Eisenbahnarbeiter sowie Arbeiter in Gewächshäusern, Forstwirtschaft und Baumschulen können einem erheblichen Risiko ausgesetzt sein auch neurotoxischen Pestiziden ausgesetzt zu sein. Kinder, die einen erheblichen Teil der landwirtschaftlichen Arbeitskräfte ausmachen, sind besonders gefährdet, da ihr Nervensystem noch nicht voll entwickelt ist. Die akuten Wirkungen von Pestiziden sind im Allgemeinen gut beschrieben, und lang anhaltende Wirkungen bei wiederholter Exposition oder einmaliger Exposition in hoher Dosis werden oft beobachtet (Tabelle 6), aber die Wirkung einer wiederholten subklinischen Exposition ist ungewiss.
Tabelle 6. Klassen üblicher neurotoxischer Pestizide, Exposition, Wirkungen und damit verbundene Symptome
|
Compounds |
Beispiele für Expositionsquellen |
Ausgewählte Branchen in Gefahr |
Effekte1 |
|
Organo-Phosphor-Verbindungen: Beomyl; Dämon; Dichlorvos; Ethylparathion; Mevinphos; Phosfolan; Terbufos; Malathion |
Handhabung; Behandlung von Feldfrüchten; Arbeiten mit behandelten Pflanzen; Hafenarbeiter |
Landwirtschaft; Forstwirtschaft; chemisch; Gartenarbeit |
M: Acetylcholinesterase-Hemmung A: Hyperaktivität; neuromuskuläre Lähmung; Sehbehinderung; Atembeschwerden; Unruhe; die Schwäche; Erbrechen; Krämpfe |
|
Carbamate: Aldicarb; Carbaryl; Carbofuran; Propoxur |
M: Axonopathie mit verzögerter Neurotoxizität2 C: Polyneuropathie; Taubheit und Kribbeln in den Füßen; Muskelschwäche; sensorische Störung; Lähmung |
||
|
Organochlor: Aldrin; Dieldrin; DDT; Endrin; Heptachlor; Lindan; Methoxychlor; Mirex; Toxaphen |
Siehe oben |
Siehe oben |
A: Erregbarkeit; Auffassung; Schwindel; Kopfschmerzen; Verwirrtheit; Gleichgewichtsverlust; die Schwäche; Ataxia; Zittern; Krämpfe; Koma C: Enzephalopathie |
|
Pyrethroiden |
Siehe oben |
Siehe oben |
M: Änderung des Flusses von Natriumionen durch die Nervenzellmembran A: Wiederholtes Feuern der Nervenzelle; Tremor; Konvulsion |
|
2,4-D |
Herbizid |
Landwirtschaft |
C: Polyneuropathie |
|
Triethylzinnhydroxid |
Oberflächenbehandlung; Umgang mit behandeltem Holz |
Holz und Holzprodukte |
A: Kopfschmerzen; die Schwäche; Lähmung; Sehstörungen C: Polyneuropathie; ZNS-Effekte |
|
Methylbromid |
Ausräuchern |
Gewächshäuser; Insektizid; Herstellung von Kühlschränken |
M: Unbekannt A: Seh- und Sprachstörungen; Delirium; Konvulsion C: Enzephalopathie |
1 M: Mechanismus; A: akute Wirkungen; C: chronische Wirkungen.
Neuropathie: Funktionsstörung motorischer und sensorischer peripherer Nervenfasern.
Enzephalopathie: Funktionsstörung des Gehirns aufgrund einer generalisierten Beeinträchtigung des Gehirns.
Ataxie: beeinträchtigte motorische Koordination.
2 Hauptsächlich Phosphate oder Phosphonate.
Andere Chemikalien
Mehrere verschiedene Chemikalien, die nicht in die oben genannten Gruppen passen, besitzen ebenfalls Neurotoxizität. Einige davon werden als Pestizide, aber auch in verschiedenen industriellen Prozessen verwendet. Einige haben gut dokumentierte akute und chronische neurotoxische Wirkungen; andere haben offensichtliche akute Wirkungen, aber die chronischen Wirkungen sind nur unzureichend untersucht. Beispiele für diese Chemikalien, ihre Verwendungen und Wirkungen sind in Tabelle 7 aufgeführt.
Tabelle 7. Andere mit Neurotoxizität assoziierte Chemikalien
|
Chemical |
Beispiele für Expositionsquellen |
Ausgewählte Branchen in Gefahr |
Effekte1 |
|
Borsäure |
Schweißen; Flussmittel; Erhaltung |
Metall; Glas |
A: Delirium; Konvulsion C: ZNS-Depression. |
|
Disulfiram |
Biowissenschaften |
Gummi |
C: Ermüdung; periphere Neuropathie; Schläfrigkeit |
|
Hexachlorophen |
Antibakterielle Seifen |
Chemical |
C: ZNS-Ödem; Schädigung der peripheren Nerven |
|
Hydrazin |
Reduktionsmittel |
Chemisch; Heer |
A: Aufregung; Appetitlosigkeit; Tremor; Konvulsion |
|
Phenol/Kresol |
Antiseptika |
Kunststoffe; Harze; chemisch; Krankenhäuser; Labore |
M: Denaturiert Proteine und Enzyme A: Reflexverlust; die Schwäche; Tremor; Schwitzen; Koma C: Appetitlosigkeit; Geistesstörung; Klingeln in den Ohren |
|
Pyridin |
Ethanol-Denaturierung |
Chemisch; Textil- |
A: ZNS-Depression; mentale Depression; Ermüdung; Appetitverlust C: Reizbarkeit; Schlafstörungen; Polyneuropathie; doppeltes Sehen |
|
Tetraethyl Blei |
Benzinzusatz |
Chemisch; Transport |
C: Reizbarkeit; die Schwäche; Tremor; Sehschwierigkeiten |
|
Arsin |
Batterien; Insektizid; schmelzen |
Schmelzen; Glasarbeiten; Keramik; Herstellung von Papier |
M: Beeinträchtigung der Enzymfunktion A: Reduzierte Empfindung; Parese; Konvulsion; Koma C: Motorische Beeinträchtigung; Ataxia; Verlust des Vibrationsgefühls; Polyneuropathie |
|
Lithium |
Ölzusatz; pharmazeutisch |
Petrochemischer Markt |
A / C: Appetitlosigkeit; Klingeln in den Ohren; verschwommenes Sehen; Tremor; Ataxia |
|
Selenium |
Schmelzen; Herstellung von Gleichrichtern; Vulkanisation; Schneidöle; Antioxidans |
Elektronisch; Glashütten; Metallindustrie; Gummiindustrie |
A: Delirium; Anosmie C: Geruch nach Knoblauch; Polyneuropathie; Nervosität |
|
Thallium |
Rodentizid |
Glas; Glasprodukte |
A: Appetitverlust; Müdigkeit; Schläfrigkeit; metallischer Geschmack; Taubheit; Ataxia |
|
Tellur |
Schmelzen; Gummi-Produktion; Katalysator |
Metall; chemisch; Gummi; elektronisch |
A: Kopfschmerzen; Schläfrigkeit; Neuropathie C: Geruch nach Knoblauch; metallischer Geschmack; Parkinsonismus; Depression |
|
Vanadium |
Schmelzen |
Bergbau; Stahlproduktion; Chemieindustrie |
A: Appetitverlust; Klingeln in den Ohren; Schläfrigkeit, Zittern C: Depression; Tremor; Blindheit |
1 M: Mechanismus; A: akute Wirkungen; C: chronische Wirkungen.
Neuropathie: Funktionsstörung motorischer und sensorischer peripherer Nervenfasern.
Enzephalopathie: Funktionsstörung des Gehirns aufgrund einer generalisierten Beeinträchtigung des Gehirns.
Ataxie: beeinträchtigte motorische Koordination
Manifestationen akuter und früher chronischer Vergiftungen
Das aktuelle Wissen über die kurz- und langfristigen Manifestationen einer Exposition gegenüber neurotoxischen Substanzen stammt aus experimentellen Tierstudien und Humankammerstudien, epidemiologischen Studien an aktiven und pensionierten und/oder kranken Arbeitern, klinischen Studien und Berichten sowie Großkatastrophen , wie jene, die in Bhopal nach einem Leck von Methylisocyanat und in Minamata aufgrund einer Methylquecksilbervergiftung auftraten.
Die Exposition gegenüber neurotoxischen Stoffen kann Sofortwirkungen (akut) und/oder Langzeitwirkungen (chronisch) hervorrufen. In beiden Fällen können die Wirkungen reversibel sein und mit der Zeit nach Verringerung oder Beendigung der Exposition verschwinden oder zu dauerhaften, irreversiblen Schäden führen. Die Schwere der akuten und chronischen Beeinträchtigung des Nervensystems hängt von der Expositionsdosis ab, die sowohl die Menge als auch die Dauer der Exposition umfasst. Wie Alkohol und Freizeitdrogen können viele neurotoxische Substanzen anfangs erregend sein, ein Gefühl von Wohlbefinden oder Euphorie hervorrufen und/oder motorische Funktionen beschleunigen; Wenn die Dosis mengenmäßig oder zeitlich zunimmt, werden dieselben Neurotoxine das Nervensystem dämpfen. In der Tat wird Narkose (ein Zustand der Benommenheit oder Betäubung) durch eine große Anzahl neurotoxischer Substanzen hervorgerufen, die bewusstseinsverändernd sind und das zentrale Nervensystem schwächen.
Akute Vergiftung
Akute Wirkungen spiegeln die unmittelbare Reaktion auf die chemische Substanz wider. Die Schwere der Symptome und daraus resultierenden Störungen hängt von der Menge ab, die das Nervensystem erreicht. Bei leichter Exposition sind die akuten Wirkungen mild und vorübergehend und verschwinden, wenn die Exposition aufhört. Kopfschmerzen, Müdigkeit, Benommenheit, Konzentrationsschwierigkeiten, Trunkenheitsgefühle, Euphorie, Reizbarkeit, Schwindel und verlangsamte Reflexe sind die Arten von Symptomen, die auftreten, wenn man neurotoxischen Chemikalien ausgesetzt ist. Obwohl diese Symptome reversibel sind, treten die Symptome auch wieder auf, wenn die Exposition Tag für Tag wiederholt wird. Da die neurotoxische Substanz nicht sofort aus dem Körper ausgeschieden wird, können die Symptome auch nach der Arbeit bestehen bleiben. Gemeldete Symptome an einem bestimmten Arbeitsplatz spiegeln gut eine chemische Störung des Nervensystems wider und sollten als Warnsignal für eine mögliche Überexposition betrachtet werden; es sollten vorbeugende Maßnahmen zur Reduzierung der Exposition eingeleitet werden.
Wenn die Exposition sehr hoch ist, wie es bei Verschüttungen, Lecks, Explosionen und anderen Unfällen vorkommen kann, sind die Symptome und Anzeichen einer Vergiftung schwächend (starke Kopfschmerzen, geistige Verwirrtheit, Übelkeit, Schwindel, Koordinationsstörungen, verschwommenes Sehen, Bewusstlosigkeit); Wenn die Exposition hoch genug ist, können die Auswirkungen langanhaltend sein und möglicherweise zu Koma und Tod führen.
Akute pestizidbedingte Erkrankungen sind bei Landarbeitern in Lebensmittel produzierenden Ländern, wo große Mengen toxischer Substanzen als Insektizide, Fungizide, Nematizide und Herbizide verwendet werden, weit verbreitet. Organophosphate, Carbamate, Organochlorine, Pyrethrum, Pyrethrin, Paraquat und Diquat gehören zu den Hauptkategorien von Pestiziden; Es gibt jedoch Tausende von Pestizidformulierungen, die Hunderte verschiedener Wirkstoffe enthalten. Einige Pestizide wie Maneb enthalten Mangan, während andere in organischen Lösungsmitteln gelöst sind. Zusätzlich zu den oben genannten Symptomen kann eine akute Organophosphat- und Carbamatvergiftung von Speichelfluss, Inkontinenz, Krämpfen, Muskelzuckungen, Durchfall, Sehstörungen sowie Atembeschwerden und Herzrasen begleitet sein; diese resultieren aus einem Überschuss des Neurotransmitters Acetylcholin, der auftritt, wenn diese Substanzen eine Chemikalie namens Cholinesterase angreifen. Die Cholinesterase im Blut nimmt proportional zum Grad der akuten Organophosphat- oder Carbamatvergiftung ab.
Bei manchen Substanzen, wie z. B. Organophosphor-Pestiziden und Kohlenmonoxid, kann eine hochgradige akute Exposition zu einer verzögerten Verschlechterung bestimmter Teile des Nervensystems führen. Bei Ersterem können einige Wochen nach der Exposition Taubheit und Kribbeln, Schwäche und Ungleichgewicht auftreten, während bei Letzterem eine verzögerte neurologische Verschlechterung mit Symptomen von geistiger Verwirrtheit, Ataxie, motorischer Koordinationsstörung und Parese eintreten kann. Wiederholte akute Episoden hoher Kohlenmonoxidspiegel wurden mit Parkinsonismus im späteren Leben in Verbindung gebracht. Es ist möglich, dass eine hohe Exposition gegenüber bestimmten neurotoxischen Chemikalien mit einem erhöhten Risiko für neurodegenerative Erkrankungen im späteren Leben einhergeht.
Chronische Vergiftung
Die Erkenntnis der Gefahren neurotoxischer Chemikalien hat viele Länder dazu veranlasst, die zulässigen Belastungsgrenzen zu reduzieren. Für die meisten Chemikalien ist jedoch noch unbekannt, bei welcher Konzentration keine nachteiligen Auswirkungen bei längerer Exposition auftreten. Die wiederholte Exposition gegenüber niedrigen bis mittleren Konzentrationen neurotoxischer Substanzen über viele Monate oder Jahre hinweg kann die Funktionen des Nervensystems auf heimtückische und fortschreitende Weise verändern. Fortgesetzte Eingriffe in molekulare und zelluläre Prozesse führen zu langsamen Veränderungen neurophysiologischer und psychologischer Funktionen, die in den frühen Stadien unbemerkt bleiben können, da in den Schaltkreisen des Nervensystems große Reserven vorhanden sind und Schäden in den ersten Stadien durch neues Lernen kompensiert werden können.
Daher wird eine anfängliche Schädigung des Nervensystems nicht notwendigerweise von funktionellen Störungen begleitet und kann reversibel sein. Mit fortschreitendem Schaden werden jedoch Symptome und Anzeichen, die oft unspezifischer Natur sind, offensichtlich, und Personen können einen Arzt aufsuchen. Schließlich kann die Beeinträchtigung so schwerwiegend werden, dass sich ein klares, im Allgemeinen irreversibles klinisches Syndrom manifestiert.
Abbildung 1 schematisiert das Kontinuum der gesundheitlichen Verschlechterung im Zusammenhang mit der Exposition gegenüber neurotoxischen Substanzen. Das Fortschreiten der neurotoxischen Dysfunktion hängt sowohl von der Dauer als auch von der Konzentration der Exposition (Dosis) ab und kann durch andere Faktoren am Arbeitsplatz, den individuellen Gesundheitszustand und die Anfälligkeit sowie den Lebensstil beeinflusst werden, insbesondere durch Alkoholkonsum und die Exposition gegenüber neurotoxischen Substanzen, die bei Hobbys verwendet werden, wie z Klebstoffe für die Möbelmontage oder den Kunststoffmodellbau, Farben und Farbentferner.
Abbildung 1. Gesundheitsverschlechterung auf einem Kontinuum mit zunehmender Dosierung
Es werden verschiedene Strategien zur Identifizierung neurotoxinbedingter Krankheiten bei einzelnen Arbeitern und zur Überwachung einer frühen Verschlechterung des Nervensystems bei aktiven Arbeitern angewandt. Die klinische Diagnose stützt sich auf eine Konstellation von Anzeichen und Symptomen, die mit der Kranken- und Expositionsgeschichte einer Person gekoppelt sind; Andere Ursachen als die Exposition müssen systematisch ausgeschlossen werden. Für die Überwachung der frühen Dysfunktion bei aktiven Arbeitern ist das Gruppenportrait der Dysfunktion wichtig. Meistens ist das für die Gruppe beobachtete Dysfunktionsmuster dem klinisch bei der Krankheit beobachteten Muster der Beeinträchtigung ähnlich. Es ist ungefähr so, als würde man frühe, leichte Veränderungen zusammenfassen, um ein Bild davon zu erhalten, was mit dem Nervensystem passiert. Das Muster oder Profil der gesamten frühen Reaktion liefert einen Hinweis auf die Spezifität und die Art der Wirkung der jeweiligen neurotoxischen Substanz oder Mischung. An Arbeitsplätzen mit potenzieller Exposition gegenüber neurotoxischen Stoffen kann sich die Gesundheitsüberwachung von Arbeitnehmergruppen als besonders nützlich für die Prävention und Maßnahmen am Arbeitsplatz erweisen, um die Entwicklung schwererer Erkrankungen zu vermeiden (siehe Abbildung 2). Weltweit durchgeführte Arbeitsplatzstudien mit aktiven Arbeitern, die bestimmten neurotoxischen Substanzen oder Mischungen verschiedener Chemikalien ausgesetzt waren, haben wertvolle Informationen über frühe Manifestationen von Funktionsstörungen des Nervensystems in Gruppen von exponierten Arbeitern geliefert.
Abbildung 2. Neurotoxizität am Arbeitsplatz verhindern.
Frühe Symptome einer chronischen Vergiftung
Veränderte Stimmungszustände sind meistens die ersten Symptome der anfänglichen Veränderungen in der Funktion des Nervensystems. Reizbarkeit, Euphorie, plötzliche Stimmungsschwankungen, übermäßige Müdigkeit, feindselige Gefühle, Ängstlichkeit, Depression und Anspannung gehören zu den Stimmungszuständen, die am häufigsten mit neurotoxischen Expositionen in Verbindung gebracht werden. Andere Symptome sind Gedächtnisprobleme, Konzentrationsschwierigkeiten, Kopfschmerzen, verschwommenes Sehen, Trunkenheitsgefühle, Schwindel, Langsamkeit, Kribbeln in Händen oder Füßen, Libidoverlust und so weiter. Obwohl diese Symptome in den frühen Stadien normalerweise nicht stark genug sind, um die Arbeit zu beeinträchtigen, spiegeln sie ein vermindertes Wohlbefinden wider und beeinträchtigen die Fähigkeit, familiäre und soziale Beziehungen in vollem Umfang zu genießen. Aufgrund der unspezifischen Natur dieser Symptome neigen Arbeitnehmer, Arbeitgeber und Arbeitsmediziner häufig dazu, sie zu ignorieren und nach anderen Ursachen als der Exposition am Arbeitsplatz zu suchen. Tatsächlich können solche Symptome zu einer bereits schwierigen persönlichen Situation beitragen oder diese verschlimmern.
An Arbeitsplätzen, an denen neurotoxische Substanzen verwendet werden, sollten sich Arbeitnehmer, Arbeitgeber und Arbeitsschutzpersonal besonders der Symptomatologie einer frühen Vergiftung bewusst sein, die auf eine Anfälligkeit des Nervensystems gegenüber einer Exposition hinweist. Für Arbeitsplatzstudien und die Überwachung von Arbeitsplätzen, an denen neurotoxische Substanzen verwendet werden, wurden Symptomfragebögen entwickelt. Tabelle 1 enthält ein Beispiel für einen solchen Fragebogen.
Tabelle 1. Checkliste für chronische Symptome
Symptome, die im letzten Monat aufgetreten sind
1. Sind Sie aufgrund der Art von Aktivität, die Sie ausüben, leichter ermüdet als erwartet?
2. Haben Sie sich benommen oder schwindelig gefühlt?
3. Hatten Sie Konzentrationsschwierigkeiten?
4. Waren Sie verwirrt oder desorientiert?
5. Hatten Sie Probleme, sich an Dinge zu erinnern?
6. Haben Ihre Angehörigen bemerkt, dass Sie Probleme haben, sich an Dinge zu erinnern?
7. Mussten Sie sich Notizen machen, um sich an Dinge zu erinnern?
8. Ist es Ihnen schwer gefallen, die Bedeutung von Zeitungen zu verstehen?
9. Haben Sie sich gereizt gefühlt?
10. Haben Sie sich deprimiert gefühlt?
11. Hatten Sie Herzklopfen, auch wenn Sie sich nicht anstrengen?
12. Hatten Sie einen Anfall?
13. Haben Sie öfter als sonst geschlafen?
14. Hatten Sie Schwierigkeiten beim Einschlafen?
15. Wurden Sie von Koordinationsstörungen oder Gleichgewichtsverlust geplagt?
16. Hatten Sie Muskelkraftverlust in Ihren Beinen oder Füßen?
17. Hatten Sie Muskelkraftverlust in Ihren Armen oder Händen?
18. Hatten Sie Schwierigkeiten, Ihre Finger zu bewegen oder Dinge zu greifen?
19. Hatten Sie Taubheit und Kribbeln in den Fingern, die länger als einen Tag anhielten?
20. Hatten Sie ein Taubheitsgefühl in den Händen und ein Kribbeln in den Zehen, das länger als einen Tag anhielt?
21. Hatten Sie mindestens einmal pro Woche Kopfschmerzen?
22. Hatten Sie Schwierigkeiten, von der Arbeit nach Hause zu fahren, weil Sie sich schwindelig oder müde fühlten?
23. Haben Sie sich von den bei der Arbeit verwendeten Chemikalien „high“ gefühlt?
24. Hatten Sie eine geringere Alkoholtoleranz (brauchen Sie weniger, um betrunken zu werden)?
Quelle: Entnommen aus Johnson 1987.
Frühe motorische, sensorische und kognitive Veränderungen bei chronischer Vergiftung
Mit zunehmender Exposition können bei Arbeitern, die neurotoxischen Substanzen ausgesetzt sind, Veränderungen der motorischen, sensorischen und kognitiven Funktionen beobachtet werden, die keine klinischen Anzeichen einer Anomalie aufweisen. Da das Nervensystem komplex ist und bestimmte Bereiche anfällig für bestimmte Chemikalien sind, während andere empfindlich auf die Wirkung einer großen Anzahl toxischer Stoffe reagieren, kann ein breites Spektrum von Funktionen des Nervensystems durch einen einzelnen toxischen Stoff oder eine Mischung davon beeinträchtigt werden Neurotoxine. Reaktionszeit, Hand-Augen-Koordination, Kurzzeitgedächtnis, visuelles und auditives Gedächtnis, Aufmerksamkeit und Wachsamkeit, manuelle Geschicklichkeit, Wortschatz, Aufmerksamkeitswechsel, Griffstärke, Motorgeschwindigkeit, Handstabilität, Stimmung, Farbsehen, vibrotaktile Wahrnehmung, Hören und Riechen gehören zu den vielen Funktionen, die nachweislich durch verschiedene neurotoxische Substanzen verändert werden.
Wichtige Informationen über die Art der frühen Defizite, die sich aus der Exposition ergeben, wurden durch den Vergleich der Leistung zwischen exponierten und nicht exponierten Arbeitnehmern und in Bezug auf das Ausmaß der Exposition geliefert. Anger (1990) bietet einen ausgezeichneten Überblick über die Forschung zum neurologischen Verhalten am Arbeitsplatz bis 1989. Tabelle 2, die diesem Artikel entnommen wurde, liefert ein Beispiel für die Art von neurofunktionellen Defiziten, die in Gruppen von aktiven Arbeitern, die einigen der am meisten ausgesetzt waren, beständig beobachtet wurden gängige neurotoxische Substanzen.
Tabelle 2. Kontinuierliche neurofunktionelle Wirkungen von Expositionen am Arbeitsplatz gegenüber einigen führenden neurotoxischen Substanzen
|
Gemischte organische Lösungsmittel |
Schwefelkohlenstoff |
Styrol |
Organophos- |
Führen (Lead) |
Merkur |
|
|
Erwerb |
+ |
|
|
|
+ |
|
|
Beeinflussen |
+ |
|
+ |
|
+ |
|
|
Kategorisierung |
+ |
|
|
|
|
|
|
Programmierung |
+ |
+ |
|
|
+ |
+ |
|
Farbsehen |
+ |
|
+ |
|
|
|
|
Konzeptverschiebung |
+ |
|
|
|
|
|
|
Ablenkbarkeit |
|
|
|
|
+ |
|
|
Intelligenz |
+ |
+ |
|
+ |
+ |
+ |
|
Memory |
+ |
+ |
+ |
+ |
+ |
+ |
|
Motor Koordination |
+ |
+ |
+ |
|
+ |
+ |
|
Motordrehzahl |
+ |
+ |
+ |
|
+ |
+ |
|
Nahezu visuelle Kontrastempfindlichkeit |
+ |
|
|
|
|
|
|
Geruchswahrnehmungsschwelle |
+ |
|
|
|
|
|
|
Geruchsidentifikation |
+ |
|
|
|
+ |
|
|
Persönlichkeit |
+ |
+ |
|
|
|
+ |
|
Räumliche Beziehungen |
+ |
+ |
|
|
+ |
|
|
Vibrotaktile Schwelle |
+ |
|
|
+ |
|
+ |
|
Wachsamkeit |
+ |
+ |
|
|
+ |
|
|
Sichtfeld |
|
|
|
|
+ |
+ |
|
Wortschatz |
|
|
|
|
+ |
|
Quelle: Adaptiert von Anger 1990.
Obwohl der Verlust in diesem Stadium des Kontinuums von Wohlbefinden zu Krankheit nicht im klinisch abnormalen Bereich liegt, können mit solchen Veränderungen gesundheitliche Folgen verbunden sein. Zum Beispiel können eine verminderte Wachsamkeit und verminderte Reflexe die Arbeiter einer größeren Unfallgefahr aussetzen. Der Geruch wird verwendet, um Lecks zu identifizieren und die Sättigung (Patronendurchbruch) zu maskieren, und ein akuter oder chronischer Geruchsverlust macht es weniger geeignet, eine potenziell gefährliche Situation zu erkennen. Stimmungsschwankungen können die zwischenmenschlichen Beziehungen bei der Arbeit, in der Gesellschaft und zu Hause beeinträchtigen. Diese Anfangsstadien der Verschlechterung des Nervensystems, die beobachtet werden können, indem man Gruppen exponierter Arbeiter untersucht und sie mit nicht exponierten Arbeitern oder in Bezug auf ihren Expositionsgrad vergleicht, spiegeln ein vermindertes Wohlbefinden wider und können auf das Risiko ernsterer neurologischer Erkrankungen hinweisen Probleme in der Zukunft.
Psychische Gesundheit bei chronischer Vergiftung
Neuropsychiatrische Störungen werden seit langem der Exposition gegenüber neurotoxischen Substanzen zugeschrieben. Klinische Beschreibungen reichen von affektiven Störungen, einschließlich Angst und Depression, bis hin zu Manifestationen von psychotischem Verhalten und Halluzinationen. Akute hochgradige Exposition gegenüber vielen Schwermetallen, organischen Lösungsmitteln und Pestiziden kann Delirium hervorrufen. „Manganwahnsinn“ wurde bei Personen mit Langzeitexposition gegenüber Mangan beschrieben, und das bekannte „Mad Hater“-Syndrom resultiert aus einer Quecksilbervergiftung. Die toxische Enzephalopathie Typ 2a, gekennzeichnet durch anhaltende Persönlichkeitsveränderungen mit Müdigkeit, emotionaler Labilität, Impulskontrolle und allgemeiner Stimmung und Motivation, wurde mit der Exposition gegenüber organischen Lösungsmitteln in Verbindung gebracht. Es gibt zunehmend Hinweise aus klinischen und bevölkerungsbezogenen Studien, dass Persönlichkeitsstörungen im Laufe der Zeit bestehen bleiben, lange nachdem die Exposition beendet wurde, obwohl sich andere Arten von Beeinträchtigungen bessern können.
Auf dem Kontinuum von Wohlbefinden bis Krankheit sind Stimmungsschwankungen, Reizbarkeit und übermäßige Müdigkeit oft die allerersten Anzeichen einer übermäßigen Exposition gegenüber neurotoxischen Substanzen. Obwohl neuropsychiatrische Symptome routinemäßig in Arbeitsplatzstudien erfasst werden, werden diese selten als psychisches Gesundheitsproblem mit möglichen Folgen für das psychische und soziale Wohlbefinden dargestellt. Zum Beispiel wirken sich Änderungen des psychischen Gesundheitszustands auf das eigene Verhalten aus und tragen zu schwierigen zwischenmenschlichen Beziehungen und Meinungsverschiedenheiten zu Hause bei; diese wiederum können den seelischen Zustand verschlimmern. An Arbeitsplätzen mit Mitarbeiterhilfsprogrammen, die Mitarbeitern bei persönlichen Problemen helfen sollen, kann die Unkenntnis der potenziellen psychischen Auswirkungen einer Exposition gegenüber neurotoxischen Substanzen zu einer Behandlung führen, die sich eher mit den Auswirkungen als mit der Ursache befasst. Es ist interessant festzustellen, dass unter den vielen gemeldeten Ausbrüchen von „Massenhysterie“ oder psychogenen Erkrankungen Branchen mit Exposition gegenüber neurotoxischen Substanzen überrepräsentiert sind. Es ist möglich, dass diese Substanzen, die größtenteils nicht gemessen wurden, zu den berichteten Symptomen beigetragen haben.
Psychische Manifestationen einer Neurotoxin-Exposition können denen ähneln, die durch psychosoziale Stressoren verursacht werden, die mit einer schlechten Arbeitsorganisation verbunden sind, sowie psychologische Reaktionen auf Unfälle, sehr belastende Ereignisse und schwere Vergiftungen, die als posttraumatische Belastungsstörung bezeichnet werden (wie an anderer Stelle in diesem Artikel beschrieben). Enzyklopädie). Ein gutes Verständnis der Beziehung zwischen psychischen Gesundheitsproblemen und Arbeitsbedingungen ist wichtig, um angemessene vorbeugende und heilende Maßnahmen einzuleiten.
Allgemeine Überlegungen zur Beurteilung früher neurotoxischer Dysfunktionen
Bei der Beurteilung einer frühen Funktionsstörung des Nervensystems bei aktiven Arbeitern müssen eine Reihe von Faktoren berücksichtigt werden. Erstens lassen viele der untersuchten neuropsychologischen und neurophysiologischen Funktionen mit zunehmendem Alter nach; einige werden durch die Kultur oder das Bildungsniveau beeinflusst. Diese Faktoren müssen berücksichtigt werden, wenn die Beziehung zwischen Exposition und Veränderungen des Nervensystems betrachtet wird. Dies kann durch den Vergleich von Gruppen mit ähnlichem soziodemografischem Status oder durch statistische Bereinigungsverfahren erfolgen. Es gibt jedoch einige Fallstricke, die vermieden werden sollten. Beispielsweise haben ältere Arbeitnehmer möglicherweise eine längere Arbeitsgeschichte, und es wurde vermutet, dass einige neurotoxische Substanzen das Altern beschleunigen können. Berufliche Segregation kann schlecht ausgebildete Arbeitnehmer, Frauen und Minderheiten auf Arbeitsplätze mit höherer Exposition beschränken. Zweitens können auch Alkoholkonsum, Rauchen und Drogen, die alle neurotoxische Substanzen enthalten, die Symptome und die Leistungsfähigkeit beeinträchtigen. Ein gutes Verständnis des Arbeitsplatzes ist wichtig, um die verschiedenen Faktoren aufzudecken, die zu Funktionsstörungen des Nervensystems beitragen, und um vorbeugende Maßnahmen umzusetzen.
Neurotoxizität am Arbeitsplatz verhindern
Ein Arbeitnehmer, der keiner neurotoxischen Substanz ausgesetzt ist, wird durch diese Substanz niemals nachteilige neurotoxische Auswirkungen auf die Gesundheit entwickeln. Null-Exposition führt zu vollständigem Schutz vor neurotoxischen Auswirkungen auf die Gesundheit. Dies ist die Essenz aller primärpräventiven Maßnahmen.
Toxizitätsprüfung
Neue chemische Verbindungen, die am Arbeitsplatz und im beruflichen Umfeld eingeführt werden, sollten bereits auf Neurotoxizität getestet worden sein. Das Versäumnis, Toxizitätstests vor dem Inverkehrbringen durchzuführen, kann zu Kontakten mit Arbeitern und potenziell schwerwiegenden gesundheitsschädlichen Auswirkungen führen. Die Einführung von Methyl-n-butylketon an einem Arbeitsplatz in den Vereinigten Staaten ist ein klassisches Beispiel für die möglichen Gefahren der Einführung ungetesteter Neurotoxine am Arbeitsplatz (Spencer und Schaumburg 1980).
Steuereinheit
Technische Kontrollen (z. B. Belüftungssysteme, geschlossene Produktionsanlagen) sind die besten Mittel, um die Exposition der Arbeiter unter den zulässigen Expositionsgrenzen zu halten. Geschlossene chemische Prozesse, die verhindern, dass alle Giftstoffe in die Arbeitsumgebung freigesetzt werden, sind ideal. Wenn dies nicht möglich ist, sind geschlossene Lüftungssysteme, die Umgebungsluftdämpfe abführen und so konstruiert sind, dass sie kontaminierte Luft von den Arbeitern wegziehen, nützlich, wenn sie gut konstruiert, angemessen gewartet und ordnungsgemäß betrieben werden.
Persönliche Schutzausrüstung
In Situationen, in denen technische Kontrollen nicht verfügbar sind, um den Kontakt der Arbeitnehmer mit Neurotoxinen zu reduzieren, muss persönliche Schutzausrüstung bereitgestellt werden. Da es viele Neurotoxine am Arbeitsplatz gibt und die Expositionswege je nach Arbeitsplatz und Arbeitsbedingungen unterschiedlich sind, muss die Art der persönlichen Schutzausrüstung sorgfältig für die jeweilige Situation ausgewählt werden. Beispielsweise kann das neurotoxische Blei seine Toxizität entfalten, wenn bleihaltiger Staub eingeatmet wird und wenn Bleipartikel in Nahrung oder Wasser aufgenommen werden. Daher muss die persönliche Schutzausrüstung vor beiden Expositionswegen schützen. Dies würde Atemschutzgeräte und persönliche Hygienemaßnahmen bedeuten, um den Verzehr von mit Blei kontaminierten Lebensmitteln oder Getränken zu verhindern. Bei vielen Neurotoxinen (wie industriellen Lösungsmitteln) ist die Aufnahme der Substanz durch intakte Haut ein Hauptexpositionsweg. Undurchlässige Handschuhe, Schürzen und andere geeignete Ausrüstung müssen daher bereitgestellt werden, um Hautabsorption zu verhindern. Dies wäre zusätzlich zu technischen Kontrollen oder persönlicher Atemschutzausrüstung. Die Anpassung der persönlichen Schutzausrüstung an die jeweilige auszuführende Arbeit muss sorgfältig geplant werden.
Administrative Kontrollen
Administrative Kontrollen bestehen aus Bemühungen des Managements, Gefahren am Arbeitsplatz durch Planung, Schulung, Mitarbeiterrotation auf Baustellen, Änderungen in Produktionsprozessen und Produktsubstitution (Urie 1992) sowie die strikte Einhaltung aller bestehenden Vorschriften zu reduzieren.
Das Recht der Arbeitnehmer auf Information
Während der Arbeitgeber die Verantwortung dafür trägt, einen Arbeitsplatz oder eine Arbeitserfahrung bereitzustellen, die die Gesundheit der Arbeitnehmer nicht beeinträchtigt, haben die Arbeitnehmer die Verantwortung, die Arbeitsplatzregeln zu befolgen, die sie schützen sollen. Arbeitnehmer müssen in der Lage sein zu wissen, welche Maßnahmen sie ergreifen müssen, um sich selbst zu schützen. Das bedeutet, dass Arbeitnehmer das Recht haben, über die Neurotoxizität von Stoffen, mit denen sie in Kontakt kommen, zu erfahren und welche Schutzmaßnahmen sie ergreifen können.
Überwachung der Gesundheit der Arbeitnehmer
Wo es die Umstände zulassen, sollten Arbeitnehmer regelmäßig medizinisch untersucht werden. Eine regelmäßige Begutachtung durch Arbeitsmediziner oder andere Fachärzte stellt eine arbeitsmedizinische Überwachung dar. Bei Arbeitern, die bekanntermaßen mit oder in der Nähe von Neurotoxinen arbeiten, sollten die Ärzte über die Auswirkungen der Exposition informiert sein. Beispielsweise führt eine geringe Exposition gegenüber vielen organischen Lösungsmitteln zu Symptomen von Müdigkeit, Schlafstörungen, Kopfschmerzen und Gedächtnisstörungen. Bei hohen Bleidosen wären ein Herabfallen des Handgelenks und eine Beeinträchtigung peripherer Nerven Anzeichen einer Bleivergiftung. Jegliche Anzeichen und Symptome einer neurotoxischen Vergiftung sollten dazu führen, dass der Arbeiter in einen Bereich versetzt wird, der frei von neurotoxischen Stoffen ist, und Anstrengungen unternommen werden, um die Konzentration des neurotoxischen Stoffs am Arbeitsplatz zu reduzieren.
Klinische Syndrome im Zusammenhang mit Neurotoxizität
Neurotoxische Syndrome, die durch Substanzen verursacht werden, die das Nervengewebe nachteilig beeinflussen, bilden eine der zehn führenden Berufskrankheiten in den Vereinigten Staaten. Neurotoxische Wirkungen bilden die Grundlage für die Festlegung von Grenzwertkriterien für etwa 40 % der Arbeitsstoffe, die vom United States National Institute for Occupational Safety and Health (NIOSH) als gefährlich eingestuft werden.
Ein Neurotoxin ist jede Substanz, die in der Lage ist, die normale Funktion von Nervengewebe zu stören, irreversible Zellschäden zu verursachen und/oder zum Zelltod führt. Abhängig von seinen besonderen Eigenschaften greift ein bestimmtes Neurotoxin ausgewählte Stellen oder spezifische zelluläre Elemente des Nervensystems an. Diese unpolaren Verbindungen haben eine größere Lipidlöslichkeit und haben somit einen besseren Zugang zum Nervengewebe als hochpolare und weniger lipidlösliche Chemikalien. Die Art und Größe der Zellen und der verschiedenen Neurotransmittersysteme, die in verschiedenen Regionen des Gehirns betroffen sind, angeborene schützende Entgiftungsmechanismen sowie die Integrität von Zellmembranen und intrazellulären Organellen beeinflussen alle die neurotoxischen Reaktionen.
Neuronen (die funktionelle Zelleinheit des Nervensystems) haben eine hohe Stoffwechselrate und sind am stärksten von neurotoxischen Schäden bedroht, gefolgt von Oligodendrozyten, Astrozyten, Mikroglia und Zellen des Kapillarendothels. Veränderungen in der Zellmembranstruktur beeinträchtigen die Erregbarkeit und behindern die Impulsübertragung. Toxische Wirkungen verändern die Proteinform, den Flüssigkeitsgehalt und die Ionenaustauschfähigkeit von Membranen, was zu einer Schwellung von Neuronen, Astrozyten und einer Schädigung der empfindlichen Zellen führt, die die Blutkapillaren auskleiden. Die Störung von Neurotransmittermechanismen blockiert den Zugang zu postsynaptischen Rezeptoren, erzeugt falsche Neurotransmitterwirkungen und verändert die Synthese, Speicherung, Freisetzung, Wiederaufnahme oder enzymatische Inaktivierung natürlicher Neurotransmitter. Somit werden klinische Manifestationen der Neurotoxizität durch eine Reihe unterschiedlicher Faktoren bestimmt: die physikalischen Eigenschaften der neurotoxischen Substanz, die Expositionsdosis, die Anfälligkeit des zellulären Ziels, die Fähigkeit des Organismus, das Toxin zu metabolisieren und auszuscheiden, und durch die reparative Fähigkeiten der betroffenen Strukturen und Mechanismen. Tabelle 1 listet verschiedene chemische Expositionen und ihre neurotoxischen Syndrome auf.
Tabelle 1. Chemische Belastungen und damit verbundene neurotoxische Syndrome
|
Neurotoxin |
Expositionsquellen |
Klinische Diagnose |
Ort der Pathologie1 |
|
Metallindustrie |
|||
|
Arsen |
Pestizide; Pigmente; Antifouling-Farbe; Galvanikindustrie; Meeresfrüchte; Hütten; Halbleiter |
Akut: Enzephalopathie Chronisch: periphere Neuropathie |
Unbekannt (a) Axon (c) |
|
Führen (Lead) |
Lot; Leitender Schuss; illegaler Whisky; Insektizide; Karosseriewerkstatt; Herstellung von Akkumulatoren; Gießereien, Hütten; Farbe auf Bleibasis; Bleirohre |
Akut: Enzephalopathie Chronisch: Enzephalopathie und periphere Neuropathie |
Blutgefäße (a) Axon (c) |
|
Mangan |
Eisen-, Stahlindustrie; Schweißarbeiten; Metallveredelung; Düngemittel; Hersteller von Feuerwerkskörpern, Streichhölzern; Hersteller von Trockenbatterien |
Akut: Enzephalopathie Chronisch: Parkinsonismus |
Unbekannt (a) Basalganglienneuronen (c) |
|
Merkur |
Wissenschaftliche Instrumente; elektrische Ausrüstung; Amalgame; Galvanikindustrie; Fotografie; Filz machen |
Akut: Kopfschmerzen, Übelkeit, Auftreten von Tremor Chronisch: Ataxie, periphere Neuropathie, Enzephalopathie |
Unbekannt (a) Axon (c) Unbekannt (c) |
|
Zinn |
Konservenindustrie; Lot; elektronische Bauteile; Polyvinylkunststoffe; Fungizide |
Akut: Gedächtnisstörungen, Krampfanfälle, Orientierungslosigkeit Chronisch: Enzephalomyelopathie |
Neuronen des limbischen Systems (a & c) Myelin (c) |
|
Lösungsmittel |
|||
|
Schwefelkohlenstoff |
Hersteller von Viskose; Konservierungsmittel; Textilien; Gummizement; Lacke; Galvanoindustrie |
Akut: Enzephalopathie Chronisch: periphere Neuropathie, Parkinsonismus |
Unbekannt (a) Axon (c) Unbekannt |
|
n-Hexan, Methylbutylketon |
Farben; Lacke; Lacke; Verbindungen zur Metallreinigung; schnell trocknende Tinten; Farbentferner; Leime, Klebstoffe |
Akut: Narkose Chronisch: periphere Neuropathie, unbekannt (a) Axon (c), |
|
|
Perchlorethylen |
Abbeizmittel; Entfetter; Extraktionsmittel; Textilreinigungsindustrie; Textilindustrie |
Akut: Narkose Chronisch: periphere Neuropathie, Enzephalopathie |
Unbekannt (a) Axon (c) Unbekannt |
|
Toluol |
Gummi-Lösungsmittel; Reinigungskraft; Klebstoffe; Hersteller von Benzol; Benzin, Flugkraftstoffe; Farben, Farbverdünner; Lacke |
Akut: Narkose Chronisch: Ataxie, Enzephalopathie |
Unbekannt (a) Kleinhirn (c) Unbekannt |
|
Trichlorethylen |
Entfetter; Malerindustrie; Lacke; Fleckenentferner; Prozess der Entkoffeinierung; Textilreinigungsindustrie; Gummilösungsmittel |
Akut: Narkose Chronisch: Enzephalopathie, kraniale Neuropathie |
Unbekannt (a) Unbekannt (c) Axon (c) |
|
Insektizide |
|||
|
Organophosphate |
Herstellung und Anwendung in der Agrarindustrie |
Akut: cholinerge Vergiftung Chronisch: Ataxie, Paralyse, periphere Neuropathie |
Acetylcholinesterase (a) Lange Rückenmarksbahnen (c) Axon (c) |
|
Carbamate |
Herstellung und Anwendung von Flohpulvern in der Agrarindustrie |
Akut: cholinerge Vergiftung. Chronisch: Tremor, periphere Neuropathie |
Acetylcholinesterase (a) Dopaminerges System (c) |
1 (a), akut; (c), chronisch.
Quelle: Modifiziert von Feldman 1990, mit Genehmigung des Herausgebers.
Um eine Diagnose eines neurotoxischen Syndroms zu stellen und es von neurologischen Erkrankungen nicht-neurotoxischer Ätiologie zu unterscheiden, ist ein Verständnis der Pathogenese der neurologischen Symptome und der beobachteten Anzeichen und Symptome erforderlich; ein Bewusstsein dafür, dass bestimmte Substanzen das Nervengewebe beeinflussen können; Dokumentation der Exposition; Nachweis des Vorhandenseins von Neurotoxin und/oder Metaboliten in Geweben einer betroffenen Person; und sorgfältige Abgrenzung eines zeitlichen Zusammenhangs zwischen der Exposition und dem Auftreten von Symptomen mit anschließendem Rückgang der Symptome nach Beendigung der Exposition.
Der Nachweis, dass eine bestimmte Substanz eine toxische Dosis erreicht hat, fehlt in der Regel nach dem Auftreten von Symptomen. Sofern keine Umweltüberwachung stattfindet, ist ein hoher Verdachtsindex erforderlich, um Fälle von neurotoxikologischen Verletzungen zu erkennen. Das Identifizieren von Symptomen, die sich auf das zentrale und/oder das periphere Nervensystem beziehen, kann dem Kliniker helfen, sich auf bestimmte Substanzen als mögliche Übeltäter zu konzentrieren, die eine größere Vorliebe für den einen oder anderen Teil des Nervensystems haben. Krämpfe, Schwäche, Zittern/Zucken, Anorexie (Gewichtsverlust), Gleichgewichtsstörung, Depression des zentralen Nervensystems, Narkose (ein Zustand von Benommenheit oder Bewusstlosigkeit), Sehstörungen, Schlafstörungen, Ataxie (Unfähigkeit, willkürliche Muskelbewegungen zu koordinieren), Müdigkeit und Taststörungen sind häufig berichtete Symptome nach Exposition gegenüber bestimmten Chemikalien. Konstellationen von Symptomen bilden Syndrome, die mit einer Exposition gegenüber Neurotoxinen assoziiert sind.
Verhaltenssyndrome
Bei einigen Arbeitern wurden Störungen mit überwiegend verhaltensbezogenen Merkmalen beschrieben, die von akuter Psychose, Depression und chronischer Apathie reichen. Es ist wichtig, Gedächtnisstörungen im Zusammenhang mit anderen neurologischen Erkrankungen, wie Alzheimer-Krankheit, Arteriosklerose oder Vorhandensein eines Gehirntumors, von den kognitiven Defiziten zu unterscheiden, die mit der Exposition gegenüber giftigen organischen Lösungsmitteln, Metallen oder Insektiziden verbunden sind. Vorübergehende Bewusstseinsstörungen oder epileptische Anfälle mit oder ohne begleitender motorischer Beteiligung müssen als Primärdiagnose getrennt von ähnlich auftretenden Bewusstseinsstörungen im Zusammenhang mit neurotoxischen Wirkungen identifiziert werden. Subjektive und verhaltensbedingte Toxizitätssyndrome wie Kopfschmerzen, Schwindel, Müdigkeit und Persönlichkeitsveränderungen manifestieren sich als leichte Enzephalopathie mit Rausch und können auf eine Exposition gegenüber Kohlenmonoxid, Kohlendioxid, Blei, Zink, Nitraten oder gemischten organischen Lösungsmitteln hinweisen. Standardisierte neuropsychologische Tests sind notwendig, um Elemente der kognitiven Beeinträchtigung bei Patienten mit Verdacht auf toxische Enzephalopathie zu dokumentieren, und diese müssen von jenen demenziellen Syndromen unterschieden werden, die durch andere Pathologien verursacht werden. Spezifische Tests, die in den diagnostischen Testbatterien verwendet werden, müssen eine breite Auswahl an kognitiven Funktionstests umfassen, die Vorhersagen über die Funktionsfähigkeit und das tägliche Leben des Patienten liefern, sowie Tests, die sich zuvor als empfindlich gegenüber den Wirkungen bekannter Neurotoxine erwiesen haben. Diese standardisierten Batterien müssen Tests enthalten, die an Patienten mit bestimmten Arten von Hirnschäden und strukturellen Defiziten validiert wurden, um diese Zustände klar von neurotoxischen Wirkungen zu trennen. Darüber hinaus müssen Tests interne Kontrollmaßnahmen umfassen, um den Einfluss von Motivation, Hypochondrie, Depression und Lernschwierigkeiten zu erkennen, und eine Sprache enthalten, die kulturelle sowie bildungsbezogene Hintergrundeffekte berücksichtigt.
Es besteht ein Kontinuum von leichten bis schweren Beeinträchtigungen des Zentralnervensystems, die bei Patienten auftreten, die toxischen Substanzen ausgesetzt sind:
- Organisches affektives Syndrom (Typ-I-Effekt), bei denen leichte affektive Störungen als Hauptbeschwerden des Patienten vorherrschen, mit Merkmalen, die am ehesten mit denen organischer affektiver Störungen des depressiven Typs übereinstimmen. Dieses Syndrom scheint reversibel zu sein, nachdem die Exposition gegenüber dem auslösenden Agens beendet wurde.
- Milde chronische toxische Enzephalopathie, bei der zusätzlich zu Stimmungsstörungen die Beeinträchtigung des Zentralnervensystems stärker ausgeprägt ist. Die Patienten haben Hinweise auf Störungen des Gedächtnisses und der psychomotorischen Funktion, die durch neuropsychologische Tests bestätigt werden können. Darüber hinaus können Merkmale räumlicher Sehbehinderung und abstrakter Begriffsbildung erkennbar sein. Aktivitäten des täglichen Lebens und Arbeitsleistung sind beeinträchtigt.
- Anhaltende Persönlichkeits- oder Stimmungsänderung (Typ-IIA-Effekt) or Beeinträchtigung der intellektuellen Funktion (Typ II) kann gesehen werden. Bei leichter chronischer toxischer Enzephalopathie ist der Verlauf schleichend. Die Merkmale können nach Beendigung der Exposition bestehen bleiben und allmählich verschwinden, während bei einigen Personen eine anhaltende funktionelle Beeinträchtigung beobachtet werden kann. Wenn die Exposition andauert, kann die Enzephalopathie zu einem schwereren Stadium fortschreiten.
- In schwere chronische toxische Enzephalopathie (Typ-III-Effekt) Demenz mit globaler Verschlechterung des Gedächtnisses und anderen kognitiven Problemen werden festgestellt. Die klinischen Wirkungen der toxischen Enzephalopathie sind nicht spezifisch für ein bestimmtes Mittel. Die mit Toluol, Blei und Arsen assoziierte chronische Enzephalopathie unterscheidet sich nicht von der anderer toxischer Ätiologien. Das Vorhandensein anderer assoziierter Befunde (Sehstörungen mit Methylalkohol) kann jedoch helfen, Syndrome nach bestimmten chemischen Ätiologien zu differenzieren.
Arbeitnehmer, die Lösungsmitteln über längere Zeit ausgesetzt sind, können dauerhafte Störungen der Funktion des Zentralnervensystems aufweisen. Da über ein Übermaß an subjektiven Symptomen wie Kopfschmerzen, Müdigkeit, Gedächtnisstörungen, Appetitlosigkeit und diffuse Brustschmerzen berichtet wurde, ist es oft schwierig, diesen Effekt im Einzelfall zu bestätigen. Eine epidemiologische Studie zum Vergleich von Anstreichern, die Lösungsmitteln ausgesetzt waren, mit nicht exponierten Industriearbeitern zeigte beispielsweise, dass Maler bei psychologischen Tests, die die intellektuelle Leistungsfähigkeit und psychomotorische Koordination messen, signifikant niedrigere Durchschnittswerte aufwiesen als Referenzpersonen. Die Maler zeigten auch bei Gedächtnis- und Reaktionszeittests deutlich schlechtere Leistungen als erwartet. Unterschiede zwischen Arbeitern, die mehrere Jahre Düsentreibstoff ausgesetzt waren, und nicht exponierten Arbeitern in Tests, die besondere Aufmerksamkeit und eine hohe sensorische Motorgeschwindigkeit erforderten, waren ebenfalls offensichtlich. Auch bei Autolackierern wurde über Beeinträchtigungen der psychischen Leistungsfähigkeit und Persönlichkeitsveränderungen berichtet. Dazu gehörten das visuelle und verbale Gedächtnis, die Verringerung der emotionalen Reaktivität und die schlechte Leistung bei verbalen Intelligenztests.
Zuletzt ein umstrittenes neurotoxisches Syndrom, multiple chemische Empfindlichkeit, wurde beschrieben. Solche Patienten entwickeln eine Vielzahl von Merkmalen, die mehrere Organsysteme betreffen, wenn sie selbst geringen Mengen verschiedener Chemikalien ausgesetzt sind, die am Arbeitsplatz und in der Umwelt vorkommen. Stimmungsstörungen sind gekennzeichnet durch Depression, Müdigkeit, Reizbarkeit und Konzentrationsschwäche. Diese Symptome treten erneut auf, wenn sie vorhersagbaren Stimuli ausgesetzt werden, durch Auslösung durch Chemikalien verschiedener struktureller und toxikologischer Klassen, und in Konzentrationen, die viel niedriger sind als diejenigen, die in der Allgemeinbevölkerung unerwünschte Reaktionen hervorrufen. Viele der Symptome der multiplen Chemikaliensensibilität werden von Personen geteilt, die nur eine leichte Form von Stimmungsstörungen, Kopfschmerzen, Müdigkeit, Reizbarkeit und Vergesslichkeit zeigen, wenn sie sich in einem Gebäude mit schlechter Belüftung und mit Ausgasung flüchtiger Substanzen aus synthetischen Baumaterialien befinden und Teppiche. Die Symptome verschwinden, wenn sie diese Umgebungen verlassen.
Bewusstseinsstörungen, Krampfanfälle und Koma
Wenn dem Gehirn Sauerstoff entzogen wird – zum Beispiel in Gegenwart von Kohlenmonoxid, Kohlendioxid, Methan oder Stoffen, die die Gewebeatmung blockieren, wie Blausäure, oder solche, die eine massive Imprägnierung des Nervs verursachen, wie bestimmte organische Lösungsmittel –, kommt es zu Störungen der Bewusstsein kann die Folge sein. Dem Verlust des Bewusstseins können Krampfanfälle bei Arbeitern vorausgehen, die Anticholinesterase-Substanzen wie Organophosphat-Insektiziden ausgesetzt sind. Krampfanfälle können auch bei Bleienzephalopathie auftreten, die mit einer Hirnschwellung einhergeht. Manifestationen akuter Toxizität nach einer Organophosphatvergiftung haben Manifestationen des autonomen Nervensystems, die dem Auftreten von Schwindel, Kopfschmerzen, verschwommenem Sehen, Myose, Brustschmerzen, erhöhten Bronchialsekreten und Krampfanfällen vorausgehen. Diese parasympathischen Wirkungen werden durch die hemmende Wirkung dieser toxischen Substanzen auf die Cholinesterase-Aktivität erklärt.
Bewegungsstörungen
Bei Arbeitern, die Mangan, Kohlenmonoxid, Schwefelkohlenstoff und der Toxizität eines Meperidin-Nebenprodukts, 1-Methyl-4-Phenyl-1,2,3,6, ausgesetzt waren, wurden Verlangsamung der Bewegung, erhöhter Muskeltonus und Haltungsstörungen beobachtet -Tetrahydropyridin (MPTP). Manchmal scheinen die Personen an der Parkinson-Krankheit zu leiden. Parkinsonismus als Folge einer Giftstoffexposition hat Merkmale anderer nervöser Störungen wie Chorea und Athetose. Der typische „Pillenrollen“-Tremor ist in diesen Fällen nicht zu sehen, und in der Regel sprechen die Fälle nicht gut auf das Medikament Levodopa an. Dyskinesie (Beeinträchtigung der Willenskraft) kann ein häufiges Symptom einer Brommethanvergiftung sein. Krampfhafte Bewegungen der Finger, des Gesichts, der peribukkalen Muskeln und des Nackens sowie Krämpfe der Extremitäten können beobachtet werden. Tremor tritt häufig nach einer Quecksilbervergiftung auf. Ein deutlicherer Tremor in Verbindung mit Ataxie (mangelnde Koordination der Muskeltätigkeit) wird bei Personen nach Inhalation von Toluol festgestellt.
Opsoklonus ist eine abnormale Augenbewegung, die in alle Richtungen ruckartig ist. Dies wird häufig bei Hirnstammenzephalitis beobachtet, kann aber auch ein Merkmal nach einer Chlordecon-Exposition sein. Die Anomalie besteht aus unregelmäßigen Ausbrüchen abrupter, unwillkürlicher, schneller, gleichzeitiger Zuckungen beider Augen in konjugierter Weise, möglicherweise multidirektional bei schwer betroffenen Personen.
Kopfschmerzen
Häufige Beschwerden über Kopfschmerzen nach Exposition gegenüber verschiedenen Metalldämpfen wie Zink und anderen Lösungsmitteldämpfen können aus Vasodilatation (Erweiterung der Blutgefäße) sowie Hirnödem (Schwellung) resultieren. Das Erleben von Schmerzen ist diesen Zuständen gemeinsam, ebenso wie Kohlenmonoxid-, Hypoxie- (niedriger Sauerstoff-) oder Kohlendioxid-Zustände. Es wird angenommen, dass das „Sick-Building-Syndrom“ Kopfschmerzen verursacht, weil überschüssiges Kohlendioxid in einem schlecht belüfteten Bereich vorhanden ist.
Periphere Neuropathie
Periphere Nervenfasern, die motorischen Funktionen dienen, beginnen in Motoneuronen im Vorderhorn des Rückenmarks. Die motorischen Axone erstrecken sich peripher zu den Muskeln, die sie innervieren. Eine sensorische Nervenfaser hat ihren Nervenzellkörper im Hinterwurzelganglion oder in der dorsalen grauen Substanz des Rückenmarks. Nach Erhalt von Informationen aus der Peripherie, die an distalen Rezeptoren erkannt werden, werden Nervenimpulse zentral zu den Nervenzellkörpern geleitet, wo sie sich mit Rückenmarksbahnen verbinden, die Informationen an den Hirnstamm und die zerebralen Hemisphären übertragen. Einige sensorische Fasern haben unmittelbare Verbindungen mit motorischen Fasern innerhalb des Rückenmarks, was eine Grundlage für Reflexaktivität und schnelle motorische Reaktionen auf schädliche Empfindungen bildet. Diese sensomotorischen Beziehungen bestehen in allen Teilen des Körpers; Die Hirnnerven sind die Äquivalente der peripheren Nerven, die eher im Hirnstamm als in den Neuronen des Rückenmarks entstehen. Sensorische und motorische Nervenfasern wandern zusammen in Bündeln und werden als periphere Nerven bezeichnet.
Toxische Wirkungen peripherer Nervenfasern können unterteilt werden in solche, die hauptsächlich Axone (Axonopathien) betreffen, solche, die an distalem sensomotorischen Verlust beteiligt sind, und solche, die hauptsächlich Myelinscheiden- und Schwann-Zellen betreffen. Axonopathien treten in frühen Stadien in den unteren Extremitäten auf, wo die Axone am längsten und am weitesten vom Nervenzellkörper entfernt sind. Zufällige Demyelinisierung tritt in Segmenten zwischen Knoten von Ranvier auf. Wenn ein ausreichender axonaler Schaden auftritt, folgt eine sekundäre Demyelinisierung; Solange die Axone erhalten bleiben, kann eine Regeneration von Schwann-Zellen und eine Remyelinisierung stattfinden. Ein bei toxischen Neuropathien häufig beobachtetes Muster ist die distale Axonopathie mit sekundärer segmentaler Demyelinisierung. Der Verlust von Myelin verringert die Geschwindigkeit der Weiterleitung von Nervenimpulsen. Daher resultiert aus einer Schädigung der motorischen und sensorischen Fasern ein allmähliches Einsetzen von intermittierendem Kribbeln und Taubheitsgefühl, das zu Gefühlslosigkeit und unangenehmen Empfindungen, Muskelschwäche und Atrophie fortschreitet. Reduzierte oder fehlende Sehnenreflexe und anatomisch konsistente Muster von Sensibilitätsverlusten, die die unteren Extremitäten mehr als die oberen betreffen, sind Merkmale einer peripheren Neuropathie.
In den distalen Extremitäten können motorische Schwächen festgestellt werden, die zu einem unsicheren Gang und der Unfähigkeit, Gegenstände zu greifen, fortschreiten. Die distalen Anteile der Extremitäten sind stärker betroffen, aber schwere Fälle können auch proximale Muskelschwäche oder -atrophie hervorrufen. Streckmuskelgruppen sind vor den Beugern beteiligt. Die Symptome können manchmal auch nach Beendigung der Exposition einige Wochen lang fortschreiten. Die Verschlechterung der Nervenfunktion kann mehrere Wochen nach Entfernung der Exposition bestehen bleiben.
Je nach Art und Schweregrad der Neuropathie ist eine elektrophysiologische Untersuchung der peripheren Nerven sinnvoll, um eine Funktionseinschränkung zu dokumentieren. Eine Verlangsamung der Leitungsgeschwindigkeit, reduzierte Amplituden von sensorischen oder motorischen Aktionspotentialen oder verlängerte Latenzen können beobachtet werden. Eine Verlangsamung der motorischen oder sensorischen Leitungsgeschwindigkeiten ist im Allgemeinen mit einer Demyelinisierung von Nervenfasern verbunden. Die Erhaltung normaler Werte der Leitungsgeschwindigkeit bei Vorliegen einer Muskelatrophie deutet auf eine axonale Neuropathie hin. Ausnahmen treten auf, wenn bei axonaler Neuropathie ein fortschreitender Verlust von motorischen und sensorischen Nervenfasern auftritt, der die maximale Leitungsgeschwindigkeit als Folge des Herausfallens von schneller leitenden Nervenfasern mit größerem Durchmesser beeinflusst. Regenerierende Fasern treten in frühen Stadien der Genesung bei Axonopathien auf, bei denen die Reizleitung insbesondere in den distalen Segmenten verlangsamt ist. Die elektrophysiologische Untersuchung von Patienten mit toxischen Neuropathien sollte Messungen der motorischen und sensorischen Leitungsgeschwindigkeit in den oberen und unteren Extremitäten umfassen. Besonderes Augenmerk sollte auf die primär sensorisch leitenden Eigenschaften des Nervus suralis im Bein gelegt werden. Dies ist von großem Wert, wenn der Nervus suralis anschließend für eine Biopsie verwendet wird, wodurch eine anatomische Korrelation zwischen der Histologie der herausgezogenen Nervenfasern und den Leitungseigenschaften bereitgestellt wird. Eine differenzielle elektrophysiologische Untersuchung der Leitungsfähigkeit proximaler Segmente im Vergleich zu distalen Segmenten eines Nervs ist nützlich, um eine distale toxische Axonopathie zu identifizieren oder einen neuropathischen Leitungsblock zu lokalisieren, der wahrscheinlich auf eine Demyelinisierung zurückzuführen ist.
Das Verständnis der Pathophysiologie einer vermuteten neurotoxischen Polyneuropathie ist von großem Wert. Beispielsweise sind bei Patienten mit einer durch n-Hexan und Methylbutylketon verursachten Neuropathie die motorischen Nervenleitgeschwindigkeiten reduziert, aber in einigen Fällen können die Werte in den normalen Bereich fallen, wenn nur die am schnellsten feuernden Fasern stimuliert und als gemessenes Ergebnis verwendet werden . Da neurotoxische Hexacarbon-Lösungsmittel eine axonale Degeneration verursachen, treten sekundäre Veränderungen im Myelin auf und erklären die allgemeine Verringerung der Leitungsgeschwindigkeit trotz des Werts innerhalb des normalen Bereichs, der durch die erhaltenen leitenden Fasern erzeugt wird.
Elektrophysiologische Techniken umfassen andere spezielle Tests als die direkten Leitungsgeschwindigkeits-, Amplituden- und Latenzstudien. Somatosensorisch evozierte Potentiale, auditiv evozierte Potentiale und visuell evozierte Potentiale sind Möglichkeiten, die Eigenschaften der sensorischen Leitungssysteme sowie spezifischer Hirnnerven zu untersuchen. Afferent-efferente Schaltkreise können getestet werden, indem Blinkreflextests verwendet werden, die die Reaktionen der innervierten Hirnnerven vom 5. Hirnnerv bis zum 7. Hirnnerv umfassen; H-Reflexe beinhalten segmentale motorische Reflexbahnen. Die Vibrationsstimulation selektiert größere Fasern aus kleineren Faserbeteiligungen. Es stehen gut kontrollierte elektronische Techniken zur Verfügung, um die zum Auslösen einer Reaktion erforderliche Schwelle zu messen und dann die Ausbreitungsgeschwindigkeit dieser Reaktion sowie die Amplitude der Muskelkontraktion oder die Amplitude und das Muster eines hervorgerufenen sensorischen Aktionspotentials zu bestimmen . Alle physiologischen Ergebnisse müssen im Lichte des klinischen Bildes und mit einem Verständnis des zugrunde liegenden pathophysiologischen Prozesses bewertet werden.
Zusammenfassung
Die Abgrenzung eines neurotoxischen Syndroms von einer primären neurologischen Erkrankung stellt den Arzt im beruflichen Umfeld vor große Herausforderungen. Es ist notwendig und lohnend, eine gute Anamnese zu erheben, ein hohes Maß an Misstrauen aufrechtzuerhalten und eine angemessene Nachverfolgung einer Einzelperson sowie von Gruppen von Personen zu gewährleisten. Die frühzeitige Erkennung von Krankheiten im Zusammenhang mit Giftstoffen in ihrer Umgebung oder einer bestimmten beruflichen Exposition ist von entscheidender Bedeutung, da eine ordnungsgemäße Diagnose dazu führen kann, dass eine Person frühzeitig von den Gefahren einer andauernden Exposition gegenüber einer giftigen Substanz befreit wird, wodurch mögliche irreversible neurologische Schäden verhindert werden. Darüber hinaus kann die Anerkennung der frühesten betroffenen Fälle in einem bestimmten Umfeld zu Änderungen führen, die andere schützen, die noch nicht betroffen sind.
Messung neurotoxischer Defizite
Neurofunktionelle Testbatterien
Subklinische neurologische Anzeichen und Symptome werden seit langem bei aktiven Arbeitern festgestellt, die Neurotoxinen ausgesetzt sind; jedoch konzentrierten sich die Forschungsbemühungen erst seit Mitte der 1960er Jahre auf die Entwicklung empfindlicher Testbatterien, die in der Lage sind, subtile, leichte Veränderungen zu erkennen, die in den frühen Stadien des Rausches in Wahrnehmungs-, psychomotorischen, kognitiven, sensorischen und motorischen Funktionen vorhanden sind , und beeinflussen.
Die erste neurobehaviorale Testbatterie zur Verwendung in Arbeitsplatzstudien wurde von Helena Hänninen entwickelt, einer Pionierin auf dem Gebiet neurobehavioraler Defizite im Zusammenhang mit toxischer Exposition (Hänninen-Testbatterie) (Hänninen und Lindstrom 1979). Seitdem gibt es weltweite Bemühungen, neurobehaviorale Testbatterien zu entwickeln, zu verfeinern und in einigen Fällen zu computerisieren. Anger (1990) beschreibt fünf neurobehaviorale Testbatterien am Arbeitsplatz aus Australien, Schweden, Großbritannien, Finnland und den Vereinigten Staaten sowie zwei neurotoxische Screening-Batterien aus den Vereinigten Staaten, die in Studien an Arbeitern verwendet wurden, die Neurotoxinen ausgesetzt waren. Darüber hinaus wurden das computergestützte neurobehaviorale Bewertungssystem (NES) und das schwedische Leistungsbewertungssystem (SPES) weltweit in großem Umfang eingesetzt. Es gibt auch Testbatterien zur Beurteilung sensorischer Funktionen, darunter Messungen des Sehens, der vibrotaktilen Wahrnehmungsschwelle, des Geruchs, des Gehörs und des Schwankens (Mergler 1995). Studien zu verschiedenen neurotoxischen Wirkstoffen, bei denen die eine oder andere dieser Batterien verwendet wurde, haben wesentlich zu unserem Wissen über frühe neurotoxische Beeinträchtigungen beigetragen; Studienübergreifende Vergleiche waren jedoch schwierig, da unterschiedliche Tests verwendet werden und Tests mit ähnlichen Namen unter Verwendung eines anderen Protokolls durchgeführt werden können.
In einem Versuch, Informationen aus Studien über neurotoxische Substanzen zu standardisieren, wurde der Begriff einer „Core“-Batterie von einem Arbeitsausschuss der Weltgesundheitsorganisation (WHO) vorgeschlagen (Johnson 1987). Basierend auf dem Wissen zum Zeitpunkt des Treffens (1985) wurde eine Reihe von Tests ausgewählt, um die Neurobehavioral Core Test Battery (NCTB) zu bilden, eine relativ kostengünstige, von Hand verabreichte Batterie, die in vielen Ländern erfolgreich eingesetzt wurde (Anger et al. 1993). Die Tests, aus denen diese Batterie besteht, wurden so ausgewählt, dass sie bestimmte Bereiche des Nervensystems abdecken, von denen zuvor gezeigt wurde, dass sie empfindlich auf neurotoxische Schäden reagieren. Eine neuere Kernbatterie, die sowohl handverabreichte als auch computerisierte Tests umfasst, wurde von einer Arbeitsgruppe der United States Agency for Toxic Substances and Disease Registry (Hutchison et al. 1992) vorgeschlagen. Beide Batterien sind in Tabelle 1 dargestellt.
Tabelle 1. Beispiele für "Core"-Batterien zur Bewertung früher neurotoxischer Wirkungen
|
Neurobehavioral Core Test Battery (NCTB)+ |
Testauftrag |
Agency for Toxic Substances and Disease Registry Adult Environmental Neurobehavioural Test Battery (AENTB)+ |
||
|
Funktionsbereich |
Test |
Funktionsbereich |
Test |
|
|
Motorischer Stand |
Zielen (Verfolgtes Zielen II) |
1 |
Vision |
Sehschärfe, nahezu Kontrastempfindlichkeit |
|
Aufmerksamkeit/Reaktionsgeschwindigkeit |
Einfache Reaktionszeit |
2 |
Farbsehen (Lanthony D-15 entsättigter Test) |
|
|
Wahrgenommene Motordrehzahl |
Ziffernsymbol (WAIS-R) |
3 |
Somatosensorisch |
Vibrotaktile Wahrnehmungsschwelle |
|
Manuelle Geschicklichkeit |
Santa Ana (Helsinki-Version) |
4 |
Motorstärke |
Dynamometer (einschließlich Ermüdungsbewertung) |
|
Visuelle Wahrnehmung/Erinnerung |
Benton Visuelle Retention |
5 |
Motor Koordination |
Santa Ana |
|
Auditives Gedächtnis |
Ziffernspanne (WAIS-R, WMS) |
6 |
Höhere intellektuelle Funktion |
Raven Progressive Matrizen (überarbeitet) |
|
Beeinflussen |
POMS (Stimmungsprofil) |
7 |
Motor Koordination |
Fingertapping-Test (eine Hand)1 |
|
8 |
Daueraufmerksamkeit (kognitiv), Schnelligkeit (motorisch) |
Einfache Reaktionszeit (SRT) (erweitert)1 |
||
|
9 |
Kognitive Kodierung |
Symbol-Ziffer mit verzögertem Abruf1 |
||
|
10 |
Lernen und Gedächtnis |
Lernen von Seriennummern1 |
||
|
11 |
Index des Bildungsniveaus |
Wortschatz1 |
||
|
12 |
Stimmung |
Stimmungsskala1 |
||
1 Verfügbar in computerisierter Version; WAIS = Wechsler Adult Intelligence Scale; WMS = Wechsler-Speicherskala.
Die Autoren beider Core-Batterien betonen, dass die Batterien zwar nützlich sind, um Ergebnisse zu standardisieren, sie aber keinesfalls eine vollständige Bewertung der Funktionen des Nervensystems liefern. Je nach Art der Exposition sollten zusätzliche Tests durchgeführt werden; Beispielsweise würde eine Testbatterie zur Bewertung von Funktionsstörungen des Nervensystems bei Mangan-exponierten Arbeitern mehr Tests der motorischen Funktionen umfassen, insbesondere solche, die schnelle Wechselbewegungen erfordern, während eine für Methylquecksilber-exponierte Arbeiter Gesichtsfeldtests umfassen würde. Die Auswahl der Tests für einen bestimmten Arbeitsplatz sollte auf der Grundlage des aktuellen Wissensstandes über die Wirkung des bestimmten Toxins oder der bestimmten Toxine, denen die Personen ausgesetzt sind, getroffen werden.
Anspruchsvollere Testbatterien, die von geschulten Psychologen verabreicht und interpretiert werden, sind ein wichtiger Bestandteil der klinischen Bewertung einer neurotoxischen Vergiftung (Hart 1988). Es umfasst Tests der intellektuellen Fähigkeiten, Aufmerksamkeit, Konzentration und Orientierung, des Gedächtnisses, der visuell-perzeptiven, konstruktiven und motorischen Fähigkeiten, der Sprache, der konzeptionellen und exekutiven Funktionen und des psychischen Wohlbefindens sowie eine Bewertung möglicher Simulationen. Das Leistungsprofil des Patienten wird im Lichte der vergangenen und gegenwärtigen medizinischen und psychologischen Vorgeschichte sowie der Expositionsgeschichte untersucht. Die endgültige Diagnose basiert auf einer Konstellation von Defiziten, die in Abhängigkeit von der Art der Exposition interpretiert werden.
Maße des emotionalen Zustands und der Persönlichkeit
Studien zur Wirkung neurotoxischer Substanzen beinhalten in der Regel affektive oder Persönlichkeitsstörungen in Form von Symptomfragebögen, Stimmungsskalen oder Persönlichkeitsindizes. Das oben beschriebene NCTB enthält das Profile of Mood States (POMS), ein quantitatives Stimmungsmaß. Unter Verwendung von 65 qualifizierenden Adjektiven von Stimmungszuständen der letzten 8 Tage werden die Grade von Anspannung, Depression, Feindseligkeit, Kraft, Müdigkeit und Verwirrung abgeleitet. Die meisten vergleichenden Arbeitsplatzstudien zur neurotoxischen Exposition weisen auf Unterschiede zwischen exponierten und nicht exponierten Personen hin. Eine kürzlich durchgeführte Studie an Arbeitern, die Styrol ausgesetzt waren, zeigt Dosis-Wirkungs-Beziehungen zwischen dem Mandelsäurespiegel im Urin nach der Schicht, einem biologischen Indikator für Styrol, und Skalenwerten für Anspannung, Feindseligkeit, Müdigkeit und Verwirrung (Sassine et al. 1996).
Längere und ausgefeiltere Affekt- und Persönlichkeitstests wie der Minnesota Multiphasic Personality Index (MMPI), die sowohl emotionale Zustände als auch Persönlichkeitsmerkmale widerspiegeln, wurden hauptsächlich für die klinische Bewertung, aber auch in Arbeitsplatzstudien verwendet. Der MMPI bietet ebenfalls eine Bewertung von Symptomübertreibung und inkonsistenten Reaktionen. In einer Studie mit Mikroelektronik-Arbeitern, die in der Vorgeschichte neurotoxischen Substanzen ausgesetzt waren, zeigten die Ergebnisse des MMPI klinisch signifikante Ausmaße an Depressionen, Angstzuständen, somatischen Sorgen und Denkstörungen (Bowler et al. 1991).
Elektrophysiologische Maßnahmen
Elektrische Aktivität, die durch die Übertragung von Informationen entlang von Nervenfasern und von einer Zelle zur anderen erzeugt wird, kann aufgezeichnet und zur Bestimmung dessen verwendet werden, was im Nervensystem von Personen mit toxischen Belastungen passiert. Eine Störung der neuronalen Aktivität kann die Übertragung verlangsamen oder das elektrische Muster verändern. Elektrophysiologische Aufzeichnungen erfordern präzise Instrumente und werden am häufigsten in einem Labor oder Krankenhaus durchgeführt. Es wurden jedoch Anstrengungen unternommen, tragbarere Geräte zur Verwendung bei Studien am Arbeitsplatz zu entwickeln.
Elektrophysiologische Messungen zeichnen eine globale Reaktion einer großen Anzahl von Nervenfasern und/oder Fasern auf, und es muss eine beträchtliche Menge an Schaden vorhanden sein, bevor sie angemessen aufgezeichnet werden kann. Daher können bei den meisten neurotoxischen Substanzen Symptome sowie sensorische, motorische und kognitive Veränderungen in der Regel in Gruppen von exponierten Arbeitern festgestellt werden, bevor elektrophysiologische Unterschiede beobachtet werden. Bei der klinischen Untersuchung von Personen mit Verdacht auf neurotoxische Erkrankungen geben elektrophysiologische Methoden Aufschluss über Art und Ausmaß der Schädigung des Nervensystems. Eine Übersicht über elektrophysiologische Techniken, die beim Nachweis einer frühen Neurotoxizität beim Menschen verwendet werden, wird von Seppalaïnen (1988) bereitgestellt.
Mittels Elektroneurographie (ENG) wird die Nervenleitgeschwindigkeit von sensorischen (zum Gehirn gehenden) und motorischen (vom Gehirn weggehenden) Nerven gemessen. Durch Stimulation an verschiedenen anatomischen Positionen und Aufzeichnung an einer anderen kann die Leitungsgeschwindigkeit berechnet werden. Diese Technik kann Informationen über die großen myelinisierten Fasern liefern; Eine Verlangsamung der Leitungsgeschwindigkeit tritt auf, wenn eine Demyelinisierung vorhanden ist. Verringerte Leitungsgeschwindigkeiten wurden häufig bei bleiexponierten Arbeitern ohne neurologische Symptome beobachtet (Maizlish und Feo 1994). Langsame Leitungsgeschwindigkeiten peripherer Nerven wurden auch mit anderen Neurotoxinen wie Quecksilber, Hexacarbonen, Schwefelkohlenstoff, Styrol, Methyl-n-butylketon, Methylethylketon und bestimmten Lösungsmittelmischungen in Verbindung gebracht. Der Trigeminusnerv (ein Gesichtsnerv) wird durch Trichlorethylen-Exposition beeinträchtigt. Wenn die toxische Substanz jedoch hauptsächlich auf dünn myelinisierte oder nicht myelinisierte Fasern einwirkt, bleiben die Leitungsgeschwindigkeiten normalerweise normal.
Elektromyographie (EMG) wird zur Messung der elektrischen Aktivität in Muskeln verwendet. Bei Arbeitern, die Stoffen wie n-Hexan, Schwefelkohlenstoff, Methyl-n-butylketon, Quecksilber und bestimmten Pestiziden ausgesetzt waren, wurden elektromyografische Anomalien beobachtet. Diese Veränderungen werden oft von Veränderungen der ENG und Symptomen einer peripheren Neuropathie begleitet.
Veränderungen in den Gehirnwellen werden durch Elektroenzephalographie (EEG) nachgewiesen. Bei Patienten mit Vergiftung durch organische Lösungsmittel wurden lokale und diffuse Anomalien langsamer Wellen beobachtet. Einige Studien berichten von dosisabhängigen EEG-Veränderungen bei aktiven Arbeitern, die organischen Lösungsmittelgemischen, Styrol und Schwefelkohlenstoff ausgesetzt waren. Organochlor-Pestizide können epileptische Anfälle mit EEG-Anomalien verursachen. EEG-Veränderungen wurden bei Langzeitexposition gegenüber Organophosphor- und Zinkphosphid-Pestiziden berichtet.
Evozierte Potentiale (EP) bieten ein weiteres Mittel zur Untersuchung der Aktivität des Nervensystems als Reaktion auf einen sensorischen Stimulus. Messelektroden werden an dem spezifischen Bereich des Gehirns platziert, der auf die jeweiligen Reize reagiert, und die Latenz und Amplitude des ereignisbezogenen langsamen Potenzials werden aufgezeichnet. Als Reaktion auf visuelle, auditive und somatosensorische Stimuli wurden für ein breites Spektrum neurotoxischer Substanzen eine erhöhte Latenzzeit und/oder verringerte Spitzenamplituden beobachtet.
Die Elektrokardiographie (EKG oder EKG) zeichnet Veränderungen in der elektrischen Leitung des Herzens auf. Obwohl es in Studien zu neurotoxischen Substanzen nicht oft verwendet wird, wurden bei Personen, die Trichlorethylen ausgesetzt waren, Veränderungen in den EKG-Wellen beobachtet. Elektrookulographische (EOG) Aufzeichnungen der Augenbewegungen haben Veränderungen bei Arbeitern mit Bleiexposition gezeigt.
Bildgebende Verfahren des Gehirns
In den letzten Jahren wurden verschiedene Techniken zur Bildgebung des Gehirns entwickelt. Computertomographische (CT) Bilder zeigen die Anatomie des Gehirns und des Rückenmarks. Sie wurden verwendet, um zerebrale Atrophie bei Arbeitern und Patienten zu untersuchen, die Lösungsmitteln ausgesetzt waren; die Ergebnisse sind jedoch nicht konsistent. Die Magnetresonanztomographie (MRT) untersucht das Nervensystem mit einem starken Magnetfeld. Klinisch ist es besonders sinnvoll, eine alternative Diagnose, wie z. B. Hirntumoren, auszuschließen. Die Positronen-Emissions-Tomographie (PET), die Bilder biochemischer Prozesse liefert, wurde erfolgreich eingesetzt, um durch Manganvergiftung induzierte Veränderungen im Gehirn zu untersuchen. Die Single-Photon-Emissions-Computertomographie (SPECT) liefert Informationen über den Hirnstoffwechsel und könnte sich als wichtiges Werkzeug erweisen, um zu verstehen, wie Neurotoxine auf das Gehirn wirken. Diese Techniken sind alle sehr kostspielig und in den meisten Krankenhäusern oder Labors auf der ganzen Welt nicht ohne weiteres verfügbar.
Diagnose
Die Diagnose einer neurotoxischen Erkrankung ist nicht einfach. Die Fehler sind normalerweise zweierlei Art: Entweder wird nicht erkannt, dass ein neurotoxischer Stoff die Ursache neurologischer Symptome ist, oder neurologische (und insbesondere neurologische Verhaltens-)Symptome werden fälschlicherweise als Folge einer beruflichen, neurotoxischen Exposition diagnostiziert. Beide Fehler können gefährlich sein, da eine frühzeitige Diagnose im Falle einer neurotoxischen Erkrankung wichtig ist und die beste Behandlung darin besteht, eine weitere Exposition für den Einzelfall zu vermeiden und den Zustand anderer Arbeitnehmer zu überwachen, um zu verhindern, dass sie derselben ausgesetzt werden Achtung. Andererseits kann am Arbeitsplatz manchmal unangemessene Besorgnis entstehen, wenn ein Arbeitnehmer behauptet, schwerwiegende Symptome zu haben und eine Chemikalienexposition als Ursache vermutet, in Wirklichkeit aber entweder der Arbeitnehmer irrt oder die Gefahr für andere nicht wirklich besteht. Es gibt auch praktische Gründe für korrekte Diagnoseverfahren, da in vielen Ländern die Diagnose und Behandlung von Berufskrankheiten und der durch diese Krankheiten verursachten Arbeitsunfähigkeit und Invalidität von der Versicherung abgedeckt sind; somit kann der finanzielle Ausgleich angefochten werden, wenn die diagnostischen Kriterien nicht stichhaltig sind. Ein Beispiel für einen Entscheidungsbaum für die neurologische Beurteilung ist in Tabelle 1 angegeben.
Tabelle 1. Entscheidungsbaum für neurotoxische Erkrankungen
I. Maßgebliche Expositionshöhe, -dauer und -art
II. Angemessene Symptome verstärken schleichend die Symptome des zentralen (ZNS) oder peripheren (PNS) Nervensystems
III. Anzeichen und zusätzliche Tests ZNS-Dysfunktion: neurologische, psychologische Tests PNS-Dysfunktion: quantitativer sensorischer Test, Nervenleitungsstudien
IV. Andere Krankheiten, die in der Differentialdiagnose ausgeschlossen wurden
Exposition und Symptome
Akute neurotoxische Syndrome treten hauptsächlich in Unfallsituationen auf, wenn Arbeiter kurzzeitig sehr hohen Konzentrationen einer Chemikalie oder einer Mischung von Chemikalien im Allgemeinen durch Einatmen ausgesetzt sind. Die üblichen Symptome sind Schwindel, Unwohlsein und möglicherweise Bewusstlosigkeit als Folge einer Depression des zentralen Nervensystems. Wenn die Person von der Exposition entfernt wird, verschwinden die Symptome ziemlich schnell, es sei denn, die Exposition war so intensiv, dass sie lebensbedrohlich ist, in diesem Fall können Koma und Tod folgen. In diesen Situationen Erkennen der Gefahr sollen am Arbeitsplatz auftreten, und das Opfer sollte sofort an die frische Luft gebracht werden.
Im Allgemeinen treten neurotoxische Symptome nach Kurzzeit- oder Langzeitexposition und häufig bei relativ geringen beruflichen Expositionsniveaus auf. In diesen Fällen können akute Symptome bei der Arbeit aufgetreten sein, aber das Vorhandensein akuter Symptome ist nicht notwendig, um die Diagnose einer chronischen toxischen Enzephalopathie oder toxischen Neuropathie zu stellen. Allerdings berichten Patienten am Ende eines Arbeitstages häufig über Kopfschmerzen, Benommenheit oder Schleimhautreizungen, die jedoch zunächst in der Nacht, am Wochenende oder im Urlaub verschwinden. Eine nützliche Checkliste findet sich in Tabelle 2.
Tabelle 2. Kontinuierliche neurofunktionelle Wirkungen von Expositionen am Arbeitsplatz gegenüber einigen führenden neurotoxischen Substanzen
|
Gemischte organische Lösungsmittel |
Schwefelkohlenstoff |
Styrol |
Organophos- |
Führen (Lead) |
Merkur |
|
|
Erwerb |
+ |
|
|
|
+ |
|
|
Beeinflussen |
+ |
|
+ |
|
+ |
|
|
Kategorisierung |
+ |
|
|
|
|
|
|
Programmierung |
+ |
+ |
|
|
+ |
+ |
|
Farbsehen |
+ |
|
+ |
|
|
|
|
Konzeptverschiebung |
+ |
|
|
|
|
|
|
Ablenkbarkeit |
|
|
|
|
+ |
|
|
Intelligenz |
+ |
+ |
|
+ |
+ |
+ |
|
Memory |
+ |
+ |
+ |
+ |
+ |
+ |
|
Motor Koordination |
+ |
+ |
+ |
|
+ |
+ |
|
Motordrehzahl |
+ |
+ |
+ |
|
+ |
+ |
|
Nahezu visuelle Kontrastempfindlichkeit |
+ |
|
|
|
|
|
|
Geruchswahrnehmungsschwelle |
+ |
|
|
|
|
|
|
Geruchsidentifikation |
+ |
|
|
|
+ |
|
|
Persönlichkeit |
+ |
+ |
|
|
|
+ |
|
Räumliche Beziehungen |
+ |
+ |
|
|
+ |
|
|
Vibrotaktile Schwelle |
+ |
|
|
+ |
|
+ |
|
Wachsamkeit |
+ |
+ |
|
|
+ |
|
|
Sichtfeld |
|
|
|
|
+ |
+ |
|
Wortschatz |
|
|
|
|
+ |
|
Quelle: Adaptiert von Anger 1990.
Unter der Annahme, dass der Patient neurotoxischen Chemikalien ausgesetzt war, beginnt die Diagnose einer neurotoxischen Erkrankung mit den Symptomen. 1985 diskutierte eine gemeinsame Arbeitsgruppe der Weltgesundheitsorganisation und des Nordischen Ministerrates die Frage der chronischen Vergiftung durch organische Lösungsmittel und stellte eine Reihe von Kernsymptomen fest, die in den meisten Fällen zu finden sind (WHO/Nordic Council 1985). Die Kernsymptome sind Ermüdbarkeit, Gedächtnisverlust, Konzentrationsschwierigkeiten und Antriebslosigkeit. Diese Symptome beginnen in der Regel nach einer grundlegenden Persönlichkeitsveränderung, die sich allmählich entwickelt und sich auf Energie, Intellekt, Emotion und Motivation auswirkt. Unter anderen Symptomen einer chronischen toxischen Enzephalopathie sind Depression, Dysphorie, emotionale Labilität, Kopfschmerzen, Reizbarkeit, Schlafstörungen und Schwindel (Vertigo). Besteht auch eine Beteiligung des peripheren Nervensystems, kommt es zu Taubheitsgefühl und möglicherweise Muskelschwäche. Solche chronischen Symptome halten mindestens ein Jahr nach Beendigung der Exposition an.
Klinische Untersuchung und Prüfung
Die klinische Untersuchung sollte eine neurologische Untersuchung umfassen, bei der auf die Beeinträchtigung höherer Nervenfunktionen wie Gedächtnis, Kognition, logisches Denken und Emotion geachtet werden sollte; zu beeinträchtigten Kleinhirnfunktionen, wie Tremor, Gang, Stand und Koordination; und auf periphere Nervenfunktionen, insbesondere Vibrationsempfindlichkeit und andere Empfindungstests. Psychologische Tests können objektive Maße für höhere Funktionen des Nervensystems liefern, einschließlich Psychomotorik, Kurzzeitgedächtnis, verbales und nonverbales Denken und Wahrnehmungsfunktionen. Bei der individuellen Diagnose sollten die Tests einige Tests umfassen, die einen Hinweis auf das prämorbide intellektuelle Niveau der Person geben. Anamnestische schulische und frühere berufliche Leistungen sowie eventuell früher durchgeführte psychologische Tests, beispielsweise im Zusammenhang mit dem Wehrdienst, können bei der Einschätzung des normalen Leistungsniveaus der Person helfen.
Das periphere Nervensystem kann mit quantitativen Tests sensorischer Modalitäten, Vibration und Thermosensibilität untersucht werden. Nervenleitgeschwindigkeitsstudien und Elektromyographie können Neuropathie oft in einem frühen Stadium aufdecken. Bei diesen Tests sollte besonderes Augenmerk auf sensorische Nervenfunktionen gelegt werden. Die Amplitude des sensorischen Aktionspotentials (SNAP) nimmt bei axonalen Neuropathien häufiger ab als die sensorische Leitungsgeschwindigkeit, und die meisten toxischen Neuropathien sind axonaler Natur. Neuroradiologische Untersuchungen wie Computertomographie (CT) und Magnetresonanztomographie (MRT) liefern in der Regel keine Hinweise auf eine chronische toxische Enzephalopathie, können aber bei der Differentialdiagnose hilfreich sein.
Bei der Differentialdiagnose sollten andere neurologische und psychiatrische Erkrankungen berücksichtigt werden. Eine Demenz anderer Ätiologie sollte ebenso ausgeschlossen werden wie Depressionen und Stresssymptome unterschiedlicher Ursache. Eine psychiatrische Beratung kann erforderlich sein. Alkoholmissbrauch ist ein relevanter Störfaktor; Übermäßiger Alkoholkonsum verursacht ähnliche Symptome wie Lösungsmittelexposition, und andererseits gibt es Veröffentlichungen, die darauf hinweisen, dass Lösungsmittelexposition Alkoholmissbrauch auslösen kann. Andere Ursachen für Neuropathie müssen ebenfalls ausgeschlossen werden, insbesondere Einklemmungsneuropathien, Diabetes und Nierenerkrankungen; auch Alkohol verursacht Neuropathie. Die Kombination von Enzephalopathie und Neuropathie ist eher toxischen Ursprungs als eine von beiden allein.
In der endgültigen Entscheidung sollte die Exposition erneut bewertet werden. Gab es eine relevante Exposition unter Berücksichtigung des Ausmaßes, der Dauer und der Qualität der Exposition? Lösungsmittel verursachen eher ein psychoorganisches Syndrom oder eine toxische Enzephalopathie; Hexacarbone verursachen jedoch normalerweise zuerst Neuropathie. Blei und einige andere Metalle verursachen Neuropathie, obwohl eine ZNS-Beteiligung später festgestellt werden kann.
Berufliche Neuroepidemiologie
Olaf Axelson*
*Adaptiert von Axelson 1996.
Durch klinische Beobachtungen entstanden frühe Erkenntnisse über die neurotoxischen Wirkungen beruflicher Expositionen. Die beobachteten Wirkungen waren mehr oder weniger akut und betrafen die Exposition gegenüber Metallen wie Blei und Quecksilber oder Lösungsmitteln wie Schwefelkohlenstoff und Trichlorethylen. Mit der Zeit wurden jedoch chronischere und klinisch weniger offensichtliche Wirkungen von neurotoxischen Wirkstoffen durch moderne Untersuchungsmethoden und systematische Studien an größeren Gruppen bewertet. Dennoch war die Interpretation der Ergebnisse umstritten und wurde diskutiert, wie z. B. die chronischen Auswirkungen einer Lösungsmittelexposition (Arlien-Søborg 1992).
Die Schwierigkeiten bei der Interpretation chronischer neurotoxischer Wirkungen hängen sowohl von der Vielfalt und Unbestimmtheit der Symptome und Anzeichen als auch von dem damit verbundenen Problem ab, eine geeignete Krankheitseinheit für schlüssige epidemiologische Studien zu definieren. Beispielsweise können die chronischen Wirkungen bei Lösungsmittelexposition Gedächtnis- und Konzentrationsprobleme, Müdigkeit, Initiativlosigkeit, Affekthaftung, Reizbarkeit und manchmal Schwindel, Kopfschmerzen, Alkoholunverträglichkeit und verminderte Libido umfassen. Neurophysiologische Methoden haben auch verschiedene funktionelle Störungen aufgedeckt, die wiederum schwer zu einer einzelnen Krankheitseinheit zu kondensieren sind.
In ähnlicher Weise scheint eine Vielzahl von neurologischen Verhaltenseffekten auch aufgrund anderer beruflicher Expositionen aufzutreten, wie z. B. mäßige Bleiexposition oder Schweißen mit einer gewissen Exposition gegenüber Aluminium, Blei und Mangan oder Exposition gegenüber Pestiziden. Wiederum gibt es auch neurophysiologische oder neurologische Anzeichen, unter anderem Polyneuropathie, Tremor und Gleichgewichtsstörungen bei Personen, die Organochlor, Organophosphor und anderen Insektiziden ausgesetzt sind.
Angesichts der epidemiologischen Probleme, die mit der Definition einer Krankheitsentität aus den vielen genannten Arten von neurologischen Verhaltenseffekten verbunden sind, ist es auch selbstverständlich geworden, einige klinisch mehr oder weniger gut definierte neuropsychiatrische Störungen in Bezug auf berufliche Expositionen zu betrachten.
Seit den 1970er Jahren haben sich mehrere Studien speziell auf die Lösungsmittelexposition und das psychoorganische Syndrom konzentriert, wenn es zu Behinderungen kommt. In jüngerer Zeit haben auch Alzheimer-Demenz, multiple Sklerose, Parkinson-Krankheit, amyotrophe Lateralsklerose und verwandte Zustände das Interesse der Berufsepidemiologie auf sich gezogen.
In Bezug auf die Lösungsmittelexposition und das psychoorganische Syndrom (oder toxische chronische Enzephalopathie in der klinischen Arbeitsmedizin, wenn die Exposition diagnostisch berücksichtigt wird) war das Problem der Definition einer angemessenen Krankheitseinheit offensichtlich und führte zunächst zu Überlegungen im Block die Diagnosen Enzephalopathie, Demenz und Hirnatrophie, aber auch Neurose, Neurasthenie und Nervositas wurden aufgenommen, da sie in der medizinischen Praxis nicht notwendigerweise voneinander unterschieden werden (Axelson, Hane und Hogstedt 1976). Kürzlich wurden auch spezifischere Krankheitsentitäten wie organische Demenz und zerebrale Atrophie mit Lösungsmittelexposition in Verbindung gebracht (Cherry, Labréche und McDonald 1992). Die Ergebnisse waren jedoch nicht ganz konsistent, da in einer groß angelegten Fall-Referenz-Studie in den Vereinigten Staaten mit nicht weniger als 3,565 Fällen verschiedener neuropsychiatrischer Störungen und 83,245 Krankenhaus-Referenten kein Übermaß an „präseniler Demenz“ auftrat (Brackbill, Maizlish und Fischbach 1990). Im Vergleich zu Maurern gab es jedoch bei weißen männlichen Malern, mit Ausnahme von Sprühmalern, einen Überschuss an behindernden neuropsychiatrischen Störungen um etwa 45 %.
Berufsbedingte Expositionen scheinen auch für spezifischere Störungen als das psychoorganische Syndrom eine Rolle zu spielen. So wurde 1982 erstmals in der italienischen Schuhindustrie auf einen Zusammenhang zwischen Multipler Sklerose und Lösungsmittelbelastung durch Klebstoffe hingewiesen (Amaducci et al. 1982). Dieser Zusammenhang wurde durch weitere Studien in Skandinavien (Flodin et al. 1988; Landtblom et al. 1993; Grönning et al. 1993) und anderswo erheblich verstärkt, so dass 13 Studien mit einigen Informationen zur Lösungsmittelexposition in einer Übersichtsarbeit berücksichtigt werden konnten ( Landtblom et al. 1996). Zehn dieser Studien lieferten genügend Daten, um in eine Metaanalyse aufgenommen zu werden, die ein etwa zweifaches Risiko für Multiple Sklerose bei Personen mit Lösungsmittelexposition zeigten. Einige Studien bringen Multiple Sklerose auch mit radiologischen Arbeiten, Schweißen und Arbeiten mit Phenoxy-Herbiziden in Verbindung (Flodin et al. 1988; Landtblom et al. 1993). Die Parkinson-Krankheit scheint in ländlichen Gebieten häufiger vorzukommen (Goldsmith et al. 1990), insbesondere in jüngeren Jahren (Tanner 1989). Interessanterweise zeigte eine Studie aus Calgary, Kanada, ein dreifaches Risiko für Herbizidbelastung (Semchuk, Love und Lee 1992).
Alle Fallpersonen, die sich an spezifische Expositionen erinnerten, berichteten von einer Exposition gegenüber Phenoxy-Herbiziden oder Thiocarbamaten. Einer von ihnen erinnerte sich an die Exposition gegenüber Paraquat, das MPTP (N-Methyl-4-Phenyl-1,2,3,6-Tetrahydropyridin), einem Auslöser eines Parkinson-ähnlichen Syndroms, chemisch ähnlich ist. Ein solches Syndrom wurde bisher jedoch noch nicht bei Paraquat-Arbeitern festgestellt (Howard 1979). Fallbezogene Studien aus Kanada, China, Spanien und Schweden haben einen Zusammenhang mit der Exposition gegenüber nicht näher bezeichneten Industriechemikalien, Pestiziden und Metallen, insbesondere Mangan, Eisen und Aluminium, aufgezeigt (Zayed et al. 1990).
In einer Studie aus den USA zeigte sich im Zusammenhang mit Schweißen und Löten ein erhöhtes Risiko für Motoneuronerkrankungen (umfasst amyotrophe Lateralsklerose, progressive bulbäre Parese und progressive Muskelatrophie) (Armon et al. 1991). Als Risikofaktor traten auch das Schweißen, Arbeiten mit Strom und auch Arbeiten mit Imprägniermitteln in einer schwedischen Studie auf (Gunnarsson et al. 1992). Die Vererbbarkeit für neurodegenerative Erkrankungen und Schilddrüsenerkrankungen zeigte in Kombination mit Lösungsmittelexposition und männlichem Geschlecht ein Risiko von bis zu 15.6. Auch andere Studien weisen darauf hin, dass die Exposition gegenüber Blei und Lösungsmitteln von Bedeutung sein könnte (Campbell, Williams und Barltrop 1970; Hawkes, Cavanagh und Fox 1989; Chio, Tribolo und Schiffer 1989; Sienko et al. 1990).
Für die Alzheimer-Krankheit ergab eine Metaanalyse von elf Fallstudien (Graves et al. 1991) keinen eindeutigen Hinweis auf ein berufliches Risiko, neuerdings wurde jedoch ein erhöhtes Risiko mit Arbeitertätigkeiten in Verbindung gebracht (Fratiglioni et al. 1993 ). Eine andere neue Studie, die auch die ältesten Altersgruppen umfasste, deutete darauf hin, dass die Lösungsmittelexposition ein ziemlich starker Risikofaktor sein könnte (Kukull et al. 1995). Die jüngste Vermutung, dass die Alzheimer-Krankheit mit der Exposition gegenüber elektromagnetischen Feldern zusammenhängen könnte, war vielleicht sogar noch überraschender (Sobel et al. 1995). Diese beiden Studien werden wahrscheinlich das Interesse an mehreren neuen Untersuchungen entlang der angegebenen Linien wecken.
Vor dem Hintergrund aktueller Perspektiven in der beruflichen Neuroepidemiologie scheint es daher, wie kurz skizziert, Anlass zu geben, zusätzliche arbeitsbezogene Studien zu verschiedenen, bisher mehr oder weniger vernachlässigten, neurologischen und neuropsychiatrischen Erkrankungen durchzuführen. Es ist nicht unwahrscheinlich, dass verschiedene berufliche Expositionen einige beitragende Wirkungen haben, so wie wir es bei vielen Krebsarten gesehen haben. Darüber hinaus können, wie in der ätiologischen Krebsforschung, aus der Berufsepidemiologie neue Hinweise auf die letztendlichen Ursachen oder Auslösemechanismen hinter einigen der schwerwiegenden neurologischen Erkrankungen gewonnen werden.
Nieren-Harn-Systeme
Das Nieren- und Harnsystem besteht aus einer komplexen Reihe von Organen, die zusammen dazu dienen, Abfallstoffe aus dem Blut zu filtern und Urin herzustellen, zu speichern und auszuscheiden. Diese Organsysteme sind lebenswichtig für die Homöostase, indem sie den Flüssigkeitshaushalt, das Säure-Basen-Gleichgewicht und den Blutdruck aufrechterhalten. Die primären Organe des Nieren-Harn-Systems sind die beiden Nieren und die Harnblase. Bei der Filterung von Abfallprodukten aus dem Blut sind die Nieren potenziell hohen Konzentrationen körpereigener und körperfremder Giftstoffe ausgesetzt. So sind manche Nierenzellen tausendfach höheren Konzentrationen ausgesetzt als im Blut.
Probleme, die zu einer Schädigung der Niere führen, können prärenal (beeinträchtigen die Blutversorgung der Niere), renal (betreffen die Niere selbst) oder postrenal (betreffen jeden Punkt auf dem Weg, den der Urin von der Niere bis zum Ende durchläuft) sein der Harnröhre oder des Penis). Postrenale Probleme sind in der Regel obstruktiver Natur; Eine häufige Obstruktionsstelle ist die Prostata, die zwischen der Blase und der Harnröhre liegt. Vorbestehende Erkrankungen der Prostata, Blase oder Harnleiter, insbesondere Infektionen, Obstruktionen oder Fremdkörper wie Steine, können die Nierenfunktion beeinträchtigen und die Anfälligkeit für erworbene oder genetische Defekte erhöhen.
Das Verständnis der Mikroanatomie und der molekularen Mechanismen der Nieren und der Blase ist wichtig, um die Anfälligkeit für berufliche Expositionen zu beurteilen und zu überwachen und zu verhindern. Giftstoffe scheinen auf bestimmte Teile der Niere oder Blase abzuzielen und führen zur Expression spezifischer Biomarker, die in direktem Zusammenhang mit dem geschädigten Segment stehen. In der Vergangenheit wurde die Prädisposition für Krankheiten aus der epidemiologischen Perspektive betrachtet, um eine Gruppe von gefährdeten Arbeitnehmern zu identifizieren. Mit einem besseren Verständnis der grundlegenden Krankheitsmechanismen zeichnet sich heute eine individuelle Risikobewertung durch die Verwendung von Biomarkern für Anfälligkeit, Exposition, Wirkung und Krankheit ab. Neue ethische Fragen entstehen aufgrund des Drucks, kosteneffiziente Strategien zum Schutz der Arbeitnehmer vor Berufsgefahren zu entwickeln. Der Druck entsteht zum Teil, weil Gentests immer mehr Akzeptanz für die Bewertung der Krankheitsprädisposition gewinnen und Biomarker für Exposition und Wirkung als Zwischenendpunkte dienen können, an denen eine Intervention von Vorteil sein kann. Zweck dieses Kapitels ist es, einen medizinischen Überblick über das Nieren- und Harnsystem zu geben, auf dessen Grundlage Leitlinien zur Bewertung und Reduzierung des individuellen Risikos am Arbeitsplatz unter gebührender Berücksichtigung der damit verbundenen ethischen Aspekte aufgestellt werden könnten.
Anatomie und Pathophysiologie der Niere
Die menschliche Niere ist ein komplexes Organ, das durch die Produktion von Urin Abfallstoffe aus dem Blut filtert. Die beiden Nieren erfüllen auch eine Vielzahl anderer lebenswichtiger Funktionen, darunter die Aufrechterhaltung der Homöostase, die Regulierung des Blutdrucks, des osmotischen Drucks und des Säure-Basen-Gleichgewichts. Die Nieren erhalten 25 % des gesamten Herzzeitvolumens an Blut, wodurch sie möglicherweise endogenen und exogenen Toxinen ausgesetzt werden.
Die Nieren befinden sich auf jeder Seite der Wirbelsäule im unteren Teil des Rückens. Jede wiegt etwa 150 Gramm und ist etwa so groß wie eine Orange. Die Niere besteht aus drei Schichten: der Rinde (äußere Schicht), dem Mark und dem Nierenbecken. Durch die Nierenarterie fließt Blut in die Rinde und das Mark und verzweigt sich in immer kleinere Arterien. Jede der Arterien endet in einer Blutfiltereinheit, die als Nephron bezeichnet wird. Eine gesunde Niere enthält ungefähr 1.2 Millionen Nephrone, die strategisch in der Rinde und im Medulla positioniert sind.
Ein Nephron besteht aus dem Glomerulus (einer Gruppe winziger Blutgefäße), der von einer Bowman-Kapsel (einer zweischichtigen Membran) umgeben ist, die sich in einen gewundenen Tubulus öffnet. Der flüssige Anteil des Blutes, Plasma, wird durch den Glomerulus in die Bowman-Kapsel gedrückt und gelangt dann als gefiltertes Plasma in den gewundenen Tubulus. Etwa 99 % des gefilterten Wassers und der essentiellen Nährstoffe werden von den Tubuluszellen resorbiert und in die Kapillaren geleitet, die den gewundenen Tubulus umgeben. Das ungefilterte Blut, das im Glomerulus verbleibt, fließt ebenfalls in Kapillaren und kehrt durch die Nierenvene zum Herzen zurück.
Die Nephrone erscheinen als lange, geschlungene Kanäle, die aus mehreren Segmenten bestehen, von denen jedes eine Vielzahl unterschiedlicher Funktionen erfüllt, die dazu bestimmt sind, die homöostatischen Mechanismen des Körpers aufrechtzuerhalten. Abbildung 1 zeigt ein Nephron und seine Orientierung innerhalb der Nierenrinde und der Medulla. Jedes Nephronsegment hat eine unterschiedliche Blutversorgung, die den Ionengradienten reguliert. Bestimmte Chemikalien können je nach Art und Dosis der Xenobiotika-Exposition akut oder chronisch bestimmte Segmente des Nephrons direkt beeinflussen. Je nach betroffenem Segment der Mikroanatomie können verschiedene Aspekte der Nierenfunktion betroffen sein.
Abbildung 1. Beziehungen der Gefäßversorgung, des Glomerulus und der röhrenförmigen Komponenten des Nephrons zueinander und die Ausrichtung dieser Komponenten innerhalb der Nierenrinde und des Nierenmarks
Blutgefäße zur Niere versorgen nur die glomerulären und tubulären Elemente, liefern zu filternde Abfälle und absorbieren Nährstoffe, Proteine und Elektrolyte zusätzlich zur Versorgung mit Sauerstoff für die Lebensfähigkeit der Organe. Neunzig Prozent des Blutflusses fließen in die Rinde, mit einer graduellen Abnahme zur Medulla. Ein derartiger unterschiedlicher Blutfluss und die Positionierung der Nephroneinheiten sind entscheidend für den Gegenstrommechanismus, der den Urin und potenzielle Nephrotoxine weiter konzentriert.
Der Glomerulus liegt zwischen den afferenten und efferenten Arteriolen. Die efferenten Arteriolen bilden ein Kapillarnetz um jede Nephroneinheit, mit Ausnahme der distalen Tubulus-Juxtaposition neben der afferenten Blutversorgung des Glomerulus. Afferente und efferente Tubuli, die von den sympathischen Nerven enerviert werden, reagieren auf autonome Stimulation und hormonelle Mediatoren wie Vasopression und antidiuretisches Hormon (ADH). Ein Bereich namens Macula densa, Teil des juxtaglomerulären Apparats, produziert Renin, einen Mediator des Blutdrucks, als Reaktion auf osmotische Veränderungen und den Blutdruck. Renin wird durch Leberenzyme in ein Octapeptid, Angiotensin II, umgewandelt, das den Blutfluss zu den Nieren reguliert und bevorzugt auf die afferenten Arteriolen und die Mesangialzellen des Glomerulus abzielt.
Der Glomerulus lässt nur Proteine bestimmter Größe mit definierter Ladung während der Filtration passieren. Die Plasmafiltration wird durch ein Gleichgewicht zwischen osmotischem und hydrostatischem Druck gesteuert. Spezialisierte Zuckermoleküle, Glykosaminoglykane, liefern eine negative anionische Ladung, die durch elektrostatische Kräfte die Filtration von negativ geladenen Materialien hemmt. Die dreizellige Schicht der glomerulären Basalmembran besteht aus mehreren Fußfortsätzen, die die Absorptionsfläche vergrößern und die Poren bilden, durch die das Filtrat strömt. Schäden an der spezialisierten Basalmembran oder dem Kapillarendothel können dazu führen, dass Albumin, eine Art Protein, in erhöhten Mengen in den Urin gelangt. Das Vorhandensein einer übermäßigen Menge an Albumin oder anderen Mikroproteinen im Urin dient als Marker für eine glomeruläre oder tubuläre Schädigung.
Das Niereninterstitium ist der Raum zwischen den Nephroneinheiten und ist im zentralen Markabschnitt stärker ausgeprägt als in der äußeren Rinde. Innerhalb des Interstitiums befinden sich interstitielle Zellen, die sich in unmittelbarer Nähe der medullären Blutgefäße und Tubuluszellen befinden. Mit zunehmendem Alter können interstitielle Zellen in der Hirnrinde mit damit verbundener Fibrose und Narbenbildung verstärkt hervortreten. Die interstitiellen Zellen enthalten Lipidtröpfchen und können an der Kontrolle des Blutdrucks mit der Freisetzung von gefäßentspannenden oder -verengenden Faktoren beteiligt sein. Eine chronische Erkrankung des Interstitiums kann den Glomerulus und die Tubuli beeinträchtigen, oder umgekehrt kann eine Erkrankung des Glomerulus und der Tubuli das Interstitium beeinträchtigen. Daher ist es bei einer Nierenerkrankung im Endstadium manchmal schwierig, die pathologischen Mechanismen des Nierenversagens genau zu definieren.
Die proximalen Sammelröhrchen absorbieren 80 % des Natriums, Wassers und Chlorids und 100 % des Harnstoffs. Jeder proximale Tubulus hat drei Segmente, wobei das letzte Segment (P-3) am anfälligsten für Xenobiotika (toxische Fremdsubstanzen) ist. Wenn die proximalen Zellen durch Schwermetalle wie Chrom geschädigt werden, wird die Konzentrationsfähigkeit der Niere beeinträchtigt und der Urin kann verdünnter sein. Die Toxizität gegenüber dem P-3-Segment führt zur Freisetzung von Enzymen wie alkalischer Phosphatase aus dem Darm, N-Acetyl-beta-D-glucosaminidase (NAG) oder Tamm-Horsfall-Protein, das mit dem bürstenartigen Syndrom in Verbindung gebracht wird, in den Urin Rand der proximalen Tubuluszellen, wodurch die effektive Absorptionsfläche vergrößert wird.
Diagnose und Prüfung auf Nephrotoxizität
Serum-Kreatinin ist eine weitere Substanz, die vom Glomerulus gefiltert, aber nur minimal von den proximalen Tubuli absorbiert wird. Eine Schädigung des Glomerulus führt zu seiner Unfähigkeit, vom Körper produzierte Toxine zu entfernen, und es kommt zu einer Anhäufung von Serum-Kreatinin. Da Serum-Kreatinin ein Produkt des Muskelstoffwechsels ist und von der Körpermasse des Patienten abhängt, hat es eine geringe Empfindlichkeit und Spezifität zur Messung der Nierenfunktion, wird aber häufig verwendet, weil es praktisch ist. Ein empfindlicherer und spezifischerer Test besteht darin, das Filtrat durch Messung der Kreatinin (Cr)-Clearance zu quantifizieren; Die Kreatinin-Clearance im Serum im Urin wird nach der allgemeinen Formel berechnet CCr=UCr V / P.Cr, Wobei UCrV ist die pro Zeiteinheit ausgeschiedene Cr-Menge und PCr ist die Plasmakonzentration des Cr. Die Kreatinin-Clearance ist jedoch hinsichtlich der Probennahme für den Test komplexer und daher für berufliche Tests unpraktisch. Isotopen-Clearance-Tests, die durch radioaktive Markierung von Verbindungen wie Ortho-Iodhippurat durchgeführt werden, die auch von der Niere ausgeschieden werden, sind ebenfalls wirksam, aber am Arbeitsplatz nicht praktikabel oder kosteneffektiv. Die unterschiedliche Funktion einzelner Nieren kann unter Verwendung von differenziellen Nierenkernscans oder einer selektiven Katheterisierung beider Nieren durch Einführen eines Katheters von der Blase nach oben durch den Harnleiter in die Niere bestimmt werden. Aber auch diese Verfahren werden nicht ohne weiteres für großangelegte Arbeitsplatztests eingesetzt. Da die Nierenfunktion vor einem nachweisbaren Anstieg des Serumkreatinins um 70 bis 80 % reduziert sein kann und andere bestehende Tests entweder unpraktisch oder kostspielig sind, werden nicht-invasive Biomarker benötigt, um eine niedrig dosierte akute intermittierende Exposition gegenüber der Niere zu erkennen. Im Abschnitt über Biomarker wird eine Reihe von Biomarkern zum Nachweis von Nierenschäden bei niedriger Dosis oder frühen Veränderungen im Zusammenhang mit der Karzinogenese diskutiert.
Obwohl die proximalen Tubuluszellen 80 % der Flüssigkeiten absorbieren, stimmen der Gegenstrommechanismus und die distalen Sammelkanäle die Menge der absorbierten Flüssigkeiten fein ab, indem sie ADH regulieren. ADH wird von der Hypophyse tief im Gehirn freigesetzt und reagiert auf osmotischen Druck und Flüssigkeitsvolumen. Exogene Verbindungen wie Lithium können die distalen Sammelrohre schädigen und zu renalem Diabetes insipidus (Verdünnungsharnabgang) führen. Vererbte genetische Störungen können diesen Defekt ebenfalls verursachen. Xenobiotika wirken sich normalerweise auf beide Nieren aus, aber die Interpretation ist kompliziert, wenn Expositionen schwer zu dokumentieren sind oder wenn eine vorbestehende Nierenerkrankung vorliegt. Folglich dienten versehentliche Hochdosis-Expositionen in vielen Fällen als Marker zur Identifizierung nephrotoxischer Verbindungen. Die meisten beruflichen Expositionen treten bei niedrigen Dosen auf und werden durch die Reservefiltration und Reparaturkompensationsfähigkeit (Hypertrophie) der Niere maskiert. Die verbleibende Herausforderung besteht darin, Niedrigdosis-Expositionen zu erkennen, die mit aktuellen Methoden klinisch unentdeckt bleiben.
Anatomie und Pathophysiologie der Blase
Die Harnblase ist eine hohle Tasche, in der Urin gespeichert wird; Normalerweise zieht es sich bei Bedarf zur kontrollierten Entleerung durch die Harnröhre zusammen. Die Blase befindet sich im vorderen, unteren Teil der Beckenhöhle. Die Blase ist auf beiden Seiten durch muskulöse, peristaltische Röhren, die Harnleiter, mit den beiden Nieren verbunden, die den Urin von den Nieren zur Blase transportieren. Nierenbecken, Harnleiter und Harnblase sind mit Übergangsepithel ausgekleidet. Die äußere Schicht des Urothels besteht aus Schirmzellen, die mit einer Kohlenhydratschicht, Glykosaminoglykan (GAG), überzogen sind. Die Übergangszellen erstrecken sich bis zur Basalmembran der Blase. Die tiefen Basalzellen werden somit durch die Schirmzellen geschützt, aber wenn die schützende GAG-Schicht beschädigt wird, sind die Basalzellen anfällig für Verletzungen durch Urinbestandteile. Die Mikroanatomie des Übergangsepithels erlaubt es, sich auszudehnen und zusammenzuziehen, und selbst bei normaler Ablösung der Schirmzellen bleibt die schützende Integrität der Basalzellen erhalten.
Das ausgeglichene neurologische System, das die Aufbewahrung und Entleerung reguliert, kann während eines Elektroschocks oder eines anderen Traumas, wie z. B. einer Rückenmarksverletzung, am Arbeitsplatz beschädigt werden. Eine Haupttodesursache bei Querschnittsgelähmten ist der Verlust der Blasenfunktion, was zu einer chronischen Nierenschädigung als Folge einer Infektion und Steinbildung führt. Chronische Infektionen durch unvollständige Entleerung aufgrund neurogener oder obstruktiver Ursachen wie Beckenfrakturen oder andere Traumata der Harnröhre und nachfolgender Strikturbildung sind häufig. Anhaltende bakterielle Infektionen oder Steinbildungen, die zu chronisch entzündlichen und bösartigen Erkrankungen der Blase führen, können durch eine verringerte Resistenz (dh Anfälligkeit) gegenüber exogenen Expositionen am Arbeitsplatz verursacht werden.
Moleküle, die mit Schäden und Reparaturen innerhalb der Blase assoziiert sind, dienen als potenzielle Zwischenendpunktmarker sowohl für toxische als auch für bösartige Zustände, da viele biochemische Veränderungen während der Veränderungen im Zusammenhang mit der Krebsentwicklung auftreten. Wie die Niere haben Blasenzellen aktive Enzymsysteme wie das Cytochrom P-450, das Xenobiotika aktivieren oder inaktivieren kann. Die funktionelle Aktivität der Enzyme wird durch genetische Vererbung bestimmt und weist einen genetischen Polymorphismus auf. Entleerter Urin enthält Zellen, die von der Niere, den Harnleitern, der Blase, der Prostata und der Harnröhre abgeblättert wurden. Diese Zellen bieten durch die Verwendung von Biomarkern Ziele zur Bewertung von Veränderungen in der Blasen- und Nierenpathologie. Wenn wir uns an Virchows Bemerkung erinnern, dass alle Krankheiten in den Zellen beginnen, lenken wir unsere Aufmerksamkeit auf die Bedeutung der Zellen, die der molekulare Spiegel der Expositionsepisoden sind.
Umwelt- und Arbeitstoxikologie
Eine beträchtliche Menge epidemiologischer Daten unterstützt den kausalen Zusammenhang beruflicher Expositionen bei Blasenkrebs, aber die genauen Beiträge der Exposition am Arbeitsplatz zu Nierenversagen und Nierenkrebs sind schwer abzuschätzen. In einem kürzlich erschienenen Bericht wurde geschätzt, dass bis zu 10 % der Nierenerkrankungen im Endstadium auf Expositionen am Arbeitsplatz zurückzuführen sind, aber die Ergebnisse sind aufgrund sich ändernder Umwelt- und chemischer Gefahren, unterschiedlicher diagnostischer Kriterien und der oft langen Latenzzeit schwer zu validieren zwischen Exposition und Krankheit. Es wird geschätzt, dass die Funktion von zwei Dritteln der Nephrone beider Nieren verloren gehen kann, bevor eine Nierenschädigung klinisch erkennbar ist. Es mehren sich jedoch die Beweise dafür, dass das, was früher als sozioökonomische oder ethnische Ursachen der Nephrotoxizität angesehen wurde, tatsächlich umweltbedingt sein kann, was die Rolle von Giftstoffen bei der Krankheitsentwicklung bestätigt.
Die Nephrotoxizität kann direkt mit dem Xenobiotikum zusammenhängen, oder das Xenobiotikum kann eine einstufige oder mehrstufige Aktivierung oder Inaktivierung in der Niere oder der Leber durchlaufen. Die Aktivierung von Xenobiotika wird durch komplexe Gruppen von Enzymen reguliert, die als Phase I, II und Nebenprodukte identifiziert werden. Ein Enzym der Phase I ist das oxidative System P-450, das über Reduktions- oder Hydrolysewege wirkt. Enzyme der Phase II katalysieren die Konjugation, während Hilfsenzyme den Arzneimittelstoffwechsel regulieren (Tabelle 1 listet diese Enzyme auf). Verschiedene Tiermodelle haben Einblicke in Stoffwechselmechanismen gegeben, und Studien von Nierenschnitten und Mikrodissektion der Nieren-Nephron-Einheiten in Gewebekultur fügen Einblicke in die pathologischen Mechanismen hinzu. Arten und individuelle Variablen sind jedoch beträchtlich, und obwohl die Mechanismen ähnlich sein können, ist bei der Extrapolation der Ergebnisse auf den Menschen am Arbeitsplatz Vorsicht geboten. Die Hauptprobleme bestehen nun darin, zu bestimmen, welche Xenobiotika nephrotoxisch und/oder karzinogen sind und an welchen Zielorten, und Methoden zu entwickeln, um die subklinische Toxizität im Nieren-Harn-System genauer zu identifizieren.
Tabelle 1. Enzyme des Arzneimittelstoffwechsels in der Niere1
| ENZYME | ||
| Phase I | Phase II | Neben- |
| Cytochrom P-450 | Esterase | GSH-Peroxide |
| Mikrosomale FAD-enthaltende Monooxygenase | N-Acetyltransferase | GSSG-Reduktase |
| Alkohol- und Aldehyddehydrogenasen | GSH S-Transferase | Hyperventilieren |
| Epoxidhydrolase | Thiol S-Methyltransferase | Katalase |
| Prostaglandin-Synthase | UDP-Glucuronosyltransferase | DT-Diaphorase |
| Monoaminoxidase | Sulfotransferase | NADPH-erzeugende Wege |
1 Enzyme der Phase I katalysieren Oxidation, Reduktion oder Hydrolyse.
Enzyme der Phase II katalysieren im Allgemeinen die Konjugation.
Hilfsenzyme wirken sekundär oder unterstützend, um den Arzneimittelstoffwechsel zu erleichtern.
Quelle: Nationaler Forschungsrat 1995.
Nicht bösartige Erkrankungen der Nieren und Harnwege
Glomerulonephritis ist ein entzündlicher reaktiver Zustand der glomerulären Basalmembran oder des kapillären Endothels. Akute und chronische Formen der Krankheit werden durch eine Vielzahl von infektiösen, autoimmunen oder entzündlichen Zuständen oder durch Exposition gegenüber toxischen Mitteln verursacht. Glomerulonephritis ist mit Vaskulitis assoziiert, entweder systemisch oder auf die Niere beschränkt. Eine sekundäre chronische Schädigung des Glomerulus tritt auch während eines intensiven Angriffszyklus von Nephrotoxizität auf das Interstitium der Tubuluszellen auf. Epitheliale glomeruläre Halbmonde oder proliferative Formen sind ein Kennzeichen der Glomerulonephritis in Nierenbiopsieproben. Blut, rote Blutkörperchen (RBC) oder Protein im Urin und Bluthochdruck sind Symptome einer Glomerulonephritis. Eine Veränderung der Blutproteine kann mit einer Verringerung bestimmter Fraktionen des Serumkomplements auftreten, einem komplexen Satz interagierender Proteine, die am Immunsystem, der Wirtsabwehr und den Gerinnungsfunktionen beteiligt sind. Direkte und indirekte Beweise unterstützen die Bedeutung von Xenobiotika als ursächlicher Faktor der Glomerulonephritis.
Der Glomerulus schützt die sauerstofftragenden roten Blutkörperchen davor, seinen Filter zu passieren. Nach der Zentrifugation enthält normaler Urin nur ein Erythrozyten pro 10 ml, wenn er mit einem Hochleistungs-Lichtmikroskop betrachtet wird. Wenn Erythrozyten durch den glomerulären Filter austreten und möglicherweise individuell dysmorph werden, bilden sich Erythrozytenabgüsse, die die zylindrische Form der sammelnden Nephrone annehmen.
Zur Unterstützung der Bedeutung von Toxinen als ätiologischer Faktor bei Glomerulonephritis zeigen epidemiologische Studien vermehrt Hinweise auf toxische Expositionen bei Patienten, die sich einer Dialyse unterzogen haben oder bei denen eine Glomerulonephritis diagnostiziert wurde. Hinweise auf eine glomeruläre Schädigung durch akute Kohlenwasserstoffexposition sind selten, wurden jedoch in epidemiologischen Studien mit Odds Ratios im Bereich von 2.0 bis 15.5 beobachtet. Ein Beispiel für akute Toxizität ist die Goodpasture-Krankheit, die aus einer Kohlenwasserstoffstimulation der Antikörperproduktion gegen Leber- und Lungenproteine resultiert, die mit der Basalmembran kreuzreagieren. Eine Verschlimmerung des nephrotischen Syndroms, große Proteinmengen im Urin, wurde auch bei Personen beobachtet, die organischen Lösungsmitteln erneut ausgesetzt waren, während andere Studien einen historischen Zusammenhang mit einem Spektrum von Nierenerkrankungen aufzeigen. Andere Lösungsmittel wie Entfettungsmittel, Farben und Klebstoffe sind an chronischeren Formen der Krankheit beteiligt. Das Bewusstsein für die Mechanismen der Lösungsmittelausscheidung und -reabsorption hilft bei der Identifizierung von Biomarkern, da selbst eine minimale Schädigung des Glomerulus zu einem erhöhten Austritt von Erythrozyten in den Urin führt. Obwohl Erythrozyten im Urin ein Kardinalzeichen einer glomerulären Schädigung sind, ist es wichtig, andere Ursachen einer Hämaturie auszuschließen.
Interstitielle und tubuläre Nephritis. Wie bereits erwähnt, ist die Ätiologie einer chronischen Nierenerkrankung im Endstadium häufig schwer zu ermitteln. Sie kann primär glomerulären, tubulären oder interstitiellen Ursprungs sein und aufgrund multipler akuter Episoden oder chronischer, niedrig dosierter Prozesse auftreten. Chronische interstitielle Nephritis umfasst Fibrose und tubuläre Atrophie. In ihrer akuten Form äußert sich die Erkrankung durch ein ausgeprägtes entzündliches Infiltrat mit begleitender Flüssigkeitsansammlung in den Zwischenräumen. Eine interstitielle Nephritis kann primär das Interstitium betreffen oder sich als sekundäres Ereignis einer chronischen tubulären Verletzung manifestieren, oder sie kann aus postrenalen Ursachen wie Obstruktion resultieren. Prostaglandin-A-Synthase, ein Enzym, kommt hauptsächlich im Interstitium vor und ist mit dem endoplasmatischen Retikulum, einem Teil der Proteinmaschinerie der Zelle, assoziiert. Bestimmte Xenobiotika wie Benzidin und Nitrofurane sind reduzierende Co-Substrate für die Prostaglandin-Synthase und sind für das tubuläre Interstitium toxisch.
Tubuläre und interstitielle Verletzungen können durch Kontakt mit Cadmium, Blei oder einer Vielzahl von organischen Lösungsmitteln auftreten. Die meisten Expositionen sind chronisch, niedrig dosiert und die Toxizität wird durch die Nierenfunktionsreserve und die Fähigkeit der Niere, einige Funktionen wiederherzustellen, maskiert. Eine interstitielle Nephritis kann auch aus einer Gefäßverletzung resultieren, wie sie beispielsweise durch eine chronische Exposition gegenüber Kohlenmonoxid verursacht wird. Proximale Tubuluszellen sind am anfälligsten für toxische Substanzen im Blut, da sie Toxinen, die durch den Glomerulus filtern, internen Enzymsystemen, die Giftstoffe aktivieren, und dem selektiven Transport von Giftstoffen intensiv ausgesetzt sind. Das Epithel in den verschiedenen Segmenten des proximalen Tubulus hat leicht unterschiedliche Qualitäten von lysosomalen Peroxidase-Enzymen und anderen Verbindungen der genetischen Maschinerie. Daher kann eine Exposition gegenüber Chrom sowohl zu interstitiellen als auch zu tubulären Verletzungen führen. Schäden an den Sammelröhrchen können auftreten, wenn bestimmte Enzyme verschiedene Xenobiotika wie Chloroform, Paracetamol und andere aktivieren p-Aminophenol und Antibiotika wie Loradine. Eine sekundäre Folge der Schädigung der Sammelrohre ist die Unfähigkeit der Niere, den Urin anzusäuern, und die nachfolgende Entwicklung einer metabolischen Übersäuerung.
Nephrogener Diabetes insipidus, der Zustand, in dem der Urin verdünnt wird, kann genetisch bedingt oder erworben sein. Bei der genetischen Form handelt es sich um Mutationen der ADH-Rezeptoren, die sich auf der basalen lateralen Membran der Sammelrohre in der absteigenden Henle-Schleife befinden. ADH reguliert die Resorption von Wasser und bestimmten Ionen wie Kalium. Erworbener Diabetes insipidus kann die Tubuluszellen oder das zugehörige Interstitium betreffen, die beide aufgrund einer Vielzahl von Zuständen erkrankt sein können. Nephrogener Diabetes insipidus kann aufgrund einer diffusen Beteiligung des Interstitiums eine Nierenerkrankung im Endstadium begleiten. Folglich ist das Interstitium nicht in der Lage, eine hypertonische Umgebung für eine passive Wasserbewegung aus den röhrenförmigen Sammelkanälen aufrechtzuerhalten. Zustände, die diffuse interstitielle Veränderungen verursachen können, sind Pyelonephritis, Sichelzellenanämie und obstruktive Uropathie. Die mögliche Assoziation dieser Zustände mit beruflicher Exposition ist eine erhöhte Anfälligkeit der Niere für Fremdstoffe. Es wurde eine begrenzte Anzahl nephrotoxischer Verbindungen identifiziert, die insbesondere auf die Sammelrohrzellen abzielen. Häufigkeit, Nykturie (häufigeres nächtliches Wasserlassen) und Polydipsie (chronischer Durst) sind Symptome des nephrogenen Diabetes insipidus. Die Bewegung von Flüssigkeiten durch die Sammelrohrzellen führt zu Kanälen, die sich als Reaktion auf ADH bilden und die mikrotubuläre Funktion der Zellen beeinflussen; Folglich können Medikamente wie Colchicin die ADH beeinflussen. Zwei Medikamente, die anscheinend durch leicht unterschiedliche Mechanismen wirken, um ADH zu korrigieren, sind Hydrochlorothiazid und Indomethacin, ein Prostaglandin-Synthase-Hemmer.
Lithiuminduzierter Diabetes insipidus korreliert mit der Dauer der Lithiumtherapie, dem durchschnittlichen Serum-Lithiumspiegel und der Lithiumcarbonat-Gesamtdosis. Interessanterweise reichert sich Lithium in den Sammelrohren an und beeinflusst zyklisches AMP, einen Teil des Pumpwegs des Energiestoffwechsels. Die Exposition gegenüber anderen Verbindungen wie Methoxyfluran und Demeclocyclin, von denen letzteres zur Behandlung von Akne verwendet wird, führt über einen alternativen Weg auch zu nephrogenem Diabetes insipidus, wodurch die Epithelzellen nicht mehr auf ADH ansprechen.
Hypertonieoder erhöhter Blutdruck, die zweithäufigste Ursache einer Nierenerkrankung im Endstadium, ist mit mehreren ätiologischen Signalwegen verbunden. Bluthochdruck kann durch diabetische Nephropathie, obstruktive Nephropathie, Glomerulonephritis, polyzystische Nierenerkrankung, Pyelonephritis und Vaskulitis verursacht werden, und viele dieser Krankheiten sind mit der Exposition gegenüber toxischen Verbindungen verbunden. Eine begrenzte Anzahl beruflicher Expositionen steht in direktem Zusammenhang mit Bluthochdruck. Eines davon ist Blei, das eine renale Gefäßischämie und Verletzungen verursacht. Der Mechanismus der bleiinduzierten Hypertonie wird wahrscheinlich durch den juxtaglomerulären Apparat, die Freisetzung von Renin und die Spaltung von Renin durch Leberenzyme zu Angiotensin II reguliert. Medikamente, die mit Bluthochdruck in Verbindung gebracht werden, umfassen Amphetamine, Östrogene und orale Kontrazeptiva, Steroide, Cisplatin, Alkohol und trizyklische Antidepressiva. Bluthochdruck kann schleichend beginnen oder akut und bösartiger Natur sein. Maligne Hypertonie, bei der der diastolische Druck größer als 110 mmHg ist, geht mit Übelkeit, Erbrechen und starken Kopfschmerzen einher und stellt einen medizinischen Notfall dar. Zur Behandlung von Bluthochdruck stehen zahlreiche Medikamente zur Verfügung, aber eine Überbehandlung kann zu einer verminderten Nierendurchblutung und einem weiteren Verlust der Nierenfunktion führen. Wann immer möglich, ist das Absetzen des Nephrotoxins die Behandlung der Wahl.
Differentialdiagnose von Hämaturie und Proteinurie
Hämaturie (rote Blutkörperchen im Urin) und Pyurie (weiße Blutkörperchen im Urin) sind primäre Symptome vieler Erkrankungen des Nieren-Harnsystems und können für kategorische Zwecke als unspezifische zelluläre Biomarker betrachtet werden. Wegen ihrer Bedeutung werden sie hier gesondert behandelt. Eine Herausforderung für den Arbeitsmediziner besteht darin, festzustellen, ob Hämaturie eine dauerhafte Grunderkrankung bedeutet, die potenziell lebensbedrohlich sein kann, oder ob sie auf berufliche Expositionen zurückzuführen ist. Die klinische Beurteilung der Hämaturie erfordert eine Standardisierung und Bestimmung, ob sie prärenalen, renalen oder postrenalen Ursprungs ist.
Hämaturie kann von Läsionen in der Niere per se oder irgendwo entlang des Weges des entleerten Urins herrühren. Ursprungsorte sind Niere, Nierenbecken, Harnleiter, Blase, Prostata und Harnröhre. Aufgrund der schwerwiegenden Erkrankungen, die mit Hämaturie einhergehen, rechtfertigt eine einzelne Episode eine medizinische oder urologische Untersuchung. Mehr als ein Erythrozyten pro Hochleistungsfeld kann ein Krankheitssignal sein, aber eine signifikante Hämaturie kann bei mikroskopischer Analyse in Gegenwart von hypotonischem (verdünntem) Urin übersehen werden, der Erythrozyten lysieren kann. Pseudohämaturie kann durch Rüben, Beeren, Pflanzenfarbstoffe und konzentrierte Urate verursacht werden. Anfängliche Hämaturie deutet auf einen urethralen Ursprung hin, terminale Hämaturie ist normalerweise prostatischen Ursprungs und das Blut während der gesamten Entleerung stammt aus der Blase, Niere oder dem Harnleiter. Eine Makrohämaturie ist in 21 % der Fälle mit Blasentumoren assoziiert, eine Mikrohämaturie jedoch viel seltener (2.2 bis 12.5 %).
Das Auffinden dysmorpher Zellen bei der quantitativen Beurteilung der Hämaturie deutet auf einen Ursprung in den oberen Trakten hin, insbesondere wenn es mit Erythrozytenabgüssen assoziiert ist. Das Verständnis von Hämaturie im Zusammenhang mit Proteinurie bietet zusätzliche Informationen. Die glomeruläre Filtrationsvorrichtung schließt Proteine mit einem Molekulargewicht von mehr als 250,000 Dalton fast vollständig aus, während Proteine mit niedrigem Molekulargewicht frei gefiltert und normal von den Tubuluszellen absorbiert werden. Das Vorhandensein von Proteinen mit hohem Molekulargewicht im Urin deutet auf eine Blutung des unteren Trakts hin, während Proteine mit niedrigem Molekulargewicht mit einer tubulären Verletzung assoziiert sind. Die Bewertung des Verhältnisses von α-Mikroglobulin zu Albumin und α-Makroglobulin zu Albumin hilft bei der Abgrenzung zwischen glomerulärer und tubulärer interstitieller Nephropathie und Blutungen des unteren Trakts, die möglicherweise mit urothelialen Neoplasien und anderen postrenalen Ursachen wie Harnwegsinfektionen verbunden sind.
Ein besonderes diagnostisches Problem ergibt sich, wenn zwei oder mehr Krankheitsprozesse gleichzeitig vorliegen, die die gleichen Symptome verursachen. Beispielsweise wird Hämaturie sowohl bei urothelialen Neoplasien als auch bei Harnwegsinfektionen beobachtet. Bei einem Patienten mit beiden Krankheiten würde der Krebs zurückbleiben, wenn die Infektion behandelt und behoben wird. Daher ist es wichtig, die wahre Ursache der Symptome zu identifizieren. Hämaturie liegt bei 13 % der gescreenten Populationen vor; Ungefähr 20 % der Personen haben signifikante Nieren- oder Blasenerkrankungen und 10 % von ihnen entwickeln eine urogenitale Malignität. Folglich ist die Hämaturie ein wichtiger Biomarker für Krankheiten, der angemessen bewertet werden muss.
Die klinische Interpretation der Hämaturie wird durch die Kenntnis des Alters und des Geschlechts des Patienten verbessert, wie in Tabelle 2 angegeben, die die Ursachen der Hämaturie im Verhältnis zum Alter und Geschlecht des Patienten zeigt. Andere Ursachen für Hämaturie sind Nierenvenenthrombose, Hyperkalurie und Vaskulitis sowie Traumata wie Joggen oder andere Sportarten und berufliche Ereignisse oder Expositionen. Die klinische Beurteilung der Hämaturie erfordert eine Röntgenaufnahme der Niere, ein intravenöses Pyelogramm (IVP), um Erkrankungen der oberen Harnwege einschließlich Nierensteine und Tumore auszuschließen, und eine Zystoskopie (Blasenspiegelung durch ein beleuchtetes Instrument), um Blase, Prostata oder Urothel auszuschließen Krebs. Subtile vaginale Ursachen müssen bei Frauen ausgeschlossen werden. Unabhängig vom Alter eines Patienten ist eine klinische Untersuchung angezeigt, wenn eine Hämaturie auftritt, und abhängig von der identifizierten Ätiologie können sequentielle Nachuntersuchungen angezeigt sein.
Tabelle 2. Die häufigsten Ursachen für Hämaturie, nach Alter und Geschlecht
| 0 – 20 Jahre | 40–60 Jahre (Frauen) |
| Akute Glomerulonephritis Akuter Harnwegsinfekt Angeborene Anomalien der Harnwege mit Obstruktion |
Akuter Harnwegsinfekt Stones Blasentumor |
| 20 – 40 Jahre | 60+ Jahre (Männer) |
| Akuter Harnwegsinfekt Stones Blasentumor |
Benigne Prostatahyperplasie Blasentumor Akuter Harnwegsinfekt |
| 40–60 Jahre (Männer) | 60+ Jahre (Frauen) |
| Blasentumor Stones Akuter Harnwegsinfekt |
Blasentumore Akuter Harnwegsinfekt |
Quelle: Wyker 1991.
Die Verwendung kürzlich identifizierter Biomarker in Verbindung mit konventioneller Zytologie zur Beurteilung der Hämaturie hilft sicherzustellen, dass keine okkulte oder beginnende Malignität übersehen wird (siehe nächster Abschnitt über Biomarker). Für den Arbeitsmediziner ist es wichtig festzustellen, ob die Hämaturie das Ergebnis einer toxischen Exposition oder einer okkulten Malignität ist. Die Kenntnis der Exposition und des Alters des Patienten sind entscheidende Parameter für eine fundierte klinische Managemententscheidung. Eine kürzlich durchgeführte Studie hat gezeigt, dass Hämaturie und Biomarkeranalyse an abgeblätterten Harnzellen aus der Blase zusammen die beiden besten Marker für die Erkennung prämaligner Blasenläsionen waren. Hämaturie wird in allen Fällen von glomerulärer Schädigung, nur bei 60 % der Patienten mit Blasenkrebs und nur bei 15 % der Patienten mit bösartigen Tumoren der Niere selbst beobachtet. Somit bleibt Hämaturie ein Kardinalsymptom von Nieren- und postrenalen Erkrankungen, aber die endgültige Diagnose kann komplex sein.
Nephrotoxizitätstests: Biomarker
In der Vergangenheit war die Überwachung von Toxinen in der Arbeitsumgebung die primäre Methode zur Identifizierung von Risiken. Allerdings sind nicht alle Giftstoffe bekannt und können daher nicht überwacht werden. Auch die Anfälligkeit ist ein Faktor dafür, ob Xenobiotika Individuen beeinflussen.
Abbildung 2. Kategorien von Biomarkern.
Biomarker bieten neue Möglichkeiten, individuelle Risiken zu definieren. Zu beschreibenden Zwecken und um einen Rahmen für die Interpretation bereitzustellen, wurden Biomarker gemäß dem in Abbildung 2 dargestellten Schema klassifiziert. Wie bei anderen Krankheiten können Biomarker für Nephrotoxizität und urogenitale Toxizität mit Anfälligkeit, Exposition, Wirkung oder Krankheit zusammenhängen. Biomarker können genotypisch oder phänotypisch sein und können funktionell, zellulär oder in Urin, Blut oder anderen Körperflüssigkeiten löslich sein. Beispiele für lösliche Marker sind Proteine, Enzyme, Zytokine und Wachstumsfaktoren. Biomarker können als Gen, Botschaft oder Proteinprodukt getestet werden. Diese variablen Systeme erhöhen die Komplexität der Bewertung und Auswahl von Biomarkern. Ein Vorteil des Testens des Proteins besteht darin, dass es das funktionelle Molekül ist. Das Gen wird möglicherweise nicht transkribiert und die Menge der Nachricht entspricht möglicherweise nicht dem Proteinprodukt. Eine Liste von Kriterien für die Biomarkerauswahl ist in Tabelle 3 dargestellt.
Tabelle 3. Kriterien für die Biomarkerauswahl
| Klinischer Nutzen | Assay-Überlegungen |
| Starker Biomarker | Stabilität des Reagenzes |
| Sensitivität | Kosten für Reagenz |
| Spezifität | Befestigungsanforderungen |
| Negativer Vorhersagewert | Reproduzierbarkeit des Assays |
| Positiv vorhergesagter Wert | Maschinensensible Parameter |
| Funktionale Rolle | Beitrag zum Biomarkerprofil |
| Sequenz in der Onkogenese | Anpassungsfähigkeit an die Automatisierung |
Quelle: Hemstreet et al. 1996.
Das internationale wissenschaftliche Engagement zur Kartierung des menschlichen Genoms, das durch Fortschritte in der Molekularbiologie ermöglicht wurde, schuf die Grundlage für die Identifizierung von Biomarkern für Anfälligkeit. Die meisten Fälle menschlicher Krankheiten, insbesondere solche, die aus der Exposition gegenüber Giftstoffen in der Umwelt resultieren, beinhalten eine Konstellation von Genen, die eine ausgeprägte genetische Vielfalt widerspiegeln (genetischer Polymorphismus). Ein Beispiel für ein solches Genprodukt ist, wie zuvor erwähnt, das oxidative Enzymsystem P-450, das Xenobiotika in der Leber, Niere oder Blase metabolisieren kann. Anfälligkeitsfaktoren können auch den grundlegenden Mechanismus für die DNA-Reparatur steuern, die Anfälligkeit verschiedener Signalwege beeinflussen, die für die Tumorentstehung wichtig sind (dh Wachstumsfaktoren) oder mit erblichen Zuständen zusammenhängen, die für Krankheiten prädisponieren. Ein wichtiges Beispiel für einen vererbten Anfälligkeitsfaktor ist der Phänotyp der langsamen oder schnellen Acetylierung, der die Acetylierung und Inaktivierung bestimmter aromatischer Amine reguliert, von denen bekannt ist, dass sie Blasenkrebs verursachen. Biomarker der Empfindlichkeit können nicht nur Gene umfassen, die die Aktivierung von Xenobiotika regulieren, sondern auch Proto-Onkogene und Suppressor-Onkogene. Die Kontrolle des Tumorzellwachstums umfasst eine Reihe komplexer, interagierender Systeme. Diese schließen ein Gleichgewicht von positiven (Proto-)Onkogenen und negativen (Suppressor-)Onkogenen ein. Proto-Onkogene kontrollieren das normale Zellwachstum und die normale Zellentwicklung, während Suppressor-Onkogene die normale Zellteilung und -differenzierung kontrollieren. Andere Gene können zu bereits bestehenden Erkrankungen beitragen, wie z. B. einer Neigung zu Nierenversagen, die durch zugrunde liegende Erkrankungen wie eine polyzystische Nierenerkrankung ausgelöst wird.
Ein Expositions-Biomarker kann das Xenobiotikum selbst, der Stoffwechselmetabolit oder Marker wie DNA-Addukte sein. In einigen Fällen kann der Biomarker an ein Protein gebunden sein. Biomarker der Exposition können auch Biomarker der Wirkung sein, wenn die Wirkung vorübergehend ist. Wenn ein Wirkungs-Biomarker bestehen bleibt, kann er zu einem Krankheits-Biomarker werden. Nützliche Biomarker der Wirkung haben eine hohe Assoziation mit einem Giftstoff und weisen auf eine Exposition hin. Für den Krankheitsnachweis hat die Expression des Biomarkers in unmittelbarer Folge zum Ausbruch der Krankheit die höchste Spezifität. Die erwartete Sensitivität und Spezifität eines Biomarkers hängt vom Nutzen-Risiko-Verhältnis der Intervention ab. Beispielsweise kann ein Biomarker wie F-Aktin, ein Zytoskelettprotein-Differenzierungsmarker, der in der frühen Karzinogenese verändert erscheint, eine schlechte Spezifität für die Erkennung von Präkanzerosen aufweisen, da nicht alle Personen mit einem abnormalen Marker eine Krankheit entwickeln. Es kann jedoch nützlich sein, um Personen auszuwählen und sie zu überwachen, während sie sich einer Chemoprävention unterziehen, vorausgesetzt, die Therapie ist nicht toxisch. Das Verständnis des Zeitrahmens und der funktionellen Verknüpfung zwischen einzelnen Biomarkern ist für die individuelle Risikobewertung und das Verständnis der Mechanismen der Karzinogenese und Nephrotoxizität äußerst wichtig.
Biomarker der Nephrotoxizität
Biomarker der Nephrotoxizität können mit der Ätiologie des Nierenversagens (dh prärenal, renal oder postrenal) und den an der Pathogenese des Prozesses beteiligten Mechanismen zusammenhängen. Dieser Prozess umfasst zelluläre Schäden und Reparaturen. Toxische Schädigungen können Zellen, Glomerulus, Interstitium oder Tubuli mit Freisetzung entsprechender Biomarker betreffen. Xenobiotika können mehr als ein Kompartiment beeinflussen oder aufgrund der gegenseitigen Abhängigkeit der Zellen innerhalb des Kompartiments Biomarkerveränderungen verursachen. Entzündliche Veränderungen, Autoimmunprozesse und immunologische Prozesse fördern zusätzlich die Freisetzung von Biomarkern. Xenobiotika können unter bestimmten Umständen auf ein Kompartiment und unter anderen Bedingungen auf ein anderes Kompartiment abzielen. Ein Beispiel ist Quecksilber, das akut nephrotoxisch für den proximalen Tubulus ist, während es chronisch die Arteriolen beeinflusst. Die Reaktion auf eine Verletzung kann in mehrere Hauptkategorien eingeteilt werden, einschließlich Hypertrophie, Proliferation, Degeneration (Nekrose und Apoptose oder programmierter Zelltod) und Membranveränderungen.
Die Mehrzahl der Anfälligkeitsfaktoren stehen im Zusammenhang mit nicht xenobiotisch bedingten Nierenerkrankungen. Jedoch werden 10 % der Fälle von Nierenversagen auf umweltbedingte Expositionen gegenüber toxischen Verbindungen oder iatrogene Induktion durch verschiedene Verbindungen, wie Antibiotika, oder Verfahren, wie die Verabreichung eines Nieren-Röntgenkontrastmittels an einen Diabetiker, zurückgeführt. Am Arbeitsplatz hat die Erkennung eines subklinischen Nierenversagens vor einer potenziellen zusätzlichen nephrotoxischen Belastung einen potenziellen praktischen Nutzen. Wenn ein Stoff im Verdacht steht, xenobiotisch zu sein, und er zu einer Wirkung speziell im kausalen Weg der Krankheit führt, ist eine Intervention zur Umkehrung der Wirkung möglich. Somit beseitigen Wirkungs-Biomarker viele der Probleme bei der Berechnung der Exposition und der Definition der individuellen Anfälligkeit. Die statistische Analyse von Wirkungsbiomarkern in Bezug auf Empfindlichkeits- und Expositionsbiomarker sollte die Markerspezifität verbessern. Je spezifischer der Biomarker der Wirkung ist, desto geringer ist die Notwendigkeit einer großen Probengröße, die für die wissenschaftliche Identifizierung potenzieller Toxine erforderlich ist.
Wirkungs-Biomarker sind die wichtigste Klasse von Markern und verknüpfen die Exposition gegenüber Anfälligkeit und Krankheit. Wir haben uns zuvor mit der Kombination von zellulären und löslichen Biomarkern befasst, um zwischen Hämaturie mit Ursprung im oberen oder unteren Trakt zu unterscheiden. Eine Liste löslicher Biomarker, die potenziell mit zellulärer Nephrotoxizität in Zusammenhang stehen, ist in Tabelle 4 aufgeführt. Bisher erkennt keiner dieser Biomarker allein oder als Multi-Biomarker-Panel eine subklinische Toxizität mit angemessener Sensitivität. Einige Probleme bei der Verwendung löslicher Biomarker sind mangelnde Spezifität, Enzyminstabilität, der Verdünnungseffekt von Urin, Schwankungen der Nierenfunktion und unspezifische Proteinwechselwirkungen, die die Spezifität der Analyse trüben können.
Tabelle 4. Potenzielle Biomarker im Zusammenhang mit Zellschädigungen
|
Immunologische Faktoren: -Humoral-Antikörper und Antikörperfragmente; Komponenten der Komplementkaskade und Gerinnungsfaktoren - Zelluläre Lymphozyten, mononukleäre Phagozyten und andere aus dem Knochenmark stammende Effektoren (Oesinophile, Basophile, Neutrophile und Blutplättchen) Lymphokine Haupthistokompatibilitätsantigene Wachstumsfaktoren und Zytokine: Thrombozyten-Wachstumsfaktor, epidermaler Wachstumsfaktor, transformierender Wachstumsfaktor (TGF), Tumor-Nekrose-Faktor, Interleukin-1 usw. Lipidmediatoren: Prostaglandine Endotheline |
Bestandteile der extrazellulären Matrix: -Kollagene -Prokollagen -Laminin -Fibronektin Reaktive Sauerstoff- und Stickstoffspezies Transkriptionsfaktoren und Protoonkogene: c-myc, c-fos, c-jun, c-Haras, c-Ki-ras und Egr-1 Hitzeschockproteine |
Quelle: Finn, Hemstreet et al. im Nationalen Forschungsrat 1995.
Ein löslicher Wachstumsfaktor mit potenzieller klinischer Anwendung ist der epidermale Wachstumsfaktor im Urin (EGF), der von der Niere ausgeschieden werden kann und auch bei Patienten mit Übergangszellkarzinom der Blase verändert ist. Die Quantifizierung von Urinenzymen wurde untersucht, aber die Nützlichkeit davon wurde durch die Unfähigkeit, den Ursprung des Enzyms zu bestimmen, und die fehlende Reproduzierbarkeit des Assays eingeschränkt. Die Verwendung von Urinenzymen und ihre weitverbreitete Akzeptanz war aufgrund der zuvor erwähnten restriktiven Kriterien langsam. Zu den bewerteten Enzymen gehören Alaminopeptidase, NAG und intestinale alkalische Phosphatase. NAG ist aufgrund seiner Lokalisierung im S3-Segment des Tubulus vielleicht der am weitesten verbreitete Marker zur Überwachung der proximalen Tubuluszellverletzung. Da die genaue Ursprungszelle und die pathologische Ursache der Enzymaktivität im Urin unbekannt sind, ist die Interpretation der Ergebnisse schwierig. Darüber hinaus können Medikamente, diagnostische Verfahren und Begleiterkrankungen wie Myokardinfarkt die Interpretation trüben.
Ein alternativer Ansatz besteht darin, monoklonale Antikörper-Biomarker zu verwenden, um tubuläre Zellen im Urin aus verschiedenen Bereichen des Nephronsegments zu identifizieren und zu quantifizieren. Die Nützlichkeit dieses Ansatzes hängt von der Aufrechterhaltung der Integrität der Zelle für die Quantifizierung ab. Dies erfordert eine geeignete Fixierung und Probenhandhabung. Jetzt sind monoklonale Antikörper verfügbar, die auf spezifische Tubuluszellen abzielen und beispielsweise proximale Tubuluszellen von distalen Tubuluszellen oder gewundenen Tubuluszellen unterscheiden. Die Transmissionsmikroskopie kann Unterschiede zwischen Leukozyten und verschiedenen Typen von Tubuluszellen nicht effektiv auflösen, im Gegensatz zur Elektronenmikroskopie, die beim Nachweis einer Transplantatabstoßung wirksam war. Techniken wie die quantitative Hochgeschwindigkeits-Fluoreszenzbildanalyse von tubulären Zellen, die mit monoklonalen Antikörpern gefärbt sind, sollten dieses Problem lösen. In naher Zukunft sollte es möglich sein, eine subklinische Nephrotoxizität bei einer Exposition mit hoher Sicherheit nachzuweisen.
Biomarker bösartiger Erkrankungen
Solide Krebsarten entstehen in vielen Fällen aus einem Feld von biochemisch veränderten Zellen, die histologisch oder zytologisch verändert sein können oder nicht. Technologien wie die quantitative Fluoreszenzbildanalyse, die in der Lage sind, Biomarker im Zusammenhang mit prämalignen Erkrankungen mit Sicherheit nachzuweisen, bieten den Horizont für eine gezielte Chemoprävention. Biochemische Veränderungen können in einem abwechslungsreichen oder geordneten Prozess auftreten. Phänotypisch äußern sich diese Veränderungen in einer allmählichen morphologischen Progression von Atypie zu Dysplasie und schließlich zu offenkundiger Malignität. Kenntnisse der „funktionale Rolle“ eines Biomarkers und „wenn es in der Sequenz der Tumorentstehung exprimiert wird“ hilft bei der Definition seines Nutzens zur Identifizierung prämaligner Erkrankungen, zur Erstellung einer Frühdiagnose und zur Entwicklung eines Panels von Biomarkern zur Vorhersage von Tumorrezidiven und -progression. Ein Paradigma für die Bewertung von Biomarkern entwickelt sich und erfordert die Identifizierung einzelner und mehrerer Biomarkerprofile.
Blasenkrebs scheint sich auf zwei getrennten Wegen zu entwickeln: einem niedergradigen Weg, der anscheinend mit Veränderungen auf Chromosom 9 verbunden ist, und einem zweiten Weg, der mit dem genetisch veränderten P-53-Suppressorgen auf Chromosom 17 verbunden ist. Offensichtlich sind mehrere genetische Faktoren mit der Krebsentstehung verbunden. und die Definition der genetischen Faktoren in jedem Individuum ist eine schwierige Aufgabe, insbesondere wenn der genetische Weg mit einer Komplexität von möglicherweise mehreren Expositionen verbunden sein muss. In epidemiologischen Studien waren Expositionen über längere Zeiträume schwer zu rekonstruieren. Batterien von phänotypischen und genotypischen Markern werden identifiziert, um gefährdete Personen in beruflichen Kohorten zu definieren. Ein Profil von phänotypischen Biomarkern und ihrer Beziehung zu Blasenkrebs ist in Abbildung 3 dargestellt, die veranschaulicht, dass G-Aktin, ein Vorläuferprotein des Zytoskelettproteins F-Aktin, ein früher Differenzierungsmarker ist, dem sequenzielle Veränderungen anderer Zwischenprodukte folgen können Endpunktmarker wie M344, DD23 und DNA-Ploidie. Die stärksten Biomarker-Panels zum Nachweis von prämalignen Erkrankungen und manifestem Krebs sowie zur Prognose müssen noch bestimmt werden. Da maschinensensible biochemische Kriterien definiert sind, kann es möglich sein, das Krankheitsrisiko an vorgeschriebenen Punkten im Krankheitskontinuum zu erkennen.
Abbildung 3. Vier Biomarker, G-Aktin, P-300, DD23 und DNA, in Bezug auf die Tumorprogression und das Ansprechen auf chirurgische Behandlung und Chemoprävention.
Diagnose und Behandlung arbeitsbedingter Nieren- und Harnwegserkrankungen
Vorbestehende Nierenerkrankung
Veränderungen in den Gesundheitsversorgungssystemen weltweit rücken Fragen der Versicherbarkeit und des Schutzes der Arbeitnehmer vor zusätzlicher Exposition in den Fokus. Eine signifikante vorbestehende Nierenerkrankung äußert sich in erhöhtem Serumkreatinin, Glucosurie (Zucker im Urin), Proteinurie, Hämaturie und verdünntem Urin. Der sofortige Ausschluss systemischer Ursachen wie Diabetes und Bluthochdruck ist erforderlich, und je nach Alter des Patienten sollten andere angeborene Ätiologien wie multiple Zysten in der Niere untersucht werden. Daher ist die Urinanalyse, sowohl mit Teststreifen als auch mit mikroskopischen Auswertungen, zum Nachweis von biochemischen und zellulären Veränderungen für den Arbeitsmediziner nützlich. Tests des Serumkreatinins und der Kreatinin-Clearance sind indiziert, wenn eine signifikante Hämaturie, Pyurie oder Proteinurie auf eine zugrunde liegende Pathologie hindeutet.
Mehrere Faktoren sind wichtig, um das Risiko für das Fortschreiten einer chronischen Erkrankung oder eines akuten Nierenversagens einzuschätzen. Die erste ist eine angeborene oder erworbene Einschränkung der Niere, um einer xenobiotischen Exposition zu widerstehen. Die Reaktion der Niere auf das Nephrotoxin, wie etwa eine Zunahme der absorbierten Giftstoffmenge oder Veränderungen im Nierenstoffwechsel, kann durch eine bereits bestehende Erkrankung beeinflusst werden. Von besonderer Bedeutung ist eine Abnahme der Entgiftungsfunktion bei sehr jungen oder sehr alten Menschen. In einer Studie korrelierte die Anfälligkeit für eine berufliche Exposition stark mit der familiären Vorgeschichte von Nierenerkrankungen, was auf die Bedeutung der erblichen Veranlagung hinweist. Grunderkrankungen wie Diabetes und Bluthochdruck erhöhen die Anfälligkeit. Seltene Erkrankungen wie Lupus erythematodes und Vaskulitis können zusätzliche Anfälligkeitsfaktoren sein. In den meisten Fällen ist eine erhöhte Anfälligkeit multifaktoriell und beinhaltet häufig eine Reihe von Beleidigungen, die entweder einzeln oder gleichzeitig auftreten. Daher sollte der Betriebsarzt die familiäre Vorgeschichte des Patienten mit Nierenerkrankungen und vorbestehenden Erkrankungen, die die Nierenfunktion beeinträchtigen, sowie alle Gefäß- oder Herzerkrankungen, insbesondere bei älteren Arbeitnehmern, kennen.
Akutes Nierenversagen
Akute Niereninsuffizienz kann prärenale, renale oder postrenale Ursachen haben. Die Erkrankung wird in der Regel durch einen akuten Infarkt verursacht, der zu einem schnellen, fortschreitenden Verlust der Nierenfunktion führt. Wenn das nephrotoxische Mittel oder der auslösende ursächliche Faktor entfernt wird, kommt es zu einer fortschreitenden Wiederherstellung der Nierenfunktion mit einer allmählichen Abnahme des Serum-Kreatinins und einer verbesserten Konzentrationsfähigkeit der Nieren. Tabelle 5 enthält eine Auflistung beruflicher Ursachen für akutes Nierenversagen. Akute Niereninsuffizienz durch hochdosierte Xenobiotika-Exposition war hilfreich, um potenzielle ätiologische Ursachen aufzuzeigen, die auch zu chronischeren Formen fortschreitender Nierenerkrankung beitragen können. Akute Niereninsuffizienz aufgrund einer Obstruktion des Ausflusstrakts durch gutartige oder bösartige Erkrankungen ist relativ selten, aber chirurgische Ursachen können häufiger dazu beitragen. Der Ultraschall des oberen Trakts beschreibt das Problem der Obstruktion, unabhängig vom beitragenden Faktor. Nierenversagen im Zusammenhang mit Drogen- oder Berufsgiften führt zu einer Sterblichkeitsrate von etwa 37 %; der Rest der betroffenen Personen verbessert sich in unterschiedlichem Maße.
Tabelle 5. Hauptursachen der akuten Niereninsuffizienz berufsbedingter Ursache
| Renale Ischämie | Tubuläre Nekrose | Hämoglobinurie, Myoglobinurie |
| Traumatischer Schock Anaphylaktischer Schock Akute Kohlenmonoxidvergiftung Hitzschlag |
Merkur Chrom Arsen Oxalsäure Tartrate Ethylenglykol Tetrachlorkohlenstoff Tetrachlorethan |
Arsin Crush-Syndrom Von einem Blitz getroffen |
Quelle: Crepet 1983.
Akute Niereninsuffizienz kann einer Vielzahl prärenaler Ursachen zugeschrieben werden, denen eine renale Ischämie zugrunde liegt, die aus einer verlängerten verminderten Nierendurchblutung resultiert. Herzinsuffizienz und Nierenarterienobstruktion sind zwei Beispiele. Tubuläre Nekrosen können durch eine ständig wachsende Zahl von Nephrotoxinen verursacht werden, die am Arbeitsplatz vorhanden sind. Herbizide und Pestizide wurden alle in eine Reihe von Studien verwickelt. In einem kürzlich erschienenen Bericht führte eine Hemlock-Vergiftung zur Ablagerung von Myosin und Aktin aus dem Abbau von Muskelzellen in den Tubuli und zu einer akuten Abnahme der Nierenfunktion. Endosulfan, ein Insektizid, und Triphenylzinnacetat (TPTA), ein Organozinn, wurden beide ursprünglich als Neurotoxine klassifiziert, aber kürzlich wurde berichtet, dass sie mit tubulärer Nekrose in Verbindung gebracht werden. Anekdotische Berichte über weitere Fälle relativieren die Notwendigkeit, Biomarker zu finden, um subklinischere Giftstoffe zu identifizieren, die möglicherweise noch nicht zu hochdosierten toxischen Expositionen geführt haben.
Anzeichen und Symptome eines akuten Nierenversagens sind: keine Urinausscheidung (Anurie); Oligurie (verringerte Urinausscheidung); verminderte Konzentrationsfähigkeit der Nieren; und/oder ein Anstieg des Serumkaliums, der das Herz in einem entspannten Zustand stoppen kann (diastolischer Stillstand). Die Behandlung beinhaltet klinische Unterstützung und, wann immer möglich, die Entfernung von der Exposition gegenüber dem Giftstoff. Ansteigendes Serumkalium oder übermäßige Flüssigkeitsretention sind die beiden Hauptindikatoren für entweder Hämodialyse oder Peritonealdialyse, wobei die Wahl von der kardiovaskulären Stabilität des Patienten und dem Gefäßzugang für die Hämodialyse abhängt. Der Nephrologe, ein medizinischer Nierenspezialist, ist der Schlüssel in der Behandlungsstrategie für diese Patienten, die möglicherweise auch die Behandlung durch einen urologischen chirurgischen Spezialisten benötigen.
Die langfristige Behandlung von Patienten nach Nierenversagen hängt weitgehend vom Grad der Genesung und Rehabilitation sowie vom allgemeinen Gesundheitszustand des Patienten ab. Eine Rückkehr zu eingeschränkter Arbeit und die Vermeidung von Bedingungen, die die zugrunde liegende Erkrankung belasten, sind wünschenswert. Patienten mit persistierender Hämaturie oder Pyurie benötigen eine sorgfältige Überwachung, möglicherweise mit Biomarkern, für 2 Jahre nach der Genesung.
Chronische Nierenerkrankung
Eine chronische oder terminale Nierenerkrankung ist am häufigsten das Ergebnis eines chronischen, fortlaufenden subklinischen Prozesses, der eine Vielzahl von Faktoren umfasst, von denen die meisten kaum verstanden werden. Glomerulonephritis, kardiovaskuläre Ursachen und Bluthochdruck sind wichtige Faktoren, die dazu beitragen. Weitere Faktoren sind Diabetes und Nephrotoxika. Die Patienten stellen sich mit progressiven Erhöhungen des Harnstoffstickstoffs im Serum, Kreatinin, Serumkalium und Oligurie (verringerte Urinausscheidung) vor. Verbesserte Biomarker oder Biomarker-Panels werden benötigt, um die subklinische Nephrotoxizität genauer zu identifizieren. Für den Berufspraktiker müssen die Bewertungsmethoden nicht-invasiv, hochspezifisch und reproduzierbar sein. Bisher hat kein einzelner Biomarker diese Kriterien erfüllt, um im großen klinischen Maßstab praktikabel zu werden.
Eine chronische Nierenerkrankung kann aus einer Vielzahl von Nephrotoxika resultieren, deren Pathogenese bei einigen besser verstanden ist als bei anderen. Eine Liste von Nephrotoxinen und Toxizitätsstellen ist in Tabelle 6 gezeigt. Wie erwähnt, können Toxine auf den Glomerulus, Segmente der Tubuli oder die interstitiellen Zellen abzielen. Zu den Symptomen einer Fremdstoffexposition können Hämaturie, Pyurie, Glukosurie, Aminosäuren im Urin, häufiges Wasserlassen und verminderte Urinausscheidung gehören. Die genauen Mechanismen der Nierenschädigung für viele Nephrotoxika wurden nicht definiert, aber die Identifizierung spezifischer Biomarker für Nephrotoxizität sollte dabei helfen, dieses Problem anzugehen. Obwohl ein gewisser Schutz der Niere durch die Verhinderung einer Vasokonstriktion geboten wird, bleibt die tubuläre Verletzung in den meisten Fällen bestehen. Beispielsweise ist die Bleitoxizität hauptsächlich vaskulären Ursprungs, während Chrom in niedrigen Dosen die proximalen Tubuluszellen beeinflusst. Diese Verbindungen scheinen die Stoffwechselmaschinerie der Zelle zu beeinflussen. Mehrere Formen von Quecksilber wurden mit akuter elementarer Nephrotoxizität in Verbindung gebracht. Cadmium greift im Gegensatz zu Quecksilber und wie viele andere beruflich bedingte Nephrotoxika zunächst die proximalen Tubuluszellen an.
Tabelle 6. Segmente des Nephrons, die von ausgewählten Giftstoffen betroffen sind
|
Proximalen Tubulus Antibiotika -Cephalosporine Aminoglykoside Antineoplastika -Nitrosoharnstoffe -Cisplatin und Analoga Röntgenkontrastmittel Halogenierte Kohlenwasserstoffe -Chlortrifluorethylen -Hexafluorpropen -Hexachlorbutadien -Trichlorethylen -Chloroform -Tetrachlorkohlenstoff Maleinsäure Citrinin Metallindustrie -Quecksilber -Uranylnitrat -Cadmium -Chrom |
Glomerulus Immunkomplexe Aminoglykosid-Antibiotika Puromycin-Aminonukleosid Adriamycin Penicillamin Distaler Tubulus/Sammelkanal -Lithium -Tetracycline -Amphotericin -Fluorid -Methoxyfluran
Brei -Aspirin -Phenacetin -Paracetamol -Nichtsteroidale entzündungshemmende Mittel -2-Bromethylamin |
Quelle: Tarloff und Goldstein 1994.
Mehr...
Nieren-Harnkrebs
Nierenkrebs
Epidemiologie
Historisch wurde Nierenkrebs verwendet, um entweder alle bösartigen Erkrankungen des Nierensystems (Nierenzellkarzinom (RCC), ICD-9 189.0; Nierenbecken, ICD-9 189.1; und Harnleiter, ICD-9 189.2) oder nur RCC zu bezeichnen. Diese Kategorisierung hat zu einiger Verwirrung in epidemiologischen Studien geführt, was dazu führte, dass zuvor gemeldete Daten überprüft werden mussten. RCC machen 75 bis 80 % der Gesamtzahl aus, wobei der Rest hauptsächlich Übergangszellkarzinome des Nierenbeckens und des Harnleiters sind. Die Trennung dieser beiden Krebsarten ist angemessen, da die Pathogenese des RCC und des Übergangszellkarzinoms sehr unterschiedlich ist und die epidemiologischen Risikofaktoren sowie die Anzeichen und Symptome der beiden Erkrankungen unterschiedlich sind. Dieser Abschnitt konzentriert sich auf RCC.
Der wichtigste identifizierte Risikofaktor für Nierenkrebs ist das Tabakrauchen, gefolgt von vermuteten, aber schlecht definierten beruflichen und umweltbedingten Risikofaktoren. Es wird geschätzt, dass die Abschaffung des Tabakrauchens die Inzidenz von Nierenkrebs in den Industrieländern um 30 bis 40 % verringern würde, aber berufliche Determinanten von RCC sind nicht gut etabliert. Das der Bevölkerung zuzurechnende Risiko aufgrund beruflicher Exposition wurde auf der Grundlage einer anerkannten Karzinogenese auf null und 21 % auf der Grundlage einer multizentrischen Fall-Kontroll-Studie an mehreren Standorten in der kanadischen Region Montreal geschätzt. Frühe Wirkungs-Biomarker in Verbindung mit Expositions-Biomarkern sollten bei der Klärung wichtiger Risikofaktoren helfen. In epidemiologischen Studien wurde festgestellt, dass mehrere Berufe und Branchen ein erhöhtes Nierenkrebsrisiko mit sich bringen. Mit der möglichen Ausnahme von Mitteln, die bei der chemischen Reinigung und Expositionen bei der Erdölraffination verwendet werden, sind die verfügbaren Beweise jedoch nicht konsistent. Die statistische Analyse epidemiologischer Expositionsdaten in Bezug auf Biomarker für Empfindlichkeit und Wirkung wird weitere ätiologische Ursachen klären.
Mehrere epidemiologische Studien haben bestimmte Branchen, Berufe und berufliche Expositionen mit einem erhöhten Nierenzellkarzinomrisiko in Verbindung gebracht. Das Muster, das sich aus diesen Studien ergibt, ist nicht vollständig konsistent. Ölraffination, Drucken, chemische Reinigung und Lkw-Fahren sind Beispiele für Berufe, die mit einem erhöhten Nierenkrebsrisiko verbunden sind. Landwirte weisen normalerweise ein verringertes RCC-Risiko auf, aber eine dänische Studie verband eine langfristige Exposition gegenüber Insektiziden und Herbiziden mit einem fast vierfach erhöhten RCC-Risiko. Dieser Befund erfordert eine Bestätigung durch unabhängige Daten, einschließlich der Angabe der möglichen kausalen Natur des Zusammenhangs. Andere Produkte, die im Verdacht stehen, mit RCC in Verbindung gebracht zu werden, umfassen: verschiedene Kohlenwasserstoffderivate und Lösungsmittel; Produkte der Ölraffination; Erdöl-, Teer- und Pechprodukte; Benzinauspuff; Kerosin; Emissionen von Düsen- und Dieselmotoren; Arsenverbindungen; Cadmium; Chrom(VI)-Verbindungen; anorganische Bleiverbindungen; und Asbest. Epidemiologische Studien haben die berufsbedingte Exposition gegenüber Benzindämpfen mit dem Risiko von Nierenkrebs in Verbindung gebracht, einige in einer Dosis-Wirkungs-Weise, ein Phänomen, das bei männlichen Ratten bei Exposition gegenüber bleifreien Benzindämpfen beobachtet wurde. Angesichts der weit verbreiteten Exposition von Menschen gegenüber Benzindämpfen in Einzelhandelstankstellen und der jüngsten Zunahme der Nierenkrebsinzidenz gewinnen diese Ergebnisse möglicherweise an Gewicht. Benzin ist ein komplexes Gemisch aus Kohlenwasserstoffen und Zusatzstoffen, einschließlich Benzol, das für den Menschen bekanntermaßen krebserregend ist.
Das Risiko für Nierenkrebs ist nicht konsequent mit der sozialen Klasse verbunden, obwohl ein erhöhtes Risiko gelegentlich mit einem höheren sozioökonomischen Status in Verbindung gebracht wurde. Bei einigen Populationen wurde jedoch ein umgekehrter Gradient beobachtet, und bei wieder anderen trat kein klares Muster auf. Möglicherweise hängen diese Schwankungen mit dem Lebensstil zusammen. Studien mit Migranten zeigen eine Veränderung des RCC-Risikos in Richtung der Bevölkerung des Aufnahmelandes, was darauf hindeutet, dass Umweltfaktoren bei der Entwicklung dieser Malignität wichtig sind.
Mit Ausnahme des Nephroblastoms (Wilms-Tumor), einer Krebsart im Kindesalter, tritt Nierenkrebs normalerweise nach dem 40. Lebensjahr auf. Schätzungsweise 127,000 neue Fälle von Nierenkrebs (einschließlich RCC und Übergangszellkarzinom (TCC) des Nierenbeckens und des Harnleiters), was 1.7 % der weltweiten Gesamtkrebsinzidenz entspricht, traten 1985 weltweit auf. Die Inzidenz von Nierenkrebs variiert je nach Population . Hohe Raten wurden sowohl für Männer als auch für Frauen in Nordamerika, Europa, Australien und Neuseeland gemeldet; niedrige Raten in Melanesien, Mittel- und Ostafrika sowie Südost- und Ostasien. Die Inzidenz von Nierenkrebs steigt in den meisten westlichen Ländern, stagniert jedoch in einigen wenigen. Die altersstandardisierte Inzidenz von Nierenkrebs war 1985 in Nordamerika und West-, Nord- und Osteuropa am höchsten und in Afrika, Asien (außer bei japanischen Männern) und im Pazifik am niedrigsten. Nierenkrebs ist bei Männern häufiger als bei Frauen und gehört in einer Reihe von Ländern zu den zehn häufigsten Krebsarten.
Das Übergangszellkarzinom (TCC) des Nierenbeckens ist mit ähnlichen Krankheitserregern wie Blasenkrebs assoziiert, darunter chronische Infektionen, Steine und Phenacetin-haltige Analgetika. Die Balkan-Nephropathie, eine langsam fortschreitende, chronische und tödliche Nephropathie, die in den Balkanländern weit verbreitet ist, ist mit einer hohen Rate an Tumoren des Nierenbeckens und der Harnleiter verbunden. Die Ursachen der Balkan-Nephropathie sind unbekannt. Eine übermäßige Exposition gegenüber Ochratoxin A, das als möglicherweise krebserregend für den Menschen gilt, wurde mit der Entwicklung einer Balkan-Nephropathie in Verbindung gebracht, aber die Rolle anderer nephrotoxischer Wirkstoffe kann nicht ausgeschlossen werden. Ochratoxin A ist ein von Pilzen produziertes Toxin, das in vielen Lebensmitteln vorkommt, insbesondere in Getreide und Schweinefleischprodukten.
Screening und Diagnose von Nierenkrebs
Das Zeichen- und Symptommuster von RCC variiert von Patient zu Patient, sogar bis zu dem Stadium, in dem Metastasen auftreten. Aufgrund der Lage der Nieren und der Mobilität benachbarter Organe zur expandierenden Masse sind diese Tumoren zum Zeitpunkt der klinischen Entdeckung häufig sehr groß. Obwohl Hämaturie das primäre Symptom von RCC ist, treten Blutungen aufgrund der intrarenalen Lokalisation von RCC im Vergleich zu Übergangszelltumoren spät auf. RCC wurde aufgrund der interessanten Konstellation von Symptomen im Zusammenhang mit paraneoplastischen Syndromen als der „Traum des Arztes“, aber auch als der „Fluch des Chirurgen“ angesehen. Es wurde über Substanzen berichtet, die die Anzahl der roten Blutkörperchen, Kalzium und Faktoren, die eine abnormale Nebennierenfunktion nachahmen, erhöhen, und es wurden Bauchmasse, Gewichtsverlust, Müdigkeit, Schmerzen, Anämie, abnormale Leberfunktion und Bluthochdruck beobachtet. Computerisierte Axialtomographie (CAT-Scan) des Abdomens und Ultraschall werden von Ärzten immer häufiger angeordnet, so dass schätzungsweise 20 % der RCCs zufällig als Ergebnis der Untersuchung anderer medizinischer Probleme diagnostiziert werden.
Die klinische Bewertung eines RCC-Falls besteht aus einer körperlichen Untersuchung, um eine Flankenmasse zu identifizieren, die bei 10 % der Patienten auftritt. Eine Nierenröntgenaufnahme mit Kontrastmittel kann eine Nierenmasse abgrenzen, und die solide oder zystische Natur wird normalerweise durch Ultraschall oder CT-Scan geklärt. Die Tumoren sind stark vaskulär und haben ein charakteristisches Aussehen, wenn die Arterie mit röntgendichtem Kontrastmaterial injiziert wird. Eine Arteriographie wird durchgeführt, um den Tumor zu embolisieren, wenn er sehr groß ist, oder um die arterielle Blutversorgung zu definieren, wenn eine partielle Nephrektomie erwartet wird. Feinnadelaspiration kann verwendet werden, um verdächtiges RCC zu entnehmen.
Lokalisierte RCC-Tumoren werden chirurgisch mit regionalen Lymphknoten entfernt, und operativ ist eine frühzeitige Ligatur der Arterie und Vene wichtig. Symptomatisch kann der Patient gebessert werden, indem große oder blutende Tumore entfernt werden, die Metastasen gebildet haben, aber dies verbessert nicht das Überleben. Bei metastasierenden Tumoren kann eine lokalisierte Schmerzkontrolle mit einer Strahlentherapie erreicht werden, aber die Behandlung der Wahl für metastasierende Erkrankungen sind biologische Reaktionsmodifikatoren (Interleukin-2 oder α-Interferon), obwohl Chemotherapie gelegentlich allein oder in Kombination mit anderen Therapien verwendet wird.
Marker wie das Krebsgen auf Chromosom 3, das in Krebsfamilien und bei der von Hippel-Lindau-Krankheit beobachtet wird, können als Biomarker für die Anfälligkeit dienen. Obwohl Tumormarker-Antigene für RCC berichtet wurden, gibt es derzeit keine Möglichkeit, diese zuverlässig mit ausreichender Sensitivität und Spezifität im Urin oder Blut nachzuweisen. Die geringe Prävalenz dieser Krankheit in der Allgemeinbevölkerung erfordert einen Test mit hoher Spezifität und Sensitivität zur Früherkennung der Krankheit. Risikogruppen im Berufsleben könnten möglicherweise mit Ultraschall gescreent werden. Die Bewertung dieses Tumors bleibt eine Herausforderung für Grundlagenwissenschaftler, Molekularepidemiologen und Kliniker gleichermaßen.
Blasenkrebs
Epidemiologie
Mehr als 90 % der Blasenkrebserkrankungen in Europa und Nordamerika sind Übergangszellkarzinome (TCC). Plattenepithelkarzinome und Adenokarzinome machen in diesen Regionen 5 bzw. 1 % des Blasenkrebses aus. Die Verteilung der histopathologischen Typen bei Blasenkrebs unterscheidet sich deutlich in Regionen wie dem Nahen Osten und Afrika, wo Blasenkrebs mit einer schistosomalen Infektion assoziiert ist. Beispielsweise ist in Ägypten, wo Bilharziose endemisch und Blasenkrebs das größte onkogene Problem ist, das Plattenepithelkarzinom der häufigste Typ, aber die Inzidenz von TCC nimmt mit der steigenden Prävalenz des Zigarettenrauchens zu. Die folgende Diskussion konzentriert sich auf TCC.
Blasenkrebs ist nach wie vor eine Krankheit von erheblicher Bedeutung. Er machte 3.5 etwa 1980 % aller bösartigen Erkrankungen weltweit aus. 1985 wurde Blasenkrebs weltweit an 11. Stelle der Häufigkeit geschätzt und war mit einer erwarteten Gesamtzahl von 243,000 Neuerkrankungen die achthäufigste Krebsart bei Männern. In der siebten Lebensdekade ist die Inzidenz am höchsten, und weltweit liegt das Verhältnis von Männern zu Frauen bei etwa drei zu eins. Die Inzidenz hat in fast allen Bevölkerungsgruppen in Europa zugenommen, insbesondere bei Männern. In Dänemark, wo die jährlichen Inzidenzraten mit 45 pro 100,000 bei Männern und 12 pro 100,000 bei Frauen zu den höchsten der Welt gehören, ist der jüngste Trend ein weiterer Anstieg von 8 bis 9 % alle 5 Jahre. In Asien sind die sehr hohen Raten unter den Chinesen in Hongkong stetig zurückgegangen, aber bei beiden Geschlechtern ist die Inzidenz von Blasenkrebs immer noch viel höher als anderswo in Asien und mehr als doppelt so hoch wie bei den Chinesen in Shanghai oder Singapur. Die Blasenkrebsraten unter den Chinesen auf Hawaii sind ebenfalls hoch.
Zigarettenrauchen ist der wichtigste ätiologische Faktor bei Blasenkrebs, an zweiter Stelle stehen berufliche Expositionen. Es wurde geschätzt, dass Tabak für ein Drittel aller Fälle von Blasenkrebs außerhalb von Regionen verantwortlich ist, in denen schistosomale Infektionen vorherrschen. Die Zahl der Blasenkrebsfälle, die 1985 dem Tabakrauchen zugeschrieben wurden, wurde weltweit auf mehr als 75,000 geschätzt und kann 50 % der Blasenkrebsfälle in der westlichen Bevölkerung ausmachen. Die Tatsache, dass nicht alle Personen, die ähnlich viel rauchen, Blasenkrebs mit der gleichen Rate entwickeln, deutet darauf hin, dass genetische Faktoren bei der Kontrolle der Anfälligkeit wichtig sind. Zwei aromatische Amine, 4-Aminobiphenyl und 2-Naphthylamin, sind Karzinogene, die mit dem Zigarettenrauchen in Verbindung gebracht werden; diese sind in „schwarzem Tabak“ (air-cured) in höheren Konzentrationen zu finden als in „Blend-Tabak“ (flue-cured). Passivrauchen erhöht die Addukte im Blut, und eine Dosis-Wirkungs-Beziehung der Adduktbildung wurde mit einem erhöhten Risiko für Blasenkrebs korreliert. Bei Zigarettenrauchern, die langsame Acetylierer sind, wurde im Vergleich zu schnellen Acetylierern ein höheres Maß an Adduktbildung beobachtet, was darauf hindeutet, dass der genetisch vererbte Acetylierungsstatus ein wichtiger Biomarker für die Anfälligkeit sein kann. Die geringere Inzidenz von Blasenkrebs bei schwarzen im Vergleich zu weißen Rassen kann der Konjugation von karzinogenen Stoffwechselzwischenprodukten durch Sulfotransferasen zugeschrieben werden, die Elektrophile produzieren. Entgiftete Phenolsulfate können das Urothel schützen. Es wurde berichtet, dass die Leber-Sulfotransferase-Aktivität für N-Hydroxyarylamine bei Schwarzen höher ist als bei Weißen. Dies kann zu einer Verringerung der Menge an freien N-Hydroxymetaboliten führen, die als Karzinogene wirken.
Berufsbedingter Blasenkrebs ist eine der frühesten bekannten und am besten dokumentierten berufsbedingten Krebserkrankungen. Der erste identifizierte Fall von berufsbedingtem Blasenkrebs trat etwa 20 Jahre nach den Anfängen der synthetischen Farbstoffindustrie in Deutschland auf. Zahlreiche weitere Berufe wurden in den letzten 25 Jahren als berufsbedingtes Blasenkrebsrisiko identifiziert. Berufsbedingte Expositionen können zu bis zu 20 % der Blasenkrebsfälle beitragen. Zu den beruflich exponierten Arbeitern gehören Arbeiter, die mit Kohleteerpechen, der Kohlevergasung und der Herstellung von Gummi, Aluminium, Auramin und Magenta arbeiten, sowie Friseure und Friseure. Es wurde gezeigt, dass aromatische Amine bei Arbeitern in vielen Ländern Blasenkrebs verursachen. Bemerkenswert unter dieser Klasse von Chemikalien sind 2-Naphthylamin, Benzidin, 4-Nitrobiphenyl und 3,3r´-Dichlorbenzidin. Zwei weitere aromatische Amine, 4,4´-Methylendianilin (MDA) und 4,4´-Methylen-bis-2-Chloranilin (MOCA), gehören zu den am häufigsten verwendeten der mutmaßlichen Blasenkarzinogene. Andere Karzinogene im Zusammenhang mit industrieller Exposition sind weitgehend unbestimmt; Am Arbeitsplatz sind jedoch häufig aromatische Amine vorhanden.
Screening und Diagnose von Blasenkrebs
Das Screening auf Blasenkrebs erhält weiterhin Aufmerksamkeit bei dem Bestreben, Blasenkrebs zu diagnostizieren, bevor er symptomatisch wird und vermutlich einer kurativen Behandlung weniger zugänglich ist. Entleerungsurin-Zytologie und Urinanalyse für Hämaturie wurden als Kandidaten für Screening-Tests angesehen. Eine zentrale Frage für das Screening ist, wie Risikogruppen und dann Personen innerhalb dieser Gruppen identifiziert werden können. Epidemiologische Studien identifizieren Risikogruppen, während Biomarker möglicherweise Personen innerhalb von Gruppen identifizieren. Im Allgemeinen war das berufliche Screening auf Blasenkrebs mit Hämaturie-Tests und Papanicolaou-Zytologie unwirksam.
Eine verbesserte Erkennung von Blasenkrebs kann mit dem von Messing und Mitarbeitern beschriebenen 14-tägigen Hämastick-Test möglich sein. Ein positiver Test wurde mindestens einmal bei 84 % von 31 Patienten mit Blasenkrebs mindestens 2 Monate vor der zystoskopischen Diagnose der Krankheit beobachtet. Dieser Test leidet unter einer falsch-positiven Rate von 16 bis 20 %, wobei die Hälfte dieser Patienten keine urologische Erkrankung hat. Die niedrigen Kosten können dies zu einem nützlichen Test in einem zweistufigen Screening in Kombination mit Biomarkern und Zytologie machen (Waples und Messing 1992).
In einer kürzlich durchgeführten Studie wies der monoklonale Antikörper DD23 mithilfe einer quantitativen Fluoreszenzbildanalyse Blasenkrebs in exfolierten Uroepithelzellen nach. Eine Sensitivität von 85 % und eine Spezifität von 95 % wurden in einer Mischung aus niedrig- und hochgradigen Übergangszellkarzinomen einschließlich TaT1-Tumoren erreicht. Das M344-Tumor-assoziierte Antigen in Verbindung mit DNA-Ploidie hatte eine Sensitivität von annähernd 90 %.
Jüngste Studien deuten darauf hin, dass die Kombination von Biomarkern und Hämaturie-Tests möglicherweise der beste Ansatz ist. Eine Liste der Anwendungen der quantitativen Fluoreszenz-Urinzytologie in Kombination mit Biomarkern ist in Tabelle 1 zusammengefasst. Genetische, biochemische und morphologische frühe Zellveränderungen im Zusammenhang mit prämalignen Erkrankungen stützen das Konzept, dass Risikopersonen Jahre vor der Entwicklung einer manifesten Erkrankung identifiziert werden können Malignität. Empfindlichkeits-Biomarker in Kombination mit Wirkungs-Biomarkern versprechen eine noch genauere Erkennung von Risikopersonen. Diese Fortschritte werden durch neue Technologien ermöglicht, die in der Lage sind, phänotypische und genotypische molekulare Veränderungen auf Einzelzellebene zu quantifizieren und so gefährdete Personen zu identifizieren. Die individuelle Risikobewertung ermöglicht eine stratifizierte, kostengünstige Überwachung ausgewählter Gruppen für eine gezielte Chemoprävention.
Tabelle 1. Anwendungen der Urinzytologie
Erkennung von CIS1 und Blasenkrebs
Überwachung der chirurgischen Therapie:
Überwachung der Blase nach TURBT2
Überwachung der oberen Harnwege
Überwachung des Harnröhrenrests
Überwachung der Harnableitung
Überwachung der intravesikalen Therapie
Auswahl der intravesikalen Therapie
Überwachung der Wirkung der Lasertherapie
Bewertung von Patienten mit Hämaturie
Feststellung der Notwendigkeit einer Zystoskopie
Screening von Hochrisikopopulationen:
Berufliche Expositionsgruppen
Drogenabhängige Gruppen mit Risiko für Blasenkrebs
Entscheidungskriterien für:
Zystektomie
Segmentale Ureterresektion versus Nephroureterektomie
Andere Indikationen:
Nachweis einer vesikoenterischen Fistel
Extraurologische Tumoren, die in die Harnwege eindringen
Definition wirksamer chemopräventiver Mittel
Überwachung einer wirksamen Chemotherapie
1 CIS, Karzinom in situ.
2 TURBT, transurethrale Resektion bei Blasentumor.
Quelle: Hemstreet et al. 1996.
Anzeichen und Symptome von Blasenkrebs ähneln denen einer Harnwegsinfektion und können Schmerzen beim Wasserlassen, häufiges Wasserlassen und Blut und Eiterzellen im Urin umfassen. Da die Symptome einer Harnwegsinfektion einen Blasentumor ankündigen können, insbesondere wenn sie bei älteren Patienten mit einer Makrohämaturie einhergehen, ist eine Bestätigung des Vorhandenseins von Bakterien und eine hohe Aufmerksamkeit des untersuchenden Arztes erforderlich. Jeder Patient, der wegen einer Harnwegsinfektion behandelt wird, die nicht sofort abklingt, sollte zur weiteren Abklärung an einen Facharzt für Urologie überwiesen werden.
Die diagnostische Abklärung von Blasenkrebs erfordert zunächst ein intravenöses Pyelogramm (IVP), um eine Erkrankung der oberen Harnwege im Nierenbecken oder in den Harnleitern auszuschließen. Zur Bestätigung von Blasenkrebs muss die Blase mit einem Licht (Zystoskop) untersucht werden, wobei mehrere Biopsien mit einem beleuchteten Instrument durch die Harnröhre durchgeführt werden, um festzustellen, ob der Tumor nicht invasiv (dh papillär oder CIS) oder invasiv ist. Zufällige Biopsien der Blase und der prostatischen Harnröhre helfen, Feldkanzerisierung und Feldeffektänderungen zu definieren. Patienten mit nicht-invasiver Erkrankung müssen engmaschig überwacht werden, da sie einem Risiko für spätere Rezidive unterliegen, obwohl eine Progression des Stadiums und des Grades ungewöhnlich ist. Patienten mit bereits hochgradigem oder in die Lamina propria invasiv auftretendem Blasenkrebs haben ein gleich hohes Rezidivrisiko, eine Progression des Stadiums ist jedoch viel wahrscheinlicher. Daher erhalten sie nach transurethraler Resektion in der Regel eine intravesikale Instillation von Immun- oder Chemotherapeutika. Patienten mit Tumoren, die in die Muscularis propria oder darüber hinaus eindringen, haben mit viel größerer Wahrscheinlichkeit bereits Metastasen und können selten konservativ behandelt werden. Aber selbst bei Behandlung durch totale Zystektomie (die Standardtherapie für muskelinvasiven Blasenkrebs) erliegen 20 bis 60 % schließlich ihrer Krankheit, fast immer aufgrund von Metastasen. Wenn zum Zeitpunkt der Diagnose regionale oder distale Metastasen vorhanden sind, sinken die 5-Jahres-Überlebensraten trotz aggressiver Behandlung auf 35 bzw. 9 %. Die systemische Chemotherapie bei metastasierendem Blasenkrebs verbessert sich mit vollständigen Ansprechraten von 30 %. Jüngste Studien deuten darauf hin, dass eine Chemotherapie vor einer Zystektomie das Überleben ausgewählter Patienten verbessern kann.
Das Blasenkrebs-Staging ist in 70 % der Fälle prädiktiv für das biologische Potenzial für Progression, Metastasierung oder Rezidiv. Das Staging von Blasenkrebs erfordert normalerweise einen CT-Scan, um Lebermetastasen auszuschließen, einen Radioisotopen-Knochenscan, um eine Ausbreitung auf den Knochen auszuschließen, und eine Röntgenaufnahme des Brustkorbs oder einen CAT-Scan, um Lungenmetastasen auszuschließen. Eine Suche nach Biomarkern im Tumor- und Blasenkrebsbereich wird fortgesetzt, die vorhersagen, welche Tumore metastasieren oder wieder auftreten werden. Die Zugänglichkeit von abgeblätterten Blasenzellen in entleerten Proben ist vielversprechend für die Verwendung von Biomarkern zur Überwachung des Wiederauftretens und zur Krebsprävention.
Fortpflanzungssystem: Einführung
Die männliche und weibliche Reproduktionstoxizität sind Themen von zunehmendem Interesse unter Berücksichtigung von Gesundheitsgefahren am Arbeitsplatz. Reproduktionstoxizität ist definiert als das Auftreten schädlicher Wirkungen auf das Fortpflanzungssystem, die aus der Exposition gegenüber Umwelteinflüssen resultieren können. Die Toxizität kann sich in Veränderungen der Fortpflanzungsorgane und/oder des zugehörigen endokrinen Systems äußern. Die Manifestationen einer solchen Toxizität können umfassen:
- Veränderungen im Sexualverhalten
- reduzierte Fruchtbarkeit
- ungünstige Schwangerschaftsergebnisse
- Modifikationen anderer Funktionen, die von der Integrität des Fortpflanzungssystems abhängen.
Mechanismen, die der Reproduktionstoxizität zugrunde liegen, sind komplex. Es wurden mehr xenobiotische Substanzen getestet und erwiesen sich als toxisch für den männlichen Fortpflanzungsprozess als für die weibliche. Es ist jedoch nicht bekannt, ob dies auf zugrunde liegende Unterschiede in der Toxizität oder auf die einfachere Untersuchung von Spermien als auf Eizellen zurückzuführen ist.
Entwicklungstoxizität
Entwicklungstoxizität ist definiert als das Auftreten von nachteiligen Wirkungen auf den sich entwickelnden Organismus, die aus einer Exposition vor der Empfängnis (beide Elternteile), während der pränatalen Entwicklung oder postnatal bis zum Zeitpunkt der Geschlechtsreife resultieren können. Nachteilige Auswirkungen auf die Entwicklung können zu jedem Zeitpunkt in der Lebensspanne des Organismus festgestellt werden. Zu den wichtigsten Manifestationen der Entwicklungstoxizität gehören:
- Tod des sich entwickelnden Organismus
- strukturelle Anomalie
- verändertes Wachstum
- funktioneller Mangel.
In der folgenden Diskussion, Entwicklungstoxizität wird als allumfassender Begriff verwendet, um sich auf Expositionen gegenüber der Mutter, dem Vater oder dem Empfängnis zu beziehen, die zu einer abnormalen Entwicklung führen. Der Begriff Teratogenese wird verwendet, um genauer auf Expositionen gegenüber dem Konzeptus hinzuweisen, die eine strukturelle Fehlbildung hervorrufen. Unsere Erörterung umfasst nicht die Auswirkungen postnataler Expositionen auf die Entwicklung.
Mutagenese
Zusätzlich zur Reproduktionstoxizität kann die Exposition gegenüber einem der Elternteile vor der Empfängnis zu Entwicklungsstörungen durch Mutagenese, Veränderungen im genetischen Material, das vom Elternteil an die Nachkommen weitergegeben wird, führen. Solche Veränderungen können entweder auf Ebene einzelner Gene oder auf chromosomaler Ebene auftreten. Veränderungen in einzelnen Genen können zur Übertragung veränderter genetischer Botschaften führen, während Veränderungen auf chromosomaler Ebene zur Übertragung von Anomalien in der Chromosomenzahl oder -struktur führen können.
Es ist interessant, dass einige der stärksten Beweise für eine Rolle von präkonzeptionellen Expositionen bei Entwicklungsstörungen aus Studien über väterliche Expositionen stammen. Beispielsweise wurde das Prader-Willi-Syndrom, ein Geburtsfehler, der durch Hypotonie in der Neugeborenenperiode und später durch ausgeprägte Fettleibigkeit und Verhaltensprobleme gekennzeichnet ist, mit einer beruflichen Exposition des Vaters gegenüber Kohlenwasserstoffen in Verbindung gebracht. Andere Studien haben Zusammenhänge zwischen väterlicher vorgefasster Exposition gegenüber physikalischen Wirkstoffen und angeborenen Fehlbildungen und Krebserkrankungen im Kindesalter gezeigt. Beispielsweise wurde die berufliche Exposition des Vaters gegenüber ionisierender Strahlung mit einem erhöhten Risiko für Neuralrohrdefekte und einem erhöhten Risiko für Leukämie im Kindesalter in Verbindung gebracht, und mehrere Studien haben einen Zusammenhang zwischen väterlicher Voreingenommenheit, beruflicher Exposition gegenüber elektromagnetischen Feldern und kindlichen Hirntumoren nahegelegt (Gold und Sever 1994 ). Bei der Bewertung sowohl der reproduktiven als auch der entwicklungsbedingten Gefährdung durch Exposition am Arbeitsplatz muss den möglichen Wirkungen bei Männern erhöhte Aufmerksamkeit geschenkt werden.
Es ist ziemlich wahrscheinlich, dass einige Defekte unbekannter Ätiologie eine genetische Komponente beinhalten, die mit der Exposition der Eltern zusammenhängen kann. Aufgrund der nachgewiesenen Zusammenhänge zwischen dem Alter des Vaters und Mutationsraten ist es logisch anzunehmen, dass andere väterliche Faktoren und Expositionen mit Genmutationen in Verbindung gebracht werden können. Der gut etablierte Zusammenhang zwischen dem mütterlichen Alter und chromosomaler Nichtdisjunktion, der zu Anomalien der Chromosomenzahl führt, legt nahe, dass mütterliche Expositionen bei chromosomalen Anomalien eine bedeutende Rolle spielen.
Mit zunehmendem Verständnis des menschlichen Genoms werden wir wahrscheinlich mehr Entwicklungsfehler auf mutagene Veränderungen in der DNA einzelner Gene oder strukturelle Veränderungen in Teilen von Chromosomen zurückführen können.
Teratogenese
Seit der Entdeckung der Teratogenität von Thalidomid im Jahr 1961 sind die nachteiligen Wirkungen der Exposition des Empfängnis gegenüber exogenen chemischen Stoffen auf die menschliche Entwicklung bekannt. Wilson (1973) hat sechs „allgemeine Prinzipien der Teratologie“ entwickelt, die für diese Diskussion relevant sind. Diese Prinzipien sind:
- Die letzten Manifestationen einer abnormalen Entwicklung sind Tod, Fehlbildung, Wachstumsverzögerung und funktionelle Störung.
- Die Empfindlichkeit des Empfängnispartners gegenüber teratogenen Stoffen variiert mit dem Entwicklungsstadium zum Zeitpunkt der Exposition.
- Teratogene Wirkstoffe wirken auf spezifische Weise (Mechanismen) auf sich entwickelnde Zellen und Gewebe, indem sie eine abnormale Embryogenese (Pathogenese) initiieren.
- Manifestationen einer anormalen Entwicklung nehmen mit zunehmender Dosierung vom Ausmaß ohne Wirkung bis zum völlig tödlichen Niveau zu.
- Der Zugang nachteiliger Umwelteinflüsse zu sich entwickelnden Geweben hängt von der Art des Mittels ab.
- Die Anfälligkeit für ein Teratogen hängt vom Genotyp des Empfängnis und von der Art und Weise ab, in der der Genotyp mit Umweltfaktoren interagiert.
Die ersten vier dieser Prinzipien werden ausführlicher erörtert, ebenso wie die Kombination der Prinzipien 1, 2 und 4 (Ergebnis, Expositionszeitpunkt und Dosis).
Spektrum der mit der Exposition verbundenen nachteiligen Folgen
Es gibt ein Spektrum von Nebenwirkungen, die möglicherweise mit der Exposition verbunden sind. Berufsbezogene Studien, die sich auf ein einzelnes Ergebnis konzentrieren, riskieren, andere wichtige Auswirkungen auf die Fortpflanzung zu übersehen.
Abbildung 1 listet einige Beispiele für Entwicklungsergebnisse auf, die möglicherweise mit der Exposition gegenüber berufsbedingten Teratogenen verbunden sind. Ergebnisse einiger Berufsstudien deuten darauf hin, dass angeborene Missbildungen und spontane Fehlgeburten mit denselben Expositionen verbunden sind – beispielsweise Anästhesiegasen und organischen Lösungsmitteln.
Spontane Abtreibung ist ein wichtiges Ergebnis, das berücksichtigt werden muss, da sie durch verschiedene pathogene Prozesse aus verschiedenen Mechanismen resultieren kann. Ein spontaner Abort kann das Ergebnis einer Embryo- oder Fötustoxizität, chromosomaler Veränderungen, einzelner Geneffekte oder morphologischer Anomalien sein. Es ist wichtig zu versuchen, bei Studien zu Spontanaborten zwischen karyotypisch normalen und abnormalen Konzepten zu unterscheiden.
Abbildung 1. Entwicklungsanomalien und Fortpflanzungsergebnisse, die möglicherweise mit beruflicher Exposition verbunden sind.
Zeitpunkt der Exposition
Wilsons zweites Prinzip bezieht die Anfälligkeit für abnormale Entwicklung auf den Zeitpunkt der Exposition, dh das Gestationsalter des Empfängnis. Dieses Prinzip ist für die Induktion struktureller Missbildungen gut etabliert, und die sensiblen Perioden für die Organogenese sind für viele Strukturen bekannt. In Anbetracht einer erweiterten Reihe von Ergebnissen muss die sensible Phase, während der eine Wirkung induziert werden kann, während der gesamten Schwangerschaft verlängert werden.
Bei der Bewertung der berufsbedingten Entwicklungstoxizität sollte die Exposition für die entsprechende kritische Periode – d. h. das/die Gestationsalter/e – für jeden Endpunkt bestimmt und klassifiziert werden. Beispielsweise stehen spontane Fehlgeburten und angeborene Missbildungen wahrscheinlich mit einer Exposition im ersten und zweiten Trimenon in Zusammenhang, während niedriges Geburtsgewicht und funktionelle Störungen wie Anfallsleiden und geistige Behinderung eher mit einer Exposition im zweiten und dritten Trimenon zusammenhängen.
Teratogene Mechanismen
Das dritte Prinzip ist die Wichtigkeit, die potenziellen Mechanismen zu berücksichtigen, die eine abnormale Embryogenese auslösen könnten. Es wurde eine Reihe unterschiedlicher Mechanismen vorgeschlagen, die zur Teratogenese führen könnten (Wilson 1977). Diese beinhalten:
- Mutationsänderungen in DNA-Sequenzen
- Chromosomenanomalien, die zu strukturellen oder quantitativen Veränderungen der DNA führen
- Veränderung oder Hemmung des intrazellulären Metabolismus, z. B. Stoffwechselblockaden und Fehlen von Coenzymen, Vorläufern oder Substraten für die Biosynthese
- Unterbrechung der DNA- oder RNA-Synthese
- Eingriff in die Mitose
- Störung der Zelldifferenzierung
- Versagen von Zell-zu-Zell-Interaktionen
- Scheitern von Zellwanderungen
- Zelltod durch direkte zytotoxische Wirkungen
- Auswirkungen auf die Zellmembranpermeabilität und osmolare Veränderungen
- physikalische Zerstörung von Zellen oder Geweben.
Durch die Berücksichtigung von Mechanismen können Forscher biologisch sinnvolle Gruppierungen von Ergebnissen entwickeln. Dies kann auch einen Einblick in potenzielle Teratogene geben; Beispielsweise werden seit einiger Zeit Zusammenhänge zwischen Karzinogenese, Mutagenese und Teratogenese diskutiert. Aus der Perspektive der Bewertung beruflicher Reproduktionsgefahren ist dies aus zwei verschiedenen Gründen von besonderer Bedeutung: (1) Stoffe, die krebserzeugend oder mutagen sind, haben eine erhöhte Wahrscheinlichkeit, teratogen zu sein, was darauf hindeutet, dass den Auswirkungen solcher Stoffe auf die Reproduktion besondere Aufmerksamkeit geschenkt werden sollte und (2) Wirkungen auf die Desoxyribonukleinsäure (DNA), die somatische Mutationen hervorruft, werden als Mechanismen sowohl für die Karzinogenese als auch für die Teratogenese angesehen.
Dosis und Ergebnis
Das vierte Prinzip der Teratogenese ist das Verhältnis von Outcome zu Dosis. Dieses Prinzip ist in vielen Tierversuchen klar belegt, und Selevan (1985) hat seine potenzielle Relevanz für die Situation beim Menschen diskutiert, wobei er die Bedeutung multipler Fortpflanzungsergebnisse innerhalb spezifischer Dosisbereiche feststellte und darauf hinwies, dass sich eine Dosis-Wirkungs-Beziehung in einer Erhöhung widerspiegeln könnte Rate eines bestimmten Outcomes mit zunehmender Dosis und/oder einer Verschiebung im Spektrum der beobachteten Outcomes.
Im Hinblick auf Teratogenese und Dosis bestehen erhebliche Bedenken hinsichtlich funktioneller Störungen, die sich aus möglichen Auswirkungen auf das Verhalten einer pränatalen Exposition gegenüber Umwelteinflüssen ergeben. Die Tierverhaltens-Teratologie breitet sich schnell aus, aber die menschliche Verhaltens-Umwelt-Teratologie befindet sich in einem relativ frühen Entwicklungsstadium. Derzeit gibt es kritische Einschränkungen bei der Definition und Ermittlung geeigneter Verhaltensergebnisse für epidemiologische Studien. Darüber hinaus ist es möglich, dass geringe Expositionen gegenüber entwicklungstoxischen Stoffen für einige funktionelle Wirkungen wichtig sind.
Mehrere Ergebnisse und Expositionszeit und -dosis
Von besonderer Bedeutung im Hinblick auf die Identifizierung von Gefährdungen durch die Entwicklung am Arbeitsplatz sind die Konzepte der multiplen Folgen sowie des Expositionszeitpunkts und der Expositionsdosis. Auf der Grundlage dessen, was wir über die Entwicklungsbiologie wissen, ist klar, dass es Beziehungen zwischen reproduktiven Ergebnissen wie spontanem Abort und intrauteriner Wachstumsverzögerung und angeborenen Fehlbildungen gibt. Darüber hinaus wurden für viele Entwicklungsgifte Mehrfachwirkungen gezeigt (Tabelle 1).
Tabelle 1. Beispiele für Expositionen im Zusammenhang mit mehreren nachteiligen reproduktiven Endpunkten
| Belichtung | Ergebnis | |||
| Spontane Abtreibung | Angeborene Fehlbildung | Niedriges Geburtsgewicht | Entwicklungsstörungen | |
| Alkohol | X | X | X | X |
| Betäubung Gase |
X | X | ||
| Führen (Lead) | X | X | X | |
| Organische Lösungsmittel | X | X | X | |
| Rauchen | X | X | X | |
Relevant sind dabei Fragen des Expositionszeitpunkts und der Dosis-Wirkungs-Beziehungen. Es ist seit langem anerkannt, dass die Embryonalperiode, in der die Organogenese stattfindet (zwei bis acht Wochen nach der Empfängnis), die Zeit der größten Empfindlichkeit gegenüber der Induktion struktureller Missbildungen ist. Die Fetalperiode von acht Wochen bis zur Entbindung ist die Zeit der Histogenese, wobei während dieser Zeit eine schnelle Zunahme der Zellzahl und Zelldifferenzierung stattfindet. Dann ist es am wahrscheinlichsten, dass funktionelle Anomalien und Wachstumsverzögerung induziert werden. Es ist möglich, dass während dieses Zeitraums Beziehungen zwischen Dosis und Wirkung bestehen, in denen eine hohe Dosis zu einer Wachstumsverzögerung und eine niedrigere Dosis zu Funktions- oder Verhaltensstörungen führen kann.
Vom Mann vermittelte Entwicklungstoxizität
Während allgemein davon ausgegangen wird, dass Entwicklungstoxizität aus der Exposition von Weibchen und Empfängnis resultiert – d. h. teratogene Wirkungen –, gibt es zunehmend Hinweise sowohl aus Tier- als auch aus Humanstudien auf männlich vermittelte Entwicklungswirkungen. Zu den vorgeschlagenen Mechanismen für solche Effekte gehören die Übertragung von Chemikalien vom Vater auf den Empfängnis über die Samenflüssigkeit, die indirekte Kontamination der Mutter und des Empfängnis durch Substanzen, die durch persönliche Kontamination vom Arbeitsplatz in die häusliche Umgebung gelangen, und – wie bereits erwähnt – väterliche Vorurteilsbelastungen die zu übertragbaren genetischen Veränderungen (Mutationen) führen.
Einführung in die männliche und weibliche Fortpflanzungsfunktion
Die Reproduktionstoxizität weist viele einzigartige und herausfordernde Unterschiede zwischen der Toxizität und anderen Systemen auf. Während andere Formen der Umwelttoxizität typischerweise die Entwicklung einer Krankheit bei einer exponierten Person beinhalten, da die Reproduktion die Interaktion zwischen zwei Personen erfordert, wird die Reproduktionstoxizität innerhalb einer reproduktiven Einheit oder eines Paares ausgedrückt. Dieser einzigartige, paarabhängige Aspekt, obwohl offensichtlich, unterscheidet die Reproduktionstoxikologie. Beispielsweise ist es möglich, dass sich die Exposition gegenüber einem Giftstoff durch ein Mitglied eines reproduktiven Paares (z. B. den Mann) in einem nachteiligen Fortpflanzungsergebnis bei dem anderen Mitglied des Paares manifestiert (z. B. erhöhte Häufigkeit spontaner Fehlgeburten). Jeder Versuch, sich mit umweltbedingten Ursachen der Reproduktionstoxizität auseinanderzusetzen, muss den paarspezifischen Aspekt berücksichtigen.
Es gibt noch andere einzigartige Aspekte, die die Herausforderungen der Reproduktionstoxikologie widerspiegeln. Im Gegensatz zur Nieren-, Herz- oder Lungenfunktion tritt die Fortpflanzungsfunktion intermittierend auf. Dies bedeutet, dass berufliche Expositionen die Fortpflanzung beeinträchtigen können, aber in Zeiten, in denen keine Fruchtbarkeit erwünscht ist, unbemerkt bleiben. Diese intermittierende Eigenschaft kann die Identifizierung eines reproduktionstoxischen Stoffes beim Menschen erschweren. Ein weiteres einzigartiges Merkmal der Fortpflanzung, das direkt aus der obigen Überlegung folgt, besteht darin, dass eine vollständige Beurteilung der funktionellen Integrität des Fortpflanzungssystems erfordert, dass das Paar eine Schwangerschaft versucht.
Männliches Fortpflanzungssystem und Toxikologie
Spermatogenese und Spermiogenese sind die zellulären Prozesse, die reife männliche Geschlechtszellen produzieren. Diese Prozesse finden in den Samenkanälchen der Hoden des geschlechtsreifen Mannes statt, wie in Abbildung 1 gezeigt. Die menschlichen Samenkanälchen sind 30 bis 70 cm lang und haben einen Durchmesser von 150 bis 300 mm (Zaneveld 1978). Die Spermatogonien (Stammzellen) sind entlang der Basalmembran der Hodenkanälchen angeordnet und sind die Grundzellen für die Spermienproduktion.
Abbildung 1. Das männliche Fortpflanzungssystem
Spermien reifen durch eine Reihe von Zellteilungen, in denen sich die Spermatogonien vermehren und zu primären Spermatozyten werden. Die ruhenden primären Spermatozyten wandern durch die von den Sertoli-Zellen gebildeten Tight Junctions zur luminalen Seite dieser Hodenbarriere. Wenn die Spermatozyten die Membranbarriere im Hoden erreichen, ist die Synthese von DNA, dem genetischen Material im Zellkern, im Wesentlichen abgeschlossen. Wenn die primären Spermatozyten tatsächlich auf das Lumen der Hodenkanälchen treffen, durchlaufen diese eine spezielle Art der Zellteilung, die nur in Keimzellen stattfindet und als Meiose bezeichnet wird. Die meiotische Zellteilung führt zur Aufspaltung der Chromosomenpaare im Zellkern, so dass jede entstehende Keimzelle nur eine einzige Kopie jedes Chromosomenstrangs enthält und nicht ein passendes Paar.
Während der Meiose verändern die Chromosomen ihre Form, indem sie kondensieren und fadenförmig werden. An einem bestimmten Punkt bricht die Kernmembran, die sie umgibt, zusammen und Mikrotubuli-Spindeln heften sich an die Chromosomenpaare, wodurch sie sich trennen. Damit ist die erste meiotische Teilung abgeschlossen und es bilden sich zwei haploide sekundäre Spermatozyten. Die sekundären Spermatozyten durchlaufen dann eine zweite meiotische Teilung, um eine gleiche Anzahl von X- und Y-Chromosom tragenden Spermatiden zu bilden.
Die morphologische Umwandlung von Spermatiden in Spermatozoen wird als Spermiogenese bezeichnet. Wenn die Spermiogenese abgeschlossen ist, wird jede Samenzelle von der Sertoli-Zelle durch einen Prozess, der als Spermiation bezeichnet wird, in das Lumen der Hodenkanälchen freigesetzt. Die Spermien wandern entlang des Tubulus zum Rete testis und in den Nebenhodenkopf. Spermien, die die Hodenkanälchen verlassen, sind unreif: Sie können keine Eizelle befruchten und nicht schwimmen. Spermatozoen, die in das Lumen der Hodenkanälchen freigesetzt werden, werden in Flüssigkeit suspendiert, die hauptsächlich von den Sertoli-Zellen produziert wird. Konzentrierte Spermien, die in dieser Flüssigkeit suspendiert sind, fließen kontinuierlich aus den Hodenkanälchen, durch geringfügige Änderungen im ionischen Milieu innerhalb der Rete testis, durch die Vasa efferentia und in die Nebenhoden. Der Nebenhoden ist ein einziger stark gewundener Schlauch (12 bis 21 Meter lang), in dem die Spermien XNUMX bis XNUMX Tage verbringen.
Innerhalb der Nebenhoden erwerben Spermien nach und nach Beweglichkeit und Befruchtungsfähigkeit. Dies kann auf die wechselnde Natur der Suspensionsflüssigkeit in den Nebenhoden zurückzuführen sein. Das heißt, wenn die Zellen reifen, absorbiert der Nebenhoden Komponenten aus der Flüssigkeit, einschließlich Sekrete von den Sertoli-Zellen (z. B. androgenbindendes Protein), wodurch die Konzentration von Spermatozoen erhöht wird. Der Nebenhoden trägt auch seine eigenen Sekrete zur Suspensionsflüssigkeit bei, einschließlich der Chemikalien Glycerylphosphorylcholin (GPC) und Carnitin.
Die Spermienmorphologie verändert sich in den Nebenhoden weiter. Das zytoplasmatische Tröpfchen wird abgestoßen und der Samenkern kondensiert weiter. Während der Nebenhoden das Hauptspeicherreservoir für Spermien bis zur Ejakulation ist, wurden etwa 30 % der Spermien in einem Ejakulat in den Samenleitern gespeichert. Häufige Ejakulation beschleunigt die Spermienpassage durch die Nebenhoden und kann die Anzahl unreifer (unfruchtbarer) Spermien im Ejakulat erhöhen (Zaneveld 1978).
Ejakulation
Sobald sie sich in den Samenleitern befinden, werden die Spermien eher durch die Muskelkontraktionen der Ejakulation als durch den Flüssigkeitsfluss transportiert. Während der Ejakulation werden Flüssigkeiten zwangsweise aus den akzessorischen Geschlechtsdrüsen ausgestoßen, wodurch das Samenplasma entsteht. Diese Drüsen stoßen ihre Sekrete nicht gleichzeitig aus. Vielmehr stößt die Bulbourethraldrüse (Cowper-Drüse) zuerst eine klare Flüssigkeit aus, gefolgt von den Prostatasekreten, den spermienkonzentrierten Flüssigkeiten aus den Nebenhoden und Ampullen des Vas deferens und schließlich der größte Teil hauptsächlich aus den Samenbläschen. Samenplasma ist also keine homogene Flüssigkeit.
Toxische Wirkungen auf Spermatogenese und Spermiogenese
Giftstoffe können die Spermatogenese an mehreren Stellen stören. Am schädlichsten sind aufgrund ihrer Irreversibilität Giftstoffe, die Spermatogonien oder Sertoli-Zellen töten oder (über Reparaturmechanismen hinaus) genetisch verändern. Tierversuche waren nützlich, um das Stadium zu bestimmen, in dem ein Giftstoff den spermatogenetischen Prozess angreift. Diese Studien verwenden eine kurzzeitige Exposition gegenüber einem Giftstoff vor der Probenahme, um die Wirkung zu bestimmen. Indem man die Dauer für jedes spermatogene Stadium kennt, kann man extrapolieren, um das betroffene Stadium abzuschätzen.
Die biochemische Analyse von Samenplasma liefert Einblicke in die Funktion der akzessorischen Geschlechtsdrüsen. Chemikalien, die hauptsächlich von jeder der akzessorischen Geschlechtsdrüsen abgesondert werden, werden typischerweise so ausgewählt, dass sie als Marker für die jeweilige Drüse dienen. Beispielsweise wird der Nebenhoden durch GPC repräsentiert, die Samenbläschen durch Fruktose und die Prostata durch Zink. Beachten Sie, dass diese Art der Analyse nur grobe Informationen über die Drüsenfunktion und wenig oder keine Informationen über die anderen sekretorischen Bestandteile liefert. Die Messung des pH-Werts und der Osmolalität des Samens liefert zusätzliche allgemeine Informationen über die Natur des Samenplasmas.
Samenplasma kann auf das Vorhandensein eines Giftstoffs oder seines Metaboliten analysiert werden. Schwermetalle wurden im Samenplasma mittels Atomabsorptionsspektrophotometrie nachgewiesen, während halogenierte Kohlenwasserstoffe in Samenflüssigkeit nach Extraktion oder proteinlimitierender Filtration gaschromatographisch gemessen wurden (Stachel et al. 1989; Zikarge 1986).
Die Lebensfähigkeit und Beweglichkeit von Spermatozoen im Samenplasma spiegelt typischerweise die Qualität des Samenplasmas wider. Veränderungen der Lebensfähigkeit der Spermien, gemessen durch Fleckenausschluss oder durch hypoosmotische Schwellung, oder Veränderungen der Spermienbeweglichkeitsparameter deuten auf posttestikuläre toxische Wirkungen hin.
Samenanalysen können auch zeigen, ob die Produktion von Samenzellen durch einen Giftstoff beeinträchtigt wurde. Spermienzahl und Spermienmorphologie liefern Indizes für die Integrität der Spermatogenese und Spermiogenese. So korreliert die Zahl der Spermien im Ejakulat direkt mit der Zahl der Keimzellen pro Gramm Hoden (Zukerman et al. 1978), während eine abnorme Morphologie wahrscheinlich das Ergebnis einer abnormen Spermiogenese ist. Tote Spermien oder unbewegliche Spermien spiegeln oft die Auswirkungen posttestikulärer Ereignisse wider. Somit kann die Art oder der Zeitpunkt einer toxischen Wirkung auf das Ziel des Giftstoffs hinweisen. Beispielsweise führte die Exposition männlicher Ratten gegenüber 2-Methoxyethanol nach vier Wochen zu einer verminderten Fertilität (Chapin et al. 1985). Dieser durch histologische Untersuchung bestätigte Nachweis weist darauf hin, dass das Ziel der Toxizität die Spermatozyte ist (Chapin et al. 1984). Während es ethisch nicht vertretbar ist, Menschen mutmaßlichen reproduktionstoxischen Stoffen auszusetzen, können Samenanalysen von Serienejakulaten von Männern, die versehentlich für kurze Zeit potenziellen toxischen Stoffen ausgesetzt wurden, ähnliche nützliche Informationen liefern.
Berufliche Exposition gegenüber 1,2-Dibromchlorpropan (DBCP) verringerte die Spermienkonzentration in Ejakulaten von einem Medianwert von 79 Millionen Zellen/ml bei nicht exponierten Männern auf 46 Millionen Zellen/ml bei exponierten Arbeitern (Whorton et al. 1979). Nachdem die Arbeiter von der Exposition entfernt wurden, erholten sich diejenigen mit reduzierter Spermienzahl teilweise, während Männer, die Azoospermie hatten, unfruchtbar blieben. Die Hodenbiopsie ergab, dass das Ziel von DBCP die Spermatogonie war. Dies belegt die Schwere der Wirkung, wenn Stammzellen das Ziel von Giftstoffen sind. Es gab keine Hinweise darauf, dass eine DBCP-Exposition bei Männern mit einem ungünstigen Schwangerschaftsausgang assoziiert war (Potashnik und Abeliovich 1985). Ein weiteres Beispiel für einen Giftstoff, der auf die Spermatogenese/Spermiogenese abzielt, war die Untersuchung von Arbeitern, die Ethylendibromid (EDB) ausgesetzt waren. Sie hatten mehr Spermien mit spitz zulaufenden Köpfen und weniger Spermien pro Ejakulat als die Kontrollen (Ratcliffe et al. 1987).
Genetische Schäden sind in menschlichen Spermien schwer nachzuweisen. Mehrere Tierstudien mit dem Dominant-Letal-Assay (Ehling et al. 1978) weisen darauf hin, dass eine väterliche Exposition zu einem ungünstigen Schwangerschaftsausgang führen kann. Epidemiologische Studien an großen Populationen haben eine erhöhte Häufigkeit spontaner Aborte bei Frauen gezeigt, deren Ehemänner als Kfz-Mechaniker arbeiteten (McDonald et al. 1989). Solche Studien weisen auf einen Bedarf an Verfahren hin, um genetische Schäden in menschlichen Spermien nachzuweisen. Solche Verfahren werden von mehreren Labors entwickelt. Diese Verfahren schließen DNA-Sonden zum Erkennen genetischer Mutationen (Hecht 1987), Spermienchromosomen-Karyotypisierung (Martin 1983) und DNA-Stabilitätsbewertung durch Durchflusszytometrie (Evenson 1986) ein.
Abbildung 2. Expositionen, die positiv mit einer nachteiligen Beeinflussung der Samenqualität assoziiert sind
Abbildung 2 listet Expositionen auf, von denen bekannt ist, dass sie die Spermienqualität beeinflussen, und Tabelle 1 bietet eine Zusammenfassung der Ergebnisse epidemiologischer Studien zu väterlichen Auswirkungen auf die Fortpflanzungsergebnisse.
Tabelle 1. Epidemiologische Studien zu väterlichen Auswirkungen auf den Schwangerschaftsausgang
| Referenz | Art der Exposition oder Beschäftigung | Assoziation mit Exposition1 | Bewirken |
| Datensatzbasierte Bevölkerungsstudien | |||
| Lindbohm et al. 1984 | Lösungsmittel | - | Spontane Abtreibung |
| Lindbohm et al. 1984 | Tankstelle | + | Spontane Abtreibung |
| Daniell und Vaughan 1988 | Organische Lösungsmittel | - | Spontane Abtreibung |
| McDonaldet al. 1989 | Mechanik | + | Spontane Abtreibung |
| McDonaldet al. 1989 | Lebensmittelverarbeitung | + | Entwicklungsstörungen |
| Lindbohm et al. 1991a | Ethylenoxid | + | Spontane Abtreibung |
| Lindbohm et al. 1991a | Erdölraffinerie | + | Spontane Abtreibung |
| Lindbohm et al. 1991a | Holz imprägniert | + | Spontane Abtreibung |
| Lindbohm et al. 1991a | Gummichemikalien | + | Spontane Abtreibung |
| Olsenet al. 1991 | Metallindustrie | + | Krebsrisiko bei Kindern |
| Olsenet al. 1991 | Maschinisten | + | Krebsrisiko bei Kindern |
| Olsenet al. 1991 | Smiths | + | Krebsrisiko bei Kindern |
| Kristensenet al. 1993 | Lösungsmittel | + | Frühgeburt |
| Kristensenet al. 1993 | Blei und Lösungsmittel | + | Frühgeburt |
| Kristensenet al. 1993 | Führen (Lead) | + | Perinataler Tod |
| Kristensenet al. 1993 | Führen (Lead) | + | Männliche Kindermorbidität |
| Fall-Kontroll-Studien | |||
| Kucera 1968 | Druckindustrie | (+) | Lippenspalte |
| Kucera 1968 | Lackieren | (+) | Gaumenspalte |
| Olsen 1983 | Lackieren | + | Schädigung des Zentralnervensystems |
| Olsen 1983 | Lösungsmittel | (+) | Schädigung des Zentralnervensystems |
| Severet al. 1988 | Niedrige Strahlung | + | Neuralrohrdefekte |
| Taskinen et al. 1989 | Organische Lösungsmittel | + | Spontane Abtreibung |
| Taskinen et al. 1989 | Aromatische Kohlenwasserstoffe | + | Spontane Abtreibung |
| Taskinen et al. 1989 | Staub | + | Spontane Abtreibung |
| Gardneret al. 1990 | Strahlung | + | Leukämie im Kindesalter |
| Bond 1992 | Schweiß- | + | Zeit bis zur Empfängnis |
| Wilkins und Sinks 1990 | Landwirtschaft | (+) | Hirntumor bei Kindern |
| Wilkins und Sinks 1990 | Hoch- und Tiefbau | (+) | Hirntumor bei Kindern |
| Wilkins und Sinks 1990 | Lebensmittel-/Tabakverarbeitung | (+) | Hirntumor bei Kindern |
| Wilkins und Sinks 1990 | Metal | + | Hirntumor bei Kindern |
| Lindbohmn et al. 1991b | Führen (Lead) | (+) | Spontane Abtreibung |
| Salmen et al. 1992 | Führen (Lead) | (+) | Angeborene Mängel |
| Veulemans et al. 1993 | Ethylenglykolether | + | Abnormales Spermiogramm |
| Chiaet al. 1992 | Metallindustrie | + | Cadmium im Sperma |
1 – kein signifikanter Zusammenhang; (+) marginal signifikante Assoziation; + signifikante Assoziation.
Quelle: Adaptiert von Taskinen 1993.
Neuroendokrines System
Die Gesamtfunktion des Fortpflanzungssystems wird durch das Nervensystem und die von den Drüsen produzierten Hormone (das endokrine System) gesteuert. Die reproduktive neuroendokrine Achse des Mannes betrifft hauptsächlich das Zentralnervensystem (ZNS), den Hypophysenvorderlappen und die Hoden. Eingaben aus dem ZNS und aus der Peripherie werden durch den Hypothalamus integriert, der direkt die Gonadotropinsekretion durch den Hypophysenvorderlappen reguliert. Die Gonadotropine wiederum wirken hauptsächlich auf die Leydig-Zellen innerhalb des Interstitiums und Sertoli und Keimzellen innerhalb der Hodenkanälchen, um die Spermatogenese und die Hormonproduktion durch die Hoden zu regulieren.
Hypothalamus-Hypophysen-Achse
Der Hypothalamus sondert das Neurohormon Gonadotropin-Releasing-Hormon (GnRH) in das hypophysäre Pfortadergefäßsystem für den Transport zum Hypophysenvorderlappen ab. Die pulsierende Sekretion dieses Dekapeptids bewirkt die gleichzeitige Freisetzung von luteinisierendem Hormon (LH) und mit geringerer Synchronität und einem Fünftel der Potenz die Freisetzung von follikelstimulierendem Hormon (FSH) (Bardin 1986). Es gibt erhebliche Beweise für das Vorhandensein eines separaten FSH-Releasing-Hormons, obwohl noch keines isoliert wurde (Savy-Moore und Schwartz 1980; Culler und Negro-Vilar 1986). Diese Hormone werden vom Hypophysenvorderlappen ausgeschüttet. LH wirkt direkt auf die Leydig-Zellen, um die Synthese und Freisetzung von Testosteron zu stimulieren, während FSH die Aromatisierung von Testosteron zu Östradiol durch die Sertoli-Zellen stimuliert. Die gonadotrope Stimulation bewirkt die Freisetzung dieser Steroidhormone in die Samenvene.
Die Gonadotropinsekretion wird wiederum durch Testosteron und Östradiol durch negative Rückkopplungsmechanismen kontrolliert. Testosteron wirkt hauptsächlich auf den Hypothalamus, um die GnRH-Sekretion zu regulieren, und verringert dadurch hauptsächlich die Pulsfrequenz der LH-Freisetzung. Östradiol hingegen wirkt auf die Hypophyse, um das Ausmaß der Gonadotropinfreisetzung zu verringern. Durch diese endokrinen Rückkopplungsschleifen werden die Hodenfunktion im Allgemeinen und die Testosteronsekretion im Besonderen in einem relativ stabilen Zustand gehalten.
Hypophysen-Hoden-Achse
LH und FSH werden allgemein als notwendig für eine normale Spermatogenese angesehen. Vermutlich ist die Wirkung von LH sekundär zur Induktion hoher intratestikulärer Konzentrationen von Testosteron. Daher wirken FSH aus der Hypophyse und Testosteron aus den Leydig-Zellen auf die Sertoli-Zellen innerhalb des Epithels der Hodenkanälchen, um die Spermatogenese einzuleiten. Die Spermienproduktion bleibt bestehen, obwohl sie quantitativ reduziert ist, nachdem entweder LH (und vermutlich die hohen intratestikulären Testosteronkonzentrationen) oder FSH entfernt wurden. FSH wird benötigt, um die Spermatogenese in der Pubertät zu initiieren und in geringerem Maße eine gestoppte Spermatogenese wieder zu initiieren (Matsumoto 1989; Sharpe 1989).
Der hormonelle Synergismus, der dazu dient, die Spermatogenese aufrechtzuerhalten, kann die Rekrutierung von differenzierten Spermatogonien durch FSH für den Eintritt in die Meiose zur Folge haben, während Testosteron spezifische nachfolgende Stadien der Spermatogenese steuern kann. FSH und Testosteron können auch auf die Sertoli-Zelle einwirken, um die Produktion eines oder mehrerer parakriner Faktoren zu stimulieren, die die Anzahl der Leydig-Zellen und die Testosteronproduktion durch diese Zellen beeinflussen können (Sharpe 1989). FSH und Testosteron stimulieren die Proteinsynthese durch Sertoli-Zellen, einschließlich der Synthese von Androgen-bindendem Protein (ABP), während FSH allein die Synthese von Aromatase und Inhibin stimuliert. ABP wird hauptsächlich in die seminifere tubuläre Flüssigkeit sezerniert und zum proximalen Teil des Caput Nebenhoden transportiert, wo es möglicherweise als lokaler Träger von Androgenen dient (Bardin 1986). Aromatase katalysiert die Umwandlung von Testosteron in Östradiol in den Sertoli-Zellen und in anderen peripheren Geweben.
Inhibin ist ein Glykoprotein, das aus zwei unterschiedlichen, Disulfid-verknüpften Untereinheiten, a und b, besteht. Obwohl Inhibin vorzugsweise die FSH-Freisetzung hemmt, kann es auch die LH-Freisetzung in Gegenwart einer GnRH-Stimulation abschwächen (Kotsugi et al. 1988). FSH und LH stimulieren die Inhibinfreisetzung mit etwa gleicher Potenz (McLachlan et al. 1988). Interessanterweise wird Inhibin in das Samenvenenblut als Pulse sezerniert, die synchron zu denen von Testosteron sind (Winters 1990). Dies spiegelt wahrscheinlich nicht die direkten Wirkungen von LH oder Testosteron auf die Aktivität der Sertoli-Zellen wider, sondern eher die Wirkungen anderer Leydig-Zellprodukte, die entweder in die Zwischenräume oder in den Kreislauf abgegeben werden.
Prolaktin, das auch von der vorderen Hypophyse ausgeschieden wird, wirkt synergistisch mit LH und Testosteron, um die männliche Fortpflanzungsfunktion zu fördern. Prolaktin bindet an spezifische Rezeptoren auf der Leydig-Zelle und erhöht die Menge des Androgenrezeptorkomplexes im Zellkern von auf Androgen ansprechenden Geweben (Baker et al. 1977). Hyperprolaktinämie ist mit einer Verringerung der Hoden- und Prostatagröße, des Samenvolumens und der zirkulierenden Konzentrationen von LH und Testosteron verbunden (Segal et al. 1979). Hyperprolaktinämie wurde auch mit Impotenz in Verbindung gebracht, anscheinend unabhängig von der Veränderung der Testosteronsekretion (Thorner et al. 1977).
Bei der Messung von Steroidhormon-Metaboliten im Urin muss das Potenzial berücksichtigt werden, dass die untersuchte Exposition den Metabolismus der ausgeschiedenen Metaboliten verändern kann. Dies ist besonders relevant, da die meisten Metaboliten von der Leber gebildet werden, einem Ziel vieler Giftstoffe. Blei verringerte beispielsweise die Menge an sulfatierten Steroiden, die in den Urin ausgeschieden wurden (Apostoli et al. 1989). Die Blutspiegel für beide Gonadotropine werden während des Schlafs erhöht, wenn der Mann in die Pubertät eintritt, während die Testosteronspiegel dieses Tagesmuster bei Männern bis ins Erwachsenenalter beibehalten (Plant 1988). Daher sollten Blut-, Urin- oder Speichelproben ungefähr zur gleichen Tageszeit entnommen werden, um Schwankungen aufgrund von Tagessekretionsmustern zu vermeiden.
Die offensichtlichen Auswirkungen einer toxischen Exposition, die auf das reproduktive neuroendokrine System abzielt, werden höchstwahrscheinlich durch veränderte biologische Manifestationen der Androgene offenbart. Deutlich durch Androgene regulierte Manifestationen beim erwachsenen Mann, die während einer grundlegenden körperlichen Untersuchung festgestellt werden können, umfassen: (1) Stickstoffretention und Muskelentwicklung; (2) Erhaltung der äußeren Genitalien und akzessorischen Geschlechtsorgane; (3) Aufrechterhaltung des vergrößerten Kehlkopfes und der verdickten Stimmbänder, die die männliche Stimme verursachen; (4) Bart-, Achsel- und Schamhaarwachstum und zeitlicher Haarrückgang und Glatzenbildung; (5) Libido und sexuelle Leistungsfähigkeit; (6) organspezifische Proteine in Geweben (z. B. Leber, Nieren, Speicheldrüsen); und (7) aggressives Verhalten (Bardin 1986). Veränderungen in einem dieser Merkmale können darauf hindeuten, dass die Androgenproduktion beeinträchtigt wurde.
Beispiele für toxische Wirkungen
Blei ist ein klassisches Beispiel für einen Giftstoff, der das neuroendokrine System direkt beeinflusst. Bei Männern, die weniger als ein Jahr Blei ausgesetzt waren, waren die Serum-LH-Konzentrationen erhöht. Dieser Effekt trat bei Männern, die länger als fünf Jahre exponiert waren, nicht fort. Serum-FSH-Spiegel wurden nicht beeinflusst. Andererseits waren bei Männern, die mehr als fünf Jahre Blei ausgesetzt waren, die ABP-Serumspiegel erhöht und die Gesamttestosteronspiegel verringert. Die Serumspiegel von freiem Testosteron waren nach drei- bis fünfjähriger Bleiexposition signifikant erniedrigt (Rodamilans et al. 1988). Im Gegensatz dazu waren die Serumkonzentrationen von LH, FSH, Gesamttestosteron, Prolaktin und neutralen 17-Ketosteroiden insgesamt bei Arbeitern mit niedrigeren zirkulierenden Bleispiegeln nicht verändert, obwohl die Verteilungshäufigkeit der Spermienzahl verändert war (Assennato et al. 1986). .
Auch die Exposition von Werftmalern gegenüber 2-Ethoxyethanol reduzierte die Spermienzahl ohne gleichzeitige Veränderung der LH-, FSH- oder Testosteronkonzentrationen im Serum (Welch et al. 1988). So können Giftstoffe die Hormonproduktion und die Spermienmessungen unabhängig voneinander beeinflussen.
Bei männlichen Arbeitern, die an der Herstellung des Nematozids DBCP beteiligt waren, traten erhöhte LH- und FSH-Serumspiegel sowie eine verringerte Spermienzahl und Fruchtbarkeit auf. Diese Wirkungen sind offensichtlich Folgen von DBCP-Einwirkungen auf die Leydig-Zellen, um die Androgenproduktion oder -wirkung zu verändern (Mattison et al. 1990).
Mehrere Verbindungen können aufgrund struktureller Ähnlichkeit mit reproduktiven Steroidhormonen Toxizität ausüben. Somit können Giftstoffe durch Bindung an den jeweiligen endokrinen Rezeptor als Agonisten oder Antagonisten wirken, um biologische Reaktionen zu unterbrechen. Chlordecon (Kepone), ein Insektizid, das an Östrogenrezeptoren bindet, verringerte die Anzahl und Beweglichkeit der Spermien, stoppte die Reifung der Spermien und verringerte die Libido. Während es verlockend ist, darauf hinzuweisen, dass diese Wirkungen darauf zurückzuführen sind, dass Chlordecon die Östrogenwirkungen auf neuroendokriner oder testikulärer Ebene beeinflusst, wurde in diesen Studien nicht gezeigt, dass die Serumspiegel von Testosteron, LH und FSH in ähnlicher Weise wie die Wirkungen einer Östradioltherapie verändert wurden . DDT und seine Metaboliten weisen auch steroidale Eigenschaften auf und es ist zu erwarten, dass sie die männliche Fortpflanzungsfunktion verändern, indem sie die Steroidhormonfunktionen stören. Xenobiotika wie polychlorierte Biphenyle, polybromierte Biphenyle und chlororganische Pestizide können auch die männlichen Fortpflanzungsfunktionen beeinträchtigen, indem sie östrogene Agonisten-/Antagonisten-Aktivität ausüben (Mattison et al. 1990).
Sexuelle Funktion
Die menschliche Sexualfunktion bezieht sich auf die integrierten Aktivitäten der Hoden und sekundären Geschlechtsdrüsen, der endokrinen Kontrollsysteme und der auf dem zentralen Nervensystem basierenden Verhaltens- und psychologischen Komponenten der Fortpflanzung (Libido). Erektion, Ejakulation und Orgasmus sind drei unterschiedliche, unabhängige, physiologische und psychodynamische Ereignisse, die normalerweise gleichzeitig bei Männern auftreten.
Aufgrund der oben beschriebenen Probleme liegen nur wenige verlässliche Daten zu den Auswirkungen beruflicher Exposition auf die Sexualfunktion vor. Es wurde gezeigt, dass Medikamente jede der drei Phasen der männlichen Sexualfunktion beeinflussen (Fabro 1985), was auf das Potenzial berufsbedingter Expositionen hindeutet, ähnliche Wirkungen auszuüben. Antidepressiva, Testosteronantagonisten und Stimulanzien der Prolaktinfreisetzung verringern wirksam die Libido bei Männern. Antihypertensiva, die auf das sympathische Nervensystem einwirken, rufen bei manchen Männern Impotenz hervor, aber überraschenderweise Priapismus bei anderen. Phenoxybenzamin, ein adrenozeptiver Antagonist, wurde klinisch verwendet, um die Samenemission, aber nicht den Orgasmus zu blockieren (Shilon, Paz und Homonnai 1984). Anticholinerge Antidepressiva ermöglichen die Samenemission, während sie den Samenerguss und den Orgasmus blockieren, was dazu führt, dass Samenplasma aus der Harnröhre sickert, anstatt ausgestoßen zu werden.
Freizeitdrogen beeinflussen auch die Sexualfunktion (Fabro 1985). Ethanol kann Impotenz reduzieren und gleichzeitig die Libido steigern. Kokain, Heroin und hohe Dosen von Cannabinoiden reduzieren die Libido. Auch Opiate verzögern oder beeinträchtigen die Ejakulation.
Die große und vielfältige Palette von Arzneimitteln, die nachweislich das männliche Fortpflanzungssystem beeinflussen, unterstützt die Vorstellung, dass Chemikalien, die am Arbeitsplatz gefunden werden, auch reproduktionstoxisch sein können. Zur Bewertung dieses wichtigen Bereichs der Reproduktionstoxikologie sind für Feldstudienbedingungen zuverlässige und praktikable Forschungsmethoden erforderlich.
HAFTUNGSAUSSCHLUSS: Die ILO übernimmt keine Verantwortung für auf diesem Webportal präsentierte Inhalte, die in einer anderen Sprache als Englisch präsentiert werden, der Sprache, die für die Erstproduktion und Peer-Review von Originalinhalten verwendet wird. Bestimmte Statistiken wurden seitdem nicht aktualisiert die Produktion der 4. Auflage der Encyclopaedia (1998)."