Categorías Niños

1. Sangre (3)

1. Sangre
Redactor del capítulo: Bernardo D. Goldstein
Índice del contenido
Mesas
Sistema Hematopoyético y Linfático
Bernardo D. Goldstein
Leucemia, Linfomas Malignos y Mieloma Múltiple
Timo Partanen, Paolo Boffetta, Elisabete Weiderpass
Agentes o condiciones de trabajo que afectan la sangre
Bernardo D. Goldstein
Mesas
Haga clic en un enlace a continuación para ver la tabla en el contexto del artículo.

2. Cáncer (4)

2. Cáncer
Redactor del capítulo: paolo bofetta
Mesa de Contenidos
Mesas
Introducción
Neil Pearce, Paolo Boffetta y Manolis Kogevinas
Carcinógenos ocupacionales
Paolo Boffetta, Rodolfo Saracci, Manolis Kogevinas, Julian Wilbourn y Harri Vainio
Cáncer ambiental
Bruce K. Armstrong y Paolo Boffetta
Prevención
Por Gustavsson
Mesas
Haga clic en un enlace a continuación para ver la tabla en el contexto del artículo.
- Cáncer ocupacional: datos clave
- Proporciones estimadas de cáncer (PAR) atribuibles a las ocupaciones
- Evaluación de la evidencia de carcinogenicidad en las Monografías de la IARC
- Grupos de clasificación de programas de monografías de IARC
- Grupo 1-Químicos cancerígenos para los humanos
- Grupo 2A: Sustancias químicas probablemente cancerígenas para los humanos
- Grupo 2B: Sustancias químicas posiblemente cancerígenas para los humanos
- Pesticidas evaluados en Monografías IARC, Volúmenes 1-63 (1972-1995)
- Medicamentos evaluados en IARC Monografías, Volúmenes 1-63 (1972-1995)
- Agentes ambientales/exposiciones conocidas o sospechadas de cáncer humano
- Industrias, ocupaciones, exposiciones que presentan un riesgo cancerígeno
- Industrias, occs., exps. con exceso de cáncer carcinógenos no definitivos
- Variaciones poblacionales registradas de la incidencia de algunos cánceres comunes

3. Sistema cardiovascular (7)

3. Sistema cardiovascular
Editores de capítulos: Lothar Heinemann y Gerd Heuchert
Índice del contenido
Tablas y Figuras
Introducción
Lothar Heinemann y Gerd Heuchert
Morbilidad y Mortalidad Cardiovascular en la Fuerza Laboral
Gottfried Enderlein y Lothar Heinemann
El concepto de factor de riesgo en la enfermedad cardiovascular
Lothar Heinemann, Gottfried Enderlein y Heide Stark
Programas de Rehabilitación y Prevención
Lothar Heinemann y Gottfried Enderlein
Riesgos físicos, químicos y biológicos
Factores físicos
Heide Stark y Gerd Heuchert
Materiales químicos peligrosos
Ulrike Tittelbach y Wolfram Dietmar Schneider
Peligros biológicos
Regina Jäckel, Ulrike Tittelbach y Wolfram Dietmar Schneider
Mesas
Haga clic en un enlace a continuación para ver la tabla en el contexto del artículo
- Mortalidad por enfermedades cardiovasculares
- Tasas de mortalidad, grupos especiales de diagnóstico cardiovascular
- Tasa de enfermedad y reducción de la capacidad de trabajo
- Trabajo asociado a riesgos cardiovasculares
- Infecciones y enfermedades relacionadas con el trabajo
Figuras
Apunte a una miniatura para ver el título de la figura, haga clic para ver la figura en el contexto del artículo.

4. Sistema Digestivo (6)

4. Sistema digestivo
Editor del capítulo: Heikki Savolainen
Índice del contenido
Figuras
Sistema digestivo
G.Frada
boca y dientes
F. Gobbato
Hígado
Jorge Kazantzis
Úlcera péptica
KS cho
Cáncer de hígado
Timo Partanen, Timo Kauppinen, Paolo Boffetta y Elisabete Weiderpass
Cancer pancreatico
Timo Partanen, Timo Kauppinen, Paolo Boffetta y Elisabete Weiderpass
Figuras
Apunte a una miniatura para ver el título de la figura, haga clic para ver la figura en el contexto del artículo.

5. Salud mental (8)

5. Salud mental
Editores de capítulos: Joseph J. Hurrell, Lawrence R. Murphy, Steven L. Sauter y Lennart Levi
Índice del contenido
Tablas y Figuras
Trabajo y Salud Mental
Irene LD Houtman y Michiel AJ Kompier
Psicosis relacionada con el trabajo
Craig Stenberg, Judith Holder y Krishna Tallur
Estado de ánimo y afecto
Depresión
Jay Lasser y Jeffrey P. Kahn
Ansiedad relacionada con el trabajo
Randal D Beaton
Trastorno de estrés postraumático y su relación con la salud ocupacional y la prevención de lesiones
marca braverman
Estrés y Burnout y su Implicación en el Ambiente Laboral
Herbert J. Freudenberger
Trastornos cognitivos
Catalina A. Heaney
Karoshi: muerte por exceso de trabajo
takashi haratani
Mesas
Haga clic en un enlace a continuación para ver la tabla en el contexto del artículo.
1. Resumen esquemático de las estrategias de gestión y ejemplos
Figuras
Apunte a una miniatura para ver el título de la figura, haga clic para ver la figura en el contexto del artículo.

6. Sistema musculoesquelético (14)

6. Sistema musculoesquelético
Editores de capítulos: Hilkka Riihimäki y Eira Viikari-Juntura
Índice del contenido
Tablas y Figuras
General
Hilkka Riihimäki
Musculatura
Gisela Sjogaard
Tendones
Thomas J Armstrong
Huesos y articulaciones
david hamerman
Discos intervertebrales
Sally Roberts y Jill PG Urban
Región de la espalda baja
Hilkka Riihimäki
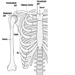
Región de la columna torácica
Jarl-Erik Michelsson
Cuello
Asa Kilbom
Shoulder
Mats Hagberg
codo
Eira Viikari Juntura
antebrazo, muñeca y mano
Eira Viikari Juntura
Cadera y rodilla
Eva Vingård
Pierna, Tobillo y Pie
Jarl-Erik Michelsson
Otras enfermedades
Marjatta Leirisalo-Repo
Mesas
Haga clic en un enlace a continuación para ver la tabla en el contexto del artículo.
- Estructura-función de los componentes de la articulación
- Prevalencia de trastornos de la espalda, en finlandeses mayores de 30 años
- Reducir los riesgos de dolor lumbar en el trabajo
- Clasificación: trastornos de la espalda baja (Quebec Task Force)
- Movimientos permisibles de cabeza en conducción prolongada
- Incidencia de epicondilitis en varias poblaciones
- Incidencia de tenosinovitis/peritendinitis
- Osteoartrosis primaria de cadera en Malmö, Suecia
- Pautas para el tratamiento de la artritis reumatoide
- Infecciones conocidas por desencadenar artritis reactiva
Figuras
Apunte a una miniatura para ver el título de la figura, haga clic para ver la figura en el contexto del artículo.

7. Sistema Nervioso (9)

7. Sistema Nervioso
Redactor del capítulo: donna mergler
Índice del contenido
Tablas y Figuras
Sistema Nervioso: Resumen
Donna Mergler y José A. Valciukas
Anatomía y fisiología
José A. Valciukas
Agentes Neurotóxicos Químicos
Peter Arlien-Søborg y Leif Simonsen
Manifestaciones de intoxicación aguda y crónica temprana
donna mergler
Prevención de la neurotoxicidad en el trabajo
barry johnson
Síndromes clínicos asociados con neurotoxicidad
Roberto G. Feldman
Medición de los déficits neurotóxicos
donna mergler
Diagnóstico
Anna María Seppäläinen
Neuroepidemiología Ocupacional
Olav Axelson
Mesas
Haga clic en un enlace a continuación para ver la tabla en el contexto del artículo.
- Nombres y funciones principales de cada par de nervios craneales
- Agrupación de efectos neurotóxicos en cuanto a neurotoxicidad.
- Gases asociados con efectos neurotóxicos
- Metales neurotóxicos y sus compuestos inorgánicos
- monómeros neurotóxicos
- Disolventes orgánicos asociados a neurotoxicidad
- Clases de pesticidas neurotóxicos comunes
- Otros productos químicos asociados con la neurotoxicidad
- Lista de verificación de síntomas crónicos
- Efectos neurofuncionales de la exposición a algunas neurotoxinas
- Exposiciones químicas y síndromes neurotóxicos asociados
- Algunas baterías "básicas" para evaluar los efectos neurotóxicos tempranos
- Árbol de decisión para la enfermedad neurotóxica
- Efectos neurofuncionales constantes de la exposición en el lugar de trabajo a algunas de las principales sustancias neurotóxicas
Figuras
Apunte a una miniatura para ver el título de la figura, haga clic para ver la figura en el contexto del artículo.

8. Sistema renal-urinario (2)

8. Sistema renal-urinario
Redactor del capítulo: George P. Hemstreet
Índice del contenido
Tablas y Figuras
Sistemas renales y urinarios
George P. Hemstreet
Cánceres renales y urinarios
Timo Partanen, Harri Vainio, Paolo Boffetta y Elisabete Weiderpass
Mesas
Haga clic en un enlace a continuación para ver la tabla en el contexto del artículo.
- Enzimas del metabolismo de fármacos en el riñón
- Las causas más comunes de hematuria, por edad y sexo
- Criterios para la selección de biomarcadores
- Posibles biomarcadores vinculados a la lesión celular
- Insuficiencia renal aguda y ocupación
- Segmentos de la nefrona afectados por tóxicos seleccionados
- Aplicaciones de la citología urinaria
Figuras
Apunte a una miniatura para ver el título de la figura, haga clic para ver la figura en el contexto del artículo.

9. Sistema reproductivo (9)

9. Sistema reproductivo
Redactor del capítulo: Gracia Kawas Lemasters
Índice del contenido
Tablas y Figuras
Sistema Reproductivo: Introducción
Lowell E. Severo
Introducción a la función reproductiva masculina y femenina
Donald R Mattison
Sistema Reproductor Masculino y Toxicología
Steven Schrader y Grace Kawas Lemasters
Estructura del sistema reproductor femenino y vulnerabilidad de órganos diana
Donald R Mattison
Exposiciones ocupacionales maternas y resultados adversos del embarazo
Gracia Kawas Lemasters
Parto prematuro y trabajo
Nicole Mamelle
Exposición ocupacional y ambiental del recién nacido
Mary S. Wolff y Patrisha M. Woolard
Protección de la maternidad en la legislación
Marie-Claire Séguret
Recomendaciones para el embarazo y el trabajo en EE. UU.
leon j warshaw
Mesas
Haga clic en un enlace a continuación para ver la tabla en el contexto del artículo.
1. Exposiciones con múltiples criterios de valoración adversos
2. Estudios epidemiológicos de los efectos paternos en el resultado del embarazo
3. Tóxicos reproductivos femeninos potenciales
4. Definición de pérdida fetal y muerte infantil
5. Factores de pequeño para la edad gestacional y pérdida fetal
6. Fuentes identificadas de fatiga ocupacional
7. Riesgos relativos e índices de fatiga del parto prematuro
8. Riesgo de prematuridad por número de índices de fatiga laboral
9. Riesgos relativos y cambios en las condiciones de trabajo
10. Fuentes y niveles de exposición de los recién nacidos
Figuras
Apunte a una miniatura para ver el título de la figura, haga clic para ver la figura en el contexto del artículo.

10. Sistema respiratorio (18)

10. Sistema respiratorio
Editores de capítulos: Alois David y Gregory R. Wagner
Índice del contenido
Tablas y Figuras
Estructura y función
Morton Lippmann
Examen de función pulmonar
Ulf Ulfvarson y Monica Dahlqvist
Enfermedades Causadas por Irritantes Respiratorios y Químicos Tóxicos
David LS Ryon y William N. Rom
Asma ocupacional
George Friedman-Jiménez y Edward L. Petsonk
Enfermedades Causadas por Polvos Orgánicos
Ragnar Rylander y Richard SF Schilling
Enfermedad del berilio
Homayoun Kazemi
Neumoconiosis: Definición
alois david
Clasificación internacional de radiografías de neumoconiosis de la OIT
michel lesage
Etiopatogenia de las neumoconiosis
Patrick Sébastien y Raymond Bégin
Silicosis
John E. Parker y Gregory R. Wagner
Enfermedades pulmonares de los trabajadores del carbón
Michael D. Attfield, Edward L. Petsonk y Gregory R. Wagner
Enfermedades relacionadas con el asbesto
margaret r. becklake
Enfermedad del metal duro
Gerolamo Chiapino
Sistema respiratorio: la variedad de neumoconiosis
Steven R. Short y Edward L. Petsonk
Afección pulmonar obstructiva crónica
Kazimierz Marek y Jan E. Zejda
Efectos sobre la salud de las fibras artificiales
James E. Lockey y Clara S. Ross
Cáncer respiratorio
Paolo Boffetta y Elisabete Weiderpass
Infecciones pulmonares adquiridas en el trabajo
Anthony A. Marfin, Ann F. Hubbs, Karl J. Musgrave y John E. Parker
Mesas
Haga clic en un enlace a continuación para ver la tabla en el contexto del artículo.
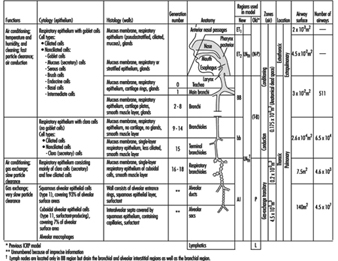
1. Regiones del tracto respiratorio y modelos de deposición de partículas
2. Criterios de polvo inhalable, torácico y respirable
3. Resumen de irritantes respiratorios
4. Mecanismos de lesión pulmonar por sustancias inhaladas
5. Compuestos capaces de toxicidad pulmonar
6. Definición de caso médico de asma ocupacional
7. Pasos en la evaluación diagnóstica del asma en el lugar de trabajo
8. Agentes sensibilizantes que pueden causar asma ocupacional
9. Ejemplos de fuentes de peligros de la exposición al polvo orgánico
10. Agentes en polvos orgánicos con actividad biológica potencial
11. Enfermedades inducidas por polvos orgánicos y sus códigos CIE
12. Criterios diagnósticos de bisinosis
13. Propiedades del berilio y sus compuestos
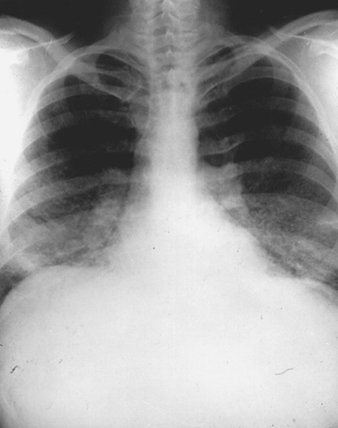
14. Descripción de las radiografías estándar
15. Clasificación OIT 1980: Radiografías de neumoconiosis
16. Enfermedades y condiciones relacionadas con el asbesto
17. Principales fuentes comerciales, productos y usos del asbesto
18. Prevalencia de la EPOC
19. Factores de riesgo implicados en la EPOC
20. Pérdida de la función ventilatoria
21. Clasificación diagnóstica, bronquitis crónica y enfisema
22. Pruebas de función pulmonar en la EPOC
23. Fibras sinteticas
24. Carcinógenos respiratorios humanos establecidos (IARC)
25. Carcinógenos respiratorios humanos probables (IARC)
26. Enfermedades infecciosas respiratorias adquiridas ocupacionalmente
Figuras
Apunte a una miniatura para ver el título de la figura, haga clic para ver la figura en el contexto del artículo.

11. Sistemas sensoriales (8)

11. Sistemas sensoriales
Redactor del capítulo: Heikki Savolainen
Índice del contenido
Tablas y Figuras
La oreja
Marcel-André Boillat
Trastornos auditivos inducidos químicamente
pedro jacobsen
Trastornos auditivos inducidos físicamente
Pedro L. Pelmear
equilibrio
lucy yardley
Visión y Trabajo
Paule Rey y Jean-Jacques Meyer
Sabor
Abril E. Mott y Norman Mann
Olor
Abril E. Mott
Receptores cutáneos
Robert Dykes y Daniel McBain
Mesas
Haga clic en un enlace a continuación para ver la tabla en el contexto del artículo.
1. Cálculo típico de la pérdida funcional de un audiograma
2. Requerimientos visuales para diferentes actividades.
3. Valores de iluminancia recomendados para el diseño de iluminación
4. Requisitos visuales para un permiso de conducir en Francia
5. Agentes/procesos reportados para alterar el sistema del gusto
6. Agentes/procesos asociados con anomalías olfativas
Figuras
Apunte a una miniatura para ver el título de la figura, haga clic para ver la figura en el contexto del artículo.

12. Enfermedades de la piel (7)

12. Enfermedades de la piel
Redactor del capítulo: Louis Philippe Durocher
Índice del contenido
Tablas y Figuras
Descripción general: Enfermedades profesionales de la piel
Donald J Birmingham
Cáncer de piel no melanocítico
Elisabete Weiderpass, Timo Partanen, Paolo Boffetta
Melanoma maligno
Timo Partanen, Paolo Boffetta, Elisabete Weiderpass
Dermatitis de contacto ocupacional
denis sasseville
Prevención de Dermatosis Laborales
Luis Felipe Durocher
Distrofia ungueal ocupacional
CD Calnan
Estigmas
H. Mierzecki
Mesas
Haga clic en un enlace a continuación para ver la tabla en el contexto del artículo.
1. Ocupaciones en riesgo
2. Tipos de dermatitis de contacto
3. Irritantes comunes
4. Alérgenos comunes de la piel
5. Factores predisponentes para la dermatitis ocupacional
6. Ejemplos de irritantes y sensibilizantes de la piel con ocupaciones
7. Dermatosis ocupacionales en Quebec en 1989
8. Factores de riesgo y sus efectos en la piel
9. Medidas colectivas (enfoque de grupo) para la prevención
Figuras
Apunte a una miniatura para ver el título de la figura, haga clic para ver la figura en el contexto del artículo.

13. Condiciones Sistémicas (3)

13. Condiciones Sistémicas
Redactor del capítulo: Howard M Kipen
Índice del contenido
Figuras
Condiciones Sistémicas: Una Introducción
Howard M Kipen
El síndrome del edificio enfermo
Michael J Hodgson
Sensibilidades químicas múltiples
marca r cullen
Figuras
Apunte a una miniatura para ver el título de la figura, haga clic para ver la figura en el contexto del artículo.
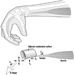
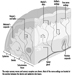
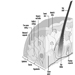
Estructura del sistema reproductor femenino y vulnerabilidad de órganos diana
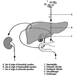
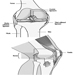
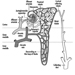
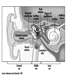
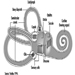
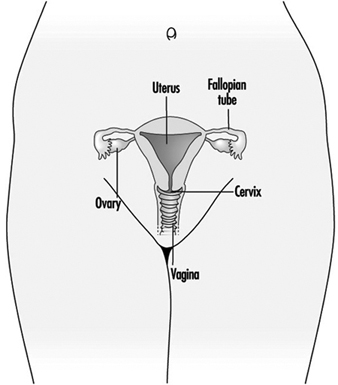
Figura 1. El aparato reproductor femenino.
El sistema reproductivo femenino está controlado por componentes del sistema nervioso central, incluidos el hipotálamo y la hipófisis. Está formado por los ovarios, las trompas de Falopio, el útero y la vagina (Figura 1). Los ovarios, las gónadas femeninas, son la fuente de ovocitos y también sintetizan y secretan estrógenos y progestágenos, las principales hormonas sexuales femeninas. Las trompas de Falopio transportan ovocitos y espermatozoides desde el útero. El útero es un órgano muscular en forma de pera, cuya parte superior se comunica a través de las trompas de Falopio con la cavidad abdominal, mientras que la parte inferior es contigua a través del estrecho canal del cuello uterino con la vagina, que pasa al exterior. La Tabla 1 resume los compuestos, las manifestaciones clínicas, el sitio y los mecanismos de acción de los posibles tóxicos para la reproducción.
Cuadro 1. Tóxicos potenciales para la reproducción femenina
| Compuesto | Manifestación clínica | Planta | Mecanismo/objetivo |
| Reaccion quimica | |||
| alquilante agentes |
menstruaciones alteradas Amenorrea atrofia ovárica Disminución de la fertilidad Menopausia prematura |
Ovario Útero |
Citotoxicidad de las células de la granulosa Citotoxicidad de ovocitos Citotoxicidad de células endometriales |
| Lidera | menstruaciones anormales atrofia ovárica Disminución de la fertilidad |
hipotálamo Pituitaria Ovario |
FSH disminuida Progesterona disminuida |
| Mercurio | menstruaciones anormales | hipotálamo Ovario |
Alteración de la producción y secreción de gonadotropinas Toxicidad folicular Proliferación de células de la granulosa |
| Cadmio | atresia folicular diestro persistente |
Ovario Pituitaria hipotálamo |
Toxicidad vascular Citotoxicidad de las células de la granulosa Citotoxicidad |
| similitud estructural | |||
| La azatioprina | Reducción del número de folículos | Ovario Ovogénesis |
Análogo de purina Interrupción de la síntesis de ADN/ARN |
| clordecona | Fertilidad deteriorada | hipotálamo | Agonista de estrógeno |
| DDT | menstruaciones alteradas | Pituitaria | Alteración de FSH, LH |
| 2,4-D | Esterilidad | ||
| Lindano | Amenorrea | ||
| Toxafeno | Hipermenorrea | ||
| PCB, PBB | menstruaciones anormales | Alteración de FSH, LH | |
Fuente: De Plowchalk, Meadows and Mattison 1992. Se sugiere que estos compuestos son tóxicos reproductivos de acción directa basados principalmente en pruebas de toxicidad en animales de experimentación.
El Hipotálamo y la Pituitaria
El hipotálamo se encuentra en el diencéfalo, que se asienta sobre el tronco encefálico y está rodeado por los hemisferios cerebrales. El hipotálamo es el principal intermediario entre los sistemas nervioso y endocrino, los dos principales sistemas de control del cuerpo. El hipotálamo regula la glándula pituitaria y la producción de hormonas.
Los mecanismos por los cuales una sustancia química puede alterar la función reproductiva del hipotálamo generalmente incluyen cualquier evento que pueda modificar la liberación pulsátil de la hormona liberadora de gonadotropina (GnRH). Esto puede implicar una alteración en la frecuencia o la amplitud de los pulsos de GnRH. Los procesos susceptibles de daño químico son los involucrados en la síntesis y secreción de GnRH, más específicamente, la transcripción o traducción, el empaquetamiento o transporte axonal y los mecanismos secretores. Estos procesos representan sitios donde los compuestos químicamente reactivos de acción directa podrían interferir con la síntesis hipotalámica o la liberación de GnRH. Una frecuencia o amplitud alterada de los pulsos de GnRH podría deberse a interrupciones en las vías de estimulación o inhibición que regulan la liberación de GnRH. Las investigaciones sobre la regulación del generador de pulsos de GnRH han demostrado que las catecolaminas, la dopamina, la serotonina, el ácido γ-aminobutírico y las endorfinas tienen cierto potencial para alterar la liberación de GnRH. Por lo tanto, los xenobióticos que son agonistas o antagonistas de estos compuestos podrían modificar la liberación de GnRH, interfiriendo así en la comunicación con la hipófisis.
La prolactina, la hormona estimulante del folículo (FSH) y la hormona luteinizante (LH) son tres hormonas proteicas secretadas por la pituitaria anterior que son esenciales para la reproducción. Estos juegan un papel fundamental en el mantenimiento del ciclo ovárico, controlando el reclutamiento y la maduración de los folículos, la esteroidogénesis, la finalización de la maduración del óvulo, la ovulación y la luteinización.
El control preciso y finamente ajustado del sistema reproductivo lo realiza la hipófisis anterior en respuesta a las señales de retroalimentación positivas y negativas de las gónadas. La liberación apropiada de FSH y LH durante el ciclo ovárico controla el desarrollo folicular normal, y la ausencia de estas hormonas es seguida por amenorrea y atrofia gonadal. Las gonadotropinas desempeñan un papel fundamental en el inicio de cambios en la morfología de los folículos ováricos y en sus microambientes esteroidales a través de la estimulación de la producción de esteroides y la inducción de poblaciones de receptores. La liberación oportuna y adecuada de estas gonadotropinas también es esencial para los eventos ovulatorios y una fase lútea funcional. Debido a que las gonadotropinas son esenciales para la función ovárica, la síntesis, el almacenamiento o la secreción alterados pueden alterar gravemente la capacidad reproductiva. La interferencia con la expresión génica, ya sea en la transcripción o la traducción, los eventos postraduccionales o el empaquetamiento o los mecanismos secretores, puede modificar el nivel de gonadotropinas que llegan a las gónadas. Las sustancias químicas que actúan por medio de la similitud estructural o la homeostasis endocrina alterada pueden producir efectos por interferencia con los mecanismos normales de retroalimentación. Los agonistas y antagonistas de los receptores de esteroides pueden iniciar una liberación inapropiada de gonadotropinas de la hipófisis, induciendo así enzimas metabolizadoras de esteroides, reduciendo la vida media de los esteroides y, posteriormente, el nivel circulante de esteroides que llega a la hipófisis.
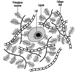
el ovario
El ovario en los primates es responsable del control de la reproducción a través de sus principales productos, los ovocitos y las hormonas esteroides y proteicas. La foliculogénesis, que implica mecanismos reguladores tanto intraováricos como extraováricos, es el proceso mediante el cual se producen ovocitos y hormonas. El ovario en sí tiene tres subunidades funcionales: el folículo, el ovocito y el cuerpo lúteo. Durante el ciclo menstrual normal, estos componentes, bajo la influencia de la FSH y la LH, funcionan en conjunto para producir un óvulo viable para la fertilización y un entorno adecuado para la implantación y la gestación subsiguiente.
Durante el período preovulatorio del ciclo menstrual, el reclutamiento y el desarrollo de los folículos ocurren bajo la influencia de la FSH y la LH. Este último estimula la producción de andrógenos por las células de la teca, mientras que el primero estimula la aromatización de andrógenos en estrógenos por parte de las células de la granulosa y la producción de inhibina, una hormona proteica. La inhibina actúa en la pituitaria anterior para disminuir la liberación de FSH. Esto evita la estimulación excesiva del desarrollo folicular y permite el desarrollo continuo del folículo dominante, el folículo destinado a ovular. La producción de estrógeno aumenta, estimulando tanto el pico de LH (que da como resultado la ovulación) como los cambios celulares y secretores en la vagina, el cuello uterino, el útero y el oviducto que mejoran la viabilidad y el transporte de los espermatozoides.
En la fase postovulatoria, las células de la teca y la granulosa que quedan en la cavidad folicular del óvulo ovulado forman el cuerpo lúteo y secretan progesterona. Esta hormona estimula el útero para proporcionar un entorno adecuado para la implantación del embrión si se produce la fertilización. A diferencia de la gónada masculina, la gónada femenina tiene un número finito de células germinales al nacer y, por lo tanto, es excepcionalmente sensible a los tóxicos para la reproducción. Tal exposición de la mujer puede conducir a una disminución de la fecundidad, un aumento de los embarazos perdidos, una menopausia precoz o infertilidad.
Como unidad reproductiva básica del ovario, el folículo mantiene el delicado entorno hormonal necesario para apoyar el crecimiento y la maduración de un ovocito. Como se señaló anteriormente, este proceso complejo se conoce como foliculogénesis e involucra la regulación tanto intraovárica como extraovárica. Numerosos cambios morfológicos y bioquímicos ocurren a medida que un folículo primordial progresa a un folículo preovulatorio (que contiene un ovocito en desarrollo), y cada etapa del crecimiento folicular exhibe patrones únicos de sensibilidad a las gonadotropinas, producción de esteroides y vías de retroalimentación. Estas características sugieren que hay varios sitios disponibles para la interacción xenobiótica. Además, existen diferentes poblaciones de folículos dentro del ovario, lo que complica aún más la situación al permitir la toxicidad diferencial de los folículos. Esto crea una situación en la que los patrones de infertilidad inducidos por un agente químico dependerían del tipo de folículo afectado. Por ejemplo, la toxicidad de los folículos primordiales no produciría signos inmediatos de infertilidad pero, en última instancia, acortaría la vida reproductiva. Por otro lado, la toxicidad para los folículos antrales o preovulatorios daría como resultado una pérdida inmediata de la función reproductiva. El complejo folicular está compuesto por tres componentes básicos: las células de la granulosa, las células de la teca y el ovocito. Cada uno de estos componentes tiene características que pueden hacerlo especialmente susceptible a daños químicos.
Varios investigadores han explorado la metodología para la selección de xenobióticos para la toxicidad de las células de la granulosa mediante la medición de los efectos sobre la producción de progesterona por parte de las células de la granulosa en cultivo. La supresión con estradiol de la producción de progesterona por parte de las células de la granulosa se ha utilizado para verificar la capacidad de respuesta de las células de la granulosa. El pesticida p,p'-DDT y su isómero o,p'-DDT producen la supresión de la producción de progesterona aparentemente con potencias iguales a las del estradiol. Por el contrario, los pesticidas malatión, aratión y dieldrín y el fungicida hexaclorobenceno no tienen efecto. Se necesita un análisis más detallado de las respuestas de las células de la granulosa aisladas a los xenobióticos para definir la utilidad de este sistema de ensayo. El atractivo de los sistemas aislados como este es la economía y la facilidad de uso; sin embargo, es importante recordar que las células de la granulosa representan solo un componente del sistema reproductivo.
Las células de la teca proporcionan precursores de los esteroides sintetizados por las células de la granulosa. Se cree que las células de la teca se reclutan a partir de las células del estroma ovárico durante la formación y el crecimiento del folículo. El reclutamiento puede implicar proliferación celular del estroma así como migración a regiones alrededor del folículo. Los xenobióticos que alteran la proliferación, migración y comunicación celular tendrán un impacto en la función celular de la teca. Los xenobióticos que alteran la producción de andrógenos tecales también pueden afectar la función del folículo. Por ejemplo, las células de la teca proporcionan los andrógenos metabolizados a estrógenos por las células de la granulosa. Se espera que las alteraciones en la producción de andrógenos de las células de la teca, ya sea aumentos o disminuciones, tengan un efecto significativo en la función del folículo. Por ejemplo, se cree que la producción excesiva de andrógenos por parte de las células de la teca provocará atresia folicular. Además, la producción deficiente de andrógenos por parte de las células de la teca puede conducir a una disminución de la producción de estrógenos por parte de las células de la granulosa. Cualquiera de las circunstancias tendrá un impacto claro en el desempeño reproductivo. Actualmente, se sabe poco sobre la vulnerabilidad de las células tecales a los xenobióticos.
Aunque existe una gran cantidad de información que define la vulnerabilidad de las células ováricas a los xenobióticos, existen datos que demuestran claramente que dichos agentes pueden dañar o destruir los ovocitos. Los agentes alquilantes destruyen los ovocitos en humanos y animales de experimentación. El plomo produce toxicidad ovárica. El mercurio y el cadmio también producen daño ovárico que puede estar mediado por la toxicidad de los ovocitos.
Fertilización a la Implantación
La gametogénesis, la liberación y la unión de células germinales masculinas y femeninas son todos eventos preliminares que conducen a un cigoto. Los espermatozoides depositados en la vagina deben ingresar al cuello uterino y moverse a través del útero y hacia la trompa de Falopio para encontrarse con el óvulo. la penetración del óvulo por el esperma y la fusión de su respectivo ADN comprenden el proceso de fertilización. Después de la fecundación se inicia la división celular y continúa durante los siguientes tres o cuatro días, formando una masa sólida de células llamada mórula. Las células de la mórula continúan dividiéndose y, cuando el embrión en desarrollo llega al útero, es una bola hueca llamada blastocisto.
Después de la fertilización, el embrión en desarrollo migra a través de la trompa de Falopio hacia el útero. El blastocisto ingresa al útero y se implanta en el endometrio aproximadamente siete días después de la ovulación. En este momento el endometrio se encuentra en la fase postovulatoria. La implantación permite que el blastocisto absorba nutrientes o sustancias tóxicas de las glándulas y los vasos sanguíneos del endometrio.
Exposiciones ocupacionales maternas y resultados adversos del embarazo
El empleo remunerado entre las mujeres está creciendo en todo el mundo. Por ejemplo, casi el 70% de las mujeres en los Estados Unidos están empleadas fuera del hogar durante sus años predominantes de procreación (de 20 a 34 años). Además, desde la década de 1940 ha habido una tendencia casi lineal en la producción de productos químicos orgánicos sintéticos, creando un ambiente más peligroso para la trabajadora embarazada y su descendencia.
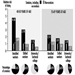
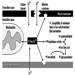
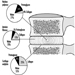
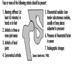
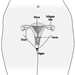
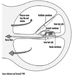
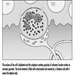
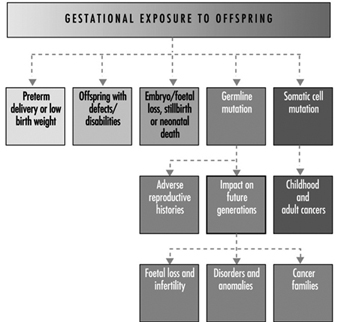
En última instancia, el éxito reproductivo de una pareja depende de un delicado equilibrio fisicoquímico dentro y entre el padre, la madre y el feto. Los cambios metabólicos que ocurren durante el embarazo pueden aumentar la exposición a sustancias tóxicas peligrosas tanto para la trabajadora como para el bebé. Estos cambios metabólicos incluyen aumento de la absorción pulmonar, aumento del gasto cardíaco, retraso en el vaciamiento gástrico, aumento de la motilidad intestinal y aumento de la grasa corporal. Como se muestra en la figura 1, la exposición del concetus puede producir efectos variables según la fase de desarrollo: embriogénesis temprana o tardía o período fetal.
Figura 1. Consecuencias de la exposición materna a tóxicos en la descendencia.
El tiempo de transporte de un óvulo fecundado antes de la implantación es de dos a seis días. Durante esta etapa temprana, el embrión puede estar expuesto a compuestos químicos que penetran en los fluidos uterinos. La absorción de compuestos xenófobos puede ir acompañada de cambios degenerativos, alteración del perfil de proteínas blastocísticas o fracaso del implante. El insulto durante este período es probable que conduzca a un aborto espontáneo. Sobre la base de datos experimentales, se cree que el embrión es bastante resistente a la agresión teratogénica en esta etapa temprana porque las células no han iniciado la compleja secuencia de diferenciación química.
El período de embriogénesis posterior se caracteriza por la diferenciación, movilización y organización de células y tejidos en rudimentos de órganos. La patogénesis temprana puede inducir la muerte celular, interacción celular fallida, biosíntesis reducida, movimiento morfogénico alterado, ruptura mecánica, adherencias o edema (Paul 1993). Los factores mediadores que determinan la susceptibilidad incluyen la vía y el nivel de exposición, el patrón de exposición y el genotipo materno y fetal. Los factores extrínsecos, como las deficiencias nutricionales o los efectos aditivos, sinérgicos o antagónicos asociados con exposiciones múltiples, pueden afectar aún más la respuesta. Las respuestas adversas durante la embriogénesis tardía pueden culminar en un aborto espontáneo, defectos estructurales graves, pérdida fetal, retraso del crecimiento o anomalías del desarrollo.
El período fetal se extiende desde la embriogénesis hasta el nacimiento y se define como comenzando entre los 54 y 60 días de gestación, y el concetus tiene una longitud corona-ron de 33 mm. La distinción entre el período embrionario y fetal es algo arbitraria. El período fetal se caracteriza desde el punto de vista del desarrollo por el crecimiento, la histogénesis y la maduración funcional. La toxicidad puede manifestarse por una reducción en el tamaño y número de células. El cerebro todavía es sensible a las lesiones; la mielinización es incompleta hasta después del nacimiento. El retraso del crecimiento, los defectos funcionales, la interrupción del embarazo, los efectos en el comportamiento, la carcinogénesis translacental o la muerte pueden resultar de la toxicidad durante el período fetal. Este artículo analiza los efectos biológicos, sociológicos y epidemiológicos de las exposiciones ambientales/ocupacionales maternas.
Pérdida embrionaria/fetal
Las etapas de desarrollo del cigoto, definidas en días desde la ovulación (DOV), proceden desde la etapa de blastocisto en los días 15 a 20 (uno a seis DOV), con la implantación en el día 20 o 21 (seis o siete DOV), hasta el período embrionario desde los días 21 a 62 (siete a 48 DOV), y el período fetal desde el día 63 (49+ DOV) hasta el período designado de viabilidad, que oscila entre 140 y 195 días. Las estimaciones de la probabilidad de interrupción del embarazo en una de estas etapas dependen tanto de la definición de pérdida fetal como del método utilizado para medir el evento. Existe una variabilidad considerable en la definición de pérdida fetal temprana versus tardía, que va desde el final de la semana 20 hasta la semana 28. Las definiciones de muerte fetal e infantil recomendadas por la Organización Mundial de la Salud (1977) se enumeran en la tabla 1. En los Estados Unidos Actualmente se acepta ampliamente que la edad gestacional que establece el límite inferior para los mortinatos es de 20 semanas.
Tabla 1. Definición de pérdida fetal y muerte infantil
| Aborto espontáneo | ≤500 g o 20-22 semanas o 25 cm de longitud |
| Nacimiento de un niño muerto | 500 g (1000 g Internacional) no viable |
| Muerte neonatal temprana | Muerte de un bebé nacido vivo ≤7 días (168 horas) |
| Muerte neonatal tardía | 7 días a ≤28 días |
Fuente: Organización Mundial de la Salud 1977.
Debido a que la mayoría de los fetos abortados tempranos tienen anomalías cromosómicas, se ha sugerido que para fines de investigación se debe hacer una distinción más precisa entre pérdida fetal temprana, antes de las 12 semanas de gestación, y pérdida fetal posterior (Källén 1988). Al examinar las pérdidas fetales tardías, también puede ser apropiado incluir las muertes neonatales tempranas, ya que la causa puede ser similar. La OMS define la muerte neonatal temprana como la muerte de un bebé de siete días o menos y la muerte neonatal tardía como la que ocurre entre los siete y los 29 días. En estudios realizados en países en desarrollo, es importante distinguir entre muertes preparto e intraparto. Debido a los partos problemáticos, las muertes intraparto representan una gran parte de los mortinatos en los países menos desarrollados.
En una revisión de Kline, Stein y Susser (1989) de nueve estudios retrospectivos o transversales, las tasas de pérdida fetal antes de las 20 semanas de gestación oscilaron entre 5.5 y 12.6%. Cuando se amplió la definición para incluir pérdidas hasta las 28 semanas de gestación, la tasa de pérdida fetal varió entre 6.2 y 19.6%. Sin embargo, las tasas de pérdida fetal entre embarazos reconocidos clínicamente en cuatro estudios prospectivos tenían un rango relativamente estrecho de 11.7 a 14.6% para el período gestacional de hasta 28 semanas. Esta tasa más baja, observada en diseños prospectivos versus retrospectivos o transversales, puede atribuirse a diferencias en las definiciones subyacentes, informes erróneos de abortos inducidos como espontáneos o clasificación errónea de menstruaciones retrasadas o abundantes como pérdida fetal.
Cuando se incluyen los abortos ocultos o las pérdidas “químicas” tempranas identificadas por un nivel elevado de gonadotrofinas coriónicas humanas (hCG), la tasa total de abortos espontáneos aumenta drásticamente. En un estudio que utilizó métodos de hCG, la incidencia de pérdida subclínica de óvulos fertilizados posterior a la implantación fue del 22% (Wilcox et al. 1988). En estos estudios, la hCG urinaria se midió con un ensayo inmunorradiométrico utilizando un anticuerpo de detección. El ensayo utilizado originalmente por Wilcox empleaba un anticuerpo de conejo policlonal de alta afinidad ahora extinto. Estudios más recientes han utilizado un anticuerpo monoclonal inagotable que requiere menos de 5 ml de orina para replicar las muestras. El factor limitante para el uso de estos ensayos en estudios de campo ocupacionales no es solo el costo y los recursos necesarios para coordinar la recolección, el almacenamiento y el análisis de las muestras de orina, sino también la gran población necesaria. En un estudio de pérdida temprana del embarazo en mujeres trabajadoras expuestas a terminales de visualización de video (VDT), se evaluaron aproximadamente 7,000 mujeres para adquirir una población utilizable de 700 mujeres. Esta necesidad de diez veces el tamaño de la población para lograr una muestra adecuada se deriva de la reducción en el número disponible de mujeres debido a la falta de elegibilidad debido a la edad, la esterilidad y la inscripción exclusivamente de mujeres que no usan anticonceptivos o que usan métodos anticonceptivos relativamente ineficaces. .
Los estudios ocupacionales más convencionales han utilizado datos registrados o de cuestionarios para identificar los abortos espontáneos. Las fuentes de datos registradas incluyen estadísticas vitales y registros de hospitales, médicos privados y clínicas ambulatorias. El uso de sistemas de registro identifica solo un subconjunto de todas las pérdidas fetales, principalmente aquellas que ocurren después del inicio de la atención prenatal, generalmente después de dos o tres períodos perdidos. Los datos del cuestionario se recopilan por correo o en entrevistas personales o telefónicas. Al entrevistar a las mujeres para obtener historias reproductivas, es posible una documentación más completa de todas las pérdidas reconocidas. Las preguntas que generalmente se incluyen en las historias reproductivas incluyen todos los resultados del embarazo; cuidado prenatal; antecedentes familiares de resultados adversos del embarazo; historia marital; Estados nutricionales; peso de reembarazo; altura; aumento de peso; consumo de cigarrillos, alcohol y medicamentos recetados y de venta libre; estado de salud de la madre durante y antes del embarazo; y exposiciones en el hogar y en el lugar de trabajo a agentes físicos y químicos tales como vibraciones, radiación, metales, solventes y pesticidas. Los datos de entrevistas sobre abortos espontáneos pueden ser una fuente válida de información, particularmente si el análisis incluye los de ocho semanas de gestación o más y los que ocurrieron en los últimos 10 años.
Los principales factores físicos, genéticos, sociales y ambientales asociados con el aborto espontáneo se resumen en la tabla 2. Para garantizar que la relación exposición-efecto observada no se deba a una relación de confusión con otro factor de riesgo, es importante identificar los factores de riesgo que puede estar asociado con el resultado de interés. Las condiciones asociadas con la pérdida fetal incluyen sífilis, rubéola, infecciones genitales por micolasma, herpes simple, infecciones uterinas e hiperpirexia general. Uno de los factores de riesgo más importantes para el aborto espontáneo clínicamente reconocido es un historial de embarazo que terminó en pérdida fetal. Una mayor gravidez se asocia con un mayor riesgo, pero esto puede no ser independiente de un historial de aborto espontáneo. Existen interpretaciones contradictorias de la gravidez como factor de riesgo debido a su asociación con la edad materna, el historial reproductivo y la heterogeneidad de las mujeres en diferentes rangos de gravidez. Las tasas de aborto espontáneo son más altas para las mujeres menores de 16 años y mayores de 36 años. Después de ajustar por gravedad y antecedentes de pérdida de embarazo, se demostró que las mujeres mayores de 40 años tenían el doble de riesgo de pérdida fetal que las mujeres más jóvenes. El mayor riesgo para las mujeres mayores se ha asociado con un aumento de las anomalías cromosómicas, en particular la trisomía. Recientemente se han revisado los posibles efectos masculinos asociados con la pérdida fetal (Savitz, Sonnerfeld y Olshaw 1994). Se mostró una relación más fuerte con la exposición paterna a mercurio y gases anestésicos, así como una relación sugerente pero inconsistente con la exposición al plomo, la fabricación de caucho, solventes seleccionados y algunos pesticidas.
Tabla 2. Factores asociados con pequeño para la edad gestacional y pérdida fetal
| Pequeño para Edad gestacional | |
| Físico-genético | Ambiental-social |
| Parto prematuro Nacimientos múltiples feto malformado Hipertensión Anomalía de la placenta o del cordón Historia médica materna Antecedentes de resultados adversos del embarazo. Carrera anomalías cromosómicas Sexo Altura materna, peso, aumento de peso Altura paterna Paridad Duración de la gestación Breve intervalo entre embarazos |
Desnutrición Bajos ingresos/mala educación Tabaquismo materno Consumo materno de alcohol Exposicion ocupacional Estrés psicosocial Altitud Historia de infecciones Consumo de marihuana |
| Pérdida fetal | |
| Físico-genético | Ambiental-social |
| Mayor gravidez Edad materna Orden de nacimiento Carrera Aborto espontáneo de repetición Diabetes dependiente de insulina Trastornos uterinos Hermanamiento Factor inmunológico Factores hormonales |
Estatus socioeconómico Historial de tabaquismo Medicamentos recetados y recreativos Consumo de alcohol La mala nutrición Infecciones/fiebre materna Espermicidas Factores de empleo Exposición a sustancias químicas Irradiación |
La situación laboral puede ser un factor de riesgo independientemente de un peligro físico o químico específico y puede actuar como factor de confusión en la evaluación de la exposición ocupacional y el aborto espontáneo. Algunos investigadores sugieren que las mujeres que permanecen en la fuerza laboral tienen más probabilidades de tener un historial de embarazo adverso y, como resultado, pueden continuar trabajando; otros creen que este grupo es una subpoblación inherentemente más en forma debido a mayores ingresos y mejor atención prenatal.
Anomalías congénitas
Durante los primeros 60 días después de la concepción, el bebé en desarrollo puede ser más sensible a los tóxicos xenobióticos que en cualquier otra etapa del ciclo de vida. Históricamente, las malformaciones terata y congénitas se referían a defectos estructurales presentados al nacer que pueden ser macroscópicos o microscópicos, internos o externos, hereditarios o no hereditarios, únicos o múltiples. Sin embargo, la anomalía congénita se define de manera más amplia como la que incluye el comportamiento, la función y la bioquímica anormales. Las malformaciones pueden ser únicas o múltiples; los defectos cromosómicos generalmente producen defectos múltiples, mientras que los cambios de un solo gen o la exposición a agentes ambientales pueden causar defectos únicos o un síndrome.
La incidencia de malformaciones depende del estado del concetus: nacido vivo, aborto espontáneo, muerte fetal. En general, la tasa de anomalías en los abortos espontáneos es de aproximadamente el 19%, un aumento diez veces superior al observado en los nacidos vivos (Sheard, Fantel y Fitsimmons 1989). Se encontró una tasa de anomalías del 32% entre los fetos nacidos muertos que pesaban más de 500 g. La incidencia de defectos importantes en los nacidos vivos es de alrededor del 2.24% (Nelson y Holmes 1989). La prevalencia de defectos menores oscila entre el 3 y el 15% (con una media del 10%). Las anomalías congénitas están asociadas a factores genéticos (10.1 %), herencia multifactorial (23 %), factores uterinos (2.5 %), gemelos (0.4 %) o teratógenos (3.2 %). Se desconocen las causas de los defectos restantes. Las tasas de malformación son aproximadamente un 41% más altas para los niños que para las niñas y esto se explica por la tasa significativamente más alta de anomalías en los órganos genitales masculinos.
Un desafío en el estudio de las malformaciones es decidir cómo agrupar los defectos para el análisis. Las anomalías se pueden clasificar según varios parámetros, incluida la gravedad (mayor, menor), la patogenia (deformación, alteración), asociadas frente a aisladas, anatómicas por sistema de órganos y etiológicas (p. ej., defectos cromosómicos, de un solo gen o inducidos por teratógenos). A menudo, todas las malformaciones se combinan o la combinación se basa en una categorización mayor o menor. Una malformación mayor se puede definir como aquella que causa la muerte, requiere cirugía o tratamiento médico o constituye una discapacidad física o psicológica sustancial. La justificación para combinar anomalías en grandes grupos es que la mayoría surgen, aproximadamente en el mismo período de tiempo, durante la organogénesis. Por lo tanto, al mantener tamaños de muestra más grandes, el número total de casos aumenta con un aumento concomitante en el poder estadístico. Sin embargo, si el efecto de la exposición es específico para un tipo particular de malformación (p. ej., sistema nervioso central), dicha agrupación puede enmascarar el efecto. Alternativamente, las malformaciones pueden agruparse por sistema de órganos. Aunque este método puede ser una mejora, ciertos defectos pueden dominar la clase, como las deformidades en varo de los pies en el sistema musculoesquelético. Dada una muestra lo suficientemente grande, el enfoque óptimo es dividir los defectos en grupos homogéneos desde el punto de vista embriológico o patogénico (Källén 1988). Se debe considerar la exclusión o inclusión de ciertas malformaciones, como aquellas que probablemente sean causadas por defectos cromosómicos, condiciones autosómicas dominantes o mala posición en el útero. En última instancia, al analizar anomalías congénitas, se debe mantener un equilibrio entre mantener la precisión y comprometer el poder estadístico.
Varios tóxicos ambientales y ocupacionales se han asociado con anomalías congénitas en la descendencia. Una de las asociaciones más fuertes es el consumo materno de alimentos contaminados con metilmercurio que causa anomalías morfológicas, del sistema nervioso central y neuroconductuales. En Japón, el grupo de casos estuvo relacionado con el consumo de pescados y mariscos contaminados con mercurio derivado del efluente de una fábrica química. La descendencia más severamente afectada desarrolló parálisis cerebral. La ingestión materna de bifenilos policlorados (CB) del aceite de arroz contaminado dio lugar a bebés con varios trastornos, que incluyen retraso del crecimiento, pigmentación de la piel de color marrón oscuro, erupción temprana de los dientes, hiperplasia gingival, sutura sagital ancha, edema facial y exoftalmosis. Las ocupaciones que involucran exposiciones a mezclas se han relacionado con una variedad de resultados adversos. Los hijos de mujeres que trabajaban en la industria de ul y aer, ya sea en trabajos de laboratorio o trabajos que implicaban "conversiones" o refinamiento de aer, también tenían un mayor riesgo de defectos en el sistema nervioso central, corazón y hendiduras orales. Las mujeres que trabajaban en trabajos industriales o de construcción con exposiciones no especificadas tenían un aumento del 50 % en los defectos del sistema nervioso central, y las mujeres que trabajaban en el transporte y la comunicación tenían el doble de riesgo de tener un hijo con fisura oral. Los veterinarios representan un grupo único de personal de atención médica expuesto a gases anestésicos, radiación, trauma por patadas de animales, insecticidas y enfermedades zoonóticas. Aunque no se encontraron diferencias en la tasa de abortos espontáneos o en el peso al nacer de las crías entre las veterinarias y las abogadas, hubo un exceso significativo de defectos de nacimiento entre las veterinarias (Schenker et al. 1990). Están disponibles listas de teratógenos conocidos, posibles e improbables, así como bases de datos informáticas y líneas de riesgo para obtener información actual sobre teratógenos potenciales (Paul 1993). Sin embargo, la evaluación de anomalías congénitas en una cohorte ocupacional es particularmente difícil debido al gran tamaño de muestra necesario para el poder estadístico y nuestra capacidad limitada para identificar exposiciones específicas que ocurren durante un período de tiempo estrecho, principalmente los primeros 55 días de gestación.
Pequeño para Edad gestacional
Entre los múltiples factores relacionados con la supervivencia infantil, el subdesarrollo físico asociado al bajo peso al nacer (BPN) presenta uno de los mayores riesgos. El aumento de peso significativo del feto no comienza hasta el segundo trimestre. El concetus pesa 1 g a las ocho semanas, 14 g a las 12 semanas y alcanza 1.1 kg a las 28 semanas. A partir de entonces, se ganan 1.1 kg adicionales cada seis semanas hasta el término. El recién nacido normal pesa aproximadamente 3,200 g a término. El peso del recién nacido depende de su tasa de crecimiento y de su edad gestacional al momento del parto. Se dice que un bebé con retraso en el crecimiento es pequeño para la edad gestacional (SGA). Si un bebé nace antes del término, tendrá un peso reducido pero no necesariamente un retraso en el crecimiento. Los factores asociados con un parto prematuro se analizan en otra parte, y el enfoque de esta discusión es sobre el recién nacido con retraso en el crecimiento. Los términos SGA y LBW se usarán indistintamente. Un recién nacido de bajo peso al nacer se define como un recién nacido que pesa menos de 2,500 g, un peso muy bajo al nacer se define como menos de 1,500 g y un peso extremadamente bajo al nacer es aquel que pesa menos de 1,000 g (OMS 1969).
Al examinar las causas de la reducción del crecimiento, es importante distinguir entre el retraso del crecimiento asimétrico y simétrico. El retraso del crecimiento asimétrico, es decir, donde el peso se ve más afectado que la estructura esquelética, se asocia principalmente con un factor de riesgo que opera durante la última etapa del embarazo. Por otro lado, es más probable que el retraso del crecimiento simétrico esté asociado con una etiología que opera durante todo el período de gestación (Kline, Stein y Susser 1989). La diferencia en las tasas entre el retraso del crecimiento asimétrico y simétrico es especialmente evidente cuando se comparan países en desarrollo y desarrollados. La tasa de retraso del crecimiento en los países en desarrollo es del 10 al 43% y es principalmente simétrica, siendo el factor de riesgo más importante la mala alimentación. En los países desarrollados el retraso del crecimiento fetal suele ser mucho menor, del 3 al 8%, y generalmente es asimétrico con una etiología multifactorial. Por lo tanto, en todo el mundo, la proporción de bebés con bajo peso al nacer definidos como retraso del crecimiento intrauterino en lugar de prematuros varía drásticamente. En Suecia y Estados Unidos, la proporción es de aproximadamente 45%, mientras que en países en desarrollo, como India, la proporción varía entre 79 y 96% aproximadamente (Villar y Belizan 1982).
Los estudios de la hambruna holandesa mostraron que la inanición limitada al tercer trimestre deprimió el crecimiento fetal en un patrón asimétrico, siendo el peso al nacer el principal afectado y el perímetro cefálico el menos afectado (Stein, Susser y Saenger 1975). La asimetría del crecimiento también se ha observado en estudios de exposiciones ambientales. En un estudio de 202 mujeres embarazadas que residían en vecindarios con alto riesgo de exposición al plomo, se recolectaron muestras de sangre materna prenatal entre la sexta y la semana 28 de gestación (Bornschein, Grote y Mitchell 1989). Los niveles de plomo en la sangre se asociaron con una disminución del peso y la longitud al nacer, pero no con la circunferencia de la cabeza, después de ajustar otros factores de riesgo relevantes, como la duración de la gestación, el nivel socioeconómico y el consumo de alcohol o cigarrillos. El hallazgo de plomo en la sangre materna como factor de la longitud al nacer se observó por completo en bebés caucásicos. La longitud al nacer de los bebés caucásicos disminuyó aproximadamente 2.5 cm por unidad logarítmica de plomo en la sangre materna. Se debe tener cuidado con la selección de la variable de resultado. Si solo se hubiera seleccionado el peso al nacer para el estudio, se podría haber pasado por alto el hallazgo de los efectos del plomo en otros parámetros de crecimiento. Además, si los caucásicos y los afroamericanos se hubieran agrupado en el análisis anterior, es posible que se hayan pasado por alto los efectos diferenciales en los caucásicos, quizás debido a las diferencias genéticas en la capacidad de almacenamiento y unión del plomo. También se observó un efecto de confusión significativo entre el plomo en sangre prenatal y la edad materna y el peso al nacer de la descendencia después del ajuste por otras covariables. Los hallazgos indican que para una mujer de 30 años con un nivel estimado de plomo en la sangre de alrededor de 20 mg/dl, la descendencia pesó aproximadamente 2,500 g en comparación con aproximadamente 3,000 g para una mujer de 20 años con niveles similares de plomo. Los investigadores especularon que esta diferencia observada puede indicar que las mujeres mayores son más sensibles al insulto adicional de la exposición al plomo o que las mujeres mayores pueden haber tenido una mayor carga total de plomo debido a una mayor cantidad de años de exposición o niveles ambientales de plomo más altos cuando eran niñas. Otro factor puede ser el aumento de la presión arterial. No obstante, la lección importante es que puede ser necesario un examen cuidadoso de las subpoblaciones de alto riesgo por edad, raza, situación económica, hábitos de vida diarios, sexo de la descendencia y otras diferencias genéticas para descubrir los efectos más sutiles de las exposiciones en el crecimiento fetal. y desarrollo.
Los factores de riesgo asociados con el bajo peso al nacer se resumen en la Tabla 5. La clase social medida por ingresos o educación persiste como factor de riesgo en situaciones en las que no existen diferencias étnicas. Otros factores que pueden estar operando bajo la clase social o la raza pueden incluir el tabaquismo, el trabajo físico, el cuidado prenatal y la nutrición. Las mujeres entre las edades de 25 y 29 años tienen menos probabilidades de dar a luz a una descendencia con retraso en el crecimiento. El tabaquismo materno aumenta el riesgo de descendencia con bajo peso al nacer en aproximadamente un 200% para las fumadoras empedernidas. Las condiciones médicas maternas asociadas con el bajo peso al nacer incluyen anomalías placentarias, enfermedades cardíacas, neumonía viral, enfermedades hepáticas, reeclamsia, eclamsia, hipertensión crónica, aumento de peso e hiéremesis. Un historial de embarazo adverso de pérdida fetal, parto prematuro o recién nacido con bajo peso al nacer aumenta de dos a cuatro veces el riesgo de un recién nacido prematuro actual con bajo peso al nacer. Un intervalo entre nacimientos de menos de un año triplica el riesgo de tener un hijo con bajo peso al nacer. Las anomalías cromosómicas asociadas con el crecimiento anormal incluyen el síndrome de Down, la trisomía 18 y la mayoría de los síndromes de malformación.
Fumar cigarrillos es uno de los principales comportamientos más directamente relacionados con una descendencia de menor peso. Se ha demostrado que el tabaquismo materno durante el embarazo aumenta de dos a tres veces el riesgo de un hijo con bajo peso al nacer y provoca un déficit de peso general de entre 150 y 400 g. La nicotina y el monóxido de carbono se consideran los agentes causales más probables, ya que ambos se transfieren rápida y referencialmente a través de la placenta. La nicotina es un potente vasoconstrictor y se han demostrado diferencias significativas en el tamaño de los vasos umbilicales de madres fumadoras. Los niveles de monóxido de carbono en el humo del cigarrillo oscilan entre 20,000 60,000 y 210 XNUMX m. El monóxido de carbono tiene una afinidad por la hemoglobina XNUMX veces mayor que la del oxígeno y, debido a la menor tensión arterial de oxígeno, el feto está especialmente comprometido. Otros han sugerido que estos efectos no se deben al tabaquismo sino que son atribuibles a las características de los fumadores. Ciertamente, las ocupaciones con exposición potencial al monóxido de carbono, como las asociadas con ul y aer, altos hornos, acetileno, cervecerías, negro de humo, hornos de coque, garajes, sintetizadores de productos químicos orgánicos y refinerías de petróleo deben considerarse posibles ocupaciones de alto riesgo para las empleadas embarazadas.
El etanol también es un agente ampliamente utilizado e investigado asociado con el retraso del crecimiento fetal (así como con anomalías congénitas). En un estudio prospectivo de 9,236 nacimientos, se encontró que el consumo materno de alcohol de más de 1.6 oz por día se asoció con un aumento de mortinatos y bebés con retraso en el crecimiento (Kaminski, Rumeau y Schwartz 1978). La longitud y el perímetro cefálico más pequeños del lactante también están relacionados con la ingestión materna de alcohol.
Al evaluar los posibles efectos de las exposiciones sobre el peso al nacer, se deben considerar algunas cuestiones problemáticas. el parto prematuro se debe considerar como un posible resultado mediador y se deben considerar los efectos potenciales sobre la edad gestacional. Además, los embarazos que tienen una duración gestacional más larga también tienen una mayor oportunidad de exposición. Si suficientes mujeres trabajan al final del embarazo, la exposición acumulada más prolongada puede estar asociada con las edades gestacionales más avanzadas y los bebés más pesados simplemente como un artefacto. Hay una serie de procedimientos que se pueden utilizar para superar este problema, incluida una variante del modelo de regresión de tabla de vida de Cox, que tiene la capacidad de manejar covariables dependientes del tiempo.
Otro problema se centra en cómo definir el bajo peso al nacer. A menudo, los estudios definen el bajo peso al nacer como una variable dicotómica, menos de 2,500 g. La exposición, sin embargo, debe tener un efecto muy poderoso para producir una caída drástica en el peso del bebé. El peso al nacer definido como una variable continua y analizado en un modelo de regresión múltiple es más sensible para detectar efectos sutiles. La escasez relativa de hallazgos significativos en la literatura en relación con las exposiciones ocupacionales y los bebés SGA puede, en el arte, deberse a que se ignoran estos problemas de diseño y análisis.
Conclusiones
Los estudios de resultados adversos del embarazo deben caracterizar las exposiciones durante un período de tiempo bastante estrecho. Si la mujer ha sido transferida a otro trabajo o despedida durante un período de tiempo crítico como la organogénesis, la relación exposición-efecto puede verse severamente alterada. Por lo tanto, el investigador debe cumplir con un alto estándar para identificar la exposición de la mujer durante un período de tiempo pequeño y crítico en comparación con otros estudios de enfermedades crónicas, donde los errores de unos pocos meses o incluso años pueden tener un impacto mínimo.
El retraso del crecimiento uterino, las anomalías congénitas y los abortos espontáneos se evalúan con frecuencia en los estudios de exposición ocupacional. Hay más de un enfoque disponible para evaluar cada resultado. Estos puntos finales son de importancia para la salud pública debido a los costos psicológicos y financieros. En general, se ha observado falta de especificidad en las relaciones exposición-resultado, por ejemplo, con la exposición al plomo, gases anestésicos y solventes. Debido al potencial de falta de especificidad en la relación exposición-efecto, los estudios deben diseñarse para evaluar varios criterios de valoración asociados con una gama de posibles mecanismos.
Parto prematuro y trabajo
La conciliación del trabajo y la maternidad es un importante problema de salud pública en los países industrializados, donde más del 50% de las mujeres en edad fértil trabajan fuera del hogar. Las mujeres trabajadoras, los sindicatos, los empleadores, los políticos y los médicos están buscando formas de prevenir resultados reproductivos desfavorables inducidos por el trabajo. Las mujeres quieren seguir trabajando durante el embarazo, e incluso pueden considerar que los consejos de su médico sobre modificaciones en el estilo de vida durante el embarazo son sobreprotectores e innecesariamente restrictivos.
Consecuencias fisiológicas del embarazo
En este punto, sería útil revisar algunas de las consecuencias fisiológicas del embarazo que pueden interferir con el trabajo.
La mujer embarazada sufre profundos cambios que le permiten adaptarse a las necesidades del feto. La mayoría de estos cambios implican la modificación de funciones fisiológicas que son sensibles a los cambios de postura o actividad física: el sistema circulatorio, el sistema respiratorio y el equilibrio hídrico. Como resultado, las mujeres embarazadas físicamente activas pueden experimentar reacciones fisiológicas y fisiopatológicas únicas.
Las principales modificaciones fisiológicas, anatómicas y funcionales que experimenta la mujer embarazada son (Mamelle et al. 1982):
- Un aumento en la demanda periférica de oxígeno, lo que lleva a la modificación de los sistemas respiratorio y circulatorio. El volumen corriente comienza a aumentar en el tercer mes y puede ascender al 40% de los valores de reembarazo al final del embarazo. El aumento resultante en el intercambio de gases puede aumentar el peligro de la inhalación de volátiles tóxicos, mientras que la hiperventilación relacionada con el aumento del volumen corriente puede causar dificultad para respirar con el esfuerzo.
- El gasto cardíaco aumenta desde el comienzo del embarazo, como resultado de un aumento en el volumen de sangre. Esto reduce la capacidad del corazón para adaptarse al esfuerzo y también aumenta la presión venosa en las extremidades inferiores, lo que dificulta estar de pie durante largos períodos.
- Las modificaciones anatómicas durante el embarazo, incluida la exageración de la lordosis dorsolumbar, la ampliación del polígono de apoyo y los aumentos del volumen abdominal, afectan las actividades estáticas.
- Una variedad de otras modificaciones funcionales ocurren durante el embarazo. Las náuseas y los vómitos provocan fatiga; la somnolencia diurna produce falta de atención; los cambios de humor y los sentimientos de ansiedad pueden conducir a conflictos interpersonales.
- Finalmente, es interesante señalar que los requerimientos energéticos diarios durante el embarazo equivalen a los requerimientos de dos a cuatro horas de trabajo.
Debido a estos profundos cambios, las exposiciones ocupacionales pueden tener consecuencias especiales en mujeres embarazadas y pueden resultar en resultados desfavorables en el embarazo.
Estudios Epidemiológicos de Condiciones Laborales y Parto Pretérmino
Aunque hay muchos posibles resultados desfavorables del embarazo, aquí revisamos los datos sobre el parto prematuro, definido como el nacimiento de un niño antes de la semana 37 de gestación. el parto prematuro se asocia con bajo peso al nacer y con importantes complicaciones para el recién nacido. Sigue siendo un importante problema de salud pública y es una reocupación constante entre los obstetras.
Cuando comenzamos la investigación en este campo a mediados de la década de 1980, había una protección legislativa relativamente fuerte de la salud de las mujeres embarazadas en Francia, con la licencia de maternidad prenatal obligatoria para comenzar seis semanas antes de la fecha prevista. Aunque la tasa de parto prematuro ha caído del 10 al 7 % desde entonces, parece haberse estabilizado. Debido a que la prevención médica aparentemente había llegado al límite de sus poderes, investigamos los factores de riesgo susceptibles de intervención social. Nuestras hipótesis fueron las siguientes:
- ¿Es el trabajo per se un factor de riesgo de parto prematuro?
- ¿Ciertas ocupaciones están asociadas con un mayor riesgo de parto prematuro?
- ¿Constituyen ciertas condiciones de trabajo un peligro para la mujer embarazada y el feto?
- ¿Existen medidas de prevención social que podrían ayudar a reducir el riesgo de parto prematuro?
Nuestro primer estudio, realizado entre 1977 y 78 en dos salas de maternidad de un hospital, examinó a 3,400 mujeres, de las cuales 1,900 trabajaron durante el embarazo y 1,500 permanecieron en casa (Mamelle, Laumon y Lazar 1984). Las mujeres fueron entrevistadas inmediatamente después del parto y se les pidió que describieran su estilo de vida en el hogar y el trabajo durante el embarazo con la mayor precisión posible.
Obtuvimos los siguientes resultados:
Trabajo per se
El mero hecho de trabajar fuera de casa no puede considerarse un factor de riesgo de parto prematuro, ya que las mujeres que se quedan en casa presentan una tasa de prematuridad mayor que las mujeres que trabajan fuera de casa (7.2 frente a 5.8%).
Las condiciones de trabajo
Una semana de trabajo excesivamente larga parece ser un factor de riesgo, ya que hubo un aumento regular en la tasa de parto prematuro con el número de horas de trabajo. Los trabajadores del sector minorista, los trabajadores sociales médicos, los trabajadores especializados y el personal de servicio tenían un mayor riesgo de parto prematuro que los trabajadores de oficina, los maestros, la gerencia, los trabajadores calificados o los supervisores. Las tasas de prematuridad en los dos grupos fueron 8.3 y 3.8% respectivamente.
Tabla 1. Fuentes de fatiga laboral identificadas
| Índice de fatiga laboral | Índice “ALTO” si: |
| Postura | De pie más de 3 horas al día |
| trabajar en maquinas | Trabajo en cintas transportadoras industriales; trabajo independiente en máquinas industriales con gran esfuerzo |
| Carga fisica | Esfuerzo físico continuo o periódico; transportar cargas de más de 10 kg |
| carga mental | Trabajo rutinario; tareas variadas que requieren poca atención sin estimulación |
| Entorno | Nivel de ruido significativo; temperatura fría; ambiente muy húmedo; manipulación de sustancias químicas |
Fuente: Mamelle, Laumon y Lazar 1984.
El análisis de tareas permitió identificar cinco fuentes de fatiga ocupacional: postura, trabajo con máquinas industriales, carga de trabajo física, carga de trabajo mental y ambiente de trabajo. Cada una de estas fuentes de fatiga ocupacional constituye un factor de riesgo de parto prematuro (ver tablas 1 y 2).
Tabla 2. Riesgos relativos (RR) e índices de fatiga del parto prematuro
| Home | Índice bajo % | Índice alto % | RR | Significancia estadística |
| Postura | 4.5 | 7.2 | 1.6 | Significativo |
| trabajar en maquinas | 5.6 | 8.8 | 1.6 | Significativo |
| Carga fisica | 4.1 | 7.5 | 1.8 | Altamente significativa |
| carga mental | 4.0 | 7.8 | 2.0 | Altamente significativa |
| Entorno | 4.9 | 9.4 | 1.9 | Altamente significativa |
Fuente: Mamelle, Laumon y Lazar 1984.
La exposición a múltiples fuentes de fatiga puede generar resultados desfavorables en el embarazo, como lo demuestra el aumento significativo de la tasa de partos prematuros con un mayor número de fuentes de fatiga (tabla 3). Por lo tanto, el 20 % de las mujeres tuvo una exposición concomitante a al menos tres fuentes de fatiga y experimentó una tasa de parto prematuro dos veces mayor que otras mujeres. La fatiga ocupacional y las semanas de trabajo excesivamente largas ejercen efectos acumulativos, de modo que las mujeres que experimentan fatiga intensa durante largas semanas de trabajo presentan una tasa de prematuridad aún mayor. las tasas de parto prematuro aumentan aún más si la mujer también tiene un factor de riesgo médico. Por lo tanto, la detección de la fatiga ocupacional es incluso más importante que la detección de factores de riesgo médicos.
Tabla 3. Riesgo relativo de prematuridad según número de índices de fatiga laboral
| Número de alto índices de fatiga |
Proporción de mujeres expuestas % |
Estimado riesgo relativo |
| 0 | 24 | 1.0 |
| 1 | 28 | 2.2 |
| 2 | 25 | 2.4 |
| 3 | 15 | 4.1 |
| 4 - 5 | 8 | 4.8 |
Fuente: Mamelle, Laumon y Lazar 1984
Los estudios europeos y norteamericanos han confirmado nuestros resultados, y se ha demostrado que nuestra escala de fatiga es reproducible en otras encuestas y países.
En un estudio de seguimiento de casos y controles realizado en Francia unos años más tarde en las mismas salas de maternidad (Mamelle y Muñoz 1987), sólo dos de los cinco índices de fatiga definidos anteriormente estaban significativamente relacionados con el parto prematuro. Sin embargo, cabe señalar que las mujeres tuvieron más oportunidades de sentarse y se retiraron de las tareas físicamente exigentes como resultado de las medidas preventivas implementadas en los lugares de trabajo durante este período. No obstante, la escala de fatiga siguió siendo un predictor de parto prematuro en este segundo estudio.
En un estudio en Montreal, Quebec (McDonald et al. 1988), se entrevistó retrospectivamente a 22,000 mujeres embarazadas acerca de sus condiciones de trabajo. Se demostró que las largas semanas de trabajo, el trabajo en turnos alternos y el transporte de cargas pesadas ejercen efectos significativos. Los otros factores estudiados no parecen estar relacionados con el parto prematuro, aunque parece haber una asociación significativa entre el parto prematuro y una escala de fatiga basada en el número total de fuentes de fatiga.
Con la excepción del trabajo con máquinas industriales, no se encontró una asociación significativa entre las condiciones de trabajo y el parto prematuro en un estudio retrospectivo francés de una muestra representativa de 5,000 mujeres embarazadas (Saurel-Cubizolles y Kaminski 1987). Sin embargo, se encontró que una escala de fatiga inspirada en la nuestra estaba significativamente asociada con el parto prematuro.
En los Estados Unidos, Homer, Beredford y James (1990), en un estudio de cohortes históricas, confirmaron la asociación entre la carga de trabajo físico y un mayor riesgo de parto prematuro. Teitelman y colaboradores (1990), en un estudio prospectivo de 1,200 mujeres embarazadas, cuyo trabajo se clasificó como sedentario, activo o de pie, sobre la base de la descripción del trabajo, demostraron una asociación entre el trabajo de pie y el parto prematuro.
Barbara Luke y colaboradores (en prensa) realizaron un estudio retrospectivo de enfermeras estadounidenses que trabajaron durante el embarazo. Utilizando nuestra escala de riesgo laboral, obtuvo resultados similares a los nuestros, es decir, una asociación entre parto prematuro y largas jornadas de trabajo, trabajo de pie, gran carga de trabajo y ambiente de trabajo desfavorable. Además, el riesgo de parto prematuro fue significativamente mayor entre las mujeres con exposición concomitante a tres o cuatro fuentes de fatiga. Cabe señalar que este estudio incluyó a más de la mitad de todas las enfermeras en los Estados Unidos.
Sin embargo, se han informado resultados contradictorios. Esto puede deberse a tamaños de muestra pequeños (Berkowitz 1981), diferentes definiciones de prematuramente (Launer et al. 1990) y clasificación de las condiciones de trabajo sobre la base de la descripción del trabajo en lugar del análisis del puesto de trabajo real (Klebanoff, Shiono y Carey 1990). En algunos casos, las estaciones de trabajo han sido caracterizadas únicamente sobre una base teórica, por ejemplo, por el médico ocupacional, en lugar de por las propias mujeres (peoples-Shes et al. 1991). Creemos que es importante tener en cuenta la fatiga subjetiva, es decir, la fatiga tal como la describen y experimentan las mujeres, en los estudios.
Finalmente, es posible que los resultados negativos estén relacionados con la implementación de medidas preventivas. Este fue el caso del estudio prospectivo de Ahlborg, Bodin y Hogstedt (1990), en el que 3,900 mujeres suecas activas completaron un cuestionario autoadministrado en su primera visita prenatal. El único factor de riesgo informado para el parto prematuro fue transportar cargas que pesaban más de 12 kg más de 50 veces por semana, e incluso entonces el riesgo relativo de 1.7 no fue significativo. El propio Ahlborg señala que se han implementado medidas preventivas en forma de ayudas a la licencia por maternidad y el derecho a realizar un trabajo menos agotador durante los dos meses posteriores a la fecha prevista para las mujeres embarazadas que realizan trabajos agotadores. Las licencias por maternidad eran cinco veces más frecuentes entre las mujeres que describían su trabajo como agotador y que implicaba el transporte de cargas pesadas. Ahlborg concluye que el riesgo de parto prematuro puede haberse minimizado con estas medidas preventivas.
Intervenciones preventivas: ejemplos en francés
¿Son los resultados de los estudios etiológicos suficientemente convincentes para aplicar y evaluar intervenciones preventivas? La primera pregunta que debe responderse es si existe una justificación de salud pública para la aplicación de medidas preventivas sociales diseñadas para reducir la tasa de parto prematuro.
Usando datos de nuestros estudios previos, hemos estimado la proporción de nacimientos prematuros causados por factores ocupacionales. Asumiendo una tasa de parto prematuro del 10% en poblaciones expuestas a fatiga intensa y una tasa de 4.5% en poblaciones no expuestas, estimamos que el 21% de los partos prematuros son causados por factores ocupacionales. Por lo tanto, reducir la fatiga laboral podría resultar en la eliminación de una quinta parte de todos los partos prematuros en mujeres trabajadoras francesas. Esta es una amplia justificación para la implementación de medidas de prevención social.
¿Qué medidas preventivas se pueden aplicar? Los resultados de todos los estudios llevan a la conclusión de que se pueden reducir las horas de trabajo, se puede disminuir la fatiga mediante la modificación del puesto de trabajo, se pueden permitir las pausas en el trabajo y se puede alargar la licencia prenatal. Hay tres alternativas de costo equivalente disponibles:
- reducción de la semana laboral a 30 horas a partir de la semana 20 de gestación
- prescribir un descanso laboral de una semana cada mes a partir de la semana 20 de gestación
- comenzando la licencia prenatal a las 28 semanas de gestación.
Es relevante recordar aquí que la legislación francesa prevé las siguientes medidas preventivas para las mujeres embarazadas:
- empleo garantizado después del parto
- reducción de la jornada laboral de 30 a 60 minutos, aplicada a través de convenios colectivos
- modificación del puesto de trabajo en casos de incompatibilidad con el embarazo
- pausas laborales durante el embarazo, prescritas por los médicos tratantes
- licencia de maternidad prenatal seis semanas antes de la fecha de parto, con dos semanas adicionales disponibles en caso de complicaciones
- licencia de maternidad posnatal de diez semanas.
Un estudio observacional prospectivo de un año de 23,000 mujeres empleadas en 50 empresas en la región de Rhône-Ales de Francia (Bertucat, Mamelle y Muñoz 1987) examinó el efecto de las condiciones de trabajo agotadoras en el parto prematuro. Durante el período del estudio, 1,150 bebés nacieron en la población de estudio. Analizamos las modificaciones de las condiciones de trabajo para acomodar el embarazo y la relación de estas modificaciones con el parto prematuro (Mamelle, Bertucat y Muñoz 1989), y observamos que:
- Se reformó la modificación del puesto de trabajo para solo el 8% de las mujeres.
- El 33% de las mujeres trabajaban sus turnos normales, mientras que las demás tenían su jornada laboral reducida de 30 a 60 minutos.
- El 50% de las mujeres tomó al menos un descanso laboral, además de su licencia prenatal por maternidad; la fatiga fue la causa en un tercio de los casos.
- El 90% de las mujeres dejó de trabajar antes de que comenzara su licencia legal por maternidad y obtuvo al menos las dos semanas de licencia permitidas en caso de complicaciones del embarazo; la fatiga fue la causa en la mitad de los casos.
- En total, dado el período legal de licencia prenatal de seis semanas previas a la fecha prevista (con dos semanas adicionales disponibles en algunos casos), la duración real de la licencia prenatal por maternidad fue de 12 semanas en esta población de mujeres sometidas a condiciones de trabajo agotadoras.
¿Estas modificaciones del trabajo tienen algún efecto sobre el resultado del embarazo? La modificación del puesto de trabajo y la ligera reducción de la jornada laboral (30 a 60 min) se asociaron con reducciones no significativas del riesgo de parto prematuro. Creemos que mayores reducciones de la semana laboral tendrían un mayor efecto (tabla 4).
Tabla 4. Riesgos relativos de prematuridad asociados a modificaciones en las condiciones de trabajo
| Modificaciones estoy trabajando condiciones |
Número de mujeres | Prematuro tasas de natalidad (%) |
Riesgo relativo (95% intervalos de confianza) |
| Cambio en la situación laboral. | |||
| No Sí |
1,062 87 |
6.2 3.4 |
0.5 (0.2-1.6) |
| Reducción de la jornada laboral semanal | |||
| No Sí |
388 761 |
7.7 5.1 |
0.7 (0.4-1.1) |
| Episodios de baja por enfermedad1 | |||
| No Sí |
357 421 |
8.0 3.1 |
0.4 (0.2-0.7) |
| Aumento de la licencia de maternidad prenatal1 | |||
| Ninguna o solo 2 semanas adicionales Sí |
487 291 |
4.3 7.2 |
1.7 (0.9-3.0) |
1 En una muestra reducida de 778 mujeres sin patología obstétrica previa o presente.
Fuente: Mamelle, Bertucat y Muñoz 1989.
Para analizar la relación entre la licencia prenatal, las pausas laborales y el parto prematuro, es necesario discriminar entre las pausas preventivas y curativas. Esto requiere restringir el análisis a mujeres con embarazos sin complicaciones. Nuestro análisis de este subgrupo reveló una reducción de la tasa de parto prematuro entre las mujeres que tomaron descansos en el trabajo durante el embarazo, pero no en aquellas que tomaron un permiso prenatal prolongado (Tabla 9).
Este estudio observacional demostró que las mujeres que trabajan en condiciones agotadoras toman más descansos laborales durante sus embarazos que otras mujeres, y que estos descansos, particularmente cuando están motivados por una fatiga intensa, se asocian con reducciones del riesgo de parto prematuro (Mamelle, Bertucat y Muñoz 1989).
Elección de estrategias preventivas en Francia
Como epidemiólogos, nos gustaría ver estas observaciones verificadas por estudios preventivos experimentales. Sin embargo, debemos preguntarnos qué es más razonable: ¿esperar a tales estudios o recomendar medidas sociales destinadas a prevenir el parto prematuro ahora?
El Gobierno francés decidió recientemente incluir una “guía de trabajo y embarazo”, idéntica a nuestra escala de fatiga, en el historial médico de cada mujer embarazada. Las mujeres pueden así calcular su puntuación de fatiga por sí mismas. Si las condiciones de trabajo son arduas, pueden solicitar al médico del trabajo o al responsable de seguridad laboral de su empresa que implemente modificaciones destinadas a aliviar su carga de trabajo. En caso de negarse, pueden solicitar a su médico tratante que prescriba semanas de descanso durante su embarazo, e incluso que prolonguen su licencia de maternidad prenatal.
El desafío ahora es identificar estrategias preventivas que estén bien adaptadas a la legislación y las condiciones sociales de cada país. Esto requiere un enfoque de economía de la salud para la evaluación y comparación de estrategias preventivas. Antes de que cualquier medida preventiva pueda considerarse de aplicación general, deben tenerse en cuenta muchos factores. Estos incluyen la eficacia, por supuesto, pero también el bajo costo para el sistema de seguridad social, la creación de empleo resultante, las referencias de las mujeres y la aceptabilidad de los empleadores y sindicatos.
Este tipo de problema se puede resolver utilizando métodos multicriterio como el método Electra. Estos métodos permiten tanto la clasificación de las estrategias preventivas sobre la base de cada una de una serie de criterios, como la ponderación de los criterios sobre la base de consideraciones políticas. Así, se puede dar especial importancia al bajo costo del sistema de seguridad social oa la capacidad de elección de las mujeres, por ejemplo (Mamelle et al. 1986). Si bien las estrategias recomendadas por estos métodos varían según los decisores y las opciones políticas, la efectividad siempre se mantiene desde el punto de vista de la salud pública.
Exposición ocupacional y ambiental del recién nacido
Los peligros ambientales representan un riesgo especial para los bebés y los niños pequeños. Los niños no son “pequeños adultos”, ya sea en la forma en que absorben y eliminan las sustancias químicas o en su respuesta a las exposiciones tóxicas. Las exposiciones neonatales pueden tener un mayor impacto porque el área de la superficie corporal es desproporcionadamente grande y la capacidad metabólica (o la capacidad de eliminar sustancias químicas) está relativamente subdesarrollada. Al mismo tiempo, los efectos tóxicos potenciales son mayores, porque el cerebro, los pulmones y el sistema inmunitario todavía se están desarrollando durante los primeros años de vida.
Existen oportunidades de exposición en el hogar, en las guarderías y en los parques infantiles:
- Los niños pequeños pueden absorber los agentes ambientales del aire (por inhalación) oa través de la piel.
- La ingestión es una ruta principal de exposición, especialmente cuando los niños comienzan a exhibir actividades de llevarse la mano a la boca.
- Las sustancias en el cabello, la ropa o las manos de los padres pueden transferirse al niño pequeño.
- La leche materna es otra fuente potencial de exposición para los bebés, aunque los posibles beneficios de amamantar superan con creces los posibles efectos tóxicos de las sustancias químicas de la leche materna.
Para varios de los efectos sobre la salud discutidos en relación con las exposiciones neonatales, es difícil distinguir los eventos prenatales de los posnatales. Las exposiciones realizadas antes del nacimiento (a través de la placenta) pueden seguir manifestándose en la primera infancia. Tanto el plomo como el humo ambiental del tabaco se han asociado con deficiencias en el desarrollo cognitivo y la función pulmonar tanto antes como después del nacimiento. En esta revisión, hemos intentado centrarnos en las exposiciones posnatales y sus efectos en la salud de los niños muy pequeños.
Plomo y otros metales pesados
Entre los metales pesados, el plomo (b) es la exposición elemental más importante para los seres humanos en circunstancias ambientales y laborales. Las exposiciones ocupacionales significativas ocurren en la fabricación de baterías, fundiciones, soldadura, construcción y remoción de pintura. Se sabe desde hace mucho tiempo que los padres empleados en estas industrias traen polvo a casa en su ropa que puede ser absorbido por sus hijos. La ruta principal de absorción por parte de los niños es a través de la ingestión de pedacitos de pintura, polvo y agua contaminados con plomo. La absorción respiratoria es eficiente y la inhalación se convierte en una vía de exposición importante si se reenvía un aerosol de plomo o alquilo de plomo (Clement International Corporation 1991).
El envenenamiento por plomo puede dañar prácticamente todos los sistemas de órganos, pero los niveles actuales de exposición se han asociado principalmente con cambios neurológicos y de desarrollo en los niños. Además, se han observado enfermedades renales y hematológicas tanto en adultos como en niños expuestos intensamente al plomo. Las enfermedades cardiovasculares y la disfunción reproductiva son secuelas conocidas de la exposición al plomo entre los adultos. Se sospecha que los efectos subclínicos renales, cardiovasculares y reproductivos surgen de una menor exposición crónica al plomo, y los datos limitados respaldan esta idea. Los datos animales respaldan los hallazgos humanos (Sager y Girard 1994).
En términos de dosis medibles, los efectos neurológicos van desde déficits de coeficiente intelectual a bajas exposiciones (plomo en sangre = 10 μg/dl) hasta encefalopatía (80 μg/dl). Los niveles de preocupación en niños en 1985 eran de 25 μg/dl, que se redujeron a 10 μg/dl en 1993.
Chisholm en 1978 describió la exposición neonatal, como resultado del polvo que traían a casa los padres que trabajaban, como “ensuciar el nido”. Desde entonces, las medidas preventivas, como ducharse y cambiarse de ropa antes de salir del lugar de trabajo, han reducido la toma de carga de polvo en el hogar. Sin embargo, el plomo de origen ocupacional sigue siendo una importante fuente potencial de exposición neonatal en la actualidad. Una encuesta de niños en Dinamarca encontró que el nivel de plomo en la sangre era aproximadamente el doble entre los hijos de trabajadores expuestos que en hogares con exposiciones no ocupacionales solamente (Grandjean y Bach 1986). Se ha documentado la exposición de los niños al plomo derivado del trabajo entre los empalmadores de cables eléctricos (Rinehart y Yanagisawa 1993) y los trabajadores de la fabricación de capacitores (Kaye, Novotny y Tucker 1987).
Las fuentes no ocupacionales de exposición ambiental al plomo continúan siendo un peligro grave para los niños pequeños. Desde la prohibición gradual del tetraetilo de plomo como aditivo de combustible en los Estados Unidos (en 1978), los niveles promedio de plomo en la sangre de los niños han disminuido de 13 a 3 μg/dl (Pirkle et al. 1994). los pedazos de pintura y el polvo de pintura son ahora la causa principal del envenenamiento infantil por plomo en los Estados Unidos (Roer 1991). Por ejemplo, en un informe, los niños más pequeños (recién nacidos menores de 11 meses) con un exceso de plomo en la sangre tenían un mayor riesgo de exposición a través del polvo y el agua, mientras que los niños mayores (24 meses) tenían un mayor riesgo por la ingestión de pedacitos de pintura ( ica) (Shannon y Graef 1992). La reducción del plomo mediante la eliminación de la pintura ha tenido éxito en la protección de los niños contra la exposición al polvo y las virutas de pintura (Farfel, Chisholm y Rohde 1994). Irónicamente, se ha demostrado que los trabajadores que participan en esta empresa llevan polvo de plomo a casa en su ropa. Además, se ha observado que la exposición continua de los niños pequeños al plomo afecta desproporcionadamente a los niños económicamente desfavorecidos (Brody et al. 1994; Goldman y Carra 1994). arte de esta inequidad surge del mal estado de las viviendas; ya en 1982 se demostró que el grado de deterioro de la vivienda estaba directamente relacionado con los niveles de plomo en la sangre de los niños (Clement International Corporation 1991).
Otra fuente potencial de exposición derivada del trabajo para los recién nacidos es el plomo en la leche materna. Los niveles más altos de plomo en la leche materna se han relacionado con fuentes tanto laborales como ambientales (Ryu, Ziegler y Fomon 1978; Dabeka et al. 1986). Las concentraciones de plomo en la leche son pequeñas en relación con la sangre (aproximadamente 1/5 a 1/2) (Wolff 1993), pero el gran volumen de leche materna ingerido por un lactante puede agregar cantidades de miligramos a la carga corporal. En comparación, normalmente hay menos de 0.03 mg b en la sangre circulante de un lactante y la ingesta habitual es de menos de 20 mg por día (Clement International Corporation 1991). De hecho, la absorción de la leche materna se refleja en el nivel de plomo en la sangre de los bebés (Rabinowitz, Leviton y Needleman 1985; Ryu et al. 1983; Ziegler et al. 1978). Cabe señalar que los niveles normales de plomo en la leche materna no son excesivos, y la lactancia aporta una cantidad similar a la de otras fuentes de nutrición infantil. En comparación, un chi de pintura pequeño podría contener más de 10 mg (10,000 XNUMX mg) de plomo.
Las disminuciones en el desarrollo de los niños se han relacionado con exposiciones prenatales y posnatales al plomo. Se cree que la exposición prenatal es responsable de los déficits relacionados con el plomo en el desarrollo mental y conductual que se han encontrado en niños hasta la edad de dos a cuatro años (Landrigan y Cambell 1991; Bellinger et al. 1987). Los efectos de la exposición posnatal al plomo, como la que experimenta el recién nacido debido a fuentes ocupacionales, pueden detectarse en niños de dos a seis años e incluso más. Entre estos se encuentran el comportamiento problemático y la baja inteligencia (Bellinger et al. 1994). Estos efectos no se limitan solo a exposiciones altas; se han observado en niveles relativamente bajos, por ejemplo, donde los niveles de plomo en la sangre están en el rango de 10 mg/dl (Needleman y Bellinger 1984).
La exposición al mercurio (Hg) del medio ambiente puede ocurrir en formas inorgánicas y orgánicas (principalmente metilo). Se han encontrado exposiciones ocupacionales recientes al mercurio entre trabajadores en la fabricación de termómetros y en la reparación de equipos de alto voltaje que contienen mercurio. Otras ocupaciones con exposiciones potenciales incluyen la pintura, la odontología, la plomería y la fabricación de cloro (Agencia para el Registro de Sustancias Tóxicas y Enfermedades 1992).
el envenenamiento por mercurio prenatal y posnatal ha sido bien documentado entre los niños. Los niños son más susceptibles a los efectos del metilmercurio que los adultos. Esto se debe en gran parte a que el sistema nervioso central humano en desarrollo es tan "notablemente sensible" al metilmercurio, un efecto que también se observa en niveles bajos en animales (Clarkson, Nordberg y Sager 1985). Las exposiciones al metilmercurio en los niños surgen principalmente de la ingestión de pescado contaminado o de la leche materna, mientras que el mercurio elemental se deriva de exposiciones ocupacionales. Se ha observado la exposición doméstica incidental a la exposición ocupacional (Zirschky y Wetherell 1987). En los últimos años se han informado exposiciones accidentales en el hogar en industrias domésticas (Meeks, Keith y Tanner 1990; Rowens et al. 1991) y en un alféizar accidental de mercurio metálico (Florentine y Sanfilio 1991). La exposición al mercurio elemental ocurre principalmente por inhalación, mientras que el alquilmercurio puede absorberse por ingestión, inhalación o contacto dérmico.
En el episodio de envenenamiento mejor estudiado, se encontraron disfunciones sensoriales y motoras y retraso mental después de exposiciones muy altas al metilmercurio, ya sea en el útero o de la leche materna (Bakir et al. 1973). Las exposiciones maternas se debieron a la ingestión de metilmercurio que se había utilizado como fungicida en los cereales.
pesticidas y productos químicos relacionados
Cada año se producen varios cientos de millones de toneladas de plaguicidas en todo el mundo. Los herbicidas, fungicidas e insecticidas se emplean principalmente en la agricultura de los países desarrollados para mejorar el rendimiento y la calidad de los cultivos. Los conservantes de madera son un arte mucho más pequeño, pero aún así importante, del mercado. El uso en el hogar y el jardín representa una proporción relativamente menor del consumo total, pero desde el punto de vista de la toxicidad neonatal, las intoxicaciones domésticas son quizás las más numerosas. La exposición ocupacional también es una fuente potencial de exposición indirecta para los bebés si uno de los padres está involucrado en un trabajo que usa pesticidas. La exposición a pesticidas es posible a través de la absorción dérmica, la inhalación y la ingestión. Más de 50 plaguicidas han sido declarados cancerígenos en animales (McConnell 1986).
Los plaguicidas organoclorados incluyen compuestos aromáticos, como el DDT (bis(4-clorohenil)-1,1,1-tricloroetano), y ciclodienos, como el dieldrín. El DDT comenzó a usarse a principios de la década de 1940 como un medio eficaz para eliminar los mosquitos que transmiten la malaria, una aplicación que todavía se emplea ampliamente en los países en desarrollo. El lindano es un organoclorado que se usa ampliamente para controlar los piojos del cuerpo y en la agricultura, especialmente en los países en desarrollo. Los bihenilos policlorados (CB), otra mezcla de organoclorados solubles en grasa utilizada desde la década de 1940, representan un riesgo potencial para la salud de los niños pequeños expuestos a través de la leche materna y otros alimentos contaminados. Tanto el lindano como los CB se analizan por separado en este capítulo. También se han detectado bihenilos polibromados (BB) en la leche materna, casi exclusivamente en Michigan. Aquí, un retardador de fuego que se mezcló inadvertidamente con el alimento para ganado en 1973-74 se dispersó ampliamente por todo el estado a través de los productos lácteos y cárnicos.
El clordano se ha utilizado como pesticida y como termiticida en las casas, donde es eficaz durante décadas, sin duda por su persistencia. La exposición a esta sustancia química puede deberse a la dieta y a la absorción respiratoria o dérmica directa. Los niveles en la leche humana en Japón podrían estar relacionados tanto con la dieta como con el tratamiento reciente de los hogares. Las mujeres que vivían en hogares tratados hacía más de dos años tenían niveles de clordano en la leche tres veces superiores a los de las mujeres que vivían en hogares no tratados (Taguchi y Yakushiji 1988).
La dieta es la principal fuente de organoclorados persistentes, pero fumar, el aire y el agua también pueden contribuir a la exposición. Esta clase de plaguicidas, también denominados hidrocarburos halogenados, es bastante persistente en el medio ambiente, ya que son lipofílicos, resistentes al metabolismo oa la biodegradación y presentan baja volatilidad. Se han encontrado varios cientos de m en grasa humana y animal entre aquellos con exposiciones más altas. Debido a su toxicidad para la reproducción en la vida silvestre y su tendencia a la bioacumulación, los organoclorados se han prohibido o restringido en gran medida en los países desarrollados.
En dosis muy altas, se ha observado neurotoxicidad con organoclorados, pero los posibles efectos a largo plazo en la salud son más preocupantes entre los humanos. Aunque los efectos crónicos en la salud no han sido ampliamente documentados, se han encontrado calortoxicidad, cáncer y disfunción reproductiva en animales de experimentación y en la vida silvestre. Los problemas de salud surgen principalmente de las observaciones en estudios con animales de carcinogénesis y de cambios profundos en el hígado y el sistema inmunitario.
Los organohoshatos y los carbamatos son menos persistentes que los organoclorados y son la clase de insecticidas más utilizada a nivel internacional. los pesticidas de esta clase se degradan con relativa rapidez en el medio ambiente y en el cuerpo. Varios organohoshatos y carbamatos exhiben una neurotoxicidad aguda alta y, en ciertos casos, también una neurotoxicidad crónica. La dermatitis también es un síntoma ampliamente informado de la exposición a pesticidas.
Los productos a base de petróleo utilizados para aplicar algunos pesticidas también son motivo de preocupación potencial. Los efectos crónicos, incluidos los cánceres hematopoyético y otros cánceres infantiles, se han asociado con exposiciones de los padres o residenciales a pesticidas, pero los datos epidemiológicos son bastante limitados. Sin embargo, según los datos de estudios en animales, se debe evitar la exposición a pesticidas.
Para el recién nacido, se ha informado un amplio espectro de posibilidades de exposición y efectos tóxicos. Entre los niños que requirieron hospitalización por intoxicación aguda, la mayoría había ingerido productos pesticidas sin darse cuenta, mientras que un número significativo había estado expuesto mientras estaban acostados sobre caretas rociadas (Casey, Thomson y Vale 1994; Zwiener y Ginsburg 1988). Hace tiempo que se reconoce la contaminación de la ropa de los trabajadores por polvo o líquido de plaguicidas. Por lo tanto, esta ruta brinda una amplia oportunidad para exposiciones en el hogar, a menos que los trabajadores tomen las precauciones higiénicas adecuadas después del trabajo. Por ejemplo, toda una familia tenía niveles elevados de clordecona (Keone) en la sangre, atribuidos al lavado doméstico de la ropa de un trabajador (Grandjean y Bach 1986). La exposición doméstica a TCDD (dioxina) ha sido documentada por la presencia de cloracné en el hijo y la esposa de dos trabajadores expuestos después de una explosión (Jensen, Sneddon y Walker 1972).
La mayoría de las posibles exposiciones de los bebés surgen de la aplicación de pesticidas dentro y alrededor del hogar (Lewis, Fortmann y Camann 1994). Se ha descubierto que el polvo en los espacios domésticos está muy contaminado con numerosos pesticidas (Fenske et al. 1994). Gran parte de la contaminación doméstica informada se ha atribuido al exterminio de pulgas oa la aplicación de pesticidas en céspedes y jardines (Davis, Bronson y García 1992). Se ha pronosticado que la absorción infantil de cloryrifos después del tratamiento de pulgas en los hogares excederá los niveles seguros. De hecho, los niveles de aire interior después de tales procedimientos de fumigación no siempre disminuyen rápidamente a niveles seguros.
La leche materna es una fuente potencial de exposición a pesticidas para el recién nacido. La contaminación de la leche humana con plaguicidas, especialmente los organoclorados, se conoce desde hace décadas. Las exposiciones ocupacionales y ambientales pueden conducir a una contaminación significativa de pesticidas en la leche materna (D'Ercole et al. 1976; McConnell 1986). Los organoclorados, que en el pasado se han encontrado en la leche materna en niveles excesivos, están disminuyendo en los países desarrollados, de forma paralela a la disminución de las concentraciones de tejido adiposo que se ha producido después de la restricción de estos compuestos. Por lo tanto, la contaminación por DDT de la leche humana es ahora más alta en los países en desarrollo. Hay poca evidencia de organohoshatos en la leche materna. Esto puede atribuirse a las propiedades de solubilidad en agua y al rápido metabolismo de estos compuestos en el cuerpo.
La ingestión de agua contaminada con pesticidas también es un riesgo potencial para la salud del recién nacido. Este problema es mayormente evitado cuando la fórmula infantil debe criarse usando agua. De lo contrario, las fórmulas infantiles comerciales están relativamente libres de contaminantes (Consejo Nacional de Investigación 1993). La contaminación de los alimentos con pesticidas también puede conducir a la exposición de los bebés. La contaminación de leche comercial, frutas y verduras con pesticidas existe en niveles muy bajos, incluso en los países desarrollados, donde la regulación y el control son más estrictos (The Referee 1994). Aunque la leche constituye la mayor parte de la dieta infantil, los niños pequeños también consumen frutas (especialmente cervezas) y verduras (especialmente zanahorias) en cantidades significativas y, por lo tanto, representan una posible fuente de exposición a pesticidas.
En los países industrializados, incluidos los Estados Unidos y Europa occidental, la mayoría de los plaguicidas organoclorados, incluidos el DDT, el clordano, el dieldrín y el lindano, han sido prohibidos, suspendidos o restringidos desde la década de 1970 (Maxcy Rosenau-Last 1994). los plaguicidas que todavía se utilizan con fines agrícolas y no agrícolas están regulados en cuanto a sus niveles en los alimentos, el agua y los productos farmacéuticos. Como resultado de esta regulación, los niveles de pesticidas en el tejido adiposo y la leche humana han disminuido significativamente durante las últimas cuatro décadas. Sin embargo, los organoclorados todavía se usan ampliamente en los países en desarrollo, donde, por ejemplo, el lindano y el DDT se encuentran entre los plaguicidas más empleados para uso agrícola y para el control de la malaria (Awumbila y Bokuma 1994).
Lindano
El lindano es el isómero γ y el ingrediente activo del grado técnico de hexacloruro de benceno (BHC). El BHC, también conocido como hexaclorociclohexano (HCH), contiene del 40 al 90 % de otros isómeros: α, β y δ. Este organoclorado se ha utilizado como pesticida agrícola y no agrícola en todo el mundo desde 1949. Pueden ocurrir exposiciones ocupacionales durante la fabricación, formulación y aplicación de BHC. El lindano como reparador farmacéutico en cremas, lociones y champús también se usa ampliamente para tratar la sarna y los piojos del cuerpo. Debido a que estas afecciones de la piel ocurren comúnmente entre bebés y niños, el tratamiento médico puede llevar a que los bebés absorban BHC a través de la piel. La exposición neonatal también puede ocurrir por inhalación de vapor o polvo que los padres pueden llevar a casa o que pueden permanecer después del uso doméstico. La ingesta dietética también es un medio posible de exposición de los bebés, ya que se ha detectado BHC en la leche humana, productos lácteos y otros alimentos, al igual que muchos insecticidas organoclorados. La exposición a través de la leche materna era más frecuente en los Estados Unidos antes de la prohibición de la producción comercial de lindano. Según la IARC (Agencia Internacional para la Investigación del Cáncer 1987), es posible que el hexaclorociclohexano sea cancerígeno para los humanos. Sin embargo, la evidencia de resultados adversos para la salud entre los bebés se ha informado principalmente como efectos en los sistemas neurológico y hematológico.
Se ha descrito exposición doméstica al lindano en la esposa de un formulador de plaguicidas, lo que demuestra el potencial de exposiciones neonatales similares. La esposa tenía 5 ng/ml de γ-BHC en sangre, una concentración inferior a la de su marido (tabla 1) (Starr et al. 1974). presumiblemente, el γ-BHC se introdujo en el hogar en el cuerpo y/o la ropa del trabajador. Los niveles de γ-BHC en la mujer y su esposo fueron más altos que los informados en niños tratados con lociones que contenían 0.3 a 1.0% de BHC.
El BHC en la leche materna existe principalmente como isómero β (Smith 1991). La vida media del isómero γ en el cuerpo humano es de aproximadamente un día, mientras que el isómero β se acumula.
Tabla 1. Fuentes potenciales y niveles de exposición de los recién nacidos
| Fuente de exposición | g-BHC en sangre (ng/ml; ppmm) |
|
| Exposiciones ocupacionales | Exposiciones bajas Altas exposiciones |
5 36 |
| Macho adulto | Intento de suicidio | 1300 |
| Niño | Envenenamiento agudo | 100 - 800 |
| Niños | 1% de loción BHC (promedio) | 13 |
| Informe de caso de exposición domiciliaria1 | Esposo Esposa |
17 5 |
| Poblaciones no expuestas desde 1980 | Yugoslavia África Brasil India |
52 72 92 752 |
1Starr et al. (1974); otros datos de Smith (1991).
2En gran parte isómero b.
La absorción dérmica del lindano de los productos farmacéuticos está en función de la cantidad aplicada a la piel y la duración de la exposición. En comparación con los adultos, los bebés y los niños pequeños parecen ser más susceptibles a los efectos tóxicos del lindano (Clement International Corporation 1992). Una razón puede ser que la absorción dérmica se ve reforzada por una mayor permeabilidad de la piel del bebé y una gran relación superficie-volumen. Los niveles en el recién nacido pueden persistir por más tiempo porque el metabolismo de BHC es menos eficiente en bebés y niños pequeños. Además, la exposición en recién nacidos puede aumentar al lamerse o llevarse la boca a las áreas tratadas (Kramer et al. 1990). Una ducha o baño caliente antes de la aplicación dérmica de productos médicos puede facilitar la absorción dérmica, lo que exacerba la toxicidad.
En varios casos notificados de envenenamiento accidental con lindano, se han descrito efectos tóxicos evidentes, algunos en niños pequeños. En un caso, un bebé de dos meses murió después de múltiples exposiciones a una loción de lindano al 1%, incluida una aplicación en todo el cuerpo después de un baño caliente (Davies et al. 1983).
La producción y el uso de lindano están restringidos en la mayoría de los países desarrollados. El lindano todavía se usa ampliamente en otros países con fines agrícolas, como se señaló en un estudio sobre el uso de pesticidas en granjas en Ghana, donde el lindano representó el 35 y el 85% del uso de pesticidas por agricultores y pastores, respectivamente (Awumbila y Bokuma 1994).
bihenilos oliclorados
Los bihenilos policlorados se utilizaron desde mediados de la década de 1940 hasta finales de la de 1970 como fluidos aislantes en transformadores y condensadores eléctricos. Los residuos aún se encuentran en el medio ambiente debido a la contaminación, que se debe en gran parte a una eliminación inadecuada oa derrames accidentales. Algunos equipos aún en uso o almacenados siguen siendo una fuente potencial de contaminación. Se informó un incidente en el que los niños tenían niveles detectables de CB en la sangre luego de la exposición mientras estaban acostados con capacitores (Wolff y Schecter 1991). También se ha informado exposición en la esposa de un trabajador expuesto (Fishbein y Wolff 1987).
En dos estudios de exposiciones ambientales, la exposición renatal y posnatal a los CB se asoció con efectos pequeños pero significativos en los niños. En un estudio, se detectó un desarrollo motor levemente afectado entre los niños cuyas madres tenían niveles de CB en la leche materna postnatales inmediatos en el percentil 95 superior del grupo de estudio (Rogan et al. 1986). En el otro, se observaron déficits sensoriales (así como un tamaño gestacional más pequeño) entre los niños con niveles en sangre de aproximadamente el 25% (Jacobson et al. 1985; Fein et al. 1984). Estos niveles de exposición estaban en el rango superior para los estudios (por encima de 3 m en la leche materna (base grasa) y por encima de 3 ng/ml en la sangre de los niños), pero no son excesivamente altos. Las exposiciones ocupacionales comunes resultan en niveles diez a 100 veces más altos (Wolff 1985). En ambos estudios, los efectos se atribuyeron a la exposición prenatal. Sin embargo, tales resultados suenan como una nota de advertencia para exponer indebidamente a los recién nacidos a tales químicos tanto antes como después del nacimiento.
disolventes
Los disolventes son un grupo de líquidos volátiles o semivolátiles que se utilizan principalmente para disolver otras sustancias. La exposición a solventes puede ocurrir en los procesos de fabricación, por ejemplo, la exposición al hexano durante la destilación de productos derivados del petróleo. Para la mayoría de las personas, la exposición a los solventes surgirá mientras se usan en el trabajo o en el hogar. Las aplicaciones industriales comunes incluyen limpieza en seco, desengrasado, pintura y eliminación de pintura e impresión. Dentro del hogar, es posible el contacto directo con solventes durante el uso de productos como limpiadores de metales, productos de limpieza en seco, diluyentes de pintura o aerosoles.
Las principales vías de exposición de los disolventes tanto en adultos como en lactantes son la absorción respiratoria y dérmica. La ingestión de leche materna es una forma de exposición neonatal a solventes derivados del trabajo de los padres. Debido a la breve vida media de la mayoría de los solventes, su duración en la leche materna será igualmente breve. Sin embargo, después de la exposición materna, algunos solventes volverán a la leche materna al menos por un corto tiempo (al menos una vida media). Los disolventes que se han detectado en la leche materna incluyen tetracloroetileno, disulfuro de carbono y halotano (un anestésico). Una revisión detallada de la posible exposición infantil al tetracloroetileno (TCE) ha concluido que los niveles en la leche materna pueden superar fácilmente las pautas de riesgo para la salud recomendadas (Schreiber 1993). El exceso de riesgo fue mayor para los bebés cuyas madres podrían estar expuestas en el lugar de trabajo (58 a 600 por millón de personas). Para las exposiciones no ocupacionales más altas, se estimó un exceso de riesgo de 36 a 220 por 10 millones de personas; tales exposiciones pueden existir en hogares directamente encima de las tintorerías. Se estimó además que las concentraciones de TCE en la leche volverían a los niveles "normales" (reexposición) de cuatro a ocho semanas después del cese de la exposición.
Las exposiciones no ocupacionales son posibles para el bebé en el hogar donde se usan solventes o productos a base de solventes. El aire interior tiene niveles muy bajos, pero consistentemente detectables, de solventes como el tetracloroetileno. El agua también puede contener compuestos orgánicos volátiles del mismo tipo.
Polvos y Fibras Minerales: Amianto, Fibra de Vidrio, Lana de Roca, Zeolitas, Talco
La exposición al polvo mineral y las fibras en el lugar de trabajo causa enfermedades respiratorias, incluido el cáncer de pulmón, entre los trabajadores. La exposición al polvo es un problema potencial para el recién nacido si uno de los padres lleva artículos a la casa en la ropa o el cuerpo. Con el asbesto, se han encontrado fibras del lugar de trabajo en el entorno del hogar, y las exposiciones resultantes de los miembros de la familia se han denominado exposiciones de espectadores o familiares. Ha sido posible documentar la enfermedad familiar por asbesto debido a la aparición de un tumor señal, el mesotelioma, que se asocia principalmente con la exposición al asbesto. El mesotelioma es un cáncer de la leura o del eritoneo (revestimiento de los pulmones y el abdomen, respectivamente) que se produce después de un largo período de latencia, normalmente de 30 a 40 años después de la primera exposición al amianto. La etiología de esta enfermedad parece estar relacionada únicamente con el tiempo transcurrido desde la exposición inicial, no con la intensidad o la duración, ni con la edad de la primera exposición (Nicholson 1986; Otte, Sigsgaard y Kjaerulff 1990). Las anomalías respiratorias también se han atribuido a la exposición al asbesto de los transeúntes (Grandjean y Bach 1986). Extensos experimentos con animales respaldan las observaciones humanas.
La mayoría de los casos de mesotelioma familiar se han informado entre esposas de mineros, molineros, fabricantes y aisladores expuestos. Sin embargo, varias exposiciones infantiles también se han asociado con enfermedades. Bastantes de estos niños tuvieron un contacto inicial que ocurrió a una edad temprana (Dawson et al. 1992; Anderson et al. 1976; Roggli y Longo 1991). Por ejemplo, en una investigación de 24 contactos familiares con mesotelioma que vivían en un pueblo minero de crocidolita asbesto, se identificaron siete casos cuyas edades tenían entre 29 y 39 años en el momento del diagnóstico o la muerte y cuya exposición inicial se había producido con menos de un año de edad ( n=5) o a los tres años (n=2) (Hansen et al. 1993).
La exposición al asbesto es claramente causante del mesotelioma, pero se ha propuesto además un mecanismo epigenético para explicar la agrupación inusual de casos dentro de ciertas familias. Por lo tanto, la aparición de mesotelioma entre 64 personas en 27 familias sugiere un rasgo genético que puede volver a ciertos individuos más sensibles a la agresión del asbesto que conduce a esta enfermedad (Dawson et al. 1992; Bianchi, Brollo y Zuch 1993). Sin embargo, también se ha sugerido que la exposición por sí sola puede proporcionar una explicación adecuada para la agregación familiar informada (Alderson 1986).
Otros polvos inorgánicos asociados con enfermedades profesionales incluyen fibra de vidrio, zeolitas y talco. Tanto el asbesto como la fibra de vidrio se han utilizado ampliamente como materiales aislantes. la fibrosis pulmonar y el cáncer se asocian con el asbesto y mucho menos claramente con la fibra de vidrio. Se ha informado mesotelioma en áreas de Turquía con exposiciones indígenas a zeolitas naturales. Las exposiciones al asbesto también pueden surgir de fuentes no ocupacionales. Los pañales (“naies”) construidos con fibra de asbesto fueron implicados como una fuente de exposición infantil al asbesto (Li, Dreyfus y Antman 1989); sin embargo, la ropa de los padres no se excluyó como fuente de contacto con el asbesto en este informe. También se ha encontrado asbesto en cigarrillos, secadores de pelo, baldosas y algunos tipos de polvos de talco. Su uso ha sido eliminado en muchos países. Sin embargo, una consideración importante para los niños es el aislamiento de amianto residual en las escuelas, que ha sido ampliamente investigado como un posible problema de salud pública.
Humo de tabaco ambiental
El humo de tabaco ambiental (ETS) es una combinación de humo exhalado y humo emitido por el cigarrillo encendido. Aunque el HTA en sí mismo no es una fuente de exposición ocupacional que pueda afectar al recién nacido, se revisa aquí debido a su potencial para causar efectos adversos para la salud y porque brinda un buen ejemplo de otras exposiciones a aerosoles. La exposición de un no fumador al HTA a menudo se describe como tabaquismo pasivo o involuntario. la exposición prenatal al HTA está claramente asociada con déficits o alteraciones en el crecimiento fetal. Es difícil distinguir los resultados posnatales de los efectos del ETS en el período prenatal, ya que el tabaquismo de los padres rara vez se limita a un momento u otro. Sin embargo, existe evidencia que respalda una relación entre la exposición posnatal al HTA y las enfermedades respiratorias y el deterioro de la función pulmonar. La similitud de estos hallazgos con las experiencias entre adultos fortalece la asociación.
El HTA ha sido bien caracterizado y ampliamente estudiado en términos de exposición humana y efectos sobre la salud. ETS es un carcinógeno humano (Agencia de Protección Ambiental de EE.UU. 1992). La exposición al HTA se puede evaluar midiendo los niveles de nicotina, un componente del tabaco, y cotinina, su principal metabolito, en fluidos biológicos, como la saliva, la sangre y la orina. También se han detectado nicotina y cotinina en la leche materna. También se ha encontrado cotinina en la sangre y la orina de lactantes que estuvieron expuestos al HTA sólo durante la lactancia (Charlton 1994; National Research Council 1986).
Se ha establecido claramente que la exposición del recién nacido al HTA se debe al tabaquismo paterno y materno en el entorno doméstico. El tabaquismo materno proporciona la fuente más importante. Por ejemplo, en varios estudios se ha demostrado que la cotinina urinaria en niños se correlaciona con el número de cigarrillos que fuma la madre por día (Marbury, Hammon y Haley 1993). Las principales vías de exposición al HTA del recién nacido son la respiratoria y la dietética (a través de la leche materna). Las guarderías representan otra posible situación de exposición; muchas instalaciones de cuidado infantil no tienen una política de no fumar (Sockrider y Coultras 1994).
La hospitalización por enfermedad respiratoria ocurre con mayor frecuencia entre los recién nacidos cuyos padres fuman. Además, la duración de las visitas al hospital es mayor entre los bebés expuestos al HTA. En términos de causalidad, la exposición al HTA no se ha asociado con enfermedades respiratorias específicas. Sin embargo, hay pruebas de que el tabaquismo pasivo aumenta la gravedad de enfermedades reexistentes como la bronquitis y el asma (Charlton 1994; Chilmonczyk et al. 1993; Rylander et al. 1993). Los niños y los bebés expuestos al HTA también tienen una mayor frecuencia de infecciones respiratorias. Además, los padres fumadores con enfermedades respiratorias pueden transmitir infecciones en el aire a los bebés al toser.
Los niños expuestos al HTA después del nacimiento muestran pequeños déficits en la función pulmonar que parecen ser independientes de las exposiciones prenatales (Frischer et al. 1992). Aunque los cambios relacionados con el ETS son pequeños (disminución del 0.5 % por año del volumen espiratorio forzado), y aunque estos efectos no son clínicamente significativos, sugieren cambios en las células del pulmón en desarrollo que pueden presagiar un riesgo posterior. el tabaquismo de los padres también se ha asociado con un mayor riesgo de otitis media, o derrame del oído medio, en niños desde la infancia hasta los nueve años. Esta condición es una causa común de sordera entre los niños que puede causar retrasos en el progreso educativo. El riesgo asociado está respaldado por estudios que atribuyen un tercio de todos los casos de otitis media al tabaquismo de los padres (Charlton 1994).
Exposiciones a la radiación
La exposición a la radiación ionizante es un peligro para la salud establecido que generalmente es el resultado de una exposición intensa, ya sea accidental o con fines médicos. Puede ser dañino para las células altamente proliferativas y, por lo tanto, puede ser muy dañino para el feto o el recién nacido en desarrollo. Las exposiciones a la radiación que resultan de los rayos X de diagnóstico son generalmente de muy bajo nivel y se consideran seguras. Una posible fuente doméstica de exposición a la radiación ionizante es el radón, que existe en ciertas áreas geográficas en formaciones rocosas.
Los efectos prenatales y posnatales de la radiación incluyen retraso mental, menor inteligencia, retraso del crecimiento, malformaciones congénitas y cáncer. La exposición a altas dosis de radiación ionizante también se asocia con una mayor prevalencia de cáncer. La incidencia de esta exposición depende de la dosis y la edad. De hecho, el riesgo relativo más alto observado para el cáncer de mama (~9) se encuentra entre las mujeres que estuvieron expuestas a la radiación ionizante a una edad temprana.
Recientemente, la atención se ha centrado en los posibles efectos de la radiación no ionizante o campos electromagnéticos (CEM). Aún no se conoce la base de una relación entre la exposición a los CEM y el cáncer, y la evidencia epidemiológica aún no está clara. Sin embargo, en varios estudios internacionales se ha informado una asociación entre los CEM y la leucemia y el cáncer de mama masculino.
La exposición infantil a la luz solar excesiva se ha asociado con el cáncer de piel y el melanoma (Marks 1988).
Cáncer infantil
Aunque no se han identificado sustancias específicas, las exposiciones ocupacionales de los padres se han relacionado con el cáncer infantil. El período de latencia para desarrollar leucemia infantil puede ser de dos a 10 años después del inicio de la exposición, lo que indica que las exposiciones en el útero o en el período postnatal temprano pueden estar implicados en la causa de esta enfermedad. La exposición a varios plaguicidas organoclorados (BHC, DDT, clordano) se ha asociado tentativamente con la leucemia, aunque estos datos no se han confirmado en estudios más detallados. Además, se ha informado un riesgo elevado de cáncer y leucemia en niños cuyos padres realizan trabajos que involucran pesticidas, productos químicos y vapores (O'Leary et al. 1991). De manera similar, el riesgo de sarcoma óseo de Ewing en los niños se asoció con las ocupaciones de los padres en la agricultura o la exposición a herbicidas y pesticidas (Holly et al. 1992).
Resumen
Muchas naciones intentan regular los niveles seguros de sustancias químicas tóxicas en el aire ambiente y los productos alimenticios y en el lugar de trabajo. No obstante, abundan las oportunidades de exposición, y los niños son particularmente susceptibles tanto a la absorción como a los efectos de las sustancias químicas tóxicas. Se ha señalado que “muchas de las 40,000 vidas infantiles que se pierden cada día en el mundo en desarrollo son consecuencia de abusos ambientales que se reflejan en suministros de agua insalubres, enfermedades y desnutrición” (Schaefer 1994). Muchas exposiciones ambientales son evitables. Por lo tanto, la prevención de enfermedades ambientales tiene una alta prioridad como defensa contra los efectos adversos para la salud de los niños.
Protección de la maternidad en la legislación
Durante el embarazo, la exposición a ciertos peligros para la salud y la seguridad del trabajo o del entorno laboral puede tener efectos adversos en la salud de una mujer trabajadora y de su hijo por nacer. Antes y después de dar a luz, ella también necesita una cantidad razonable de tiempo fuera de su trabajo para recuperarse, amamantar y vincularse con su hijo. Muchas mujeres quieren y necesitan poder volver a trabajar después del parto; esto se reconoce cada vez más como un derecho básico en un mundo donde la participación de las mujeres en la fuerza laboral aumenta continuamente y se acerca a la de los hombres en muchos países. Dado que la mayoría de las mujeres necesitan mantenerse a sí mismas y a sus familias, la continuidad de los ingresos durante la licencia de maternidad es vital.
Con el tiempo, los gobiernos han promulgado una serie de medidas legislativas para proteger a las trabajadoras durante el embarazo y el parto. Una característica de las medidas más recientes es la prohibición de la discriminación en el empleo por motivos de embarazo. Otra tendencia es proporcionar el derecho de las madres y los padres a compartir los derechos de licencia después del nacimiento para que cualquiera pueda cuidar al niño. La negociación colectiva en muchos países contribuye a la aplicación más eficaz de tales medidas y, a menudo, las mejora. Los empleadores también desempeñan un papel importante en la promoción de la protección de la maternidad a través de las condiciones de los contratos individuales de empleo y las políticas empresariales.
Los límites de la protección
Las leyes que brindan protección a la maternidad para las mujeres trabajadoras suelen estar restringidas al sector formal, que puede representar una pequeña proporción de la actividad económica. Estos no se aplican a las mujeres que trabajan en actividades económicas no registradas en el sector informal, que en muchos países representan la mayoría de las mujeres trabajadoras. Si bien existe una tendencia mundial a mejorar y ampliar la protección de la maternidad, sigue siendo un gran desafío cómo proteger al gran segmento de la población que vive y trabaja fuera de la economía formal.
En la mayoría de los países, la legislación laboral brinda protección a la maternidad para las mujeres empleadas en empresas industriales y no industriales en el sector privado y, a menudo, también en el público. Con frecuencia quedan excluidos los trabajadores a domicilio, los empleados domésticos, los trabajadores por cuenta propia y los trabajadores de empresas que emplean únicamente a miembros de la familia. Dado que muchas mujeres trabajan en pequeñas empresas, la exclusión relativamente frecuente de empresas que emplean a menos de un cierto número de trabajadores (por ejemplo, cinco trabajadores permanentes en la República de Corea) es motivo de preocupación.
Muchas trabajadoras en empleos precarios, como las trabajadoras temporales o eventuales en Irlanda, están excluidas del ámbito de aplicación de la legislación laboral en varios países. Según el número de horas que trabajen, los trabajadores a tiempo parcial también pueden quedar excluidos. Otros grupos de mujeres pueden quedar excluidos, como las mujeres gerentes (p. ej., Singapur, Suiza), las mujeres cuyos ingresos superan un determinado máximo (p. ej., Mauricio) o las mujeres que cobran por resultados (p. ej., Filipinas). En casos raros, las mujeres solteras (por ejemplo, maestras en Trinidad y Tobago) no califican para la licencia de maternidad. Sin embargo, en Australia (federal), donde la licencia parental está disponible para los empleados y sus cónyuges, el término “cónyuge” se define para incluir a un cónyuge de facto. Cuando se establecen límites de edad (p. ej., en Israel, mujeres menores de 18 años), generalmente no excluyen a muchas mujeres, ya que normalmente se fijan por debajo o por encima de la edad ideal para tener hijos.
Los servidores públicos a menudo están cubiertos por reglas especiales, que pueden prever condiciones más favorables que las aplicables al sector privado. Por ejemplo, la licencia de maternidad puede ser más prolongada, los beneficios en efectivo pueden corresponder al salario completo en lugar de un porcentaje del mismo, es más probable que se disponga de la licencia parental o el derecho a la reincorporación puede estar más claramente establecido. En un número significativo de países, las condiciones en el servicio público pueden actuar como un agente de progreso, ya que los convenios colectivos en el sector privado a menudo se negocian de acuerdo con las normas de protección de la maternidad del servicio público.
Al igual que la legislación laboral, las leyes de seguridad social pueden limitar su aplicación a ciertos sectores o categorías de trabajadores. Si bien esta legislación suele ser más restrictiva que las leyes laborales correspondientes de un país, puede proporcionar acceso a prestaciones en efectivo por maternidad a grupos no cubiertos por las leyes laborales, como las mujeres que trabajan por cuenta propia o las mujeres que trabajan con sus maridos que trabajan por cuenta propia. En muchos países en desarrollo, debido a la falta de recursos, es posible que la legislación sobre seguridad social solo se aplique a un número limitado de sectores.
A lo largo de las décadas, sin embargo, la cobertura de la legislación se ha ampliado a más sectores económicos y categorías de trabajadores. Sin embargo, si bien un empleado puede estar cubierto por una ley, el disfrute de ciertos beneficios, en particular la licencia de maternidad y los beneficios en efectivo, puede depender de ciertos requisitos de elegibilidad. Así, mientras que la mayoría de los países protegen la maternidad, las mujeres trabajadoras no disfrutan de un derecho universal a dicha protección.
Licencia de maternidad
El tiempo libre para el parto puede variar desde unas pocas semanas hasta varios meses, a menudo dividido en dos partes, antes y después del parto. Se puede estipular un período de prohibición de empleo para una parte o la totalidad del derecho a garantizar que las mujeres tengan suficiente descanso. La licencia de maternidad suele extenderse en caso de enfermedad, parto prematuro o tardío y parto múltiple, o acortarse en caso de aborto espontáneo, muerte fetal o muerte infantil.
Duración normal
Según el Convenio sobre la protección de la maternidad de la OIT, 1919 (núm. 3), “una mujer no podrá trabajar durante las seis semanas siguientes a su parto; [y] tendrá derecho a dejar su trabajo si presenta un certificado médico en el que conste que su parto probablemente tendrá lugar dentro de las seis semanas”. El Convenio sobre la protección de la maternidad (revisado), 1952 (núm. 103), confirma la licencia de 12 semanas, incluida la prohibición de trabajar durante seis semanas después del nacimiento, pero no prescribe el uso de las seis semanas restantes. La Recomendación sobre la protección de la maternidad, 1952 (núm. 95), sugiere una licencia de 14 semanas. La Recomendación sobre la protección de la maternidad, 2000 (núm. 191) sugiere una licencia de 18 semanas [Editado, 2011]. La mayoría de los países encuestados cumplen con el estándar de 12 semanas y al menos un tercio otorga períodos más largos.
Varios países ofrecen la posibilidad de elegir la distribución de la licencia de maternidad. En algunos, la ley no prescribe la distribución de la licencia de maternidad (p. ej., Tailandia), y las mujeres tienen derecho a comenzar la licencia tan pronto como lo deseen. En otro grupo de países, la ley indica el número de días a tomar después del parto; el saldo se puede tomar antes o después del nacimiento.
Otros países no permiten flexibilidad: la ley prevé dos períodos de licencia, antes y después del parto. Estos períodos pueden ser iguales, especialmente cuando la licencia total es relativamente corta. Cuando la licencia total a la que se tiene derecho supera las 12 semanas, el período prenatal suele ser más breve que el período posnatal (por ejemplo, en Alemania, seis semanas antes y ocho semanas después del nacimiento).
En un número relativamente pequeño de países (por ejemplo, Benin, Chile, Italia), el empleo de mujeres está prohibido durante todo el período de la licencia de maternidad. En otros, se prescribe un período de licencia obligatoria, a menudo después del parto (por ejemplo, Barbados, Irlanda, India, Marruecos). El requisito más común es un período obligatorio de seis semanas después del nacimiento. Durante la última década, ha aumentado el número de países que prevén alguna licencia obligatoria antes del nacimiento. Por otro lado, en algunos países (p. ej., Canadá) no existe un período de licencia obligatoria, ya que se considera que la licencia es un derecho que debe ejercerse libremente y que el tiempo libre debe organizarse para adaptarse a las necesidades individuales de la mujer. y preferencias.
Elegibilidad para la licencia de maternidad
La legislación de la mayoría de los países reconoce el derecho de la mujer a la licencia de maternidad al establecer la cantidad de licencia a la que tiene derecho la mujer; una mujer solo necesita estar empleada en el momento de tomar la licencia para tener derecho a la licencia. Sin embargo, en varios países, la ley exige que las mujeres hayan estado empleadas durante un período mínimo anterior a la fecha en que se ausentaron. Este período oscila entre 13 semanas en Ontario o Irlanda y dos años en Zambia.
En varios países, las mujeres deben haber trabajado un cierto número de horas a la semana o al mes para tener derecho a la licencia o beneficios por maternidad. Cuando tales umbrales son altos (como en Malta, 35 horas por semana), pueden resultar en la exclusión de un gran número de mujeres, que constituyen la mayoría de los trabajadores a tiempo parcial. En varios países, sin embargo, los umbrales se han reducido recientemente (p. ej., en Irlanda, de 16 a XNUMX horas por semana).
Un pequeño número de países limitan el número de veces que una mujer puede solicitar la licencia de maternidad durante un período determinado (por ejemplo, dos años), o restringen la elegibilidad a un cierto número de embarazos, ya sea con el mismo empleador o a lo largo de la vida de la mujer (por ejemplo, Egipto, Malasia). En Zimbabue, por ejemplo, las mujeres tienen derecho a la licencia de maternidad una vez cada 24 meses y un máximo de tres veces durante el período en que trabajan para el mismo empleador. En otros países, las mujeres que tienen más hijos del número prescrito son elegibles para la licencia de maternidad, pero no para los beneficios en efectivo (por ejemplo, Tailandia), o son elegibles para un período más corto de licencia con beneficios (por ejemplo, Sri Lanka: 12 semanas para los dos primeros hijos, seis semanas para el tercero y siguientes). El número de países que limitan la elegibilidad para el permiso o las prestaciones de maternidad a un número determinado de embarazos, hijos o hijos supervivientes (entre dos y cuatro) parece ir en aumento, aunque no es seguro que la duración del permiso de maternidad sea un factor decisivo. factor en la motivación de las decisiones sobre el tamaño de la familia.
Aviso previo al empleador
En la mayoría de los países, el único requisito para que las mujeres tengan derecho a la licencia de maternidad es la presentación de un certificado médico. En otros lugares, también se exige a las mujeres que notifiquen a su empleador su intención de tomar la licencia de maternidad. El período de preaviso va desde el momento en que se conoce el embarazo (p. ej., Alemania) hasta una semana antes de la baja (p. ej., Bélgica). El incumplimiento del requisito de notificación puede hacer perder a la mujer su derecho a la licencia de maternidad. Por lo tanto, en Irlanda, la información sobre el momento de la licencia de maternidad debe proporcionarse tan pronto como sea razonablemente posible, pero a más tardar cuatro semanas antes del comienzo de la licencia. Una empleada pierde su derecho a la licencia de maternidad si no cumple con este requisito. En Canadá (federal), se renuncia al requisito de notificación cuando existe una razón válida por la que no se puede dar la notificación; a nivel provincial, el plazo de preaviso oscila entre cuatro meses y dos semanas. Si no se cumple con el período de preaviso, una mujer trabajadora todavía tiene derecho a la licencia de maternidad normal en Manitoba; ella tiene derecho a períodos más cortos (generalmente seis semanas en lugar de 17 o 18) en la mayoría de las demás provincias. En otros países, la ley no aclara las consecuencias de la falta de notificación.
Beneficios en efectivo
La mayoría de las mujeres no pueden darse el lujo de perder sus ingresos durante la licencia de maternidad; si tuvieran que hacerlo, muchos no utilizarían todo su permiso. Dado que el nacimiento de niños saludables beneficia a toda la nación, por una cuestión de equidad, los empleadores no deben asumir el costo total de las ausencias de sus trabajadores. Desde 1919, las normas de la OIT han establecido que durante la licencia de maternidad, las mujeres deben recibir beneficios en efectivo y que estos deben pagarse con fondos públicos o mediante un sistema de seguro. El Convenio núm. 103 exige que las cotizaciones adeudadas en virtud de un régimen de seguro social obligatorio se paguen sobre la base del número total de hombres y mujeres empleados por las empresas de que se trate, sin distinción de sexo. Aunque en unos pocos países las prestaciones de maternidad representan sólo un porcentaje relativamente pequeño de los salarios, el nivel de dos tercios exigido en el Convenio núm. 103 se alcanza en varios y se supera en muchos otros. En más de la mitad de los países encuestados, las prestaciones de maternidad constituyen el 100% del salario asegurado o del salario completo.
Muchas leyes de seguridad social pueden proporcionar un beneficio de maternidad específico, reconociendo así la maternidad como una contingencia por derecho propio. Otros prevén que durante la licencia de maternidad, la trabajadora tendrá derecho a prestaciones por enfermedad o desempleo. Tratar la maternidad como una incapacidad o el permiso como un período de desempleo podría considerarse un trato desigual ya que, en general, tales beneficios solo están disponibles durante un período determinado, y las mujeres que los utilizan en relación con la maternidad pueden encontrar que no les queda suficiente. para cubrir períodos posteriores de enfermedad o desempleo. De hecho, cuando se redactó la Directiva del Consejo Europeo de 1992, se cuestionó enérgicamente la propuesta de que durante la licencia de maternidad las mujeres recibieran prestaciones por enfermedad; se argumentó que en términos de igualdad de trato entre hombres y mujeres, la maternidad debía ser reconocida como un motivo independiente para obtener beneficios. Como compromiso, el subsidio de maternidad se definió como la garantía de un ingreso por lo menos equivalente al que recibiría la trabajadora en caso de enfermedad.
En casi 80 de los países encuestados, las prestaciones son pagadas por los regímenes nacionales de seguridad social, y en más de 40, estas corren a cargo del empleador. En unos 15 países, la responsabilidad de financiar las prestaciones de maternidad se comparte entre la seguridad social y el empleador. Cuando los beneficios son financiados conjuntamente por la seguridad social y el empleador, se puede exigir que cada uno pague la mitad (p. ej., Costa Rica), aunque se pueden encontrar otros porcentajes (p. ej., Honduras: dos tercios por la seguridad social y un tercio por el empleador). ). Se puede exigir otro tipo de contribución a los empleadores: cuando el monto de la prestación de maternidad pagada por la seguridad social se basa en un ingreso asegurable por ley y representa un porcentaje bajo del salario total de una mujer, la ley a veces establece que el empleador pagará el saldo entre el salario de la mujer y el beneficio de maternidad pagado por el fondo de seguridad social (por ejemplo, en Burkina Faso). El pago adicional voluntario por parte del empleador es una característica de muchos convenios colectivos y también de los contratos de trabajo individuales. La participación de los empleadores en el pago de las prestaciones de maternidad en efectivo puede ser una solución realista al problema que plantea la falta de otros fondos.
Protección de la Salud de las Mujeres Embarazadas y Lactantes
En consonancia con los requisitos de la Recomendación sobre la protección de la maternidad, 1952 (núm. 95), muchos países prevén diversas medidas para proteger la salud de las mujeres embarazadas y sus hijos, buscando minimizar la fatiga mediante la reorganización del tiempo de trabajo o proteger a las mujeres contra trabajos peligrosos o insalubres.
En algunos países (p. ej., los Países Bajos, Panamá), la ley especifica la obligación del empleador de organizar el trabajo para que no afecte el resultado del embarazo. Este enfoque, que está en consonancia con la práctica moderna de salud y seguridad en el trabajo, permite hacer coincidir las necesidades de cada mujer con las medidas preventivas correspondientes y, por lo tanto, es muy satisfactorio. De manera mucho más general, la protección se busca prohibiendo o limitando el trabajo que puede ser perjudicial para la salud de la madre o el niño. Tal prohibición puede redactarse en términos generales o puede aplicarse a ciertos tipos de trabajo peligroso. Sin embargo, en México, la prohibición de emplear a mujeres en trabajos insalubres o peligrosos no aplica si se han tomado las medidas necesarias de protección de la salud, a juicio de la autoridad competente; tampoco se aplica a las mujeres en cargos directivos o que cuenten con título universitario o diploma técnico, o con los conocimientos y experiencia necesarios para desempeñar el trabajo.
En muchos países, la ley establece que no se puede permitir que las mujeres embarazadas y las madres lactantes realicen trabajos que “están más allá de sus fuerzas”, que “implican riesgos”, “es peligroso para su salud o la de sus hijos” o “requiere un esfuerzo físico no adecuado a su condición”. Sin embargo, la aplicación de una prohibición general de este tipo puede presentar problemas: ¿cómo y por quién se determinará que un trabajo está más allá de las fuerzas de una persona? ¿Por el trabajador en cuestión, el empleador, el inspector de trabajo, el médico de salud ocupacional, el médico de la propia mujer? Las diferencias de apreciación pueden conducir a que una mujer se mantenga alejada del trabajo que de hecho podría hacer, mientras que otra puede no ser apartada del trabajo que es demasiado exigente.
Otros países enumeran, a veces con gran detalle, el tipo de trabajo que está prohibido para las mujeres embarazadas y las madres lactantes (p. ej., Austria, Alemania). El manejo de cargas está frecuentemente regulado. La legislación de algunos países prohíbe específicamente la exposición a determinados productos químicos (p. ej., benceno), agentes biológicos, plomo y radiación. El trabajo subterráneo está prohibido en Japón durante el embarazo y un año después del parto. En Alemania, el trabajo a destajo y el trabajo en una cadena de montaje con un ritmo fijo están prohibidos. En unos pocos países, las trabajadoras embarazadas pueden no ser asignadas a trabajar fuera de su lugar de residencia permanente (p. ej., Ghana, después del cuarto mes). En Austria, no está permitido fumar en lugares donde trabajan mujeres embarazadas.
En varios países (por ejemplo, Angola, Bulgaria, Haití, Alemania), el empleador está obligado a transferir al trabajador a un trabajo adecuado. A menudo, la trabajadora debe conservar su salario anterior incluso si el salario del puesto al que es trasladada es inferior. En la República Democrática Popular Lao, la mujer mantiene su salario anterior durante un período de tres meses, y luego se le paga a la tarifa correspondiente al trabajo que realmente está desempeñando. En la Federación Rusa, donde se va a dar un puesto adecuado a una mujer que ya no puede realizar su trabajo, conserva su salario durante el período en que se encuentra un nuevo puesto. En ciertos casos (p. ej., Rumania), la diferencia entre los dos salarios la paga la seguridad social, un arreglo al que se hace referencia, ya que el costo de la protección de la maternidad no debería, en la medida de lo posible, ser sufragado por empleadores individuales.
La transferencia también puede estar disponible desde un trabajo que no es peligroso en sí mismo pero que un médico ha certificado que es perjudicial para el estado de salud de una mujer en particular (p. ej., Francia). En otros países, la transferencia es posible a petición del trabajador en cuestión (p. ej., Canadá, Suiza). Cuando la ley permita al empleador sugerir una transferencia, si hay un desacuerdo entre el empleador y el trabajador, un médico ocupacional determinará si existe alguna necesidad médica para cambiar de trabajo y si el trabajador es apto para asumir el trabajo que tiene. le han sugerido.
Unos pocos países aclaran el hecho de que la transferencia es temporal y que la trabajadora debe ser reasignada a su trabajo anterior cuando regrese de la licencia de maternidad o en un momento específico posterior (p. ej., Francia). Cuando no es posible una transferencia, algunos países prevén que se concederá a la trabajadora licencia por enfermedad (p. ej., Seychelles) o, como se discutió anteriormente, que la licencia por maternidad comenzará antes (p. ej., Islandia).
No discriminación
En un número creciente de países se toman medidas para garantizar que las mujeres no sufran discriminación por motivos de embarazo. Su objetivo es garantizar que las mujeres embarazadas sean consideradas para el empleo y tratadas durante el empleo en igualdad de condiciones con los hombres y con otras mujeres y, en particular, no sean degradadas, no pierdan antigüedad o no se les niegue el ascenso únicamente por motivos de embarazo. Ahora es cada vez más común que la legislación nacional prohíba la discriminación por razón de sexo. Tal prohibición podría ser, y de hecho ha sido en muchos casos, interpretada por los tribunales como una prohibición de discriminar por motivos de embarazo. El Tribunal de Justicia de las Comunidades Europeas ha seguido este enfoque. En una sentencia de 1989, el Tribunal dictaminó que un empleador que despide o se niega a contratar a una mujer porque está embarazada infringe la Directiva 76/207/CEE del Consejo Europeo sobre igualdad de trato. Esta sentencia fue importante para aclarar el hecho de que existe discriminación sexual cuando las decisiones de empleo se toman sobre la base del embarazo, aunque la ley no menciona específicamente el embarazo como motivo prohibido de discriminación. Es costumbre en casos de igualdad de sexos comparar el trato dado a una mujer con el trato dado a un hombre hipotético. La Corte dictaminó que tal comparación no era necesaria en el caso de una mujer embarazada, ya que el embarazo es exclusivo de las mujeres. Cuando se da un trato desfavorable por motivos de embarazo, existe por definición discriminación por motivos de sexo. Esto es coherente con la posición de la Comisión de Expertos en Aplicación de Convenios y Recomendaciones de la OIT relativa al alcance del Convenio sobre la discriminación (empleo y ocupación), 1958 (núm. 111), que señala el carácter discriminatorio de las distinciones basadas en embarazo, parto y condiciones médicas relacionadas (OIT 1988).
Varios países prevén una prohibición explícita de la discriminación por motivos de embarazo (p. ej., Australia, Italia, EE. UU., Venezuela). Otros países definen la discriminación por motivos de sexo para incluir la discriminación por motivos de embarazo o ausencia por licencia de maternidad (p. ej., Finlandia). En los EE. UU., la protección se garantiza aún más al tratar el embarazo como una discapacidad: en empresas con más de 15 trabajadores, se prohíbe la discriminación contra las mujeres embarazadas, las mujeres que dan a luz y las mujeres afectadas por afecciones médicas relacionadas; y las políticas y prácticas relacionadas con el embarazo y asuntos relacionados deben aplicarse en los mismos términos y condiciones que se aplican a otras discapacidades.
En varios países, la ley contiene requisitos precisos que ilustran casos de discriminación por motivos de embarazo. Por ejemplo, en la Federación Rusa, un empleador no puede negarse a contratar a una mujer porque está embarazada; si no se contrata a una mujer embarazada, el empleador debe exponer por escrito las razones por las cuales no la contrata. En Francia, es ilegal que un empleador tenga en cuenta el embarazo al negarse a emplear a una mujer, al rescindir su contrato durante un período de prueba o al ordenar su traslado. También es ilegal que el empleador intente determinar si una solicitante está embarazada o que haga que se busque dicha información. Asimismo, no se puede exigir a las mujeres que revelen el hecho de que están embarazadas, ya sea que soliciten un empleo o estén empleadas en uno, excepto cuando soliciten acogerse a alguna ley o reglamento que regule la protección de las mujeres embarazadas.
Las transferencias impuestas unilateral y arbitrariamente a una mujer embarazada pueden constituir discriminación. En Bolivia, como en otros países de la región, la mujer está protegida contra la transferencia involuntaria durante el embarazo y hasta un año después del nacimiento de su hijo.
La cuestión de combinar el derecho de las mujeres trabajadoras a la protección de la salud durante el embarazo y su derecho a no sufrir discriminación plantea una dificultad especial a la hora de la contratación. ¿Debe una candidata embarazada revelar su condición, especialmente una que solicita un puesto que implica un trabajo que está prohibido para las mujeres embarazadas? En una sentencia de 1988, el Tribunal Laboral Federal de Alemania sostuvo que una mujer embarazada que solicita un trabajo exclusivamente nocturno, que está prohibido para mujeres embarazadas según la legislación alemana, debe informar a un empleador potencial de su condición. La sentencia fue anulada por el Tribunal de Justicia de las Comunidades Europeas por ser contraria a la Directiva de la CE de 1976 sobre igualdad de trato. El Tribunal consideró que la Directiva impedía que un contrato de trabajo se declarara nulo debido a la prohibición legal del trabajo nocturno, o que el empleador lo anulara debido a un error de su parte en cuanto a una característica personal esencial de la mujer en el momento de la celebración del contrato. La incapacidad de la empleada, a causa del embarazo, para realizar el trabajo para el que fue contratada fue temporal ya que el contrato no se celebró con un plazo fijo. Por lo tanto, sería contrario al objetivo de la Directiva declararla inválida o nula por tal incapacidad.
Seguridad laboral
Muchas mujeres han perdido su trabajo a causa de un embarazo. Hoy en día, aunque el grado de protección varía, la seguridad en el empleo es un componente importante de las políticas de protección de la maternidad.
Las normas internacionales del trabajo abordan el tema de dos maneras diferentes. Los Convenios de protección de la maternidad prohíben el despido durante la licencia de maternidad y cualquier prórroga de la misma, o en el momento en que la notificación de despido expiraría durante la licencia en los términos del Convenio núm. 3, artículo 4 y el Convenio núm. 103, artículo 6. Despido por motivos que podrían considerarse legítimos no se consideran permitidos durante este período (OIT 1965). En caso de que una mujer haya sido despedida antes de irse de baja por maternidad, el preaviso debe suspenderse por el tiempo que ella esté ausente y continuar después de su regreso. La Recomendación sobre la protección de la maternidad, 1952 (núm. 95), exige la protección del empleo de una mujer embarazada desde la fecha en que se informa al empleador del embarazo hasta un mes después de su regreso de la licencia de maternidad. Identifica los casos de falta grave de la mujer empleada, el cierre de la empresa y la extinción del contrato de duración determinada como causas legítimas de despido durante el período protegido. El Convenio sobre la terminación de la relación laboral, 1982 (núm. 158; artículo 5, d) a e)), no prohíbe el despido, pero establece que el embarazo o la ausencia del trabajo con licencia de maternidad no constituirán razones válidas para la terminación de la relación laboral.
A nivel de la Unión Europea, la Directiva de 1992 prohíbe el despido desde el inicio del embarazo hasta el final del permiso de maternidad, salvo casos excepcionales no relacionados con la condición de la trabajadora.
Por lo general, los países prevén dos conjuntos de reglas con respecto al despido. El despido con preaviso se aplica en casos tales como el cierre de la empresa, el despido y cuando, por diversas razones, el trabajador no puede realizar el trabajo para el que ha sido contratado o no lo hace a satisfacción del empleador. . El despido sin preaviso se utiliza para rescindir los servicios de un trabajador que es culpable de negligencia grave, falta grave de conducta u otros comportamientos graves, generalmente detallados en la legislación.
En lo que se refiere al despido con preaviso, es evidente que los empleadores pueden arbitrariamente decidir que el embarazo es incompatible con las tareas de una trabajadora y despedirla por motivo de embarazo. Aquellos que deseen eludir sus obligaciones con las mujeres embarazadas, o simplemente no les guste tener mujeres embarazadas en el lugar de trabajo, podrían encontrar un pretexto para despedir a los trabajadores durante el embarazo incluso si, en vista de la existencia de normas de no discriminación, abstenerse de utilizar el embarazo como causal de despido. Mucha gente está de acuerdo en que es legítimo proteger a los trabajadores contra tales decisiones discriminatorias: la prohibición del despido con preaviso por motivos de embarazo o durante el embarazo y la licencia de maternidad se considera a menudo como una medida de equidad y está vigente en muchos países.
El Comité de Expertos en Aplicación de Convenios y Recomendaciones de la OIT considera que la protección contra el despido no impide que un empleador rescinda una relación laboral porque haya detectado una falta grave por parte de una trabajadora: más bien, cuando existen razones como éste para justificar el despido, el empleador está obligado a prorrogar el plazo legal de preaviso por cualquier período necesario para completar el período de protección en virtud de los Convenios. Esta es la situación, por ejemplo, en Bélgica, donde un empleador que tiene motivos legales para despedir a una mujer no puede hacerlo mientras ella está en licencia de maternidad, pero puede notificar para que expire después de que la mujer regrese de la licencia.
La protección de las mujeres embarazadas contra el despido en caso de cierre de la empresa o reducción económica plantea un problema similar. De hecho, es una carga para una empresa que deja de operar continuar pagando el salario de una persona que ya no trabaja para ellos, incluso por un período breve. Sin embargo, las perspectivas de contratación suelen ser más sombrías para las mujeres embarazadas que para las mujeres que no lo están, o para los hombres, y las mujeres embarazadas necesitan especialmente la seguridad emocional y financiera de seguir trabajando. Cuando las mujeres no pueden ser despedidas durante el embarazo, pueden postergar la búsqueda de trabajo hasta después del parto. De hecho, cuando la legislación establece el orden en que deben despedirse varias categorías de trabajadores, las mujeres embarazadas se encuentran entre los últimos o penúltimos en ser despedidos (por ejemplo, Etiopía).
Licencia y beneficios para padres y madres
Más allá de la protección de la salud y la situación laboral de las mujeres embarazadas y lactantes, muchos países prevén la licencia de paternidad (un breve período de licencia en el momento del nacimiento o cerca de este). Otras formas de licencia están vinculadas a las necesidades de los niños. Un tipo es la licencia por adopción y otro es la licencia para facilitar la crianza de los hijos. Muchos países prevén este último tipo de licencia, pero utilizan diferentes enfoques. Un grupo prevé tiempo libre para la madre de niños muy pequeños (licencia de maternidad opcional), mientras que otro proporciona licencia adicional para ambos padres (licencia de educación de los padres). La opinión de que tanto el padre como la madre deben estar disponibles para cuidar a los niños pequeños también se refleja en los sistemas de licencia parental integrados, que proporcionan un largo período de licencia disponible para ambos padres.
Recomendaciones para el embarazo y el trabajo en EE. UU.
Los cambios en la vida familiar en las últimas décadas han tenido efectos dramáticos en la relación entre el trabajo y el embarazo. Estos incluyen lo siguiente:
- Las mujeres, en particular las que están en edad de procrear, continúan ingresando a la fuerza laboral en cantidades considerables.
- Se ha desarrollado una tendencia por parte de muchas de estas mujeres a diferir el inicio de sus familias hasta que son mayores, momento en el que a menudo han alcanzado puestos de responsabilidad y se han convertido en miembros importantes del aparato productivo.
- Al mismo tiempo, hay un número creciente de embarazos adolescentes, muchos de los cuales son embarazos de alto riesgo.
- Como reflejo de las crecientes tasas de separación, de divorcio y de opciones de estilos de vida alternativos, así como del aumento del número de familias en las que ambos padres deben trabajar, las presiones financieras están obligando a muchas mujeres a seguir trabajando el mayor tiempo posible durante el embarazo.
El impacto de las ausencias relacionadas con el embarazo y la pérdida o disminución de la productividad, así como la preocupación por la salud y el bienestar tanto de las madres como de sus bebés, han llevado a los empleadores a ser más proactivos en el tratamiento del problema del embarazo y el trabajo. Cuando los empleadores pagan la totalidad o parte de las primas del seguro de salud, la perspectiva de evitar los costos a veces abrumadores de embarazos complicados y problemas neonatales es un incentivo potente. Ciertas respuestas están dictadas por leyes y reglamentos gubernamentales, por ejemplo, la protección contra posibles riesgos laborales y ambientales y la concesión de licencias por maternidad y otros beneficios. Otros son voluntarios: programadores de atención y educación prenatal, arreglos de trabajo modificados como horarios flexibles y otros arreglos de horarios de trabajo, cuidado de dependientes y otros beneficios.
Manejo del embarazo
De primordial importancia para la mujer embarazada, y para su empleador, ya sea que continúe o no trabajando durante el embarazo, es el acceso a un programa profesional de gestión de la salud diseñado para identificar y evitar o minimizar los riesgos para la madre y el feto, permitiéndole así permanecer en el trabajo sin preocupaciones. En cada una de las visitas prenatales programadas, el médico o la partera debe evaluar la información médica (antecedentes médicos y de maternidad, quejas actuales, exámenes físicos y pruebas de laboratorio) y la información sobre su trabajo y entorno laboral, y desarrollar las recomendaciones apropiadas.
Es importante que los profesionales de la salud no confíen en las simples descripciones de funciones relacionadas con el trabajo de sus pacientes, ya que a menudo son inexactas y engañosas. La información del trabajo debe incluir detalles sobre la actividad física, la exposición a sustancias químicas y de otro tipo y el estrés emocional, la mayoría de los cuales pueden ser proporcionados por la propia mujer. En algunos casos, sin embargo, puede ser necesario el aporte de un supervisor, a menudo transmitido por el departamento de seguridad o el servicio de salud de los empleados (donde haya uno), para proporcionar una imagen más completa de las actividades laborales peligrosas o difíciles y la posibilidad de controlar su potencial de daño. Esto también puede servir para controlar a los pacientes que inadvertida o deliberadamente engañan a sus médicos; pueden exagerar los riesgos o, si creen que es importante seguir trabajando, pueden subestimarlos.
Recomendaciones para el trabajo
Las recomendaciones sobre el trabajo durante el embarazo se dividen en tres categorías:
La mujer puede continuar trabajando sin cambios en sus actividades o el medio ambiente. Esto es aplicable en la mayoría de los casos. Después de una extensa deliberación, el Grupo de Trabajo sobre la Discapacidad del embarazo compuesto por profesionales de la salud obstétrica, médicos y enfermeras ocupacionales y representantes de mujeres reunidos por ACOG (Colegio Estadounidense de Obstetras y Ginecólogos) y NIOSH (Instituto Nacional para la Seguridad y Salud Ocupacional) concluyó que “la mujer normal con un embarazo sin complicaciones que tiene un trabajo que no presenta mayores riesgos que los que se encuentran en la vida diaria normal en la comunidad, puede continuar trabajando sin interrupción hasta el inicio del trabajo de parto y puede reanudar el trabajo varias semanas después de un parto sin complicaciones”. entrega” (Isenman y Warshaw, 1977).
La mujer puede continuar trabajando, pero solo con ciertas modificaciones en el ambiente de trabajo o en sus actividades laborales. Estas modificaciones serían o “deseables” o “imprescindibles” (en este último caso, debería dejar de trabajar si no se pueden realizar).
La mujer no debe trabajar.. A juicio del médico o de la matrona, cualquier trabajo probablemente sería perjudicial para su salud o la del feto en desarrollo.
Las recomendaciones no solo deben detallar las modificaciones laborales necesarias, sino que también deben estipular la duración de su vigencia e indicar la fecha del próximo examen profesional.
Consideraciones no médicas
Las recomendaciones sugeridas anteriormente se basan enteramente en consideraciones de la salud de la madre y su feto en relación con los requisitos del trabajo. No tienen en cuenta la carga de actividades fuera del trabajo, como los desplazamientos hacia y desde el lugar de trabajo, las tareas domésticas y el cuidado de otros niños y miembros de la familia; estos a veces pueden ser incluso más exigentes que los del trabajo. Cuando se requiere la modificación o restricción de actividades, se debe considerar la cuestión de si debe implementarse en el trabajo, en el hogar o en ambos.
Además, las recomendaciones a favor o en contra de continuar con el trabajo pueden formar la base de una variedad de consideraciones no médicas, por ejemplo, elegibilidad para beneficios, licencia con goce de sueldo o sin goce de sueldo o retención laboral garantizada. Una cuestión crítica es si la mujer se considera discapacitada. Algunos empleadores categóricamente consideran discapacitadas a todas las trabajadoras embarazadas y se esfuerzan por eliminarlas de la fuerza laboral, aunque muchas pueden continuar trabajando. Otros empleadores asumen que todas las empleadas embarazadas tienden a magnificar cualquier discapacidad para ser elegibles para todos los beneficios disponibles. Y algunos incluso cuestionan la noción de que un embarazo, incapacitante o no, es un asunto que les deba preocupar en absoluto. Así, la discapacidad es un concepto complejo que, si bien se basa fundamentalmente en hallazgos médicos, implica consideraciones jurídicas y sociales.
Embarazo y Discapacidad
En muchas jurisdicciones, es importante distinguir entre la discapacidad del embarazo y el embarazo como un período de la vida que exige beneficios y dispensas especiales. La discapacidad del embarazo se divide en tres categorías:
- Invalidez tras el parto. Desde un punto de vista puramente médico, la recuperación después de la interrupción del embarazo a través de un parto sin complicaciones dura solo unas pocas semanas, pero convencionalmente se extiende a seis u ocho semanas porque es cuando la mayoría de los obstetras programan habitualmente su primer control posnatal. Sin embargo, desde un punto de vista práctico y sociológico, muchos consideran deseable una licencia más prolongada para mejorar los lazos familiares, facilitar la lactancia materna, etc.
- Invalidez resultante de complicaciones médicas.. Las complicaciones médicas como la eclampsia, la amenaza de aborto, los problemas cardiovasculares o renales, etc., dictarán periodos de reducción de actividad o incluso de hospitalización que durarán mientras persista la condición médica o hasta que la mujer se haya recuperado tanto del problema médico como del embarazo. .
- Discapacidad que refleja la necesidad de evitar la exposición a peligros de toxicidad o estrés físico anormal. Debido a la mayor sensibilidad del feto a muchos peligros ambientales, la mujer embarazada puede considerarse incapacitada aunque su propia salud no corra peligro de verse comprometida.
Conclusión
El desafío de equilibrar las responsabilidades familiares y el trabajo fuera del hogar no es nuevo para las mujeres. Lo que puede ser nuevo es una sociedad moderna que valore la salud y el bienestar de las mujeres y sus hijos, al mismo tiempo que confronta a las mujeres con el doble desafío de lograr la realización personal a través del empleo y hacer frente a las presiones económicas de mantener un nivel de vida aceptable. El número cada vez mayor de padres solteros y de parejas casadas que deben trabajar sugiere que no se pueden ignorar las cuestiones trabajo-familia. Muchas mujeres empleadas que quedan embarazadas simplemente deben continuar trabajando.
¿De quién es la responsabilidad de satisfacer las necesidades de estas personas? Algunos argumentarían que es un problema puramente personal que debe ser tratado por completo por el individuo o la familia. Otros lo consideran una responsabilidad social y promulgarían leyes y proporcionarían beneficios financieros y de otro tipo a toda la comunidad.
¿Cuánto se debe cargar en el empleador? Esto depende en gran medida de la naturaleza, la ubicación y, a menudo, del tamaño de la organización. El empleador se rige por dos conjuntos de consideraciones: las impuestas por las leyes y los reglamentos (ya veces por la necesidad de satisfacer las demandas ganadas por el trabajo organizado) y las dictadas por la responsabilidad social y la necesidad práctica de mantener una productividad óptima. En última instancia, depende de otorgar un alto valor a los recursos humanos y reconocer la interdependencia de las responsabilidades laborales y los compromisos familiares y sus efectos a veces compensatorios sobre la salud y la productividad.
Estructura y función
El sistema respiratorio se extiende desde la zona de respiración justo fuera de la nariz y la boca a través de las vías respiratorias conductoras en la cabeza y el tórax hasta los alvéolos, donde tiene lugar el intercambio de gases respiratorios entre los alvéolos y la sangre capilar que fluye a su alrededor. Su función principal es entregar oxígeno (O2) a la región de intercambio de gases del pulmón, donde puede difundirse hacia y a través de las paredes de los alvéolos para oxigenar la sangre que pasa a través de los capilares alveolares según sea necesario en una amplia gama de niveles de trabajo o actividad. Además, el sistema también debe: (1) eliminar un volumen igual de dióxido de carbono que ingresa a los pulmones desde los capilares alveolares; (2) mantener la temperatura corporal y la saturación de vapor de agua dentro de las vías respiratorias de los pulmones (para mantener la viabilidad y las capacidades funcionales de los fluidos y células superficiales); (3) mantener la esterilidad (para prevenir infecciones y sus consecuencias adversas); y (4) eliminar el exceso de fluidos superficiales y desechos, tales como partículas inhaladas y células fagocíticas y epiteliales senescentes. Debe realizar todas estas tareas exigentes de forma continua durante toda la vida y hacerlo con una alta eficiencia en términos de rendimiento y utilización de energía. El sistema puede ser abusado y abrumado por agresiones graves, como altas concentraciones de humo de cigarrillo y polvo industrial, o por bajas concentraciones de patógenos específicos que atacan o destruyen sus mecanismos de defensa, o provocan su mal funcionamiento. Su capacidad para superar o compensar tales insultos de manera tan competente como lo hace habitualmente es un testimonio de su elegante combinación de estructura y función.
Transferencia de masa
La estructura compleja y las numerosas funciones de las vías respiratorias humanas han sido resumidas de forma concisa por un grupo de trabajo de la Comisión Internacional de Protección Radiológica (ICRP 1994), como se muestra en la figura 1. Las vías respiratorias conductoras, también conocidas como espacio muerto respiratorio, ocupan unos 0.2 litros. Acondicionan el aire inhalado y lo distribuyen, mediante flujo convectivo (a granel), a los aproximadamente 65,000 ácinos respiratorios que salen de los bronquiolos terminales. A medida que aumentan los volúmenes corrientes, el flujo convectivo domina el intercambio de gases más profundamente en los bronquiolos respiratorios. En cualquier caso, dentro del ácino respiratorio, la distancia desde el frente de marea convectivo hasta las superficies alveolares es lo suficientemente corta como para que el CO eficiente2-O2 el intercambio tiene lugar por difusión molecular. Por el contrario, las partículas en el aire, con coeficientes de difusión más pequeños en órdenes de magnitud que los de los gases, tienden a permanecer suspendidas en el aire de las mareas y pueden exhalarse sin depositarse.
Figura 1. Morfometría, citología, histología, función y estructura del tracto respiratorio y regiones utilizadas en el modelo dosimétrico ICRP de 1994.
Una fracción significativa de las partículas inhaladas se deposita en el tracto respiratorio. En la figura 2 se resumen los mecanismos que explican el depósito de partículas en las vías respiratorias de los pulmones durante la fase inspiratoria de una respiración tidal. puede tener un impulso significativo y depositarse por impacto a las velocidades relativamente altas presentes en las vías respiratorias más grandes. Las partículas mayores de aproximadamente 2 mm pueden depositarse por sedimentación en las vías respiratorias conductoras más pequeñas, donde las velocidades de flujo son muy bajas. Finalmente, las partículas con diámetros entre 1 y 0.1 mm, que tienen una probabilidad muy baja de depositarse durante una sola respiración tidal, pueden retenerse dentro de aproximadamente el 1 % del aire tidal inspirado que se intercambia con el aire pulmonar residual durante cada ciclo tidal. Este intercambio volumétrico ocurre debido a las constantes de tiempo variables para el flujo de aire en los diferentes segmentos de los pulmones. Debido a los tiempos de residencia mucho más largos del aire residual en los pulmones, los bajos desplazamientos intrínsecos de partículas de 15 a 0.1 mm dentro de tales volúmenes atrapados de aire inhalado se vuelven suficientes para causar su depósito por sedimentación y/o difusión en el transcurso de respiraciones sucesivas.
Figura 2. Mecanismos de depósito de partículas en las vías respiratorias pulmonares
El aire pulmonar residual esencialmente libre de partículas que representa aproximadamente el 15% del flujo corriente espiratorio tiende a actuar como una vaina de aire limpio alrededor del núcleo axial del aire corriente que se mueve distalmente, de modo que la deposición de partículas en el ácino respiratorio se concentra en el interior. superficies como las bifurcaciones de las vías respiratorias, mientras que las paredes de las vías respiratorias entre ramas tienen poca deposición.
El número de partículas depositadas y su distribución a lo largo de las superficies del tracto respiratorio son, junto con las propiedades tóxicas del material depositado, los determinantes críticos del potencial patógeno. Las partículas depositadas pueden dañar las células epiteliales y/o fagocíticas móviles en o cerca del sitio de depósito, o pueden estimular la secreción de fluidos y mediadores derivados de células que tienen efectos secundarios en el sistema. Los materiales solubles depositados como, sobre o dentro de las partículas pueden difundirse hacia ya través de los fluidos y células de la superficie y ser transportados rápidamente por el torrente sanguíneo por todo el cuerpo.
La solubilidad acuosa de los materiales a granel es una mala guía para la solubilidad de las partículas en el tracto respiratorio. La solubilidad generalmente aumenta en gran medida por la gran proporción de superficie a volumen de partículas lo suficientemente pequeñas como para ingresar a los pulmones. Además, los contenidos iónicos y lipídicos de los fluidos superficiales dentro de las vías respiratorias son complejos y muy variables, y pueden conducir a una mayor solubilidad o a una rápida precipitación de solutos acuosos. Además, las vías de eliminación y los tiempos de residencia de las partículas en las superficies de las vías respiratorias son muy diferentes en las distintas partes funcionales de las vías respiratorias.
El modelo de limpieza revisado del Grupo de trabajo de la ICRP identifica las principales vías de limpieza dentro del tracto respiratorio que son importantes para determinar la retención de varios materiales radiactivos y, por lo tanto, las dosis de radiación recibidas por los tejidos respiratorios y otros órganos después de la translocación. El modelo de deposición ICRP se usa para estimar la cantidad de material inhalado que ingresa a cada vía de eliminación. Estas rutas discretas están representadas por el modelo de compartimento que se muestra en la figura 3. Corresponden a los compartimentos anatómicos ilustrados en la figura 1 y se resumen en la tabla 1, junto con los de otros grupos que brindan orientación sobre la dosimetría de partículas inhaladas.
Figura 3. Modelo de compartimiento para representar el transporte de partículas dependiente del tiempo desde cada región en el modelo ICRP de 1994
Tabla 1. Regiones del tracto respiratorio definidas en los modelos de deposición de partículas
| Estructuras anatómicas incluidas | Región ACGIH | Regiones ISO y CEN | 1966 Región del grupo de tareas de la ICRP | 1994 Región del grupo de tareas de la ICRP |
| Nariz, nasofaringe Boca, orofaringe, laringofaringe |
Vías aéreas de la cabeza (HAR) | Extratorácica (E) | Nasofaringe (NP) | Fosas nasales anteriores (ET1 ) Todos los demás extratorácicos (ET2 ) |
| tráquea, bronquios | Traqueobronquial (TBR) | Traqueobronquial (B) | Traqueobronquial (TB) | Tráquea y grandes bronquios (BB) |
| Bronquiolos (a bronquiolos terminales) | Bronquiolos (bb) | |||
| bronquiolos respiratorios, conductos alveolares, sacos alveolares, alvéolos |
Intercambio de gases (GER) | Alveolar (A) | Pulmonar (P) | Alveolar-intersticial (AI) |
vías respiratorias extratorácicas
Como se muestra en la figura 1, la ICRP (1994) dividió las vías respiratorias extratorácicas en dos regiones de aclaramiento y dosimétricas distintas: las fosas nasales anteriores (ET1) y todas las demás vías respiratorias extratorácicas (ET2), es decir, las fosas nasales posteriores, la naso- y la orofaringe, y la laringe. Partículas depositadas en la superficie de la piel que recubre las fosas nasales anteriores (ET1) se supone que están sujetos únicamente a la eliminación por medios extrínsecos (sonarse la nariz, limpiarse, etc.). La mayor parte del material depositado en la naso-orofaringe o laringe (ET2) está sujeto a una eliminación rápida en la capa de líquido que cubre estas vías respiratorias. El nuevo modelo reconoce que la deposición por difusión de partículas ultrafinas en las vías respiratorias extratorácicas puede ser sustancial, mientras que los modelos anteriores no lo hacían.
vías respiratorias torácicas
El material radiactivo depositado en el tórax generalmente se divide entre la región traqueobronquial (TB), donde las partículas depositadas están sujetas a una eliminación mucociliar relativamente rápida, y la región alveolar-intersticial (AI), donde la eliminación de partículas es mucho más lenta.
A efectos de dosimetría, la ICRP (1994) dividió el depósito de material inhalado en la región de la tuberculosis entre la tráquea y los bronquios (BB) y las vías respiratorias pequeñas más distales, los bronquiolos (bb). Sin embargo, la eficiencia posterior con la que los cilios en cualquier tipo de vías respiratorias pueden eliminar las partículas depositadas es controvertida. Para estar seguro de que las dosis en los epitelios bronquiales y bronquiolares no se subestimarían, el grupo de trabajo asumió que hasta la mitad del número de partículas depositadas en estas vías respiratorias está sujeta a una eliminación mucociliar relativamente “lenta”. La probabilidad de que el sistema mucociliar elimine una partícula con relativa lentitud parece depender de su tamaño físico.
El material depositado en la región AI se subdivide en tres compartimentos (AI1AI2 y AI3) que se eliminan más lentamente que la deposición de TB, con las subregiones eliminadas a diferentes tasas características.
Figura 4. Deposición fraccional en cada región del tracto respiratorio para trabajadores ligeros de referencia (respirador nasal normal) en el modelo ICRP de 1994.
La figura 4 muestra las predicciones del modelo ICRP (1994) en términos de la deposición fraccional en cada región en función del tamaño de las partículas inhaladas. Refleja la deposición pulmonar mínima entre 0.1 y 1 mm, donde la deposición está determinada en gran medida por el intercambio, en el pulmón profundo, entre el aire pulmonar corriente y residual. La deposición aumenta por debajo de 0.1 mm a medida que la difusión se vuelve más eficiente al disminuir el tamaño de las partículas. La deposición aumenta con el aumento del tamaño de las partículas por encima de 1 mm a medida que la sedimentación y la impactación se vuelven cada vez más efectivas.
Los profesionales y agencias de salud ocupacional y contaminación del aire en la comunidad han adoptado modelos menos complejos para la deposición selectiva por tamaño, y estos se han utilizado para desarrollar límites de exposición por inhalación dentro de rangos específicos de tamaño de partículas. Se hacen distinciones entre:
- aquellas partículas que no son aspiradas por la nariz o la boca y por lo tanto no representan peligro de inhalación
- el inhalable (también conocido como inspirador) masa de partículas (IPM): aquellas que se inhalan y son peligrosas cuando se depositan en cualquier lugar dentro del tracto respiratorio
- la masa de partículas torácicas (TPM): aquellas que penetran en la laringe y son peligrosas cuando se depositan en cualquier lugar dentro del tórax y
- la masa de partículas respirables (RPM): aquellas partículas que penetran a través de los bronquiolos terminales y son peligrosas cuando se depositan dentro de la región de intercambio de gases de los pulmones.
A principios de la década de 1990 hubo una armonización internacional de las definiciones cuantitativas de IPM, TPM y RPM. Las especificaciones de entrada de tamaño selectivo para muestreadores de aire que cumplen con los criterios de la Conferencia Estadounidense de Higienistas Industriales Gubernamentales (ACGIH 1993), la Organización Internacional para la Estandarización (ISO 1991) y el Comité Europeo de Estandarización (CEN 1991) se enumeran en la tabla 2. difieren de las fracciones de deposición de ICRP (1994), especialmente para partículas más grandes, porque adoptan la posición conservadora de que se debe brindar protección a quienes participan en la inhalación oral y, por lo tanto, eluden la eficiencia de filtración más eficiente de las fosas nasales.
Tabla 2. Criterios de polvo inhalable, torácico y respirable de ACGIH, ISO y CEN, y PM10 criterios de la EPA de EE.UU.
| inhalables | torácica | respirable | PM10 | ||||
| partículas aero- diámetro dinámico (mm) |
inhalables Partículas Misa (MIP) (%) |
partículas aero- diámetro dinámico (mm) |
torácica Partículas Masa (TPM) (%) |
partículas aero- diámetro dinámico (mm) |
respirable Partículas Masa (RPM) (%) |
partículas aero- diámetro dinámico (mm) |
torácica Partículas Masa (TPM) (%) |
| 0 | 100 | 0 | 100 | 0 | 100 | 0 | 100 |
| 1 | 97 | 2 | 94 | 1 | 97 | 2 | 94 |
| 2 | 94 | 4 | 89 | 2 | 91 | 4 | 89 |
| 5 | 87 | 6 | 80.5 | 3 | 74 | 6 | 81.2 |
| 10 | 77 | 8 | 67 | 4 | 50 | 8 | 69.7 |
| 20 | 65 | 10 | 50 | 5 | 30 | 10 | 55.1 |
| 30 | 58 | 12 | 35 | 6 | 17 | 12 | 37.1 |
| 40 | 54.5 | 14 | 23 | 7 | 9 | 14 | 15.9 |
| 50 | 52.5 | 16 | 15 | 8 | 5 | 16 | 0 |
| 100 | 50 | 18 | 9.5 | 10 | 1 | ||
| 20 | 6 | ||||||
| 25 | 2 | ||||||
El estándar de la Agencia de Protección Ambiental de EE. UU. (EPA 1987) para la concentración de partículas en el aire ambiental se conoce como PM10, es decir, material particulado de menos de 10 mm de diámetro aerodinámico. Tiene un criterio de entrada del muestreador que es similar (funcionalmente equivalente) al TPM pero, como se muestra en la Tabla 2, tiene especificaciones numéricas algo diferentes.
Contaminantes del aire
Los contaminantes pueden dispersarse en el aire a temperaturas y presiones ambientales normales en forma gaseosa, líquida y sólida. Los dos últimos representan suspensiones de partículas en el aire y recibieron el término genérico aerosoles por Gibbs (1924) sobre la base de la analogía con el término hidrosol, se utiliza para describir sistemas dispersos en el agua. Los gases y vapores, que están presentes como moléculas discretas, forman verdaderas soluciones en el aire. Las partículas que consisten en materiales de presión de vapor de moderada a alta tienden a evaporarse rápidamente porque las que son lo suficientemente pequeñas para permanecer suspendidas en el aire durante más de unos pocos minutos (es decir, las que tienen menos de 10 mm) tienen una gran relación superficie-volumen. Algunos materiales con presiones de vapor relativamente bajas pueden tener fracciones apreciables tanto en forma de vapor como de aerosol simultáneamente.
Gases y vapores
Una vez dispersos en el aire, los gases y vapores contaminantes generalmente forman mezclas tan diluidas que sus propiedades físicas (como densidad, viscosidad, entalpía, etc.) no se pueden distinguir de las del aire limpio. Se puede considerar que tales mezclas siguen las relaciones de la ley de los gases ideales. No existe una diferencia práctica entre un gas y un vapor, excepto que este último generalmente se considera la fase gaseosa de una sustancia que puede existir como sólido o líquido a temperatura ambiente. Mientras están dispersas en el aire, todas las moléculas de un compuesto dado son esencialmente equivalentes en su tamaño y probabilidades de captura por las superficies ambientales, las superficies del tracto respiratorio y los colectores o muestreadores de contaminantes.
Aerosoles
Los aerosoles, al ser dispersiones de partículas sólidas o líquidas en el aire, tienen la variable adicional muy importante del tamaño de las partículas. El tamaño afecta el movimiento de las partículas y, por lo tanto, las probabilidades de fenómenos físicos como la coagulación, la dispersión, la sedimentación, el impacto en las superficies, los fenómenos interfaciales y las propiedades de dispersión de la luz. No es posible caracterizar una partícula dada por un solo parámetro de tamaño. Por ejemplo, las propiedades aerodinámicas de una partícula dependen de la densidad y la forma, así como de las dimensiones lineales, y el tamaño efectivo para la dispersión de la luz depende del índice de refracción y la forma.
En algunos casos especiales, todas las partículas son esencialmente del mismo tamaño. Dichos aerosoles se consideran monodispersos. Algunos ejemplos son los pólenes naturales y algunos aerosoles generados en laboratorio. Más típicamente, los aerosoles están compuestos de partículas de muchos tamaños diferentes y, por lo tanto, se denominan heterodispersos o polidispersos. Diferentes aerosoles tienen diferentes grados de dispersión de tamaño. Por lo tanto, es necesario especificar al menos dos parámetros para caracterizar el tamaño del aerosol: una medida de tendencia central, como una media o mediana, y una medida de dispersión, como una desviación estándar aritmética o geométrica.
Las partículas generadas por una sola fuente o proceso generalmente tienen diámetros que siguen una distribución logarítmica normal; es decir, los logaritmos de sus diámetros individuales tienen una distribución gaussiana. En este caso, la medida de dispersión es la desviación estándar geométrica, que es la relación entre el tamaño del percentil 84.1 y el tamaño del percentil 50. Cuando más de una fuente de partículas es significativa, el aerosol mixto resultante normalmente no seguirá una única distribución logarítmica normal, y puede ser necesario describirlo mediante la suma de varias distribuciones.
Características de las partículas
Hay muchas propiedades de las partículas además de su tamaño lineal que pueden influir en gran medida en su comportamiento en el aire y sus efectos sobre el medio ambiente y la salud. Éstas incluyen:
Superficie. Para partículas esféricas, la superficie varía con el cuadrado del diámetro. Sin embargo, para un aerosol de una concentración másica determinada, la superficie total del aerosol aumenta al disminuir el tamaño de las partículas. Para partículas no esféricas o agregadas, y para partículas con grietas internas o poros, la relación entre superficie y volumen puede ser mucho mayor que para las esferas.
Volumen. El volumen de las partículas varía con el cubo del diámetro; por lo tanto, las pocas partículas más grandes en un aerosol tienden a dominar su concentración de volumen (o masa).
Forma. La forma de una partícula afecta su resistencia aerodinámica, así como su área de superficie y, por lo tanto, sus probabilidades de movimiento y deposición.
Densidad. La velocidad de una partícula en respuesta a fuerzas gravitatorias o de inercia aumenta como la raíz cuadrada de su densidad.
Diámetro aerodinámico. El diámetro de una esfera de densidad unitaria que tiene la misma velocidad terminal de sedimentación que la partícula bajo consideración es igual a su diámetro aerodinámico. La velocidad de sedimentación terminal es la velocidad de equilibrio de una partícula que cae bajo la influencia de la gravedad y la resistencia del fluido. El diámetro aerodinámico está determinado por el tamaño real de las partículas, la densidad de las partículas y un factor de forma aerodinámico.
tipos de aerosoles
Los aerosoles se clasifican generalmente en términos de sus procesos de formación. Aunque la siguiente clasificación no es precisa ni completa, se usa y acepta comúnmente en los campos de la higiene industrial y la contaminación del aire.
Polvo. Aerosol formado por la subdivisión mecánica del material a granel en partículas suspendidas en el aire que tienen la misma composición química. Las partículas de polvo son generalmente sólidas y de forma irregular y tienen diámetros superiores a 1 mm.
Humo. Aerosol de partículas sólidas formadas por condensación de vapores formados por combustión o sublimación a temperaturas elevadas. Las partículas primarias son generalmente muy pequeñas (menos de 0.1 mm) y tienen formas esféricas o cristalinas características. Pueden ser químicamente idénticos al material original o pueden estar compuestos por un producto de oxidación como el óxido metálico. Dado que pueden formarse en concentraciones de alto número, a menudo se coagulan rápidamente, formando grupos agregados de baja densidad general.
Fumar. Aerosol formado por condensación de productos de combustión, generalmente de materia orgánica. Las partículas son generalmente gotitas líquidas con diámetros inferiores a 0.5 mm.
Niebla. Un aerosol de gotitas formado por cizallamiento mecánico de un líquido a granel, por ejemplo, por atomización, nebulización, burbujeo o rociado. El tamaño de las gotas puede cubrir un rango muy amplio, normalmente desde unos 2 mm hasta más de 50 mm.
Niebla. Aerosol acuoso formado por condensación de vapor de agua en núcleos atmosféricos a humedades relativas altas. Los tamaños de gota son generalmente mayores de 1 mm.
Niebla tóxica. Término popular para un aerosol contaminante derivado de una combinación de humo y niebla. Ahora se usa comúnmente para cualquier mezcla de contaminación atmosférica.
Calina. Aerosol de tamaño submicrométrico de partículas higroscópicas que absorben vapor de agua a humedades relativas relativamente bajas.
Aitken o núcleos de condensación (CN). Partículas atmosféricas muy pequeñas (en su mayoría menores de 0.1 mm) formadas por procesos de combustión y por conversión química de precursores gaseosos.
Modo de acumulación. Término dado a las partículas en la atmósfera ambiente que van desde 0.1 hasta aproximadamente 1.0 mm de diámetro. Estas partículas generalmente son esféricas (con superficies líquidas) y se forman por coagulación y condensación de partículas más pequeñas que se derivan de precursores gaseosos. Siendo demasiado grandes para una coagulación rápida y demasiado pequeños para una sedimentación eficaz, tienden a acumularse en el aire ambiente.
Modo de partículas gruesas. Partículas de aire ambiente de más de 2.5 mm de diámetro aerodinámico y generalmente formadas por procesos mecánicos y resuspensión de polvo superficial.
Respuestas biológicas del sistema respiratorio a los contaminantes del aire
Las respuestas a los contaminantes del aire van desde molestias hasta necrosis tisular y muerte, desde efectos sistémicos generalizados hasta ataques altamente específicos en tejidos individuales. Los factores ambientales y del huésped sirven para modificar los efectos de las sustancias químicas inhaladas, y la respuesta final es el resultado de su interacción. Los principales factores del huésped son:
- edad: por ejemplo, personas mayores, especialmente aquellas con funciones cardiovasculares y respiratorias crónicamente reducidas, que pueden no ser capaces de hacer frente a tensiones pulmonares adicionales
- estado de salud, por ejemplo, enfermedad o disfunción concurrente
- Estados nutricionales
- estado inmunológico
- sexo y otros factores genéticos, por ejemplo, diferencias relacionadas con enzimas en los mecanismos de biotransformación, como vías metabólicas deficientes e incapacidad para sintetizar ciertas enzimas de desintoxicación
- estado psicológico, por ejemplo, estrés, ansiedad y
- factores culturales, por ejemplo, fumar cigarrillos, que puede afectar las defensas normales o puede potenciar el efecto de otras sustancias químicas.
Los factores ambientales incluyen la concentración, la estabilidad y las propiedades fisicoquímicas del agente en el entorno de exposición y la duración, frecuencia y vía de exposición. Las exposiciones agudas y crónicas a un químico pueden resultar en diferentes manifestaciones patológicas.
Cualquier órgano puede responder solo en un número limitado de formas, y existen numerosas etiquetas de diagnóstico para las enfermedades resultantes. Las siguientes secciones discuten los tipos generales de respuestas del sistema respiratorio que pueden ocurrir luego de la exposición a contaminantes ambientales.
respuesta irritante
Los irritantes producen un patrón de inflamación tisular generalizada e inespecífica, y la destrucción puede resultar en el área de contacto con el contaminante. Algunos irritantes no producen ningún efecto sistémico porque la respuesta irritante es mucho mayor que cualquier efecto sistémico, mientras que algunos también tienen efectos sistémicos significativos después de la absorción, por ejemplo, el sulfuro de hidrógeno absorbido a través de los pulmones.
En altas concentraciones, los irritantes pueden causar una sensación de ardor en la nariz y la garganta (y generalmente también en los ojos), dolor en el pecho y tos que producen inflamación de la mucosa (traqueítis, bronquitis). Ejemplos de irritantes son gases tales como cloro, flúor, dióxido de azufre, fosgeno y óxidos de nitrógeno; nieblas de ácidos o álcalis; vapores de cadmio; polvos de cloruro de zinc y pentóxido de vanadio. Las altas concentraciones de irritantes químicos también pueden penetrar profundamente en los pulmones y causar edema pulmonar (los alvéolos se llenan de líquido) o inflamación (neumonitis química).
Concentraciones muy elevadas de polvos que no tienen propiedades irritantes químicas también pueden irritar mecánicamente los bronquios y, después de ingresar al tracto gastrointestinal, también pueden contribuir al cáncer de estómago y colon.
La exposición a irritantes puede resultar en la muerte si los órganos críticos están gravemente dañados. Por otro lado, el daño puede ser reversible o puede resultar en la pérdida permanente de algún grado de función, como una capacidad de intercambio gaseoso deteriorada.
Respuesta fibrótica
Varios polvos conducen al desarrollo de un grupo de trastornos pulmonares crónicos denominados neumoconiosis. Este término general abarca muchas afecciones fibróticas del pulmón, es decir, enfermedades caracterizadas por la formación de cicatrices en el tejido conjuntivo intersticial. Las neumoconiosis se deben a la inhalación y posterior retención selectiva de ciertos polvos en los alvéolos, de los cuales están sujetos al secuestro intersticial.
Las neumoconiosis se caracterizan por lesiones fibróticas específicas, que difieren en tipo y patrón según el polvo involucrado. Por ejemplo, la silicosis, debida al depósito de sílice libre de cristales, se caracteriza por un tipo de fibrosis nodular, mientras que en la asbestosis se encuentra una fibrosis difusa, debida a la exposición a fibras de amianto. Ciertos polvos, como el óxido de hierro, producen únicamente alteraciones radiológicas (siderosis) sin deterioro funcional, mientras que los efectos de otros van desde una mínima invalidez hasta la muerte.
Respuesta alérgica
Las respuestas alérgicas implican el fenómeno conocido como sensibilización. La exposición inicial a un alérgeno da como resultado la inducción de la formación de anticuerpos; la exposición posterior del individuo ahora "sensibilizado" da como resultado una respuesta inmunitaria, es decir, una reacción antígeno-anticuerpo (el antígeno es el alérgeno en combinación con una proteína endógena). Esta reacción inmunitaria puede ocurrir inmediatamente después de la exposición al alérgeno o puede ser una respuesta tardía.
Las reacciones alérgicas respiratorias primarias son el asma bronquial, reacciones en las vías respiratorias superiores que implican la liberación de histamina o mediadores similares a la histamina tras reacciones inmunitarias en la mucosa, y un tipo de neumonitis (inflamación pulmonar) conocida como alveolitis alérgica extrínseca. Además de estas reacciones locales, una reacción alérgica sistémica (choque anafiláctico) puede seguir a la exposición a algunos alérgenos químicos.
Respuesta infecciosa
Los agentes infecciosos pueden causar tuberculosis, ántrax, ornitosis, brucelosis, histoplasmosis, enfermedad del legionario, etc.
Respuesta cancerígena
El cáncer es un término general para un grupo de enfermedades relacionadas que se caracterizan por el crecimiento descontrolado de los tejidos. Su desarrollo se debe a un proceso complejo de interacción de múltiples factores en el huésped y el medio ambiente.
Una de las grandes dificultades al intentar relacionar la exposición a un agente específico con el desarrollo de cáncer en humanos es el largo período de latencia, típicamente de 15 a 40 años, entre el inicio de la exposición y la manifestación de la enfermedad.
Ejemplos de contaminantes del aire que pueden producir cáncer de pulmón son el arsénico y sus compuestos, cromatos, sílice, partículas que contienen hidrocarburos aromáticos policíclicos y ciertos polvos que contienen níquel. Las fibras de asbesto pueden causar cáncer bronquial y mesotelioma de la pleura y el peritoneo. Las partículas radiactivas depositadas pueden exponer el tejido pulmonar a altas dosis locales de radiación ionizante y ser la causa del cáncer.
Respuesta sistémica
Muchos productos químicos ambientales producen una enfermedad sistémica generalizada debido a sus efectos sobre varios sitios objetivo. Los pulmones no solo son el objetivo de muchos agentes nocivos, sino también el sitio de entrada de sustancias tóxicas que pasan a través de los pulmones al torrente sanguíneo sin dañar los pulmones. Sin embargo, cuando se distribuyen por la circulación sanguínea a varios órganos, pueden dañarlos o causar un envenenamiento general y tener efectos sistémicos. Este papel de los pulmones en la patología ocupacional no es objeto de este artículo. Sin embargo, debe mencionarse el efecto de las partículas finamente dispersas (humos) de varios óxidos metálicos que a menudo se asocian con un síndrome sistémico agudo conocido como fiebre de los humos metálicos.
Examen de función pulmonar
La función pulmonar se puede medir de varias maneras. Sin embargo, el objetivo de las mediciones debe estar claro antes del examen, para poder interpretar los resultados correctamente. En este artículo discutiremos el examen de la función pulmonar con especial atención al campo ocupacional. Es importante recordar las limitaciones en las diferentes mediciones de la función pulmonar. Los efectos temporales agudos en la función pulmonar pueden no ser perceptibles en caso de exposición a polvo fibrogénico como el cuarzo y el asbesto, pero los efectos crónicos en la función pulmonar después de una exposición a largo plazo (>20 años) pueden serlo. Esto se debe a que los efectos crónicos ocurren años después de que el polvo es inhalado y depositado en los pulmones. Por otro lado, los efectos temporales agudos del polvo orgánico e inorgánico, así como el moho, los humos de soldadura y los gases de escape de los motores, son adecuados para el estudio. Esto se debe a que el efecto irritante de estos polvos se producirá a las pocas horas de exposición. Los efectos agudos o crónicos de la función pulmonar también pueden ser perceptibles en casos de exposición a concentraciones de gases irritantes (dióxido de nitrógeno, aldehídos, ácidos y cloruros de ácido) en la vecindad de valores límite de exposición bien documentados, especialmente si el efecto es potenciado por la contaminación del aire por partículas. .
Las mediciones de la función pulmonar deben ser seguras para los sujetos examinados y el equipo de función pulmonar debe ser seguro para el examinador. Se encuentra disponible un resumen de los requisitos específicos para diferentes tipos de equipos de función pulmonar (p. ej., Quanjer et al. 1993). Por supuesto, el equipo debe estar calibrado de acuerdo con estándares independientes. Esto puede ser difícil de lograr, especialmente cuando se utiliza equipo computarizado. El resultado de la prueba de función pulmonar depende tanto del sujeto como del examinador. Para proporcionar resultados satisfactorios del examen, los técnicos deben estar bien capacitados y ser capaces de instruir al sujeto cuidadosamente y también alentarlo a realizar la prueba correctamente. El examinador también debe tener conocimientos sobre las vías respiratorias y los pulmones para interpretar correctamente los resultados de los registros.
Se recomienda que los métodos utilizados tengan una reproducibilidad bastante alta tanto entre como dentro de los sujetos. La reproducibilidad puede medirse como el coeficiente de variación, es decir, la desviación estándar multiplicada por 100 dividida por el valor medio. Los valores por debajo del 10% en mediciones repetidas sobre el mismo sujeto se consideran aceptables.
Para determinar si los valores medidos son patológicos o no, deben compararse con ecuaciones de predicción. Habitualmente las ecuaciones de predicción de las variables espirométricas se basan en la edad y la talla, estratificadas por sexo. Los hombres tienen en promedio valores de función pulmonar más altos que las mujeres, de la misma edad y altura. La función pulmonar disminuye con la edad y aumenta con la altura. Por lo tanto, un sujeto alto tendrá un volumen pulmonar mayor que un sujeto bajo de la misma edad. El resultado de las ecuaciones de predicción puede diferir considerablemente entre diferentes poblaciones de referencia. La variación en edad y altura en la población de referencia también influirá en los valores predichos. Esto significa, por ejemplo, que no debe usarse una ecuación de predicción si la edad y/o la altura del sujeto examinado están fuera de los rangos de la población que es la base de la ecuación de predicción.
Fumar también disminuirá la función pulmonar y el efecto puede verse potenciado en sujetos que están expuestos ocupacionalmente a agentes irritantes. Antes se consideraba que la función pulmonar no era patológica si los valores obtenidos estaban dentro del 80 % del valor predicho, derivado de una ecuación de predicción.
Medidas
Las mediciones de la función pulmonar se llevan a cabo para juzgar el estado de los pulmones. Las mediciones pueden referirse a volúmenes pulmonares medidos únicos o múltiples, o las propiedades dinámicas en las vías respiratorias y los pulmones. Este último suele determinarse mediante maniobras dependientes del esfuerzo. Las condiciones de los pulmones también pueden examinarse con respecto a su función fisiológica, es decir, la capacidad de difusión, la resistencia y la distensibilidad de las vías respiratorias (véase más adelante).
Las medidas relativas a la capacidad ventilatoria se obtienen por espirometría. La maniobra de respiración generalmente se realiza como una inspiración máxima seguida de una espiración máxima, capacidad vital (VC, medida en litros). Deben realizarse al menos tres registros técnicamente satisfactorios (es decir, esfuerzo de inspiración y espiración completos y ausencia de fugas) y notificarse el valor más alto. El volumen puede medirse directamente mediante una campana sellada con agua o de baja resistencia, o medirse indirectamente mediante neumotacografía (es decir, integración de una señal de flujo a lo largo del tiempo). Es importante señalar aquí que todos los volúmenes pulmonares medidos deben expresarse en BTPS, es decir, temperatura corporal y presión ambiental saturada con vapor de agua.
La capacidad vital espirada forzada (FVC, en litros) se define como una medición de VC realizada con un esfuerzo espiratorio forzado máximo. Debido a la sencillez de la prueba y al equipo relativamente barato, el expirograma forzado se ha convertido en una prueba útil en la monitorización de la función pulmonar. Sin embargo, esto ha resultado en muchas grabaciones deficientes, cuyo valor práctico es discutible. Para realizar registros satisfactorios, puede ser de utilidad la guía actualizada para la toma y uso del expirograma forzado, publicada por la American Thoracic Society en 1987.
Los flujos instantáneos se pueden medir en curvas de flujo-volumen o flujo-tiempo, mientras que los flujos o tiempos promedio de tiempo se derivan del espirograma. Las variables asociadas que se pueden calcular a partir del expirograma forzado son el volumen espirado forzado en un segundo (FEV1, en litros por segundo), en porcentaje de FVC (FEV1%), flujo pico (PEF, l/s), flujos máximos al 50% y 75% de la capacidad vital forzada (MEF50 y MEF25, respectivamente). Una ilustración de la derivación de FEV1 del expirograma forzado se describe en la figura 1. En sujetos sanos, las tasas de flujo máximas a grandes volúmenes pulmonares (es decir, al comienzo de la espiración) reflejan principalmente las características de flujo de las vías respiratorias grandes, mientras que a volúmenes pulmonares pequeños (es decir, al final de la espiración). de espiración) suelen sostenerse para reflejar las características de las vías respiratorias pequeñas, figura 2. En estas últimas el flujo es laminar, mientras que en las vías respiratorias grandes puede ser turbulento.
Figura 1. Espirograma de espiración forzada que muestra la derivación del FEV1 y FVC según el principio de extrapolación.
Figura 2. Curva de flujo-volumen que muestra la derivación del flujo espiratorio máximo (PEF), flujos máximos al 50% y al 75% de la capacidad vital forzada (![]() y
y ![]() , respectivamente).
, respectivamente).
El PEF también puede medirse con un pequeño dispositivo portátil como el desarrollado por Wright en 1959. Una ventaja de este equipo es que el sujeto puede realizar mediciones en serie, por ejemplo, en el lugar de trabajo. Sin embargo, para obtener grabaciones útiles, es necesario instruir bien a los sujetos. Además, hay que tener en cuenta que las medidas de PEF con, por ejemplo, un medidor de Wright y las medidas por espirometría convencional no deben compararse debido a las diferentes técnicas de soplado.
Las variables espirométricas VC, FVC y FEV1 muestran una variación razonable entre individuos donde la edad, la altura y el sexo suelen explicar del 60 al 70% de la variación. Los trastornos restrictivos de la función pulmonar darán lugar a valores más bajos de VC, FVC y FEV1. Las mediciones de flujos durante la espiración muestran una gran variación individual, ya que los flujos medidos dependen tanto del esfuerzo como del tiempo. Esto significa, por ejemplo, que un sujeto tendrá un flujo extremadamente alto en caso de disminución del volumen pulmonar. Por otro lado, el flujo puede ser extremadamente bajo en caso de un volumen pulmonar muy alto. Sin embargo, el flujo suele disminuir en el caso de una enfermedad obstructiva crónica (p. ej., asma, bronquitis crónica).
Figura 3. Esquema principal del equipo para la determinación de la capacidad pulmonar total (TLC) según la técnica de dilución con helio.
La proporción de volumen residual (RV), es decir, el volumen de aire que aún queda en los pulmones después de una espiración máxima, puede determinarse por dilución de gas o por pletismografía corporal. La técnica de dilución de gas requiere un equipo menos complicado y, por lo tanto, es más conveniente para usar en estudios realizados en el lugar de trabajo. En la figura 3 se describe el principio de la técnica de dilución de gas. La técnica se basa en la dilución de un gas indicador en un circuito de reinhalación. El gas indicador debe ser poco soluble en los tejidos biológicos para que no sea absorbido por los tejidos y la sangre en el pulmón. Inicialmente se utilizó hidrógeno, pero debido a su capacidad para formar mezclas explosivas con el aire, se reemplazó por helio, que se detecta fácilmente mediante el principio de conductividad térmica.
El sujeto y el aparato forman un sistema cerrado y, por lo tanto, la concentración inicial del gas se reduce cuando se diluye en el volumen de gas en los pulmones. Después del equilibrio, la concentración de gas indicador es la misma en los pulmones que en el aparato, y la capacidad residual funcional (FRC) se puede calcular mediante una ecuación de dilución simple. El volumen del espirómetro (incluida la adición de la mezcla de gases al espirómetro) se indica mediante VS, VL es el volumen del pulmón, Fi es la concentración inicial de gas y Ff es la concentración final.
CRF = VL = [(VS · Fi) / Ff] - VS
Se realizan de dos a tres maniobras de VC para proporcionar una base confiable para el cálculo de TLC (en litros). Las subdivisiones de los diferentes volúmenes pulmonares se describen en la figura 4.
Figura 4. Espirograma etiquetado para mostrar las subdivisiones de la capacidad total.
Debido al cambio en las propiedades elásticas de las vías respiratorias, RV y FRC aumentan con la edad. En las enfermedades obstructivas crónicas se suelen observar valores elevados de RV y FRC, mientras que VC está disminuido. Sin embargo, en sujetos con áreas pulmonares mal ventiladas, por ejemplo, sujetos con enfisema, la técnica de dilución de gas puede subestimar RV, FRC y también TLC. Esto se debe al hecho de que el gas indicador no se comunicará con las vías respiratorias cerradas y, por lo tanto, la disminución en la concentración del gas indicador dará valores erróneamente pequeños.
Figura 5. Esquema principal del registro del cierre de la vía aérea y la pendiente de la meseta alveolar (%![]() ).
).
Las medidas de cierre de la vía aérea y distribución de gas en los pulmones se pueden obtener en una misma maniobra mediante la técnica de lavado con respiración única, figura 5. El equipo consta de un espirómetro conectado a un sistema bag-in-box y un registrador de mediciones continuas de la concentración de nitrógeno. La maniobra se realiza mediante una inspiración máxima de oxígeno puro de la bolsa. Al comienzo de la espiración, la concentración de nitrógeno aumenta como resultado del vaciamiento del espacio muerto del sujeto, que contiene oxígeno puro. La espiración continúa con el aire de las vías respiratorias y los alvéolos. Finalmente, se exhala el aire de los alvéolos, que contiene del 20 al 40% de nitrógeno. Cuando aumenta la espiración de las partes basales de los pulmones, la concentración de nitrógeno aumentará abruptamente en caso de cierre de las vías respiratorias en las regiones pulmonares dependientes, figura 5. Este volumen por encima del RV, en el que las vías respiratorias se cierran durante una espiración, generalmente se expresa como volumen de cierre (CV) en porcentaje de VC (CV%). La distribución del aire inspirado en los pulmones se expresa como la pendiente de la meseta alveolar (%N2 o fase III, %N2/l). Se obtiene tomando la diferencia de concentración de nitrógeno entre el punto en que se exhala el 30% del aire y el punto en que se cierran las vías respiratorias, y dividiéndola por el volumen correspondiente.
El envejecimiento, así como los trastornos obstructivos crónicos, darán como resultado valores elevados tanto para el % CV como para la fase III. Sin embargo, ni siquiera los sujetos sanos tienen una distribución uniforme del gas en los pulmones, lo que resulta en valores ligeramente elevados para la fase III, es decir, 1 a 2 % de N2/l. Se considera que las variables CV% y fase III reflejan las condiciones en las vías aéreas pequeñas periféricas con un diámetro interno de aproximadamente 2 mm. Normalmente, las vías respiratorias periféricas contribuyen con una pequeña parte (10 a 20 %) de la resistencia total de las vías respiratorias. Pueden ocurrir cambios bastante extensos que no son detectables por pruebas de función pulmonar convencionales como la espirometría dinámica, por ejemplo, como resultado de una exposición a sustancias irritantes en el aire en las vías respiratorias periféricas. Esto sugiere que la obstrucción de las vías respiratorias comienza en las vías respiratorias pequeñas. Los resultados de los estudios también han mostrado alteraciones en el %CV y la fase III antes de que se produzcan cambios en la espirometría dinámica y estática. Estos cambios tempranos pueden entrar en remisión cuando cesa la exposición a agentes peligrosos.
El factor de transferencia del pulmón (mmol/min; kPa) es una expresión de la capacidad de difusión del transporte de oxígeno hacia los capilares pulmonares. El factor de transferencia se puede determinar utilizando técnicas de respiración única o múltiple; la técnica de respiración única se considera la más adecuada en los estudios en el lugar de trabajo. Se utiliza monóxido de carbono (CO) ya que la contrapresión del CO es muy baja en la sangre periférica, en contraste con la del oxígeno. Se supone que la captación de CO sigue un modelo exponencial, y esta suposición se puede utilizar para determinar el factor de transferencia para el pulmón.
Determinación de TLCO (factor de transferencia medido con CO) se realiza mediante una maniobra de respiración que incluye una espiración máxima, seguida de una inspiración máxima de una mezcla gaseosa que contiene monóxido de carbono, helio, oxígeno y nitrógeno. Después de un período de contención de la respiración, se realiza una exhalación máxima, reflejando el contenido en el aire alveolar, Figura 10. Se usa helio para la determinación del volumen alveolar (VA). Suponiendo que la dilución de CO es la misma que para el helio, se puede calcular la concentración inicial de CO, antes de que comience la difusión. TLCO se calcula de acuerdo con la ecuación que se describe a continuación, donde k depende de las dimensiones de los términos componentes, t es el tiempo efectivo para aguantar la respiración y log es logaritmo en base 10. El volumen inspirado se denota Vi y las fracciones F de CO y helio se denotan por i y a para inspirado y alveolar, respectivamente.
TLCO = k Vi (Fa,Él/Fi,He) Iniciar sesión (Fi,CO Fa,He/Fa,CO Fi,Él) (t)-1
Figura 6. Esquema principal del registro del factor de transferencia
El tamaño de TLCO dependerá de una variedad de condiciones, por ejemplo, la cantidad de hemoglobina disponible, el volumen de los alvéolos ventilados y los capilares pulmonares perfundidos y su relación entre ellos. Valores para TLCO disminuyen con la edad y aumentan con la actividad física y el aumento de los volúmenes pulmonares. Disminuido TLCO se encontrará tanto en trastornos pulmonares restrictivos como obstructivos.
La distensibilidad (l/kPa) es una función, entre otras cosas, de la propiedad elástica de los pulmones. Los pulmones tienen una tendencia intrínseca a colaborar, es decir, colapsar. El poder para mantener los pulmones estirados dependerá del tejido pulmonar elástico, la tensión superficial en los alvéolos y la musculatura bronquial. Por otro lado, la pared torácica tiende a expandirse a volúmenes pulmonares de 1 a 2 litros por encima del nivel de FRC. A volúmenes pulmonares más altos, se debe aplicar potencia para expandir aún más la pared torácica. Al nivel de FRC, la tendencia correspondiente en los pulmones se equilibra con la tendencia a expandirse. Por lo tanto, el nivel de FRC se denota por el nivel de reposo del pulmón.
La distensibilidad del pulmón se define como el cambio de volumen dividido por el cambio de la presión transpulmonar, es decir, la diferencia entre las presiones en la boca (atmosférica) y en el pulmón, como resultado de una maniobra de respiración. Las mediciones de la presión en el pulmón no se realizan fácilmente y, por lo tanto, se reemplazan por mediciones de la presión en el esófago. La presión en el esófago es casi la misma que la presión en el pulmón y se mide con un catéter delgado de polietileno con un globo que cubre los 10 cm distales. Durante las maniobras de inspiración y espiración, los cambios de volumen y presión se registran mediante un espirómetro y un transductor de presión, respectivamente. Cuando las mediciones se realizan durante la respiración corriente, se puede medir el cumplimiento dinámico. La distensibilidad estática se obtiene cuando se realiza una maniobra de VC lenta. En este último caso, las medidas se realizan en un pletismógrafo corporal, y la espiración se interrumpe intermitentemente por medio de un obturador. Sin embargo, las mediciones de cumplimiento son engorrosas de realizar cuando se examinan los efectos de la exposición sobre la función pulmonar en el lugar de trabajo, y esta técnica se considera más apropiada en el laboratorio.
En la fibrosis se observa una disminución de la distensibilidad (aumento de la elasticidad). Para provocar un cambio de volumen, se requieren grandes cambios de presión. Por otro lado, se observa una alta distensibilidad, por ejemplo, en el enfisema como consecuencia de la pérdida de tejido elástico y por tanto también de elasticidad en el pulmón.
La resistencia en las vías respiratorias depende esencialmente del radio y la longitud de las vías respiratorias, pero también de la viscosidad del aire. La resistencia de las vías respiratorias (RL en (kPa/l) /s), puede determinarse mediante el uso de un espirómetro, un transductor de presión y un neumotacógrafo (para medir el flujo). Las mediciones también se pueden realizar utilizando un pletismógrafo corporal para registrar los cambios de flujo y presión durante las maniobras de jadeo. Mediante la administración de un fármaco destinado a provocar broncoconstricción, se pueden identificar sujetos sensibles, como consecuencia de sus vías respiratorias hiperreactivas. Los sujetos con asma suelen tener valores elevados de RL.
Efectos agudos y crónicos de la exposición ocupacional sobre la función pulmonar
La medición de la función pulmonar puede usarse para revelar un efecto de exposición ocupacional en los pulmones. El examen previo al empleo de la función pulmonar no debe usarse para excluir a los sujetos que buscan trabajo. Esto se debe a que la función pulmonar de sujetos sanos varía dentro de amplios límites y es difícil trazar un límite por debajo del cual se pueda afirmar con seguridad que el pulmón es patológico. Otra razón es que el ambiente de trabajo debe ser lo suficientemente bueno como para permitir que incluso los sujetos con una leve alteración de la función pulmonar trabajen de manera segura.
Los efectos crónicos en los pulmones en sujetos ocupacionalmente expuestos pueden detectarse de varias maneras. Sin embargo, las técnicas están diseñadas para determinar los efectos históricos y son menos adecuadas para servir como pautas para prevenir el deterioro de la función pulmonar. Un diseño de estudio común es comparar los valores reales en sujetos expuestos con los valores de función pulmonar obtenidos en una población de referencia sin exposición ocupacional. Los sujetos de referencia pueden ser reclutados del mismo (o cercano) lugar de trabajo o de la misma ciudad.
El análisis multivariado se ha utilizado en algunos estudios para evaluar las diferencias entre los sujetos expuestos y los referentes no expuestos emparejados. Los valores de función pulmonar en sujetos expuestos también pueden estandarizarse por medio de una ecuación de referencia basada en los valores de función pulmonar en sujetos no expuestos.
Otro enfoque es estudiar la diferencia entre los valores de función pulmonar en trabajadores expuestos y no expuestos después del ajuste por edad y altura con el uso de valores de referencia externos, calculados mediante una ecuación de predicción basada en sujetos sanos. La población de referencia también puede compararse con los sujetos expuestos según el grupo étnico, el sexo, la edad, la altura y los hábitos de fumar para controlar mejor esos factores influyentes.
Sin embargo, el problema es decidir si una disminución es lo suficientemente grande como para clasificarla como patológica, cuando se utilizan valores de referencia externos. Aunque los instrumentos de los estudios tienen que ser portátiles y sencillos, se debe prestar atención tanto a la sensibilidad del método elegido para detectar pequeñas anomalías en vías aéreas y pulmones como a la posibilidad de combinar diferentes métodos. Hay indicios de que los sujetos con síntomas respiratorios, como disnea de esfuerzo, tienen un mayor riesgo de sufrir una disminución acelerada de la función pulmonar. Esto significa que la presencia de síntomas respiratorios es importante y, por lo tanto, no debe descuidarse.
El sujeto también puede ser seguido por espirometría, por ejemplo, una vez al año, durante varios años, para advertir sobre el desarrollo de una enfermedad. Sin embargo, existen limitaciones, ya que esto requerirá mucho tiempo y la función pulmonar puede haberse deteriorado permanentemente cuando se pueda observar la disminución. Por lo tanto, este enfoque no debe ser una excusa para retrasar la adopción de medidas destinadas a reducir las concentraciones nocivas de contaminantes atmosféricos.
Finalmente, los efectos crónicos sobre la función pulmonar también pueden estudiarse examinando los cambios individuales en la función pulmonar en sujetos expuestos y no expuestos durante varios años. Una ventaja del diseño de estudio longitudinal es que se elimina la variabilidad entre sujetos; sin embargo, se considera que el diseño requiere mucho tiempo y es costoso.
Los sujetos susceptibles también pueden identificarse comparando su función pulmonar con y sin exposición durante los turnos de trabajo. Con el fin de minimizar los posibles efectos de las variaciones diurnas, la función pulmonar se mide a la misma hora del día en una ocasión no expuesta y expuesta. La condición de no expuesto se puede obtener, por ejemplo, trasladando ocasionalmente al trabajador a un área no contaminada o mediante el uso de un respirador adecuado durante todo el turno, o en algunos casos realizando mediciones de la función pulmonar en la tarde del día libre del trabajador.
Una preocupación especial es que los efectos temporales repetidos pueden resultar en efectos crónicos. Una disminución temporal aguda de la función pulmonar puede no solo ser un indicador de exposición biológica, sino también un predictor de una disminución crónica de la función pulmonar. La exposición a los contaminantes del aire puede provocar efectos agudos perceptibles en la función pulmonar, aunque los valores medios de los contaminantes del aire medidos están por debajo de los valores límite higiénicos. Surge así la cuestión de si estos efectos son realmente perjudiciales a largo plazo. Esta pregunta es difícil de responder directamente, especialmente porque la contaminación del aire en los lugares de trabajo a menudo tiene una composición compleja y la exposición no se puede describir en términos de concentraciones medias de compuestos individuales. El efecto de una exposición ocupacional también se debe en parte a la sensibilidad del individuo. Esto significa que algunos sujetos reaccionarán antes o en mayor medida que otros. La base fisiopatológica subyacente para una disminución aguda y temporal de la función pulmonar no se comprende completamente. La reacción adversa tras la exposición a un contaminante irritante del aire es, sin embargo, una medida objetiva, en contraste con experiencias subjetivas como síntomas de diferente origen.
La ventaja de detectar cambios tempranos en las vías respiratorias y los pulmones causados por contaminantes peligrosos del aire es obvia: la exposición predominante puede reducirse para prevenir enfermedades más graves. Por lo tanto, un objetivo importante a este respecto es utilizar las mediciones de los efectos temporales agudos sobre la función pulmonar como un sistema de alerta temprana sensible que se puede utilizar al estudiar grupos de trabajadores sanos.
Monitoreo de Irritantes
La irritación es uno de los criterios más frecuentes para establecer valores límite de exposición. Sin embargo, no es seguro que el cumplimiento de un límite de exposición basado en la irritación proteja contra la irritación. Se debe considerar que un límite de exposición para un contaminante del aire generalmente contiene al menos dos partes: un límite promedio ponderado en el tiempo (TWAL) y un límite de exposición a corto plazo (STEL), o al menos reglas para exceder el promedio ponderado en el tiempo. límite, “límites de excursión”. En el caso de sustancias muy irritantes, como el anhídrido sulfuroso, la acroleína y el fosgeno, es importante limitar la concentración incluso durante periodos muy breves, por lo que ha sido práctica habitual fijar valores límite de exposición laboral en forma de límites máximos, con un período de muestreo que se mantenga tan corto como lo permitan las instalaciones de medición.
Los valores límite promedio ponderados en el tiempo para un día de ocho horas combinados con reglas para la excursión por encima de estos valores se dan para la mayoría de las sustancias en la lista de valores límite umbral (TLV) de la Conferencia Estadounidense de Higienistas Industriales Gubernamentales (ACGIH). La lista TLV de 1993-94 contiene la siguiente declaración sobre los límites de excursión para exceder los valores límite:
“Para la gran mayoría de las sustancias con un TLV-TWA, no hay suficientes datos toxicológicos disponibles para garantizar un STEL = límite de exposición a corto plazo). Sin embargo, las excursiones por encima del TLV-TWA deben controlarse incluso cuando el TWA de ocho horas se encuentra dentro de los límites recomendados”.
Las mediciones de exposición de contaminantes del aire conocidos y la comparación con valores límite de exposición bien documentados deben llevarse a cabo de manera rutinaria. Sin embargo, hay muchas situaciones en las que la determinación del cumplimiento de los valores límite de exposición no es suficiente. Este es el caso en las siguientes circunstancias (entre otras):
- cuando el valor límite es demasiado alto para proteger contra la irritación
- cuando el irritante es desconocido
- cuando el irritante es una mezcla compleja y no se conoce un indicador adecuado.
Como se recomendó anteriormente, la medición de los efectos agudos y temporales sobre la función pulmonar se puede utilizar en estos casos como una advertencia contra la sobreexposición a los irritantes.
En los casos (2) y (3), los efectos agudos y temporales sobre la función pulmonar pueden ser aplicables también al probar la eficacia de las medidas de control para disminuir la exposición a la contaminación del aire o en investigaciones científicas, por ejemplo, al atribuir efectos biológicos a los componentes del aire. contaminantes A continuación se presentan varios ejemplos en los que los efectos agudos y temporales de la función pulmonar se han empleado con éxito en investigaciones de salud ocupacional.
Estudios de efectos agudos y temporales de la función pulmonar
La disminución temporal relacionada con el trabajo de la función pulmonar durante un turno de trabajo se registró en trabajadores del algodón a fines de 1950. Más tarde, varios autores informaron cambios agudos y temporales relacionados con el trabajo de la función pulmonar en trabajadores textiles y de cáñamo, mineros expuestos a diisocianato de tolueno, bomberos, trabajadores de procesamiento de caucho, moldeadores y machos, soldadores, enceradores de esquís, trabajadores expuestos a polvo orgánico e irritantes en pinturas a base de agua.
Sin embargo, también hay varios ejemplos en los que las mediciones antes y después de la exposición, generalmente durante un turno, no han podido demostrar ningún efecto agudo, a pesar de una exposición alta. Esto probablemente se deba al efecto de la variación circadiana normal, principalmente en variables de función pulmonar en función del tamaño del calibre de la vía aérea. Por lo tanto, la disminución temporal de estas variables debe exceder la variación circadiana normal para ser reconocida. Sin embargo, el problema puede evitarse midiendo la función pulmonar a la misma hora del día en cada ocasión de estudio. Al utilizar al empleado expuesto como su propio control, la variación interindividual se reduce aún más. Los soldadores se estudiaron de esta manera, y aunque la diferencia media entre los valores de FVC no expuestos y expuestos fue inferior al 3 % en 15 soldadores examinados, esta diferencia fue significativa al nivel de confianza del 95 % con una potencia superior al 99 %.
Los efectos transitorios reversibles en los pulmones pueden usarse como un indicador de exposición de componentes irritantes complicados. En el estudio citado anteriormente, las partículas en el ambiente de trabajo fueron cruciales para los efectos irritantes en las vías respiratorias y los pulmones. Las partículas fueron eliminadas por un respirador que consiste en un filtro combinado con un casco de soldadura. Los resultados indicaron que los efectos en los pulmones fueron causados por las partículas en los humos de soldadura y que el uso de un respirador de partículas podría prevenir este efecto.
La exposición a los gases de escape de diésel también produce efectos irritantes medibles en los pulmones, que se muestran como una disminución aguda y temporal de la función pulmonar. Los filtros mecánicos instalados en los tubos de escape de los camiones utilizados en las operaciones de carga por parte de los estibadores aliviaron los trastornos subjetivos y redujeron la disminución aguda y temporal de la función pulmonar que se observaba cuando no se realizaba filtración. Por lo tanto, los resultados indican que la presencia de partículas en el ambiente de trabajo juega un papel en el efecto irritante sobre las vías respiratorias y los pulmones, y que es posible evaluar el efecto mediante mediciones de cambios agudos en la función pulmonar.
Una multiplicidad de exposiciones y un entorno de trabajo en constante cambio pueden presentar dificultades para discernir la relación causal de los diferentes agentes existentes en un entorno de trabajo. El escenario de exposición en los aserraderos es un ejemplo esclarecedor. No es posible (p. ej., por razones económicas) realizar mediciones de exposición de todos los agentes posibles (terpenos, polvo, moho, bacterias, endotoxinas, micotoxinas, etc.) en este entorno de trabajo. Un método factible puede ser seguir el desarrollo de la función pulmonar longitudinalmente. En un estudio de trabajadores de un aserradero en el departamento de corte de madera, se examinó la función pulmonar antes y después de una semana laboral y no se encontró una disminución estadísticamente significativa. Sin embargo, un estudio de seguimiento realizado unos años más tarde reveló que aquellos trabajadores que realmente tenían una disminución numérica en la función pulmonar durante una semana laboral también tenían una disminución acelerada a largo plazo de la función pulmonar. Esto puede indicar que los sujetos vulnerables pueden detectarse midiendo los cambios en la función pulmonar durante una semana laboral.
Enfermedades Causadas por Irritantes Respiratorios y Químicos Tóxicos
La presencia de irritantes respiratorios en el lugar de trabajo puede ser desagradable y distraer, lo que conduce a una baja moral y una disminución de la productividad. Ciertas exposiciones son peligrosas, incluso letales. En cualquier extremo, el problema de los irritantes respiratorios y los productos químicos tóxicos inhalados es común; muchos trabajadores enfrentan una amenaza diaria de exposición. Estos compuestos causan daño por una variedad de mecanismos diferentes, y la extensión de la lesión puede variar ampliamente, dependiendo del grado de exposición y de las propiedades bioquímicas del inhalante. Sin embargo, todos tienen la característica de inespecificidad; es decir, por encima de cierto nivel de exposición, prácticamente todas las personas experimentan una amenaza para su salud.
Existen otras sustancias inhaladas que provocan que sólo las personas susceptibles desarrollen problemas respiratorios; tales dolencias se abordan más apropiadamente como enfermedades de origen alérgico e inmunológico. Ciertos compuestos, como los isocianatos, los anhídridos de ácido y las resinas epoxi, pueden actuar no solo como irritantes inespecíficos en altas concentraciones, sino que también pueden predisponer a ciertos sujetos a la sensibilización alérgica. Estos compuestos provocan síntomas respiratorios en personas sensibilizadas a muy bajas concentraciones.
Los irritantes respiratorios incluyen sustancias que causan inflamación de las vías respiratorias después de ser inhaladas. Pueden producirse daños en las vías respiratorias superiores e inferiores. Más peligrosa es la inflamación aguda del parénquima pulmonar, como en la neumonitis química o el edema pulmonar no cardiogénico. Los compuestos que pueden causar daño parenquimatoso se consideran sustancias químicas tóxicas. Muchos químicos tóxicos inhalados también actúan como irritantes respiratorios, advirtiéndonos de su peligro con su olor nocivo y síntomas de irritación de nariz y garganta y tos. La mayoría de los irritantes respiratorios también son tóxicos para el parénquima pulmonar si se inhalan en cantidad suficiente.
Muchas sustancias inhaladas tienen efectos tóxicos sistémicos después de ser absorbidas por inhalación. Los efectos inflamatorios en el pulmón pueden estar ausentes, como en el caso del plomo, el monóxido de carbono o el cianuro de hidrógeno. La inflamación pulmonar mínima normalmente se observa en el fiebres por inhalación (p. ej., síndrome tóxico por polvo orgánico, fiebre por humos metálicos y fiebre por humos de polímeros). Se producen daños graves en los pulmones y los órganos distales con una exposición significativa a toxinas como el cadmio y el mercurio.
Las propiedades físicas de las sustancias inhaladas predicen el sitio de depósito; los irritantes producirán síntomas en estos sitios. Las partículas grandes (10 a 20 mm) se depositan en la nariz y las vías respiratorias superiores, las partículas más pequeñas (5 a 10 mm) se depositan en la tráquea y los bronquios, y las partículas de menos de 5 mm pueden llegar a los alvéolos. Las partículas de menos de 0.5 mm son tan pequeñas que se comportan como gases. Los gases tóxicos se depositan según su solubilidad. Un gas soluble en agua será absorbido por la mucosa húmeda de las vías respiratorias superiores; los gases menos solubles se depositarán de manera más aleatoria en todo el tracto respiratorio.
Irritantes respiratorios
Los irritantes respiratorios causan una inflamación no específica del pulmón después de ser inhalados. Estas sustancias, sus fuentes de exposición, propiedades físicas y de otro tipo, y los efectos sobre la víctima se describen en la Tabla 1. Los gases irritantes tienden a ser más solubles en agua que los gases más tóxicos para el parénquima pulmonar. Los humos tóxicos son más peligrosos cuando tienen un umbral irritante alto; es decir, hay poca advertencia de que se está inhalando el humo porque hay poca irritación.
Tabla 1. Resumen de irritantes respiratorios
|
Química |
Fuentes de exposición |
Propiedades importantes |
lesión producida |
Nivel de exposición peligrosa por debajo de 15 min (PPM) |
|
El acetaldehído |
Plásticos, industria del caucho sintético, productos de combustión |
Alta presión de vapor; alta solubilidad en agua |
lesión de la vía aérea superior; rara vez causa edema pulmonar tardío |
|
|
Ácido acético, ácidos orgánicos |
Industria química, electrónica, productos de combustión |
Agua soluble |
Lesión ocular y de la vía aérea superior |
|
|
anhídridos de ácido |
industrias de productos químicos, pinturas y plásticos; componentes de resinas epoxi |
Soluble en agua, altamente reactivo, puede causar sensibilización alérgica |
Ocular, lesión de la vía aérea superior, broncoespasmo; hemorragia pulmonar tras exposición masiva |
|
|
Acroleína |
Plásticos, textiles, fabricación farmacéutica, productos de combustión |
Alta presión de vapor, hidrosolubilidad intermedia, extremadamente irritante |
Lesión difusa de la vía aérea y del parénquima |
|
|
Amoníaco |
Fabricación de fertilizantes, alimentos para animales, productos químicos y productos farmacéuticos |
Gas alcalino, muy alta solubilidad en agua |
Quemadura principalmente ocular y de las vías respiratorias superiores; la exposición masiva puede causar bronquiectasias |
500 |
|
Tricloruro de antimonio, pentacloruro de antimonio |
Aleaciones, catalizadores orgánicos |
Poca solubilidad, daño probablemente debido al ion haluro |
Neumonitis, edema pulmonar no cardiogénico |
|
|
Berilio |
Aleaciones (con cobre), cerámica; equipos electrónicos, aeroespaciales y de reactores nucleares |
Metal irritante, también actúa como antígeno para promover una respuesta granulomatosa a largo plazo |
Lesión aguda de la vía aérea superior, traqueobronquitis, neumonitis química |
25 μg/m3 |
|
Boranos (diborano) |
Combustible para aeronaves, fabricación de fungicidas |
gas soluble en agua |
Lesión de vía aérea superior, neumonitis con exposición masiva |
|
|
Bromuro de hidrógeno |
refinación del petróleo |
Lesión de vía aérea superior, neumonitis con exposición masiva |
||
|
Bromuro de metilo |
Refrigeración, fumigación de productos |
Gas moderadamente soluble |
Lesión de las vías respiratorias superiores e inferiores, neumonitis, depresión del SNC y convulsiones |
|
|
Cadmio |
Aleaciones con Zn y Pb, galvanoplastia, baterías, insecticidas |
Efectos respiratorios agudos y crónicos. |
Traqueobronquitis, edema pulmonar (a menudo aparición tardía de 24 a 48 horas); la exposición crónica de bajo nivel conduce a cambios inflamatorios y enfisema |
100 |
|
Óxido de calcio, hidróxido de calcio |
Cal, fotografía, bronceado, insecticidas |
Moderadamente cáustico, se requieren dosis muy altas para la toxicidad |
Inflamación de las vías respiratorias superiores e inferiores, neumonitis |
|
|
Cloro |
Blanqueo, formación de compuestos clorados, limpiadores domésticos |
Solubilidad en agua intermedia |
Inflamación de vías aéreas superiores e inferiores, neumonitis y edema pulmonar no cardiogénico |
5-10 |
|
cloroacetofenona |
Agente de control de multitudes, “gas lacrimógeno” |
Las cualidades irritantes se utilizan para incapacitar; agente alquilante |
Inflamación ocular y de la vía aérea superior, lesión de la vía aérea inferior y del parénquima con exposición masiva |
1-10 |
|
o-Clorobenzomalo- nitrilo |
Agente de control de multitudes, “gas lacrimógeno” |
Las cualidades irritantes se utilizan para incapacitar |
Inflamación ocular y de las vías respiratorias superiores, lesión de las vías respiratorias inferiores con exposición masiva |
|
|
Éteres de clorometilo |
Disolventes, utilizados en la fabricación de otros compuestos orgánicos. |
Irritación de las vías respiratorias superiores e inferiores, también cancerígeno de las vías respiratorias |
||
|
Cloropicrina |
Fabricación de productos químicos, componente fumigante |
Antiguo gas de la Primera Guerra Mundial |
Inflamación de las vías respiratorias superiores e inferiores |
15 |
|
Ácido crómico (Cr(IV)) |
Soldadura, chapado |
Irritante soluble en agua, sensibilizador alérgico |
Inflamación y ulceración nasal, rinitis, neumonitis con exposición masiva |
|
|
Cobalt |
Aleaciones de alta temperatura, imanes permanentes, herramientas de metal duro (con carburo de tungsteno) |
Irritante no específico, también sensibilizante alérgico |
broncoespasmo agudo y/o neumonitis; la exposición crónica puede causar fibrosis pulmonar |
|
|
Formaldehído |
Fabricación de aislamiento de espuma, madera contrachapada, textiles, papel, fertilizantes, resinas; agentes de embalsamamiento; productos de combustion |
Altamente soluble en agua, rápidamente metabolizado; actúa principalmente a través de la estimulación de los nervios sensoriales; sensibilización reportada |
Irritación ocular y de las vías respiratorias superiores; broncoespasmo en exposición severa; dermatitis de contacto en personas sensibilizadas |
3 |
|
Ácido clorhídrico |
Refinación de metales, fabricación de caucho, fabricación de compuestos orgánicos, materiales fotográficos |
Altamente soluble en agua |
Inflamación ocular y de las vías respiratorias superiores, inflamación de las vías respiratorias inferiores solo con exposición masiva |
100 |
|
Ácido fluorhídrico |
Catalizador químico, pesticidas, blanqueo, soldadura, grabado |
Altamente soluble en agua, potente y rápido oxidante, reduce el calcio sérico en exposición masiva |
Inflamación ocular y de las vías respiratorias superiores, traqueobronquitis y neumonitis con exposición masiva |
20 |
|
Isocianatos |
Producción de poliuretano; pinturas; productos herbicidas e insecticidas; laminado, muebles, esmaltado, trabajos en resina |
Compuestos orgánicos de bajo peso molecular, irritantes, causan sensibilización en personas susceptibles |
Inflamación ocular, superior e inferior; asma, neumonitis por hipersensibilidad en personas sensibilizadas |
0.1 |
|
Hidruro de litio |
Aleaciones, cerámica, electrónica, catalizadores químicos |
Baja solubilidad, altamente reactivo |
Neumonitis, edema pulmonar no cardiogénico |
|
|
Mercurio |
Electrólisis, extracción de minerales y amalgamas, fabricación de productos electrónicos |
Sin síntomas respiratorios con bajo nivel, exposición crónica |
Inflamación ocular y del tracto respiratorio, neumonitis, SNC, riñones y efectos sistémicos |
1.1 mg/mXNUMX3 |
|
carbonilo de níquel |
Refinación de níquel, galvanoplastia, reactivos químicos |
Toxina potente |
Irritación de las vías respiratorias inferiores, neumonitis, efectos tóxicos sistémicos retardados |
8 μg/m3 |
|
Dioxido de nitrogeno |
Silos después del nuevo almacenamiento de granos, fabricación de fertilizantes, soldadura por arco, productos de combustión |
Baja solubilidad en agua, gas marrón a alta concentración |
Inflamación ocular y de las vías respiratorias superiores, edema pulmonar no cardiogénico, bronquiolitis de aparición tardía |
50 |
|
mostazas nitrogenadas; mostazas de azufre |
gases militares |
Provoca lesiones graves, propiedades vesicantes. |
Inflamación ocular, de las vías respiratorias superiores e inferiores, neumonitis |
20 mg / m3 (N) 1 mg/mXNUMX3 (S) |
|
Tetroxido de osmio |
Refinación de cobre, aleación con iridio, catalizador para la síntesis de esteroides y formación de amoníaco |
El osmio metálico es inerte, se forma tetraóxido cuando se calienta en el aire. |
Irritación severa de los ojos y las vías respiratorias superiores; daño renal transitorio |
1 mg/mXNUMX3 |
|
Ozone |
Soldadura por arco, fotocopiadoras, blanqueo de papel |
Gas de olor dulce, solubilidad moderada en agua |
inflamación de las vías respiratorias superiores e inferiores; asmáticos más susceptibles |
1 |
|
Fosgeno |
Fabricación de plaguicidas y otros productos químicos, soldadura por arco, eliminación de pintura |
Poco soluble en agua, no irrita las vías respiratorias en dosis bajas |
inflamación de las vías respiratorias superiores y neumonitis; edema pulmonar retardado en dosis bajas |
2 |
|
sulfuros de fósforo |
Producción de insecticidas, compuestos de ignición, fósforos |
Inflamación ocular y de las vías respiratorias superiores |
||
|
Cloruros fosfóricos |
Fabricación de compuestos orgánicos clorados, colorantes, aditivos para gasolina |
Forma ácido fosfórico y ácido clorhídrico en contacto con superficies mucosas |
Inflamación ocular y de las vías respiratorias superiores |
10 mg/mXNUMX3 |
|
Dióxido de selenio |
Fundición de cobre o níquel, calentamiento de aleaciones de selenio |
Fuerte vesicante, forma ácido selenioso (H2SEO3) en superficies mucosas |
Inflamación ocular y de vías aéreas superiores, edema pulmonar en exposición masiva |
|
|
Seleniuro de hidrógeno |
Refinación de cobre, producción de ácido sulfúrico |
Agua soluble; la exposición a los compuestos de selenio da lugar al aliento con olor a ajo |
Inflamación ocular y de las vías respiratorias superiores, edema pulmonar tardío |
|
|
Estireno |
Fabricación de poliestireno y resinas, polímeros |
Altamente irritante |
Inflamación ocular, de las vías respiratorias superiores e inferiores, deficiencias neurológicas |
600 |
|
dióxido de azufre |
Refinación de petróleo, plantas de celulosa, plantas de refrigeración, fabricación de sulfito de sodio |
Gas altamente soluble en agua |
Inflamación de las vías respiratorias superiores, broncoconstricción, neumonitis por exposición masiva |
100 |
|
Tetracloruro de titanio |
Tintes, pigmentos, escritura del cielo. |
Los iones de cloruro forman HCl en la mucosa |
Lesión de la vía aérea superior |
|
|
Hexafluoruro de uranio |
Removedores de capa de metal, selladores de piso, pinturas en aerosol |
Toxicidad probable por iones de cloruro |
Lesión de las vías respiratorias superiores e inferiores, broncoespasmo, neumonitis |
|
|
Pentóxido de vanadio |
Limpieza de tanques de aceite, metalurgia |
Síntomas oculares, de las vías respiratorias superiores e inferiores |
70 |
|
|
Cloruro de zinc |
Granadas de humo, artillería |
Más grave que la exposición al óxido de zinc |
Irritación de las vías respiratorias superiores e inferiores, fiebre, neumonitis de aparición tardía |
200 |
|
Tetracloruro de circonio |
Pigmentos, catalizadores |
Toxicidad por iones de cloruro |
Irritación de las vías respiratorias superiores e inferiores, neumonitis |
Se cree que esta condición es el resultado de una inflamación persistente con una reducción de la permeabilidad de la capa de células epiteliales o un umbral de conductancia reducido para las terminaciones nerviosas subepiteliales. Adaptado de Sheppard 1988; Graham 1994; Roma 1992; Blanc y Schwartz 1994; Nemery 1990; Skornik 1988.
La naturaleza y extensión de la reacción a un irritante depende de las propiedades físicas del gas o aerosol, la concentración y el tiempo de exposición, y también de otras variables, como la temperatura, la humedad y la presencia de patógenos u otros gases (Man y Hulbert 1988). Factores del huésped como la edad (Cabral-Anderson, Evans y Freeman 1977; Evans, Cabral-Anderson y Freeman 1977), la exposición previa (Tyler, Tyler y Last 1988), el nivel de antioxidantes (McMillan y Boyd 1982) y la presencia de infección pueden desempeñan un papel en la determinación de los cambios patológicos observados. Esta amplia gama de factores ha dificultado el estudio sistemático de los efectos patógenos de los irritantes respiratorios.
Los irritantes mejor entendidos son aquellos que infligen daño oxidativo. La mayoría de los irritantes inhalados, incluidos los principales contaminantes, actúan por oxidación o dan lugar a compuestos que actúan de esta forma. La mayoría de los humos metálicos son en realidad óxidos del metal calentado; estos óxidos causan daño oxidativo. Los oxidantes dañan las células principalmente por peroxidación de lípidos y puede haber otros mecanismos. A nivel celular, inicialmente hay una pérdida bastante específica de células ciliadas del epitelio de las vías respiratorias y de células epiteliales alveolares de tipo I, con la consiguiente violación de la interfaz de unión estrecha entre las células epiteliales (Man y Hulbert 1988; Gordon, Salano y Kleinerman 1986). ; Stephens et al. 1974). Esto conduce a daño subepitelial y submucoso, con estimulación del músculo liso y terminaciones nerviosas aferentes sensoriales parasimpáticas que causan broncoconstricción (Holgate, Beasley y Twentyman 1987; Boucher 1981). Sigue una respuesta inflamatoria (Hogg 1981), y los neutrófilos y los eosinófilos liberan mediadores que provocan una mayor lesión oxidativa (Castleman et al. 1980). Los neumocitos tipo II y las células cuboidales actúan como células madre para la reparación (Keenan, Combs y McDowell 1982; Keenan, Wilson y McDowell 1983).
Otros mecanismos de lesión pulmonar finalmente involucran la vía oxidativa del daño celular, particularmente después de que ha ocurrido daño a la capa protectora de células epiteliales y se ha provocado una respuesta inflamatoria. Los mecanismos descritos con mayor frecuencia se describen en la tabla 2.
Tabla 2. Mecanismos de lesión pulmonar por sustancias inhaladas
|
Mecanismo de lesión |
Compuestos de ejemplo |
Daño que se produce |
|
Oxidación |
Ozono, dióxido de nitrógeno, dióxido de azufre, cloro, óxidos |
Daño epitelial irregular de las vías respiratorias, con aumento de la permeabilidad y exposición de las terminaciones de las fibras nerviosas; pérdida de cilios de las células ciliadas; necrosis de neumocitos tipo I; formación de radicales libres y posterior unión a proteínas y peroxidación lipídica |
|
Formación de ácido |
Dióxido de azufre, cloro, haluros |
El gas se disuelve en agua para formar ácido que daña las células epiteliales por oxidación; acción principalmente en la vía aérea superior |
|
formación de álcali |
Amoníaco, óxido de calcio, hidróxidos |
El gas se disuelve en agua para formar una solución alcalina que puede causar la licuefacción del tejido; Daño predominante de las vías respiratorias superiores, vías respiratorias inferiores en exposiciones intensas |
|
Enlace proteico |
Formaldehído |
Las reacciones con aminoácidos conducen a intermediarios tóxicos con daño a la capa de células epiteliales |
|
Estimulación nerviosa aferente |
amoníaco, formaldehído |
La estimulación directa de las terminaciones nerviosas provoca síntomas |
|
antigenicidad |
Platino, anhídridos de ácido |
Moléculas de bajo peso molecular sirven como haptenos en personas sensibilizadas |
|
Estimulación de la respuesta inflamatoria del huésped |
Óxidos de cobre y zinc, lipoproteínas |
Estimulación de citocinas y mediadores inflamatorios sin daño celular directo aparente |
|
Formación de radicales libres |
Paraquat |
Promoción de la formación o retraso de la eliminación de radicales superóxido, lo que lleva a la peroxidación lipídica y al daño oxidativo |
|
Eliminación de partículas retardada |
Cualquier inhalación prolongada de polvo mineral. |
Abrumamiento de las escaleras mecánicas mucociliares y los sistemas de macrófagos alveolares con partículas, lo que lleva a una respuesta inflamatoria no específica |
Los trabajadores expuestos a niveles bajos de irritantes respiratorios pueden tener síntomas subclínicos atribuibles a la irritación de las membranas mucosas, como ojos llorosos, dolor de garganta, secreción nasal y tos. Con una exposición significativa, la sensación adicional de dificultad para respirar a menudo requerirá atención médica. Es importante obtener un buen historial médico para determinar la composición probable de la exposición, la cantidad de exposición y el período de tiempo durante el cual tuvo lugar la exposición. Deben buscarse signos de edema laríngeo, incluidos ronquera y estridor, y deben examinarse los pulmones en busca de signos de afectación de las vías respiratorias inferiores o del parénquima. La evaluación de las vías respiratorias y la función pulmonar, junto con la radiografía de tórax, son importantes en el tratamiento a corto plazo. La laringoscopia puede estar indicada para evaluar las vías respiratorias.
Si las vías respiratorias están amenazadas, el paciente debe someterse a intubación y atención de apoyo. Los pacientes con signos de edema laríngeo deben observarse durante al menos 12 horas para asegurarse de que el proceso se autolimite. El broncoespasmo debe tratarse con agonistas beta y, si es refractario, con corticosteroides intravenosos. Las mucosas bucales y oculares irritadas deben irrigarse a fondo. Los pacientes con crepitantes en el examen o anomalías en la radiografía de tórax deben ser hospitalizados para observación ante la posibilidad de neumonitis o edema pulmonar. Dichos pacientes corren el riesgo de sobreinfección bacteriana; sin embargo, no se ha demostrado ningún beneficio con el uso de antibióticos profilácticos.
La abrumadora mayoría de los pacientes que sobreviven al insulto inicial se recuperan por completo de las exposiciones irritantes. Las posibilidades de secuelas a largo plazo son más probables con una lesión inicial mayor. El termino síndrome de disfunción reactiva de las vías respiratorias (RADS) se ha aplicado a la persistencia de síntomas parecidos al asma después de una exposición aguda a irritantes respiratorios (Brooks, Weiss y Bernstein 1985).
Las exposiciones de alto nivel a álcalis y ácidos pueden causar quemaduras en las vías respiratorias superiores e inferiores que conducen a enfermedades crónicas. Se sabe que el amoníaco causa bronquiectasias (Kass et al. 1972); Se informa que el cloro gaseoso (que se convierte en HCl en la mucosa) causa enfermedad pulmonar obstructiva (Donelly y Fitzgerald 1990; Das y Blanc 1993). Las exposiciones crónicas de bajo nivel a irritantes pueden causar síntomas oculares y de las vías respiratorias superiores continuos (Korn, Dockery y Speizer 1987), pero el deterioro de la función pulmonar no se ha documentado de manera concluyente. Los estudios de los efectos de los irritantes crónicos de bajo nivel en la función de las vías respiratorias se ven obstaculizados por la falta de seguimiento a largo plazo, lo que se confunde con el tabaquismo, el "efecto del trabajador sano" y el efecto clínico real mínimo, si es que existe (Brooks y Kalica 1987).
Después de que un paciente se recupera de la lesión inicial, se necesita un seguimiento regular por parte de un médico. Claramente, debe haber un esfuerzo para investigar el lugar de trabajo y evaluar las precauciones respiratorias, la ventilación y la contención de los irritantes culpables.
Químicos tóxicos
Los productos químicos tóxicos para los pulmones incluyen la mayoría de los irritantes respiratorios con una exposición lo suficientemente alta, pero hay muchos productos químicos que causan una lesión pulmonar parenquimatosa significativa a pesar de poseer propiedades irritantes de bajas a moderadas. Estos compuestos ejercen sus efectos mediante mecanismos revisados en la Tabla 3 y discutidos anteriormente. Las toxinas pulmonares tienden a ser menos solubles en agua que los irritantes de las vías respiratorias superiores. En la tabla 3 se revisan ejemplos de toxinas pulmonares y sus fuentes de exposición.
Tabla 3. Compuestos capaces de producir toxicidad pulmonar después de una exposición de baja a moderada
|
Compuesto |
Fuentes de exposición |
Toxicidad |
|
Acroleína |
Plásticos, textiles, fabricación farmacéutica, productos de combustión |
Lesión difusa de la vía aérea y del parénquima |
|
tricloruro de antimonio; antimonio |
Aleaciones, catalizadores orgánicos |
Neumonitis, edema pulmonar no cardiogénico |
|
Cadmio |
Aleaciones con zinc y plomo, galvanoplastia, baterías, insecticidas |
Traqueobronquitis, edema pulmonar (a menudo aparición tardía de 24 a 48 horas), daño renal: proteinuria tubular |
|
Cloropicrina |
Fabricación de productos químicos, componentes fumigantes |
Inflamación de las vías respiratorias superiores e inferiores |
|
Cloro |
Blanqueo, formación de compuestos clorados, limpiadores domésticos |
Inflamación de vías aéreas superiores e inferiores, neumonitis y edema pulmonar no cardiogénico |
|
Sulfuro de hidrógeno |
Pozos de gas natural, minas, estiércol |
Irritación ocular, de las vías respiratorias superiores e inferiores, edema pulmonar retardado, asfixia por hipoxia tisular sistémica |
|
Hidruro de litio |
Aleaciones, cerámica, electrónica, catalizadores químicos |
Neumonitis, edema pulmonar no cardiogénico |
|
Isocianato de metilo |
Síntesis de plaguicidas |
Irritación del tracto respiratorio superior e inferior, edema pulmonar |
|
Mercurio |
Electrólisis, extracción de minerales y amalgamas, fabricación de productos electrónicos |
Inflamación ocular y del tracto respiratorio, neumonitis, SNC, riñones y efectos sistémicos |
|
carbonilo de níquel |
Refinación de níquel, galvanoplastia, reactivos químicos |
Irritación de las vías respiratorias inferiores, neumonitis, efectos tóxicos sistémicos retardados |
|
Dioxido de nitrogeno |
Silos después del nuevo almacenamiento de granos, fabricación de fertilizantes, soldadura por arco; productos de combustion |
Inflamación ocular y de las vías respiratorias superiores, edema pulmonar no cardiogénico, bronquiolitis de aparición tardía |
|
Mostazas nitrogenadas, azufre |
Agentes militares, vesicantes |
Inflamación ocular y del tracto respiratorio, neumonitis |
|
Paraquat |
Herbicidas (ingeridos) |
Daño selectivo a los neumocitos tipo 2 que conduce a RADS, fibrosis pulmonar; insuficiencia renal, irritación GI |
|
Fosgeno |
Fabricación de plaguicidas y otros productos químicos, soldadura por arco, eliminación de pintura |
inflamación de las vías respiratorias superiores y neumonitis; edema pulmonar retardado en dosis bajas |
|
Cloruro de zinc |
Granadas de humo, artillería |
Irritación de las vías respiratorias superiores e inferiores, fiebre, neumonitis de aparición tardía |
Un grupo de toxinas inhalables se denomina asfixiantes. Cuando están presentes en concentraciones lo suficientemente altas, los asfixiantes, dióxido de carbono, metano y nitrógeno, desplazan al oxígeno y asfixian a la víctima. El cianuro de hidrógeno, el monóxido de carbono y el sulfuro de hidrógeno actúan inhibiendo la respiración celular a pesar del aporte adecuado de oxígeno a los pulmones. Las toxinas inhaladas no asfixiantes dañan los órganos diana, causando una amplia variedad de problemas de salud y mortalidad.
El manejo médico de las toxinas pulmonares inhaladas es similar al manejo de los irritantes respiratorios. Estas toxinas a menudo no provocan su efecto clínico máximo hasta varias horas después de la exposición; Puede estar indicado el control durante la noche para los compuestos que se sabe que causan edema pulmonar de aparición tardía. Dado que la terapia de toxinas sistémicas está más allá del alcance de este capítulo, se remite al lector a las discusiones de las toxinas individuales en otras partes de este capítulo. Enciclopedia y en otros textos sobre el tema (Goldfrank et al. 1990; Ellenhorn y Barceloux 1988).
Fiebres por Inhalación
Ciertas exposiciones por inhalación que ocurren en una variedad de entornos laborales diferentes pueden provocar enfermedades debilitantes similares a la gripe que duran unas pocas horas. Estos se conocen colectivamente como fiebres por inhalación. A pesar de la gravedad de los síntomas, la toxicidad parece ser autolimitada en la mayoría de los casos y hay pocos datos que sugieran secuelas a largo plazo. La exposición masiva a los compuestos incitadores puede provocar una reacción más grave con neumonitis y edema pulmonar; estos casos poco frecuentes se consideran más complicados que la simple fiebre por inhalación.
Las fiebres por inhalación tienen en común la característica de la inespecificidad: el síndrome se puede producir en casi cualquier persona, con una exposición adecuada al agente incitador. No se requiere sensibilización, y no es necesaria una exposición previa. Algunos de los síndromes presentan el fenómeno de la tolerancia; es decir, con la exposición regular repetida los síntomas no ocurren. Se cree que este efecto está relacionado con una mayor actividad de los mecanismos de eliminación, pero no se ha estudiado adecuadamente.
Síndrome Tóxico del Polvo Orgánico
Síndrome tóxico del polvo orgánico (ODTS) es un término amplio que denota los síntomas autolimitados similares a los de la gripe que ocurren después de una exposición intensa a polvos orgánicos. El síndrome abarca una amplia gama de enfermedades febriles agudas que tienen nombres derivados de las tareas específicas que conducen a la exposición al polvo. Los síntomas ocurren solo después de una exposición masiva al polvo orgánico, y la mayoría de las personas así expuestas desarrollarán el síndrome.
El síndrome tóxico del polvo orgánico ha sido previamente llamado micotoxicosis pulmonar, debido a su supuesta etiología en la acción de las esporas de moho y actinomicetos. Con algunos pacientes, uno puede cultivar especies de Aspergilo, penicilliumy mesófilos y termófilos actinomicetos (Emmanuel, Marx y Ault 1975; Emmanuel, Marx y Ault 1989). Más recientemente, se ha propuesto que las endotoxinas bacterianas desempeñan un papel al menos igual de importante. El síndrome ha sido provocado experimentalmente por la inhalación de endotoxinas derivadas de Enterobacter aglomerantes, un componente principal del polvo orgánico (Rylander, Bake y Fischer 1989). Los niveles de endotoxinas se han medido en el entorno de la granja, con niveles que oscilan entre 0.01 y 100 μg/m3. Muchas muestras tenían un nivel superior a 0.2 μg/m3, que es el nivel donde se sabe que ocurren los efectos clínicos (May, Stallones y Darrow 1989). Existe la especulación de que las citocinas, como la IL-1, pueden mediar los efectos sistémicos, dado lo que ya se sabe acerca de la liberación de IL-1 de los macrófagos alveolares en presencia de endotoxina (Richerson 1990). Los mecanismos alérgicos son poco probables dada la falta de necesidad de sensibilización y el requisito de una alta exposición al polvo.
Clínicamente, el paciente suele presentar síntomas de 2 a 8 horas después de la exposición a cereales, heno, algodón, lino, cáñamo o virutas de madera (normalmente mohosas), o tras la manipulación de cerdos (Do Pico 1992). A menudo, los síntomas comienzan con irritación de los ojos y las membranas mucosas con tos seca, que progresa a fiebre y malestar general, opresión en el pecho, mialgias y dolor de cabeza. El paciente parece enfermo pero por lo demás normal en el examen físico. Con frecuencia se presenta leucocitosis, con niveles de hasta 25,000 XNUMX glóbulos blancos (WBC)/mm3. La radiografía de tórax es casi siempre normal. La espirometría puede revelar un defecto obstructivo modesto. En los casos en los que se realizó broncoscopia de fibra óptica y se obtuvieron lavados bronquiales, se encontró elevación de leucocitos en el líquido de lavado. El porcentaje de neutrófilos fue significativamente más alto de lo normal (Emmanuel, Marx y Ault 1989; Lecours, Laviolette y Cormier 1986). La broncoscopia de 1 a 4 semanas después del evento muestra una celularidad persistentemente alta, predominantemente linfocitos.
Dependiendo de la naturaleza de la exposición, el diagnóstico diferencial puede incluir la exposición a gases tóxicos (como dióxido de nitrógeno o amoníaco), particularmente si el episodio ocurrió en un silo. Se debe considerar la neumonitis por hipersensibilidad, especialmente si hay anomalías significativas en la radiografía de tórax o en las pruebas de función pulmonar. La distinción entre neumonitis por hipersensibilidad (HP) y ODTS es importante: HP requerirá evitar la exposición estricta y tiene un peor pronóstico, mientras que ODTS tiene un curso benigno y autolimitado. ODTS también se distingue de HP porque ocurre con más frecuencia, requiere niveles más altos de exposición al polvo, no induce la liberación de anticuerpos precipitantes en suero y (inicialmente) no da lugar a la alveolitis linfocítica que es característica de HP.
Los casos se manejan con antipiréticos. No se ha recomendado un papel para los esteroides dada la naturaleza autolimitada de la enfermedad. Se debe educar a los pacientes sobre cómo evitar la exposición masiva. Se cree que el efecto a largo plazo de las ocurrencias repetidas es insignificante; sin embargo, esta cuestión no ha sido adecuadamente estudiada.
Fiebre de humos metálicos
La fiebre por humos metálicos (MFF, por sus siglas en inglés) es otra enfermedad autolimitada similar a la gripe que se desarrolla después de la exposición por inhalación, en este caso a humos metálicos. El síndrome se desarrolla más comúnmente después de la inhalación de óxido de zinc, como ocurre en las fundiciones de latón y en la fundición o soldadura de metal galvanizado. Los óxidos de cobre y hierro también causan MFF, y ocasionalmente se han implicado vapores de aluminio, arsénico, cadmio, mercurio, cobalto, cromo, plata, manganeso, selenio y estaño (Rose 1992). Los trabajadores desarrollan taquifalaxis; es decir, los síntomas aparecen solo cuando la exposición ocurre después de varios días sin exposición, no cuando hay exposiciones regulares repetidas. Un TLV de ocho horas de 5 mg/m3 para el óxido de zinc ha sido establecido por la Administración de Salud y Seguridad Ocupacional de los Estados Unidos (OSHA), pero los síntomas se han obtenido experimentalmente después de una exposición de dos horas a esta concentración (Gordon et al. 1992).
La patogenia de MFF sigue sin estar clara. El inicio reproducible de los síntomas, independientemente del individuo expuesto, argumenta en contra de una sensibilización alérgica o inmunológica específica. La falta de síntomas asociados con la liberación de histamina (sofocos, picazón, sibilancias, urticaria) también va en contra de la probabilidad de un mecanismo alérgico. Paul Blanc y colaboradores han desarrollado un modelo que implica la liberación de citoquinas (Blanc et al. 1991; Blanc et al. 1993). Midieron los niveles del factor de necrosis tumoral (TNF) y de las interleucinas IL-1, IL-4, IL-6 e IL-8 en el líquido lavado de los pulmones de 23 voluntarios expuestos experimentalmente a vapores de óxido de zinc (Blanc et al. al. 1993). Los voluntarios desarrollaron niveles elevados de TNF en su líquido de lavado broncoalveolar (BAL) 3 horas después de la exposición. Veinte horas más tarde, se observaron niveles elevados de IL-8 (un potente atrayente de neutrófilos) en el LBA y una impresionante alveolitis neutrofílica. Se ha demostrado que el TNF, una citocina capaz de causar fiebre y estimular las células inmunitarias, se libera de los monocitos en cultivos expuestos al zinc (Scuderi 1990). En consecuencia, la presencia de TNF aumentado en el pulmón explica la aparición de los síntomas observados en MFF. Se sabe que el TNF estimula la liberación tanto de IL-6 como de IL-8, en un período de tiempo que se correlaciona con los picos de las citoquinas en el líquido BAL de estos voluntarios. El reclutamiento de estas citocinas puede explicar la alveolitis de neutrófilos resultante y los síntomas similares a los de la gripe que caracterizan a la MFF. Por qué la alveolitis se resuelve tan rápido sigue siendo un misterio.
Los síntomas comienzan de 3 a 10 horas después de la exposición. Inicialmente, puede haber un sabor dulce metálico en la boca, acompañado de un empeoramiento de la tos seca y dificultad para respirar. A menudo se desarrollan fiebre y escalofríos y el trabajador se siente enfermo. El examen físico es por lo demás normal. La evaluación de laboratorio muestra una leucocitosis y una radiografía de tórax normal. Los estudios de función pulmonar pueden mostrar un FEF ligeramente reducido25 - 75 y niveles de DLCO (Nemery 1990; Rose 1992).
Con una buena historia, el diagnóstico se establece fácilmente y el trabajador puede ser tratado sintomáticamente con antipiréticos. Los síntomas y las anomalías clínicas se resuelven en 24 a 48 horas. De lo contrario, se deben considerar las etiologías bacterianas y virales de los síntomas. En casos de exposición extrema, o exposiciones que involucran contaminación por toxinas como cloruro de zinc, cadmio o mercurio, la MFF puede ser un presagio de una neumonitis química clínica que evolucionará durante los próximos 2 días (Blount 1990). Tales casos pueden exhibir infiltrados difusos en una radiografía de tórax y signos de edema pulmonar e insuficiencia respiratoria. Si bien esta posibilidad debe considerarse en la evaluación inicial de un paciente expuesto, un curso tan fulminante es inusual y no es característico de MFF sin complicaciones.
MFF no requiere una sensibilidad específica del individuo para los humos metálicos; más bien, indica un control ambiental inadecuado. El problema de exposición debe abordarse para prevenir síntomas recurrentes. Aunque el síndrome se considera benigno, los efectos a largo plazo de episodios repetidos de MFF no se han investigado adecuadamente.
Fiebre de humo de polímero
La fiebre por vapores de polímeros es una enfermedad febril autolimitada similar a la MFF, pero causada por productos de pirólisis inhalados de fluoropolímeros, incluido el politetrafluoroetano (PTFE; nombres comerciales Teflon, Fluon, Halon). El PTFE se usa ampliamente por sus propiedades lubricantes, de estabilidad térmica y de aislamiento eléctrico. Es inofensivo a menos que se caliente por encima de los 30 °C, cuando comienza a liberar productos de degradación (Shusterman 1993). Esta situación ocurre cuando se sueldan materiales recubiertos con PTFE, se calienta PTFE con el borde de una herramienta durante el mecanizado de alta velocidad, se operan máquinas de moldeo o extrusión (Rose 1992) y rara vez durante la cirugía láser endotraqueal (Rom 1992a).
Una causa común de la fiebre por vapores de polímeros se descubrió después de un período de trabajo detectivesco clásico de salud pública a principios de la década de 1970 (Wegman y Peters 1974; Kuntz y McCord 1974). Los trabajadores textiles estaban desarrollando enfermedades febriles autolimitadas con exposiciones a formaldehído, amoníaco y fibra de nailon; no estuvieron expuestos a vapores de fluoropolímero, pero manipularon polímero triturado. Después de encontrar que los niveles de exposición de los otros posibles agentes etiológicos estaban dentro de los límites aceptables, el trabajo con fluoropolímeros se examinó más de cerca. Al final resultó que, solo los fumadores de cigarrillos que trabajaban con el fluoropolímero eran sintomáticos. Se planteó la hipótesis de que los cigarrillos se contaminaban con fluoropolímero en las manos del trabajador, luego el producto se quemaba en el cigarrillo cuando se fumaba, exponiendo al trabajador a gases tóxicos. Después de prohibir fumar cigarrillos en el lugar de trabajo y establecer reglas estrictas para lavarse las manos, no se informaron más enfermedades (Wegman y Peters 1974). Desde entonces, este fenómeno se ha reportado después de trabajar con compuestos impermeabilizantes, compuestos desmoldantes (Albrecht y Bryant 1987) y después de usar ciertos tipos de cera para esquí (Strom y Alexandersen 1990).
Se desconoce la patogenia de la fiebre por vapores de polímeros. Se cree que es similar a las otras fiebres por inhalación debido a su presentación similar y su respuesta inmunitaria aparentemente inespecífica. No ha habido estudios experimentales en humanos; sin embargo, tanto las ratas como las aves desarrollan daño epitelial alveolar severo al exponerse a productos de pirólisis de PTFE (Wells, Slocombe y Trapp 1982; Blandford et al. 1975). No se ha realizado una medición precisa de la función pulmonar o los cambios de líquido del BAL.
Los síntomas aparecen varias horas después de la exposición, y no hay un efecto de tolerancia o taquifalaxis como se ve en MFF. La debilidad y las mialgias van seguidas de fiebre y escalofríos. A menudo hay opresión en el pecho y tos. Por lo demás, la exploración física suele ser normal. A menudo se observa leucocitosis y la radiografía de tórax suele ser normal. Los síntomas se resuelven espontáneamente en 12 a 48 horas. Ha habido algunos casos de personas que desarrollaron edema pulmonar después de la exposición; en general, se piensa que los humos de PTFE son más tóxicos que los humos de zinc o cobre en la causa de MFF (Shusterman 1993; Brubaker 1977). Se ha informado disfunción crónica de las vías respiratorias en personas que han tenido múltiples episodios de fiebre por vapores de polímeros (Williams, Atkinson y Patchefsky 1974).
El diagnóstico de fiebre por vapores de polímeros requiere una historia cuidadosa con alta sospecha clínica. Después de determinar la fuente de los productos de pirólisis de PTFE, se deben hacer esfuerzos para evitar una mayor exposición. Las reglas obligatorias de lavado de manos y la eliminación de fumar en el lugar de trabajo han eliminado efectivamente los casos relacionados con cigarrillos contaminados. Los trabajadores que han tenido múltiples episodios de fiebre por vapores de polímeros o edema pulmonar asociado deben tener un seguimiento médico a largo plazo.
Asma ocupacional
El asma es una enfermedad respiratoria caracterizada por la obstrucción de las vías respiratorias que es parcial o completamente reversible, ya sea espontáneamente o con tratamiento; inflamación de las vías respiratorias; y mayor capacidad de respuesta de las vías respiratorias a una variedad de estímulos (NAEP 1991). El asma ocupacional (OA, por sus siglas en inglés) es asma causada por exposiciones ambientales en el lugar de trabajo. Se ha informado que varios cientos de agentes causan OA. El asma preexistente o la hiperreactividad de las vías respiratorias, con síntomas que empeoran por la exposición laboral a irritantes o estímulos físicos, generalmente se clasifican por separado como asma agravada por el trabajo (WAA). Existe un acuerdo general de que la OA se ha convertido en la enfermedad pulmonar ocupacional más frecuente en los países desarrollados, aunque las estimaciones de la prevalencia e incidencia reales son bastante variables. Está claro, sin embargo, que en muchos países el asma de etiología ocupacional causa una carga de enfermedad y discapacidad en gran medida no reconocida con altos costos económicos y no económicos. Gran parte de esta carga económica y de salud pública se puede prevenir potencialmente identificando y controlando o eliminando las exposiciones en el lugar de trabajo que causan el asma. Este artículo resumirá los enfoques actuales para el reconocimiento, manejo y prevención de la OA. Varias publicaciones recientes discuten estos temas con más detalle (Chan-Yeung 1995; Bernstein et al. 1993).
Magnitud del problema
Las prevalencias de asma en adultos generalmente oscilan entre el 3 y el 5%, según la definición de asma y las variaciones geográficas, y pueden ser considerablemente más altas en algunas poblaciones urbanas de bajos ingresos. Se informa que la proporción de casos de asma en adultos en la población general que está relacionada con el entorno laboral oscila entre el 2 y el 23 %, y las estimaciones recientes tienden hacia el extremo superior del rango. Las prevalencias de asma y OA se han estimado en estudios transversales y de cohortes pequeñas de grupos ocupacionales de alto riesgo. En una revisión de 22 estudios seleccionados de lugares de trabajo con exposiciones a sustancias específicas, las prevalencias de asma u OA, definidas de varias maneras, oscilaron entre el 3 y el 54 %, y 12 estudios informaron prevalencias superiores al 15 % (Becklake, en Bernstein et al. 1993). ). El amplio rango refleja la variación real en la prevalencia real (debido a diferentes tipos y niveles de exposición). También refleja las diferencias en los criterios de diagnóstico y la variación en la fuerza de los sesgos, como el "sesgo del sobreviviente" que puede resultar de la exclusión de los trabajadores que desarrollaron OA y abandonaron el lugar de trabajo antes de que se realizara el estudio. Las estimaciones poblacionales de incidencia oscilan entre 14 por millón de adultos empleados por año en los Estados Unidos y 140 por millón de adultos empleados por año en Finlandia (Meredith y Nordman 1996). En Finlandia, la determinación de los casos fue más completa y los métodos de diagnóstico, en general, más rigurosos. La evidencia de estas diferentes fuentes es consistente en su implicación de que la OA es a menudo subdiagnosticada y/o subnotificada y es un problema de salud pública de mayor magnitud de lo que generalmente se reconoce.
Causas del asma ocupacional
Se han informado más de 200 agentes (sustancias específicas, ocupaciones o procesos industriales) que causan OA, según la evidencia epidemiológica y/o clínica. En la OA, la inflamación de las vías respiratorias y la broncoconstricción pueden ser causadas por una respuesta inmunológica a los agentes sensibilizantes, por efectos irritantes directos o por otros mecanismos no inmunológicos. Algunos agentes (p. ej., insecticidas organofosforados) también pueden causar broncoconstricción por acción farmacológica directa. Se cree que la mayoría de los agentes informados inducen una respuesta de sensibilización. Los irritantes respiratorios a menudo empeoran los síntomas en los trabajadores con asma preexistente (es decir, WAA) y, a altos niveles de exposición, pueden causar una nueva aparición de asma (denominada síndrome de disfunción reactiva de las vías respiratorias (RADS) o asma inducida por irritantes) (Brooks, Weiss y Bernstein 1985; Alberts y Do Pico 1996).
La OA puede ocurrir con o sin un período de latencia. El período de latencia se refiere al tiempo entre la exposición inicial y el desarrollo de los síntomas, y es muy variable. A menudo es menos de 2 años, pero en alrededor del 20% de los casos es de 10 años o más. La OA con latencia generalmente es causada por la sensibilización a uno o más agentes. RADS es un ejemplo de OA sin latencia.
Los agentes sensibilizantes de alto peso molecular (5,000 daltons (Da) o más) a menudo actúan por un mecanismo dependiente de IgE. Los agentes sensibilizantes de bajo peso molecular (menos de 5,000 Da), que incluyen sustancias químicas altamente reactivas como los isocianatos, pueden actuar mediante mecanismos independientes de IgE o pueden actuar como haptenos, combinándose con proteínas corporales. Una vez que un trabajador se sensibiliza a un agente, la reexposición (con frecuencia a niveles muy por debajo del nivel que causó la sensibilización) da como resultado una respuesta inflamatoria en las vías respiratorias, a menudo acompañada de aumentos en la limitación del flujo de aire y una respuesta bronquial no específica (NBR).
En estudios epidemiológicos de OA, las exposiciones en el lugar de trabajo son consistentemente los determinantes más fuertes de la prevalencia del asma, y el riesgo de desarrollar OA con latencia tiende a aumentar con la intensidad estimada de exposición. La atopia es un factor determinante importante y el tabaquismo algo menos consistente de la aparición de asma en estudios de agentes que actúan a través de un mecanismo dependiente de IgE. Ni la atopia ni el tabaquismo parecen ser un determinante importante del asma en los estudios de agentes que actúan a través de mecanismos independientes de IgE.
Presentación clínica
El espectro de síntomas de la OA es similar al asma no ocupacional: sibilancias, tos, opresión en el pecho y dificultad para respirar. Los pacientes a veces presentan asma tos-variante o nocturna. La OA puede ser grave e incapacitante, y se han informado muertes. El inicio de la OA ocurre debido a un entorno laboral específico, por lo que identificar las exposiciones que ocurrieron en el momento del inicio de los síntomas asmáticos es clave para un diagnóstico preciso. En WAA, las exposiciones en el lugar de trabajo causan un aumento significativo en la frecuencia y/o gravedad de los síntomas de asma preexistente.
Varias características de la historia clínica pueden sugerir una etiología ocupacional (Chan-Yeung 1995). Los síntomas con frecuencia empeoran en el trabajo o por la noche después del trabajo, mejoran en los días libres y reaparecen al regresar al trabajo. Los síntomas pueden empeorar progresivamente hacia el final de la semana laboral. El paciente puede notar actividades o agentes específicos en el lugar de trabajo que desencadenan síntomas de manera reproducible. La irritación ocular relacionada con el trabajo o la rinitis pueden estar asociadas con síntomas asmáticos. Estos patrones de síntomas típicos pueden estar presentes solo en las etapas iniciales de la OA. La resolución parcial o completa durante los fines de semana o las vacaciones es común al principio del curso de la OA, pero con exposiciones repetidas, el tiempo requerido para la recuperación puede aumentar a una o dos semanas, o la recuperación puede dejar de ocurrir. La mayoría de los pacientes con OA cuyas exposiciones finalizan continúan teniendo asma sintomática incluso años después del cese de la exposición, con deterioro e incapacidad permanentes. La exposición continua se asocia con un mayor empeoramiento del asma. La duración breve y la gravedad leve de los síntomas en el momento del cese de la exposición son factores de buen pronóstico y disminuyen la probabilidad de asma permanente.
Se han informado varios patrones temporales característicos de los síntomas de la OA. Las reacciones asmáticas tempranas suelen ocurrir poco tiempo (menos de una hora) después de comenzar a trabajar o de la exposición laboral específica que causa el asma. Las reacciones asmáticas tardías comienzan de 4 a 6 horas después de que comienza la exposición y pueden durar de 24 a 48 horas. Las combinaciones de estos patrones ocurren como reacciones asmáticas duales con resolución espontánea de los síntomas que separan una reacción temprana de una tardía, o como reacciones asmáticas continuas sin resolución de los síntomas entre las fases. Con excepciones, las reacciones tempranas tienden a ser mediadas por IgE y las reacciones tardías tienden a ser independientes de IgE.
El aumento de NBR, generalmente medido por metacolina o histamina, se considera una característica cardinal del asma ocupacional. El curso temporal y el grado de NBR pueden ser útiles en el diagnóstico y seguimiento. La NBR puede disminuir dentro de varias semanas después del cese de la exposición, aunque la NBR anormal comúnmente persiste durante meses o años después de que finalizan las exposiciones. En personas con asma ocupacional inducida por irritantes, no se espera que la NBR varíe con la exposición y/o los síntomas.
Reconocimiento y Diagnóstico
El diagnóstico preciso de la OA es importante, dadas las consecuencias negativas sustanciales del diagnóstico insuficiente o excesivo. En trabajadores con OA o en riesgo de desarrollar OA, el reconocimiento, identificación y control oportunos de las exposiciones ocupacionales que causan el asma mejoran las posibilidades de prevención o recuperación completa. Esta prevención primaria puede reducir en gran medida los altos costos financieros y humanos del asma crónica e incapacitante. Por el contrario, dado que un diagnóstico de OA puede obligar a un cambio completo de ocupación o intervenciones costosas en el lugar de trabajo, distinguir con precisión la OA del asma que no es ocupacional puede evitar costos sociales y financieros innecesarios tanto para los empleadores como para los trabajadores.
Se han propuesto varias definiciones de caso de OA, apropiadas en diferentes circunstancias. Las definiciones que se consideran valiosas para la detección o vigilancia de los trabajadores (Hoffman et al. 1990) pueden no ser del todo aplicables con fines clínicos o de compensación. Un consenso de investigadores ha definido la OA como “una enfermedad caracterizada por limitación variable del flujo de aire y/o hiperreactividad de las vías respiratorias debido a causas y condiciones atribuibles a un entorno ocupacional particular y no a estímulos encontrados fuera del lugar de trabajo” (Bernstein et al. 1993) . Esta definición se ha operacionalizado como una definición de caso médico, resumida en la tabla 1 (Chan-Yeung 1995).
Tabla 1. Definición de caso médico de asma ocupacional de la ACCP
Criterios para el diagnóstico de asma ocupacional1 (requiere los 4, AD):
(A) Diagnóstico médico de asma y/o evidencia fisiológica de hiperreactividad de las vías respiratorias
(B) La exposición ocupacional precedió al inicio de los síntomas asmáticos1
(C) Asociación entre síntomas de asma y trabajo
(D) Exposición y/o evidencia fisiológica de la relación del asma con el ambiente del lugar de trabajo (El diagnóstico de OA requiere uno o más de D2-D5, probablemente OA requiere solo D1)
(1) Exposición en el lugar de trabajo a un agente informado que da lugar a OA
(2) Cambios relacionados con el trabajo en FEV1 y/o FEM
(3) Cambios relacionados con el trabajo en las pruebas en serie para la respuesta bronquial no específica (p. ej., prueba de provocación con metacolina)
(4) Prueba de provocación bronquial específica positiva
(5) Aparición de asma con una clara asociación con una exposición sintomática a un irritante inhalado en el lugar de trabajo (generalmente RADS)
Criterios para el diagnóstico de RADS (deben cumplir los 7):
(1) Ausencia documentada de síntomas similares al asma preexistentes
(2) Aparición de síntomas después de un solo incidente de exposición o accidente
(3) Exposición a un gas, humo, humo, vapor o polvo con propiedades irritantes presente en alta concentración
(4) Inicio de los síntomas dentro de las 24 horas posteriores a la exposición con persistencia de los síntomas durante al menos 3 meses
(5) Síntomas compatibles con asma: tos, sibilancias, disnea
(6) Presencia de obstrucción del flujo de aire en las pruebas de función pulmonar y/o presencia de hiperreactividad bronquial no específica (las pruebas deben realizarse poco después de la exposición)
(7) Otras enfermedades pulmonares descartadas
Criterios para el diagnóstico de asma agravada por el trabajo (WAA):
(1) Cumple con los criterios A y C de la definición de OA de caso médico de la ACCP
(2) Asma preexistente o antecedentes de síntomas asmáticos (con síntomas activos durante el año anterior al inicio del empleo o exposición de interés)
(3) Aumento claro de los síntomas o necesidad de medicación, o documentación de cambios en el PEF relacionados con el trabajoR o VEF1 después del inicio del empleo o exposición de interés
1 Una definición de caso que requiera A, C y cualquiera de D1 a D5 puede ser útil en la vigilancia de OA, WAA y RADS.
Fuente: Chan-Yeung 1995.
La evaluación clínica exhaustiva de la OA puede llevar mucho tiempo, ser costosa y difícil. Puede requerir ensayos de diagnóstico de retiro y regreso al trabajo y, a menudo, requiere que el paciente registre de manera confiable mediciones de flujo espiratorio máximo (PEF) en serie. Algunos componentes de la evaluación clínica (p. ej., provocación bronquial específica o pruebas cuantitativas en serie para NBR) pueden no estar fácilmente disponibles para muchos médicos. Es posible que otros componentes simplemente no se puedan lograr (p. ej., el paciente ya no trabaja, los recursos de diagnóstico no están disponibles, las mediciones de PEF en serie son inadecuadas). Es probable que la precisión diagnóstica aumente con la minuciosidad de la evaluación clínica. En cada paciente individual, las decisiones sobre el alcance de la evaluación médica deberán equilibrar los costos de la evaluación con las consecuencias clínicas, sociales, financieras y de salud pública de diagnosticar o descartar incorrectamente la OA.
Teniendo en cuenta estas dificultades, en la tabla 2 se describe un enfoque escalonado para el diagnóstico de la OA. Esta pretende ser una guía general para facilitar una evaluación diagnóstica precisa, práctica y eficiente, reconociendo que algunos de los procedimientos sugeridos pueden no estar disponibles en algunos entornos. . El diagnóstico de OA implica establecer tanto el diagnóstico de asma como la relación entre el asma y las exposiciones en el lugar de trabajo. Después de cada paso, para cada paciente, el médico deberá determinar si el nivel de certeza diagnóstica alcanzado es adecuado para respaldar las decisiones necesarias, o si la evaluación debe continuar con el siguiente paso. Si las instalaciones y los recursos están disponibles, el tiempo y el costo de continuar con la evaluación clínica generalmente se justifican por la importancia de hacer una determinación precisa de la relación entre el asma y el trabajo. Se resumirán los aspectos más destacados de los procedimientos de diagnóstico para la OA; los detalles se pueden encontrar en varias de las referencias (Chan-Yeung 1995; Bernstein et al. 1993). Se puede considerar la consulta con un médico con experiencia en OA, ya que el proceso de diagnóstico puede ser difícil.
Tabla 2. Pasos en la evaluación diagnóstica del asma en el lugar de trabajo
Paso 1 Historia médica y ocupacional completa y examen físico dirigido.
Paso 2 Evaluación fisiológica de obstrucción reversible de las vías respiratorias y/o hiperreactividad bronquial inespecífica.
Paso 3 Valoración inmunológica, si procede.
Evaluar el estado del trabajo:
Trabajando actualmente: Continúe con el Paso 4 primero.
Actualmente no trabaja, prueba diagnóstica de regreso al trabajo factible: Paso 5 primero, luego Paso 4.
Actualmente no trabaja, prueba diagnóstica de regreso al trabajo no factible: Paso 6.
Paso 4 Evaluación clínica de asma en el trabajo o ensayo diagnóstico de reincorporación al trabajo.
Paso 5 Evaluación clínica de asma fuera del trabajo o prueba diagnóstica de retiro del trabajo.
Paso 6 Pruebas de desafío en el lugar de trabajo o de desafío bronquial específico. Si está disponible para exposiciones causales sospechosas, este paso se puede realizar antes del Paso 4 para cualquier paciente.
Esto pretende ser una guía general para facilitar una evaluación diagnóstica práctica y eficiente. Se recomienda que los médicos que diagnostican y manejan la OA también consulten la literatura clínica actual.
El RADS, cuando es causado por una exposición ocupacional, generalmente se considera una subclase de OA. Se diagnostica clínicamente, utilizando los criterios de la Tabla 6. Los pacientes que han experimentado una lesión respiratoria significativa debido a inhalaciones de irritantes de alto nivel deben ser evaluados para detectar síntomas persistentes y presencia de obstrucción del flujo de aire poco después del evento. Si la historia clínica es compatible con RADS, la evaluación adicional debe incluir pruebas cuantitativas para NBR, si no está contraindicado.
WAA puede ser común y puede causar una carga prevenible sustancial de discapacidad, pero se ha publicado poco sobre el diagnóstico, el tratamiento o el pronóstico. Como se resume en la Tabla 6, la WAA se reconoce cuando los síntomas asmáticos precedieron a la exposición causal sospechada pero se agravan claramente por el entorno laboral. El empeoramiento en el trabajo se puede documentar mediante evidencia fisiológica o mediante la evaluación de registros médicos y el uso de medicamentos. Es un juicio clínico si los pacientes con antecedentes de asma en remisión, que tienen recurrencia de síntomas asmáticos que de otro modo cumplen los criterios para OA, son diagnosticados con OA o WAA. Se ha propuesto un año como un período asintomático lo suficientemente largo como para que la aparición de los síntomas represente un nuevo proceso causado por la exposición en el lugar de trabajo, aunque todavía no existe consenso.
Paso 1: Historial médico y ocupacional completo y examen físico dirigido
La sospecha inicial de una posible OA en situaciones clínicas y laborales adecuadas es clave, dada la importancia del diagnóstico y la intervención precoz para mejorar el pronóstico. El diagnóstico de OA o WAA se debe considerar en todos los pacientes asmáticos en quienes los síntomas se desarrollaron como un adulto trabajador (especialmente de inicio reciente), o en quienes la gravedad del asma ha aumentado sustancialmente. La OA también debe considerarse en cualquier otra persona que tenga síntomas parecidos al asma y trabaje en ocupaciones en las que esté expuesta a agentes causantes del asma o que esté preocupada de que sus síntomas estén relacionados con el trabajo.
Se debe pedir a los pacientes con posible OA que proporcionen un historial médico y ocupacional/ambiental completo, con una documentación detallada de la naturaleza y la fecha de aparición de los síntomas y el diagnóstico de asma, y cualquier exposición potencialmente causal en ese momento. Debe evaluarse la compatibilidad de la historia clínica con la presentación clínica de la OA descrita anteriormente, especialmente el patrón temporal de los síntomas en relación con el horario de trabajo y los cambios en las exposiciones laborales. Se deben anotar los patrones y cambios en los patrones de uso de medicamentos para el asma, y el período mínimo de tiempo fuera del trabajo requerido para mejorar los síntomas. Son pertinentes las enfermedades respiratorias previas, las alergias/atopia, el tabaquismo y otras exposiciones tóxicas, y antecedentes familiares de alergia.
Las exposiciones ocupacionales y otras exposiciones ambientales a agentes o procesos potenciales que causan asma deben explorarse a fondo, con documentación objetiva de las exposiciones si es posible. Las exposiciones sospechosas deben compararse con una lista completa de agentes que causan OA (Harber, Schenker y Balmes 1996; Chan-Yeung y Malo 1994; Bernstein et al. 1993; Rom 1992b), aunque la incapacidad para identificar agentes específicos no es infrecuente y también es posible la inducción del asma por agentes no descritos previamente. En la tabla 3 se muestran algunos ejemplos ilustrativos. El historial ocupacional debe incluir detalles del empleo actual y anterior relevante con fechas, títulos de trabajo, tareas y exposiciones, especialmente el trabajo actual y el trabajo realizado en el momento del inicio de los síntomas. Otros antecedentes ambientales deben incluir una revisión de las exposiciones en el hogar o la comunidad que podrían causar asma. Es útil comenzar el historial de exposición de manera abierta, preguntando sobre categorías amplias de agentes transportados por el aire: polvos (especialmente polvos orgánicos de origen animal, vegetal o microbiano), productos químicos, productos farmacéuticos y gases o vapores irritantes o visibles. El paciente puede identificar agentes específicos, procesos de trabajo o categorías genéricas de agentes que han desencadenado síntomas. Pedir al paciente que describa paso a paso las actividades y exposiciones involucradas en el día de trabajo sintomático más reciente puede proporcionar pistas útiles. Los materiales utilizados por los compañeros de trabajo, o aquellos liberados en alta concentración por un derrame u otra fuente, pueden ser relevantes. A menudo se puede obtener más información sobre el nombre del producto, los ingredientes y el nombre del fabricante, la dirección y el número de teléfono. Los agentes específicos se pueden identificar llamando al fabricante oa través de una variedad de otras fuentes, incluidos libros de texto, bases de datos de CD ROM o centros de control de intoxicaciones. Dado que la OA suele ser causada por niveles bajos de alérgenos en el aire, las inspecciones de higiene industrial en el lugar de trabajo que evalúan cualitativamente las exposiciones y las medidas de control suelen ser más útiles que la medición cuantitativa de los contaminantes del aire.
Tabla 3. Agentes sensibilizantes que pueden causar asma ocupacional
|
Clasificación |
Subgrupos |
Ejemplos de sustancias |
Ejemplos de trabajos e industrias |
|
Antígenos proteicos de alto peso molecular |
Sustancias de origen animal Sustancias de origen vegetal |
Animales de laboratorio, cangrejos/mariscos, ácaros, insectos Polvos de harina y cereales, guantes de látex de caucho natural, enzimas bacterianas, polvo de ricino, gomas vegetales |
Cuidadores de animales, agricultura y procesamiento de alimentos. Panaderías, trabajadores de la salud, fabricación de detergentes, procesamiento de alimentos |
|
Bajo peso molecular/químico |
Plastificantes, pinturas bicomponentes, adhesivos, espumas Metales Polvos de madera Productos farmacéuticos, drogas |
Isocianatos, anhídridos de ácido, aminas Sales de platino, cobalto Cedro (ácido plicatico), roble psilio, antibióticos |
Auto pintura en aerosol, barnizado, carpintería Refinerías de platino, molienda de metales Trabajos de aserradero, carpintería Fabricación y envasado de productos farmacéuticos |
|
Otros productos químicos |
Cloramina T, vapores de cloruro de polivinilo, insecticidas organofosforados |
Trabajo de limpieza, envasado de carne |
La historia clínica parece ser mejor para excluir que para confirmar el diagnóstico de OA, y una historia abierta tomada por un médico es mejor que un cuestionario cerrado. Un estudio comparó los resultados de una historia clínica abierta tomada por especialistas capacitados en OA con un "estándar de oro" de prueba de provocación bronquial específica en 162 pacientes remitidos para evaluación de una posible OA. Los investigadores informaron que la sensibilidad de una historia clínica sugestiva de OA fue del 87 %, la especificidad del 55 %, el valor predictivo positivo del 63 % y el valor predictivo negativo del 83 %. En este grupo de pacientes derivados, la prevalencia de asma y OA fue del 80% y 46%, respectivamente (Malo et al. 1991). En otros grupos de pacientes derivados, los valores predictivos positivos de un cuestionario cerrado oscilaron entre el 8 y el 52 % para una variedad de exposiciones en el lugar de trabajo (Bernstein et al. 1993). El médico debe evaluar la aplicabilidad de estos resultados a otros entornos.
El examen físico a veces es útil y deben anotarse los hallazgos relevantes para el asma (p. ej., sibilancias, pólipos nasales, dermatitis eccematosa), irritación respiratoria o alergia (p. ej., rinitis, conjuntivitis) u otras posibles causas de los síntomas.
Paso 2: Evaluación fisiológica para obstrucción reversible de las vías respiratorias y/o hiperreactividad bronquial inespecífica
Si ya hay suficientes pruebas fisiológicas que respaldan el diagnóstico de asma (NAEP 1991) en la historia clínica, se puede omitir el Paso 2. De lo contrario, se debe realizar una espirometría dirigida por un técnico, preferiblemente después del turno de trabajo en un día en que el paciente experimente síntomas asmáticos. Si la espirometría revela una obstrucción de la vía aérea que se revierte con un broncodilatador, esto confirma el diagnóstico de asma. En pacientes sin evidencia clara de limitación del flujo de aire en la espirometría, se deben realizar pruebas cuantitativas de NBR con metacolina o histamina, el mismo día si es posible. La prueba cuantitativa de NBR en esta situación es un procedimiento clave por dos razones. En primer lugar, a menudo puede identificar a los pacientes con OA leve o en etapa temprana que tienen el mayor potencial de curación pero que no se verían si se detuvieran las pruebas con una espirometría normal. En segundo lugar, si la NBR es normal en un trabajador que tiene una exposición continua en el entorno laboral asociada con los síntomas, por lo general se puede descartar la OA sin más pruebas. Si es anormal, la evaluación puede continuar con el Paso 3 o 4, y el grado de NBR puede ser útil para controlar la mejoría del paciente después de la prueba de diagnóstico de eliminación de la exposición causal sospechosa (Paso 5). Si la espirometría revela una limitación significativa del flujo de aire que no mejora después del broncodilatador inhalado, se debe considerar una reevaluación después de un tratamiento más prolongado, incluidos los corticosteroides (ATS 1995; NAEP 1991).
Paso 3: Evaluación inmunológica, si corresponde
Las pruebas cutáneas o serológicas (p. ej., RAST) pueden demostrar sensibilización inmunológica a un agente específico del lugar de trabajo. Estas pruebas inmunológicas se han utilizado para confirmar la relación laboral del asma y, en algunos casos, eliminar la necesidad de pruebas específicas de provocación por inhalación. Por ejemplo, entre los pacientes expuestos a psyllium con un historial clínico compatible con OA, asma documentada o hiperreactividad de las vías respiratorias, y evidencia de sensibilización inmunológica al psyllium, aproximadamente el 80% tenía OA confirmada en pruebas de provocación bronquial específicas posteriores (Malo et al. 1990). ). En la mayoría de los casos, la importancia diagnóstica de las pruebas inmunológicas negativas es menos clara. La sensibilidad diagnóstica de las pruebas inmunológicas depende en gran medida de si se han incluido en la prueba todos los antígenos causales probables en el lugar de trabajo o los complejos hapteno-proteína. Aunque la implicación de la sensibilización para un trabajador asintomático no está bien definida, el análisis de resultados agrupados puede ser útil para evaluar los controles ambientales. La utilidad de la evaluación inmunológica es mayor para los agentes para los que existen normas estandarizadas. in vitro pruebas o reactivos de punción cutánea, como sales de platino y enzimas detergentes. Desafortunadamente, la mayoría de los alérgenos ocupacionales de interés actualmente no están disponibles comercialmente. El uso de soluciones no comerciales en las pruebas de punción cutánea se ha asociado en ocasiones con reacciones graves, incluida la anafilaxia, por lo que es necesario tener precaución.
Si los resultados de los Pasos 1 y 2 son compatibles con OA, se debe realizar una evaluación adicional si es posible. El orden y el alcance de la evaluación adicional dependen de la disponibilidad de recursos de diagnóstico, el estado laboral del paciente y la viabilidad de los ensayos de diagnóstico de retiro y regreso al trabajo como se indica en la Tabla 7. Si no es posible una evaluación adicional, el diagnóstico debe basarse en la información disponible en este momento.
Paso 4: Evaluación clínica del asma en el trabajo o prueba de diagnóstico de regreso al trabajo
A menudo, la prueba fisiológica de obstrucción de las vías respiratorias más fácilmente disponible es la espirometría. Para mejorar la reproducibilidad, la espirometría debe ser dirigida por un técnico capacitado. Desafortunadamente, la espirometría de un solo día entre turnos, realizada antes y después del turno de trabajo, no es sensible ni específica para determinar la obstrucción de las vías respiratorias asociada al trabajo. Es probable que si se realizan múltiples espirometrías cada día durante y después de varios días de trabajo, se pueda mejorar la precisión diagnóstica, pero esto aún no se ha evaluado adecuadamente.
Debido a las dificultades con la espirometría de turnos cruzados, la medición del PEF en serie se ha convertido en una técnica de diagnóstico importante para la OA. Usando un medidor portátil de bajo costo, las mediciones de PEF se registran cada dos horas, durante las horas de vigilia. Para mejorar la sensibilidad, las mediciones deben realizarse durante un período en el que el trabajador esté expuesto a los presuntos agentes causales en el trabajo y experimente un patrón de síntomas relacionados con el trabajo. Se realizan tres repeticiones en cada momento y las mediciones se realizan todos los días en el trabajo y fuera del trabajo. Las mediciones deben continuarse durante al menos 16 días consecutivos (p. ej., dos semanas laborales de cinco días y 3 fines de semana libres) si el paciente puede tolerar con seguridad continuar trabajando. Las mediciones del PEF se registran en un diario junto con la anotación de las horas de trabajo, los síntomas, el uso de medicamentos broncodilatadores y las exposiciones significativas. Para facilitar la interpretación, los resultados del diario deben representarse gráficamente. Ciertos patrones sugieren OA, pero ninguno es patognomónico, y la interpretación por parte de un lector experimentado suele ser útil. Las ventajas de las pruebas de PEF en serie son el bajo costo y la correlación razonable con los resultados de las pruebas de provocación bronquial. Las desventajas incluyen el grado significativo de cooperación del paciente requerido, la incapacidad de confirmar definitivamente que los datos son precisos, la falta de un método estandarizado de interpretación y la necesidad de que algunos pacientes se tomen 1 o 2 semanas consecutivas de baja para mostrar una mejoría significativa. Los espirómetros de registro electrónico portátiles diseñados para el autocontrol del paciente, cuando están disponibles, pueden abordar algunas de las desventajas del PEF en serie.
Los medicamentos para el asma tienden a reducir el efecto de las exposiciones laborales en las medidas del flujo de aire. Sin embargo, no es aconsejable suspender los medicamentos durante la monitorización del flujo de aire en el trabajo. Más bien, se debe mantener al paciente con una dosis segura mínima constante de medicamentos antiinflamatorios durante todo el proceso de diagnóstico, con un control estricto de los síntomas y el flujo de aire, y se debe anotar en el diario el uso de broncodilatadores de acción corta para controlar los síntomas.
El hecho de que no se observen cambios en el PEF relacionados con el trabajo mientras un paciente trabaja en horas de rutina no excluye el diagnóstico de OA, ya que muchos pacientes requerirán más de dos días de fin de semana para mostrar una mejoría significativa en el PEF. En este caso, se debe considerar una prueba de diagnóstico de retiro prolongado del trabajo (Paso 5). Si el paciente aún no se ha realizado una prueba cuantitativa de NBR y no tiene una contraindicación médica, se debe realizar en este momento, inmediatamente después de al menos dos semanas de exposición en el lugar de trabajo.
Paso 5: Evaluación clínica del asma fuera del trabajo o prueba de diagnóstico de suspensión prolongada del trabajo
Este paso consiste en completar el diario serial PEF de 2 horas diarias durante al menos 9 días consecutivos fuera del trabajo (p. ej., 5 días libres más los fines de semana antes y después). Si este registro, comparado con el diario serial de FEM en el trabajo, no es suficiente para diagnosticar OA, debe continuarse por una segunda semana consecutiva fuera del trabajo. Después de 2 o más semanas fuera del trabajo, se pueden realizar pruebas cuantitativas para NBR y compararlas con NBR mientras se está en el trabajo. Si aún no se ha realizado el PEF en serie durante al menos dos semanas en el trabajo, entonces se puede realizar una prueba de diagnóstico de regreso al trabajo (ver Paso 4), después de un asesoramiento detallado y en estrecho contacto con el médico tratante. El paso 5 suele ser de vital importancia para confirmar o excluir el diagnóstico de OA, aunque también puede ser el paso más difícil y costoso. Si se intenta una suspensión prolongada del trabajo, es mejor maximizar el rendimiento y la eficiencia del diagnóstico al incluir PEF, FEV1, y pruebas NBR en una evaluación completa. Las visitas semanales al médico para asesoramiento y para revisar el gráfico de PEF pueden ayudar a asegurar resultados completos y precisos. Si, después de monitorear al paciente durante al menos dos semanas en el trabajo y dos semanas fuera de él, la evidencia diagnóstica aún no es suficiente, se debe considerar el Paso 6 a continuación, si está disponible y es factible.
Paso 6: prueba de provocación bronquial específica o provocación en el lugar de trabajo
La prueba de provocación bronquial específica que usa una cámara de exposición y niveles de exposición estandarizados ha sido etiquetada como el "estándar de oro" para el diagnóstico de OA. Las ventajas incluyen la confirmación definitiva de la OA con la capacidad de identificar la respuesta asmática a niveles subirritantes de agentes sensibilizantes específicos, que luego pueden evitarse escrupulosamente. De todos los métodos de diagnóstico, es el único que puede distinguir de forma fiable el asma inducida por sensibilizantes de la provocada por irritantes. Varios problemas con este enfoque han incluido el costo inherente del procedimiento, el requisito general de observación estrecha u hospitalización durante varios días y la disponibilidad en muy pocos centros especializados. Pueden producirse falsos negativos si no se dispone de una metodología estandarizada para todos los agentes sospechosos, si se sospecha de los agentes equivocados o si ha transcurrido demasiado tiempo entre la última exposición y la prueba. Pueden producirse falsos positivos si se obtienen niveles irritantes de exposición sin darse cuenta. Por estas razones, la prueba de provocación bronquial específica para OA sigue siendo un procedimiento de investigación en la mayoría de las localidades.
Las pruebas de provocación en el lugar de trabajo implican una espirometría en serie dirigida por un técnico en el lugar de trabajo, realizada a intervalos frecuentes (por ejemplo, cada hora) antes y durante el transcurso de una jornada laboral de exposición a los agentes o procesos causales sospechosos. Puede ser más sensible que la prueba de provocación bronquial específica porque involucra exposiciones de la “vida real”, pero dado que la obstrucción de las vías respiratorias puede ser provocada por irritantes y agentes sensibilizantes, las pruebas positivas no necesariamente indican sensibilización. También requiere la cooperación del empleador y mucho tiempo técnico con un espirómetro móvil. Ambos procedimientos conllevan cierto riesgo de precipitar un ataque asmático grave y, por lo tanto, deben realizarse bajo la estrecha supervisión de especialistas con experiencia en los procedimientos.
Tratamiento y Prevención
El manejo de la OA incluye intervenciones médicas y preventivas para pacientes individuales, así como medidas de salud pública en los lugares de trabajo identificados como de alto riesgo de OA. El manejo médico es similar al del asma no ocupacional y está bien revisado en otro lugar (NAEP 1991). El manejo médico por sí solo rara vez es adecuado para controlar de manera óptima los síntomas, y la intervención preventiva mediante el control o el cese de la exposición es una parte integral del tratamiento. Este proceso comienza con un diagnóstico preciso y la identificación de las exposiciones y condiciones causales. En la OA inducida por sensibilizadores, la reducción de la exposición al sensibilizador no suele dar lugar a una resolución completa de los síntomas. Los episodios asmáticos severos o el empeoramiento progresivo de la enfermedad pueden ser causados por exposiciones a concentraciones muy bajas del agente y se recomienda el cese completo y permanente de la exposición. La derivación oportuna para rehabilitación vocacional y capacitación laboral puede ser un componente necesario del tratamiento para algunos pacientes. Si es imposible el cese completo de la exposición, una opción puede ser una reducción sustancial de la exposición acompañada de un estrecho control y manejo médico, aunque dicha reducción de la exposición no siempre es factible y no se ha probado la seguridad a largo plazo de este enfoque. Como ejemplo, sería difícil justificar la toxicidad del tratamiento a largo plazo con corticosteroides sistémicos para permitir que el paciente continúe en el mismo empleo. Para el asma inducida y/o provocada por irritantes, la respuesta a la dosis puede ser más predecible, y la reducción de los niveles de exposición al irritante, acompañada de una estrecha vigilancia médica, puede ser menos riesgosa y más probable que sea eficaz que para la OA inducida por sensibilizantes. Si el paciente continúa trabajando en condiciones modificadas, el seguimiento médico debe incluir visitas frecuentes al médico con revisión del diario de PEF, acceso bien planificado a los servicios de emergencia y espirometría en serie y/o pruebas de provocación con metacolina, según corresponda.
Una vez que se sospecha que un lugar de trabajo en particular es de alto riesgo, ya sea debido a la ocurrencia de un caso centinela de OA o al uso de agentes causantes de asma conocidos, los métodos de salud pública pueden ser muy útiles. El reconocimiento temprano y el tratamiento y la prevención efectivos de la discapacidad de los trabajadores con OA existente, y la prevención de nuevos casos, son prioridades claras. Es importante identificar los agentes causales específicos y los procesos de trabajo. Un enfoque inicial práctico es una encuesta de cuestionario en el lugar de trabajo, evaluando los criterios A, B, C y D1 o D5 en la definición de caso de OA. Este enfoque puede identificar a las personas para las que podría estar indicada una evaluación clínica adicional y ayudar a identificar posibles agentes o circunstancias causales. La evaluación de los resultados del grupo puede ayudar a decidir si es necesaria una mayor investigación o intervención en el lugar de trabajo y, de ser así, proporcionar una guía valiosa para orientar los futuros esfuerzos de prevención de la manera más eficaz y eficiente. Sin embargo, una encuesta de cuestionario no es adecuada para establecer diagnósticos médicos individuales, ya que los valores predictivos positivos de los cuestionarios para OA no son lo suficientemente altos. Si se necesita un mayor nivel de certeza diagnóstica, también se pueden considerar las pruebas de detección médica que utilizan procedimientos de diagnóstico como la espirometría, las pruebas cuantitativas para NBR, el registro serial de PEF y las pruebas inmunológicas. En lugares de trabajo con problemas conocidos, los programas continuos de vigilancia y detección pueden ser útiles. Sin embargo, la exclusión diferencial de trabajadores asintomáticos con antecedentes de atopia u otros posibles factores de susceptibilidad de los lugares de trabajo que se cree que son de alto riesgo daría lugar a la eliminación de un gran número de trabajadores para prevenir relativamente pocos casos de OA, y no está respaldada por la literatura actual.
El control o la eliminación de las exposiciones causales y la prevención y el manejo adecuado de derrames o episodios de exposiciones de alto nivel pueden conducir a una prevención primaria eficaz de la sensibilización y la OA en los compañeros de trabajo del caso centinela. La jerarquía habitual de control de exposición de sustitución, controles administrativos y de ingeniería y equipo de protección personal, así como la educación de los trabajadores y gerentes, deben implementarse según corresponda. Los empleadores proactivos iniciarán o participarán en algunos o en todos estos enfoques, pero en el caso de que se tomen medidas preventivas inadecuadas y los trabajadores permanezcan en alto riesgo, las agencias de aplicación gubernamentales pueden ser útiles.
Deficiencia y Discapacidad
Incapacidad médica es una anormalidad funcional que resulta de una condición médica. Discapacidad se refiere al efecto total de la discapacidad médica en la vida del paciente y está influenciado por muchos factores no médicos, como la edad y el nivel socioeconómico (ATS 1995).
La evaluación del deterioro médico la realiza el médico y puede incluir un índice de deterioro calculado, así como otras consideraciones clínicas. El índice de deterioro se basa en (1) el grado de limitación del flujo de aire después del broncodilatador, (2) el grado de reversibilidad de la limitación del flujo de aire con el broncodilatador o el grado de hiperreactividad de las vías respiratorias en las pruebas cuantitativas de NBR, y (3) la medicación mínima requerida para controlar asma. El otro componente principal de la evaluación de la discapacidad médica es el juicio médico del médico sobre la capacidad del paciente para trabajar en el entorno laboral que causa el asma. Por ejemplo, un paciente con OA inducida por un sensibilizador puede tener una discapacidad médica que es muy específica del agente al que se ha sensibilizado. El trabajador que experimenta síntomas solo cuando se expone a este agente puede trabajar en otros trabajos, pero permanentemente incapacitado para trabajar en el trabajo específico para el que tiene más capacitación y experiencia.
La evaluación de la discapacidad debida al asma (incluida la OA) requiere la consideración de la discapacidad médica, así como otros factores no médicos que afectan la capacidad para trabajar y funcionar en la vida cotidiana. La evaluación de la discapacidad la realiza inicialmente el médico, quien debe identificar todos los factores que afectan el impacto de la discapacidad en la vida del paciente. Muchos factores, como la ocupación, el nivel educativo, la posesión de otras habilidades comerciales, las condiciones económicas y otros factores sociales, pueden dar lugar a diferentes niveles de discapacidad en personas con el mismo nivel de discapacidad médica. Esta información luego puede ser utilizada por los administradores para determinar la discapacidad con fines de compensación.
El deterioro y la discapacidad pueden clasificarse como temporales o permanentes, según la probabilidad de una mejora significativa y si se implementan con éxito controles de exposición efectivos en el lugar de trabajo. Por ejemplo, un individuo con OA inducida por sensibilizadores generalmente se considera permanentemente, totalmente discapacitado para cualquier trabajo que implique exposición al agente causal. Si los síntomas se resuelven parcial o completamente después del cese de la exposición, estos individuos pueden clasificarse con menos o ningún impedimento para otros trabajos. A menudo, esto se considera un impedimento/discapacidad parcial permanente, pero la terminología puede variar. Se consideraría que una persona con asma desencadenada de manera dependiente de la dosis por irritantes en el lugar de trabajo tiene una discapacidad temporal mientras presenta síntomas, y una discapacidad menor o nula si se instalan controles de exposición adecuados y son efectivos para reducir o eliminar los síntomas. Si no se implementan controles de exposición efectivos, es posible que se deba considerar que el mismo individuo tiene una discapacidad permanente para trabajar en ese trabajo, con recomendación de remoción médica. Si es necesario, se puede realizar una evaluación repetida del deterioro/discapacidad a largo plazo dos años después de que se reduce o finaliza la exposición, cuando se espera que la mejora de la OA se haya estancado. Si el paciente continúa trabajando, el control médico debe ser continuo y la reevaluación del deterioro/discapacidad debe repetirse según sea necesario.
Los trabajadores que quedan discapacitados por OA o WAA pueden calificar para una compensación financiera por gastos médicos y/o salarios perdidos. Además de reducir directamente el impacto financiero de la discapacidad en los trabajadores individuales y sus familias, puede ser necesaria una compensación para brindar un tratamiento médico adecuado, iniciar una intervención preventiva y obtener rehabilitación vocacional. La comprensión del trabajador y del médico de cuestiones médicas y legales específicas puede ser importante para garantizar que la evaluación diagnóstica cumpla con los requisitos locales y no comprometa los derechos del trabajador afectado.
Aunque las discusiones sobre el ahorro de costos con frecuencia se enfocan en la insuficiencia de los sistemas de compensación, la reducción real de la carga financiera y de salud pública impuesta a la sociedad por OA y WAA dependerá no solo de las mejoras en los sistemas de compensación sino, lo que es más importante, de la efectividad de los sistemas implementados para identificar y rectificar, o prevenir por completo, las exposiciones en el lugar de trabajo que están provocando la aparición de nuevos casos de asma.
Conclusiones
La OA se ha convertido en la enfermedad respiratoria ocupacional más prevalente en muchos países. Es más común de lo que generalmente se reconoce, puede ser grave e incapacitante, y generalmente se puede prevenir. El reconocimiento temprano y las intervenciones preventivas efectivas pueden reducir sustancialmente el riesgo de discapacidad permanente y los altos costos humanos y financieros asociados con el asma crónica. Por muchas razones, OA merece una atención más amplia entre médicos, especialistas en salud y seguridad, investigadores, formuladores de políticas de salud, higienistas industriales y otras personas interesadas en la prevención de enfermedades relacionadas con el trabajo.
Más...
Enfermedades Causadas por Polvos Orgánicos
Polvo Orgánico y Enfermedad
Los polvos de origen vegetal, animal y microbiano siempre han formado parte del entorno humano. Cuando los primeros organismos acuáticos se trasladaron a la tierra hace unos 450 millones de años, pronto desarrollaron sistemas de defensa contra las numerosas sustancias nocivas presentes en el medio terrestre, la mayoría de ellas de origen vegetal. La exposición a este entorno no suele causar problemas específicos, aunque las plantas contienen una serie de sustancias extremadamente tóxicas, en particular las presentes en los mohos o producidas por ellos.
Durante el desarrollo de la civilización, las condiciones climáticas en algunas partes del mundo requerían que ciertas actividades se realizaran en interiores. La trilla en los países escandinavos se realizaba bajo techo durante el invierno, práctica mencionada por los cronistas en la antigüedad. El encierro de procesos polvorientos provocó enfermedades entre las personas expuestas, y uno de los primeros relatos publicados de esto es el del obispo danés Olaus Magnus (1555, citado por Rask-Andersen 1988). Describió una enfermedad entre las trilladoras en Escandinavia de la siguiente manera:
“Al separar el grano de la paja, se debe tener cuidado de elegir un momento en que haya un viento adecuado que arrastre el polvo del grano, para que no dañe los órganos vitales de las trilladoras. Este polvo es tan fino que casi imperceptiblemente penetrará en la boca y se acumulará en la garganta. Si esto no se soluciona rápidamente bebiendo cerveza fresca, el trillador no puede volver a comer nunca más o solo por un corto período de tiempo lo que ha trillado”.
Con la introducción del procesamiento mecánico de materiales orgánicos, el tratamiento de grandes cantidades de materiales en interiores con poca ventilación generó altos niveles de polvo en el aire. Las descripciones del obispo Olaus Magnus y luego de Ramazzini (1713) fueron seguidas por varios informes sobre enfermedades y polvos orgánicos en el siglo XIX, particularmente entre los trabajadores de las fábricas de algodón (Leach 1863; Prausnitz 1936). Posteriormente, también se describió la enfermedad pulmonar específica común entre los agricultores que manejan materiales mohosos (Campbell 1932).
Durante las últimas décadas se han publicado un gran número de informes sobre enfermedades entre personas expuestas a polvos orgánicos. Inicialmente, la mayoría de estos se basaron en personas que buscaban ayuda médica. Los nombres de las enfermedades, cuando se publicaban, a menudo se relacionaban con el entorno particular donde la enfermedad se reconoció por primera vez, y resultó en una desconcertante variedad de nombres, como pulmón del granjero, pulmón del cultivador de hongos, pulmón marrón y fiebre del humidificador.
Con el advenimiento de la epidemiología moderna, se obtuvieron cifras más confiables para la incidencia de enfermedades respiratorias ocupacionales relacionadas con el polvo orgánico (Rylander, Donham y Peterson 1986; Rylander y Peterson 1990). También hubo avances en la comprensión de los mecanismos patológicos subyacentes a estas enfermedades, en particular la respuesta inflamatoria (Henson y Murphy 1989). Esto allanó el camino para una imagen más coherente de las enfermedades causadas por los polvos orgánicos (Rylander y Jacobs 1997).
A continuación se describirán los diferentes ambientes de polvo orgánico donde se ha informado la enfermedad, las entidades de la enfermedad en sí mismas, la enfermedad de bisinosis clásica y las medidas preventivas específicas.
Entornos
Los polvos orgánicos son partículas suspendidas en el aire de origen vegetal, animal o microbiano. La Tabla 1 enumera ejemplos de entornos, procesos de trabajo y agentes que implican el riesgo de exposición a polvos orgánicos.
Tabla 1. Ejemplos de fuentes de peligros de exposición a polvo orgánico
Agricultura
Manipulación de cereales, heno u otros cultivos
Procesamiento de caña de azúcar
Invernaderos
Silos
Animales
Edificios de confinamiento porcino/lechero
Gallineros y plantas procesadoras
Animales de laboratorio, animales de granja y mascotas.
Tratamiento de residuos
Aguas residuales y limo
Basura doméstica
El compostaje
Industria
Procesamiento de fibra vegetal (algodón, lino, cáñamo, yute, sisal)
Fermentación
Procesamiento de madera y madera
Panaderías
Procesamiento biotecnológico
Edificios
Agua contaminada en humidificadores
Crecimiento microbiano en estructuras o en conductos de ventilación.
Agentes
Ahora se entiende que los agentes específicos en los polvos son la razón principal por la que se desarrolla la enfermedad. Los polvos orgánicos contienen multitud de agentes con potenciales efectos biológicos. Algunos de los principales agentes se encuentran en la tabla 2.
Tabla 2. Principales agentes en polvos orgánicos con actividad biológica potencial
Agentes vegetales
Taninos
La histamina
ácido plicatico
Alcaloides (p. ej., nicotina)
Citocalasinas
Agentes animales
Proteínas
Enzimas
Agentes microbianos
Endotoxinas
(1→3)–β–D-glucanos
Las proteasas
Micotoxinas
El papel relativo de cada uno de estos agentes, solos o en combinación con otros, para el desarrollo de la enfermedad, es mayormente desconocido. La mayor parte de la información disponible se refiere a las endotoxinas bacterianas que están presentes en todos los polvos orgánicos.
Las endotoxinas son compuestos de lipopolisacáridos que se adhieren a la superficie celular externa de las bacterias Gram-negativas. La endotoxina tiene una amplia variedad de propiedades biológicas. Después de la inhalación provoca una inflamación aguda (Snella y Rylander 1982; Brigham y Meyrick 1986). Una entrada de neutrófilos (leucocitos) en el pulmón y las vías respiratorias es el sello distintivo de esta reacción. Se acompaña de activación de otras células y secreción de mediadores inflamatorios. Después de exposiciones repetidas, la inflamación disminuye (adaptación). La reacción se limita a la mucosa de las vías respiratorias y no hay afectación extensa del parénquima pulmonar.
Otro agente específico del polvo orgánico es el (1→3)-β-D-glucano. Este es un compuesto de poliglucosa presente en la estructura de la pared celular de mohos y algunas bacterias. Mejora la respuesta inflamatoria causada por la endotoxina y altera la función de las células inflamatorias, en particular los macrófagos y las células T (Di Luzio 1985; Fogelmark et al. 1992).
Otros agentes específicos presentes en los polvos orgánicos son las proteínas, los taninos, las proteasas y otras enzimas, y las toxinas de los mohos. Se dispone de muy pocos datos sobre las concentraciones de estos agentes en polvos orgánicos. Varios de los agentes específicos de los polvos orgánicos, como las proteínas y las enzimas, son alérgenos.
Enfermedades
Las enfermedades causadas por polvos orgánicos se muestran en la tabla 3 con los números correspondientes de la Clasificación Internacional de Enfermedades (CIE) (Rylander y Jacobs 1994).
Tabla 3. Enfermedades inducidas por polvos orgánicos y sus códigos CIE
Bronquitis y neumonitis (ICD J40)
Neumonitis tóxica (fiebre por inhalación, síndrome tóxico por polvo orgánico)
Inflamación de las vías respiratorias (inflamación de la membrana mucosa)
Bronquitis crónica (ICD J42)
Neumonitis por hipersensibilidad (alveolitis alérgica) (ICD J67)
Asma (ICD J45)
Rinitis, conjuntivitis
La vía principal de exposición a los polvos orgánicos es la inhalación y, en consecuencia, los efectos sobre los pulmones han recibido la mayor parte de la atención tanto en la investigación como en el trabajo clínico. Sin embargo, existe un creciente cuerpo de evidencia de estudios epidemiológicos publicados e informes de casos, así como informes anecdóticos, de que también se producen efectos sistémicos. El mecanismo implicado parece ser una inflamación local en el sitio objetivo, el pulmón, y una posterior liberación de citocinas con efectos sistémicos (Dunn 1992; Michel et al. 1991) o un efecto sobre el epitelio del intestino (Axmacher et al. . 1991). Los efectos clínicos no respiratorios son fiebre, dolores articulares, efectos neurosensoriales, problemas de la piel, enfermedades intestinales, fatiga y dolor de cabeza.
Las diferentes entidades patológicas descritas en la tabla 3 son fáciles de diagnosticar en casos típicos y la patología subyacente es claramente diferente. Sin embargo, en la vida real, un trabajador que tiene una enfermedad debido a la exposición a polvo orgánico, a menudo presenta una mezcla de las diferentes entidades de la enfermedad. Una persona puede tener inflamación de las vías respiratorias durante varios años, desarrollar repentinamente asma y además tener síntomas de neumonitis tóxica durante una exposición particularmente intensa. Otra persona puede tener neumonitis por hipersensibilidad subclínica con linfocitosis en las vías respiratorias y desarrollar neumonitis tóxica durante una exposición particularmente fuerte.
Un buen ejemplo de la mezcla de entidades patológicas que pueden aparecer es la bisinosis. Esta enfermedad se describió por primera vez en las fábricas de algodón, pero las entidades individuales de la enfermedad también se encuentran en otros ambientes de polvo orgánico. A continuación se presenta una descripción general de la enfermedad.
Bisinosis
La enfermedad
La bisinosis se describió por primera vez en el siglo XIX, y Prausnitz (1800) proporcionó un informe clásico que incluía trabajo clínico y experimental. Describió los síntomas entre los trabajadores de las fábricas de algodón de la siguiente manera:
“Después de trabajar durante años sin ningún problema apreciable excepto un poco de tos, los trabajadores de las fábricas de algodón notan un repentino empeoramiento de la tos, que se vuelve seca y extremadamente irritante¼ Estos ataques generalmente ocurren los lunes¼ pero gradualmente los síntomas comienzan a extenderse durante los días siguientes de la semana; con el tiempo la diferencia desaparece y sufren continuamente”.
Las primeras investigaciones epidemiológicas se realizaron en Inglaterra en la década de 1950 (Schilling et al. 1955; Schilling 1956). El diagnóstico inicial se basó en la aparición de una opresión torácica típica los lunes por la mañana, diagnosticada mediante un cuestionario (Roach y Schilling 1960). Se desarrolló un esquema para clasificar la gravedad de la bisinosis según el tipo y la periodicidad de los síntomas (Mekky, Roach y Schilling 1967; Schilling et al. 1955). La duración de la exposición se utilizó como medida de la dosis y se relacionó con la gravedad de la respuesta. Basado en entrevistas clínicas de un gran número de trabajadores, este esquema de clasificación se modificó posteriormente para reflejar con mayor precisión los intervalos de tiempo para la disminución del FEVXNUMX.1 (Berry et al. 1973).
En un estudio, se encontró una diferencia en la prevalencia de bisinosis en fábricas que procesan diferentes tipos de algodón (Jones et al. 1979). Las hilanderías que usaban algodón de alta calidad para producir hilos más finos tenían una menor prevalencia de bisinosis que las hilanderías que producían hilos gruesos y usaban algodón de menor calidad. Así, además de la intensidad y la duración de la exposición, ambas variables relacionadas con la dosis, el tipo de polvo se convirtió en una variable importante para evaluar la exposición. Posteriormente se demostró que las diferencias en la respuesta de los trabajadores expuestos a algodones gruesos y medianos dependía no solo del tipo de algodón sino de otras variables que afectan la exposición, entre ellas: variables de procesamiento como la velocidad de cardado, variables ambientales como la humidificación y ventilación y variables de fabricación, como diferentes tratamientos de hilo (Berry et al. 1973).
El siguiente refinamiento de la relación entre la exposición al polvo de algodón y una respuesta (síntomas o medidas objetivas de la función pulmonar) fueron los estudios de los Estados Unidos, que compararon a quienes trabajaban con 100% algodón con trabajadores que usaban el mismo algodón pero en un Mezcla 50:50 con sintéticos y trabajadores sin exposición al algodón (Merchant et al. 1973). Los trabajadores expuestos al algodón 100 % tenían la mayor prevalencia de bisinosis independientemente del tabaquismo, uno de los factores de confusión de la exposición al polvo de algodón. Esta relación semicuantitativa entre la dosis y la respuesta al polvo de algodón se perfeccionó aún más en un grupo de trabajadores textiles estratificados por sexo, tabaquismo, área de trabajo y tipo de fábrica. Se observó una relación en cada una de estas categorías entre la concentración de polvo en los rangos inferiores de polvo y la prevalencia de bisinosis y/o el cambio en el volumen espiratorio forzado en un segundo (FEV1).
En investigaciones posteriores, la FEV1 La disminución durante el turno de trabajo se ha utilizado para evaluar los efectos de la exposición, y también es parte del Estándar de polvo de algodón de EE. UU.
La bisinosis se consideró durante mucho tiempo como una enfermedad peculiar con una mezcla de diferentes síntomas y sin conocimiento de la patología específica. Algunos autores sugirieron que se trataba de un asma ocupacional (Bouhuys 1976). Una reunión del grupo de trabajo en 1987 analizó la sintomatología y la patología de la enfermedad (Rylander et al. 1987). Se acordó que la enfermedad comprendía varias entidades clínicas, generalmente relacionadas con la exposición a polvos orgánicos.
Neumonitis tóxica puede aparecer la primera vez que un empleado trabaja en el molino, particularmente cuando trabaja en las secciones de apertura, soplado y cardado (Trice 1940). Aunque se desarrolla la habituación, los síntomas pueden reaparecer después de una exposición inusualmente fuerte más adelante.
Inflamación de las vías respiratorias es la enfermedad más extendida y se presenta en diferentes grados de severidad, desde una leve irritación en la nariz y las vías respiratorias hasta una tos seca severa y dificultad para respirar. La inflamación provoca la constricción de las vías respiratorias y un VEF reducido.1. La capacidad de respuesta de las vías respiratorias aumenta según se mide con una prueba de provocación con metacolina o histamina. Se ha discutido si la inflamación de las vías respiratorias debe aceptarse como una entidad patológica en sí misma o si representa simplemente un síntoma. Dado que los hallazgos clínicos en términos de tos severa con estrechamiento de las vías respiratorias pueden conducir a una disminución de la capacidad laboral, se justifica considerarla como una enfermedad profesional.
La inflamación continua de las vías respiratorias durante varios años puede convertirse en bronquitis crónica, particularmente entre los trabajadores muy expuestos en las áreas de soplado y cardado. El cuadro clínico sería el de enfermedad pulmonar obstructiva crónica (EPOC).
Asma ocupacional se desarrolla en un pequeño porcentaje de la población activa, pero no suele diagnosticarse en estudios transversales ya que los trabajadores se ven obligados a dejar el trabajo a causa de la enfermedad. Neumonitis por hipersensibilidad no se ha detectado en ninguno de los estudios epidemiológicos realizados, ni ha habido informes de casos relacionados con la exposición al polvo de algodón. La ausencia de neumonitis por hipersensibilidad puede deberse a la cantidad relativamente baja de moho en el algodón, ya que el algodón mohoso no es aceptable para el procesamiento.
Un sentimiento subjetivo de opresión en el pecho, más común los lunes, es el síntoma clásico de la exposición al polvo de algodón (Schilling et al. 1955). Sin embargo, no es una característica exclusiva de la exposición al polvo de algodón, ya que también aparece entre las personas que trabajan con otros tipos de polvos orgánicos (Donham et al. 1989). La opresión en el pecho se desarrolla lentamente a lo largo de varios años, pero también se puede inducir en personas no expuestas previamente, siempre que el nivel de dosis sea alto (Haglind y Rylander 1984). La presencia de opresión torácica no está directamente relacionada con una disminución del FEVXNUMX1.
La patología detrás de la opresión en el pecho no ha sido explicada. Se ha sugerido que los síntomas se deben a una mayor adhesividad de las plaquetas que se acumulan en los capilares pulmonares y aumentan la presión de la arteria pulmonar. Es probable que la opresión en el pecho implique algún tipo de sensibilización celular, ya que se requieren exposiciones repetidas para que se desarrolle el síntoma. Esta hipótesis está respaldada por los resultados de estudios sobre monocitos sanguíneos de trabajadores del algodón (Beijer et al. 1990). Se encontró una mayor capacidad para producir factor procoagulante, indicativo de sensibilización celular, entre los trabajadores del algodón en comparación con los controles.
El entorno
La enfermedad se describió originalmente entre los trabajadores de las fábricas de algodón, lino y cáñamo blando. En la primera fase del tratamiento del algodón dentro de las fábricas (apertura de balas, soplado y cardado), más de la mitad de los trabajadores pueden tener síntomas de opresión en el pecho e inflamación de las vías respiratorias. La incidencia disminuye a medida que se procesa el algodón, reflejando la limpieza sucesiva del agente causal de la fibra. La bisinosis se ha descrito en todos los países donde se han realizado investigaciones en fábricas de algodón. Sin embargo, algunos países como Australia tienen cifras de incidencia inusualmente bajas (Gun et al. 1983).
Ahora existe evidencia uniforme de que las endotoxinas bacterianas son el agente causante de la neumonitis tóxica y la inflamación de las vías respiratorias (Castellan et al. 1987; Pernis et al. 1961; Rylander, Haglind y Lundholm 1985; Rylander y Haglind 1986; Herbert et al. 1992; Sigsgaard et al. 1992). Se han descrito relaciones dosis-respuesta y los síntomas típicos han sido inducidos por inhalación de endotoxina purificada (Rylander et al. 1989; Michel et al. 1995). Aunque esto no excluye la posibilidad de que otros agentes puedan contribuir a la patogenia, las endotoxinas pueden servir como marcadores del riesgo de enfermedad. Es poco probable que las endotoxinas estén relacionadas con el desarrollo del asma ocupacional, pero podrían actuar como un adyuvante de los posibles alérgenos del polvo de algodón.
El caso
El diagnóstico de bisinosis se realiza clásicamente mediante cuestionarios con la pregunta específica "¿Siente opresión en el pecho y, de ser así, en qué día de la semana?". Las personas con opresión torácica los lunes por la mañana se clasifican como bisinóticas según un esquema sugerido por Schilling (1956). Se puede realizar una espirometría, y, según las diferentes combinaciones de opresión torácica y disminución del FEVXNUMX1, el esquema de diagnóstico ilustrado en la tabla 4 ha evolucionado.
Tabla 4. Criterios diagnósticos de bisinosis
Grado ½. Opresión en el pecho el primer día de algunas semanas laborales
Grado 1. Opresión en el pecho el primer día de cada semana laboral
Grado 2. Opresión en el pecho el primer y otros días de la semana laboral
Grado 3. Síntomas de grado 2 acompañados de evidencia de incapacidad permanente en forma de intolerancia al esfuerzo disminuido y/o capacidad ventilatoria reducida
Tratamiento
El tratamiento en las etapas leves de la bisinosis es sintomático, y la mayoría de los trabajadores aprenden a vivir con la leve opresión torácica y la broncoconstricción que experimentan los lunes o cuando limpian maquinaria o realizan tareas similares con una exposición superior a la normal. Las etapas más avanzadas de inflamación de las vías respiratorias o la opresión torácica regular varios días de la semana requieren la transferencia a operaciones menos polvorientas. La presencia de asma ocupacional requiere mayoritariamente un cambio de trabajo.
Prevención
La prevención en general se trata en detalle en otra parte del Enciclopedia. Los principios básicos para la prevención en términos de sustitución de productos, limitación de la exposición, protección de los trabajadores y detección de enfermedades se aplican también a la exposición al polvo de algodón.
En cuanto a los productos sustitutos, se ha sugerido utilizar algodón con un bajo nivel de contaminación bacteriana. Una prueba inversa de este concepto se encuentra en informes de 1863 donde el cambio a algodón sucio provocó un aumento en la prevalencia de síntomas entre los trabajadores expuestos (Leach 1863). También existe la posibilidad de cambiar a otras fibras, especialmente fibras sintéticas, aunque esto no siempre es factible desde el punto de vista del producto. Actualmente no existe ninguna técnica aplicada a la producción para disminuir el contenido de endotoxinas de las fibras de algodón.
Con respecto a la reducción del polvo, se han implementado programas exitosos en los Estados Unidos y en otros lugares (Jacobs 1987). Dichos programas son costosos y los costos de una eliminación de polvo altamente eficiente pueden ser prohibitivos para los países en desarrollo (Corn 1987).
En cuanto al control de la exposición, el nivel de polvo no es una medida suficientemente precisa del riesgo de exposición. Según el grado de contaminación con bacterias gramnegativas y, por lo tanto, con endotoxinas, un determinado nivel de polvo puede o no estar asociado con un riesgo. Para las endotoxinas, no se han establecido pautas oficiales. Se ha sugerido que un nivel de 200 ng/m3 es el umbral para la neumonitis tóxica, 100 a 200 ng/m3 para la constricción aguda de las vías respiratorias durante el turno de trabajo y 10 ng/m3 para la inflamación de las vías respiratorias (Rylander y Jacobs 1997).
El conocimiento sobre los factores de riesgo y las consecuencias de la exposición son importantes para la prevención. La base de información se ha expandido rápidamente durante los últimos años, pero gran parte de ella aún no está presente en los libros de texto u otras fuentes de fácil acceso. Otro problema es que los síntomas y hallazgos en enfermedades respiratorias inducidas por polvo orgánico son inespecíficos y ocurren normalmente en la población. Por lo tanto, es posible que no se diagnostiquen correctamente en las primeras etapas.
La difusión adecuada de los conocimientos sobre los efectos del algodón y otros polvos orgánicos requiere el establecimiento de programas de formación apropiados. Estos deben estar dirigidos no solo a los trabajadores con exposición potencial, sino también a los empleadores y al personal de salud, en particular, a los ingenieros e inspectores de salud ocupacional. La información debe incluir la identificación de la fuente, los síntomas y la descripción de la enfermedad, y los métodos de protección. Un trabajador informado puede reconocer más fácilmente los síntomas relacionados con el trabajo y comunicarse de manera más efectiva con un proveedor de atención médica. En cuanto a la vigilancia y el cribado de la salud, los cuestionarios son un instrumento importante a utilizar. Varias versiones de cuestionarios diseñados específicamente para diagnosticar enfermedades inducidas por polvo orgánico han sido reportadas en la literatura (Rylander, Peterson y Donham 1990; Schwartz et al. 1995). Las pruebas de función pulmonar también son una herramienta útil para la vigilancia y el diagnóstico. Se ha encontrado que las mediciones de la capacidad de respuesta de las vías respiratorias son útiles (Rylander y Bergström 1993; Carvalheiro et al. 1995). Otras herramientas de diagnóstico, como las mediciones de mediadores inflamatorios o la actividad celular, aún se encuentran en fase de investigación.
Enfermedad del berilio
La enfermedad del berilio es un trastorno sistémico que involucra múltiples órganos, siendo las manifestaciones pulmonares las más prominentes y comunes. Ocurre por exposición al berilio en su forma de aleación o en uno de sus diversos compuestos químicos. La vía de exposición es por inhalación y la enfermedad puede ser aguda o crónica. La enfermedad aguda es extremadamente rara en la actualidad, y no se ha informado ninguna desde el primer uso industrial generalizado del berilio en la década de 1940 después de que se implementaron medidas de higiene industrial para limitar las exposiciones a dosis altas. La enfermedad crónica por berilio continúa siendo reportada.
Berilio, Aleaciones y Compuestos
El berilio, una sustancia industrial sospechosa de tener potencial cancerígeno, destaca por su ligereza, alta resistencia a la tracción y resistencia a la corrosión. La Tabla 1 describe las propiedades del berilio y sus compuestos.
Tabla 1. Propiedades del berilio y sus compuestos
|
Fórmula |
Ciertas |
Punto de fusión/ebullición (ºC) |
Solubilidad |
Descripción |
|
|
Berilio (Be) |
9.01 (aw) |
1.85 |
1,298 ± 5 / 2,970 |
- |
Gris a metal plateado |
|
Óxido de berilio (BeO) |
25 |
3.02 |
2,530±30/— |
Soluble en ácidos y álcalis; insoluble en agua |
Polvo blanco amorfo |
|
Fluoruro de berilio1 (BeF2 ) |
47.02 |
1.99 |
Sublima 800 °C |
Fácilmente soluble en agua; escasamente soluble en alcohol etílico |
Sólido higroscópico |
|
Cloruro de berilio2 (BeCl2 ) |
79.9 |
1.90 |
405/520 |
Muy soluble en agua; soluble en alcohol etílico, benceno, éter etílico y disulfuro de carbono |
Cristales delicuescentes blancos o ligeramente amarillos. |
|
Nitrato de berilio3 (Ser (NO3 )2 · 3H2 O) |
187.08 |
1.56 |
60/142 |
Soluble en agua y alcohol etílico |
Cristales delicuescentes de color blanco a ligeramente amarillo. |
|
Nitruro de berilio4 (Ser3 N2 ) |
55.06 |
- |
2,200±100/— |
- |
Cristales blancos duros y refractarios. |
|
sulfato de berilio |
177.2 |
1.71 |
100 / - |
Soluble en agua; insoluble en alcohol etílico |
Cristales incoloros |
1 El fluoruro de berilio se produce mediante la descompensación a 900–950 ºC de fluoruro de amonio y berilio. Su uso principal es en la producción de berilio metálico por reducción con magnesio.
2 El cloruro de berilio se fabrica pasando cloro sobre una mezcla de óxido de berilio y carbono.
3 El nitrato de berilio se produce por la acción del ácido nítrico sobre el óxido de berilio. Se utiliza como reactivo químico y como endurecedor del manto de gas.
4 El nitruro de berilio se prepara calentando polvo de metal de berilio en una atmósfera de nitrógeno libre de oxígeno a 700-1,400 ºC. Se utiliza en reacciones de energía atómica, incluida la producción del isótopo de carbono radiactivo carbono-14.
5 El hidrato de sulfato de berilio se produce mediante el tratamiento del mineral fritado con ácido sulfúrico concentrado. Se utiliza en la producción de berilio metálico mediante el proceso de sulfato.
Fuentes
Berilo (3BeO·Al2O3·6SiO2) es la principal fuente comercial de berilio, el más abundante de los minerales que contienen altas concentraciones de óxido de berilio (10 a 13%). Las principales fuentes de berilo se encuentran en Argentina, Brasil, India, Zimbabue y la República de Sudáfrica. En los Estados Unidos, el berilo se encuentra en Colorado, Dakota del Sur, Nuevo México y Utah. La bertrandita, un mineral de baja ley (0.1 a 3 %) con un contenido de berilio soluble en ácido, ahora se extrae y procesa en Utah.
Producción
Los dos métodos más importantes para extraer berilio del mineral son el proceso de sulfato y el proceso de fluoruro.
En el proceso de sulfato, el berilo triturado se funde en un horno de arco a 1,65 °C y se vierte a través de un chorro de agua a alta velocidad para formar una frita. Después del tratamiento térmico, la frita se muele en un molino de bolas y se mezcla con ácido sulfúrico concentrado para formar una suspensión, que se rocía en forma de chorro en un molino de sulfatación giratorio calentado directamente. El berilio, ahora en una forma soluble en agua, se lixivia del lodo y se agrega hidróxido de amonio al licor de lixiviación, que luego se alimenta a un cristalizador donde se cristaliza el alumbre de amonio. Se agregan agentes quelantes al licor para mantener el hierro y el níquel en solución, luego se agrega hidróxido de sodio y el berilato de sodio así formado se hidroliza para precipitar hidróxido de berilio. Este último producto se puede convertir en fluoruro de berilio para la reducción con magnesio a berilio metálico, o en cloruro de berilio para la reducción electrolítica.
En el proceso de fluoruro (figura 1), una mezcla en briquetas de mineral molido, silicofluoruro de sodio y carbonato de sodio se sinteriza en un horno de solera giratoria. El material sinterizado es triturado, molido y lixiviado. Se añade hidróxido de sodio a la solución de fluoruro de berilio así obtenida y el precipitado de hidróxido de berilio se filtra en un filtro rotatorio. El berilio metálico se obtiene como en el proceso anterior por reducción de magnesio del fluoruro de berilio o por electrólisis del cloruro de berilio.
Figura 1. Producción de óxido de berilio por el proceso de fluoruro
Usos
El berilio se usa en aleaciones con una serie de metales, incluidos acero, níquel, magnesio, zinc y aluminio, siendo la aleación más utilizada el berilio-cobre, propiamente llamado "bronce", que tiene una alta resistencia a la tracción y capacidad para ser endurecido. por tratamiento térmico. Los bronces de berilio se utilizan en herramientas que no producen chispas, piezas de interruptores eléctricos, resortes de relojes, diafragmas, cuñas, levas y bujes.
Uno de los mayores usos del metal es como moderador de neutrones térmicos en reactores nucleares y como reflector para reducir la fuga de neutrones del núcleo del reactor. A menudo se utiliza una fuente mixta de uranio y berilio como fuente de neutrones. Como lámina, el berilio se utiliza como material de ventana en los tubos de rayos X. Su ligereza, alto módulo elástico y estabilidad térmica lo convierten en un material atractivo para la industria aeronáutica y aeroespacial.
El óxido de berilio se obtiene calentando nitrato o hidróxido de berilio.
Se utiliza en la fabricación de cerámica, materiales refractarios y otros compuestos de berilio. Se utilizó para la fabricación de fósforos para lámparas fluorescentes hasta que la incidencia de la enfermedad del berilio en la industria hizo que se abandonara su uso con este fin (en 1949 en Estados Unidos).
Peligros
Los riesgos de incendio y para la salud están asociados con procesos que involucran berilio. El polvo de berilio finamente dividido arderá, siendo el grado de combustibilidad una función del tamaño de las partículas. Se han producido incendios en las unidades de filtración de polvo y durante la soldadura de los conductos de ventilación en los que había berilio finamente dividido.
El berilio y sus compuestos son sustancias altamente tóxicas. El berilio puede afectar a todos los sistemas de órganos, aunque el principal órgano afectado es el pulmón. El berilio causa enfermedad sistémica por inhalación y puede distribuirse ampliamente por todo el cuerpo después de la absorción de los pulmones. Poco berilio se absorbe del tracto gastrointestinal. El berilio puede causar irritación de la piel y su introducción traumática en el tejido subcutáneo puede causar irritación local y formación de granulomas.
Patogenesia
El berilio en todas sus formas, excepto el mineral de berilo, se ha asociado con enfermedades. La vía de entrada es por inhalación y en la enfermedad aguda se produce un efecto tóxico directo tanto en la mucosa nasofaríngea como en todo el árbol traqueobronquial, provocando edema e inflamación. En el pulmón provoca una neumonitis química aguda. La principal forma de toxicidad por berilio en este momento es la enfermedad crónica por berilio. Un tipo de hipersensibilidad retardada específica del berilio es la vía principal de la enfermedad crónica. La entrada de berilio en el sistema a través de los pulmones conduce a la proliferación de CD específicas+ linfocitos, con el berilio actuando como un antígeno específico, ya sea solo o como un hapteno a través de una vía de receptor de interleucina-2 (IL2). Por lo tanto, la susceptibilidad individual al berilio se puede explicar sobre la base de la CD individual.+ respuesta. La liberación de linfocinas de los linfocitos activados puede conducir a la formación de granulomas y al reclutamiento de macrófagos. El berilio se puede transportar a sitios fuera del pulmón donde puede causar la formación de granulomas. El berilio se libera lentamente desde diferentes sitios y se excreta por los riñones. Esta liberación lenta puede ocurrir en un lapso de 20 a 30 años. La cronicidad y latencia de la enfermedad probablemente se puede explicar sobre la base del fenómeno de liberación y metabolismo lento. Los mecanismos inmunitarios involucrados en la patogenia de la enfermedad por berilio también permiten enfoques específicos para el diagnóstico, que se analizarán a continuación.
Histopatología
El principal hallazgo patológico en la enfermedad por berilio es la formación de granulomas no caseificantes en los pulmones, ganglios linfáticos y en otros sitios. Los estudios histopatológicos de los pulmones en pacientes con enfermedad aguda por berilio han mostrado un patrón inespecífico de bronquitis y neumonitis aguda y subaguda. En la enfermedad crónica por berilio, hay diversos grados de infiltración linfocitaria del intersticio pulmonar y formación de granulomas no caseificantes (figura 2).
Figura 2. Tejido pulmonar en un paciente con enfermedad crónica por berilio
Tanto los granulomas como la infiltración de células redondas son visibles.
Muchos de los granulomas se localizan en las áreas peribronquiolares. Además, puede haber histiocitos, células plasmáticas y células gigantes con cuerpos de inclusión calcificados. Si se trata únicamente de formación de granulomas, el pronóstico a largo plazo es mejor. La histología del pulmón en la enfermedad crónica por berilio es indistinguible de la de la sarcoidosis. Los granulomas no caseificantes también se encuentran en los ganglios linfáticos, el hígado, el bazo, los músculos y la piel.
Manifestaciones clínicas
Lesiones cutáneas
Las sales ácidas de berilio causan dermatitis alérgica de contacto. Tales lesiones pueden ser eritematosas, papulares o papulovesiculares, son comúnmente pruriginosas y se encuentran en partes expuestas del cuerpo. Por lo general, hay un retraso de 2 semanas desde la primera exposición hasta la aparición de la dermatitis, excepto en el caso de exposiciones intensas, cuando una reacción irritante puede ser inmediata. Este retraso se considera como el tiempo necesario para desarrollar el estado de hipersensibilidad.
La implantación accidental de metal de berilio o cristales de un compuesto de berilio soluble en una abrasión, una fisura en la piel o debajo de la uña puede causar un área indurada con supuración central. Los granulomas también se pueden formar en dichos sitios.
La conjuntivitis y la dermatitis pueden ocurrir solas o juntas. En casos de conjuntivitis, el edema periorbitario puede ser severo.
Enfermedad aguda
La nasofaringitis por berilio se caracteriza por membranas mucosas inflamadas e hiperémicas, puntos sangrantes, fisuras y ulceración. Se ha descrito perforación del tabique nasal. La eliminación de la exposición da como resultado la reversión de este proceso inflamatorio dentro de 3 a 6 semanas.
La afectación de la tráquea y el árbol bronquial después de la exposición a niveles más altos de berilio provoca tos no productiva, dolor retroesternal y dificultad respiratoria moderada. Los roncus y/o los estertores pueden ser audibles, y la radiografía de tórax puede mostrar un aumento de las marcas broncovasculares. El carácter y la velocidad de aparición y la gravedad de estos signos y síntomas dependen de la calidad y cantidad de la exposición. Se espera una recuperación dentro de 1 a 4 semanas si se retira al trabajador de una mayor exposición.
El uso de esteroides es bastante útil para contrarrestar la enfermedad aguda. No se han notificado nuevos casos de enfermedad aguda al Registro de casos de berilio de EE. UU. en más de 30 años. El Registro, que fue iniciado por Harriet Hardy en 1952, tiene casi 1,000 registros de casos, entre los que se enumeran 212 casos agudos. Casi todos estos ocurrieron en la industria de fabricación de lámparas fluorescentes. Cuarenta y cuatro sujetos con la enfermedad aguda desarrollaron posteriormente una enfermedad crónica.
Enfermedad crónica por berilio
La enfermedad crónica por berilio es una enfermedad granulomatosa pulmonar y sistémica causada por la inhalación de berilio. La latencia de la enfermedad puede ser de 1 a 30 años, ocurriendo más comúnmente de 10 a 15 años después de la primera exposición. La enfermedad crónica por berilio tiene un curso variable con exacerbaciones y remisiones en sus manifestaciones clínicas. Sin embargo, la enfermedad suele ser progresiva. Ha habido algunos casos con anomalías en la radiografía de tórax con un curso clínico estable y sin síntomas significativos.
La disnea de esfuerzo es el síntoma más común de la enfermedad crónica por berilio. Otros síntomas son tos, fatiga, pérdida de peso, dolor torácico y artralgias. Los hallazgos físicos pueden ser completamente normales o pueden incluir crepitantes bibasales, linfadenopatía, lesiones cutáneas, hepatoesplenomegalia y acropaquias. Los signos de hipertensión pulmonar pueden estar presentes en la enfermedad grave y prolongada.
En algunos pacientes pueden ocurrir cálculos renales e hiperuricemia y ha habido informes raros de agrandamiento de la glándula parótida y compromiso del sistema nervioso central. Las manifestaciones clínicas de la enfermedad crónica por berilio son muy similares a las de la sarcoidosis.
Características radiológicas
El patrón de rayos X en la enfermedad crónica por berilio es inespecífico y es similar al que se puede observar en la sarcoidosis, la fibrosis pulmonar idiopática, la tuberculosis, las micosis y la enfermedad del polvo (figura 3). Al principio del curso de la enfermedad, las películas pueden mostrar densidades granulares, nodulares o lineales. Estas anormalidades pueden aumentar, disminuir o permanecer sin cambios, con o sin fibrosis. La afectación del lóbulo superior es común. La adenopatía hiliar, que se observa en aproximadamente un tercio de los pacientes, suele ser bilateral y se acompaña de manchas en los campos pulmonares. La ausencia de cambios pulmonares en presencia de adenopatías es una consideración diferencial relativa pero no absoluta a favor de la sarcoidosis frente a la enfermedad crónica por berilio. Se ha informado adenopatía hiliar unilateral, pero es bastante rara.
Figura 3. Radiografía de tórax de un paciente con enfermedad crónica por berilio, que muestra infiltrados fibronodulares difusos y hilio prominente.
La imagen de rayos X no se correlaciona bien con el estado clínico y no refleja aspectos cualitativos o cuantitativos particulares de la exposición causal.
Pruebas de función pulmonar.
Los datos del Registro de casos de berilio muestran que se pueden encontrar 3 patrones de deterioro en la enfermedad crónica por berilio. De 41 pacientes estudiados durante un período de un promedio de 23 años después de la exposición inicial al berilio, el 20 % tenía un defecto restrictivo, el 36 % tenía un defecto intersticial (volúmenes pulmonares y tasas de flujo de aire normales pero capacidad de difusión reducida para el monóxido de carbono), el 39 % tenían un defecto obstructivo y el 5% eran normales. El patrón obstructivo, que se presentó tanto en fumadores como en no fumadores, se asoció a granulomas en la región peribronquial. Este estudio indicó que el patrón de deterioro afecta el pronóstico. A los pacientes con defecto intersticial les fue mejor, con el menor deterioro en un intervalo de cinco años. Los pacientes con defectos obstructivos y restrictivos experimentaron un empeoramiento de su deterioro a pesar de la terapia con corticosteroides.
Los estudios de función pulmonar en trabajadores de extracción de berilio que estaban asintomáticos mostraron la presencia de hipoxemia arterial leve. Esto ocurrió generalmente dentro de los primeros 10 años de exposición. En trabajadores expuestos al berilio durante 20 años o más hubo una reducción de la capacidad vital forzada (FVC) y del volumen espiratorio forzado en un segundo (FEV1). Estos hallazgos sugieren que la hipoxemia leve inicial podría deberse a la alveolitis temprana y que, con una mayor exposición y el transcurso del tiempo, la reducción del VEFXNUMX1 y FVC podría representar fibrosis y formación de granulomas.
Otras pruebas de laboratorio
Se han informado pruebas de laboratorio anormales no específicas en la enfermedad crónica por berilio e incluyen velocidad de sedimentación elevada, eritrocitosis, niveles elevados de gammaglobulina, hiperuricemia e hipercalcemia.
La prueba cutánea de Kveim es negativa en la enfermedad por berilio, mientras que puede ser positiva en la sarcoidosis. El nivel de la enzima convertidora de angiotensina (ECA) suele ser normal en la enfermedad por berilio, pero puede aumentar en el 60 % o más de los pacientes con sarcoidosis activa.
Diagnóstico
El diagnóstico de la enfermedad crónica por berilio durante muchos años se basó en los criterios desarrollados a través del Registro de casos de berilio, que incluían:
- un historial de exposición significativa al berilio
- evidencia de enfermedad del tracto respiratorio inferior
- radiografía de tórax anormal con enfermedad fibronodular intersticial
- pruebas de función pulmonar anormales con disminución de la capacidad de difusión de monóxido de carbono (DLCO)
- cambios patológicos compatibles con la exposición al berilio en los ganglios linfáticos torácicos o pulmonares
- la presencia de berilio en el tejido.
Cuatro de los seis criterios tenían que cumplirse y deberían haber incluido (1) o (6). Desde la década de 1980, los avances en inmunología han hecho posible el diagnóstico de la enfermedad por berilio sin necesidad de muestras de tejido para el examen histológico o el análisis de berilio. La transformación de linfocitos en sangre en respuesta a la exposición al berilio (como en la prueba de transformación de linfocitos, LTT) o linfocitos de lavado broncoalveolar (BAL) ha sido propuesta por Newman et al. (1989) como herramientas diagnósticas útiles para hacer el diagnóstico de enfermedad por berilio en sujetos expuestos. Sus datos sugieren que un LTT en sangre positivo es indicativo de sensibilización. Sin embargo, datos recientes muestran que el LTT en sangre no se correlaciona bien con la enfermedad pulmonar. La transformación de linfocitos del BAL se correlaciona mucho mejor con la función pulmonar anormal y no se correlaciona bien con anomalías concurrentes en el LTT sanguíneo. Por lo tanto, para hacer un diagnóstico de enfermedad por berilio, se necesita una combinación de anomalías clínicas, radiológicas y de la función pulmonar y un LTT positivo en el LBA. Un LTT en sangre positivo por sí solo no es diagnóstico. El análisis con microsonda de pequeñas muestras de tejido para detectar berilio es otra innovación reciente que podría ayudar en el diagnóstico de enfermedades en pequeñas muestras de tejido pulmonar obtenidas mediante biopsia pulmonar transbronquial.
La sarcoidosis es el trastorno que más se parece a la enfermedad crónica por berilio y la diferenciación puede ser difícil. Hasta el momento, no ha aparecido ninguna enfermedad ósea quística o afectación del ojo o la amígdala en la enfermedad crónica por berilio. De manera similar, la prueba de Kveim es negativa en la enfermedad por berilio. No se recomiendan las pruebas cutáneas para demostrar la sensibilización al berilio, ya que la prueba en sí es sensibilizante, es posible que desencadene reacciones sistémicas en personas sensibilizadas y no establece por sí misma que la enfermedad que se presenta esté necesariamente relacionada con el berilio.
Los enfoques inmunológicos más sofisticados en el diagnóstico diferencial deberían permitir una mejor diferenciación de la sarcoidosis en el futuro.
Pronóstico
El pronóstico de la enfermedad crónica por berilio se ha alterado favorablemente a lo largo de los años; se ha sugerido que los retrasos más prolongados en el inicio observados entre los trabajadores del berilio pueden reflejar una menor exposición o una menor carga corporal de berilio, lo que da como resultado un curso clínico más leve. La evidencia clínica es que la terapia con esteroides, si se usa cuando aparece por primera vez una discapacidad medible, en dosis adecuadas durante períodos suficientemente largos, ha mejorado el estado clínico de muchos pacientes, permitiendo que algunos de ellos regresen a trabajos útiles. No hay pruebas claras de que los esteroides hayan curado la intoxicación crónica por berilio.
Berilio y cáncer
En animales, el berilio administrado experimentalmente es un carcinógeno que causa sarcoma osteogénico después de la inyección intravenosa en conejos y cáncer de pulmón después de la inhalación en ratas y monos. Si el berilio puede ser un carcinógeno humano es un tema controvertido. Algunos estudios epidemiológicos han sugerido una asociación, particularmente después de la enfermedad aguda por berilio. Este hallazgo ha sido cuestionado por otros. Se puede concluir que el berilio es cancerígeno en animales y que puede haber un vínculo entre el cáncer de pulmón y el berilio en humanos, particularmente en aquellos con la enfermedad aguda.
Medidas de Seguridad y Salud
Las precauciones de seguridad y salud deben cubrir el peligro de incendio, así como el peligro de toxicidad mucho más grave.
Prevención de fuego
Deben tomarse las medidas necesarias para evitar posibles fuentes de ignición, como chispas o arcos de aparatos eléctricos, fricción, etc., en las proximidades del polvo de berilio finamente dividido. El equipo en el que haya estado presente este polvo debe vaciarse y limpiarse antes de utilizar acetileno o un aparato de soldadura eléctrica. El polvo de berilio ultrafino sin óxido que se ha preparado en gas inerte puede encenderse espontáneamente al exponerse al aire.
Se debe usar polvo seco adecuado, no agua, para extinguir un incendio de berilio. Se debe usar equipo de protección personal completo, incluido el equipo de protección respiratoria, y los bomberos deben bañarse después y hacer arreglos para que su ropa se lave por separado.
Proteccion de la salud
Los procesos de berilio deben realizarse de manera cuidadosamente controlada para proteger tanto al trabajador como a la población en general. El principal riesgo adopta la forma de contaminación del aire y el proceso y la planta deben diseñarse para generar la menor cantidad posible de polvo o humo. Deben usarse procesos húmedos en lugar de procesos secos, y los ingredientes de las preparaciones que contienen berilio deben unificarse como suspensiones acuosas en lugar de polvos secos; siempre que sea posible, la planta debe diseñarse como grupos de unidades cerradas separadas. La concentración permisible de berilio en la atmósfera es tan baja que se debe aplicar el aislamiento incluso en procesos húmedos, de lo contrario, las salpicaduras y los derrames pueden secarse y el polvo puede entrar en la atmósfera.
Las operaciones de las que se puede desprender polvo deben realizarse en áreas con el máximo grado de cerramiento compatible con las necesidades de manipulación. Algunas operaciones se realizan en cajas de guantes, pero muchas más se llevan a cabo en recintos provistos de ventilación de extracción similar a la instalada en armarios de gases químicos. Las operaciones de maquinado pueden ser ventiladas por sistemas de escape local de bajo volumen y alta velocidad o por recintos con capota con ventilación de escape.
Para comprobar la eficacia de estas medidas de precaución, el control de la atmósfera debe realizarse de forma que se pueda calcular la exposición media diaria de los trabajadores al berilio respirable. El área de trabajo debe limpiarse regularmente con una aspiradora adecuada o un trapeador húmedo. Los procesos de berilio deben separarse de las demás operaciones en la fábrica.
Se debe proporcionar equipo de protección personal a los trabajadores que participen en procesos de berilio. Cuando estén totalmente empleados en procesos que impliquen la manipulación de compuestos de berilio o en procesos asociados con la extracción del metal del mineral, debería preverse un cambio completo de ropa para que los trabajadores no se vayan a casa con ropa que estado trabajando. Deben tomarse medidas para el lavado seguro de dicha ropa de trabajo, y deben proporcionarse monos protectores incluso a los trabajadores de lavandería para garantizar que ellos tampoco estén expuestos a riesgos. Estos arreglos no deben dejarse a los procedimientos normales de lavado en el hogar. Los casos de envenenamiento por berilio en las familias de los trabajadores se han atribuido a que los trabajadores se llevaron ropa contaminada a casa o la usaron en el hogar.
Un estándar de salud ocupacional de 2 μg/m3, propuesta en 1949 por un comité que operaba bajo los auspicios de la Comisión de Energía Atómica de los Estados Unidos, sigue siendo ampliamente observada. Las interpretaciones existentes generalmente permiten fluctuaciones hasta un "techo" de 5 μg/m3 siempre que no se supere la media ponderada en el tiempo. Además, un “pico máximo aceptable por encima de la concentración máxima para un turno de ocho horas” de 25 μg/m3 También se permite hasta 30 min. Estos niveles operativos se pueden lograr en la práctica industrial actual, y no hay evidencia de experiencias adversas para la salud entre las personas que trabajan en un entorno así controlado. Debido a un posible vínculo entre el berilio y el cáncer de pulmón, se ha sugerido que el límite permisible se reduzca a 1 μg/m3, pero no se ha tomado ninguna acción oficial sobre esta sugerencia en los Estados Unidos.
La población en riesgo de desarrollar la enfermedad del berilio es aquella que de alguna manera trata con el berilio en su extracción o uso posterior. Sin embargo, se han informado algunos casos de “vecindario” a una distancia de 1 a 2 km de las plantas de extracción de berilio.
Los exámenes médicos previos al empleo y periódicos de los trabajadores expuestos al berilio y sus compuestos son obligatorios en varios países. La evaluación recomendada incluye un cuestionario respiratorio anual, una radiografía de tórax y pruebas de función pulmonar. Con los avances en inmunología, el LTT también puede convertirse en una evaluación de rutina, aunque en este momento no hay suficientes datos disponibles para recomendar su uso de forma rutinaria. Con evidencia de enfermedad por berilio, no es prudente permitir que un trabajador se exponga más al berilio, aunque el lugar de trabajo cumpla con los criterios de umbral para la concentración de berilio en el aire.
Tratamiento
El paso principal en la terapia es evitar una mayor exposición al berilio. Los corticosteroides son el principal modo de terapia en la enfermedad crónica por berilio. Los corticosteroides parecen alterar favorablemente el curso de la enfermedad, pero no la “curan”.
Los corticosteroides deben comenzar diariamente con una dosis relativamente alta de prednisona de 0.5 a 1 mg por kg o más, y continuar hasta que se produzca una mejoría o no se produzca un mayor deterioro en las pruebas clínicas o de función pulmonar. Por lo general, esto toma de 4 a 6 semanas. Se recomienda una reducción lenta de los esteroides y, eventualmente, puede ser posible una terapia en días alternos. La terapia con esteroides normalmente se convierte en una necesidad de por vida.
Otras medidas de apoyo como oxígeno suplementario, diuréticos, digitálicos y antibióticos (cuando existe infección) están indicadas según lo dicte la condición clínica del paciente. También se debe considerar la inmunización contra la influenza y el neumococo, como con cualquier paciente con enfermedad respiratoria crónica.
Neumoconiosis: Definición
La expresion neumoconiosis del griego pneuma (aire, viento) y konis (polvo) fue acuñado en Alemania por Zenker en 1867 para denotar cambios en los pulmones causados por la retención de polvo inhalado. Gradualmente, se hizo evidente la necesidad de distinguir entre los efectos de varios tipos de polvo. Era necesario discriminar entre polvo mineral o vegetal y su componente microbiológico. En consecuencia, la Tercera Conferencia Internacional de Expertos en Neumoconiosis, organizada por la OIT en Sydney en 1950, adoptó la siguiente definición: “La neumoconiosis es una enfermedad diagnosticable de los pulmones producida por la inhalación de polvo, entendiéndose por el término 'polvo' a la materia particulada en la fase sólida, pero excluyendo los organismos vivos”.
Sin embargo, la palabra enfermedades parece implicar algún grado de deterioro de la salud que puede no ser el caso de las neumoconiosis no relacionadas con el desarrollo de fibrosis/cicatrización pulmonar. En general, la reacción del tejido pulmonar a la presencia de polvo varía según el polvo. Los polvos no fibrogénicos provocan una reacción tisular en los pulmones caracterizada por una mínima reacción fibrótica y ausencia de deterioro de la función pulmonar. Dichos polvos, ejemplos de los cuales son polvos finamente divididos de caolinita, dióxido de titanio, óxido estannoso, sulfato de bario y óxido férrico, se denominan con frecuencia biológicamente inertes.
El polvo fibrogénico como el sílice o el amianto provoca una reacción fibrogénica más pronunciada que produce cicatrices en el tejido pulmonar y enfermedades evidentes. La división de polvos en variedades fibrogénicas y no fibrogénicas no es en modo alguno nítida porque hay muchos minerales, especialmente silicatos, que tienen una capacidad intermedia para producir lesiones fibróticas en los pulmones. Sin embargo, resultó útil para fines clínicos y se refleja en la clasificación de las neumoconiosis.
En la Cuarta Conferencia Internacional sobre Neumoconiosis, Bucarest, 1971, se adoptó una nueva definición de neumoconiosis: “La neumoconiosis es la acumulación de polvo en los pulmones y las reacciones tisulares ante su presencia. A los efectos de esta definición, se entiende por 'polvo' un aerosol compuesto de partículas sólidas inanimadas”.
Para evitar cualquier mala interpretación, la expresión no neoplásico se añade a veces a las palabras "reacción tisular".
El Grupo de Trabajo en la Conferencia hizo la siguiente declaración integral:
La definición de neumoconiosis
Anteriormente, en 1950, se estableció una definición de neumoconiosis en la 3ª Conferencia Internacional de Expertos en Neumoconiosis y se ha seguido utilizando hasta la actualidad. Mientras tanto, el desarrollo de nuevas tecnologías ha resultado en más riesgos laborales, particularmente aquellos relacionados con la inhalación de contaminantes en el aire. El aumento de los conocimientos en el campo de la medicina del trabajo ha permitido reconocer nuevas enfermedades pulmonares de origen profesional, pero también ha demostrado la necesidad de reexaminar la definición de neumoconiosis establecida en 1950. Por lo tanto, la OIT dispuso que se convocara un grupo de trabajo en el marco de la IV Conferencia Internacional de Neumoconiosis para examinar la cuestión de la definición de neumoconiosis. El Grupo de Trabajo celebró una discusión general sobre el tema y procedió a examinar una serie de propuestas presentadas por sus miembros. Finalmente adoptó una nueva definición de neumoconiosis que se preparó junto con un comentario. Este texto se reproduce a continuación.
En los últimos años, varios países han incluido dentro de la neumoconiosis, por razones socioeconómicas, condiciones que manifiestamente no son neumoconiosis, pero que sin embargo son enfermedades pulmonares ocupacionales. Bajo el término “enfermedad” se incluyen por razones preventivas las manifestaciones más tempranas que no son necesariamente incapacitantes o acortadoras de la vida. Por lo tanto, el Grupo de Trabajo se ha comprometido a redefinir la neumoconiosis como la acumulación de polvo en los pulmones y las reacciones tisulares ante su presencia. A los efectos de esta definición, se entiende por "polvo" un aerosol compuesto de partículas inanimadas sólidas. Desde un punto de vista patológico, la neumoconiosis se puede dividir por conveniencia en formas colagenosas o no colagenosas. Una neumoconiosis no colágena es causada por un polvo no fibrogénico y tiene las siguientes características:
- la arquitectura alveolar permanece intacta
- la reacción estromal es mínima y consiste principalmente en fibras de reticulina
- la reacción del polvo es potencialmente reversible.
Ejemplos de neumoconiosis no colágena son las causadas por polvos puros de óxido de estaño (estannosis) y sulfato de bario (baritosis).
La neumoconiosis colágena se caracteriza por:
- alteración permanente o destrucción de la arquitectura alveolar
- reacción colagenosa del estroma de grado moderado a máximo, y
- cicatrización permanente del pulmón.
Tal neumoconiosis colágena puede ser causada por polvos fibrogénicos o por una respuesta tisular alterada a un polvo no fibrogénico.
Ejemplos de neumoconiosis colágena causada por polvos fibrogénicos son la silicosis y la asbestosis, mientras que la neumoconiosis de los trabajadores del carbón complicada o la fibrosis masiva progresiva (PMF) es una respuesta tisular alterada a un polvo relativamente no fibrogénico. En la práctica, la distinción entre neumoconiosis colágena y no colágena es difícil de establecer. La exposición continua al mismo polvo, como el polvo de carbón, puede provocar la transición de una forma no colagenosa a una colagenosa. Además, la exposición a un solo polvo es ahora cada vez menos común y las exposiciones a polvos mixtos que tienen diferentes grados de potencial fibrogénico pueden dar como resultado neumoconiosis que puede variar desde las formas no colagenosas a las colagenosas. Existen además enfermedades pulmonares crónicas profesionales que, aunque se desarrollan por la inhalación de polvo, se excluyen de la neumoconiosis porque no se sabe que las partículas se acumulen en los pulmones. Los siguientes son ejemplos de enfermedades pulmonares crónicas ocupacionales potencialmente incapacitantes: bisinosis, beriliosis, pulmón de granjero y enfermedades relacionadas. Tienen un denominador común, a saber, el componente etiológico del polvo ha sensibilizado el tejido pulmonar o bronquial de modo que si el tejido pulmonar responde, la inflamación tiende a ser granulomatosa y si el tejido bronquial responde, es probable que haya constricción bronquial. Las exposiciones a materiales inhalados nocivos en ciertas industrias están asociadas con un mayor riesgo de mortalidad por carcinoma de las vías respiratorias. Ejemplos de tales materiales son los minerales radiactivos, el asbesto y los cromatos.
Adoptado en la IV Conferencia Internacional de la OIT sobre Neumoconiosis. Bucarest, 1971.
Clasificación internacional de radiografías de neumoconiosis de la OIT
A pesar de todas las energías nacionales e internacionales dedicadas a su prevención, las neumoconiosis siguen estando muy presentes tanto en los países industrializados como en vías de desarrollo, y son responsables de la invalidez y el deterioro de muchos trabajadores. Es por eso que la Oficina Internacional del Trabajo (OIT), la Organización Mundial de la Salud (OMS) y muchos institutos nacionales de salud y seguridad ocupacional continúan su lucha contra estas enfermedades y proponen programas sostenibles para prevenirlas. Por ejemplo, la OIT, la OMS y el Instituto Nacional de Seguridad y Salud Ocupacional (NIOSH) de EE. UU. han propuesto en sus programas trabajar en cooperación en una lucha global contra la silicosis. Parte de este programa se basa en la vigilancia médica que incluye la lectura de radiografías torácicas para ayudar a diagnosticar esta neumoconiosis. Este es un ejemplo que explica por qué la OIT, en cooperación con muchos expertos, ha desarrollado y actualizado de forma continua una clasificación de radiografías de neumoconiosis que proporciona un medio para registrar sistemáticamente las anomalías radiográficas en el tórax provocadas por la inhalación de polvo. El esquema está diseñado para clasificar las apariencias de las radiografías de tórax posterioanteriores.
El objeto de la clasificación es codificar las anormalidades radiográficas de las neumoconiosis de una manera simple y reproducible. La clasificación no define entidades patológicas, ni tiene en cuenta la capacidad de trabajo. La clasificación no implica definiciones legales de neumoconiosis con fines de compensación, ni implica un nivel en el que se pague compensación. Sin embargo, se ha encontrado que la clasificación tiene usos más amplios de lo previsto. Ahora se utiliza ampliamente a nivel internacional para la investigación epidemiológica, para la vigilancia de las ocupaciones de la industria y para fines clínicos. El uso del esquema puede conducir a una mejor comparabilidad internacional de las estadísticas de neumoconiosis. También se utiliza para describir y registrar, de manera sistemática, parte de la información necesaria para evaluar la compensación.
La condición más importante para utilizar este sistema de clasificación con pleno valor desde un punto de vista científico y ético es leer, en todo momento, las películas que se van a clasificar consultando sistemáticamente las 22 películas estándar proporcionadas en el conjunto de normas de Clasificación Internacional de la OIT. Película (s. Si el lector intenta clasificar una película sin hacer referencia a ninguna de las películas estándar, entonces no se debe mencionar la lectura de acuerdo con la Clasificación Internacional de Radiografías de la OIT. La posibilidad de desviarse de la clasificación por sobrelectura o sublectura es tan riesgosa que su lectura no debe ser utilizada al menos para investigación epidemiológica o comparabilidad internacional de estadísticas de neumoconiosis.
La primera clasificación se propuso para la silicosis en la Primera Conferencia Internacional de Expertos en Neumoconiosis, celebrada en Johannesburgo en 1930. Combinaba aspectos radiográficos y deterioro de las funciones pulmonares. En 1958 se estableció una nueva clasificación basada puramente en cambios radiográficos (clasificación de Ginebra 1958). Desde entonces, ha sido revisado varias veces, la última vez en 1980, siempre con el objetivo de brindar versiones mejoradas para ser ampliamente utilizadas con fines clínicos y epidemiológicos. Cada nueva versión de la clasificación promovida por la OIT ha traído modificaciones y cambios basados en la experiencia internacional adquirida en el uso de clasificaciones anteriores.
Con el fin de proporcionar instrucciones claras para el uso de la clasificación, la OIT publicó en 1970 una publicación titulada Clasificación Internacional de Radiografías de Neumoconiosis/1968 en la Serie Seguridad y Salud en el Trabajo (Nº 22). Esta publicación fue revisada en 1972 como Clasificación Internacional de Radiografías de Neumoconiosis ILO U/C/1971 y nuevamente en 1980 como Directrices para el uso de la Clasificación Internacional de Radiografías de Neumoconiosis de la OIT, edición revisada 1980. La descripción de las radiografías estándar se da en la tabla 1.
Tabla 1. Descripción de las radiografías estándar
| 1980 Radiografías estándar que muestran | Pequeñas opacidades | Engrosamiento pleural | ||||||||||
| Pared de pecho | ||||||||||||
| Calidad técnica | Profusión | Tamaño de la forma | Grado | Grandes opacidades | circunscrito (placas) | Difuso | Diafragma | Obliteración del ángulo costofrénico | Calcificación pleural | Símbolos | Comentarios | |
| 0/0 (ejemplo 1) | 1 | 0/0 | – | – | No | No | No | No | No | No | Ninguna | El patrón vascular está bien ilustrado. |
| 0/0 (ejemplo 2) | 1 | 0/0 | – | – | No | No | No | No | No | No | Ninguna | También muestra el patrón vascular, pero no tan claramente como el ejemplo 1 |
| 1/1; páginas | 1 | 1/1 | páginas | R L x x x x x x | A | No | No | No | No | No | rp. | Neumoconiosis reumatoide en zona inferior izquierda. Pequeñas opacidades están presentes en todas las zonas, pero la profusión en la zona superior derecha es típica (algunos dirían un poco más profusa) que clasificable como categoría 1/1 |
| 2/2; páginas | 2 | 2/2 | páginas | R L x x x x x x | No | No | No | No | No | No | Pi; tuberculosis. | Defecto de calidad: la radiografía es demasiado clara |
| 3/3; páginas | 1 | 3/3 | páginas | R L x x x x x x | No | No | No | No | Sí R L x – | No | hacha. | Ninguna |
| 1/1; q/q | 1 | 1/1 | q / q | R L x x x x – – | No | No | No | No | No | No | Ninguna | Ilustra la profusión 1/1 mejor que la forma o el tamaño |
| 2/2; q/q | 1 | 2/2 | q / q | R L x x x x x x | No | No | Sí R L x x ancho: a a extensión: 1 1 | No | Sí R L x x | No | Ninguna | Ninguna |
| 3/3; q/q | 2 | 3/3 | q / q | R L x x x x x x | No | No | No | No | No | No | Pi. | Defectos de calidad: mala definición de la pleura y ángulos basales cortados |
| 1/1; r/r | 2 | 1/1 | a / a | R L x x x x – – | No | No | No | No | Sí R L – x | No | Ninguna | Defecto de calidad: movimiento del sujeto. La profusión de pequeñas opacidades es más marcada en el pulmón derecho. |
| 2/2; r/r | 2 | 2/2 | a / a | R L x x x x x x | No | No | No | No | No | No | Ninguna | Defectos de calidad: radiografía demasiado clara y contraste demasiado alto. La sombra del corazón está ligeramente desplazada hacia la izquierda. |
| 3/3; r/r | 1 | 3/3 | a / a | R L x x x x x x | No | No | No | No | No | No | hacha; yo | Ninguna |
| 1/1; S t | 2 | 1/1 | S t | R L x – x x x x | No | No | No | No | No | No | kl. | Defecto de calidad: bases cortadas. Líneas de Kerley en zona inferior derecha |
| 2/2; s/s | 2 | 2/2 | s / s | R L – – x x x x | No | No | No | No | No | No | em. | Defecto de calidad: distorsión de bases por encogimiento. Enfisema en zonas superiores |
| 3/3; s/s | 2 | 3/3 | s / s | R L x x x x x x | No | No | Sí R L x x ancho: a a extensión: 3 3 | No | No | No | Ho; yo; Pi. | Defecto de calidad: la radiografía es demasiado clara. La apariencia del pulmón en panal no está marcada |
| 1/1; t/t Obliteración del ángulo costofrénico | 1 | 1/1 | t / t | R L – – x x x x | No | No | Sí R L x x ancho: a a extensión: 2 2 | No | Sí R L x – | Sí R L – x extensión: 2 | Ninguna | Esta radiografía define el límite inferior para la obliteración del ángulo costofrénico. Note la contracción en los campos pulmonares inferiores |
| 2/2; t/t | 1 | 2/2 | t / t | R L x x x x x x | No | No | Sí R L x x ancho: a a extensión: 1 1 | No | No | No | yo | El engrosamiento pleural está presente en los vértices del pulmón. |
| 3/3; t/t | 1 | 3/3 | t / t | R L x x x x x x | No | No | No | No | No | No | hola; Ho; identificación; yo; tuberculosis. | Ninguna |
| 1/1; u/u 2/2; u/u 3/3; tu/tu | – | – | – | – | – | – | – | – | – | – | – | Esta radiografía compuesta ilustra las categorías medias de profusión de pequeñas opacidades clasificables por forma y tamaño como u/u. |
| A | 2 | 2/2 | p / q | R L x x x x x x | A | No | No | No | No | No | No | Defectos de calidad: la radiografía es demasiado clara y la definición pleural es pobre |
| B | 1 | 1/2 | p / q | R L x x x x x x | B | No | No | No | No | No | hacha; co. | La definición de pleura es ligeramente imperfecta. |
| C | 1 | 2/1 | q/t | R L x x x x x x | C | No | No | No | No | No | bu; di; em; es; hola; yo | Las opacidades pequeñas son difíciles de clasificar debido a la presencia de opacidades grandes. Nótese la obliteración del ángulo costofrénico izquierdo. Este no es clasificable porque no alcanza el límite inferior definido por la radiografía estándar 1/1; t/t |
| Engrosamiento pleural (circunscrito) | – | – | – | – | – | Sí | No | No | No | No | El engrosamiento pleural se presenta de frente, es de ancho indeterminado y extensión 2 | |
| Engrosamiento pleural (difuso) | – | – | – | – | – | No | Sí | No | No | Sí | El engrosamiento pleural presente de perfil, es de ancho a, y extensión 2. No asocia pequeñas calcificaciones | |
| Engrosamiento pleural (calcificación) diafragma | – | – | – | – | – | No | No | Sí | No | Sí | Engrosamiento pleural circunscrito, calcificado de extensión 2 | |
| Engrosamiento pleural (calcificación) de la pared torácica | – | – | – | – | – | Sí | No | No | No | Sí | Engrosamiento pleural calcificado y no calcificado presente de frente, de ancho indeterminado y extensión 2 | |
Clasificación de la OIT de 1980
La revisión de 1980 fue realizada por la OIT con la cooperación de la Comisión de las Comunidades Europeas, NIOSH y el Colegio Americano de Radiología. El resumen de la clasificación se da en la tabla 2. Mantuvo el principio de las clasificaciones anteriores (1968 y 1971).
Cuadro 2. Clasificación internacional de radiografías de neumoconiosis de la OIT de 1980: resumen de los detalles de la clasificación
| Caracteristicas | Códigos | Definiciones | |
| Calidad técnica | |||
| 1 | Buena. | ||
| 2 | Aceptable, sin defecto técnico que pueda perjudicar la clasificación de la radiografía de neumoconiosis. | ||
| 3 | Pobre, con algún defecto técnico pero aún aceptable a efectos de clasificación. | ||
| 4 | Inaceptable. | ||
| anomalías del parénquima | |||
| Pequeñas opacidades | Profusión | La categoría de profusión se basa en la evaluación de la concentración de opacidades en comparación con las radiografías estándar. | |
| 0/- 0/0 0/1 1/0 1/1 1/2 2/1 2/2 2/3 3/2 3/3 3/+ | Categoría O: opacidades pequeñas ausentes o menos profusas que el límite inferior de la categoría 1. Categorías 1, 2 y 3: profusión creciente de opacidades pequeñas según lo definido por las radiografías estándar correspondientes. | ||
| Grado | RU RM RL LU LM LL | Se registran las zonas en las que se ven las opacidades. El tórax derecho (R) e izquierdo (L) se dividen en tres zonas: superior (U), media (M) e inferior (L). La categoría de profusión se determina considerando la profusión como un todo sobre las zonas afectadas del pulmón y comparándola con las radiografías estándar. | |
| Forma y tamaño | |||
| Redondeado | p/p q/q r/r | Las letras p, q y r denotan la presencia de pequeñas opacidades redondeadas. Se definen tres tamaños por las apariencias en las radiografías estándar: p = diámetro de hasta aproximadamente 1.5 mm q = diámetro superior a aproximadamente 1.5 mm y hasta aproximadamente 3 mm r = diámetro superior a aproximadamente 3 mm y hasta aproximadamente 10 mm | |
| Irregular | s/s t/t u/u | Las letras s, t y u denotan la presencia de pequeñas opacidades irregulares. Se definen tres tamaños por las apariencias en las radiografías estándar: s = ancho de hasta aproximadamente 1.5 mm t = ancho superior a aproximadamente 1.5 mm y hasta aproximadamente 3 mm u = ancho superior a 3 mm y hasta aproximadamente 10 mm | |
| Mixto | p/s p/t p/u p/q p/r q/s q/t q/u q/p q/r r/s r/t r/u r/p r/q s/p s/q s/r s/t s/u t/p t/q t/r t/s t/ u u/p u/q u/r u/s u/t | Para formas (o tamaños) mixtos de pequeñas opacidades, se registra primero la forma y el tamaño predominantes. La presencia de un número significativo de otra forma y tamaño se registra después del trazo oblicuo. | |
| Grandes opacidades | A B C | Las categorías se definen en términos de las dimensiones de las opacidades. Categoría A: una opacidad que tiene un diámetro mayor que excede aproximadamente 10 mm y hasta 50 mm inclusive, o varias opacidades cada una mayor de aproximadamente 10 mm, la suma de cuyos diámetros mayores no excede aproximadamente 50 mm. Categoría B: una o más opacidades mayores o más numerosas que las de la categoría A cuya área combinada no exceda el equivalente de la zona superior derecha. Categoría C: una o más opacidades cuya área combinada excede el equivalente de la zona superior derecha. | |
| anomalías pleurales | |||
| Engrosamiento pleural | |||
| Pared de pecho | Tipo de Propiedad | Se reconocen dos tipos de engrosamiento pleural de la pared torácica: circunscrito (placas) y difuso. Ambos tipos pueden ocurrir juntos. | |
| Planta | R L | El engrosamiento pleural de la pared torácica se registra por separado para el tórax derecho (R) e izquierdo (L). | |
| Ancho Mínimo | a B C | Para el engrosamiento pleural que se observa a lo largo de la pared torácica lateral, la medición del ancho máximo se realiza desde la línea interna de la pared torácica hasta el margen interno de la sombra que se observa con mayor nitidez en el límite parenquimatoso-pleural. El ancho máximo generalmente ocurre en el margen interno de la sombra de la costilla en su punto más externo. a = ancho máximo hasta 5 mm b = ancho máximo sobre 5 mm y hasta 10 mm c = ancho máximo sobre 10 mm | |
| Afróntalo | S N | Se registra la presencia de engrosamiento pleural visto de frente aunque también puede verse de perfil. Si el engrosamiento pleural se ve solo de frente, por lo general no se puede medir el ancho. | |
| Grado | 1 2 3 | La extensión del engrosamiento pleural se define en términos de la longitud máxima de afectación pleural, o como la suma de las longitudes máximas, ya sea visto de perfil o de frente. 1 = longitud total equivalente a hasta un cuarto de la proyección de la pared torácica lateral 2 = longitud total superior a un cuarto pero no a la mitad de la proyección de la pared torácica lateral 3 = longitud total superior a la mitad de la proyección de la pared torácica lateral pared | |
| Diafragma | Presencia | S N | Una placa que afecta a la pleura diafragmática se registra como presente (Y) o ausente (N), por separado para el tórax derecho (R) e izquierdo (L). |
| Planta | R L | ||
| Obliteración del ángulo costofrénico | Presencia | S N | La presencia (Y) o ausencia (N) de obliteración del ángulo costofrénico se registra por separado del engrosamiento sobre otras áreas, para el tórax derecho (R) e izquierdo (L). El límite inferior para esta obliteración está definido por una radiografía estándar |
| Planta | R L | Si el engrosamiento se extiende hacia arriba de la pared torácica, deben registrarse tanto la obliteración del ángulo costofrénico como el engrosamiento pleural. | |
| Calcificación pleural | Planta | El sitio y la extensión de la calcificación pleural se registran por separado para los dos pulmones y la extensión se define en términos de dimensiones. | |
| Pared de pecho | R L | ||
| Diafragma | R L | ||
| Otro | R L | “Otros” incluye calcificación de la pleura mediastínica y pericárdica. | |
| Grado | 1 2 3 | 1 = un área de pleura calcificada con un diámetro mayor de hasta unos 20 mm, o un número de tales áreas cuya suma de diámetros mayores no exceda de unos 20 mm. 2 = un área de pleura calcificada con un diámetro mayor que excede alrededor de 20 mm y hasta alrededor de 100 mm, o un número de tales áreas cuya suma de diámetros mayores excede alrededor de 20 mm pero no excede alrededor de 100 mm. 3 = un área de pleura calcificada con un diámetro mayor que excede los 100 mm, o un número de tales áreas cuya suma de diámetros mayores excede los 100 mm. | |
| Símbolos | |||
| Se debe considerar que la definición de cada uno de los símbolos está precedida por una palabra o frase apropiada como “sospechoso”, “cambios sugestivos de”, u “opacidades sugestivas de”, etc. | |||
| ax | Coalescencia de pequeñas opacidades neumoconióticas | ||
| bu | bulla(e) | ||
| ca | Cáncer de pulmón o pleura | ||
| cn | Calcificación en pequeñas opacidades neumoconioticas | ||
| co | Anomalía del tamaño o la forma del corazón | ||
| cp | corazón pulmonar | ||
| cv | Cavidad2 | ||
| di | Marcada distorsión de los órganos intratorácicos | ||
| ef | Efusión | ||
| em | Enfisema definitivo | ||
| es | Calcificación en cáscara de huevo de ganglios linfáticos hiliares o mediastínicos | ||
| fr | Costilla(s) fracturada(s) | ||
| hi | Agrandamiento de los ganglios linfáticos hiliares o mediastínicos | ||
| ho | pulmón de panal | ||
| id | Diafragma mal definido | ||
| ih | Contorno del corazón mal definido | ||
| kl | Líneas septales (de Kerley) | ||
| od | Otra anormalidad significativa | ||
| pi | Engrosamiento pleural en la fisura interlobar del mediastino | ||
| px | Neumotórax | ||
| rp | Neumoconiosis reumatoide | ||
| tb | Tuberculosis | ||
| Comentarios | |||
| Presencia | S N | Se deben registrar los comentarios relacionados con la clasificación de la radiografía, particularmente si se cree que alguna otra causa es responsable de una sombra que otros podrían pensar que se debe a la neumoconiosis; también para identificar radiografías cuya calidad técnica puede haber afectado materialmente la lectura. | |
La Clasificación se basa en un conjunto de radiografías estándar, un texto escrito y un conjunto de notas (OHS No. 22). No hay características que se vean en una radiografía de tórax que sean patognomónicas de la exposición al polvo. El principio esencial es que todas las apariencias que sean consistentes con las definidas y representadas en las radiografías estándar y la guía para el uso de la Clasificación Internacional de la OIT, deben ser clasificadas. Si el lector cree que alguna apariencia probablemente o definitivamente no está relacionada con el polvo, la radiografía no debe clasificarse, pero debe agregarse un comentario apropiado. Las 22 radiografías estándar han sido seleccionadas después de ensayos internacionales, de tal manera que ilustran los estándares de profusión de categorías medias de opacidades pequeñas y dan ejemplos de estándares de categoría A, B y C para opacidades grandes. Las anomalías pleurales (engrosamiento pleural difuso, placas y obliteración del ángulo costofrénico) también se ilustran en diferentes radiografías.
La discusión en particular en la Séptima Conferencia Internacional sobre Neumoconiosis, celebrada en Pittsburgh en 1988, indicó la necesidad de mejorar algunas partes de la clasificación, en particular las relacionadas con los cambios pleurales. En noviembre de 1989, la OIT convocó en Ginebra a un grupo de discusión sobre la revisión de la Clasificación Internacional de Radiografías de Neumoconiosis de la OIT. Los expertos sugirieron que la clasificación abreviada no tiene ninguna ventaja y puede eliminarse. En cuanto a las anomalías pleurales, el grupo acordó que esta clasificación ahora se dividiría en tres partes: “Engrosamiento pleural difuso”; “Placas pleurales”; y “Obliteración del ángulo costofrénico”. El engrosamiento pleural difuso se puede dividir en pared torácica y diafragma. Se identificaron según las seis zonas: superior, media e inferior, de los pulmones derecho e izquierdo. Si se circunscribe un engrosamiento pleural, podría identificarse como una placa. Todas las placas deben medirse en centímetros. La obliteración del ángulo costofrénico debe anotarse sistemáticamente (ya sea que exista o no). Es importante identificar si el ángulo costofrénico es visible o no. Esto se debe a su especial importancia en relación con el engrosamiento pleural difuso. Si las placas están clasificadas o no, debe indicarse simplemente mediante un símbolo. El aplanamiento del diafragma debe registrarse con un símbolo adicional, ya que es una característica muy importante en la exposición al asbesto. La presencia de placas debe registrarse en estas casillas utilizando el símbolo apropiado “c” (calcificado) o “h” (hialino).
En la publicación (OIT 1980) se encuentra una descripción completa de la clasificación, incluidas sus aplicaciones y limitaciones. La revisión de la clasificación de las radiografías es un proceso continuo de la OIT, y en un futuro próximo (1997-98) debería publicarse una directriz revisada que tenga en cuenta las recomendaciones de estos expertos.
" EXENCIÓN DE RESPONSABILIDAD: La OIT no se responsabiliza por el contenido presentado en este portal web que se presente en un idioma que no sea el inglés, que es el idioma utilizado para la producción inicial y la revisión por pares del contenido original. Ciertas estadísticas no se han actualizado desde la producción de la 4ª edición de la Enciclopedia (1998)."