Categorias crianças

1. Sangue (3)

1. Sangue
Editor de Capítulo: Bernard D. Goldstein
Conteúdo
Tabelas
Sistema hematopoiético e linfático
Bernard D. Goldstein
Leucemia, Linfomas Malignos e Mieloma Múltiplo
Timo Partanen, Paolo Boffetta, Elisabete Weiderpass
Agentes ou Condições de Trabalho que Afetam o Sangue
Bernard D. Goldstein
Tabelas
Clique em um link abaixo para visualizar a tabela no contexto do artigo.

2. Câncer (4)

2. Câncer
Editor de Capítulo: Paulo Boffetta
mesa de conteúdo
Tabelas
Introdução
Neil Pearce, Paolo Boffetta e Manolis Kogevinas
Carcinógenos ocupacionais
Paolo Boffetta, Rodolfo Saracci, Manolis Kogevinas, Julian Wilbourn e Harri Vainio
Câncer Ambiental
Bruce K. Armstrong e Paolo Boffetta
Prevenção
Por Gustavsson
Tabelas
Clique em um link abaixo para visualizar a tabela no contexto do artigo.
- Câncer ocupacional: principais fatos
- Proporções estimadas de câncer (PAR) atribuíveis a ocupações
- Avaliação de evidências de carcinogenicidade nas monografias da IARC
- Grupos de classificação do programa de monografias da IARC
- Grupo 1-Produtos químicos cancerígenos para humanos
- Grupo 2A - Produtos químicos provavelmente cancerígenos para humanos
- Grupo 2B—Produtos químicos possivelmente cancerígenos para humanos
- Pesticidas avaliados em Monografias da IARC, Volumes 1-63 (1972-1995)
- Drogas avaliadas nas Monografias da IARC, Volumes 1-63 (1972-1995)
- Agentes ambientais/exposições conhecidas ou suspeitas de câncer humano
- Indústrias, ocupações, exposições que apresentam um risco cancerígeno
- Indústrias, occs., exps. com excesso de câncer não carcinógenos definitivos
- Variações populacionais registradas de incidência de alguns cânceres comuns

3. Sistema cardiovascular (7)

3. Sistema Cardiovascular
Editores de Capítulo: Lothar Heinemann e Gerd Heuchert
Conteúdo
Tabelas e Figuras
Introdução
Lothar Heinemann e Gerd Heuchert
Morbidade e Mortalidade Cardiovascular na Força de Trabalho
Gottfried Enderlein e Lothar Heinemann
O conceito de fator de risco em doenças cardiovasculares
Lothar Heinemann, Gottfried Enderlein e Heide Stark
Programas de reabilitação e prevenção
Lothar Heinemann e Gottfried Enderlein
Perigos Físicos, Químicos e Biológicos
Fatores físicos
Heide Stark e Gerd Heuchert
Materiais Químicos Perigosos
Ulrike Tittelbach e Wolfram Dietmar Schneider
Riscos Biológicos
Regina Jäckel, Ulrike Tittelbach e Wolfram Dietmar Schneider
Tabelas
Clique em um link abaixo para ver a tabela no contexto do artigo
- Mortalidade por doenças cardiovasculares
- Taxas de mortalidade, grupos especiais de diagnóstico cardiovascular
- Taxa de doenças e capacidade de trabalho reduzida
- Trabalho associado a riscos cardiovasculares
- Infecções e doenças ocupacionais
figuras
Aponte para uma miniatura para ver a legenda da figura, clique para ver a figura no contexto do artigo.

4. Sistema Digestivo (6)

4. Sistema Digestivo
Editor de Capítulo: Heikki Savolainen
Conteúdo
figuras
Sistema digestivo
G.Frada
Boca e dentes
F. Gobbato
Fígado
George Kazantzis
Úlcera péptica
KS Cho
Câncer de fígado
Timo Partanen, Timo Kauppinen, Paolo Boffetta e Elisabete Weiderpass
Câncer de pâncreas
Timo Partanen, Timo Kauppinen, Paolo Boffetta e Elisabete Weiderpass
figuras
Aponte para uma miniatura para ver a legenda da figura, clique para ver a figura no contexto do artigo.

5. Saúde Mental (8)

5. Saúde mental
Editores de capítulos: Joseph J. Hurrell, Lawrence R. Murphy, Steven L. Sauter e Lennart Levi
Conteúdo
Tabelas e Figuras
Trabalho e Saúde Mental
Irene LD Houtman e Michiel AJ Kompier
Psicose relacionada ao trabalho
Craig Stenberg, Judith Holder e Krishna Tallur
Humor e Afeto
Depressão
Jay Lasser e Jeffrey P. Kahn
Ansiedade relacionada ao trabalho
Randal D. Beaton
Transtorno de estresse pós-traumático e sua relação com a saúde ocupacional e prevenção de lesões
Mark Braverman
Estresse e Burnout e suas Implicações no Ambiente de Trabalho
Herbert J. Freudenberger
Distúrbios Cognitivos
Catherine A. Heaney
Karoshi: Morte por excesso de trabalho
Takashi Haratani
Tabelas
Clique em um link abaixo para visualizar a tabela no contexto do artigo.
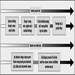
1. Visão geral esquemática de estratégias e exemplos de gerenciamento
figuras
Aponte para uma miniatura para ver a legenda da figura, clique para ver a figura no contexto do artigo.

6. Sistema musculoesquelético (14)

6. Sistema musculoesquelético
Editores de Capítulo: Hilkka Riihimäki e Eira Viikari-Juntura
Conteúdo
Tabelas e Figuras
Visão geral
Hilkka Riihimäki
Músculos
Gisela Sjøgaard
Tendões
Thomas J Armstrong
Ossos e articulações
David Hamerman
Discos intervertebrais
Sally Roberts e Jill PG Urban
Região lombar
Hilkka Riihimäki
Região da Coluna Torácica
Jarl-Erik Michelsson
Pescoço
Åsa Kilbom
Ombro
Mats Hagberg
Cotovelo
Eira Viikari-Juntura
Antebraço, Punho e Mão
Eira Viikari-Juntura
Quadril e Joelho
Eva Vingård
Perna, Tornozelo e Pé
Jarl-Erik Michelsson
Outras doenças
Marjatta Leirisalo-Repo
Tabelas
Clique em um link abaixo para visualizar a tabela no contexto do artigo.
- Estrutura-função dos componentes da junta
- Prevalência de problemas nas costas, em finlandeses com mais de 30 anos
- Reduzindo os riscos de lombalgia no trabalho
- Classificação de distúrbios lombares (Força-Tarefa de Quebec)
- Movimentos permitidos para a cabeça em condução prolongada
- Incidência de epicondilite em várias populações
- Incidência de tenossinovite/peritendinite
- Osteoartrose primária do quadril em Malmö, Suécia
- Diretrizes para o tratamento da artrite reumatoide
- Infecções conhecidas por desencadear artrite reativa
figuras
Aponte para uma miniatura para ver a legenda da figura, clique para ver a figura no contexto do artigo.

7. Sistema Nervoso (9)

7. Sistema Nervoso
Editor de Capítulo: Donna Mergler
Conteúdo
Tabelas e Figuras
Sistema Nervoso: Visão Geral
Donna Mergler e José A. Valciukas
Anatomia e Fisiologia
José A. Valciukas
Agentes Químicos Neurotóxicos
Peter Arlien-Søborg e Leif Simonsen
Manifestações de Intoxicação Aguda e Crônica Precoce
Donna Mergler
Prevenção da Neurotoxicidade no Trabalho
Barry johnson
Síndromes clínicas associadas à neurotoxicidade
Roberto G. Feldman
Medindo Déficits Neurotóxicos
Donna Mergler
Diagnóstico
Anna Maria Seppäläinen
Neuroepidemiologia Ocupacional
Olav Axelson
Tabelas
Clique em um link abaixo para visualizar a tabela no contexto do artigo.
- Nomes e principais funções de cada par de nervos cranianos
- Agrupando efeitos neurotóxicos quanto à neurotoxicidade
- Gases associados a efeitos neurotóxicos
- Metais neurotóxicos e seus compostos inorgânicos
- monômeros neurotóxicos
- Solventes orgânicos associados à neurotoxicidade
- Classes de pesticidas neurotóxicos comuns
- Outros produtos químicos associados à neurotoxicidade
- Lista de verificação de sintomas crônicos
- Efeitos neurofuncionais da exposição a algumas neurotoxinas
- Exposições químicas e síndromes neurotóxicas associadas
- Algumas baterias “centrais” para avaliar os efeitos neurotóxicos precoces
- Árvore de decisão para doenças neurotóxicas
- Efeitos neurofuncionais consistentes de exposições no local de trabalho a algumas das principais substâncias neurotóxicas
figuras
Aponte para uma miniatura para ver a legenda da figura, clique para ver a figura no contexto do artigo.

8. Sistema renal-urinário (2)

8. Sistema Renal-Urinário
Editor de Capítulo: George P. Hemstreet
Conteúdo
Tabelas e Figuras
Sistemas Renais-Urinários
George P. Hemstreet
Cânceres Renais-Urinários
Timo Partanen, Harri Vainio, Paolo Boffetta e Elisabete Weiderpass
Tabelas
Clique em um link abaixo para visualizar a tabela no contexto do artigo.
- Enzimas do metabolismo de drogas nos rins
- As causas mais comuns de hematúria, por idade e sexo
- Critérios para seleção de biomarcadores
- Biomarcadores potenciais ligados à lesão celular
- Insuficiência renal aguda e ocupação
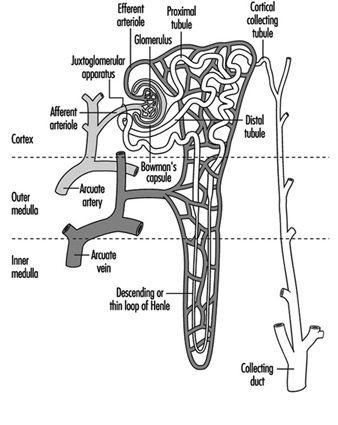
- Segmentos do néfron afetados por substâncias tóxicas selecionadas
- Aplicações da citologia urinária
figuras
Aponte para uma miniatura para ver a legenda da figura, clique para ver a figura no contexto do artigo.

9. Sistema Reprodutivo (9)

9. Sistema reprodutivo
Editor de Capítulo: Graça Kawas Lemasters
Conteúdo
Tabelas e Figuras
Sistema Reprodutivo: Introdução
Lowell E. Sever
Introdução à função reprodutiva masculina e feminina
Donald R Mattison
Sistema Reprodutor Masculino e Toxicologia
Steven Schrader e Grace Kawas Lemasters
Estrutura do Sistema Reprodutivo Feminino e Vulnerabilidade do Órgão Alvo
Donald R Mattison
Exposições ocupacionais maternas e resultados adversos da gravidez
Graça Kawas Lemasters
Parto prematuro e trabalho
Nicole Mamelle
Exposições ocupacionais e ambientais ao recém-nascido
Mary S. Wolff e Patrisha M. Woolard
Proteção à Maternidade na Legislação
Marie-Claire Séguret
Gravidez e recomendações de trabalho nos EUA
Leon J. Warshaw
Tabelas
Clique em um link abaixo para visualizar a tabela no contexto do artigo.
1. Exposições com múltiplos endpoints adversos
2. Estudos epidemiológicos dos efeitos paternos no resultado da gravidez
3. Potenciais tóxicos reprodutivos femininos
4. Definição de perda fetal e morte infantil
5. Fatores para pequeno para idade gestacional e perda fetal
6. Fontes identificadas de fadiga ocupacional
7. Riscos relativos e índices de fadiga para parto prematuro
8. Risco de prematuridade por número de índices de fadiga ocupacional
9. Riscos relativos e mudanças nas condições de trabalho
10. Fontes e níveis de exposição de recém-nascidos
figuras
Aponte para uma miniatura para ver a legenda da figura, clique para ver a figura no contexto do artigo.

10. Sistema Respiratório (18)

10. Sistema respiratório
Editores de capítulos: Alois David e Gregory R. Wagner
Conteúdo
Tabelas e Figuras
Estrutura e função
Morton Lippmann
Exame de Função Pulmonar
Ulf Ulfvarson e Monica Dahlqvist
Doenças Causadas por Irritantes Respiratórios e Produtos Químicos Tóxicos
David LS Ryon e William N. Rom
Asma Ocupacional
George Friedman-Jimenez e Edward L. Petsonk
Doenças Causadas por Poeiras Orgânicas
Ragnar Rylander e Richard SF Schilling
Doença do berílio
Homayoun Kazemi
Pneumoconioses: Definição
Alois David
Classificação Internacional de Radiografias de Pneumoconioses da OIT
Michel Lesage
Etiopatogenia das Pneumoconioses
Patrick Sébastien e Raymond Bégin
Silicose
John E. Parker e Gregory R. Wagner
Doenças Pulmonares dos Carvoeiros
Michael D. Attfield, Edward L. Petsonk e Gregory R. Wagner
Doenças Relacionadas ao Amianto
Margaret R. Becklake
Doença do Metal Duro
Gerolamo Chiappino
Sistema respiratório: a variedade de pneumoconioses
Steven R. Short e Edward L. Petsonk
Doença de obstrução pulmonar crônica
Kazimierz Marek e Jan E. Zejda
Efeitos para a saúde de fibras sintéticas
James E. Lockey e Clara S. Ross
Câncer Respiratório
Paolo Boffetta e Elisabete Weiderpass
Infecções pulmonares adquiridas ocupacionalmente
Anthony A. Marfin, Ann F. Hubbs, Karl J. Musgrave e John E. Parker
Tabelas
Clique em um link abaixo para visualizar a tabela no contexto do artigo.
1. Regiões do trato respiratório e modelos de deposição de partículas
2. Critérios de poeira inalável, torácica e respirável
3. Resumo de irritantes respiratórios
4. Mecanismos de lesão pulmonar por substâncias inaladas
5. Compostos capazes de toxicidade pulmonar
6. Definição de caso médico de asma ocupacional
7. Passos na avaliação diagnóstica da asma no local de trabalho
8. Agentes sensibilizantes que podem causar asma ocupacional
9. Exemplos de fontes de perigos de exposição a poeira orgânica
10. Agentes em poeiras orgânicas com potencial atividade biológica
11. Doenças induzidas por poeiras orgânicas e seus códigos CID
12. Critérios diagnósticos para bissinose
13. Propriedades do berílio e seus compostos
14. Descrição das radiografias padrão
15. Classificação OIT 1980: Radiografias de Pneumoconioses
16. Doenças e condições relacionadas ao amianto
17. Principais fontes comerciais, produtos e usos do amianto
18. Prevalência de DPOC
19. Fatores de risco implicados na DPOC
20. Perda da função ventilatória
21. Classificação diagnóstica, bronquite crônica e enfisema
22. Teste de função pulmonar na DPOC
23. Fibras sintéticas
24. Carcinógenos respiratórios humanos estabelecidos (IARC)
25. Prováveis carcinógenos respiratórios humanos (IARC)
26. Doenças Infecciosas Respiratórias Adquiridas Ocupacionalmente
figuras
Aponte para uma miniatura para ver a legenda da figura, clique para ver a figura no contexto do artigo.

11. Sistemas sensoriais (8)

11. Sistemas Sensoriais
Editor de Capítulo: Heikki Savolainen
Conteúdo
Tabelas e Figuras
A orelha
Marcel-André Boillat
Distúrbios auditivos induzidos quimicamente
Peter Jacobsen
Distúrbios auditivos induzidos fisicamente
Pedro L. Pelmear
Equilíbrio
Lucy Yardley
Visão e Trabalho
Paule Rey e Jean-Jacques Meyer
Gosto
April E. Mott e Norman Mann
Cheiro
Abril E. Mott
Receptores cutâneos
Robert Dykes e Daniel McBain
Tabelas
Clique em um link abaixo para visualizar a tabela no contexto do artigo.
1. Cálculo típico de perda funcional de um audiograma
2. Requisitos visuais para diferentes atividades
3. Valores de iluminância recomendados para o projeto de iluminação
4. Requisitos visuais para uma carteira de motorista na França
5. Agentes/processos relatados para alterar o sistema de sabor
6. Agentes/processos associados a anormalidades olfativas
figuras
Aponte para uma miniatura para ver a legenda da figura, clique para ver a figura no contexto do artigo.

12. Doenças de pele (7)

12. Doenças da Pele
Editor de Capítulo: Louis-Philippe Durocher
Conteúdo
Tabelas e Figuras
Visão geral: doenças ocupacionais da pele
Donald J.Birmingham
Câncer de pele não melanocítico
Elisabete Weiderpass, Timo Partanen, Paolo Boffetta
Melanoma maligno
Timo Partanen, Paolo Boffetta, Elisabete Weiderpass
Dermatite de contato ocupacional
Denis Sasseville
Prevenção de Dermatoses Ocupacionais
Louis Philippe Durocher
Distrofia Ocupacional das Unhas
CD Calnan
Stigmata
H. Mierzecki
Tabelas
Clique em um link abaixo para visualizar a tabela no contexto do artigo.
1. Ocupações de risco
2. Tipos de dermatite de contato
3. irritantes comuns
4. Alérgenos comuns da pele
5. Fatores predisponentes para dermatite ocupacional
6. Exemplos de irritantes e sensibilizadores da pele com ocupações
7. Dermatoses ocupacionais em Quebec em 1989
8. Fatores de risco e seus efeitos na pele
9. Medidas coletivas (abordagem de grupo) para prevenção
figuras
Aponte para uma miniatura para ver a legenda da figura, clique para ver a figura no contexto do artigo.

13. Condições Sistêmicas (3)

13. Condições Sistêmicas
Editor de Capítulo: Howard M. Kipen
Conteúdo
figuras
Condições Sistêmicas: Uma Introdução
Howard M. Kipen
Síndrome do Edifício Doente
Michael J. Hodgson
Múltiplas sensibilidades químicas
Mark R. Cullen
figuras
Aponte para uma miniatura para ver a legenda da figura, clique para ver a figura no contexto do artigo.
Sistema Nervoso: Visão Geral
O conhecimento do sistema nervoso em geral e do cérebro e do comportamento humano em particular são de suma importância para quem se dedica a um ambiente seguro e saudável. As condições de trabalho e as exposições que afetam diretamente as operações do cérebro influenciam a mente e o comportamento. Avaliar informações, tomar decisões e reagir de maneira consistente e razoável às percepções do mundo exige que o sistema nervoso funcione adequadamente e que o comportamento não seja prejudicado por condições perigosas, como acidentes (por exemplo, queda de um veículo mal projetado). escada) ou exposição a níveis perigosos de substâncias químicas neurotóxicas.
Danos ao sistema nervoso podem causar alterações na entrada sensorial (perda de visão, audição, olfato, etc.), podem prejudicar a capacidade de controlar o movimento e as funções do corpo e/ou podem afetar a capacidade do cérebro de tratar ou armazenar informações. Além disso, o funcionamento alterado do sistema nervoso pode causar distúrbios comportamentais ou psicológicos. Mudanças de humor e personalidade são uma ocorrência comum após danos físicos ou orgânicos ao cérebro. À medida que nosso conhecimento se desenvolve, aprendemos mais sobre a maneira como os processos do sistema nervoso são modificados. Substâncias neurotóxicas podem atravessar a barreira natural do cérebro e interferir diretamente em seu intrincado funcionamento. Embora algumas substâncias tenham uma afinidade particular com certas áreas do sistema nervoso, a maioria das neurotoxinas tem efeitos generalizados, visando os processos celulares envolvidos no transporte da membrana, reações químicas celulares internas, liberação de substâncias secretoras e assim por diante.
Danos aos vários componentes do sistema nervoso podem ocorrer de diferentes maneiras:
- lesão física direta por queda de objetos, colisões, golpes ou pressão indevida sobre os nervos
- mudanças no ambiente interno, como oxigênio insuficiente devido a asfixiantes e exposição ao calor
- interferência nos processos celulares através da ação química de substâncias, como metais, solventes orgânicos e pesticidas
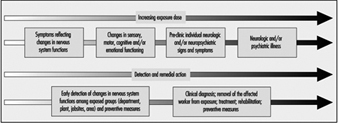
O desenvolvimento insidioso e multifacetado de muitos distúrbios do sistema nervoso exige que as pessoas que trabalham no campo da saúde ocupacional adotem abordagens diferentes, mas complementares, para o estudo, compreensão, prevenção e tratamento do problema. Alterações precoces podem ser detectadas em grupos de trabalhadores ativos e expostos por meio de medidas sensíveis de comprometimento. A identificação da disfunção inicial pode levar a ações preventivas. Nas últimas fases, é necessário um bom conhecimento clínico e o diagnóstico diferencial é essencial para o tratamento e cuidados adequados dos trabalhadores com deficiência.
Embora as substâncias químicas sejam, em sua maioria, examinadas uma a uma, deve-se lembrar que em muitos locais de trabalho são utilizadas misturas de substâncias químicas potencialmente neurotóxicas, expondo os trabalhadores ao que se pode chamar de “coquetel”. Em processos como impressão, pintura, limpeza, em escritórios mal ventilados, em laboratórios, aplicação de agrotóxicos, microeletrônica e tantos outros setores, os trabalhadores estão expostos a misturas químicas. Embora possa haver informações sobre cada uma das substâncias separadamente, devemos considerar a nocividade combinada e possíveis efeitos aditivos ou mesmo sinérgicos no sistema nervoso. Em alguns casos de exposição múltipla, cada produto químico específico pode estar presente em quantidade muito pequena, mesmo abaixo do nível de detecção das técnicas de avaliação de exposição; no entanto, quando todos são somados, a concentração total pode ser muito alta.
O leitor deve estar ciente de três grandes dificuldades em revisar fatos sobre o sistema nervoso no âmbito deste enciclopédia.
Primeiro, a compreensão das doenças ocupacionais que afetam o sistema nervoso e o comportamento mudou substancialmente à medida que novas abordagens para visualizar as relações cérebro-comportamentais foram desenvolvidas. O interesse principal pela caracterização de alterações morfológicas grosseiras que ocorrem devido a traumas mecânicos no sistema nervoso – particularmente, mas não exclusivamente no cérebro – foi seguido pelo interesse na absorção de agentes neurotóxicos pelo sistema nervoso; interesse no estudo dos mecanismos celulares da patologia do sistema nervoso; e finalmente, a busca pela base molecular desses processos patológicos começou a crescer. Essas abordagens coexistem hoje e todas contribuem com informações para avaliar as condições de trabalho que afetam o cérebro, a mente e o comportamento.
Em segundo lugar, as informações geradas pelos neurocientistas são impressionantes. A terceira edição do livro Princípios das Ciências Neurais editado por Kandel, Schwartz e Kessell que apareceu em 1991 - uma das revisões mais valiosas do campo - pesa 3.5 kg e tem mais de 1,000 páginas.
Em terceiro lugar, é muito difícil revisar o conhecimento sobre a organização funcional do sistema nervoso, uma vez que se aplica a todos os nichos de saúde e segurança ocupacional. Até cerca de 25 anos atrás, as visões teóricas que davam suporte aos especialistas em saúde preocupados, especializados na detecção, monitoramento, prevenção e tratamento clínico de um trabalhador que absorveu um agente neurotóxico, às vezes não se sobrepunham às visões teóricas sobre a saúde do trabalhador trauma cerebral e as manifestações comportamentais de dano cerebral mínimo. Manifestações comportamentais ditas como consequência da interrupção de vias químicas específicas no cérebro eram território exclusivo do neurotoxicologista; tanto danos estruturais em tecidos de regiões específicas do cérebro, quanto estruturas neurais distantes ligadas à área onde ocorreram as lesões, foram explicações invocadas por neurologistas. É apenas nos últimos anos que visões convergentes estão aparecendo.
Pensando nisso, este capítulo aborda questões importantes para a compreensão do sistema nervoso e os efeitos das condições do local de trabalho sobre seu funcionamento. Começa com uma descrição da anatomia e fisiologia, seguida por uma seção sobre neurotoxicidade, que analisa a exposição, os resultados e a prevenção.
Como o sistema nervoso é fundamental para o bem-estar do corpo, muitos perigos não químicos também podem afetar seu funcionamento normal. Muitos deles são considerados em diferentes capítulos que lidam com esses perigos. Traumatismos cranianos estão incluídos em Primeiros Socorros, o estresse térmico é considerado no artigo “Efeitos do estresse térmico e do trabalho no calor” e a doença descompressiva é revisada no artigo “Estresse gravitacional”. Vibração mão-braço (“Vibração transmitida pela mão”) e movimento repetitivo (“Resultados crônicos musculoesqueléticos”) no capítulo Sistema musculo-esquelético, que são fatores de risco para neuropatias periféricas, também são considerados nestas seções do enciclopédia.
O capítulo termina com uma revisão de questões especiais e as perspectivas para futuras avenidas de pesquisa.
Anatomia e Fisiologia
As células nervosas são as unidades funcionais do sistema nervoso. Acredita-se que o sistema nervoso tenha dez bilhões dessas células, chamadas neurônios e glia, a glia estando presente em maior número do que os neurônios.
o neurônio
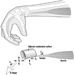
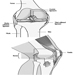
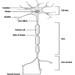
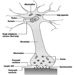
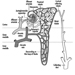
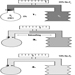
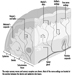
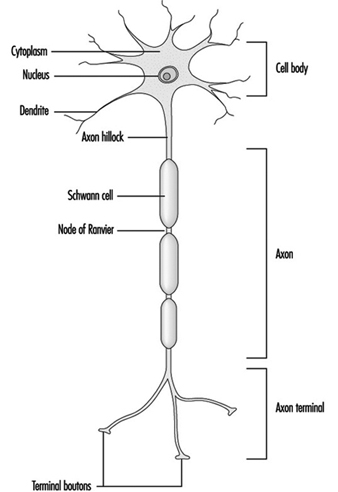
A Figura 1 é um diagrama idealizado de um neurônio com suas três características estruturais mais importantes: o corpo celular, os dendritos e o terminal axônico.
Figura 1. A anatomia do neurônio
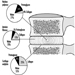
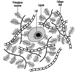
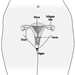
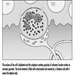
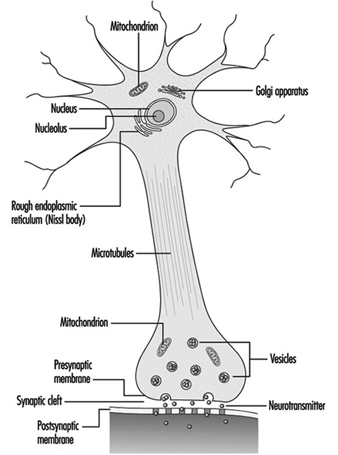
Os dendritos são processos finamente ramificados que surgem perto do corpo celular de um neurônio. Os dendritos recebem efeitos excitatórios ou inibitórios por meio de mensageiros químicos chamados neurotransmissores. O citoplasma é o material do corpo celular no qual as organelas - incluindo o núcleo da célula - e outras inclusões são encontradas Figura 2. O núcleo contém a cromatina da célula, ou material genético.
Figura 2. As organelas
O núcleo da célula nervosa é atípico em comparação com o de outras células vivas, pois, embora contenha o material genético ácido desoxirribonucléico (DNA), o DNA não está envolvido no processo de divisão celular; ou seja, após atingirem a maturidade, as células nervosas não se dividem. (Uma exceção a essa regra são os neurônios da mucosa nasal (epitélio olfatório).) O núcleo é rico em ácido ribonucléico (RNA), necessário para a síntese de proteínas. Três tipos de proteínas foram identificadas: proteínas citosólicas, que formam os elementos fibrilares da célula nervosa; proteínas intracondriais, que geram energia para a atividade celular; e proteínas que formam membranas e produtos secretores. Os neurônios são agora concebidos como células secretoras modificadas. Grânulos de secreção são formados, armazenados em vesículas sinápticas e posteriormente liberados como substâncias neurotransmissoras, os mensageiros químicos entre as células nervosas.
Os elementos fibrilares, que formam o esqueleto do neurônio, participam da função trófica do neurônio, atuando como veículos de transmissão. O transporte axonal pode ser anterógrado (corpo celular ao terminal axônico) e retrógrado (terminal axônico ao corpo celular). Do mais grosso ao mais fino, três tipos de elementos fibrilares são reconhecidos: microtúbulos, neurofilamentos e microfilamentos.
Células da glia
Em contraste com os neurônios, as células gliais não carregam, por si mesmas, mensagens elétricas. Existem dois tipos de células gliais: as macróglia e os votos de microglia. A macroglia é um nome dado a pelo menos três tipos de células: astrócitos, oligodendrócitos e células ependimárias. As células microgliais são principalmente células necrófagas para remover detritos após a ocorrência de dano neural ou infecção.
As células gliais também têm características microscópicas e ultramicroscópicas distintas. As células gliais suportam fisicamente os neurônios, mas uma série de propriedades fisiológicas também estão começando a ser compreendidas. Entre as interações neurônio-glia mais importantes está o papel da célula glial em fornecer nutrientes aos neurônios, removendo fragmentos de neurônios após sua morte e, mais importante, contribuindo para o processo de comunicação química. As células gliais, em nítido contraste com os neurônios, podem se dividir e, assim, se reproduzir. Os tumores do sistema nervoso, por exemplo, resultam de uma reprodução anormal das células da glia.
Mielina
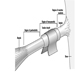
O que aparece na observação macroscópica do tecido neural como “substância cinzenta” e “substância branca” tem uma base microscópica e bioquímica. Microscopicamente, a substância cinzenta contém os corpos celulares neuronais, enquanto a substância branca é onde se encontram as fibras neurais ou axônios. A aparência “branca” se deve a uma bainha – composta por uma substância gordurosa chamada mielina – que recobre essas fibras. A mielina dos nervos periféricos origina-se da membrana da célula de Schwann que envolve o axônio. A mielina das fibras no sistema nervoso central é fornecida pelas membranas dos oligodendrócitos (uma variedade de células gliais). Os oligodendrócitos geralmente mielinizam vários axônios, enquanto a célula de Schwann está associada a apenas um axônio. Existe uma descontinuidade da bainha de mielina - designada como nódulos de Ranvier - entre células de Schwann contínuas ou oligodendrócitos. Estima-se que na via motora central mais longa, até 2,000 células de Schwann formem a cobertura de mielina. A mielina, cujo papel é facilitar a propagação do potencial de ação, pode ser um alvo específico de agentes neurotóxicos. Uma classificação morfológica das substâncias neurotóxicas descreve alterações neuropatológicas características da mielina como mielinopatias.
Função Trófica do Neurônio
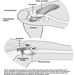
As funções normais do neurônio incluem síntese de proteínas, transporte axonal, geração e condução do potencial de ação, transmissão sináptica e formação e manutenção da mielina. Algumas das funções tróficas básicas do neurônio foram descritas já no século 19, seccionando os axônios (axotomia). Entre os processos descobertos, um dos mais importantes foi a degeneração walleriana — em homenagem a Waller, o fisiologista inglês que a descreveu.
A degeneração walleriana oferece uma boa oportunidade para descrever alterações bem conhecidas em organelas como resultado de dano traumático ou tóxico. Entre parênteses, os termos usados para descrever a degeneração walleriana produzida por axotomia traumática são os mesmos usados para descrever alterações decorrentes de agentes neurotóxicos. No nível celular, as alterações neuropatológicas resultantes do dano tóxico ao tecido neural são muito mais complexas do que aquelas que ocorrem como resultado do dano traumático. Apenas recentemente foram observadas alterações em neurônios afetados por agentes neurotóxicos.
Vinte e quatro horas após o corte do axônio, a característica mais marcante é o inchaço de ambos os lados do trauma mecânico. O inchaço resulta do acúmulo de fluidos e elementos membranosos em ambos os lados do local da lesão. Essas mudanças não são diferentes daquelas observadas em uma estrada de mão dupla inundada pela chuva com veículos parados em ambos os lados da área inundada. Nesta analogia, os veículos parados são o inchaço. Depois de alguns dias, ocorre a regeneração dos axônios revestidos - isto é, aqueles cobertos por mielina. Os brotos crescem a partir do toco proximal, movendo-se a uma taxa de 1 a 3 mm por dia. Em condições favoráveis, os brotos atingem o coto distal (mais distante do corpo celular). Quando a renervação – união dos cotos – é concluída, as características básicas da transmissão normal foram restabelecidas. O corpo celular do neurônio lesado sofre profundas alterações estruturais na síntese proteica e no transporte axonal.
Se a neurobiologia molecular é considerada uma disciplina jovem, a neurobiologia dos processos neurotóxicos é ainda mais jovem e ainda está em sua infância. É verdade que a base molecular da ação de muitas neurotoxinas e agentes farmacológicos é agora bem compreendida. Mas, com algumas exceções notáveis (por exemplo, chumbo, metilmercúrio, acrilamida), a base molecular da toxicidade da grande maioria dos agentes ambientais e neurotóxicos é desconhecida. É por isso que, em vez de descrever a neurobiologia molecular de um grupo seleto de agentes neurotóxicos ocupacionais e ambientais, ainda somos forçados a nos referir às estratégias e exemplos comparativamente abundantes da neurofarmacologia clássica ou do trabalho na fabricação de medicamentos modernos.
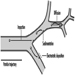
Neurotransmissores
Um neurotransmissor é uma substância química que, ao ser liberada dos terminais axônicos pelo potencial de ação, produz a mudança momentânea no potencial elétrico quando outra fibra nervosa é estimulada. Os neurotransmissores estimulam ou inibem neurônios adjacentes ou órgãos efetores, como músculos e glândulas. Neurotransmissores conhecidos e suas vias neurais estão agora sendo intensamente estudados, e novos estão sendo constantemente descobertos. Alguns distúrbios neurológicos e psiquiátricos são agora considerados causados por alterações químicas na neurotransmissão - por exemplo, miastenia grave, doença de Parkinson, certas formas de distúrbios afetivos, como depressão, distorção grave dos processos de pensamento, como na esquizofrenia e doença de Alzheimer. Embora tenham sido publicados excelentes relatos isolados sobre o efeito de vários agentes neurotóxicos ambientais e ocupacionais na neurotransmissão, o corpo de conhecimento é escasso em comparação com o existente para doenças neuropsiquiátricas. Os estudos farmacológicos de drogas manufaturadas requerem uma compreensão de como as drogas afetam a neurotransmissão. A fabricação de medicamentos e a pesquisa de neurotransmissão estão, portanto, intimamente relacionadas. As novas visões da ação das drogas foram resumidas por Feldman e Quenzer (1984).
Os efeitos dos agentes neurotóxicos na neurotransmissão são caracterizados por onde eles agem no sistema nervoso, seus receptores químicos, o curso temporal de seus efeitos, se os agentes neurotóxicos facilitam, bloqueiam ou inibem a neurotransmissão, ou se os agentes neurotóxicos alteram a terminação ou remoção do ação farmacológica do neurotransmissor.
Uma dificuldade experimentada pelos neurocientistas é a necessidade de vincular processos conhecidos que ocorrem no nível molecular no neurônio com eventos no nível celular, o que por sua vez pode explicar como ocorrem as mudanças neuropsicológicas normais e patológicas, como claramente afirmado a seguir, que a um em grande medida ainda se aplica: “(A) no nível molecular, muitas vezes é possível uma explicação da ação de uma droga; no nível celular, uma explicação às vezes é possível, mas no nível comportamental, nossa ignorância é abismal” (Cooper, Bloom e Roth 1986).
Os principais componentes do sistema nervoso
O conhecimento dos principais componentes do sistema nervoso é essencial para a compreensão das manifestações neuropsicológicas gerais da doença neurotóxica, a justificativa para o uso de técnicas específicas para a avaliação das funções do sistema nervoso e a compreensão dos mecanismos farmacológicos da ação neurotóxica. Do ponto de vista funcional, o sistema nervoso pode ser dividido em dois grandes compartimentos: sistema nervoso somático transmite informações sensoriais (toque, temperatura, dor e posição dos membros - mesmo quando os olhos estão fechados) dos segmentos corporais e carrega as vias neurais que inervam e controlam o movimento dos músculos esqueléticos, como os dos braços, dedos, pernas e dedos do pé. o sistema nervoso visceral controla os órgãos internos que normalmente não estão sob a influência dos vasos sanguíneos, a dilatação e constrição das pupilas dos olhos e assim por diante.
Do ponto de vista anatômico, quatro componentes principais precisam ser identificados: o do sistema nervoso central, sistema nervoso periférico incluindo nervos cranianos, o sistema autonômico e os votos de sistema neuroendócrino.
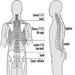
O sistema nervoso central
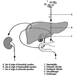
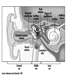
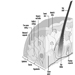
O sistema nervoso central contém o cérebro e a medula espinhal Figura 3. O cérebro fica na cavidade do crânio e é protegido pelas meninges. É dividido em três componentes principais; em ordem ascendente - isto é, da parte caudal (cauda) para a porção cervical (cabeça) do sistema nervoso - eles são o rombencéfalo (também chamado de rombencéfalo), o mesencéfalo (o mescéfalo) e o prosencéfalo (o proscencéfalo).
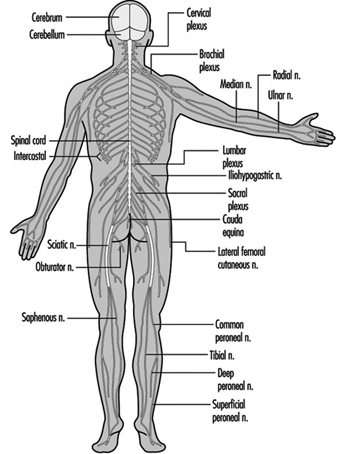
Figura 3. As divisões central e periférica do sistema nervoso
O cérebro posterior
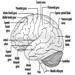
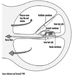
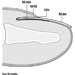
Os três principais componentes do rombencéfalo são a medula oblonga, a ponte e a figura 4 do cerebelo.
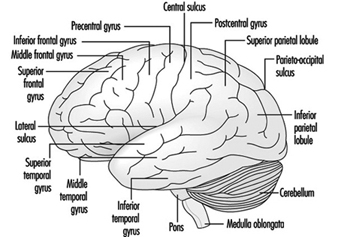
Figura 4. O cérebro mostrado de lado.
A medula oblongata contém estruturas neurais que controlam a frequência cardíaca e a respiração, às vezes alvos de agentes neurotóxicos e drogas que causam a morte. Localizada entre o bulbo e o mesencéfalo, a ponte (ponte) recebe seu nome do grande número de fibras que atravessam sua face anterior em direção aos hemisférios cerebelares. O cerebelo — em latim, pequeno cérebro — tem uma aparência caracteristicamente ondulada. O cerebelo recebe informações sensoriais e envia mensagens motoras essenciais para a coordenação motora. É responsável (entre outras funções) pela execução de movimentos finos. Essa programação - ou programação - requer o tempo adequado de entradas sensoriais e respostas motoras. O cerebelo é frequentemente alvo de numerosos agentes neurotóxicos – por exemplo, bebidas alcoólicas, muitos solventes industriais, chumbo – que afetam as respostas motoras.
O mesencéfalo
O mesencéfalo é uma parte estreita do cérebro que conecta o mesencéfalo ao prosencéfalo. As estruturas do mesencéfalo são o aqueduto cerebral, o tectum, os pedúnculos cerebrais, a substância negra e o núcleo vermelho. O aqueduto cerebral é um canal que liga o terceiro ao quarto ventrículos (cavidades do cérebro cheias de líquido); o líquido cefalorraquidiano (CSF) flui através desta abertura.
O prosencéfalo
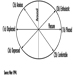
Esta parte do cérebro é subdividida em diencéfalo (“entre o cérebro”) e o cérebro. As principais regiões do diencéfalo são o tálamo e o hipotálamo. “Tálamo” significa “quarto interno”. Os tálamos são formados por agrupamentos neuronais, chamados núcleos, que possuem cinco funções principais:
- receber informações sensoriais e enviá-las para áreas primárias do córtex cerebral
- enviando informações sobre o movimento em andamento para as áreas motoras do córtex cerebral
- enviando informações sobre a atividade do sistema límbico para áreas do córtex cerebral relacionadas a esse sistema
- enviando informações sobre a atividade intratalâmica para áreas de associação do córtex cerebral
- enviando informações da atividade de formação reticular do tronco cerebral para áreas amplas do córtex cerebral.
O nome hipotálamo significa “sob o tálamo”. Ele forma a base do terceiro ventrículo, um importante ponto de referência para a geração de imagens do cérebro. O hipotálamo é uma estrutura neural complexa e diminuta responsável por muitos aspectos do comportamento, como impulsos biológicos básicos, motivação e emoção. É o elo entre o sistema nervoso e o sistema neuroendócrino, a ser analisado a seguir. A glândula pituitária (também chamada de hipófise) está ligada por neurônios aos núcleos hipotalâmicos. Está bem estabelecido que as células nervosas hipotalâmicas desempenham muitas funções neurossecretoras. O hipotálamo está ligado a muitas outras regiões importantes do cérebro, incluindo o rinencéfalo - o córtex primitivo originalmente associado ao olfato - e o sistema límbico, incluindo o hipocampo.
O córtex cerebral é o maior componente do cérebro, consistindo de dois hemisférios cerebrais conectados por uma massa de substância branca chamada corpo caloso. O córtex cerebral é a camada superficial de cada hemisfério cerebral. Sulcos profundos no córtex cerebral - os sulcos central e lateral Figura 4 - são tomados como pontos de referência para separar as regiões anatômicas do cérebro. O lobo frontal situa-se à frente do sulco central. O lobo parietal começa na parte de trás do sulco central e fica próximo ao lobo occipital, que ocupa a porção posterior do cérebro. O lobo temporal começa bem dentro da dobra do sulco lateral e se estende até os aspectos ventrais dos hemisférios cerebrais. Dois componentes importantes do cérebro são os gânglios da base e o sistema límbico.
Os gânglios da base são núcleos - isto é, aglomerados de células nervosas - localizados no centro do cérebro. Os gânglios da base compreendem os principais centros do sistema motor extrapiramidal. (O sistema piramidal, ao qual o termo é contrastado, está envolvido no controle voluntário do movimento.) O sistema extrapiramidal é afetado seletivamente por muitos agentes neurotóxicos (por exemplo, manganês). Nas últimas duas décadas, importantes descobertas foram feitas sobre o papel que esses núcleos desempenham em várias doenças degenerativas neurais (por exemplo, doença de Parkinson, coreia de Huntington).
O sistema límbico é composto de estruturas neurais complicadas que se ramificam em várias direções e estabelecem conexões com muitas regiões “antigas” do cérebro, particularmente com o hipotálamo. Está envolvido no controle da expressão emocional. Acredita-se que o hipocampo seja uma estrutura onde ocorrem muitos processos de memória.
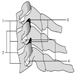
A medula espinhal
A medula espinhal é uma estrutura esbranquiçada situada dentro do canal vertebral. É dividido em quatro regiões: cervical, torácica, lombar e sacro-coccixeal. As duas características mais facilmente reconhecíveis da medula espinhal são a substância cinzenta que contém os corpos celulares dos neurônios e a substância branca que contém os axônios mielinizados dos neurônios. A região ventral da substância cinzenta da medula espinhal contém células nervosas que regulam a função motora; a região média da medula espinhal torácica está associada a funções autonômicas. A porção dorsal recebe informações sensoriais dos nervos espinhais.
O Sistema Nervoso Periférico
O sistema nervoso periférico inclui aqueles neurônios que estão fora do sistema nervoso central. O termo periférico descreve a distribuição anatômica desse sistema, mas funcionalmente é artificial. Os corpos celulares das fibras motoras periféricas, por exemplo, estão localizados no sistema nervoso central. Em neurotoxicologia experimental, clínica e epidemiológica, o termo sistema nervoso periférico (PNS) descreve um sistema que é seletivamente vulnerável aos efeitos de agentes tóxicos e que é capaz de se regenerar.
Os nervos espinhais
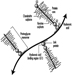
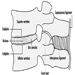
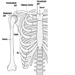
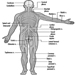
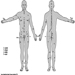
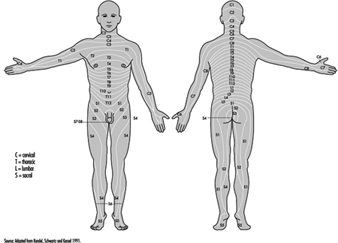
As raízes ventrais e dorsais são onde os nervos periféricos entram e saem da medula espinhal ao longo de sua extensão. As vértebras adjacentes contêm aberturas para permitir que as fibras das raízes que formam os nervos espinhais saiam do canal espinhal. Existem 31 pares de nervos espinhais, que são nomeados de acordo com a região da coluna vertebral à qual estão associados: 8 cervicais, 12 torácicos, 5 lombares, 5 sacrais e 1 coccixeal. Um metámero é uma região do corpo inervada por um nervo espinhal figura 5.
Figura 5. A distribuição segmentar dos nervos espinais (os metámeros).
Examinando cuidadosamente as funções motoras e sensoriais dos metámeros, os neurologistas podem inferir a localização das lesões onde ocorreu o dano.
Tabela 1. Nomes e principais funções de cada par de nervos cranianos
| Nervo1 | Conduz impulsos | Funções |
| I. Olfativo | Do nariz ao cérebro | Sentido de olfato |
| II. Ótico | Do olho ao cérebro | Visão |
| III. Oculomotor | Do cérebro aos músculos oculares | Movimentos oculares |
| XNUMX. Troclear | Do cérebro aos músculos oculares externos | Movimentos oculares |
| V. Trigêmeo (ou trifacial) |
Da pele e membrana mucosa da cabeça e dos dentes ao cérebro; também do cérebro aos músculos da mastigação | Sensações da face, couro cabeludo e dentes; movimentos de mastigação |
| VI. abducente | Do cérebro aos músculos oculares externos | Virando os olhos para fora |
| VII. Facial | Das papilas gustativas da língua ao cérebro; do cérebro aos músculos do rosto | Sentido do paladar; contração dos músculos da expressão facial |
| VIII. Acústico | De orelha a cérebro | Audição; senso de equilíbrio |
| IX. glossofaríngeo | Da garganta e papilas gustativas da língua ao cérebro; também do cérebro aos músculos da garganta e glândulas salivares | Sensações de garganta, paladar, movimentos de deglutição, secreção de saliva |
| X. Vago | Da garganta, laringe e órgãos nas cavidades torácica e abdominal ao cérebro; também do cérebro aos músculos da garganta e aos órgãos nas cavidades torácica e abdominal | Sensações da garganta, laringe e órgãos torácicos e abdominais; deglutição, produção de voz, desaceleração dos batimentos cardíacos, aceleração do peristaltismo |
| XI. Acessório espinhal | Do cérebro a certos músculos do ombro e pescoço | Movimentos do ombro; movimentos de rotação da cabeça |
| XII. hipoglosso | Do cérebro aos músculos da língua | Movimentos da língua |
1 A primeira letra das palavras da frase a seguir são as primeiras letras dos nomes dos nervos cranianos: “Nos topos minúsculos do Velho Olimpo, um finlandês e um alemão viram alguns saltos”. Muitas gerações de estudantes usaram esta ou uma frase semelhante para ajudá-los a lembrar os nomes dos nervos cranianos.
Os nervos cranianos
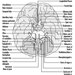
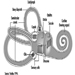
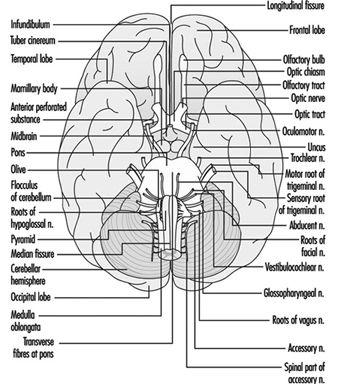
Tronco cerebral é um termo abrangente que designa a região do sistema nervoso que inclui o bulbo, a ponte e o mesencéfalo. O tronco cerebral é uma continuação da medula espinhal para cima e para frente (ventralmente). É nessa região que a maioria dos nervos cranianos fazem suas saídas e entradas. Existem 12 pares de nervos cranianos; A Tabela 1 descreve o nome e a função principal de cada par e a Figura 6 mostra a entrada e saída de alguns nervos cranianos no cérebro.
Figura 6. O cérebro mostrado de baixo com a entrada e saída de muitos nervos cranianos.
O Sistema Nervoso Autônomo
O sistema nervoso autônomo é a parte do sistema nervoso que controla a atividade dos componentes viscerais do corpo humano. É chamado de “autônomo” porque executa suas funções automaticamente, o que significa que seu funcionamento não pode ser facilmente controlado à vontade. Do ponto de vista anatômico, o sistema autônomo possui dois componentes principais: o sistema nervoso simpático e o parassimpático. Os nervos simpáticos que controlam a atividade visceral surgem das porções torácica e lombar da medula espinal; nervos parassimpáticos originam-se do tronco encefálico e da porção sacral da medula espinhal.
Do ponto de vista fisiológico, não se pode fazer uma única generalização que se aplique à maneira pela qual os sistemas nervosos simpático e parassimpático controlam os diferentes órgãos do corpo. Na maioria dos casos, os órgãos viscerais são inervados por ambos os sistemas, e cada tipo tem um efeito oposto em um sistema de freios e contrapesos. O coração, por exemplo, é inervado por nervos simpáticos cuja excitação produz uma aceleração do batimento cardíaco e por nervos parassimpáticos cuja excitação produz uma desaceleração do batimento cardíaco. Qualquer sistema pode estimular ou inibir os órgãos que inerva. Em outros casos, os órgãos são predominantemente ou exclusivamente controlados por um ou outro sistema. Uma função vital do sistema nervoso autônomo é a manutenção da homeostase (estado estável de equilíbrio) e para a adaptação do corpo animal ao seu ambiente externo. A homeostase é o estado de equilíbrio das funções corporais alcançado por um processo ativo; o controle da temperatura corporal, água e eletrólitos são exemplos de processos homeostáticos.
Do ponto de vista farmacológico, não existe um único neurotransmissor associado às funções simpática ou parassimpática, como se acreditava. A velha visão de que a acetilcolina era o transmissor predominante do sistema autônomo teve que ser abandonada quando novas classes de neurotransmissores e neuromoduladores foram encontradas (por exemplo, dopamina, serotonina, purinas e vários neuropeptídeos).
Os neurocientistas reviveram recentemente o ponto de vista comportamental do sistema nervoso autônomo. O sistema nervoso autônomo está envolvido na reação instintiva de luta ou fuga ainda presente nos seres humanos, que é, em grande parte, a base das reações fisiológicas causadas pelo estresse. As interações entre o sistema nervoso e as funções imunológicas são possíveis através do sistema nervoso autônomo. As emoções que se originam do sistema nervoso autônomo podem ser expressas por meio dos músculos esqueléticos.
O controle autonômico dos músculos lisos
Os músculos das vísceras - exceto o coração - são os músculos lisos. O músculo cardíaco tem características de músculo esquelético e liso. Assim como os músculos esqueléticos, os músculos lisos também contêm as duas proteínas actina e, em proporções menores, miosina. Ao contrário dos músculos esqueléticos, eles não apresentam a organização regular dos sarcolemas, a unidade contrátil da fibra muscular. O coração é o único que pode gerar atividade miogênica - mesmo depois que suas inervações neurais foram cortadas, ele pode se contrair e relaxar por várias horas sozinho.
O acoplamento neuromuscular nos músculos lisos difere daquele dos músculos esqueléticos. Nos músculos esqueléticos, a junção neuromuscular é a ligação entre o nervo e as fibras musculares. No músculo liso, não há junção neuromuscular; as terminações nervosas entram no músculo, espalhando-se em todas as direções. Os eventos elétricos dentro do músculo liso, portanto, são muito mais lentos do que aqueles nos músculos esqueléticos. Finalmente, o músculo liso tem a característica única de exibir contrações espontâneas, como a exibida pelo intestino. Em grande parte, o sistema nervoso autônomo regula a atividade espontânea dos músculos lisos.
Os componentes centrais do sistema nervoso autônomo
O principal papel do sistema nervoso autônomo é regular a atividade dos músculos lisos, do coração, das glândulas do trato digestivo, das glândulas sudoríparas, das glândulas supra-renais e de outras glândulas endócrinas. O sistema nervoso autônomo tem um componente central – o hipotálamo, localizado na base do cérebro – onde muitas funções autônomas são integradas. Mais importante ainda, os componentes centrais do sistema autônomo estão diretamente envolvidos na regulação de impulsos biológicos (regulação de temperatura, fome, sede, sexo, micção, defecação e assim por diante), motivação, emoção e, em grande medida, em funções “psicológicas”. como humores, afetos e sentimentos.
Sistema Neuroendócrino
As glândulas são os órgãos do sistema endócrino. Elas são chamadas de glândulas endócrinas porque suas mensagens químicas são entregues dentro do corpo, diretamente na corrente sanguínea (em contraste com as glândulas exócrinas, como as glândulas sudoríparas, cujas secreções aparecem na superfície externa do corpo). O sistema endócrino fornece controle lento, mas duradouro, sobre órgãos e tecidos por meio de mensageiros químicos chamados hormônios. Os hormônios são os principais reguladores do metabolismo corporal. Mas, por causa das ligações íntimas entre os sistemas nervoso central, periférico e autônomo, o sistema neuroendócrino—um termo que capta ligações tão complexas—é agora concebido como um poderoso modificador da estrutura e função do corpo humano e do comportamento.
Os hormônios foram definidos como mensageiros químicos que são liberados das células na corrente sanguínea para exercer sua ação nas células-alvo a alguma distância. Até recentemente, os hormônios eram distinguidos dos neurotransmissores, discutidos acima. Os últimos são mensageiros químicos liberados dos neurônios em uma sinapse entre os terminais nervosos e outro neurônio ou um efetor (ou seja, músculo ou glândula). No entanto, com a descoberta de que os neurotransmissores clássicos, como a dopamina, também podem atuar como hormônios, a distinção entre neurotransmissores e hormônios tornou-se cada vez menos clara. Assim, com base em considerações puramente anatômicas, os hormônios derivados das células nervosas podem ser chamados de neuro-hormônios. Do ponto de vista funcional, o sistema nervoso pode ser pensado como um verdadeiro sistema neurossecretor.
O hipotálamo controla as funções endócrinas através de uma ligação com a glândula pituitária (também chamada de hipófise, uma pequena glândula localizada na base do cérebro). Até meados da década de 1950, as glândulas endócrinas eram vistas como um sistema separado governado pela glândula pituitária, muitas vezes chamada de “glândula mestra”. Nessa época, foi avançada uma hipótese neurovascular que estabeleceu o papel funcional dos fatores hipotalâmicos/hipofisários no controle da função endócrina. Nessa visão, o hipotálamo endócrino fornece a via neuroendócrina comum final no controle do sistema endócrino. Agora está firmemente estabelecido que o próprio sistema endócrino é regulado pelo sistema nervoso central, bem como pelas entradas endócrinas. Desta forma, neuroendocrinologia é agora um termo apropriado para descrever a disciplina que estuda os papéis integrados recíprocos dos sistemas nervoso e endócrino no controle dos processos fisiológicos.
Com o aumento da compreensão da neuroendocrinologia, as divisões originais estão se desfazendo. O hipotálamo, localizado acima e conectado à glândula pituitária, é o elo entre os sistemas nervoso e endócrino, e muitas de suas células nervosas desempenham funções secretoras. Também está ligado a outras regiões importantes do cérebro, incluindo o rinencéfalo – o córtex primitivo originalmente associado ao olfato ou ao olfato – e o sistema límbico, associado às emoções. É no hipotálamo que são produzidos os hormônios liberados pela hipófise posterior. O hipotálamo também produz substâncias que são chamadas de hormônios liberadores e inibidores. Estes atuam na adeno-hipófise, fazendo com que ela potencialize ou iniba a produção de hormônios da hipófise anterior, que atuam sobre as glândulas localizadas em outras regiões (tireoide, córtex adrenal, ovários, testículos e outras).
Agentes Químicos Neurotóxicos
Definição de neurotoxicidade
Neurotoxicidade refere-se à capacidade de induzir efeitos adversos no sistema nervoso central, nervos periféricos ou órgãos sensoriais. Um produto químico é considerado neurotóxico se for capaz de induzir um padrão consistente de disfunção neural ou alteração na química ou estrutura do sistema nervoso.
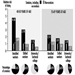
A neurotoxicidade geralmente se manifesta como um continuum de sintomas e efeitos, que dependem da natureza do produto químico, da dose, da duração da exposição e das características do indivíduo exposto. A gravidade dos efeitos observados, bem como a evidência de neurotoxicidade, aumenta dos níveis 1 a 6, mostrados na Tabela 1. A exposição de curto prazo ou de baixa dose a um produto químico neurotóxico pode resultar em sintomas subjetivos, como dor de cabeça e tontura, mas o efeito geralmente é reversível. Com o aumento da dose, podem aparecer alterações neurológicas e, eventualmente, gerar alterações morfológicas irreversíveis. O grau de anormalidade necessário para implicar a neurotoxicidade de um agente químico é uma questão controversa. De acordo com a definição, um padrão consistente de disfunção neural ou alteração na química ou estrutura do sistema nervoso é considerado se houver evidência bem documentada de efeitos persistentes nos níveis 3, 4, 5 ou 6 na Tabela 1. Esses níveis refletem o peso da evidência fornecida por diferentes sinais de neurotoxicidade. Substâncias neurotóxicas incluem elementos naturais como chumbo, mercúrio e manganês; compostos biológicos como tetrodotoxina (do baiacu, uma iguaria japonesa) e ácido domóico (de mexilhões contaminados); e compostos sintéticos, incluindo muitos pesticidas, solventes industriais e monômeros.
Tabela 1. Agrupamento de efeitos neurotóxicos para refletir sua força relativa para estabelecer a neurotoxicidade
|
Nível |
Agrupamento |
Explicação/Exemplos |
|
6 |
Mudanças morfológicas |
Alterações morfológicas incluem morte celular e axonopatia, bem como alterações morfológicas subcelulares. |
|
5 |
Mudanças neurológicas |
A alteração neurológica abrange achados anormais em exames neurológicos em indivíduos individuais. |
|
4 |
Alterações fisiológicas/comportamentais |
Alterações fisiológicas/comportamentais compreendem achados experimentais em grupos de animais ou humanos, como alterações em potenciais evocados e EEG, ou alterações em testes psicológicos e comportamentais. |
|
3 |
Mudanças bioquímicas |
Alterações bioquímicas abrangem alterações em parâmetros bioquímicos relevantes (por exemplo, nível do transmissor, conteúdo de proteína GFA (proteína glial fibrilar ácida) ou atividades enzimáticas). |
|
21 |
Sintomas subjetivos irreversíveis |
Sintomas subjetivos. Nenhuma evidência de anormalidade no exame neurológico, psicológico ou outro exame médico. |
|
11 |
Sintomas subjetivos reversíveis |
Sintomas subjetivos. Nenhuma evidência de anormalidade no exame neurológico, psicológico ou outro exame médico. |
1 apenas humanos
Fonte: Modificado de Simonsen et al. 1994.
Nos Estados Unidos, entre 50,000 e 100,000 produtos químicos estão no comércio, e 1,000 a 1,600 novos produtos químicos são enviados para avaliação a cada ano. Mais de 750 produtos químicos e várias classes ou grupos de compostos químicos são suspeitos de serem neurotóxicos (O'Donoghue 1985), mas a maioria dos produtos químicos nunca foi testada quanto a propriedades neurotóxicas. A maioria dos produtos químicos neurotóxicos conhecidos disponíveis hoje foram identificados por relatos de casos ou por acidentes.
Embora produtos químicos neurotóxicos sejam frequentemente produzidos para atender a usos específicos, a exposição pode surgir de várias fontes – uso em residências particulares, na agricultura e nas indústrias, ou de água potável poluída e assim por diante. Preconceitos fixos a priori sobre quais compostos neurotóxicos devem ser encontrados em quais ocupações devem, portanto, ser vistos com cautela, e as citações a seguir devem ser consideradas como possíveis exemplos, incluindo alguns dos produtos químicos neurotóxicos mais comuns (Arlien-Søborg 1992; O 'Donoghue 1985; Spencer e Schaumburg 1980; OMS 1978).
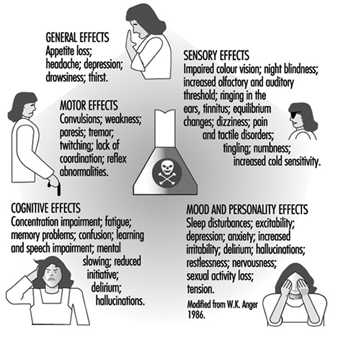
Sintomas de neurotoxicidade
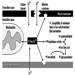
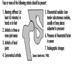
O sistema nervoso geralmente reage de forma bastante estereotipada à exposição a substâncias neurotóxicas Figura 1. Algumas síndromes típicas são indicadas abaixo.
Figura 1. Efeitos neurológicos e comportamentais da exposição a produtos químicos neurotóxicos.
Polineuropatia
Isso é causado pelo comprometimento da função nervosa motora e sensorial levando à fraqueza dos músculos, com paresia geralmente mais pronunciada perifericamente nas extremidades superiores e inferiores (mãos e pés). Pode ocorrer parestesia prévia ou simultânea (formigamento ou dormência nos dedos das mãos e dos pés). Isso pode levar a dificuldades na caminhada ou na coordenação fina das mãos e dedos. Metais pesados, solventes e pesticidas, entre outros produtos químicos, podem resultar em tal incapacidade, mesmo que o mecanismo tóxico desses compostos seja totalmente diferente.
Encefalopatia
Isso é causado por um comprometimento difuso do cérebro e pode resultar em fadiga; comprometimento da aprendizagem, memória e capacidade de concentração; ansiedade, depressão, aumento da irritabilidade e instabilidade emocional. Tais sintomas podem indicar distúrbio cerebral degenerativo difuso precoce, bem como encefalopatia tóxica crônica ocupacional. Muitas vezes, o aumento da frequência de dores de cabeça, tonturas, alterações no padrão de sono e redução da atividade sexual também podem estar presentes desde os estágios iniciais da doença. Esses sintomas podem se desenvolver após exposição prolongada e de baixo nível a vários produtos químicos diferentes, como solventes, metais pesados ou sulfeto de hidrogênio, e também são observados em vários distúrbios demenciais não relacionados ao trabalho. Em alguns casos, sintomas neurológicos mais específicos podem ser observados (por exemplo, parkinsonismo com tremor, rigidez dos músculos e lentidão dos movimentos ou sintomas cerebelares, como tremor e coordenação reduzida dos movimentos das mãos e da marcha). Tais quadros clínicos podem ser vistos após a exposição a alguns produtos químicos específicos, como manganês ou MPTP (1-metil-4-fenil-1,2,3,6-tetra-hidropiridina) na primeira condição, e tolueno ou mercúrio na segunda.
gases
Uma grande variedade de produtos químicos com estruturas químicas totalmente diferentes são gases em temperatura normal e comprovadamente neurotóxicos. Tabela 3. Alguns deles são extremamente tóxicos mesmo em doses muito pequenas, e foram usados até mesmo como gases de guerra (fosgênio e cianeto); outros requerem altas doses por períodos mais longos para causar sintomas (por exemplo, dióxido de carbono). Alguns são usados para anestesia geral (por exemplo, óxido nitroso); outros são amplamente utilizados na indústria e em agentes usados para desinfecção (por exemplo, formaldeído). O primeiro pode induzir alterações irreversíveis no sistema nervoso após exposição repetida a baixos níveis, o segundo aparentemente produz apenas sintomas agudos. A exposição em salas pequenas com pouca ventilação é particularmente perigosa. Alguns dos gases são inodoros, o que os torna particularmente perigosos (por exemplo, monóxido de carbono). Conforme mostrado na Tabela 2, alguns gases são constituintes importantes na produção industrial, enquanto outros são resultado de combustão incompleta ou completa (por exemplo, CO e CO2 respectivamente). Isso é visto em minas, siderúrgicas, usinas elétricas e assim por diante, mas também pode ser visto em residências particulares com ventilação insuficiente. Essencial para o tratamento é interromper a exposição e fornecer ar fresco ou oxigênio e, em casos graves, ventilação artificial.
Tabela 2. Gases associados a efeitos neurotóxicos
|
Produtos Químicos |
Exemplos de fonte de exposição |
Setores selecionados em risco |
Efeito1 |
|
Dióxido de carbono (CO2 ) |
Soldagem; fermentação; fabricação, armazenamento e uso de gelo seco |
Indústria metalúrgica; mineração; cervejarias |
M: Vasos dilatados A: Dor de cabeça; dispneia; tremor; perda de consciência C: Quase nenhum |
|
Monóxido de carbono (CO) |
Reparo do carro; Soldagem; fusão de metais; motoristas; bombeiros |
Indústria metalúrgica; mineração; transporte; estação de energia |
M: Privação de oxigênio A: Dor de cabeça; sonolência; perda de consciência |
|
Sulfeto de hidrogênio (H2S) |
Fumigação de casa verde; estrume; pescadores; desembarque de pescado; tratamento de esgoto |
Agricultura; pescaria; trabalho de esgoto |
M: Bloqueio do metabolismo oxidativo A: Perda de consciência C: Encefalopatia |
|
Cianeto (HCN) |
Electro-soldagem; tratamento superficial galvânico com níquel; cobre e prata; fumigação de navios, casas, alimentos e solo em estufas |
Indústria metalúrgica; indústria química; berçário; mineração; fábrica de gás |
M: Bloqueio de enzimas respiratórias A: Dispneia; queda da pressão arterial; convulsões; perda de consciência; morte C: Encefalopatia; ataxia; neuropatia (por exemplo, depois de comer cavasava) Incapacidade ocupacional incerta |
|
Óxido nitroso (N2O) |
Anestesia geral durante a operação; narcose leve no atendimento odontológico e no parto |
Hospitais (anestesia); Dentistas; parteira |
M: Alteração aguda na membrana das células nervosas; degeneração das células nervosas após exposição prolongada A: Tontura; sonolência; perda de consciência C: Dormência dos dedos das mãos e dos pés; coordenação reduzida; encefalopatia |
1 M: mecanismo; A: efeitos agudos; C: efeitos crônicos.
Neuropatia: disfunção das fibras nervosas periféricas motoras e sensitivas.
Encefalopatia: disfunção cerebral devido ao comprometimento generalizado do cérebro.
Ataxia: coordenação motora prejudicada.
Metais
Via de regra, a toxicidade dos metais aumenta com o aumento do peso atômico, sendo o chumbo e o mercúrio particularmente tóxicos. Os metais geralmente são encontrados na natureza em baixas concentrações, mas em certas indústrias são utilizados em grandes quantidades (ver Tabela 3) e podem acarretar riscos ocupacionais para os trabalhadores. Além disso, quantidades consideráveis de metais são encontradas nas águas residuais e podem gerar riscos ambientais para os moradores próximos às usinas, mas também a distâncias maiores. Frequentemente, os metais (ou, por exemplo, compostos orgânicos de mercúrio) são absorvidos pela cadeia alimentar e se acumulam em peixes, pássaros e animais, representando um risco para os consumidores. A toxicidade e a forma como os metais são manipulados pelo organismo podem depender da estrutura química. Metais puros podem ser absorvidos por inalação ou contato com a pele de vapor (mercúrio) e/ou pequenas partículas (chumbo) ou oralmente (chumbo). Compostos inorgânicos de mercúrio (por exemplo, HgCl2) são absorvidos principalmente pela boca, enquanto os compostos de metal orgânico (por exemplo, chumbo tetraetila) são absorvidos principalmente por inalação ou contato com a pele. A carga corporal pode, até certo ponto, ser refletida na concentração de metal no sangue ou na urina. Esta é a base para o monitoramento biológico. No tratamento, deve-se lembrar que especialmente o chumbo é liberado muito lentamente dos depósitos no corpo. A quantidade de chumbo nos ossos normalmente será reduzida em apenas 50% em 10 anos. Essa liberação pode ser acelerada pelo uso de agentes quelantes: BAL (dimercapto-1-propanol), Ca-EDTA ou penicilamina.
Tabela 3. Metais e seus compostos inorgânicos associados à neurotoxicidade
|
Produtos Químicos |
Exemplos de fonte de exposição |
Setores selecionados em risco |
Efeito1 |
|
Conduzir |
Derretendo; de solda; esmerilhamento; reparar; envidraçamento; plastificante |
Metalurgia; mineração; plantas acumuladoras; reparo do carro; estaleiros; trabalhadores de vidro; cerâmica; cerâmica; plástico |
M: Comprometimento do metabolismo oxidativo das células nervosas e da glia A: Dor abdominal; dor de cabeça; encefalopatia; convulsões C: Encefalopatia; polineuropatia, incluindo mão caída |
|
Mercúrio Elemental |
Eletrólise; instrumentos elétricos (giroscópio; manômetro; termômetro; bateria; lâmpada elétrica; tubos, etc.); enchimento de amálgama |
plantas cloralcalinas; mineração; eletrônicos; odontologia; produção de polímeros; indústria de papel e celulose |
M: Comprometimento em vários locais nas células nervosas A: Inflamação pulmonar; dor de cabeça; fala prejudicada C: Inflamação das gengivas; perda de apetite; encefalopatia; incluindo tremor; irritabilidade |
|
Calomelano Hg2Cl2 |
Laboratórios |
A: Efeitos tóxicos crônicos de baixa toxicidade aguda, ver acima |
|
|
Sublimar HgCl2 |
Sistema de Certificação |
Hospitais; clínicas; laboratórios |
M: Degeneração renal tubular e glomerular aguda. Muito tóxico mesmo em pequenas doses orais, letal até 30 mg/kg de peso C: Veja acima. |
|
Manganês |
Fusão (liga de aço); corte; soldagem em aço; baterias secas |
mineração de manganês; produção de aço e alumínio; indústria metalúrgica; produção de baterias; indústria química; olaria |
M: Desconhecido, possíveis alterações na dopamina e catecolamina nos gânglios da base no centro do cérebro A: Disforia C: Encefalopatia incluindo Parkinsonismo; psicose; perda de apetite; irritabilidade; dor de cabeça; fraqueza |
|
alumínio |
Metalurgia; esmerilhamento; polimento |
Indústria metal |
M: Desconhecido C: Possivelmente encefalopatia |
1 M: mecanismo; A: efeitos agudos; C: efeitos crônicos.
Neuropatia: disfunção das fibras nervosas periféricas motoras e sensitivas.
Encefalopatia: disfunção cerebral devido ao comprometimento generalizado do cérebro.
Monômeros
Os monômeros constituem um grupo grande e heterogêneo de produtos químicos reativos usados para síntese química e produção de polímeros, resinas e plásticos. Os monômeros compreendem compostos aromáticos polihalogenados, como p-clorobenzeno e 1,2,4-triclorobenzeno; solventes orgânicos insaturados, como estireno e viniltolueno, acrilamida e compostos relacionados, fenóis, ɛ-caprolactama e ζ-aminobutirolactama. Alguns dos monômeros neurotóxicos amplamente utilizados e seus efeitos sobre o sistema nervoso estão listados na Tabela 3. A exposição ocupacional a monômeros neurotóxicos pode ocorrer nas indústrias de fabricação, transporte e uso de produtos químicos e plásticos. Durante o manuseio de polímeros contendo monômeros de repouso e durante a moldagem em estaleiros e em clínicas odontológicas, ocorre uma exposição substancial a monômeros neurotóxicos. Após a exposição a esses monômeros, a absorção pode ocorrer durante a inalação (por exemplo, dissulfeto de carbono e estireno) ou por contato com a pele (por exemplo, acrilamida). Como os monômeros são um grupo heterogêneo de produtos químicos, vários mecanismos diferentes de toxicidade são prováveis. Isso se reflete nas diferenças nos sintomas (Tabela 4).
Tabela 4. Monômeros neurotóxicos
|
Compound |
Exemplos de fonte de exposição |
Setores selecionados em risco |
Efeito1 |
|
Acrilamida |
Funcionários expostos ao monômero |
Produção de polímeros; operações de escavação e perfuração |
M: Transporte axonal prejudicado C: Polineuropatia; tontura; tremor e ataxia |
|
Acrilonitrilo |
Acidentes em laboratórios e indústrias; fumigação da casa |
Produção de polímeros e borracha; síntese química |
A: Hiperexcitabilidade; salivação; vômito; cianose; ataxia; dificuldade para respirar |
|
Dissulfeto de carbono |
Produção de borracha e rayon de viscose |
Indústrias de rayon de borracha e viscose |
M: É provável que o transporte axonal prejudicado e a atividade enzimática C: Neuropatia periférica; encefalopatia; dor de cabeça; vertigem; distúrbios gastrointestinais |
|
Estireno |
Produção de plásticos reforçados com fibra de vidro; fabricação e transporte de monômeros; uso de resinas e revestimentos contendo estireno |
Indústria química; produção de fibra de vidro; indústria de polímeros |
M: Desconhecido A: Depressão do sistema nervoso central; dor de cabeça C: Polineuropatia; encefalopatia; Perda de audição |
|
viniltolueno |
Produção de resina; compostos inseticidas |
Indústria química e de polímeros |
C: Polineuropatia; redução da velocidade de condução nervosa motora |
1 M: mecanismo; A: efeitos agudos; C: efeitos crônicos.
Neuropatia: disfunção das fibras nervosas periféricas motoras e sensitivas.
Encefalopatia: disfunção cerebral devido ao comprometimento generalizado do cérebro.
Ataxia: coordenação motora prejudicada.
Solventes orgânicos
Solventes orgânicos é uma designação comum para um grande grupo de mais de 200 compostos químicos lipofílicos capazes de dissolver gorduras, óleos, ceras, resinas, borracha, asfalto, filamentos de celulose e materiais plásticos. Geralmente são fluidos à temperatura ambiente com pontos de ebulição abaixo de 200 a 250°C e são facilmente evaporados. Eles são absorvidos principalmente pelos pulmões, mas alguns também podem penetrar na pele. Devido à sua lipofilicidade, eles são distribuídos para órgãos ricos em gordura. Assim, altas concentrações são encontradas na gordura corporal, medula óssea, fígado e cérebro, que também podem atuar como reservatórios de solventes. O coeficiente de partição octanol/água pode indicar se altas concentrações cerebrais são esperadas. O mecanismo de toxicidade ainda não é conhecido, mas várias possibilidades foram vislumbradas: bloquear enzimas importantes na quebra metabólica da glicose e, assim, reduzir a energia disponível para o processamento neuronal; reduzindo a formação de energia nas mitocôndrias; alteração das membranas neuronais, levando ao comprometimento da função do canal iônico; lentificação do fluxo axonal. O cloreto de metileno é metabolizado em CO, que bloqueia o transporte de oxigênio no sangue. Grandes grupos de trabalhadores em uma grande variedade de profissões são expostos diariamente ou pelo menos com frequência (ver Tabela 5). Em alguns países, o consumo de solventes orgânicos diminuiu em algumas ocupações devido a melhorias higiênicas e substituição (por exemplo, pintores de casas, trabalhadores da indústria gráfica, metalúrgicos), enquanto em outras ocupações o padrão de exposição mudou, mas a quantidade total de solventes orgânicos permaneceu inalterado. Por exemplo, o tricloroetileno foi substituído por 1,1,1-tricloroetano e freon. Portanto, os solventes ainda são um grande problema de higiene em muitos locais de trabalho. As pessoas correm um risco particular quando expostas em salas pequenas com pouca ventilação e com alta temperatura, aumentando a evaporação. O trabalho físico aumenta a captação pulmonar de solventes. Em vários países (em particular nos países nórdicos), foram concedidas indenizações a trabalhadores que desenvolveram encefalopatia tóxica crônica após exposição prolongada e de baixo nível a solventes.
Tabela 5. Solventes orgânicos associados à neurotoxicidade
|
Produtos Químicos |
Exemplos de fonte de exposição |
Setores selecionados em risco |
Efeito1 |
|
Hidrocarbonetos clorados: tricloroetileno; 1,1,1-tricloroetano; tetracloroetileno |
Desengordurante; galvanoplastia; quadro; impressão; limpeza; anestesia geral e leve |
Indústria metalúrgica; indústria gráfica; indústria eletrônica; lavanderias a seco; anestesistas |
M: Desconhecido A: Sintomas pré-narcóticos C: Encefalopatia; polineuropatia; afecção do trigêmeo (TRI); Perda de audição |
|
Cloreto de metileno |
Extração, incluindo extração de cafeína; Removedor de tinta |
Indústria alimentícia; pintores; indústria gráfica |
M: Metabolismo ® CO A: Sintomas pré-narcóticos; coma C: Encefalopatia |
|
Cloreto de metila |
Produção e reparação de frigoríficos |
Frigorífico produção; indústria da borracha; indústria de plástico |
M: Desconhecido A: Sintomas pré-narcóticos; perda de consciência; morte C: Encefalopatia |
|
Tolueno |
Impressão; limpeza; desengordurante; galvanoplastia; quadro; pintura em spray |
Indústria gráfica; indústria eletrônica |
M: Desconhecido A: Sintomas pré-narcóticos C: Encefalopatia; disfunção cerebelar; polineuropatia; Perda de audição; Distúrbio visual |
|
xileno |
Impressão; síntese de anidrido ftálico; quadro; procedimentos laboratoriais de histologia |
Indústria gráfica; indústria de plástico; laboratórios de histologia |
M: Desconhecido A: Sintomas pré-narcóticos C: Encefalopatia; Distúrbio visual; Perda de audição |
|
Estireno |
Polimerização; moldagem |
Indústria de plástico; produção de fibra de vidro |
M: Desconhecido A: Sintomas pré-narcóticos C: Encefalopatia; polineuropatia; Perda de audição |
|
Hexacarbonos: n-hexano; metil butil cetona (MBK); metiletilcetona (MEK) |
Colagem; impressão; revestimento plástico; quadro; Extração |
Indústria de couro e calçados; indústria gráfica; pintor; laboratórios |
M: Comprometimento do transporte axonal A: Pré-narcótico C: Polineuropatia; encefalopatia |
|
Vários solventes: Freon 113 |
Produção e reparação de frigoríficos; limpeza à seco; desengordurante |
Frigorífico produção; indústria metalúrgica; indústria eletrônica; limpeza à seco |
M: Desconhecido A: Sintomas pré-narcóticos leves C: Encefalopatia |
|
éter dietílico; halotano |
Anestésicos gerais (enfermeiros; médicos) |
Hospitais; clínicas |
M: Desconhecido A: Sintomas pré-narcóticos C: Encefalopatia |
|
Dissulfeto de carbono |
Ver monômeros |
Ver monômeros |
Ver monômeros |
|
Misturas: white spirit e diluente |
Quadro; desengordurante; limpeza; impressão; impregnação; tratamento da superfície |
Indústria metalúrgica; indústria gráfica; indústria madeireira; pintores |
M: Desconhecido A: Sintomas pré-narcóticos C: Encefalopatia |
1 M: mecanismo; A: efeitos agudos; C: efeitos crônicos.
Neuropatia: disfunção das fibras nervosas periféricas motoras e sensitivas.
Encefalopatia: disfunção cerebral devido ao comprometimento generalizado do cérebro
Pesticidas
Pesticidas é usado como um termo genérico para qualquer produto químico projetado para matar grupos de plantas ou animais que são um perigo para a saúde humana ou podem causar perdas econômicas. Inclui inseticidas, fungicidas, raticidas, fumigantes e herbicidas. Aproximadamente 5 bilhões de libras de produtos pesticidas compostos por mais de 600 ingredientes ativos de pesticidas são usados anualmente na agricultura em todo o mundo. Pesticidas organofosforados, carbamatos e organoclorados, juntamente com piretróides, herbicidas clorofenoxi e compostos de metais orgânicos usados como fungicidas, possuem propriedades neurotóxicas (Tabela 6). Entre os diversos produtos químicos usados como raticidas, alguns (por exemplo, estricnina, fosfeto de zinco e tálio) também são neurotóxicos. A exposição ocupacional a pesticidas neurotóxicos está principalmente associada ao trabalho agrícola, como manuseio de pesticidas e trabalho com culturas tratadas, mas exterminadores, funcionários de fabricação e formulação de pesticidas, trabalhadores rodoviários e ferroviários, bem como trabalhadores de estufas, silvicultura e viveiros podem ter um risco substancial de sendo expostos a pesticidas neurotóxicos também. As crianças, que constituem uma proporção significativa da força de trabalho agrícola, são especialmente vulneráveis porque seus sistemas nervosos não estão totalmente desenvolvidos. Os efeitos agudos dos pesticidas são geralmente bem descritos, e efeitos duradouros após exposição repetida ou exposição única a altas doses são frequentemente observados (Tabela 6), mas o efeito da exposição subclínica repetida é incerto.
Tabela 6. Classes de pesticidas neurotóxicos comuns, exposição, efeitos e sintomas associados
|
Compound |
Exemplos de fonte de exposição |
Setores selecionados em risco |
Efeito1 |
|
Compostos organofosforados: Beomil; Deméton; Diclorvós; paratião de etilo; Mevinfos; Fosfolano; Terbufos; malatião |
Tratamento; tratamento de colheitas; trabalhar com culturas tratadas; estivador |
Agricultura; silvicultura; químico; jardinagem |
M: Inibição da acetilcolinesterase A: Hiperatividade; paralisia neuromuscular; deficiência visual; dificuldade respiratória; inquietação; fraqueza; vômito; convulsões |
|
Carbamatos: Aldicarbe; Carbarilo; Carbofurano; Propoxur |
M: Axonopatia por neurotoxicidade tardia2 C: Polineuropatia; dormência e formigamento nos pés; fraqueza muscular; perturbação sensorial; paralisia |
||
|
Organoclorados: Aldrin; Dieldrin; DDT; Endrina; Heptacloro; Lindano; Metoxicloro; Mirex; Toxafeno |
Veja acima |
Veja acima |
A: Excitabilidade; apreensão; tontura; dor de cabeça; confusão; perda de equilíbrio; fraqueza; ataxia; tremores; convulsões; coma C: Encefalopatia |
|
Piretróides |
Veja acima |
Veja acima |
M: Alteração do fluxo de íons de sódio através da membrana celular nervosa A: Disparo repetido da célula nervosa; tremor; convulsão |
|
2,4-D |
Herbicida |
Agricultura |
C: Polineuropatia |
|
hidróxido de trietilestanho |
Tratamento da superfície; manuseio de madeira tratada |
Madeira e produtos de madeira |
A: Dor de cabeça; fraqueza; paralisia; distúrbios visuais C: Polineuropatia; efeitos do SNC |
|
Brometo de metilo |
fumigação |
Estufas; inseticida; fabricação de geladeiras |
M: Desconhecido A: Distúrbios visuais e da fala; delírio; convulsão C: Encefalopatia |
1 M: mecanismo; A: efeitos agudos; C: efeitos crônicos.
Neuropatia: disfunção das fibras nervosas periféricas motoras e sensitivas.
Encefalopatia: disfunção cerebral devido ao comprometimento generalizado do cérebro.
Ataxia: coordenação motora prejudicada.
2 Principalmente fosfatos ou fosfonatos.
Outros produtos químicos
Vários produtos químicos diferentes que não se enquadram nos grupos mencionados acima também possuem neurotoxicidade. Alguns deles são usados como pesticidas, mas também em diferentes processos industriais. Alguns têm efeitos neurotóxicos agudos e crônicos bem documentados; outros têm efeitos agudos óbvios, mas os efeitos crônicos são mal examinados. Exemplos desses produtos químicos, seus usos e efeitos estão listados na Tabela 7.
Tabela 7. Outros produtos químicos associados à neurotoxicidade
|
Produtos Químicos |
Exemplos de fonte de exposição |
Setores selecionados em risco |
Efeito1 |
|
Ácido bórico |
Soldagem; fluxos; preservação |
Metal; copo |
A: Delírio; convulsão C: depressão do SNC. |
|
Disulfiram |
Farmacêutica |
Caucho |
C: Fadiga; neuropatia periférica; sonolência |
|
Hexaclorofeno |
sabonetes antibacterianos |
Produtos Químicos |
C: edema do SNC; danos nos nervos periféricos |
|
Hidrazina |
Agentes redutores |
Químico; exército |
A: Excitação; perda de apetite; tremor; convulsão |
|
Fenol/Cresol |
Anti-sépticos |
Plásticos; resinas; químico; hospitais; laboratórios |
M: Desnatura proteínas e enzimas A: Perda de reflexo; fraqueza; tremor; sudorese; coma C: Perda de apetite; perturbação mental; zumbido nos ouvidos |
|
Piridina |
Desnaturação do etanol |
Químico; têxtil |
A: depressão do SNC; depressão mental; fadiga; perda de apetite C: Irritabilidade; distúrbios do sono; polineuropatia; visão dupla |
|
Chumbo tetraetila |
Aditivo de gasolina |
Químico; transporte |
C: Irritabilidade; fraqueza; tremor; dificuldades de visão |
|
Arsino |
Baterias; inseticida; Derretendo |
Fundição; vidraria; cerâmica; fabricação de papel |
M: Função enzimática prejudicada A: Sensação reduzida; paresia; convulsão; coma C: Deficiência motora; ataxia; perda do sentido de vibração; polineuropatia |
|
Lítio |
Aditivo de óleo; farmacêutico |
Mercado Petroquímico |
A / C: Perda de apetite; zumbido nos ouvidos; visão embaçada; tremor; ataxia |
|
Selênio |
Derretendo; produção de retificadores; vulcanização; óleos de corte; antioxidante |
Eletrônico; obras de vidro; indústria metalúrgica; indústria da borracha |
A: Delírio; anosmia C: Odor de alho; polineuropatia; nervosismo |
|
tálio |
Rodenticida |
Copo; produtos de vidro |
A: Perda de apetite; cansaço; sonolência; sabor metálico; dormência; ataxia |
|
Telúrio |
Derretendo; produção de borracha; catalisador |
Metal; químico; borracha; eletrônico |
A: Dor de cabeça; sonolência; neuropatia C: Odor de alho; sabor metálico; parkinsonismo; depressão |
|
Vanádio |
Fusão |
Mineração; produção de aço; indústria química |
A: Perda de apetite; zumbido nos ouvidos; sonolência, tremor C: Depressão; tremor; cegueira |
1 M: mecanismo; A: efeitos agudos; C: efeitos crônicos.
Neuropatia: disfunção das fibras nervosas periféricas motoras e sensitivas.
Encefalopatia: disfunção cerebral devido ao comprometimento generalizado do cérebro.
Ataxia: coordenação motora prejudicada
Manifestações de Intoxicação Aguda e Crônica Precoce
O conhecimento atual das manifestações de curto e longo prazo da exposição a substâncias neurotóxicas vem de estudos experimentais com animais e estudos em câmaras humanas, estudos epidemiológicos de trabalhadores ativos e aposentados e/ou doentes, estudos e relatórios clínicos, bem como desastres de grande escala , como os ocorridos em Bhopal, após vazamento de isocianato de metila, e em Minamata, por envenenamento por metilmercúrio.
A exposição a substâncias neurotóxicas pode produzir efeitos imediatos (agudos) e/ou prolongados (crônicos). Em ambos os casos, os efeitos podem ser reversíveis e desaparecer com o tempo após a redução ou cessação da exposição, ou resultar em danos permanentes e irreversíveis. A gravidade do comprometimento agudo e crônico do sistema nervoso depende da dose de exposição, que inclui tanto a quantidade quanto a duração da exposição. Assim como o álcool e as drogas recreativas, muitas substâncias neurotóxicas podem inicialmente ser excitatórias, produzindo uma sensação de bem-estar ou euforia e/ou acelerando as funções motoras; à medida que a dose aumenta em quantidade ou no tempo, essas mesmas neurotoxinas deprimem o sistema nervoso. De fato, a narcose (um estado de estupor ou insensibilidade) é induzida por um grande número de substâncias neurotóxicas, que alteram a mente e deprimem o sistema nervoso central.
Envenenamento Agudo
Os efeitos agudos refletem a resposta imediata à substância química. A gravidade dos sintomas e distúrbios resultantes depende da quantidade que atinge o sistema nervoso. Com exposições leves, os efeitos agudos são leves e transitórios, desaparecendo quando a exposição cessa. Dor de cabeça, cansaço, tontura, dificuldade de concentração, sensação de embriaguez, euforia, irritabilidade, tontura e reflexos lentos são os tipos de sintomas experimentados durante a exposição a produtos químicos neurotóxicos. Embora esses sintomas sejam reversíveis, quando a exposição é repetida dia após dia, os sintomas também reaparecem. Além disso, como a substância neurotóxica não é imediatamente eliminada do corpo, os sintomas podem persistir após o trabalho. Os sintomas relatados em uma determinada estação de trabalho são um bom reflexo da interferência química no sistema nervoso e devem ser considerados um sinal de alerta para uma possível superexposição; medidas preventivas para reduzir os níveis de exposição devem ser iniciadas.
Se a exposição for muito elevada, como pode ocorrer com derrames, fugas, explosões e outros acidentes, os sintomas e sinais de intoxicação são debilitantes (fortes dores de cabeça, confusão mental, náuseas, tonturas, incoordenação, visão turva, perda de consciência); se a exposição for alta o suficiente, os efeitos podem ser duradouros, possivelmente resultando em coma e morte.
Distúrbios agudos relacionados a pesticidas são uma ocorrência comum entre trabalhadores agrícolas em países produtores de alimentos, onde grandes quantidades de substâncias tóxicas são usadas como inseticidas, fungicidas, nematicidas e herbicidas. Organofosfatos, carbamatos, organoclorados, piretro, piretrina, paraquat e diquat estão entre as principais categorias de pesticidas; no entanto, existem milhares de formulações de pesticidas, contendo centenas de ingredientes ativos diferentes. Alguns pesticidas, como o maneb, contêm manganês, enquanto outros são dissolvidos em solventes orgânicos. Além dos sintomas mencionados acima, a intoxicação aguda por organofosforados e carbamatos pode ser acompanhada por salivação, incontinência, convulsões, espasmos musculares, diarreia, distúrbios visuais, bem como dificuldades respiratórias e batimentos cardíacos acelerados; estes resultam de um excesso do neurotransmissor acetilcolina, que ocorre quando essas substâncias atacam uma substância química chamada colinesterase. A colinesterase sanguínea diminui proporcionalmente ao grau de intoxicação aguda por organofosforados ou carbamatos.
Com algumas substâncias, como pesticidas organofosforados e monóxido de carbono, exposições agudas de alto nível podem produzir deterioração retardada de certas partes do sistema nervoso. Para os primeiros, podem ocorrer dormência e formigamento, fraqueza e desequilíbrio algumas semanas após a exposição, enquanto para os segundos pode ocorrer deterioração neurológica tardia, com sintomas de confusão mental, ataxia, incoordenação motora e paresia. Episódios agudos repetidos de altos níveis de monóxido de carbono foram associados ao parkinsonismo tardio. É possível que altas exposições a certos produtos químicos neurotóxicos possam estar associadas a um risco aumentado de distúrbios neurodegenerativos mais tarde na vida.
Envenenamento Crônico
O reconhecimento dos perigos dos produtos químicos neurotóxicos levou muitos países a reduzir os níveis de exposição permitidos. No entanto, para a maioria dos produtos químicos, o nível em que nenhum efeito adverso ocorrerá durante a exposição a longo prazo ainda é desconhecido. A exposição repetida a níveis baixos a médios de substâncias neurotóxicas ao longo de muitos meses ou anos pode alterar as funções do sistema nervoso de forma insidiosa e progressiva. A interferência contínua nos processos moleculares e celulares faz com que as funções neurofisiológicas e psicológicas sofram alterações lentas, que nas fases iniciais podem passar despercebidas, pois há grandes reservas nos circuitos do sistema nervoso e os danos podem, nas primeiras fases, ser compensados por novas aprendizagens.
Assim, a lesão inicial do sistema nervoso não é necessariamente acompanhada por distúrbios funcionais e pode ser reversível. No entanto, à medida que o dano progride, sintomas e sinais, geralmente de natureza inespecífica, tornam-se aparentes e os indivíduos podem procurar atendimento médico. Finalmente, o comprometimento pode se tornar tão grave que se manifesta uma síndrome clínica clara, geralmente irreversível.
A Figura 1 esquematiza o continuum de deterioração da saúde associado à exposição a substâncias neurotóxicas. A progressão da disfunção neurotóxica depende tanto da duração quanto da concentração da exposição (dose) e pode ser influenciada por outros fatores do local de trabalho, estado de saúde individual e suscetibilidade, bem como estilo de vida, particularmente bebida e exposição a substâncias neurotóxicas usadas em hobbies, como colas aplicadas na montagem de móveis ou construção de maquetes plásticas, tintas e decapantes.
Figura 1. Deterioração da saúde em um continuum com o aumento da dosagem
Diferentes estratégias são adotadas para a identificação de doenças relacionadas a neurotoxinas entre trabalhadores individuais e para a vigilância da deterioração precoce do sistema nervoso entre trabalhadores ativos. O diagnóstico clínico depende de uma constelação de sinais e sintomas, juntamente com o histórico médico e de exposição de um indivíduo; outras etiologias além da exposição devem ser sistematicamente descartadas. Para a vigilância da disfunção precoce entre trabalhadores ativos, o retrato grupal da disfunção é importante. Na maioria das vezes, o padrão de disfunção observado para o grupo será semelhante ao padrão de comprometimento observado clinicamente na doença. É mais ou menos como somar alterações precoces e brandas para produzir uma imagem do que está acontecendo com o sistema nervoso. O padrão ou perfil da resposta precoce geral fornece uma indicação da especificidade e do tipo de ação da substância ou mistura neurotóxica específica. Em locais de trabalho com potencial exposição a substâncias neurotóxicas, a vigilância sanitária de grupos de trabalhadores pode revelar-se particularmente útil para a prevenção e ação laboral de forma a evitar o desenvolvimento de doenças mais graves (ver Figura 2). Estudos laborais realizados em todo o mundo, com trabalhadores ativos expostos a substâncias neurotóxicas específicas ou a misturas de vários produtos químicos, têm fornecido informações valiosas sobre as manifestações precoces de disfunção do sistema nervoso em grupos de trabalhadores expostos.
Figura 2. Prevenção da neurotoxicidade no trabalho.
Os primeiros sintomas de envenenamento crônico
Estados de humor alterados são, na maioria das vezes, os primeiros sintomas das mudanças iniciais no funcionamento do sistema nervoso. Irritabilidade, euforia, mudanças repentinas de humor, cansaço excessivo, sentimentos de hostilidade, ansiedade, depressão e tensão estão entre os estados de humor mais frequentemente associados a exposições neurotóxicas. Outros sintomas incluem problemas de memória, dificuldades de concentração, dores de cabeça, visão turva, sensação de embriaguez, tontura, lentidão, sensação de formigamento nas mãos ou pés, perda da libido e assim por diante. Embora nos estágios iniciais esses sintomas geralmente não sejam suficientemente graves para interferir no trabalho, eles refletem uma diminuição do bem-estar e afetam a capacidade de desfrutar plenamente das relações familiares e sociais. Muitas vezes, devido à natureza inespecífica desses sintomas, trabalhadores, empregadores e profissionais de saúde ocupacional tendem a ignorá-los e procurar outras causas além da exposição no local de trabalho. De fato, tais sintomas podem contribuir ou agravar uma situação pessoal já difícil.
Em locais de trabalho onde são usadas substâncias neurotóxicas, trabalhadores, empregadores e pessoal de saúde e segurança ocupacional devem estar particularmente atentos à sintomatologia de intoxicação precoce, indicativa de vulnerabilidade do sistema nervoso à exposição. Questionários de sintomas foram desenvolvidos para estudos de locais de trabalho e vigilância de locais de trabalho onde são usadas substâncias neurotóxicas. A Tabela 1 contém um exemplo desse questionário.
Tabela 1. Lista de verificação de sintomas crônicos
Sintomas experimentados no último mês
1. Você se cansa mais facilmente do que o esperado para o tipo de atividade que faz?
2. Você se sentiu tonto ou tonto?
3. Você tem dificuldade de concentração?
4. Você tem se sentido confuso ou desorientado?
5. Você teve problemas para se lembrar das coisas?
6. Seus parentes perceberam que você tem dificuldade para se lembrar das coisas?
7. Você teve que fazer anotações para se lembrar das coisas?
8. Você achou difícil entender o significado dos jornais?
9. Você se sentiu irritado?
10. Você se sentiu deprimido?
11. Você já teve palpitações cardíacas mesmo quando não está se exercitando?
12. Você teve uma convulsão?
13. Você tem dormido com mais frequência do que o habitual?
14. Você teve dificuldade para dormir?
15. Você tem sido incomodado por falta de coordenação ou perda de equilíbrio?
16. Você teve alguma perda de força muscular nas pernas ou pés?
17. Você teve alguma perda de força muscular em seus braços ou mãos?
18. Você teve dificuldade para mover os dedos ou pegar coisas?
19. Você já teve dormência nas mãos e formigamento nos dedos por mais de um dia?
20. Você já teve dormência nas mãos e formigamento nos dedos dos pés por mais de um dia?
21. Você tem dores de cabeça pelo menos uma vez por semana?
22. Você já teve dificuldade em dirigir do trabalho para casa porque se sentiu tonto ou cansado?
23. Você se sentiu “alto” com os produtos químicos usados no trabalho?
24. Você teve uma tolerância menor ao álcool (leva menos para ficar bêbado)?
Fonte: Retirado de Johnson 1987.
Alterações motoras, sensoriais e cognitivas precoces na intoxicação crônica
Com o aumento da exposição, podem ser observadas alterações nas funções motoras, sensoriais e cognitivas em trabalhadores expostos a substâncias neurotóxicas, que não apresentam evidências clínicas de anormalidade. Como o sistema nervoso é complexo e certas áreas são vulneráveis a produtos químicos específicos, enquanto outras são sensíveis à ação de um grande número de agentes tóxicos, uma ampla gama de funções do sistema nervoso pode ser afetada por um único agente tóxico ou uma mistura de neurotoxinas. Tempo de reação, coordenação mão-olho, memória de curto prazo, memória visual e auditiva, atenção e vigilância, destreza manual, vocabulário, troca de atenção, força de preensão, velocidade motora, firmeza da mão, humor, visão de cores, percepção vibrotátil, audição e olfato estão entre as muitas funções que demonstraram ser alteradas por diferentes substâncias neurotóxicas.
Informações importantes sobre o tipo de déficits precoces resultantes da exposição foram fornecidas comparando o desempenho entre trabalhadores expostos e não expostos e quanto ao grau de exposição. Anger (1990) fornece uma excelente revisão da pesquisa neurocomportamental no local de trabalho até 1989. A Tabela 2, adaptada deste artigo, fornece um exemplo do tipo de déficits neurofuncionais que têm sido consistentemente observados em grupos de trabalhadores ativos expostos a alguns dos mais substâncias neurotóxicas comuns.
Tabela 2. Efeitos neurofuncionais consistentes de exposições no local de trabalho a algumas das principais substâncias neurotóxicas
|
Solventes orgânicos mistos |
dissulfeto de carbono |
Estireno |
Organofos- |
Conduzir |
Mercúrio |
|
|
Aquisição |
+ |
|
|
|
+ |
|
|
Afetar |
+ |
|
+ |
|
+ |
|
|
Categorização |
+ |
|
|
|
|
|
|
Codificação |
+ |
+ |
|
|
+ |
+ |
|
Visão de cores |
+ |
|
+ |
|
|
|
|
Mudança de conceito |
+ |
|
|
|
|
|
|
Distração |
|
|
|
|
+ |
|
|
Inteligência |
+ |
+ |
|
+ |
+ |
+ |
|
Memória |
+ |
+ |
+ |
+ |
+ |
+ |
|
Coordenação motora |
+ |
+ |
+ |
|
+ |
+ |
|
A velocidade do motor |
+ |
+ |
+ |
|
+ |
+ |
|
Sensibilidade ao contraste visual próximo |
+ |
|
|
|
|
|
|
Limiar de percepção de odor |
+ |
|
|
|
|
|
|
Identificação de odor |
+ |
|
|
|
+ |
|
|
Personalidade |
+ |
+ |
|
|
|
+ |
|
Relações espaciais |
+ |
+ |
|
|
+ |
|
|
Limiar vibratório |
+ |
|
|
+ |
|
+ |
|
vigilância |
+ |
+ |
|
|
+ |
|
|
Campo visual |
|
|
|
|
+ |
+ |
|
Vocabulário |
|
|
|
|
+ |
|
Fonte: Adaptado de Anger 1990.
Embora neste estágio do continuum do bem-estar à doença, a perda não esteja na faixa clinicamente anormal, pode haver consequências relacionadas à saúde associadas a tais alterações. Por exemplo, a diminuição da vigilância e os reflexos reduzidos podem colocar os trabalhadores em maior risco de acidentes. O cheiro é usado para identificar vazamentos e mascarar a saturação (ruptura do cartucho), e a perda aguda ou crônica do olfato torna a pessoa menos apta a identificar uma situação potencialmente perigosa. Alterações de humor podem interferir nas relações interpessoais no trabalho, socialmente e em casa. Esses estágios iniciais de deterioração do sistema nervoso, que podem ser observados examinando grupos de trabalhadores expostos e comparando-os com trabalhadores não expostos ou quanto ao seu grau de exposição, refletem diminuição do bem-estar e podem ser preditivos de risco de doenças neurológicas mais graves problemas no futuro.
Saúde mental na intoxicação crônica
Os distúrbios neuropsiquiátricos têm sido atribuídos à exposição a substâncias neurotóxicas. As descrições clínicas variam de distúrbios afetivos, incluindo ansiedade e depressão, a manifestações de comportamento psicótico e alucinações. A exposição aguda de alto nível a muitos metais pesados, solventes orgânicos e pesticidas pode produzir delirium. A “loucura do manganês” foi descrita em pessoas com exposição prolongada ao manganês, e a conhecida síndrome do “chapeleiro maluco” resulta da intoxicação por mercúrio. A encefalopatia tóxica tipo 2a, caracterizada por mudança sustentada na personalidade envolvendo fadiga, labilidade emocional, controle de impulsos e humor e motivação gerais, tem sido associada à exposição a solventes orgânicos. Há evidências crescentes de estudos clínicos e populacionais de que os transtornos de personalidade persistem ao longo do tempo, muito tempo após a exposição cessar, embora outros tipos de comprometimento possam melhorar.
No continuum do bem-estar à doença, alterações de humor, irritabilidade e fadiga excessiva são muitas vezes as primeiras indicações de superexposição a substâncias neurotóxicas. Embora os sintomas neuropsiquiátricos sejam rotineiramente pesquisados em estudos no local de trabalho, eles raramente são apresentados como um problema de saúde mental com possíveis consequências no bem-estar mental e social. Por exemplo, mudanças no estado de saúde mental afetam o comportamento de alguém, contribuindo para difíceis relacionamentos interpessoais e desacordos em casa; estes, por sua vez, podem agravar o estado mental de alguém. Em locais de trabalho com programas de ajuda aos funcionários, projetados para ajudar os funcionários com problemas pessoais, a ignorância dos possíveis efeitos na saúde mental da exposição a substâncias neurotóxicas pode levar a um tratamento que lida com os efeitos e não com a causa. É interessante notar que entre os muitos surtos relatados de “histeria em massa” ou doença psicogênica, as indústrias com exposição a substâncias neurotóxicas estão super-representadas. É possível que essas substâncias, que em grande parte não foram dosadas, tenham contribuído para os sintomas relatados.
As manifestações de saúde mental da exposição a neurotoxinas podem ser semelhantes àquelas causadas por estressores psicossociais associados à má organização do trabalho, bem como reações psicológicas a acidentes, ocorrências muito estressantes e intoxicações graves, chamadas de transtorno de estresse pós-traumático (conforme discutido em outra parte deste enciclopédia). Uma boa compreensão da relação entre problemas de saúde mental e condições de trabalho é importante para iniciar ações preventivas e curativas adequadas.
Considerações gerais na avaliação da disfunção neurotóxica precoce
Ao avaliar a disfunção precoce do sistema nervoso entre trabalhadores ativos, vários fatores devem ser levados em consideração. Em primeiro lugar, muitas das funções neuropsicológicas e neurofisiológicas examinadas diminuem com a idade; alguns são influenciados pela cultura ou nível educacional. Esses fatores devem ser levados em consideração quando se considera a relação entre exposição e alterações do sistema nervoso. Isso pode ser feito comparando grupos com status sociodemográfico semelhante ou usando métodos estatísticos de ajuste. No entanto, existem certas armadilhas que devem ser evitadas. Por exemplo, trabalhadores mais velhos podem ter históricos de trabalho mais longos, e foi sugerido que algumas substâncias neurotóxicas podem acelerar o envelhecimento. A segregação do trabalho pode confinar trabalhadores com baixa escolaridade, mulheres e minorias em empregos com maior exposição. Em segundo lugar, o consumo de álcool, tabagismo e drogas, todos contendo substâncias neurotóxicas, também podem afetar os sintomas e o desempenho. Uma boa compreensão do local de trabalho é importante para desvendar os diferentes fatores que contribuem para a disfunção do sistema nervoso e para a implementação de medidas preventivas.
Prevenção da Neurotoxicidade no Trabalho
Um trabalhador não exposto a uma substância neurotóxica nunca desenvolverá nenhum efeito neurotóxico adverso à saúde dessa substância. A exposição zero leva à proteção total contra efeitos neurotóxicos à saúde. Esta é a essência de todas as medidas de prevenção primária.
Teste de Toxicidade
Novos compostos químicos introduzidos no local de trabalho e em ambientes ocupacionais já deveriam ter sido testados quanto à neurotoxicidade. A não realização de testes de toxicidade pré-comercialização pode levar ao contato dos trabalhadores e a efeitos adversos potencialmente graves à saúde. A introdução de metil n-butil cetona em um local de trabalho nos Estados Unidos é um exemplo clássico dos possíveis perigos de neurotóxicos não testados sendo introduzidos no local de trabalho (Spencer e Schaumburg 1980).
Controles de Engenharia
Os controles de engenharia (por exemplo, sistemas de ventilação, instalações de produção fechadas) são os melhores meios para manter a exposição dos trabalhadores abaixo dos limites de exposição permitidos. Os processos químicos fechados que impedem que todos os tóxicos sejam liberados no ambiente de trabalho são os ideais. Se isso não for possível, os sistemas de ventilação fechados que extraem os vapores do ar ambiente e são projetados para afastar o ar contaminado dos trabalhadores são úteis quando bem projetados, adequadamente mantidos e operados adequadamente.
Equipamento de proteção pessoal
Em situações em que os controles de engenharia não estão disponíveis para reduzir o contato dos trabalhadores com neurotóxicos, deve ser fornecido equipamento de proteção individual. Como os neurotóxicos no local de trabalho são muitos e as vias de exposição diferem entre os locais de trabalho e as condições de trabalho, o tipo de equipamento de proteção individual deve ser cuidadosamente selecionado para a situação em questão. Por exemplo, o chumbo neurotóxico pode exercer sua toxicidade quando poeira carregada de chumbo é respirada e quando partículas de chumbo são ingeridas em alimentos ou água. Portanto, o equipamento de proteção individual deve proteger contra ambas as vias de exposição. Isso significaria equipamentos de proteção respiratória e adoção de medidas de higiene pessoal para evitar o consumo de alimentos ou bebidas contaminadas com chumbo. Para muitos neurotóxicos (como solventes industriais), a absorção da substância através da pele intacta é a principal via de exposição. Luvas impermeáveis, aventais e outros equipamentos adequados devem, portanto, ser fornecidos para evitar a absorção pela pele. Isso seria um acréscimo aos controles de engenharia ou equipamentos de proteção respiratória individual. Um planejamento considerável deve ser feito para combinar o equipamento de proteção individual com o trabalho específico que está sendo executado.
Controles Administrativos
Os controles administrativos consistem em esforços gerenciais para reduzir os riscos no local de trabalho por meio de planejamento, treinamento, rotação de funcionários nos locais de trabalho, mudanças nos processos de produção e substituição de produtos (Urie 1992), bem como o cumprimento estrito de todos os regulamentos existentes.
Direito de saber dos trabalhadores
Enquanto o empregador tem a responsabilidade de fornecer um local de trabalho ou experiência de trabalho que não prejudique a saúde dos trabalhadores, os trabalhadores têm a responsabilidade de seguir as regras do local de trabalho que visam protegê-los. Os trabalhadores devem estar em posição de saber quais ações tomar para se protegerem. Isso significa que os trabalhadores têm o direito de saber sobre a neurotoxicidade das substâncias com as quais entram em contato e quais medidas de proteção podem tomar.
Vigilância em Saúde do Trabalhador
Sempre que as condições o permitirem, os trabalhadores devem ser submetidos a exames médicos regulares. A avaliação regular por médicos do trabalho ou outros médicos especialistas constitui vigilância da saúde do trabalhador. Para os trabalhadores que trabalham com ou perto de neurotóxicos, os médicos devem estar informados sobre os efeitos da exposição. Por exemplo, a exposição de baixo nível a muitos solventes orgânicos produzirá sintomas de fadiga, distúrbios do sono, dores de cabeça e distúrbios da memória. Para altas doses de chumbo, pulso caído e comprometimento dos nervos periféricos seriam sinais de intoxicação por chumbo. Quaisquer sinais e sintomas de intoxicação por neurotóxicos devem resultar na realocação do trabalhador para uma área livre do neurotóxico e esforços para reduzir os níveis do neurotóxico no local de trabalho.
Síndromes clínicas associadas à neurotoxicidade
As síndromes neurotóxicas, provocadas por substâncias que afetam adversamente o tecido nervoso, constituem um dos dez principais distúrbios ocupacionais nos Estados Unidos. Os efeitos neurotóxicos constituem a base para o estabelecimento de critérios de limite de exposição para aproximadamente 40% dos agentes considerados perigosos pelo Instituto Nacional de Segurança e Saúde Ocupacional dos Estados Unidos (NIOSH).
Uma neurotoxina é qualquer substância capaz de interferir na função normal do tecido nervoso, causando dano celular irreversível e/ou resultando em morte celular. Dependendo de suas propriedades particulares, uma determinada neurotoxina atacará locais selecionados ou elementos celulares específicos do sistema nervoso. Esses compostos, que são apolares, têm maior lipossolubilidade e, portanto, têm maior acesso ao tecido nervoso do que produtos químicos altamente polares e menos lipossolúveis. O tipo e o tamanho das células e os vários sistemas de neurotransmissores afetados em diferentes regiões do cérebro, os mecanismos de desintoxicação protetores inatos, bem como a integridade das membranas celulares e organelas intracelulares, todos influenciam as respostas neurotóxicas.
Os neurônios (a unidade celular funcional do sistema nervoso) têm uma alta taxa metabólica e correm maior risco de danos neurotóxicos, seguidos por oligodendrócitos, astrócitos, micróglia e células do endotélio capilar. Alterações na estrutura da membrana celular prejudicam a excitabilidade e impedem a transmissão do impulso. Os efeitos tóxicos alteram a forma da proteína, o conteúdo do fluido e a capacidade de troca iônica das membranas, levando ao inchaço dos neurônios, astrócitos e danos às delicadas células que revestem os capilares sanguíneos. A interrupção dos mecanismos de neurotransmissores bloqueia o acesso aos receptores pós-sinápticos, produz falsos efeitos de neurotransmissores e altera a síntese, armazenamento, liberação, recaptação ou inativação enzimática de neurotransmissores naturais. Assim, as manifestações clínicas da neurotoxicidade são determinadas por uma série de fatores diferentes: as características físicas da substância neurotóxica, a dose de exposição a ela, a vulnerabilidade do alvo celular, a capacidade do organismo de metabolizar e excretar a toxina e pela capacidades reparativas das estruturas e mecanismos afetados. A Tabela 1 lista várias exposições químicas e suas síndromes neurotóxicas.
Tabela 1. Exposições químicas e síndromes neurotóxicas associadas
|
Neurotoxina |
Fontes de exposição |
Diagnóstico clínico |
Locus de patologia1 |
|
Metais |
|||
|
Arsênico |
Pesticidas; pigmentos; tinta anti-incrustante; indústria de galvanoplastia; frutos do mar; fundições; semicondutores |
Aguda: encefalopatia Crônica: neuropatia periférica |
Desconhecido (um) Axônio (c) |
|
Conduzir |
Solda; munição de chumbo; uísque ilícito; inseticidas; oficina mecânica; fabricação de baterias de armazenamento; fundições, fundições; tinta à base de chumbo; canos de chumbo |
Aguda: encefalopatia Crônica: encefalopatia e neuropatia periférica |
Vasos sanguíneos (a) Axônio (c) |
|
Manganês |
Ferro, siderurgia; operações de soldagem; operações de acabamento de metais; fertilizantes; fabricantes de fogos de artifício, fósforos; fabricantes de baterias secas |
Aguda: encefalopatia Crônica: parkinsonismo |
Desconhecido (um) Neurônios dos gânglios da base (c) |
|
Mercúrio |
Instrumentos científicos; equipamento elétrico; amálgamas; indústria de galvanoplastia; fotografia; feltro fazendo |
Aguda: dor de cabeça, náusea, início de tremor Crônica: ataxia, neuropatia periférica, encefalopatia |
Desconhecido (um) Axônio (c) Desconhecido (c) |
|
Estanho |
Indústria de conservas; solda; componentes eletrônicos; plásticos polivinílicos; fungicidas |
Aguda: defeitos de memória, convulsões, desorientação Crônica: encefalomielopatia |
Neurônios do sistema límbico (a e c) Mielina (c) |
|
solventes |
|||
|
Dissulfeto de carbono |
Fabricantes de rayon de viscose; conservantes; têxteis; cimento de borracha; vernizes; indústria de galvanoplastia |
Aguda: encefalopatia Crônica: neuropatia periférica, parkinsonismo |
Desconhecido (um) Axônio (c) Desconhecido |
|
n-hexano, metil butil cetona |
Tintas; lacas; vernizes; compostos de limpeza de metais; tintas de secagem rápida; removedores de tinta; colas, adesivos |
Aguda: narcose Crônica: neuropatia periférica, desconhecida (a) Axônio (c), |
|
|
Percloroetileno |
Removedores de tinta; desengordurantes; agentes de extração; indústria de limpeza a seco; industria têxtil |
Aguda: narcose Crônica: neuropatia periférica, encefalopatia |
Desconhecido (um) Axônio (c) Desconhecido |
|
Tolueno |
Solventes de borracha; agentes de limpeza; colas; fabricantes de benzeno; gasolina, combustíveis de aviação; tintas, diluentes para tintas; lacas |
Aguda: narcose Crônica: ataxia, encefalopatia |
Desconhecido (um) Cerebelo (c) Desconhecido |
|
Tricloroetileno |
Desengordurantes; indústria de pintura; vernizes; removedores de manchas; processo de descafeinação; indústria de limpeza a seco; solventes de borracha |
Aguda: narcose Crônica: encefalopatia, neuropatia craniana |
Desconhecido (um) Desconhecido (c) Axônio (c) |
|
Inseticidas |
|||
|
Organofosforados |
Fabricação e aplicação na indústria agrícola |
Aguda: intoxicação colinérgica Crônica: ataxia, paralisia, neuropatia periférica |
Acetilcolinesterase (a) Longos tratos da medula espinhal (c) Axônio (c) |
|
Carbamatos |
Pós de pulga de fabricação e aplicação da indústria agrícola |
Aguda: intoxicação colinérgica Crônica: tremor, neuropatia periférica |
Acetilcolinesterase (a) Sistema dopaminérgico (c) |
1 (a), aguda; (c), crônica.
Fonte: Modificado de Feldman 1990, com permissão do editor.
Estabelecer o diagnóstico de uma síndrome neurotóxica e diferenciá-la de doenças neurológicas de etiologia não neurotóxica requer uma compreensão da patogênese dos sintomas neurológicos e dos sinais e sintomas observados; uma consciência de que determinadas substâncias são capazes de afetar o tecido nervoso; documentação da exposição; evidência da presença de neurotoxina e/ou metabólitos em tecidos de um indivíduo afetado; e delineamento cuidadoso de uma relação de tempo entre a exposição e o aparecimento de sintomas com subsequente diminuição dos sintomas após o término da exposição.
A prova de que uma determinada substância atingiu um nível de dose tóxica geralmente não existe após o aparecimento dos sintomas. A menos que o monitoramento ambiental esteja em andamento, um alto índice de suspeição é necessário para reconhecer casos de lesão neurotoxicológica. A identificação de sintomas atribuíveis ao sistema nervoso central e/ou periférico pode ajudar o clínico a focar certas substâncias, que têm maior predileção por uma parte ou outra do sistema nervoso, como possíveis culpadas. Convulsões, fraqueza, tremores/contrações musculares, anorexia (perda de peso), distúrbios do equilíbrio, depressão do sistema nervoso central, narcose (estado de estupor ou inconsciência), distúrbios visuais, distúrbios do sono, ataxia (incapacidade de coordenar movimentos musculares voluntários), fadiga e distúrbios táteis são sintomas comumente relatados após a exposição a certos produtos químicos. Constelações de sintomas formam síndromes associadas à exposição a neurotóxicos.
Síndromes Comportamentais
Distúrbios com características predominantemente comportamentais variando de psicose aguda, depressão e apatia crônica têm sido descritos em alguns trabalhadores. É fundamental diferenciar o comprometimento da memória associado a outras doenças neurológicas, como mal de Alzheimer, arteriosclerose ou presença de tumor cerebral, dos déficits cognitivos associados à exposição tóxica a solventes orgânicos, metais ou inseticidas. Distúrbios transitórios da consciência ou crises epilépticas com ou sem envolvimento motor associado devem ser identificados como um diagnóstico primário separado de distúrbios semelhantes da consciência relacionados a efeitos neurotóxicos. Síndromes tóxicas subjetivas e comportamentais, como cefaléia, vertigem, fadiga e alteração da personalidade, manifestam-se como encefalopatia leve com embriaguez e podem indicar a presença de exposição a monóxido de carbono, dióxido de carbono, chumbo, zinco, nitratos ou solventes orgânicos mistos. Testes neuropsicológicos padronizados são necessários para documentar elementos de comprometimento cognitivo em pacientes com suspeita de encefalopatia tóxica, e estes devem ser diferenciados das síndromes demenciais causadas por outras patologias. Os testes específicos utilizados nas baterias de testes diagnósticos devem incluir uma ampla amostragem de testes de função cognitiva que irão gerar previsões sobre o funcionamento e a vida diária do paciente, bem como testes que tenham demonstrado anteriormente serem sensíveis aos efeitos de neurotoxinas conhecidas. Essas baterias padronizadas devem incluir testes que foram validados em pacientes com tipos específicos de danos cerebrais e déficits estruturais, para separar claramente essas condições dos efeitos neurotóxicos. Além disso, os testes devem incluir medidas de controle interno para detectar a influência da motivação, hipocondria, depressão e dificuldades de aprendizagem, e devem conter uma linguagem que leve em consideração os efeitos culturais e educacionais.
Existe um continuum de comprometimento leve a grave do sistema nervoso central experimentado por pacientes expostos a substâncias tóxicas:
- Síndrome afetiva orgânica (Efeito Tipo I), em que predominam os transtornos de humor leves como queixa principal do paciente, com características mais compatíveis com os transtornos afetivos orgânicos do tipo depressivo. Esta síndrome parece ser reversível após a cessação da exposição ao agente agressor.
- Encefalopatia tóxica crônica leve, em que, além dos distúrbios do humor, o comprometimento do sistema nervoso central é mais proeminente. Os pacientes apresentam evidências de distúrbios da memória e da função psicomotora que podem ser confirmados por testes neuropsicológicos. Além disso, características de deficiência visual espacial e formação de conceitos abstratos podem ser vistas. As atividades da vida diária e o desempenho no trabalho são prejudicados.
- Mudança sustentada de personalidade ou humor (Efeito Tipo IIA) or comprometimento da função intelectual (Tipo II) pode ser visto. Na encefalopatia tóxica crônica leve, o curso é insidioso. As características podem persistir após o término da exposição e desaparecer gradualmente, enquanto em alguns indivíduos pode ser observado comprometimento funcional persistente. Se a exposição continuar, a encefalopatia pode progredir para um estágio mais grave.
- In encefalopatia tóxica crônica grave (efeito tipo III) observam-se demências com deterioração global da memória e outros problemas cognitivos. Os efeitos clínicos da encefalopatia tóxica não são específicos de um determinado agente. A encefalopatia crônica associada ao tolueno, chumbo e arsênico não é diferente daquela de outras etiologias tóxicas. A presença de outros achados associados, no entanto (distúrbios visuais com álcool metílico), pode ajudar a diferenciar as síndromes de acordo com etiologias químicas específicas.
Trabalhadores expostos a solventes por longos períodos de tempo podem apresentar distúrbios da função do sistema nervoso central que são permanentes. Uma vez que foi relatado um excesso de sintomas subjetivos, incluindo dor de cabeça, fadiga, perda de memória, perda de apetite e dores no peito difusas, muitas vezes é difícil confirmar esse efeito em qualquer caso individual. Um estudo epidemiológico comparando pintores de casas expostos a solventes com trabalhadores industriais não expostos mostrou, por exemplo, que os pintores tiveram pontuações médias significativamente mais baixas em testes psicológicos que medem a capacidade intelectual e a coordenação psicomotora do que os sujeitos de referência. Os pintores também tiveram desempenhos significativamente inferiores ao esperado em testes de memória e tempo de reação. Diferenças entre trabalhadores expostos por vários anos a combustível de aviação e trabalhadores não expostos, em testes que exigem muita atenção e alta velocidade motora sensorial, também foram aparentes. Prejuízos no desempenho psicológico e mudanças de personalidade também foram relatados entre os pintores de automóveis. Estes incluíram memória visual e verbal, redução da reatividade emocional e baixo desempenho em testes de inteligência verbal.
Mais recentemente, uma controversa síndrome neurotóxica, sensibilidade química múltipla, foi descrito. Esses pacientes desenvolvem uma variedade de características envolvendo múltiplos sistemas de órgãos quando são expostos a níveis baixos de vários produtos químicos encontrados no local de trabalho e no ambiente. Os distúrbios do humor são caracterizados por depressão, fadiga, irritabilidade e falta de concentração. Esses sintomas reaparecem na exposição a estímulos previsíveis, por eliciação por produtos químicos de diversas classes estruturais e toxicológicas, e em níveis muito mais baixos do que aqueles que causam respostas adversas na população em geral. Muitos dos sintomas de sensibilidade química múltipla são compartilhados por indivíduos que apresentam apenas uma forma leve de perturbação do humor, dor de cabeça, fadiga, irritabilidade e esquecimento quando estão em um prédio com pouca ventilação e com liberação de gases de substâncias voláteis de materiais de construção sintéticos e tapetes. Os sintomas desaparecem quando eles saem desses ambientes.
Distúrbios da consciência, convulsões e coma
Quando o cérebro é privado de oxigênio - por exemplo, na presença de monóxido de carbono, dióxido de carbono, metano ou agentes que bloqueiam a respiração dos tecidos, como ácido cianídrico, ou aqueles que causam impregnação maciça do nervo, como certos solventes orgânicos - distúrbios de consciência pode resultar. A perda de consciência pode ser precedida por convulsões em trabalhadores expostos a substâncias anticolinesterásicas, como inseticidas organofosforados. Convulsões também podem ocorrer com encefalopatia por chumbo associada a edema cerebral. Manifestações de toxicidade aguda após envenenamento por organofosforados têm manifestações do sistema nervoso autônomo que precedem a ocorrência de tontura, dor de cabeça, visão turva, miose, dor no peito, aumento das secreções brônquicas e convulsões. Esses efeitos parassimpáticos são explicados pela ação inibitória dessas substâncias tóxicas sobre a atividade da colinesterase.
Distúrbios do movimento
Lentidão de movimento, aumento do tônus muscular e anormalidades posturais foram observados em trabalhadores expostos a manganês, monóxido de carbono, dissulfeto de carbono e à toxicidade de um subproduto da meperidina, 1-metil-4-fenil-1,2,3,6 -tetrahidropiridina (MPTP). Às vezes, os indivíduos podem parecer ter a doença de Parkinson. Parkinsonismo secundário à exposição a tóxicos apresenta características de outros distúrbios nervosos, como coreia e atetose. O tremor típico de “rolar pílulas” não é observado nesses casos e, geralmente, os casos não respondem bem ao medicamento levodopa. A discinesia (comprometimento do poder de movimento voluntário) pode ser um sintoma comum de envenenamento por bromometano. Podem ser observados movimentos espasmódicos dos dedos, face, músculos peribucais e pescoço, bem como espasmos das extremidades. O tremor é comum após envenenamento por mercúrio. Tremor mais óbvio associado à ataxia (falta de coordenação da ação muscular) é observado em indivíduos após a inalação de tolueno.
Opsoclonia é um movimento ocular anormal que é espasmódico em todas as direções. Isso é frequentemente observado na encefalite do tronco cerebral, mas também pode ser uma característica após a exposição à clordecona. A anormalidade consiste em rajadas irregulares de espasmos abruptos, involuntários, rápidos e simultâneos de ambos os olhos de maneira conjugada, possivelmente multidirecional em indivíduos gravemente afetados.
Dor de cabeça
Queixas comuns de dor de cabeça após a exposição a vários vapores metálicos, como zinco e outros vapores de solventes, podem resultar de vasodilatação (alargamento dos vasos sanguíneos), bem como edema cerebral (inchaço). A experiência de dor é comum a essas condições, bem como condições de monóxido de carbono, hipóxia (baixo oxigênio) ou dióxido de carbono. Acredita-se que a “síndrome do edifício doente” cause dores de cabeça devido ao excesso de dióxido de carbono presente em uma área mal ventilada.
Neuropatia periférica
Fibras nervosas periféricas que servem funções motoras começam em neurônios motores no corno ventral da medula espinhal. Os axônios motores estendem-se perifericamente aos músculos que inervam. Uma fibra nervosa sensorial tem seu corpo celular nervoso no gânglio da raiz dorsal ou na substância cinzenta dorsal da medula espinhal. Tendo recebido informações da periferia detectadas em receptores distais, os impulsos nervosos são conduzidos centralmente para os corpos das células nervosas, onde se conectam com as vias da medula espinhal que transmitem informações ao tronco cerebral e aos hemisférios cerebrais. Algumas fibras sensoriais têm conexões imediatas com fibras motoras dentro da medula espinhal, fornecendo uma base para atividade reflexa e respostas motoras rápidas a sensações nocivas. Essas relações sensório-motoras existem em todas as partes do corpo; os nervos cranianos são os equivalentes dos nervos periféricos que surgem no tronco cerebral, em vez dos neurônios da medula espinhal. Fibras nervosas sensoriais e motoras viajam juntas em feixes e são chamadas de nervos periféricos.
Os efeitos tóxicos das fibras nervosas periféricas podem ser divididos naqueles que afetam principalmente os axônios (axonopatias), aqueles que estão envolvidos na perda sensório-motora distal e aqueles que afetam principalmente a bainha de mielina e as células de Schwann. As axonopatias são evidentes nos estágios iniciais nas extremidades inferiores, onde os axônios são os mais longos e mais distantes do corpo da célula nervosa. A desmielinização aleatória ocorre em segmentos entre os nodos de Ranvier. Se ocorrer dano axonal suficiente, segue-se a desmielinização secundária; desde que os axônios sejam preservados, pode ocorrer regeneração das células de Schwann e remielinização. Um padrão observado comumente em neuropatias tóxicas é a axonopatia distal com desmielinização segmentar secundária. A perda de mielina reduz a velocidade de condução dos impulsos nervosos. Assim, o início gradual de formigamento intermitente e dormência progredindo para falta de sensibilidade e sensações desagradáveis, fraqueza muscular e atrofia resulta de danos às fibras motoras e sensoriais. Reflexos tendinosos reduzidos ou ausentes e padrões anatomicamente consistentes de perda sensorial, envolvendo mais os membros inferiores do que os superiores, são características da neuropatia periférica.
Fraquezas motoras podem ser observadas nas extremidades distais e progredir para marcha instável e incapacidade de agarrar objetos. As porções distais das extremidades estão envolvidas em maior extensão, mas casos graves também podem produzir fraqueza muscular proximal ou atrofia. Os grupos musculares extensores estão envolvidos antes dos flexores. Às vezes, os sintomas podem progredir por algumas semanas, mesmo após a remoção da exposição. A deterioração da função nervosa pode persistir por várias semanas após a remoção da exposição.
Dependendo do tipo e gravidade da neuropatia, um exame eletrofisiológico dos nervos periféricos é útil para documentar o comprometimento da função. Pode-se observar diminuição da velocidade de condução, amplitudes reduzidas de potenciais de ação sensoriais ou motores ou latências prolongadas. A diminuição das velocidades de condução motora ou sensorial geralmente está associada à desmielinização das fibras nervosas. A preservação dos valores normais da velocidade de condução na presença de atrofia muscular sugere neuropatia axonal. Exceções ocorrem quando há perda progressiva de fibras nervosas motoras e sensitivas na neuropatia axonal que afeta a velocidade máxima de condução como resultado da queda das fibras nervosas de condução mais rápida de diâmetro maior. Fibras regeneradoras ocorrem em estágios iniciais de recuperação em axonopatias, nas quais a condução é lentificada, principalmente nos segmentos distais. O estudo eletrofisiológico de pacientes com neuropatias tóxicas deve incluir medições da velocidade de condução motora e sensitiva nas extremidades superiores e inferiores. Atenção especial deve ser dada às características de condução principalmente sensorial do nervo sural na perna. Isso é de grande valia quando o nervo sural é então utilizado para biópsia, fornecendo correlação anatômica entre a histologia das fibras nervosas desencadeadas e as características de condução. Um estudo eletrofisiológico diferencial das capacidades de condução dos segmentos proximais versus segmentos distais de um nervo é útil para identificar uma axonopatia tóxica distal ou para localizar um bloqueio neuropático da condução, provavelmente devido à desmielinização.
Compreender a fisiopatologia de uma suspeita de polineuropatia neurotóxica é de grande valia. Por exemplo, em pacientes com neuropatia causada por n-hexano e metilbutil cetona, as velocidades de condução nervosa motora são reduzidas, mas em alguns casos, os valores podem cair dentro da faixa normal se apenas as fibras de disparo mais rápido forem estimuladas e usadas como resultado medido . Como os solventes hexacarbonados neurotóxicos causam degeneração axonal, surgem alterações secundárias na mielina e explicam a redução geral da velocidade de condução, apesar do valor dentro da faixa normal produzido pelas fibras condutoras preservadas.
As técnicas eletrofisiológicas incluem testes especiais além dos estudos de velocidade de condução direta, amplitude e latência. Potenciais evocados somatossensoriais, potenciais evocados auditivos e potenciais evocados visuais são formas de estudar as características dos sistemas de condução sensorial, bem como de nervos cranianos específicos. Os circuitos aferentes-eferentes podem ser testados usando testes de reflexo de piscada envolvendo as respostas do 5º nervo craniano ao 7º músculo inervado craniano; Os reflexos H envolvem vias reflexas motoras segmentares. A estimulação de vibração seleciona fibras maiores de envolvimentos de fibras menores. Técnicas eletrônicas bem controladas estão disponíveis para medir o limiar necessário para eliciar uma resposta e, em seguida, determinar a velocidade de propagação dessa resposta, bem como a amplitude da contração muscular ou a amplitude e o padrão de um potencial de ação sensorial evocado. . Todos os resultados fisiológicos devem ser avaliados à luz do quadro clínico e com a compreensão do processo fisiopatológico subjacente.
Conclusão
A diferenciação de uma síndrome neurotóxica de uma doença neurológica primária representa um desafio formidável para os médicos no ambiente ocupacional. Obter uma boa história, manter um alto grau de suspeição e um acompanhamento adequado de um indivíduo, bem como de grupos de indivíduos, é necessário e gratificante. O reconhecimento precoce de doenças relacionadas a agentes tóxicos em seu ambiente ou a uma determinada exposição ocupacional é fundamental, pois o diagnóstico adequado pode levar o indivíduo a afastar-se precocemente dos perigos da exposição contínua a uma substância tóxica, prevenindo possíveis danos neurológicos irreversíveis. Além disso, o reconhecimento dos primeiros casos afetados em um determinado ambiente pode resultar em mudanças que protegerão outras pessoas que ainda não foram afetadas.
Medindo Déficits Neurotóxicos
Baterias de teste neurofuncionais
Sinais e sintomas neurológicos subclínicos têm sido notados há muito tempo entre trabalhadores ativos expostos a neurotoxinas; entretanto, somente a partir de meados da década de 1960 é que os esforços de pesquisa se concentraram no desenvolvimento de baterias de testes sensíveis capazes de detectar alterações sutis e leves presentes nos estágios iniciais da intoxicação, nas funções perceptivas, psicomotoras, cognitivas, sensoriais e motoras , e afetam.
A primeira bateria de testes neurocomportamentais para uso em estudos no local de trabalho foi desenvolvida por Helena Hänninen, pioneira no campo de déficits neurocomportamentais associados à exposição tóxica (Hänninen Test Battery) (Hänninen e Lindstrom 1979). Desde então, tem havido esforços mundiais para desenvolver, refinar e, em alguns casos, informatizar baterias de testes neurocomportamentais. Anger (1990) descreve cinco baterias de teste neurocomportamentais de locais de trabalho da Austrália, Suécia, Grã-Bretanha, Finlândia e Estados Unidos, bem como duas baterias de triagem neurotóxica dos Estados Unidos, que foram usadas em estudos de trabalhadores expostos a neurotoxinas. Além disso, o Sistema Computadorizado de Avaliação Neurocomportamental (NES) e o Sistema Sueco de Avaliação de Desempenho (SPES) têm sido amplamente utilizados em todo o mundo. Existem também baterias de teste projetadas para avaliar funções sensoriais, incluindo medidas de visão, limiar de percepção vibrotátil, olfato, audição e oscilação (Mergler 1995). Estudos de vários agentes neurotóxicos usando uma ou outra dessas baterias contribuíram muito para o nosso conhecimento do comprometimento neurotóxico precoce; no entanto, as comparações entre estudos têm sido difíceis, uma vez que diferentes testes são usados e testes com nomes semelhantes podem ser administrados usando um protocolo diferente.
Em uma tentativa de padronizar informações de estudos sobre substâncias neurotóxicas, a noção de uma bateria “central” foi apresentada por um comitê de trabalho da Organização Mundial da Saúde (OMS) (Johnson 1987). Com base no conhecimento da época do encontro (1985), uma série de testes foi selecionada para compor a Neurobehavioral Core Test Battery (NCTB), uma bateria relativamente barata, administrada manualmente, que tem sido utilizada com sucesso em muitos países (Anger e outros 1993). Os testes que compõem essa bateria foram escolhidos para abranger domínios específicos do sistema nervoso, que já haviam se mostrado sensíveis a danos neurotóxicos. Uma bateria básica mais recente, que inclui testes administrados manualmente e computadorizados, foi proposta por um grupo de trabalho da Agência dos Estados Unidos para Substâncias Tóxicas e Registro de Doenças (Hutchison et al. 1992). Ambas as baterias são apresentadas na Tabela 1.
Tabela 1. Exemplos de baterias "centrais" para avaliação de efeitos neurotóxicos precoces
|
Bateria de Teste Núcleo Neurocomportamental (NCTB)+ |
pedido de teste |
Agência para Substâncias Tóxicas e Registro de Doenças Bateria de Teste Neurocomportamental Ambiental para Adultos (AENTB)+ |
||
|
domínio funcional |
Test |
domínio funcional |
Test |
|
|
Estabilidade motora |
Mira (Mira de Perseguição II) |
1 |
Visão |
Acuidade visual, sensibilidade ao contraste próximo |
|
Atenção/velocidade de resposta |
Tempo de Reação Simples |
2 |
Visão de cores (teste dessaturado Lanthony D-15) |
|
|
Percepção da velocidade do motor |
Símbolo de dígito (WAIS-R) |
3 |
Somatosensorial |
Limiar de percepção vibrotátil |
|
Destreza manual |
Santa Ana (Versão de Helsinque) |
4 |
Força motora |
Dinamômetro (incluindo avaliação de fadiga) |
|
Percepção/memória visual |
Benton Retenção Visual |
5 |
Coordenação motora |
Santa Ana |
|
memória auditiva |
Extensão de dígitos (WAIS-R, WMS) |
6 |
Função intelectual superior |
Matrizes progressivas de Raven (revisadas) |
|
Afetar |
POMS (Perfil de Estados de Humor) |
7 |
Coordenação motora |
Teste de digitação (uma mão)1 |
|
8 |
Atenção sustentada (cognitiva), velocidade (motora) |
Tempo de Reação Simples (SRT) (estendido)1 |
||
|
9 |
Codificação cognitiva |
Dígito-símbolo com recuperação atrasada1 |
||
|
10 |
Aprendizagem e memória |
Aprendizagem de dígitos seriais1 |
||
|
11 |
Índice de nível educacional |
Vocabulário1 |
||
|
12 |
Humor |
Escala de humor1 |
||
1 Disponível em versão computadorizada; WAIS = Escala Wechsler de Inteligência para Adultos; WMS = Escala de Memória Wechsler.
Os autores de ambas as baterias principais enfatizam que, embora as baterias sejam úteis para padronizar os resultados, elas não fornecem uma avaliação completa das funções do sistema nervoso. Testes adicionais devem ser usados dependendo do tipo de exposição; por exemplo, uma bateria de testes para avaliar a disfunção do sistema nervoso entre trabalhadores expostos ao manganês incluiria mais testes de funções motoras, particularmente aquelas que requerem movimentos alternados rápidos, enquanto uma para trabalhadores expostos ao metilmercúrio incluiria testes de campo visual. A escolha dos testes para qualquer local de trabalho específico deve ser feita com base no conhecimento atual sobre a ação da toxina ou toxinas específicas às quais as pessoas estão expostas.
Baterias de testes mais sofisticadas, administradas e interpretadas por psicólogos treinados, são uma parte importante da avaliação clínica do envenenamento neurotóxico (Hart 1988). Inclui testes de capacidade intelectual, atenção, concentração e orientação, memória, habilidades visuo-perceptivas, construtivas e motoras, linguagem, funções conceituais e executivas e bem-estar psicológico, bem como uma avaliação de possível simulação. O perfil de desempenho do paciente é examinado à luz do histórico médico e psicológico passado e presente, bem como do histórico de exposição. O diagnóstico final é baseado em uma constelação de déficits interpretados em relação ao tipo de exposição.
Medidas de estado emocional e personalidade
Estudos dos efeitos de substâncias neurotóxicas geralmente incluem medidas de distúrbios afetivos ou de personalidade, na forma de questionários de sintomas, escalas de humor ou índices de personalidade. O NCTB, descrito acima, inclui o Profile of Mood States (POMS), uma medida quantitativa do humor. Usando 65 adjetivos de qualificação de estados de humor nos últimos 8 dias, os graus de tensão, depressão, hostilidade, vigor, fadiga e confusão são derivados. A maioria dos estudos comparativos de exposição a neurotóxicos no local de trabalho indicam diferenças entre expostos e não expostos. Um estudo recente de trabalhadores expostos ao estireno mostra relações dose-resposta entre o nível de ácido mandélico urinário pós-turno, um indicador biológico de estireno, e escalas de tensão, hostilidade, fadiga e confusão (Sassine et al. 1996).
Testes mais longos e sofisticados de afeto e personalidade, como o Minnesota Multiphasic Personality Index (MMPI), que refletem estados emocionais e traços de personalidade, têm sido usados principalmente para avaliação clínica, mas também em estudos no local de trabalho. O MMPI também fornece uma avaliação do exagero de sintomas e respostas inconsistentes. Em um estudo de trabalhadores de microeletrônica com histórico de exposição a substâncias neurotóxicas, os resultados do MMPI indicaram níveis clinicamente significativos de depressão, ansiedade, preocupações somáticas e distúrbios do pensamento (Bowler et al. 1991).
Medidas Eletrofisiológicas
A atividade elétrica gerada pela transmissão de informações ao longo das fibras nervosas e de uma célula para outra pode ser registrada e usada na determinação do que está acontecendo no sistema nervoso de pessoas com exposições tóxicas. A interferência na atividade neuronal pode retardar a transmissão ou modificar o padrão elétrico. Os registros eletrofisiológicos requerem instrumentos precisos e são mais frequentemente realizados em laboratório ou hospital. Houve, no entanto, esforços para desenvolver equipamentos mais portáteis para uso em estudos no local de trabalho.
As medidas eletrofisiológicas registram uma resposta global de um grande número de fibras nervosas e/ou fibras, e uma boa quantidade de dano deve existir antes que possa ser adequadamente registrada. Assim, para a maioria das substâncias neurotóxicas, sintomas, bem como alterações sensoriais, motoras e cognitivas, geralmente podem ser detectados em grupos de trabalhadores expostos antes que diferenças eletrofisiológicas sejam observadas. Para o exame clínico de pessoas com suspeita de distúrbios neurotóxicos, os métodos eletrofisiológicos fornecem informações sobre o tipo e a extensão do dano ao sistema nervoso. Uma revisão das técnicas eletrofisiológicas usadas na detecção de neurotoxicidade precoce em humanos é fornecida por Seppalaïnen (1988).
A velocidade de condução nervosa dos nervos sensoriais (indo em direção ao cérebro) e dos nervos motores (indo para longe do cérebro) é medida por eletroneurografia (ENG). Ao estimular em diferentes posições anatômicas e registrar em outra, a velocidade de condução pode ser calculada. Essa técnica pode fornecer informações sobre as grandes fibras mielinizadas; a diminuição da velocidade de condução ocorre quando a desmielinização está presente. Velocidades de condução reduzidas têm sido freqüentemente observadas entre trabalhadores expostos ao chumbo, na ausência de sintomas neurológicos (Maizlish e Feo 1994). As velocidades lentas de condução dos nervos periféricos também foram associadas a outras neurotoxinas, como mercúrio, hexacarbonos, dissulfeto de carbono, estireno, metil-n-butil cetona, metiletilcetona e certas misturas de solventes. O nervo trigêmeo (um nervo facial) é afetado pela exposição ao tricloroetileno. No entanto, se a substância tóxica agir principalmente em fibras finamente mielinizadas ou não mielinizadas, as velocidades de condução geralmente permanecem normais.
A eletromiografia (EMG) é usada para medir a atividade elétrica nos músculos. Anormalidades eletromiográficas foram observadas entre trabalhadores expostos a substâncias como n-hexano, dissulfeto de carbono, metil-n-butil cetona, mercúrio e certos pesticidas. Essas alterações são frequentemente acompanhadas por alterações na ENG e sintomas de neuropatia periférica.
Alterações nas ondas cerebrais são evidenciadas por eletroencefalografia (EEG). Em pacientes com intoxicação por solventes orgânicos, foram observadas anormalidades locais e difusas de ondas lentas. Alguns estudos relatam evidências de alterações do EEG relacionadas à dose em trabalhadores ativos, com exposição a misturas de solventes orgânicos, estireno e dissulfeto de carbono. Pesticidas organoclorados podem causar convulsões epilépticas, com anormalidades no EEG. Alterações no EEG foram relatadas com exposição prolongada a pesticidas organofosforados e fosfeto de zinco.
Os potenciais evocados (EP) fornecem outro meio de examinar a atividade do sistema nervoso em resposta a um estímulo sensorial. Os eletrodos de registro são colocados na área específica do cérebro que responde aos estímulos específicos, e a latência e a amplitude do potencial lento relacionado ao evento são registradas. Latência aumentada e/ou amplitudes de pico reduzidas foram observadas em resposta a estímulos visuais, auditivos e somatossensoriais para uma ampla gama de substâncias neurotóxicas.
A eletrocardiografia (ECG ou EKG) registra alterações na condução elétrica do coração. Embora não seja frequentemente usado em estudos de substâncias neurotóxicas, foram observadas alterações nas ondas de ECG entre pessoas expostas ao tricloroetileno. Registros eletro-oculográficos (EOG) dos movimentos oculares têm mostrado alterações entre trabalhadores expostos ao chumbo.
Técnicas de imagem cerebral
Nos últimos anos, diferentes técnicas foram desenvolvidas para imagens cerebrais. Imagens de tomografia computadorizada (TC) revelam a anatomia do cérebro e da medula espinhal. Eles têm sido usados para estudar a atrofia cerebral entre trabalhadores e pacientes expostos a solventes; no entanto, os resultados não são consistentes. A ressonância magnética (MRI) examina o sistema nervoso usando um poderoso campo magnético. É particularmente útil clinicamente descartar um diagnóstico alternativo, como tumores cerebrais. A Tomografia por Emissão de Pósitrons (PET), que produz imagens de processos bioquímicos, tem sido usada com sucesso para estudar alterações no cérebro induzidas pela intoxicação por manganês. A tomografia computadorizada por emissão de fóton único (SPECT) fornece informações sobre o metabolismo cerebral e pode ser uma ferramenta importante na compreensão de como as neurotoxinas agem no cérebro. Essas técnicas são todas muito caras e não estão prontamente disponíveis na maioria dos hospitais ou laboratórios em todo o mundo.
Diagnóstico
O diagnóstico de doença neurotóxica não é fácil. Os erros são geralmente de dois tipos: ou não se reconhece que um agente neurotóxico é a causa dos sintomas neurológicos, ou sintomas neurológicos (e especialmente neurocomportamentais) são erroneamente diagnosticados como resultantes de uma exposição ocupacional neurotóxica. Ambos os erros podem ser perigosos, pois o diagnóstico precoce é importante no caso de doença neurotóxica, e o melhor tratamento é evitar a exposição adicional para o caso individual e a vigilância da condição de outros trabalhadores para evitar sua exposição ao mesmo perigo. Por outro lado, às vezes, um alarme indevido pode se desenvolver no local de trabalho se um trabalhador alegar ter sintomas graves e suspeitar de uma exposição química como causa, mas, na verdade, o trabalhador está enganado ou o perigo não está realmente presente para os outros. Também há uma razão prática para procedimentos diagnósticos corretos, já que em muitos países o diagnóstico e tratamento de doenças ocupacionais e a perda da capacidade de trabalho e invalidez causada por essas doenças são cobertos por seguros; assim, a compensação financeira pode ser contestada, se os critérios diagnósticos não forem sólidos. Um exemplo de árvore de decisão para avaliação neurológica é dado na Tabela 1.
Tabela 1. Árvore de decisão para doença neurotóxica
I. Nível, duração e tipo de exposição relevante
II. Sintomas apropriados sintomas crescentes insidiosos do sistema nervoso central (SNC) ou periférico (SNP)
III. Sinais e testes adicionais Disfunção do SNC: neurologia, testes psicológicos Disfunção do SNP: teste sensorial quantitativo, estudos de condução nervosa
XNUMX. Outras doenças excluídas no diagnóstico diferencial
Exposição e Sintomas
As síndromes neurotóxicas agudas ocorrem principalmente em situações acidentais, quando os trabalhadores são expostos a níveis muito elevados de um produto químico ou a uma mistura de produtos químicos, geralmente por inalação. Os sintomas habituais são vertigem, mal-estar e possível perda de consciência como resultado da depressão do sistema nervoso central. Quando o sujeito é removido da exposição, os sintomas desaparecem rapidamente, a menos que a exposição tenha sido tão intensa que ameace a vida, caso em que pode ocorrer coma e morte. Nestas situações, o reconhecimento do perigo devo ocorrer no local de trabalho, e a vítima deve ser levada imediatamente para o ar livre.
Em geral, os sintomas neurotóxicos surgem após exposições de curto ou longo prazo e, muitas vezes, em níveis relativamente baixos de exposição ocupacional. Nesses casos, sintomas agudos podem ter ocorrido no trabalho, mas a presença de sintomas agudos não é necessária para o diagnóstico de encefalopatia tóxica crônica ou neuropatia tóxica. No entanto, os pacientes costumam relatar dor de cabeça, tontura ou irritação da mucosa no final de um dia de trabalho, mas esses sintomas desaparecem inicialmente durante a noite, fim de semana ou férias. Uma lista de verificação útil pode ser encontrada na Tabela 2.
Tabela 2. Efeitos neurofuncionais consistentes de exposições no local de trabalho a algumas das principais substâncias neurotóxicas
|
Solventes orgânicos mistos |
Dissulfeto de carbono |
Estireno |
Organofos- |
Conduzir |
Mercúrio |
|
|
Aquisição |
+ |
|
|
|
+ |
|
|
Afetar |
+ |
|
+ |
|
+ |
|
|
Categorização |
+ |
|
|
|
|
|
|
Codificação |
+ |
+ |
|
|
+ |
+ |
|
Visão de cores |
+ |
|
+ |
|
|
|
|
Mudança de conceito |
+ |
|
|
|
|
|
|
Distração |
|
|
|
|
+ |
|
|
Inteligência |
+ |
+ |
|
+ |
+ |
+ |
|
Memória |
+ |
+ |
+ |
+ |
+ |
+ |
|
Coordenação motora |
+ |
+ |
+ |
|
+ |
+ |
|
A velocidade do motor |
+ |
+ |
+ |
|
+ |
+ |
|
Sensibilidade ao contraste visual próximo |
+ |
|
|
|
|
|
|
Limiar de percepção de odor |
+ |
|
|
|
|
|
|
Identificação de odor |
+ |
|
|
|
+ |
|
|
Personalidade |
+ |
+ |
|
|
|
+ |
|
Relações espaciais |
+ |
+ |
|
|
+ |
|
|
Limiar vibratório |
+ |
|
|
+ |
|
+ |
|
vigilância |
+ |
+ |
|
|
+ |
|
|
Campo visual |
|
|
|
|
+ |
+ |
|
Vocabulário |
|
|
|
|
+ |
|
Fonte: Adaptado de Anger 1990.
Supondo que o paciente tenha sido exposto a substâncias químicas neurotóxicas, o diagnóstico de doença neurotóxica começa com os sintomas. Em 1985, um grupo de trabalho conjunto da Organização Mundial da Saúde e do Conselho Nórdico de Ministros discutiu a questão da intoxicação crônica por solvente orgânico e encontrou um conjunto de sintomas centrais, que são encontrados na maioria dos casos (OMS/Conselho Nórdico 1985). Os principais sintomas são fatigabilidade, perda de memória, dificuldades de concentração e perda de iniciativa. Esses sintomas geralmente começam após uma mudança básica na personalidade, que se desenvolve gradualmente e afeta a energia, o intelecto, a emoção e a motivação. Entre outros sintomas da encefalopatia tóxica crônica estão depressão, disforia, labilidade emocional, dor de cabeça, irritabilidade, distúrbios do sono e tontura (vertigem). Se também houver envolvimento do sistema nervoso periférico, ocorre dormência e possivelmente fraqueza muscular. Esses sintomas crônicos duram pelo menos um ano após o término da própria exposição.
Exame Clínico e Testes
O exame clínico deve incluir um exame neurológico, onde se deve atentar para o comprometimento das funções nervosas superiores, como memória, cognição, raciocínio e emoção; a funções cerebelares prejudicadas, como tremor, marcha, postura e coordenação; e às funções nervosas periféricas, especialmente sensibilidade à vibração e outros testes de sensação. Os testes psicológicos podem fornecer medidas objetivas das funções do sistema nervoso superior, incluindo psicomotora, memória de curto prazo, raciocínio verbal e não verbal e funções perceptivas. No diagnóstico individual, os testes devem incluir alguns testes que dão uma pista sobre o nível intelectual pré-mórbido da pessoa. A história do desempenho escolar e do trabalho anterior, bem como possíveis testes psicológicos administrados anteriormente, por exemplo, em conexão com o serviço militar, podem ajudar na avaliação do nível normal de desempenho da pessoa.
O sistema nervoso periférico pode ser estudado com testes quantitativos de modalidades sensoriais, vibração e termossensibilidade. Estudos de velocidade de condução nervosa e eletromiografia podem frequentemente revelar neuropatia em um estágio inicial. Nesses testes, deve-se dar ênfase especial às funções dos nervos sensoriais. A amplitude do potencial de ação sensorial (SNAP) diminui mais frequentemente do que a velocidade de condução sensorial nas neuropatias axonais, e a maioria das neuropatias tóxicas são de caráter axonal. Estudos neurorradiológicos como tomografia computadorizada (TC) e ressonância magnética (RM) geralmente não revelam nada pertinente à encefalopatia tóxica crônica, mas podem ser úteis no diagnóstico diferencial.
No diagnóstico diferencial devem ser consideradas outras doenças neurológicas e psiquiátricas. Demência de outra etiologia deve ser descartada, bem como depressão e sintomas de estresse de várias causas. Consulta psiquiátrica pode ser necessária. O abuso de álcool é um fator de confusão relevante; o uso excessivo de álcool causa sintomas semelhantes aos da exposição a solventes e, por outro lado, existem trabalhos que indicam que a exposição a solventes pode induzir ao abuso de álcool. Outras causas de neuropatia também devem ser descartadas, especialmente neuropatias de encarceramento, diabetes e doença renal; também o álcool causa neuropatia. A combinação de encefalopatia e neuropatia é mais provável de origem tóxica do que qualquer uma delas isoladamente.
Na decisão final, a exposição deve ser avaliada novamente. Houve exposição relevante, considerando o nível, duração e qualidade da exposição? Os solventes são mais propensos a induzir síndrome psico-orgânica ou encefalopatia tóxica; os hexacarbonos, no entanto, geralmente causam primeiro a neuropatia. Chumbo e alguns outros metais causam neuropatia, embora o envolvimento do SNC possa ser detectado posteriormente.
Neuroepidemiologia Ocupacional
Olav Axelson*
*Adaptado de Axelson 1996.
O conhecimento inicial sobre os efeitos neurotóxicos das exposições ocupacionais surgiu por meio de observações clínicas. Os efeitos observados foram mais ou menos agudos e diziam respeito à exposição a metais como chumbo e mercúrio ou solventes como dissulfeto de carbono e tricloroetileno. Com o tempo, no entanto, efeitos mais crônicos e clinicamente menos óbvios de agentes neurotóxicos foram avaliados por meio de métodos de exame modernos e estudos sistemáticos de grupos maiores. Ainda assim, a interpretação dos resultados tem sido controversa e debatida, como os efeitos crônicos da exposição a solventes (Arlien-Søborg 1992).
As dificuldades encontradas na interpretação dos efeitos neurotóxicos crônicos dependem tanto da diversidade quanto da imprecisão dos sintomas e sinais e do problema associado de definir uma entidade de doença apropriada para estudos epidemiológicos conclusivos. Por exemplo, na exposição a solventes, os efeitos crônicos podem incluir problemas de memória e concentração, cansaço, falta de iniciativa, responsabilidade afetiva, irritabilidade e, às vezes, tontura, dor de cabeça, intolerância ao álcool e libido reduzida. Os métodos neurofisiológicos também revelaram vários distúrbios funcionais, novamente difíceis de condensar em uma única entidade patológica.
Da mesma forma, uma variedade de efeitos neurocomportamentais também parece ocorrer devido a outras exposições ocupacionais, como exposição moderada ao chumbo ou soldagem com alguma exposição a alumínio, chumbo e manganês ou exposição a pesticidas. Novamente também ocorrem sinais neurofisiológicos ou neurológicos, entre outros, polineuropatia, tremor e perturbação do equilíbrio, em indivíduos expostos a organoclorados, organofosforados e outros inseticidas.
Tendo em vista os problemas epidemiológicos envolvidos na definição de uma entidade patológica dentre os vários tipos de efeitos neurocomportamentais referidos, tornou-se também natural considerar alguns transtornos neuropsiquiátricos clinicamente mais ou menos bem definidos em relação a exposições ocupacionais.
Desde a década de 1970, vários estudos têm se concentrado especialmente na exposição a solventes e na síndrome psico-orgânica, quando de gravidade incapacitante. Mais recentemente, também a demência de Alzheimer, esclerose múltipla, doença de Parkinson, esclerose lateral amiotrófica e condições relacionadas atraíram o interesse da epidemiologia ocupacional.
Em relação à exposição a solventes e à síndrome psico-orgânica (ou encefalopatia crônica tóxica na medicina ocupacional clínica, quando a exposição é levada em conta no diagnóstico), o problema de definir uma entidade de doença adequada era aparente e primeiro levou a considerar em bloco os diagnósticos de encefalopatia, demência e atrofia cerebral, mas neurose, neurastenia e nervositas também foram incluídos como não necessariamente distintos entre si na prática médica (Axelson, Hane e Hogstedt 1976). Recentemente, doenças mais específicas, como demência orgânica e atrofia cerebral, também foram associadas à exposição a solventes (Cherry, Labréche e McDonald 1992). Os resultados não foram totalmente consistentes, no entanto, como nenhum excesso de “demência pré-senil” apareceu em um estudo de referência de caso em grande escala nos Estados Unidos com até 3,565 casos de vários distúrbios neuropsiquiátricos e 83,245 referentes hospitalares (Brackbill, Maizlish e Fischbach 1990). No entanto, em comparação com os pedreiros, houve cerca de 45% de excesso de distúrbios neuropsiquiátricos incapacitantes entre os pintores homens brancos, exceto os pintores com spray.
As exposições ocupacionais também parecem desempenhar um papel para distúrbios mais específicos do que a síndrome psico-orgânica. Assim, em 1982, uma associação entre esclerose múltipla e exposição a solventes de colas foi indicada pela primeira vez na indústria italiana de calçados (Amaducci et al. 1982). Essa relação foi consideravelmente fortalecida por estudos adicionais na Escandinávia (Flodin et al. 1988; Landtblom et al. 1993; Grönning et al. 1993) e em outros lugares, de modo que 13 estudos com alguma informação sobre exposição a solventes poderiam ser considerados em uma revisão ( Landtblom et al. 1996). Dez desses estudos forneceram dados suficientes para inclusão em uma meta-análise, mostrando um risco duplo de esclerose múltipla entre indivíduos com exposição a solventes. Alguns estudos também associam a esclerose múltipla com trabalho radiológico, soldagem e trabalho com herbicidas fenoxi (Flodin et al. 1988; Landtblom et al. 1993). A doença de Parkinson parece ser mais comum em áreas rurais (Goldsmith et al. 1990), especialmente em idades mais jovens (Tanner 1989). Mais interessante, um estudo de Calgary, Canadá, mostrou um risco três vezes maior de exposição a herbicida (Semchuk, Love e Lee 1992).
Todas as pessoas com casos que se lembraram de exposições específicas relataram exposição a herbicidas fenoxi ou tiocarbamatos. Um deles lembrou a exposição ao paraquat, que é quimicamente semelhante ao MPTP (N-metil-4-fenil-1,2,3,6-tetraidropiridina), um indutor de uma síndrome semelhante a Parkinson. No entanto, os trabalhadores do paraquat ainda não sofreram de tal síndrome (Howard 1979). Estudos de caso referentes do Canadá, China, Espanha e Suécia indicaram uma relação com a exposição a produtos químicos industriais não especificados, pesticidas e metais, especialmente manganês, ferro e alumínio (Zayed et al. 1990).
Em um estudo dos Estados Unidos, um risco aumentado de doença do neurônio motor (abrangendo esclerose lateral amiotrófica, paralisia bulbar progressiva e atrofia muscular progressiva) apareceu em relação à soldagem e soldagem (Armon et al. 1991). A soldagem também apareceu como um fator de risco, assim como o trabalho com eletricidade e também com agentes de impregnação em um estudo sueco (Gunnarsson et al. 1992). A hereditariedade para doenças neurodegenerativas e da tireoide, combinada com exposição a solventes e sexo masculino, mostrou um risco de até 15.6. Outros estudos também indicam que a exposição ao chumbo e solventes pode ser importante (Campbell, Williams e Barltrop 1970; Hawkes, Cavanagh e Fox 1989; Chio, Tribolo e Schiffer 1989; Sienko et al. 1990).
Para a doença de Alzheimer, nenhuma indicação clara de qualquer risco ocupacional apareceu em uma meta-análise de onze estudos de referência de caso (Graves et al. 1991), mas, mais recentemente, um risco aumentado foi relacionado ao trabalho de colarinho azul (Fratiglioni et al. 1993). ). Outro novo estudo, que incluiu também as idades mais avançadas, indicou que a exposição a solventes pode ser um fator de risco bastante forte (Kukull et al. 1995). A sugestão recente de que a doença de Alzheimer pode estar relacionada à exposição a campos eletromagnéticos foi talvez ainda mais surpreendente (Sobel et al. 1995). Ambos os estudos provavelmente estimularão o interesse em várias novas investigações nas linhas indicadas.
Assim, tendo em vista as perspectivas atuais em neuroepidemiologia ocupacional, conforme brevemente delineado, parece haver uma razão para a realização de estudos adicionais relacionados ao trabalho de diferentes distúrbios neurológicos e neuropsiquiátricos, até então mais ou menos negligenciados. Não é improvável que existam alguns efeitos contribuintes de várias exposições ocupacionais, da mesma forma que vimos para muitos tipos de câncer. Além disso, como na pesquisa etiológica do câncer, novas pistas sugerindo as causas finais ou os mecanismos desencadeantes por trás de alguns dos distúrbios neurológicos graves podem ser obtidos da epidemiologia ocupacional.
Sistemas Renais-Urinários
Os sistemas renal e urinário são compostos por uma série complexa de órgãos que, juntos, funcionam para filtrar os resíduos do sangue e fabricar, armazenar e eliminar a urina. Esses sistemas de órgãos são vitais para a homeostase por meio da manutenção do equilíbrio de fluidos, equilíbrio ácido-base e pressão sanguínea. Os órgãos primários do sistema renal-urinário são os dois rins e a bexiga urinária. No processo de filtragem de resíduos do sangue, os rins são potencialmente expostos a altas concentrações de substâncias tóxicas endógenas e exógenas. Assim, algumas células renais são expostas a concentrações mil vezes maiores do que no sangue.
Os problemas que resultam em dano ao rim podem ser pré-renais (afetam o suprimento de sangue para o rim), renais (afetam o próprio rim) ou pós-renais (afetam qualquer ponto ao longo do caminho que a urina percorre do rim até o fim da uretra ou pênis). Os problemas pós-renais são geralmente de natureza obstrutiva; um local comum de obstrução é a próstata, justaposicionada entre a bexiga e a uretra. Doenças pré-existentes da próstata, bexiga ou ureteres, particularmente infecção, obstrução ou corpos estranhos como cálculos, podem comprometer a função renal e aumentar a suscetibilidade a defeitos adquiridos ou genéticos.
Compreender a microanatomia e os mecanismos moleculares dos rins e da bexiga é importante para avaliar a suscetibilidade, monitorar e prevenir exposições ocupacionais. Os tóxicos parecem ter como alvo partes específicas do rim ou da bexiga e resultam na expressão de biomarcadores específicos diretamente relacionados ao segmento danificado. Historicamente, a predisposição ao adoecimento tem sido vista sob a perspectiva epidemiológica de identificação de um grupo de trabalhadores em situação de risco. Hoje, com uma melhor compreensão dos mecanismos fundamentais da doença, a avaliação de risco individual por meio do uso de biomarcadores de suscetibilidade, exposição, efeito e doença está no horizonte. Novas questões éticas surgem devido à pressão para desenvolver estratégias econômicas para proteger os trabalhadores dos riscos ocupacionais. A pressão surge, em parte, porque os testes genéticos estão ganhando aceitação para avaliar a predisposição a doenças e os biomarcadores de exposição e efeito podem servir como pontos finais intermediários nos quais a intervenção pode ser benéfica. O objetivo deste capítulo é fornecer uma revisão médica dos sistemas renal e urinário com base na qual as diretrizes para avaliar e reduzir o risco individual no local de trabalho podem ser estabelecidas, levando em consideração os aspectos éticos envolvidos.
Anatomia e Fisiopatologia do Rim
O rim humano é um órgão complexo que funciona para filtrar os resíduos do sangue através da produção de urina. Os dois rins também desempenham uma variedade de outras funções vitais, incluindo a manutenção da homeostase, regulação da pressão sanguínea, pressão osmótica e equilíbrio ácido-base. Os rins recebem 25% do débito cardíaco total de sangue, expondo-os potencialmente a toxinas endógenas e exógenas.
Os rins estão localizados em cada lado da coluna vertebral na parte inferior das costas. Cada um pesa cerca de 150 gramas e tem aproximadamente o tamanho de uma laranja. O rim consiste em três camadas: o córtex (camada externa), a medula e a pelve renal. O sangue flui para o córtex e a medula através da artéria renal e se ramifica em artérias cada vez menores. Cada uma das artérias termina em uma unidade de filtração do sangue chamada néfron. Um rim saudável contém aproximadamente 1.2 milhão de néfrons, estrategicamente posicionados no córtex e na medula.
Um néfron consiste no glomérulo (um grupo de minúsculos vasos sanguíneos) cercado pela cápsula de Bowman (uma membrana de duas camadas) que se abre em um túbulo contorcido. A porção fluida do sangue, o plasma, é forçada através do glomérulo para a cápsula de Bowman e então, como plasma filtrado, passa para o túbulo contorcido. Cerca de 99% da água e nutrientes essenciais que foram filtrados são reabsorvidos pelas células tubulares e passam para os capilares que circundam o túbulo contorcido. O sangue não filtrado que permanece no glomérulo também flui para os capilares e retorna pela veia renal ao coração.
Os néfrons aparecem como longos dutos em loop compostos por vários segmentos, cada um dos quais desempenha uma variedade de funções diferentes destinadas a manter os mecanismos homeostáticos do corpo. A Figura 1 mostra um néfron e sua orientação dentro do córtex renal e da medula. Cada segmento do néfron tem um suprimento sanguíneo diferencial que regula o gradiente iônico. Certos produtos químicos podem afetar diretamente segmentos específicos do néfron de forma aguda ou crônica, dependendo do tipo e da dose de exposição ao xenobiótico. Dependendo do segmento da microanatomia alvo, vários aspectos da função renal podem ser afetados.
Figura 1. Relações entre o suprimento vascular, o glomérulo e os componentes tubulares do néfron e a orientação desses componentes no córtex e na medula renal
Os vasos sanguíneos para o rim fornecem apenas os elementos glomerulares e tubulares, entregando resíduos a serem filtrados e absorvendo nutrientes, proteínas e eletrólitos, além de fornecer oxigênio para a viabilidade do órgão. Noventa por cento do fluxo sanguíneo é para o córtex, com uma diminuição do gradiente para a medula. Esse fluxo sanguíneo diferencial e o posicionamento das unidades de néfrons são vitais para o mecanismo de contracorrente que concentra ainda mais a urina e as potenciais nefrotoxinas.
O glomérulo está posicionado entre as arteríolas aferentes e eferentes. As arteríolas eferentes formam uma teia de capilares ao redor de cada unidade de néfron, com exceção da justaposição do túbulo distal adjacente ao suprimento sanguíneo aferente do glomérulo. Os túbulos aferentes e eferentes enervados pelos nervos simpáticos respondem à estimulação autonômica e a mediadores hormonais, como vasopressão e hormônio antidiurético (ADH). Uma área chamada mácula densa, parte do aparelho justaglomerular, produz renina, um mediador da pressão sanguínea, em resposta às alterações osmóticas e à pressão sanguínea. A renina é convertida por enzimas hepáticas em um octapeptídeo, a angiotensina II, que regula o fluxo sanguíneo para os rins, preferencialmente visando as arteríolas aferentes e as células mesangiais do glomérulo.
O glomérulo permite que apenas certas proteínas de tamanho com carga definida passem durante a filtração. A filtração de plasma é controlada por um equilíbrio de pressão osmótica e hidrostática. Moléculas de açúcar especializadas, glicosaminoglicanos, fornecem carga aniônica negativa que inibe, por forças eletrostáticas, a filtração de materiais carregados negativamente. A camada de três células da membrana basal glomerular consiste em múltiplos processos pélvicos que aumentam a área de absorção e criam os poros através dos quais o filtrado passa. Danos à membrana basal especializada ou ao endotélio capilar podem permitir que a albumina, um tipo de proteína, seja derramada em quantidades maiores na urina. A presença de uma quantidade excessiva de albumina ou outras microproteínas na urina serve como um marcador de dano glomerular ou tubular.
O interstício renal é o espaço entre as unidades de néfrons e é mais proeminente na porção medular central do que no córtex externo. Dentro do interstício estão as células intersticiais que estão próximas aos vasos sanguíneos medulares e às células dos túbulos. Com o envelhecimento pode haver um aumento da proeminência das células intersticiais no córtex com fibrose e cicatrização associadas. As células intersticiais contêm gotículas lipídicas e podem estar envolvidas no controle da pressão arterial com a liberação de fatores relaxantes ou constritores vasculares. A doença crônica do interstício pode afetar o glomérulo e os túbulos ou, inversamente, a doença do glomérulo e dos túbulos pode afetar o interstício. Assim, na doença renal terminal, às vezes é difícil definir com precisão os mecanismos patológicos da insuficiência renal.
Os túbulos coletores proximais absorvem 80% do sódio, água e cloreto e 100% da uréia. Cada túbulo proximal tem três segmentos, sendo o último segmento (P-3) o mais vulnerável a exposições a xenobióticos (substâncias estranhas tóxicas). Quando as células proximais são danificadas por metais pesados, como o cromo, a capacidade de concentração do rim é prejudicada e a urina pode ser mais diluída. A toxicidade para o segmento P-3 resulta na liberação na urina de enzimas, como fosfatase alcalina intestinal, N-acetil-beta-D-glucosaminidase (NAG) ou proteína Tamm-Horsfall, que está associada à borda das células do túbulo proximal aumentando a área de absorção efetiva.
Diagnóstico e Teste de Nefrotoxicidade
A creatinina sérica é outra substância filtrada pelo glomérulo, mas minimamente absorvida pelos túbulos proximais. A lesão do glomérulo resulta na sua incapacidade de eliminar as toxinas produzidas pelo organismo e há acúmulo de creatinina sérica. Por ser um produto do metabolismo muscular e dependente da massa corporal do paciente, a creatinina sérica tem baixa sensibilidade e especificidade para medir a função renal, mas é usada com frequência por sua conveniência. Um teste mais sensível e específico é quantificar o filtrado medindo a depuração da creatinina (Cr); a depuração da creatinina urinária sérica é calculada pela fórmula geral CCr=UCr V/PCr, Onde UCrV é a quantidade de Cr excretada por unidade de tempo e PCr é a concentração plasmática de Cr. No entanto, a depuração da creatinina é mais complexa em termos de amostragem para o teste e, portanto, impraticável para testes ocupacionais. Os testes de eliminação de isótopos realizados por marcação radioativa de compostos como o orto-iodoipurato, que também são eliminados pelo rim, também são eficazes, mas não são práticos ou econômicos no ambiente de trabalho. A função diferencial de rins individuais pode ser determinada usando varreduras nucleares renais diferenciais ou cateterismo seletivo de ambos os rins pela passagem de um cateter da bexiga até o ureter até o rim. No entanto, esses métodos também não são prontamente empregados para testes em locais de trabalho em larga escala. Como a função renal pode ser reduzida em 70 a 80% antes de uma elevação detectável na creatinina sérica, e porque outros testes existentes são impraticáveis ou caros, biomarcadores não invasivos são necessários para detectar exposições intermitentes agudas de baixa dose ao rim. Vários biomarcadores para detectar danos renais de baixa dose ou alterações precoces associadas à carcinogênese são discutidos na seção sobre biomarcadores.
Embora as células dos túbulos proximais absorvam 80% dos fluidos, o mecanismo de contracorrente e os ductos coletores distais ajustam a quantidade de fluidos absorvidos pela regulação do ADH. O ADH é liberado da glândula pituitária profundamente dentro do cérebro e responde a pressões osmóticas e volume de fluido. Compostos exógenos, como o lítio, podem danificar os ductos coletores distais e resultar em diabetes insipidus renal (passagem de urina diluída). Distúrbios genéticos hereditários também podem causar esse defeito. Os xenobióticos normalmente afetam ambos os rins, mas surgem complexidades de interpretação quando as exposições são difíceis de documentar ou quando há doença renal pré-existente. Consequentemente, exposições acidentais a altas doses serviram como marcadores para identificar compostos nefrotóxicos em muitos casos. A maioria das exposições ocupacionais ocorre em doses baixas e são mascaradas pela filtração de reserva e capacidade compensatória de reparo (hipertrofia) do rim. O desafio que permanece é detectar exposições de baixa dose clinicamente não detectadas pelos métodos atuais.
Anatomia e Fisiopatologia da Bexiga
A bexiga urinária é uma bolsa oca na qual a urina é armazenada; normalmente, ele se contrai sob demanda para esvaziamento controlado pela uretra. A bexiga está localizada na parte frontal inferior da cavidade pélvica. A bexiga é unida em ambos os lados aos dois rins por tubos peristálticos musculares, os ureteres, que transportam a urina dos rins para a bexiga. A pelve renal, os ureteres e a bexiga são revestidos por epitélio de transição. A camada externa do urotélio consiste em células guarda-chuva revestidas com uma camada de carboidrato, glicosaminoglicano (GAG). As células de transição se estendem até a membrana basal da bexiga. As células basais profundas são, portanto, protegidas pelas células guarda-chuva, mas se a camada protetora de GAG for danificada, as células basais são suscetíveis a lesões por componentes urinários. A microanatomia do epitélio de transição permite que ele se expanda e contraia, e mesmo com a descamação normal das células guarda-chuva, a integridade protetora das células basais é mantida.
O sistema neurológico equilibrado que regula o armazenamento e o esvaziamento pode ser danificado durante o choque elétrico ou outro trauma, como lesão da medula espinhal, ocorrido no local de trabalho. Uma das principais causas de morte entre tetraplégicos é a perda da função da bexiga, resultando em dano renal crônico secundário a infecção e formação de cálculos. Infecção crônica por esvaziamento incompleto devido a causas neurogênicas ou obstrutivas, como fratura pélvica ou outro trauma na uretra e subsequente formação de estenose, é comum. Infecção bacteriana persistente ou formação de cálculos que resultam em condições inflamatórias e malignas crônicas da bexiga podem ser causadas por resistência reduzida (ou seja, suscetibilidade) a exposições exógenas no local de trabalho.
Moléculas associadas com dano e reparo dentro da bexiga servem como potenciais marcadores intermediários para condições tóxicas e malignas porque muitas alterações bioquímicas ocorrem durante as mudanças relacionadas ao desenvolvimento do câncer. Como o rim, as células da bexiga possuem sistemas enzimáticos ativos, como o citocromo P-450, que podem ativar ou inativar os xenobióticos. A atividade funcional das enzimas é determinada por herança genética e exibe polimorfismo genético. A urina anulada contém células esfoliadas do rim, ureteres, bexiga, próstata e uretra. Essas células fornecem alvos, por meio do uso de biomarcadores, para avaliar alterações na bexiga e patologia renal. Relembrar o comentário de Virchow de que todas as doenças começam nas células chama nossa atenção para a importância das células, que são o espelho molecular dos episódios de exposição.
Toxicologia Ambiental e Ocupacional
Um volume considerável de dados epidemiológicos apóia a relação causal das exposições ocupacionais no câncer de bexiga, mas as contribuições precisas das exposições no local de trabalho à insuficiência renal e ao câncer renal são difíceis de estimar. Em um relatório recente, estimou-se que até 10% das doenças renais em estágio terminal podem ser atribuídas a exposições no local de trabalho, mas os resultados são difíceis de validar devido à mudança de riscos químicos e ambientais, variações nos critérios de diagnóstico e o frequentemente longo período de latência entre a exposição e a doença. Estima-se que a função de dois terços dos néfrons de ambos os rins pode ser perdida antes que o dano renal seja clinicamente evidente. No entanto, há cada vez mais evidências de que o que antes se pensava serem causas socioeconômicas ou étnicas de nefrotoxicidade podem, na verdade, ser ambientais, acrescentando validade ao papel dos tóxicos no desenvolvimento da doença.
A nefrotoxicidade pode estar diretamente relacionada ao xenobiótico, ou o xenobiótico pode passar por uma ativação ou inativação em uma ou várias etapas no rim ou no fígado. A ativação de xenobióticos é regulada por conjuntos complexos de enzimas identificadas como Fase I, II e Auxiliar. Uma das enzimas da Fase I é o sistema oxidativo P-450 que atua pelas vias de redução ou hidrólise. As enzimas da Fase II catalisam a conjugação enquanto as enzimas auxiliares regulam o metabolismo de drogas (a Tabela 1 lista essas enzimas). Vários modelos animais forneceram informações sobre os mecanismos metabólicos, e estudos de fatias renais e microdissecção das unidades de néfrons renais em cultura de tecidos adicionam informações sobre os mecanismos patológicos. No entanto, espécies e variáveis individuais são consideráveis e, embora os mecanismos possam ser semelhantes, é necessário cautela ao extrapolar os resultados para humanos no local de trabalho. As principais questões agora são determinar quais xenobióticos são nefrotóxicos e/ou carcinogênicos, e para quais locais-alvo, e desenvolver métodos para identificar com mais precisão a toxicidade subclínica no sistema renal-urinário.
Tabela 1. Enzimas do metabolismo de drogas no rim1
| ENZIMAS | ||
| fase I | Fase II | Auxiliar |
| Citocromo P-450 | Esterase | peróxidos de GSH |
| Monooxigenase contendo FAD microssomal | N-Acetiltransferase | GSSG redutase |
| Álcool e aldeído desidrogenases | GSH S-transferase | Superoxido dismutação |
| Epóxido hidrolase | Tiol S-metil-transferase | Catalase |
| Prostaglandina sintase | UDP glucuronosiltransferase | DT-diaforase |
| Monoamina oxidase | Sulfotransferase | Vias geradoras de NADPH |
1 As enzimas da Fase I catalisam oxidação, redução ou hidrólise.
As enzimas da Fase II geralmente catalisam a conjugação.
As enzimas auxiliares funcionam de maneira secundária ou de suporte para facilitar o metabolismo do fármaco.
Fonte: Conselho Nacional de Pesquisa 1995.
Distúrbios Renais-Urinários Não Malignos
A glomerulonefrite é uma condição inflamatória reativa da membrana basal glomerular ou do endotélio capilar. As formas aguda e crônica da doença são causadas por uma variedade de condições infecciosas, autoimunes ou inflamatórias ou pela exposição a agentes tóxicos. A glomerulonefrite está associada à vasculite, seja sistêmica ou limitada ao rim. Danos crônicos secundários ao glomérulo também ocorrem durante um ciclo intenso de ataque de nefrotoxicidade ao interstício das células tubulares. Crescentes glomerulares epiteliais ou formas proliferativas são uma característica da glomerulonefrite em espécimes de biópsia renal. Sangue, cilindros de glóbulos vermelhos (RBC) ou proteína na urina e hipertensão são sintomas de glomerulonefrite. Uma alteração nas proteínas sanguíneas pode ocorrer com diminuição de certas frações do complemento sérico, um conjunto complexo de proteínas interativas envolvidas no sistema imunológico, defesas do hospedeiro e funções de coagulação. Evidências diretas e indiretas apóiam a importância dos xenobióticos como fator causal da glomerulonefrite.
O glomérulo protege os glóbulos vermelhos que transportam oxigênio de passar por seu filtro. Após a centrifugação, a urina normal contém apenas uma hemácia em 10 ml quando visualizada com microscopia de alta potência. Quando os eritrócitos vazam através do filtro glomerular e talvez se tornem individualmente dismórficos, formam-se cilindros eritrocitários que assumem a forma cilíndrica dos néfrons coletores.
Em apoio à importância das toxinas como fator etiológico na glomerulonefrite, estudos epidemiológicos revelam evidências crescentes de exposições tóxicas em pacientes submetidos a diálise ou diagnosticados com glomerulonefrite. A evidência de lesão glomerular por exposição aguda a hidrocarbonetos é rara, mas tem sido observada em estudos epidemiológicos, com odds ratio variando de 2.0 a 15.5. Um exemplo de toxicidade aguda é a doença de Goodpasture, que resulta da estimulação de hidrocarbonetos da produção de anticorpos para proteínas hepáticas e pulmonares que reagem de forma cruzada com a membrana basal. A exacerbação da síndrome nefrótica, grandes quantidades de proteína na urina, também foi observada em indivíduos reexpostos a solventes orgânicos, enquanto outros estudos revelam uma relação histórica com um espectro de distúrbios renais. Outros solventes como desengordurantes, tintas e colas estão implicados em formas mais crônicas da doença. O conhecimento dos mecanismos de excreção e reabsorção de solventes auxilia na identificação de biomarcadores porque mesmo um dano mínimo ao glomérulo resulta em aumento do vazamento de hemácias na urina. Embora os eritrócitos na urina sejam um sinal fundamental de lesão glomerular, é importante descartar outras causas de hematúria.
Nefrite intersticial e tubular. Como mencionado anteriormente, a etiologia da doença renal crônica terminal é frequentemente difícil de determinar. Pode ter origem principalmente glomerular, tubular ou intersticial e ocorrer devido a múltiplos episódios agudos ou processos crônicos de baixa dosagem. A nefrite intersticial crônica envolve fibrose e atrofia tubular. Em sua forma aguda, a doença se expressa por infiltrado inflamatório acentuado com acúmulo de líquido nos espaços intersticiais. A nefrite intersticial pode envolver principalmente o interstício, ou se manifestar como um evento secundário de lesão tubular crônica, ou pode resultar de causas pós-renais, como obstrução. A prostaglandina-A sintase, uma enzima, é encontrada principalmente no interstício e está associada ao retículo endoplasmático, uma parte da maquinaria protéica da célula. Certos xenobióticos, como benzidina e nitrofuranos, são co-substratos redutores da prostaglandina sintase e são tóxicos para o interstício tubular.
Lesões tubulares e intersticiais podem ocorrer devido à exposição ao cádmio, chumbo ou uma variedade de solventes orgânicos. A maioria das exposições são crônicas, de baixa dose e a toxicidade é mascarada pela reserva da função renal e pela capacidade do rim de recuperar algumas funções. A nefrite intersticial também pode resultar de lesão vascular causada, por exemplo, pela exposição crônica ao monóxido de carbono. As células dos túbulos proximais são as mais vulneráveis a substâncias tóxicas no sangue devido à intensa exposição a toxinas que se filtram através do glomérulo, sistemas enzimáticos internos que ativam substâncias tóxicas e o transporte seletivo de substâncias tóxicas. O epitélio nos vários segmentos do túbulo proximal tem qualidades ligeiramente diferentes de enzimas peroxidase lisossomal e outros compostos da maquinaria genética. Assim, a exposição ao cromo pode resultar em lesões intersticiais e tubulares. Danos aos túbulos coletores podem ocorrer quando enzimas específicas ativam vários xenobióticos, como clorofórmio, acetaminofeno e p-aminofenol e antibióticos como a Loradina. Um resultado secundário do dano aos dutos coletores é a incapacidade do rim de acidificar a urina e o subseqüente desenvolvimento de um estado de ácido metabólico.
Diabetes insípido nefrogênico, a condição na qual a urina se torna diluída, pode ser genética ou adquirida. A forma genética envolve mutações dos receptores de ADH que se localizam na membrana basal lateral dos ductos coletores, na alça descendente de Henle. ADH ajusta a reabsorção de água e certos íons, como o potássio. O diabetes insipidus adquirido pode envolver as células tubulares ou o interstício associado, ambos os quais podem estar doentes devido a uma variedade de condições. O diabetes insipidus nefrogênico pode acompanhar a doença renal terminal devido ao envolvimento difuso do interstício. Consequentemente, o interstício é incapaz de manter um ambiente hipertônico para o movimento passivo de água dos ductos coletores tubulares. As condições que podem causar alterações intersticiais difusas são pielonefrite, anemia falciforme e uropatia obstrutiva. A possível associação dessas condições em relação à exposição ocupacional é uma maior suscetibilidade do rim aos xenobióticos. Foi identificado um número limitado de compostos nefrotóxicos que visam especialmente as células dos túbulos coletores. Frequência, noctúria (micção mais frequente à noite) e polidipsia (sede crônica) são sintomas de diabetes insípido nefrogênico. O movimento de fluidos através das células do ducto coletor resulta em canais que se formam em resposta ao ADH, afetando a função microtubular das células; conseqüentemente, drogas como a colchicina podem afetar o ADH. Duas drogas que parecem agir por mecanismos ligeiramente diferentes para corrigir o ADH são a hidroclorotiazida e a indometacina, um inibidor da prostaglandina sintase.
O diabetes insipidus induzido por lítio se correlaciona com a duração da terapia com lítio, nível sérico médio de lítio e dose total de carbonato de lítio. Curiosamente, o lítio se concentra nos dutos coletores e afeta o AMP cíclico, parte da via da bomba metabólica de energia. A exposição a outros compostos, como o metoxiflurano e a demeclociclina, esta última utilizada no tratamento da acne, também resulta em diabetes insípido nefrogênico por meio de uma via alternativa que torna as células epiteliais não responsivas ao ADH.
Hipertensão, ou pressão arterial elevada, a segunda causa mais comum de doença renal terminal, está associada a múltiplas vias etiológicas. A hipertensão pode ser causada por nefropatia diabética, nefropatia obstrutiva, glomerulonefrite, doença renal policística, pielonefrite e vasculite, e muitas dessas doenças estão associadas à exposição a compostos tóxicos. Um número limitado de exposições ocupacionais está diretamente associado à hipertensão. Um deles é o chumbo, que causa isquemia e lesão vascular renal. O mecanismo da hipertensão induzida pelo chumbo é provavelmente regulado pelo aparelho justaglomerular, pela liberação de renina e pela clivagem da renina pelas enzimas hepáticas em angiotensina II. Drogas implicadas na hipertensão incluem anfetaminas, estrogênios e contraceptivos orais, esteróides, cisplatina, álcool e antidepressivos tricíclicos. A hipertensão pode ser gradual no início ou aguda e de natureza maligna. A hipertensão maligna na qual a pressão diastólica é superior a 110 mm Hg está associada a náuseas, vômitos e cefaléia intensa e constitui uma emergência médica. Numerosos medicamentos estão disponíveis para o tratamento da hipertensão, mas o tratamento excessivo pode resultar em diminuição da perfusão renal e perda adicional da função renal. Sempre que possível, a retirada do nefrotóxico é o tratamento de escolha.
Diagnóstico diferencial de hematúria e proteinúria
Hematúria (hemácias na urina) e piúria (glóbulos brancos na urina) são sintomas primários de muitas doenças do sistema renal-urinário e, para fins categóricos, podem ser considerados biomarcadores celulares não específicos. Devido à sua importância, eles são discutidos separadamente aqui. Um desafio para o profissional ocupacional é determinar se a hematúria significa uma condição médica subjacente permanente que pode ser potencialmente fatal ou se é atribuível a exposições ocupacionais. A avaliação clínica da hematúria requer padronização e determinação se é de origem pré-renal, renal ou pós-renal.
A hematúria pode ser derivada de lesões no rim per se ou em qualquer lugar ao longo do caminho da micção. Os locais de origem incluem o rim, pelve renal coletora, ureteres, bexiga, próstata e uretra. Devido às doenças graves associadas à hematúria, um único episódio justifica uma avaliação médica ou urológica. Mais de um eritrócito por campo de grande aumento pode ser um sinal de doença, mas hematúria significativa pode ser perdida na análise microscópica na presença de urina hipotônica (diluída) que pode lisar eritrócitos. A pseudo-hematúria pode ser causada por beterraba, frutas vermelhas, corantes vegetais e uratos concentrados. A hematúria inicial sugere uma origem uretral, a hematúria terminal geralmente é de origem prostática e o sangue durante a micção vem da bexiga, rim ou ureter. A hematúria macroscópica está associada a tumores de bexiga em 21% dos casos, mas a hematúria microscópica é muito menos frequente (2.2 a 12.5%).
Encontrar células dismórficas quando a hematúria é avaliada quantitativamente sugere uma origem no trato superior, particularmente quando associada a cilindros de hemácias. Compreender a hematúria em relação à proteinúria fornece informações adicionais. O dispositivo de filtração glomerular exclui quase completamente as proteínas de peso molecular superior a 250,000 Daltons, enquanto as proteínas de baixo peso molecular são livremente filtradas e absorvidas normalmente pelas células tubulares. A presença de proteínas de alto peso molecular na urina sugere sangramento do trato inferior, enquanto proteínas de baixo peso molecular estão associadas a lesão tubular. A avaliação da proporção de α-microglobulina para albumina e α-macroglobulina para albumina ajuda a delinear glomerular de nefropatia intersticial tubular e sangramento do trato inferior potencialmente associado a neoplasia urotelial e outras causas pós-renais, como infecções do trato urinário.
Um problema especial de diagnóstico surge quando dois ou mais processos patológicos que causam os mesmos sintomas estão presentes simultaneamente. Por exemplo, a hematúria é observada tanto na neoplasia urotelial quanto nas infecções do trato urinário. Em um paciente com ambas as doenças, se a infecção for tratada e resolvida, o câncer permanecerá. Portanto, é importante identificar a verdadeira causa dos sintomas. A hematúria está presente em 13% das populações rastreadas; aproximadamente 20% dos indivíduos têm distúrbios renais ou da bexiga significativos e 10% deles desenvolverão malignidade geniturinária. Consequentemente, a hematúria é um importante biomarcador de doença que deve ser adequadamente avaliado.
A interpretação clínica da hematúria é aprimorada pelo conhecimento da idade e do sexo do paciente, conforme indicado na Tabela 2, que mostra as causas da hematúria em relação à idade e ao sexo do paciente. Outras causas de hematúria incluem trombose da veia renal, hipercalciúria e vasculite, bem como trauma, como corrida ou outros esportes, e eventos ou exposições ocupacionais. A avaliação clínica da hematúria requer um raio-x do rim, pielograma intravenoso (PIV), para descartar doenças do trato superior, incluindo cálculos renais e tumores, e uma cistoscopia (observação da bexiga através de um instrumento iluminado) para excluir bexiga, próstata ou urotelial cânceres. Causas vaginais sutis devem ser excluídas em mulheres. Independentemente da idade do paciente, uma avaliação clínica é indicada se ocorrer hematúria e, dependendo da etiologia identificada, avaliações sequenciais de acompanhamento podem ser indicadas.
Tabela 2. Causas mais comuns de hematúria, por idade e sexo
| 0-20 anos | 40–60 anos (mulheres) |
| Glomerulonefrite aguda Infecção urinária aguda Anomalias congênitas do trato urinário com obstrução |
Infecção urinária aguda Pedras Tumor de bexiga |
| 20-40 anos | 60+ anos (masculino) |
| Infecção urinária aguda Pedras Tumor de bexiga |
A hiperplasia prostática benigna Tumor de bexiga Infecção urinária aguda |
| 40–60 anos (homens) | 60+ anos (mulheres) |
| Tumor de bexiga Pedras Infecção urinária aguda |
Tumores de bexiga Infecção urinária aguda |
Fonte: Wyker 1991.
O uso de biomarcadores recentemente identificados em conjunto com citologia convencional para avaliação de hematúria ajuda a garantir que nenhuma malignidade oculta ou incipiente seja perdida (consulte a próxima seção sobre biomarcadores). Para o especialista ocupacional, é importante determinar se a hematúria é resultado de exposição tóxica ou malignidade oculta. O conhecimento da exposição e a idade do paciente são parâmetros críticos para tomar uma decisão informada sobre o manejo clínico. Um estudo recente demonstrou que, juntos, a hematúria e a análise de biomarcadores em células urinárias esfoliadas da bexiga foram os dois melhores marcadores para detectar lesões pré-malignas da bexiga. A hematúria é observada em todos os casos de lesão glomerular, em apenas 60% dos pacientes com câncer de bexiga e em apenas 15% dos pacientes com malignidades do próprio rim. Assim, a hematúria continua sendo um sintoma cardinal da doença renal e pós-renal, mas o diagnóstico final pode ser complexo.
Testes de nefrotoxicidade: biomarcadores
Historicamente, o monitoramento de toxinas no ambiente de trabalho tem sido o principal método de identificação de riscos. No entanto, nem todos os tóxicos são conhecidos e, portanto, não podem ser monitorados. Além disso, a suscetibilidade é um fator que determina se os xenobióticos afetarão os indivíduos.
Figura 2. Categorias de biomarcadores.
Os biomarcadores fornecem novas oportunidades para definir o risco individual. Para fins descritivos e para fornecer uma estrutura para interpretação, os biomarcadores foram classificados de acordo com o esquema representado na Figura 2. Como em outras doenças, os biomarcadores de nefrotoxicidade e toxicidade geniturinária podem estar relacionados à suscetibilidade, exposição, efeito ou doença. Os biomarcadores podem ser genotípicos ou fenotípicos e podem ser funcionais, celulares ou solúveis na urina, sangue ou outros fluidos corporais. Exemplos de marcadores solúveis são proteínas, enzimas, citocinas e fatores de crescimento. Os biomarcadores podem ser testados como gene, mensagem ou produto proteico. Esses sistemas variáveis aumentam a complexidade da avaliação e seleção de biomarcadores. Uma vantagem de testar a proteína é que ela é a molécula funcional. O gene pode não ser transcrito e a quantidade de mensagem pode não corresponder ao produto proteico. Uma lista de critérios para seleção de biomarcadores é mostrada na Tabela 3.
Tabela 3. Critérios para seleção de biomarcadores
| Utilidade clínica | Considerações do ensaio |
| Biomarcador forte | Estabilidade do reagente |
| Sensibilidade | Custo do reagente |
| Especificidade | Requisitos de fixação |
| Valor preditivo negativo | Reprodutibilidade do ensaio |
| Valor preditivo positivo | Parâmetros sensatos da máquina |
| papel funcional | Contribuição para o perfil do biomarcador |
| Sequência na oncogênese | Adaptabilidade à automação |
Fonte: Hemstreet et al. 1996.
O compromisso científico internacional de mapear o genoma humano, possibilitado pelos avanços da biologia molecular, estabeleceu as bases para a identificação de biomarcadores de suscetibilidade. A maioria dos casos de doenças humanas, especialmente aquelas resultantes da exposição ambiental a substâncias tóxicas, envolve uma constelação de genes que refletem uma diversidade genética acentuada (polimorfismo genético). Um exemplo de tal produto gênico, como mencionado anteriormente, é o sistema de enzima oxidativa P-450 que pode metabolizar xenobióticos no fígado, rim ou bexiga. Os fatores de suscetibilidade também podem controlar o mecanismo básico de reparo do DNA, influenciar a suscetibilidade de várias vias de sinalização importantes para a tumorigênese (ou seja, fatores de crescimento) ou estar relacionados a condições hereditárias que predispõem à doença. Um exemplo importante de um fator de suscetibilidade herdado é o fenótipo de acetilação lenta ou rápida que regula a acetilação e a inativação de certas aminas aromáticas conhecidas por causar câncer de bexiga. Biomarcadores de suscetibilidade podem incluir não apenas genes que regulam a ativação de xenobióticos, mas também proto-oncogenes e supressores-oncogenes. O controle do crescimento de células tumorais envolve uma série de sistemas complexos e interativos. Estes incluem um equilíbrio de oncogenes positivos (proto) e oncogenes negativos (supressores). Os proto-oncogenes controlam o crescimento e desenvolvimento celular normal, enquanto os oncogenes supressores controlam a divisão e diferenciação celular normal. Outros genes podem contribuir para condições pré-existentes, como propensão à insuficiência renal desencadeada por condições subjacentes, como doença renal policística.
Um biomarcador de exposição pode ser o próprio xenobiótico, o metabólito metabólico ou marcadores como adutos de DNA. Em alguns casos, o biomarcador pode estar ligado a uma proteína. Os biomarcadores de exposição também podem ser biomarcadores de efeito, se o efeito for transitório. Se um biomarcador de efeito persistir, ele pode se tornar um biomarcador de doença. Biomarcadores úteis de efeito têm alta associação com um tóxico e são indicativos de exposição. Para a detecção de doenças, a expressão do biomarcador em sequência próxima ao início da doença terá a maior especificidade. A sensibilidade e especificidade esperadas de um biomarcador dependem do risco versus benefício da intervenção. Por exemplo, um biomarcador como a F-actina, um marcador de diferenciação de proteínas do citoesqueleto, que parece alterado na carcinogênese inicial pode ter uma especificidade pobre para a detecção de estados pré-cancerígenos porque nem todos os indivíduos com um marcador anormal irão progredir para a doença. Pode, no entanto, ser útil para selecionar indivíduos e monitorá-los durante a quimioprevenção, desde que a terapia seja atóxica. Compreender o período de tempo e a ligação funcional entre biomarcadores individuais é extremamente importante para a avaliação de risco individual e para compreender os mecanismos de carcinogênese e nefrotoxicidade.
Biomarcadores de nefrotoxicidade
Os biomarcadores de nefrotoxicidade podem estar relacionados com a etiologia da insuficiência renal (ou seja, pré-renal, renal ou pós-renal) e os mecanismos envolvidos na patogénese do processo. Este processo inclui dano celular e reparação. A lesão tóxica pode afetar as células, glomérulo, interstício ou túbulos com liberação de biomarcadores correspondentes. Os xenobióticos podem afetar mais de um compartimento ou podem causar alterações nos biomarcadores devido à interdependência das células dentro do compartimento. Alterações inflamatórias, processos autoimunes e processos imunológicos promovem ainda mais a liberação de biomarcadores. Os xenobióticos podem atingir um compartimento em algumas circunstâncias e outro em diferentes condições. Um exemplo é o mercúrio que é agudamente nefrotóxico para o túbulo proximal enquanto cronicamente afeta as arteríolas. A resposta à lesão pode ser dividida em várias categorias principais, incluindo hipertrofia, proliferação, degeneração (necrose e apoptose ou morte celular programada) e alterações de membrana.
A maioria dos fatores de suscetibilidade está relacionada à doença renal não associada a xenobióticos. No entanto, 10% dos casos de insuficiência renal são atribuídos a exposições ambientais a compostos tóxicos ou indução iatrogênica por vários compostos, como antibióticos, ou procedimentos como a administração de contraste de raios-x renal a um diabético. No local de trabalho, a identificação de insuficiência renal subclínica antes de potencial estresse nefrotóxico adicional tem potencial utilidade prática. Se um composto for suspeito de ser xenobiótico e resultar em um efeito específico na via causal da doença, a intervenção para reverter o efeito é uma possibilidade. Assim, os biomarcadores de efeito eliminam muitos dos problemas de cálculo da exposição e definição da suscetibilidade individual. A análise estatística de biomarcadores de efeito em relação aos biomarcadores de suscetibilidade e exposição deve melhorar a especificidade do marcador. Quanto mais específico for o biomarcador de efeito, menor será a necessidade de um grande tamanho de amostra para identificar cientificamente toxinas potenciais.
Os biomarcadores de efeito são a classe mais importante de marcadores e vinculam a exposição à suscetibilidade e à doença. Abordamos anteriormente a combinação de biomarcadores celulares e solúveis para diferenciar entre hematúria originada no trato superior ou no trato inferior. Uma lista de biomarcadores solúveis potencialmente relacionados à nefrotoxicidade celular é apresentada na Tabela 4. Até o momento, nenhum deles isoladamente ou como múltiplos painéis de biomarcadores detecta toxicidade subclínica com sensibilidade adequada. Alguns problemas com o uso de biomarcadores solúveis são falta de especificidade, instabilidade enzimática, efeito de diluição da urina, variações na função renal e interações de proteínas não específicas que podem ofuscar a especificidade da análise.
Tabela 4. Potenciais biomarcadores ligados à lesão celular
|
Fatores imunológicos: -Anticorpos humorais e fragmentos de anticorpos; componentes da cascata do complemento e fatores de coagulação - Linfócitos celulares, fagócitos mononucleares e outros efetores derivados da medula (esinófilos, basófilos, neutrófilos e plaquetas) Linfocinas Principais antígenos de histocompatibilidade Fatores de crescimento e citocinas: fator de crescimento derivado de plaquetas, fator de crescimento epidérmico, fator de crescimento transformador (TGF), fator de necrose tumoral, interleucina-1, etc. Mediadores lipídicos: prostaglandinas Endotelina |
Componentes da matriz extracelular: -Colágenos -Procolágeno -Laminina -Fibronectina Espécies reativas de oxigênio e nitrogênio Fatores de transcrição e proto-oncogenes: c-myc, c-fos, c-jun, c-Haras, c-Ki-ras e Egr-1 Proteínas de choque térmico |
Fonte: Finn, Hemstreet et al. no Conselho Nacional de Pesquisa de 1995.
Um fator de crescimento solúvel com aplicação clínica potencial é o fator de crescimento epidérmico urinário (EGF), que pode ser excretado pelo rim e também está alterado em pacientes com carcinoma de células transicionais da bexiga. A quantificação de enzimas urinárias foi investigada, mas a utilidade disso foi limitada pela incapacidade de determinar a origem da enzima e falta de reprodutibilidade do ensaio. O uso de enzimas urinárias e sua ampla aceitação tem sido lento devido aos critérios restritivos mencionados anteriormente. As enzimas avaliadas incluem alaminopeptidase, NAG e fosfatase alcalina intestinal. O NAG é talvez o marcador mais amplamente aceito para monitorar a lesão celular do túbulo proximal devido à sua localização no segmento S3 do túbulo. Como a célula exata de origem e a causa patológica da atividade enzimática urinária são desconhecidas, a interpretação dos resultados é difícil. Além disso, medicamentos, procedimentos diagnósticos e doenças coexistentes, como infarto do miocárdio, podem obscurecer a interpretação.
Uma abordagem alternativa é usar biomarcadores de anticorpos monoclonais para identificar e quantificar células tubulares na urina de várias áreas do segmento do néfron. A utilidade desta abordagem dependerá da manutenção da integridade da célula para quantificação. Isso requer fixação apropriada e manuseio da amostra. Estão agora disponíveis anticorpos monoclonais que têm como alvo células específicas do túbulo e distinguem, por exemplo, células do túbulo proximal das células do túbulo distal ou células do túbulo contorcido. A microscopia de transmissão não pode resolver efetivamente as diferenças entre leucócitos e vários tipos de células tubulares, em contraste com a microscopia eletrônica, que tem sido eficaz na detecção da rejeição de transplantes. Técnicas como análise quantitativa de imagens de fluorescência de alta velocidade de células tubulares coradas com anticorpos monoclonais devem resolver esse problema. Num futuro próximo, deve ser possível detectar a nefrotoxicidade subclínica com um alto grau de certeza à medida que a exposição ocorre.
Biomarcadores de doenças malignas
Os cânceres sólidos surgem em muitos casos de um campo de células bioquimicamente alteradas que podem ou não ser histológica ou citologicamente alteradas. Tecnologias como a análise quantitativa de imagens de fluorescência capazes de detectar biomarcadores associados a condições pré-malignas com certeza fornecem o horizonte para a quimioprevenção direcionada. Alterações bioquímicas podem ocorrer em um processo variado ou ordenado. Fenotipicamente, essas alterações são expressas por uma progressão morfológica gradual de atipia para displasia e, finalmente, para malignidade evidente. Conhecimento do “papel funcional” de um biomarcador e “quando na sequência da tumorigénese se expressa” auxilia na definição de sua utilidade para identificar doenças pré-malignas, para fazer um diagnóstico precoce e para desenvolver um painel de biomarcadores para prever a recorrência e progressão do tumor. Um paradigma para avaliação de biomarcadores está evoluindo e requer a identificação de perfis únicos e múltiplos de biomarcadores.
O câncer de bexiga parece se desenvolver ao longo de duas vias distintas: uma via de baixo grau aparentemente associada a alterações no cromossomo 9 e uma segunda via associada ao gene supressor P-53 geneticamente alterado no cromossomo 17. Claramente, múltiplos fatores genéticos estão relacionados ao desenvolvimento do câncer, e definir os fatores genéticos em cada indivíduo é uma tarefa difícil, principalmente quando a via genética deve estar ligada a uma complexidade de talvez múltiplas exposições. Em estudos epidemiológicos, as exposições em intervalos prolongados têm sido difíceis de reconstruir. Baterias de marcadores fenotípicos e genotípicos estão sendo identificadas para definir indivíduos em risco em coortes ocupacionais. Um perfil de biomarcadores fenotípicos e sua relação com o câncer de bexiga é mostrado na Figura 3, que ilustra que a G-actina, uma proteína precursora da proteína F-actina do citoesqueleto, é um marcador de diferenciação precoce e pode ser seguido por alterações sequenciais de outros intermediários marcadores de ponto final, como M344, DD23 e ploidia de DNA. Os painéis de biomarcadores mais fortes para detectar doenças pré-malignas e câncer evidente, e para prognóstico, ainda precisam ser determinados. À medida que os critérios bioquímicos sensíveis à máquina são definidos, pode ser possível detectar o risco de doença em pontos prescritos no continuum da doença.
Figura 3. Quatro biomarcadores, G-actina, P-300, DD23 e DNA, em relação à progressão tumoral e resposta ao tratamento cirúrgico e quimioprevenção.
Diagnóstico e manejo da doença renal-urinária relacionada ao trabalho
Doença renal preexistente
As mudanças nos sistemas de prestação de cuidados de saúde em todo o mundo colocam em foco questões de segurabilidade e proteção dos trabalhadores contra exposição adicional. Doença renal preexistente significativa manifesta-se por aumento da creatinina sérica, glicosúria (açúcar na urina), proteinúria, hematúria e urina diluída. É necessário descartar imediatamente causas subjacentes sistêmicas, como diabetes e hipertensão, e, dependendo da idade do paciente, outras etiologias congênitas, como cistos múltiplos no rim, devem ser investigadas. Assim, a urinálise, tanto com vareta reagente quanto com avaliações microscópicas, para detecção de alterações bioquímicas e celulares, é útil ao médico do trabalho. Testes de creatinina sérica e depuração de creatinina são indicados se hematúria significativa, piúria ou proteinúria sugerirem patologia subjacente.
Múltiplos fatores são importantes para avaliar o risco de progressão de doença crônica ou insuficiência renal aguda. A primeira é a limitação inerente ou adquirida do rim para resistir à exposição a xenobióticos. A resposta do rim ao nefrotóxico, como aumento na quantidade de tóxico absorvido ou alterações no metabolismo renal, pode ser influenciada por uma condição pré-existente. De particular importância é uma diminuição na função desintoxicante nos muito jovens ou nos muito velhos. Em um estudo, a suscetibilidade à exposição ocupacional foi altamente correlacionada com a história familiar de doença renal, significando a importância da predisposição hereditária. Condições subjacentes, como diabetes e hipertensão, aumentam a suscetibilidade. Condições raras, como lúpus eritematoso e vasculite, podem ser fatores adicionais de suscetibilidade. Na maioria dos casos, o aumento da suscetibilidade é multifatorial e freqüentemente envolve uma bateria de insultos que ocorrem isoladamente ou simultaneamente. Assim, o médico do trabalho deve conhecer a história familiar do paciente de doença renal e condições pré-existentes que afetem a função renal, bem como qualquer doença vascular ou cardíaca, principalmente em trabalhadores mais velhos.
A insuficiência renal aguda
A insuficiência renal aguda pode surgir de causas pré-renais, renais ou pós-renais. A condição geralmente é causada por um insulto agudo, resultando em perda rápida e progressiva da função renal. Quando o nefrotóxico ou o fator causal precipitante é removido, há um retorno progressivo da função renal com declínio gradual da creatinina sérica e melhora da capacidade de concentração renal. Uma lista de causas ocupacionais de insuficiência renal aguda é apresentada na Tabela 5. A insuficiência renal aguda decorrente da exposição a altas doses de xenobióticos tem sido útil para sinalizar causas etiológicas potenciais que também podem contribuir para formas mais crônicas de doença renal progressiva. Insuficiência renal aguda por obstrução da via de saída causada por doença benigna ou malignidade é relativamente rara, mas causas cirúrgicas podem contribuir com mais frequência. A ultrassonografia do trato superior delineia o problema de obstrução, qualquer que seja o fator contribuinte. A insuficiência renal associada a drogas ou substâncias tóxicas ocupacionais resulta em uma taxa de mortalidade de aproximadamente 37%; o restante dos indivíduos afetados melhora em vários graus.
Tabela 5. Principais causas de insuficiência renal aguda de origem ocupacional
| Isquemia renal | necrose tubular | Hemoglobinúria, mioglobinúria |
| Choque traumático Choque anafilático Intoxicação aguda por monóxido de carbono Insolação |
Mercúrio crômio Arsênico Ácido oxálico Tartaratos Etilenoglicol Tetracloreto de carbono tetracloroetano |
Arsino Síndrome de esmagamento Atingido por um raio |
Fonte: Crepet 1983. See More
A insuficiência renal aguda pode ser atribuída a uma variedade de causas pré-renais que têm como tema subjacente a isquemia renal resultante de uma diminuição prolongada da perfusão renal. Insuficiência cardíaca e obstrução da artéria renal são dois exemplos. A necrose tubular pode ser causada por um número cada vez maior de nefrotóxicos presentes no local de trabalho. Herbicidas e pesticidas têm sido implicados em uma série de estudos. Em um relatório recente, o envenenamento por cicuta resultou na deposição de miosina e actina a partir da quebra das células musculares nos túbulos e uma diminuição aguda da função renal. Endosulfan, um inseticida, e acetato de trifenilestanho (TPTA), um organoestanho, ambos foram inicialmente classificados como neurotoxinas, mas recentemente foram relatados como associados à necrose tubular. Relatos anedóticos de casos adicionais colocam em perspectiva a necessidade de encontrar biomarcadores para identificar substâncias tóxicas subclínicas mais sutis que podem ainda não ter resultado em exposições tóxicas a altas doses.
Os sinais e sintomas de insuficiência renal aguda são: ausência de produção de urina (anúria); oligúria (diminuição da produção de urina); diminuição da capacidade de concentração renal; e/ou aumento do potássio sérico que pode parar o coração em um estado relaxado (parada diastólica). O tratamento envolve suporte clínico e, sempre que possível, afastamento da exposição ao tóxico. O aumento do potássio sérico ou a retenção excessiva de líquidos são os dois principais indicadores para hemodiálise ou diálise peritoneal, com a escolha dependente da estabilidade cardiovascular do paciente e do acesso vascular para hemodiálise. O nefrologista, um médico especialista em rins, é fundamental na estratégia de manejo desses pacientes, que também podem exigir cuidados de um especialista em cirurgia urológica.
O tratamento a longo prazo de pacientes após insuficiência renal depende em grande parte do grau de recuperação e reabilitação e do estado geral de saúde do paciente. É desejável retornar ao trabalho limitado e evitar condições que estressem a condição subjacente. Pacientes com hematúria persistente ou piúria requerem monitoramento cuidadoso, possivelmente com biomarcadores, por 2 anos após a recuperação.
doença renal crônica
A doença renal crônica ou em estágio terminal é mais frequentemente o resultado de um processo subclínico crônico e contínuo que envolve uma multiplicidade de fatores, a maioria dos quais mal compreendidos. Glomerulonefrite, causas cardiovasculares e hipertensão são os principais fatores contribuintes. Outros fatores incluem diabetes e nefrotóxicos. Os pacientes apresentam elevações progressivas no nitrogênio ureico sérico, creatinina, potássio sérico e oligúria (diminuição da produção de urina). São necessários biomarcadores ou painéis de biomarcadores aprimorados para identificar com mais precisão a nefrotoxicidade subclínica. Para o profissional ocupacional, os métodos de avaliação precisam ser não invasivos, altamente específicos e reprodutíveis. Até o momento, nenhum biomarcador atendeu a esses critérios para se tornar prático em grande escala clínica.
A doença renal crônica pode resultar de uma variedade de nefrotóxicos, cuja patogênese é mais bem compreendida para alguns do que para outros. Uma lista de nefrotóxicos e locais de toxicidade é apresentada na Tabela 6. Conforme mencionado, as toxinas podem atingir o glomérulo, segmentos dos túbulos ou células intersticiais. Os sintomas de exposição a xenobióticos podem incluir hematúria, piúria, glicosúria, aminoácidos na urina, micção frequente e diminuição da produção de urina. Os mecanismos precisos de dano renal para muitos nefrotóxicos não foram definidos, mas a identificação de biomarcadores específicos de nefrotoxicidade deve ajudar a resolver esse problema. Embora alguma proteção do rim seja proporcionada pela prevenção da vasoconstrição, a lesão tubular persiste na maioria dos casos. Por exemplo, a toxicidade do chumbo é principalmente de origem vascular, enquanto o cromo em baixas doses afeta as células dos túbulos proximais. Esses compostos parecem afetar a maquinaria metabólica da célula. Múltiplas formas de mercúrio têm sido implicadas na nefrotoxicidade elementar aguda. O cádmio, em contraste com o mercúrio e como muitos outros nefrotóxicos ocupacionais, atinge primeiro as células dos túbulos proximais.
Tabela 6. Segmentos do néfron afetados por substâncias tóxicas selecionadas
|
Túbulo proximal Antibióticos -Cefalosporinas Aminoglicosídeos Antineoplásicos -Nitrosoureias -Cisplatina e análogos Agentes de contraste radiográfico hidrocarbonetos halogenados -Clorotrifluoroetileno -Hexafluropropeno -Hexaclorobutadieno -Tricloroetileno -Clorofórmio -Tetracloreto de carbono Ácido maleico Citrinina Metais -Mercúrio -Nitrato de Uranila -Cádmio -Crómio |
Glomérulo Complexos imunes Antibióticos aminoglicosídeos Puromicina aminonucleosídeo Adriamicina Penicilamina Túbulo distal/duto coletor -Lítio -Tetraciclinas -Anfotericina -Fluoreto -Metoxiflurano
Papa, mingau -Aspirina -Fenacetina -Paracetamol -Anti-inflamatórios não esteróides -2-Bromoetilamina |
Fonte: Tarloff e Goldstein 1994.
Mais...
Cânceres Renais-Urinários
Cancêr de rins
Epidemiologia
Historicamente, o câncer renal tem sido usado para significar todas as malignidades do sistema renal (carcinoma de células renais (CCR), CID-9 189.0; pelve renal, CID-9 189.1; e ureter, CID-9 189.2) ou apenas RCC. Essa categorização gerou alguma confusão nos estudos epidemiológicos, resultando na necessidade de examinar os dados relatados anteriormente. O CCR compreende 75 a 80% do total, sendo o restante principalmente carcinomas de células transicionais da pelve renal e ureter. A separação desses dois tipos de câncer é apropriada, uma vez que a patogênese do CCR e do carcinoma de células transicionais é bastante diferente, e os fatores de risco epidemiológicos são distintos, assim como os sinais e sintomas das duas doenças. Esta seção se concentra no RCC.
O principal fator de risco identificado para o câncer renal é o tabagismo, seguido por fatores de risco ocupacionais e ambientais suspeitos, mas mal definidos. Estima-se que a eliminação do tabagismo diminuiria a incidência de câncer renal em 30 a 40% nos países industrializados, mas os determinantes ocupacionais do CCR não estão bem estabelecidos. O risco atribuível à população devido a exposições ocupacionais foi estimado entre zero, com base na carcinogênese reconhecida, e 21%, com base em um estudo de caso-controle multicêntrico multicêntrico na área de Montreal, no Canadá. Biomarcadores precoces de efeito em associação com biomarcadores de exposição devem ajudar a esclarecer importantes fatores de risco. Estudos epidemiológicos demonstraram que várias ocupações e indústrias acarretam um risco aumentado de câncer renal. No entanto, com a possível exceção de agentes usados na lavagem a seco e exposições no refino de petróleo, as evidências disponíveis não são consistentes. A análise estatística dos dados de exposição epidemiológica em relação aos biomarcadores de suscetibilidade e efeito esclarecerá causas etiológicas adicionais.
Vários estudos epidemiológicos associaram indústrias específicas, ocupações e exposições ocupacionais com riscos aumentados de carcinoma de células renais. O padrão que emerge desses estudos não é totalmente consistente. Refino de petróleo, impressão, lavagem a seco e direção de caminhões são exemplos de trabalhos associados ao risco excessivo de câncer renal. Os agricultores geralmente apresentam risco reduzido de RCC, mas um estudo dinamarquês relacionou a exposição a longo prazo a inseticidas e herbicidas com quase quatro vezes o excesso de risco de CCR. Esse achado requer confirmação em dados independentes, incluindo a especificação da possível natureza causal da associação. Outros produtos suspeitos de estarem associados ao RCC incluem: vários derivados de hidrocarbonetos e solventes; produtos de refino de petróleo; derivados de petróleo, alcatrão e piche; escape de gasolina; combustível de avião; emissões de motores a jato e diesel; compostos de arsênico; cádmio; compostos de crómio (VI); compostos inorgânicos de chumbo; e amianto. Estudos epidemiológicos associaram a exposição ocupacional ao vapor de gasolina com risco de câncer renal, alguns de forma dose-resposta, um fenômeno observado no rato macho para exposição ao vapor de gasolina sem chumbo. Essas descobertas ganham algum peso potencial, dada a ampla exposição humana a vapores de gasolina em postos de gasolina e o recente aumento na incidência de câncer renal. A gasolina é uma mistura complexa de hidrocarbonetos e aditivos, incluindo o benzeno, que é um conhecido carcinógeno humano.
O risco de câncer renal não está consistentemente relacionado com a classe social, embora o aumento do risco tenha sido ocasionalmente associado a um nível socioeconômico mais elevado. No entanto, em algumas populações foi observado um gradiente reverso e, em outras, nenhum padrão claro emergiu. Possivelmente essas variações podem estar relacionadas ao estilo de vida. Estudos com migrantes mostram modificação no risco de CCR em relação ao nível da população do país anfitrião, sugerindo que fatores ambientais são importantes no desenvolvimento dessa malignidade.
Com exceção do nefroblastoma (tumor de Wilms), que é um câncer infantil, o câncer renal geralmente ocorre após os 40 anos de idade. Estima-se que 127,000 novos casos de câncer renal (incluindo RCC e carcinoma de células transicionais (CCT) da pelve renal e ureter), correspondendo a 1.7% da incidência mundial total de câncer, ocorreram globalmente em 1985. A incidência de câncer renal varia entre as populações . Altas taxas foram relatadas para homens e mulheres na América do Norte, Europa, Austrália e Nova Zelândia; baixas taxas na Melanésia, África central e oriental e sudeste e leste da Ásia. A incidência de câncer renal tem aumentado na maioria dos países ocidentais, mas estagnou em alguns. A incidência padronizada por idade de câncer renal em 1985 foi maior na América do Norte e oeste, norte e leste da Europa, e menor na África, Ásia (exceto em homens japoneses) e Pacífico. O câncer de rim é mais frequente em homens do que em mulheres e está entre os dez tipos de câncer mais frequentes em vários países.
O carcinoma de células transicionais (CCT) da pelve renal está associado a agentes etiológicos semelhantes ao câncer de bexiga, incluindo infecção crônica, cálculos e analgésicos contendo fenacetina. A nefropatia balcânica, uma nefropatia lentamente progressiva, crônica e fatal prevalente nos países balcânicos, está associada a altas taxas de tumores da pelve renal e ureter. As causas da nefropatia dos Balcãs são desconhecidas. A exposição excessiva à ocratoxina A, que é considerada possivelmente cancerígena para humanos, foi associada ao desenvolvimento de nefropatia dos Bálcãs, mas o papel de outros agentes nefrotóxicos não pode ser excluído. A ocratoxina A é uma toxina produzida por fungos que pode ser encontrada em muitos alimentos, principalmente cereais e produtos suínos.
Rastreamento e diagnóstico do câncer renal
O padrão de sinais e sintomas do CCR varia entre os pacientes, mesmo até o estágio em que a metástase aparece. Devido à localização dos rins e à mobilidade dos órgãos contíguos à massa em expansão, esses tumores são frequentemente muito grandes no momento da detecção clínica. Embora a hematúria seja o principal sintoma do CCR, o sangramento ocorre tardiamente em comparação com os tumores de células transicionais devido à localização intra-renal do CCR. O CCR tem sido considerado o “sonho do médico”, mas a “maldição do cirurgião” devido à interessante constelação de sintomas relacionados às síndromes paraneoplásicas. Substâncias que aumentam a contagem de glóbulos vermelhos, cálcio e fatores que simulam função anormal da glândula adrenal foram relatadas, e massa abdominal, perda de peso, fadiga, dor, anemia, função hepática anormal e hipertensão foram todos observados. A tomografia axial computadorizada (TCA) do abdome e a ultrassonografia estão sendo solicitadas pelos médicos com maior frequência e, consequentemente, estima-se que 20% dos CCRs sejam diagnosticados por acaso como resultado da avaliação de outros problemas médicos.
A avaliação clínica de um caso de CCR consiste em um exame físico para identificar uma massa no flanco, que ocorre em 10% dos pacientes. Uma radiografia renal com contraste pode delinear uma massa renal e a natureza sólida ou cística geralmente é esclarecida por ultrassom ou tomografia computadorizada. Os tumores são altamente vascularizados e têm uma aparência característica quando a artéria é injetada com material de contraste radiopaco. A arteriografia é realizada para embolizar o tumor se for muito grande ou para definir o suprimento de sangue arterial se uma nefrectomia parcial for antecipada. A aspiração com agulha fina pode ser usada para coletar amostras de CCR suspeito.
Tumores de CCR localizados são removidos cirurgicamente com linfonodos regionais e, cirurgicamente, a ligadura precoce da artéria e veia é importante. Sintomaticamente, o paciente pode melhorar com a remoção de tumores grandes ou hemorrágicos que metastatizaram, mas isso não melhora a sobrevida. Para tumores metastáticos, o controle da dor localizada pode ser obtido com radioterapia, mas o tratamento de escolha para a doença metastática são os modificadores da resposta biológica (interleucina-2 ou α-interferon), embora a quimioterapia seja ocasionalmente usada sozinha ou em combinação com outras terapias.
Marcadores como o gene do câncer no cromossomo 3 observado em famílias de câncer e na doença de von Hippel-Lindau podem servir como biomarcadores de suscetibilidade. Embora antígenos marcadores tumorais tenham sido relatados para RCC, atualmente não há como detectá-los de forma confiável na urina ou no sangue com sensibilidade e especificidade adequadas. A baixa prevalência desta doença na população geral requer um teste de alta especificidade e sensibilidade para a detecção precoce da doença. Coortes ocupacionais em risco poderiam potencialmente ser rastreadas com ultrassom. A avaliação desse tumor continua sendo um desafio para o cientista básico, epidemiologista molecular e clínico.
Câncer de bexiga
Epidemiologia
Mais de 90% dos cânceres de bexiga na Europa e na América do Norte são carcinomas de células transicionais (CCT). O carcinoma de células escamosas e o adenocarcinoma representam 5 e 1%, respectivamente, dos cânceres de bexiga nessas regiões. A distribuição dos tipos histopatológicos no câncer de bexiga é notavelmente diferente em regiões como o Oriente Médio e a África, onde o câncer de bexiga está associado à infecção esquistossomótica. Por exemplo, no Egito, onde a esquistossomose é endêmica e o câncer de bexiga é o principal problema oncogênico, o tipo mais comum é o carcinoma de células escamosas, mas a incidência de CCT está aumentando com o aumento da prevalência do tabagismo. A discussão que se segue centra-se no TCC.
O cancro da bexiga continua a ser uma doença de importância significativa. Correspondia a cerca de 3.5% de todas as neoplasias malignas no mundo em 1980. Em 1985, o câncer de bexiga era estimado em 11º lugar na escala global, sendo o oitavo câncer mais frequente entre os homens, com um total esperado de 243,000 novos casos. Há um pico de incidência na sétima década de vida e, em todo o mundo, a proporção entre homens e mulheres é de cerca de três para um. A incidência tem aumentado em quase todas as populações da Europa, particularmente nos homens. Na Dinamarca, onde as taxas de incidência anual estão entre as mais altas do mundo, em 45 por 100,000 em homens e 12 por 100,000 em mulheres, a tendência recente tem sido um aumento adicional de 8 a 9% a cada 5 anos. Na Ásia, as taxas muito altas entre os chineses em Hong Kong diminuíram constantemente, mas em ambos os sexos a incidência de câncer de bexiga ainda é muito maior do que em outras partes da Ásia e mais de duas vezes maior do que entre os chineses em Xangai ou Cingapura. As taxas de câncer de bexiga entre os chineses no Havaí também são altas.
O tabagismo é o fator etiológico mais importante no câncer de bexiga, e as exposições ocupacionais ocupam o segundo lugar. Estima-se que o tabaco seja responsável por um terço de todos os casos de câncer de bexiga fora das regiões onde a infecção esquistossomótica é prevalente. O número de casos de câncer de bexiga atribuídos em 1985 ao tabagismo foi estimado em mais de 75,000 em todo o mundo e pode representar 50% do câncer de bexiga nas populações ocidentais. O fato de que todos os indivíduos que fumam quantidades semelhantes não desenvolvem câncer de bexiga na mesma proporção sugere que fatores genéticos são importantes no controle da suscetibilidade. Duas aminas aromáticas, 4-aminobifenil e 2-naftilamina, são carcinógenos associados ao tabagismo; estes são encontrados em concentrações mais altas no “tabaco preto” (curado ao ar) do que no “tabaco misturado” (curado em estufa). O fumo passivo aumenta os adutos no sangue e uma dose-resposta de formação de adutos foi correlacionada com o aumento do risco de câncer de bexiga. Níveis mais altos de formação de adutos foram observados em fumantes de cigarros que são acetiladores lentos em comparação com acetiladores rápidos, o que sugere que o estado de acetilação herdado geneticamente pode ser um importante biomarcador de suscetibilidade. A menor incidência de câncer de bexiga em raças negras em comparação com raças brancas pode ser atribuída à conjugação de intermediários metabólicos cancerígenos por sulfotransferases que produzem eletrófilos. Sulfatos fenólicos desintoxicados podem proteger o urotélio. Foi relatado que a atividade da sulfotransferase hepática para N-hidroxiarilaminas é maior em negros do que em brancos. Isso pode resultar em uma diminuição na quantidade de N-hidroximetabólitos livres para funcionar como carcinógenos.
O câncer de bexiga ocupacional é um dos cânceres ocupacionais mais antigos conhecidos e melhor documentados. O primeiro caso identificado de câncer de bexiga ocupacional apareceu cerca de 20 anos após o início da indústria de corantes sintéticos na Alemanha. Numerosas outras ocupações foram identificadas nos últimos 25 anos como riscos ocupacionais de câncer de bexiga. As exposições ocupacionais podem contribuir para até 20% dos cânceres de bexiga. Os trabalhadores expostos ocupacionalmente incluem aqueles que trabalham com alcatrão de hulha, gaseificação de carvão e produção de borracha, alumínio, auramina e magenta, bem como os que trabalham como cabeleireiros e barbeiros. Foi demonstrado que as aminas aromáticas causam câncer de bexiga em trabalhadores em muitos países. Destacam-se nesta classe de produtos químicos a 2-naftilamina, benzidina, 4-nitrobifenil e 3,3r´-diclorobenzidina. Duas outras aminas aromáticas, 4,4'-metileno dianilina (MDA) e 4,4'-metileno-bis-2-cloroanilina (MOCA) estão entre os carcinógenos da bexiga mais amplamente usados. Outros carcinógenos associados a exposições industriais são amplamente indeterminados; no entanto, as aminas aromáticas estão frequentemente presentes no local de trabalho.
Rastreamento e diagnóstico do câncer de bexiga
O rastreamento do câncer de bexiga continua recebendo atenção na busca pelo diagnóstico do câncer de bexiga antes que se torne sintomático e, presumivelmente, menos passível de tratamento curativo. A citologia da urina miccional e a urinálise para hematúria foram consideradas testes de triagem candidatos. Uma questão fundamental para a triagem é como identificar os grupos de alto risco e, em seguida, os indivíduos dentro desses grupos. Estudos epidemiológicos identificam grupos de risco, enquanto biomarcadores potencialmente identificam indivíduos dentro de grupos. Em geral, a triagem ocupacional para câncer de bexiga com teste de hematúria e citologia de Papanicolaou tem sido ineficaz.
A detecção aprimorada do câncer de bexiga pode ser possível usando o teste hemostick de 14 dias descrito por Messing e colaboradores. Um teste positivo foi observado pelo menos uma vez em 84% dos 31 pacientes com câncer de bexiga pelo menos 2 meses antes do diagnóstico cistoscópico da doença. Este teste sofre de uma taxa de falso-positivo de 16 a 20%, com metade desses pacientes sem doença urológica. O baixo custo pode tornar este teste útil em uma triagem de dois níveis em combinação com biomarcadores e citologia (Waples e Messing 1992).
Em um estudo recente, o anticorpo monoclonal DD23 usando análise quantitativa de imagens de fluorescência detectou câncer de bexiga em células uroepiteliais esfoliadas. Uma sensibilidade de 85% e especificidade de 95% foram alcançadas em uma mistura de carcinomas de células transicionais de baixo e alto grau, incluindo tumores TaT1. O antígeno associado ao tumor M344 em conjunto com a ploidia do DNA apresentou uma sensibilidade de aproximadamente 90%.
Estudos recentes indicam que a combinação de biomarcadores com testes de hematúria pode ser a melhor abordagem. Uma lista das aplicações da citologia urinária de fluorescência quantitativa em combinação com biomarcadores está resumida na Tabela 1. As alterações celulares precoces genéticas, bioquímicas e morfológicas associadas a condições pré-malignas sustentam o conceito de que os indivíduos em risco podem ser identificados anos antes do desenvolvimento malignidade. Biomarcadores de suscetibilidade em combinação com biomarcadores de efeito prometem detectar indivíduos em risco com uma precisão ainda maior. Esses avanços são possibilitados por novas tecnologias capazes de quantificar alterações moleculares fenotípicas e genotípicas no nível de uma única célula, identificando assim os indivíduos em risco. A avaliação de risco individual facilita o monitoramento estratificado e econômico de grupos selecionados para quimioprevenção direcionada.
Tabela 1. Aplicações da citologia urinária
Detecção de CIS1 e câncer de bexiga
Monitoramento da terapia cirúrgica:
Monitoramento da bexiga após TURBT2
Monitoramento do trato urinário superior
Monitoramento do remanescente uretral
Monitoramento do desvio urinário
Monitoramento da terapia intravesical
Seleção de terapia intravesical
Monitorando o efeito da terapia a laser
Avaliação de pacientes com hematúria
Estabelecimento da necessidade de cistoscopia
Triagem de populações de alto risco:
Grupos de exposição ocupacional
Grupos de abuso de drogas em risco de câncer de bexiga
Critérios de decisão para:
Cistectomia
Ressecção ureteral segmentar versus nefroureterectomia
Outras indicações:
Detecção de fístula vesicoentérica
Tumores extraurológicos que invadem o trato urinário
Definindo agentes quimiopreventivos eficazes
Monitoramento de quimioterapia eficaz
1 CIS, carcinoma in situ.
2 TURBT, ressecção transuretral para tumor de bexiga.
Fonte: Hemstreet et al. 1996.
Os sinais e sintomas do câncer de bexiga são semelhantes aos da infecção do trato urinário e podem incluir dor ao urinar, micção frequente e sangue e células pus na urina. Como os sintomas de uma infecção do trato urinário podem anunciar um tumor de bexiga, especialmente quando associados a hematúria macroscópica em pacientes idosos, é necessária a confirmação da presença de bactérias e uma atenção aguçada por parte do médico examinador. Qualquer paciente tratado para uma infecção do trato urinário que não se resolva imediatamente deve ser encaminhado a um especialista em urologia para uma avaliação mais aprofundada.
A avaliação diagnóstica do câncer de bexiga primeiro requer um pielograma intravenoso (PIV) para excluir doença do trato superior na pelve renal ou ureteres. A confirmação do câncer de bexiga requer a observação da bexiga com uma luz (cistoscópio) com múltiplas biópsias realizadas com um instrumento iluminado através da uretra para determinar se o tumor é não invasivo (ou seja, papilar ou CIS) ou invasivo. Biópsias aleatórias da bexiga e da uretra prostática ajudam a definir a cancerização de campo e as alterações de efeito de campo. Pacientes com doença não invasiva requerem monitoramento rigoroso, pois correm o risco de recorrências subsequentes, embora a progressão de estágio e grau seja incomum. Os pacientes que apresentam câncer de bexiga que já é de alto grau ou invasivo na lâmina própria têm risco igualmente alto de recorrência, mas a progressão do estágio é muito mais provável. Assim, eles geralmente recebem instilação intravesical de agentes imuno ou quimioterápicos após a ressecção transuretral. Pacientes com tumores que invadem a muscular própria ou além têm muito mais probabilidade de já ter metástase e raramente podem ser tratados por meios conservadores. No entanto, mesmo quando tratados por cistectomia total (a terapia padrão para câncer de bexiga com invasão muscular), 20 a 60% eventualmente sucumbem à doença, quase sempre devido a metástases. Quando a metástase regional ou distal está presente ao diagnóstico, as taxas de sobrevida em 5 anos caem para 35 e 9%, respectivamente, apesar do tratamento agressivo. A quimioterapia sistêmica para câncer de bexiga metastático está melhorando, com taxas de resposta completa relatadas em 30%. Estudos recentes sugerem que a quimioterapia antes da cistectomia pode melhorar a sobrevida em pacientes selecionados.
O estadiamento do câncer de bexiga é preditivo do potencial biológico de progressão, metástase ou recorrência em 70% dos casos. O estadiamento do câncer de bexiga geralmente requer tomografia computadorizada para descartar metástase hepática, cintilografia óssea com radioisótopo para excluir disseminação para o osso e radiografia de tórax ou tomografia computadorizada para excluir metástase pulmonar. Uma busca continua por biomarcadores no tumor e no campo do câncer de bexiga que irão prever quais tumores irão metastatizar ou recorrer. A acessibilidade das células da bexiga esfoliadas em amostras anuladas mostra-se promissora para o uso de biomarcadores para monitorar a recorrência e para a prevenção do câncer.
Sistema Reprodutivo: Introdução
Toxicidade reprodutiva masculina e feminina são tópicos de interesse crescente em consideração aos riscos à saúde ocupacional. Toxidade reprodutiva tem sido definida como a ocorrência de efeitos adversos no sistema reprodutivo que podem resultar da exposição a agentes ambientais. A toxicidade pode ser expressa como alterações nos órgãos reprodutivos e/ou no sistema endócrino relacionado. As manifestações de tal toxicidade podem incluir:
- alterações no comportamento sexual
- fertilidade reduzida
- resultados adversos da gravidez
- modificações de outras funções que dependem da integridade do sistema reprodutivo.
Os mecanismos subjacentes à toxicidade reprodutiva são complexos. Mais substâncias xenobióticas foram testadas e demonstraram ser tóxicas para o processo reprodutivo masculino do que para o feminino. No entanto, não se sabe se isso se deve a diferenças subjacentes na toxicidade ou à maior facilidade de estudar espermatozóides do que ovócitos.
Toxicidade no desenvolvimento
A toxicidade do desenvolvimento foi definida como a ocorrência de efeitos adversos no organismo em desenvolvimento que podem resultar da exposição antes da concepção (qualquer um dos pais), durante o desenvolvimento pré-natal ou pós-natal até o momento da maturação sexual. Efeitos adversos no desenvolvimento podem ser detectados em qualquer ponto da vida do organismo. As principais manifestações de toxicidade no desenvolvimento incluem:
- morte do organismo em desenvolvimento
- anormalidade estrutural
- crescimento alterado
- deficiência funcional.
Na discussão a seguir, toxicidade do desenvolvimento será usado como um termo abrangente para se referir a exposições à mãe, pai ou concepto que levam a um desenvolvimento anormal. O termo teratogênese será usado para se referir mais especificamente a exposições ao concepto que produzem uma malformação estrutural. Nossa discussão não incluirá os efeitos das exposições pós-natais no desenvolvimento.
Mutagênese
Além da toxicidade reprodutiva, a exposição a um dos pais antes da concepção tem o potencial de resultar em defeitos de desenvolvimento por meio de mutagênese, alterações no material genético que é passado de pai para filho. Tais mudanças podem ocorrer tanto no nível de genes individuais quanto no nível cromossômico. Alterações em genes individuais podem resultar na transmissão de mensagens genéticas alteradas, enquanto alterações no nível cromossômico podem resultar na transmissão de anormalidades no número ou estrutura cromossômica.
É interessante que algumas das evidências mais fortes de um papel para exposições pré-concepcionais em anormalidades do desenvolvimento venham de estudos de exposições paternas. Por exemplo, a síndrome de Prader-Willi, um defeito congênito caracterizado por hipotonicidade no período neonatal e, posteriormente, obesidade acentuada e problemas de comportamento, tem sido associada a exposições ocupacionais paternas a hidrocarbonetos. Outros estudos mostraram associações entre exposições paternas pré-concepcionais a agentes físicos e malformações congênitas e cânceres infantis. Por exemplo, a exposição ocupacional paterna à radiação ionizante tem sido associada a um risco aumentado de defeitos do tubo neural e risco aumentado de leucemia infantil, e vários estudos sugeriram associações entre a exposição ocupacional pré-concepcional paterna a campos eletromagnéticos e tumores cerebrais infantis (Gold e Sever 1994 ). Ao avaliar os riscos reprodutivos e de desenvolvimento das exposições no local de trabalho, deve-se prestar mais atenção aos possíveis efeitos entre os homens.
É bastante provável que alguns defeitos de etiologia desconhecida envolvam um componente genético que pode estar relacionado a exposições parentais. Devido às associações demonstradas entre a idade do pai e as taxas de mutação, é lógico acreditar que outros fatores e exposições paternas possam estar associados a mutações genéticas. A associação bem estabelecida entre idade materna e não disjunção cromossômica, resultando em anormalidades no número cromossômico, sugere um papel significativo para exposições maternas em anormalidades cromossômicas.
À medida que aumenta a nossa compreensão do genoma humano, é provável que seremos capazes de rastrear mais defeitos de desenvolvimento para alterações mutagênicas no DNA de genes únicos ou alterações estruturais em porções dos cromossomos.
Teratogênese
Os efeitos adversos no desenvolvimento humano da exposição do concepto a agentes químicos exógenos foram reconhecidos desde a descoberta da teratogenicidade da talidomida em 1961. Wilson (1973) desenvolveu seis “princípios gerais de teratologia” que são relevantes para esta discussão. Esses princípios são:
- As manifestações finais do desenvolvimento anormal são morte, malformação, retardo de crescimento e distúrbio funcional.
- A suscetibilidade do concepto a agentes teratogênicos varia com o estágio de desenvolvimento no momento da exposição.
- Os agentes teratogênicos atuam de maneiras específicas (mecanismos) nas células e tecidos em desenvolvimento, iniciando a embriogênese anormal (patogênese).
- Manifestações de desenvolvimento anormal aumentam em grau desde o nível sem efeito até o nível totalmente letal à medida que a dosagem aumenta.
- O acesso de influências ambientais adversas aos tecidos em desenvolvimento depende da natureza do agente.
- A suscetibilidade a um teratógeno depende do genótipo do concepto e da maneira como o genótipo interage com fatores ambientais.
Os primeiros quatro desses princípios serão discutidos em mais detalhes, assim como a combinação dos princípios 1, 2 e 4 (resultado, tempo de exposição e dose).
Espectro de resultados adversos associados à exposição
Existe um espectro de resultados adversos potencialmente associados à exposição. Estudos ocupacionais que se concentram em um único risco de resultado negligenciam outros efeitos reprodutivos importantes.
A Figura 1 lista alguns exemplos de resultados de desenvolvimento potencialmente associados à exposição a teratógenos ocupacionais. Os resultados de alguns estudos ocupacionais sugeriram que malformações congênitas e abortos espontâneos estão associados às mesmas exposições – por exemplo, gases anestésicos e solventes orgânicos.
O aborto espontâneo é um resultado importante a ser considerado, pois pode resultar de diferentes mecanismos através de vários processos patogênicos. Um aborto espontâneo pode ser o resultado de toxicidade para o embrião ou feto, alterações cromossômicas, efeitos de um único gene ou anormalidades morfológicas. É importante tentar diferenciar entre conceptos cariotipicamente normais e anormais em estudos de abortos espontâneos.
Figura 1. Anormalidades de desenvolvimento e resultados reprodutivos potencialmente associados a exposições ocupacionais.
Tempo de Exposição
O segundo princípio de Wilson relaciona a suscetibilidade ao desenvolvimento anormal com o tempo de exposição, ou seja, a idade gestacional do concepto. Este princípio foi bem estabelecido para a indução de malformações estruturais, e os períodos sensíveis para a organogênese são conhecidos para muitas estruturas. Considerando uma gama expandida de resultados, o período sensível durante o qual qualquer efeito pode ser induzido deve ser estendido ao longo da gestação.
Ao avaliar a toxicidade do desenvolvimento ocupacional, a exposição deve ser determinada e classificada para o período crítico apropriado – ou seja, idade(s) gestacional(is) – para cada resultado. Por exemplo, abortos espontâneos e malformações congênitas provavelmente estão relacionados à exposição no primeiro e segundo trimestre, enquanto o baixo peso ao nascer e distúrbios funcionais, como distúrbios convulsivos e retardo mental, provavelmente estão relacionados à exposição no segundo e terceiro trimestres.
Mecanismos Teratogênicos
O terceiro princípio é a importância de considerar os mecanismos potenciais que podem iniciar a embriogênese anormal. Vários mecanismos diferentes foram sugeridos que poderiam levar à teratogênese (Wilson 1977). Esses incluem:
- alterações mutacionais nas sequências de DNA
- anormalidades cromossômicas que levam a alterações estruturais ou quantitativas no DNA
- alteração ou inibição do metabolismo intracelular, por exemplo, bloqueios metabólicos e falta de coenzimas, precursores ou substratos para a biossíntese
- interrupção da síntese de DNA ou RNA
- interferência na mitose
- interferência na diferenciação celular
- falha nas interações célula a célula
- falha nas migrações celulares
- morte celular por efeitos citotóxicos diretos
- efeitos na permeabilidade da membrana celular e alterações osmolares
- ruptura física de células ou tecidos.
Ao considerar os mecanismos, os investigadores podem desenvolver agrupamentos de resultados biologicamente significativos. Isso também pode fornecer informações sobre potenciais teratógenos; por exemplo, as relações entre carcinogênese, mutagênese e teratogênese têm sido discutidas há algum tempo. Do ponto de vista da avaliação dos riscos reprodutivos ocupacionais, isso é de particular importância por dois motivos distintos: (1) substâncias que são cancerígenas ou mutagênicas têm uma probabilidade aumentada de serem teratogênicas, sugerindo que atenção especial deve ser dada aos efeitos reprodutivos de tais substâncias , e (2) os efeitos no ácido desoxirribonucleico (DNA), produzindo mutações somáticas, são considerados mecanismos tanto para a carcinogênese quanto para a teratogênese.
Dose e Resultado
O quarto princípio relativo à teratogênese é a relação do resultado com a dose. Este princípio está claramente estabelecido em muitos estudos com animais, e Selevan (1985) discutiu sua relevância potencial para a situação humana, observando a importância de múltiplos resultados reprodutivos dentro de faixas de dose específicas e sugerindo que uma relação dose-resposta pode ser refletida em um aumento taxa de um resultado particular com o aumento da dose e/ou uma mudança no espectro dos resultados observados.
Com relação à teratogênese e à dose, há grande preocupação com os distúrbios funcionais resultantes dos possíveis efeitos comportamentais da exposição pré-natal a agentes ambientais. A teratologia comportamental animal está se expandindo rapidamente, mas a teratologia ambiental comportamental humana está em um estágio relativamente inicial de desenvolvimento. Atualmente, existem limitações críticas na definição e determinação de resultados comportamentais apropriados para estudos epidemiológicos. Além disso, é possível que exposições de baixo nível a substâncias tóxicas para o desenvolvimento sejam importantes para alguns efeitos funcionais.
Múltiplos resultados e tempo de exposição e dose
De particular importância no que diz respeito à identificação de riscos de desenvolvimento no local de trabalho são os conceitos de resultados múltiplos e tempo de exposição e dose. Com base no que sabemos sobre a biologia do desenvolvimento, fica claro que existem relações entre resultados reprodutivos, como aborto espontâneo e retardo de crescimento intrauterino e malformações congênitas. Além disso, vários efeitos foram demonstrados para muitos tóxicos para o desenvolvimento (tabela 1).
Tabela 1. Exemplos de exposições associadas a múltiplos desfechos reprodutivos adversos
| Exposição | Resultado | |||
| Aborto espontâneo | Malformação congênita | Baixo peso de nascimento | Deficiências de desenvolvimento | |
| Álcool | X | X | X | X |
| Anestésico gases |
X | X | ||
| Conduzir | X | X | X | |
| Solventes orgânicos | X | X | X | |
| Fumar | X | X | X | |
Relevantes para isso são questões de tempo de exposição e relações dose-resposta. Há muito se reconhece que o período embrionário durante o qual ocorre a organogênese (duas a oito semanas após a concepção) é o momento de maior sensibilidade à indução de malformações estruturais. O período fetal de oito semanas até o termo é o tempo de histogênese, com rápido aumento no número de células e diferenciação celular ocorrendo durante esse período. É então que as anormalidades funcionais e o retardo de crescimento são mais prováveis de serem induzidos. É possível que possa haver relações entre a dose e a resposta durante este período, onde uma dose alta pode levar ao retardo do crescimento e uma dose mais baixa pode resultar em distúrbios funcionais ou comportamentais.
Toxicidade de desenvolvimento mediada por homens
Embora a toxicidade do desenvolvimento seja geralmente considerada como resultado da exposição da fêmea e do concepto - isto é, efeitos teratogênicos - há evidências crescentes de estudos em animais e humanos para efeitos de desenvolvimento mediados por homens. Os mecanismos propostos para tais efeitos incluem a transmissão de substâncias químicas do pai para o concepto via fluido seminal, contaminação indireta da mãe e do concepto por substâncias transportadas do local de trabalho para o ambiente doméstico por meio de contaminação pessoal e, como observado anteriormente, exposições pré-concepcionais paternas que resultam em alterações genéticas transmissíveis (mutações).
Introdução à função reprodutiva masculina e feminina
A toxicidade reprodutiva tem muitas diferenças únicas e desafiadoras da toxicidade para outros sistemas. Enquanto outras formas de toxicidade ambiental normalmente envolvem o desenvolvimento da doença em um indivíduo exposto, porque a reprodução requer interação entre dois indivíduos, a toxicidade reprodutiva será expressa dentro de uma unidade reprodutiva ou casal. Esse aspecto único dependente do casal, embora óbvio, torna a toxicologia reprodutiva distinta. Por exemplo, é possível que a exposição a um tóxico por um membro de um casal reprodutivo (por exemplo, o homem) se manifeste por um resultado reprodutivo adverso no outro membro do casal (por exemplo, aumento da frequência de aborto espontâneo). Qualquer tentativa de lidar com as causas ambientais da toxicidade reprodutiva deve abordar o aspecto específico do casal.
Existem outros aspectos únicos que refletem os desafios da toxicologia reprodutiva. Ao contrário da função renal, cardíaca ou pulmonar, a função reprodutiva ocorre de forma intermitente. Isso significa que as exposições ocupacionais podem interferir na reprodução, mas passam despercebidas durante os períodos em que a fertilidade não é desejada. Essa característica intermitente pode dificultar a identificação de um tóxico reprodutivo em humanos. Outra característica única da reprodução, que decorre diretamente da consideração acima, é que a avaliação completa da integridade funcional do sistema reprodutivo exige que o casal tente a gravidez.
Sistema Reprodutor Masculino e Toxicologia
A espermatogênese e a espermiogênese são os processos celulares que produzem células sexuais masculinas maduras. Esses processos ocorrem dentro dos túbulos seminíferos dos testículos do homem sexualmente maduro, conforme mostrado na Figura 1. Os túbulos seminíferos humanos têm 30 a 70 cm de comprimento e 150 a 300 mm de diâmetro (Zaneveld 1978). As espermatogônias (células-tronco) estão posicionadas ao longo da membrana basal dos túbulos seminíferos e são as células básicas para a produção de espermatozoides.
Figura 1. O sistema reprodutor masculino
O esperma amadurece através de uma série de divisões celulares nas quais as espermatogônias proliferam e se tornam espermatócitos primários. Os espermatócitos primários em repouso migram através das junções apertadas formadas pelas células de Sertoli para o lado luminal desta barreira testicular. No momento em que os espermatócitos atingem a barreira da membrana no testículo, a síntese de DNA, o material genético no núcleo da célula, está essencialmente completa. Quando os espermatócitos primários realmente encontram o lúmen do túbulo seminífero, eles sofrem um tipo especial de divisão celular que ocorre apenas nas células germinativas e é conhecida como meiose. A divisão celular meiótica resulta na divisão dos pares de cromossomos no núcleo, de modo que cada célula germinativa resultante contém apenas uma única cópia de cada filamento de cromossomo, em vez de um par correspondente.
Durante a meiose, os cromossomos mudam de forma, condensando-se e tornando-se filamentosos. A certa altura, a membrana nuclear que os envolve se rompe e os fusos microtubulares se ligam aos pares cromossômicos, fazendo com que se separem. Isso completa a primeira divisão meiótica e dois espermatócitos secundários haploides são formados. Os espermatócitos secundários então sofrem uma segunda divisão meiótica para formar números iguais de espermátides contendo cromossomos X e Y.
A transformação morfológica das espermátides em espermatozoides é chamada de espermiogênese. Quando a espermiogênese está completa, cada espermatozoide é liberado pela célula de Sertoli no lúmen do túbulo seminífero por um processo conhecido como espermiação. Os espermatozóides migram ao longo do túbulo para a rete testis e para a cabeça do epidídimo. Os espermatozóides que saem dos túbulos seminíferos são imaturos: incapazes de fertilizar um óvulo e incapazes de nadar. Os espermatozóides liberados no lúmen dos túbulos seminíferos são suspensos em fluido produzido principalmente pelas células de Sertoli. Os espermatozóides concentrados suspensos neste fluido fluem continuamente dos túbulos seminíferos, através de ligeiras alterações no meio iônico dentro da rete testis, através dos vasos eferentes e para o epidídimo. O epidídimo é um único tubo altamente enrolado (cinco a seis metros de comprimento) no qual os espermatozoides passam de 12 a 21 dias.
Dentro do epidídimo, os espermatozóides adquirem progressivamente motilidade e capacidade de fertilização. Isso pode ser devido à natureza mutável do fluido em suspensão no epidídimo. Isto é, à medida que as células amadurecem, o epidídimo absorve componentes do fluido, incluindo secreções das células de Sertoli (por exemplo, proteína de ligação ao andrógeno), aumentando assim a concentração de espermatozóides. O epidídimo também contribui com suas próprias secreções para o fluido em suspensão, incluindo os produtos químicos glicerilfosforilcolina (GPC) e carnitina.
A morfologia do esperma continua a se transformar no epidídimo. A gota citoplasmática é derramada e o núcleo do esperma se condensa ainda mais. Enquanto o epidídimo é o principal reservatório de armazenamento de esperma até a ejaculação, cerca de 30% do esperma em uma ejaculação foi armazenado no ducto deferente. A ejaculação frequente acelera a passagem do esperma através do epidídimo e pode aumentar o número de espermatozóides imaturos (inférteis) no ejaculado (Zaneveld 1978).
Ejaculação
Uma vez dentro do ducto deferente, os espermatozóides são transportados pelas contrações musculares da ejaculação, e não pelo fluxo de fluido. Durante a ejaculação, os fluidos são expelidos à força das glândulas sexuais acessórias, dando origem ao plasma seminal. Essas glândulas não expelem suas secreções ao mesmo tempo. Em vez disso, a glândula bulbouretral (de Cowper) primeiro expulsa um fluido claro, seguido pelas secreções prostáticas, os fluidos concentrados em espermatozoides dos epidídimos e da ampola dos ductos deferentes e, finalmente, a maior fração, principalmente das vesículas seminais. Assim, o plasma seminal não é um fluido homogêneo.
Ações tóxicas na espermatogênese e espermiogênese
Os tóxicos podem interromper a espermatogênese em vários pontos. Os mais prejudiciais, por causa da irreversibilidade, são os tóxicos que matam ou alteram geneticamente (além dos mecanismos de reparo) as espermatogônias ou células de Sertoli. Estudos em animais têm sido úteis para determinar o estágio em que um tóxico ataca o processo espermatogênico. Esses estudos empregam exposição de curto prazo a um tóxico antes da amostragem para determinar o efeito. Conhecendo a duração de cada estágio espermatogênico, pode-se extrapolar para estimar o estágio afetado.
A análise bioquímica do plasma seminal fornece informações sobre a função das glândulas sexuais acessórias. Os produtos químicos que são secretados principalmente por cada uma das glândulas sexuais acessórias são tipicamente selecionados para servir como um marcador para cada respectiva glândula. Por exemplo, o epidídimo é representado pelo GPC, as vesículas seminais pela frutose e a próstata pelo zinco. Observe que esse tipo de análise fornece apenas informações brutas sobre a função glandular e pouca ou nenhuma informação sobre os outros constituintes secretores. Medir o pH e a osmolalidade do sêmen fornece informações gerais adicionais sobre a natureza do plasma seminal.
O plasma seminal pode ser analisado quanto à presença de um tóxico ou seu metabólito. Metais pesados foram detectados no plasma seminal usando espectrofotometria de absorção atômica, enquanto hidrocarbonetos halogenados foram medidos no fluido seminal por cromatografia gasosa após extração ou filtração limitadora de proteínas (Stachel et al. 1989; Zikarge 1986).
A viabilidade e motilidade dos espermatozóides no plasma seminal é tipicamente um reflexo da qualidade do plasma seminal. Alterações na viabilidade do esperma, conforme medido por exclusão de coloração ou por inchaço hiposmótico, ou alterações nos parâmetros de motilidade do esperma sugeririam efeitos tóxicos pós-testiculares.
As análises do sêmen também podem indicar se a produção de células espermáticas foi afetada por um tóxico. A contagem e a morfologia dos espermatozoides fornecem índices da integridade da espermatogênese e da espermiogênese. Assim, o número de espermatozóides no ejaculado está diretamente correlacionado com o número de células germinativas por grama de testículo (Zukerman et al. 1978), enquanto a morfologia anormal é provavelmente resultado de espermiogênese anormal. Espermas mortos ou espermatozóides imóveis geralmente refletem os efeitos de eventos pós-testiculares. Assim, o tipo ou momento de um efeito tóxico pode indicar o alvo do tóxico. Por exemplo, a exposição de ratos machos ao 2-metoxietanol resultou em redução da fertilidade após quatro semanas (Chapin et al. 1985). Esta evidência, corroborada pelo exame histológico, indica que o alvo da toxicidade é o espermatócito (Chapin et al. 1984). Embora não seja ético expor humanos intencionalmente a tóxicos reprodutivos suspeitos, análises de sêmen de ejaculados em série de homens inadvertidamente expostos por um curto período de tempo a tóxicos potenciais podem fornecer informações úteis semelhantes.
A exposição ocupacional ao 1,2-dibromocloropropano (DBCP) reduziu a concentração de espermatozoides nos ejaculados de uma média de 79 milhões de células/ml em homens não expostos para 46 milhões de células/ml em trabalhadores expostos (Whorton et al. 1979). Ao remover os trabalhadores da exposição, aqueles com contagens reduzidas de espermatozóides tiveram uma recuperação parcial, enquanto os homens que haviam sido azoospérmicos permaneceram estéreis. A biópsia testicular revelou que o alvo do DBCP era a espermatogônia. Isso substancia a gravidade do efeito quando as células-tronco são alvo de substâncias tóxicas. Não houve indicações de que a exposição de homens ao DBCP estivesse associada a resultados adversos da gravidez (Potashnik e Abeliovich 1985). Outro exemplo de um tóxico direcionado à espermatogênese/espermiogênese foi o estudo de trabalhadores expostos ao dibrometo de etileno (EDB). Eles tinham mais espermatozoides com cabeças afiladas e menos espermatozóides por ejaculação do que os controles (Ratcliffe et al. 1987).
Danos genéticos são difíceis de detectar no esperma humano. Vários estudos em animais usando o ensaio letal dominante (Ehling et al. 1978) indicam que a exposição paterna pode produzir um resultado adverso na gravidez. Estudos epidemiológicos de grandes populações demonstraram maior frequência de abortos espontâneos em mulheres cujos maridos trabalhavam como mecânicos de veículos motorizados (McDonald et al. 1989). Tais estudos indicam a necessidade de métodos para detectar danos genéticos no esperma humano. Tais métodos estão sendo desenvolvidos por diversos laboratórios. Esses métodos incluem sondas de DNA para discernir mutações genéticas (Hecht 1987), cariótipo cromossômico espermático (Martin 1983) e avaliação da estabilidade do DNA por citometria de fluxo (Evenson 1986).
Figura 2. Exposições associadas positivamente a efeitos adversos na qualidade do sêmen
A Figura 2 lista as exposições conhecidas por afetar a qualidade do esperma e a Tabela 1 fornece um resumo dos resultados de estudos epidemiológicos dos efeitos paternos nos resultados reprodutivos.
Tabela 1. Estudos epidemiológicos dos efeitos paternos no resultado da gravidez
| Referência | Tipo de exposição ou ocupação | Associação com exposição1 | Efeito |
| Estudos populacionais baseados em registros | |||
| Lindbohm et ai. 1984 | solventes | - | Aborto espontâneo |
| Lindbohm et ai. 1984 | Estação de serviço | + | Aborto espontâneo |
| Daniell e Vaughan 1988 | Solventes orgânicos | - | Aborto espontâneo |
| McDonald et al. 1989 | Mecânica | + | Aborto espontâneo |
| McDonald et al. 1989 | Processamento de alimentos | + | defeitos de desenvolvimento |
| Lindbohm et ai. 1991a | Óxido de etileno | + | Aborto espontâneo |
| Lindbohm et ai. 1991a | Refinaria de petróleo | + | Aborto espontâneo |
| Lindbohm et ai. 1991a | impregnados de madeira | + | Aborto espontâneo |
| Lindbohm et ai. 1991a | Produtos químicos de borracha | + | Aborto espontâneo |
| Olsen et ai. 1991 | Metais | + | Risco de câncer infantil |
| Olsen et ai. 1991 | Machinists | + | Risco de câncer infantil |
| Olsen et ai. 1991 | Smiths | + | Risco de câncer infantil |
| Kristensen e outros. 1993 | solventes | + | Nascimento prematuro |
| Kristensen e outros. 1993 | Chumbo e solventes | + | Nascimento prematuro |
| Kristensen e outros. 1993 | Conduzir | + | Morte perinatal |
| Kristensen e outros. 1993 | Conduzir | + | Morbidade infantil do sexo masculino |
| Estudos de caso-controle | |||
| Kucera 1968 | Indústria de impressão | (+) | Lábio leporino |
| Kucera 1968 | pintar | (+) | Fenda palatina |
| Olsen 1983 See More | pintar | + | Danos ao sistema nervoso central |
| Olsen 1983 See More | solventes | (+) | Danos ao sistema nervoso central |
| Sever et ai. 1988 | Radiação de baixo nível | + | Defeitos do tubo neural |
| Taskinen et ai. 1989 | Solventes orgânicos | + | Aborto espontâneo |
| Taskinen et ai. 1989 | Hidrocarbonetos aromáticos | + | Aborto espontâneo |
| Taskinen et ai. 1989 | Dust | + | Aborto espontâneo |
| Gardner e outros. 1990 | Radiação | + | leucemia infantil |
| Bonde 1992 | Soldagem | + | Tempo para a concepção |
| Wilkins e Sinks 1990 | Agricultura | (+) | Tumor cerebral infantil |
| Wilkins e Sinks 1990 | Construção | (+) | Tumor cerebral infantil |
| Wilkins e Sinks 1990 | Processamento de alimentos/tabaco | (+) | Tumor cerebral infantil |
| Wilkins e Sinks 1990 | Metal | + | Tumor cerebral infantil |
| Lindbohmn et al. 1991b | Conduzir | (+) | Aborto espontâneo |
| Salmen et ai. 1992 | Conduzir | (+) | Defeitos congênitos |
| Veulemans et ai. 1993 | Éter de etileno glicol | + | Espermograma anormal |
| Chia et ai. 1992 | Metais | + | Cádmio no sêmen |
1 – sem associação significativa; (+) associação marginalmente significativa; + associação significativa.
Fonte: Adaptado de Taskinen 1993.
Sistema Neuroendócrino
O funcionamento geral do sistema reprodutivo é controlado pelo sistema nervoso e pelos hormônios produzidos pelas glândulas (o sistema endócrino). O eixo neuroendócrino reprodutivo do homem envolve principalmente o sistema nervoso central (SNC), a glândula pituitária anterior e os testículos. As entradas do SNC e da periferia são integradas pelo hipotálamo, que regula diretamente a secreção de gonadotrofina pela hipófise anterior. As gonadotrofinas, por sua vez, atuam principalmente nas células de Leydig no interstício e nas células de Sertoli e germinativas nos túbulos seminíferos para regular a espermatogênese e a produção de hormônios pelos testículos.
Eixo hipotalâmico-hipofisário
O hipotálamo secreta o neuro-hormônio liberador de gonadotrofina (GnRH) na vasculatura portal hipofisária para transporte para a glândula pituitária anterior. A secreção pulsátil desse decapeptídeo causa a liberação concomitante do hormônio luteinizante (LH) e, com menor sincronia e um quinto da potência, a liberação do hormônio folículo estimulante (FSH) (Bardin 1986). Existem evidências substanciais para apoiar a presença de um hormônio liberador de FSH separado, embora nenhum ainda tenha sido isolado (Savy-Moore e Schwartz 1980; Culler e Negro-Vilar 1986). Esses hormônios são secretados pela glândula pituitária anterior. O LH atua diretamente sobre as células de Leydig para estimular a síntese e liberação de testosterona, enquanto o FSH estimula a aromatização da testosterona em estradiol pela célula de Sertoli. A estimulação gonadotrópica causa a liberação desses hormônios esteróides na veia espermática.
A secreção de gonadotrofinas é, por sua vez, verificada pela testosterona e estradiol por meio de mecanismos de feedback negativo. A testosterona atua principalmente sobre o hipotálamo para regular a secreção de GnRH e, assim, reduz a frequência de pulso, principalmente, da liberação de LH. O estradiol, por outro lado, atua na glândula pituitária para reduzir a magnitude da liberação de gonadotrofinas. Por meio desses ciclos de feedback endócrino, a função testicular em geral e a secreção de testosterona especificamente são mantidas em um estado relativamente estável.
Eixo pituitário-testicular
LH e FSH são geralmente vistos como necessários para a espermatogênese normal. Presumivelmente, o efeito do LH é secundário à indução de altas concentrações intratesticulares de testosterona. Portanto, o FSH da hipófise e a testosterona das células de Leydig agem sobre as células de Sertoli dentro do epitélio dos túbulos seminíferos para iniciar a espermatogênese. A produção de espermatozoides persiste, embora quantitativamente reduzida, após a remoção do LH (e presumivelmente das altas concentrações intratesticulares de testosterona) ou do FSH. O FSH é necessário para iniciar a espermatogênese na puberdade e, em menor grau, para reiniciar a espermatogênese que foi interrompida (Matsumoto 1989; Sharpe 1989).
O sinergismo hormonal que serve para manter a espermatogênese pode envolver o recrutamento pelo FSH de espermatogônias diferenciadas para entrar na meiose, enquanto a testosterona pode controlar estágios subsequentes específicos da espermatogênese. O FSH e a testosterona também podem atuar sobre a célula de Sertoli para estimular a produção de um ou mais fatores parácrinos que podem afetar o número de células de Leydig e a produção de testosterona por essas células (Sharpe 1989). O FSH e a testosterona estimulam a síntese de proteínas pelas células de Sertoli, incluindo a síntese da proteína de ligação ao andrógeno (ABP), enquanto o FSH sozinho estimula a síntese de aromatase e inibina. ABP é secretada principalmente no fluido tubular seminífero e é transportada para a porção proximal da cabeça do epidídimo, possivelmente servindo como um carreador local de andrógenos (Bardin 1986). A aromatase catalisa a conversão de testosterona em estradiol nas células de Sertoli e em outros tecidos periféricos.
A inibina é uma glicoproteína que consiste em duas subunidades dissimilares ligadas por dissulfeto, a e b. Embora a inibina iniba preferencialmente a liberação de FSH, ela também pode atenuar a liberação de LH na presença de estimulação de GnRH (Kotsugi et al. 1988). FSH e LH estimulam a liberação de inibina com potência aproximadamente igual (McLachlan et al. 1988). Curiosamente, a inibina é secretada no sangue da veia espermática como pulsos que são sincronizados com os da testosterona (Winters 1990). Isso provavelmente não reflete as ações diretas do LH ou da testosterona na atividade das células de Sertoli, mas sim os efeitos de outros produtos das células de Leydig secretados nos espaços intersticiais ou na circulação.
A prolactina, que também é secretada pela glândula pituitária anterior, atua sinergicamente com LH e testosterona para promover a função reprodutiva masculina. A prolactina se liga a receptores específicos na célula de Leydig e aumenta a quantidade de complexo receptor de andrógeno dentro do núcleo de tecidos responsivos a andrógenos (Baker et al. 1977). A hiperprolactinemia está associada a reduções do tamanho testicular e da próstata, volume do sêmen e concentrações circulantes de LH e testosterona (Segal et al. 1979). A hiperprolactinemia também tem sido associada à impotência, aparentemente independente da alteração da secreção de testosterona (Thorner et al. 1977).
Ao medir metabólitos de hormônios esteróides na urina, deve-se levar em consideração o potencial de que a exposição em estudo possa alterar o metabolismo dos metabólitos excretados. Isso é especialmente pertinente, uma vez que a maioria dos metabólitos é formada pelo fígado, um alvo de muitos tóxicos. O chumbo, por exemplo, reduziu a quantidade de esteróides sulfatados excretados na urina (Apostoli et al. 1989). Os níveis sanguíneos de ambas as gonadotrofinas tornam-se elevados durante o sono à medida que o homem entra na puberdade, enquanto os níveis de testosterona mantêm esse padrão diurno durante a idade adulta nos homens (Plant 1988). Assim, amostras de sangue, urina ou saliva devem ser coletadas aproximadamente na mesma hora do dia para evitar variações devido a padrões secretores diurnos.
Os efeitos evidentes da exposição tóxica visando o sistema neuroendócrino reprodutivo são mais prováveis de serem revelados através de manifestações biológicas alteradas dos andrógenos. As manifestações significativamente reguladas por andrógenos no homem adulto que podem ser detectadas durante um exame físico básico incluem: (1) retenção de nitrogênio e desenvolvimento muscular; (2) manutenção da genitália externa e dos órgãos sexuais acessórios; (3) manutenção da laringe aumentada e cordas vocais espessas causando a voz masculina; (4) barba, crescimento de pêlos axilares e pubianos e recessão e calvície de pêlos temporais; (5) libido e desempenho sexual; (6) proteínas específicas de órgãos em tecidos (por exemplo, fígado, rins, glândulas salivares); e (7) comportamento agressivo (Bardin 1986). Modificações em qualquer uma dessas características podem indicar que a produção de andrógenos foi afetada.
Exemplos de efeitos tóxicos
O chumbo é um exemplo clássico de um tóxico que afeta diretamente o sistema neuroendócrino. As concentrações séricas de LH foram elevadas em homens expostos ao chumbo por menos de um ano. Este efeito não progrediu em homens expostos por mais de cinco anos. Os níveis séricos de FSH não foram afetados. Por outro lado, os níveis séricos de ABP foram elevados e os de testosterona total reduzidos em homens expostos ao chumbo por mais de cinco anos. Os níveis séricos de testosterona livre foram significativamente reduzidos após a exposição ao chumbo por três a cinco anos (Rodamilans et al. 1988). Em contraste, as concentrações séricas de LH, FSH, testosterona total, prolactina e 17-cetosteróides neutros totais não foram alteradas em trabalhadores com níveis circulantes mais baixos de chumbo, embora a frequência de distribuição da contagem de espermatozóides tenha sido alterada (Assennato et al. 1986) .
A exposição de pintores de estaleiros ao 2-etoxietanol também reduziu a contagem de espermatozóides sem uma alteração concomitante nas concentrações séricas de LH, FSH ou testosterona (Welch et al. 1988). Assim, os tóxicos podem afetar a produção de hormônios e as medidas de esperma de forma independente.
Trabalhadores do sexo masculino envolvidos na fabricação do nematocida DBCP experimentaram níveis séricos elevados de LH e FSH e reduziram a contagem de esperma e a fertilidade. Esses efeitos são aparentemente sequelas das ações do DBCP sobre as células de Leydig para alterar a produção ou ação do andrógeno (Mattison et al. 1990).
Vários compostos podem exercer toxicidade em virtude da semelhança estrutural com os hormônios esteroides reprodutivos. Assim, pela ligação ao respectivo receptor endócrino, os tóxicos podem atuar como agonistas ou antagonistas para interromper as respostas biológicas. Clordecona (Kepone), um inseticida que se liga aos receptores de estrogênio, reduz a contagem e motilidade dos espermatozóides, interrompe a maturação dos espermatozóides e reduz a libido. Embora seja tentador sugerir que esses efeitos resultam da interferência da clordecona nas ações do estrogênio no nível neuroendócrino ou testicular, os níveis séricos de testosterona, LH e FSH não se mostraram alterados nesses estudos de maneira semelhante aos efeitos da terapia com estradiol . O DDT e seus metabólitos também exibem propriedades esteróides e pode-se esperar que alterem a função reprodutiva masculina ao interferir nas funções hormonais esteróides. Xenobióticos, como bifenilos policlorados, bifenilos polibromados e pesticidas organoclorados, também podem interferir nas funções reprodutivas masculinas ao exercer atividade agonista/antagonista estrogênica (Mattison et al. 1990).
Função Sexual
A função sexual humana refere-se às atividades integradas dos testículos e das glândulas sexuais secundárias, dos sistemas de controle endócrino e dos componentes comportamentais e psicológicos da reprodução (libido) baseados no sistema nervoso central. Ereção, ejaculação e orgasmo são três eventos distintos, independentes, fisiológicos e psicodinâmicos que normalmente ocorrem concomitantemente nos homens.
Poucos dados confiáveis estão disponíveis sobre os efeitos da exposição ocupacional na função sexual devido aos problemas descritos acima. Foi demonstrado que as drogas afetam cada um dos três estágios da função sexual masculina (Fabro 1985), indicando o potencial de exposições ocupacionais para exercer efeitos semelhantes. Antidepressivos, antagonistas da testosterona e estimulantes da liberação de prolactina reduzem efetivamente a libido nos homens. Drogas anti-hipertensivas que atuam no sistema nervoso simpático induzem impotência em alguns homens, mas surpreendentemente, priapismo em outros. A fenoxibenzamina, um antagonista adrenoceptivo, tem sido usada clinicamente para bloquear a emissão seminal, mas não o orgasmo (Shilon, Paz e Homonnai, 1984). Drogas antidepressivas anticolinérgicas permitem a emissão seminal enquanto bloqueiam a ejeção seminal e o orgasmo, o que resulta em plasma seminal vazando da uretra em vez de ser ejetado.
Drogas recreativas também afetam a função sexual (Fabro 1985). O etanol pode reduzir a impotência enquanto aumenta a libido. Cocaína, heroína e altas doses de canabinóides reduzem a libido. Os opiáceos também atrasam ou prejudicam a ejaculação.
A vasta e variada gama de produtos farmacêuticos que demonstraram afetar o sistema reprodutor masculino fornece suporte para a noção de que os produtos químicos encontrados no local de trabalho também podem ser tóxicos reprodutivos. Métodos de pesquisa que sejam confiáveis e práticos para condições de estudo de campo são necessários para avaliar esta importante área da toxicologia reprodutiva.
" ISENÇÃO DE RESPONSABILIDADE: A OIT não se responsabiliza pelo conteúdo apresentado neste portal da Web em qualquer idioma que não seja o inglês, que é o idioma usado para a produção inicial e revisão por pares do conteúdo original. Algumas estatísticas não foram atualizadas desde a produção da 4ª edição da Enciclopédia (1998)."