Categorias crianças

1. Sangue (3)

1. Sangue
Editor de Capítulo: Bernard D. Goldstein
Conteúdo
Tabelas
Sistema hematopoiético e linfático
Bernard D. Goldstein
Leucemia, Linfomas Malignos e Mieloma Múltiplo
Timo Partanen, Paolo Boffetta, Elisabete Weiderpass
Agentes ou Condições de Trabalho que Afetam o Sangue
Bernard D. Goldstein
Tabelas
Clique em um link abaixo para visualizar a tabela no contexto do artigo.

2. Câncer (4)

2. Câncer
Editor de Capítulo: Paulo Boffetta
mesa de conteúdo
Tabelas
Introdução
Neil Pearce, Paolo Boffetta e Manolis Kogevinas
Carcinógenos ocupacionais
Paolo Boffetta, Rodolfo Saracci, Manolis Kogevinas, Julian Wilbourn e Harri Vainio
Câncer Ambiental
Bruce K. Armstrong e Paolo Boffetta
Prevenção
Por Gustavsson
Tabelas
Clique em um link abaixo para visualizar a tabela no contexto do artigo.
- Câncer ocupacional: principais fatos
- Proporções estimadas de câncer (PAR) atribuíveis a ocupações
- Avaliação de evidências de carcinogenicidade nas monografias da IARC
- Grupos de classificação do programa de monografias da IARC
- Grupo 1-Produtos químicos cancerígenos para humanos
- Grupo 2A - Produtos químicos provavelmente cancerígenos para humanos
- Grupo 2B—Produtos químicos possivelmente cancerígenos para humanos
- Pesticidas avaliados em Monografias da IARC, Volumes 1-63 (1972-1995)
- Drogas avaliadas nas Monografias da IARC, Volumes 1-63 (1972-1995)
- Agentes ambientais/exposições conhecidas ou suspeitas de câncer humano
- Indústrias, ocupações, exposições que apresentam um risco cancerígeno
- Indústrias, occs., exps. com excesso de câncer não carcinógenos definitivos
- Variações populacionais registradas de incidência de alguns cânceres comuns

3. Sistema cardiovascular (7)

3. Sistema Cardiovascular
Editores de Capítulo: Lothar Heinemann e Gerd Heuchert
Conteúdo
Tabelas e Figuras
Introdução
Lothar Heinemann e Gerd Heuchert
Morbidade e Mortalidade Cardiovascular na Força de Trabalho
Gottfried Enderlein e Lothar Heinemann
O conceito de fator de risco em doenças cardiovasculares
Lothar Heinemann, Gottfried Enderlein e Heide Stark
Programas de reabilitação e prevenção
Lothar Heinemann e Gottfried Enderlein
Perigos Físicos, Químicos e Biológicos
Fatores físicos
Heide Stark e Gerd Heuchert
Materiais Químicos Perigosos
Ulrike Tittelbach e Wolfram Dietmar Schneider
Riscos Biológicos
Regina Jäckel, Ulrike Tittelbach e Wolfram Dietmar Schneider
Tabelas
Clique em um link abaixo para ver a tabela no contexto do artigo
- Mortalidade por doenças cardiovasculares
- Taxas de mortalidade, grupos especiais de diagnóstico cardiovascular
- Taxa de doenças e capacidade de trabalho reduzida
- Trabalho associado a riscos cardiovasculares
- Infecções e doenças ocupacionais
figuras
Aponte para uma miniatura para ver a legenda da figura, clique para ver a figura no contexto do artigo.

4. Sistema Digestivo (6)

4. Sistema Digestivo
Editor de Capítulo: Heikki Savolainen
Conteúdo
figuras
Sistema digestivo
G.Frada
Boca e dentes
F. Gobbato
Fígado
George Kazantzis
Úlcera péptica
KS Cho
Câncer de fígado
Timo Partanen, Timo Kauppinen, Paolo Boffetta e Elisabete Weiderpass
Câncer de pâncreas
Timo Partanen, Timo Kauppinen, Paolo Boffetta e Elisabete Weiderpass
figuras
Aponte para uma miniatura para ver a legenda da figura, clique para ver a figura no contexto do artigo.

5. Saúde Mental (8)

5. Saúde mental
Editores de capítulos: Joseph J. Hurrell, Lawrence R. Murphy, Steven L. Sauter e Lennart Levi
Conteúdo
Tabelas e Figuras
Trabalho e Saúde Mental
Irene LD Houtman e Michiel AJ Kompier
Psicose relacionada ao trabalho
Craig Stenberg, Judith Holder e Krishna Tallur
Humor e Afeto
Depressão
Jay Lasser e Jeffrey P. Kahn
Ansiedade relacionada ao trabalho
Randal D. Beaton
Transtorno de estresse pós-traumático e sua relação com a saúde ocupacional e prevenção de lesões
Mark Braverman
Estresse e Burnout e suas Implicações no Ambiente de Trabalho
Herbert J. Freudenberger
Distúrbios Cognitivos
Catherine A. Heaney
Karoshi: Morte por excesso de trabalho
Takashi Haratani
Tabelas
Clique em um link abaixo para visualizar a tabela no contexto do artigo.
1. Visão geral esquemática de estratégias e exemplos de gerenciamento
figuras
Aponte para uma miniatura para ver a legenda da figura, clique para ver a figura no contexto do artigo.

6. Sistema musculoesquelético (14)

6. Sistema musculoesquelético
Editores de Capítulo: Hilkka Riihimäki e Eira Viikari-Juntura
Conteúdo
Tabelas e Figuras
Visão geral
Hilkka Riihimäki
Músculos
Gisela Sjøgaard
Tendões
Thomas J Armstrong
Ossos e articulações
David Hamerman
Discos intervertebrais
Sally Roberts e Jill PG Urban
Região lombar
Hilkka Riihimäki
Região da Coluna Torácica
Jarl-Erik Michelsson
Pescoço
Åsa Kilbom
Ombro
Mats Hagberg
Cotovelo
Eira Viikari-Juntura
Antebraço, Punho e Mão
Eira Viikari-Juntura
Quadril e Joelho
Eva Vingård
Perna, Tornozelo e Pé
Jarl-Erik Michelsson
Outras doenças
Marjatta Leirisalo-Repo
Tabelas
Clique em um link abaixo para visualizar a tabela no contexto do artigo.
- Estrutura-função dos componentes da junta
- Prevalência de problemas nas costas, em finlandeses com mais de 30 anos
- Reduzindo os riscos de lombalgia no trabalho
- Classificação de distúrbios lombares (Força-Tarefa de Quebec)
- Movimentos permitidos para a cabeça em condução prolongada
- Incidência de epicondilite em várias populações
- Incidência de tenossinovite/peritendinite
- Osteoartrose primária do quadril em Malmö, Suécia
- Diretrizes para o tratamento da artrite reumatoide
- Infecções conhecidas por desencadear artrite reativa
figuras
Aponte para uma miniatura para ver a legenda da figura, clique para ver a figura no contexto do artigo.

7. Sistema Nervoso (9)

7. Sistema Nervoso
Editor de Capítulo: Donna Mergler
Conteúdo
Tabelas e Figuras
Sistema Nervoso: Visão Geral
Donna Mergler e José A. Valciukas
Anatomia e Fisiologia
José A. Valciukas
Agentes Químicos Neurotóxicos
Peter Arlien-Søborg e Leif Simonsen
Manifestações de Intoxicação Aguda e Crônica Precoce
Donna Mergler
Prevenção da Neurotoxicidade no Trabalho
Barry johnson
Síndromes clínicas associadas à neurotoxicidade
Roberto G. Feldman
Medindo Déficits Neurotóxicos
Donna Mergler
Diagnóstico
Anna Maria Seppäläinen
Neuroepidemiologia Ocupacional
Olav Axelson
Tabelas
Clique em um link abaixo para visualizar a tabela no contexto do artigo.
- Nomes e principais funções de cada par de nervos cranianos
- Agrupando efeitos neurotóxicos quanto à neurotoxicidade
- Gases associados a efeitos neurotóxicos
- Metais neurotóxicos e seus compostos inorgânicos
- monômeros neurotóxicos
- Solventes orgânicos associados à neurotoxicidade
- Classes de pesticidas neurotóxicos comuns
- Outros produtos químicos associados à neurotoxicidade
- Lista de verificação de sintomas crônicos
- Efeitos neurofuncionais da exposição a algumas neurotoxinas
- Exposições químicas e síndromes neurotóxicas associadas
- Algumas baterias “centrais” para avaliar os efeitos neurotóxicos precoces
- Árvore de decisão para doenças neurotóxicas
- Efeitos neurofuncionais consistentes de exposições no local de trabalho a algumas das principais substâncias neurotóxicas
figuras
Aponte para uma miniatura para ver a legenda da figura, clique para ver a figura no contexto do artigo.

8. Sistema renal-urinário (2)

8. Sistema Renal-Urinário
Editor de Capítulo: George P. Hemstreet
Conteúdo
Tabelas e Figuras
Sistemas Renais-Urinários
George P. Hemstreet
Cânceres Renais-Urinários
Timo Partanen, Harri Vainio, Paolo Boffetta e Elisabete Weiderpass
Tabelas
Clique em um link abaixo para visualizar a tabela no contexto do artigo.
- Enzimas do metabolismo de drogas nos rins
- As causas mais comuns de hematúria, por idade e sexo
- Critérios para seleção de biomarcadores
- Biomarcadores potenciais ligados à lesão celular
- Insuficiência renal aguda e ocupação
- Segmentos do néfron afetados por substâncias tóxicas selecionadas
- Aplicações da citologia urinária
figuras
Aponte para uma miniatura para ver a legenda da figura, clique para ver a figura no contexto do artigo.

9. Sistema Reprodutivo (9)

9. Sistema reprodutivo
Editor de Capítulo: Graça Kawas Lemasters
Conteúdo
Tabelas e Figuras
Sistema Reprodutivo: Introdução
Lowell E. Sever
Introdução à função reprodutiva masculina e feminina
Donald R Mattison
Sistema Reprodutor Masculino e Toxicologia
Steven Schrader e Grace Kawas Lemasters
Estrutura do Sistema Reprodutivo Feminino e Vulnerabilidade do Órgão Alvo
Donald R Mattison
Exposições ocupacionais maternas e resultados adversos da gravidez
Graça Kawas Lemasters
Parto prematuro e trabalho
Nicole Mamelle
Exposições ocupacionais e ambientais ao recém-nascido
Mary S. Wolff e Patrisha M. Woolard
Proteção à Maternidade na Legislação
Marie-Claire Séguret
Gravidez e recomendações de trabalho nos EUA
Leon J. Warshaw
Tabelas
Clique em um link abaixo para visualizar a tabela no contexto do artigo.
1. Exposições com múltiplos endpoints adversos
2. Estudos epidemiológicos dos efeitos paternos no resultado da gravidez
3. Potenciais tóxicos reprodutivos femininos
4. Definição de perda fetal e morte infantil
5. Fatores para pequeno para idade gestacional e perda fetal
6. Fontes identificadas de fadiga ocupacional
7. Riscos relativos e índices de fadiga para parto prematuro
8. Risco de prematuridade por número de índices de fadiga ocupacional
9. Riscos relativos e mudanças nas condições de trabalho
10. Fontes e níveis de exposição de recém-nascidos
figuras
Aponte para uma miniatura para ver a legenda da figura, clique para ver a figura no contexto do artigo.

10. Sistema Respiratório (18)

10. Sistema respiratório
Editores de capítulos: Alois David e Gregory R. Wagner
Conteúdo
Tabelas e Figuras
Estrutura e função
Morton Lippmann
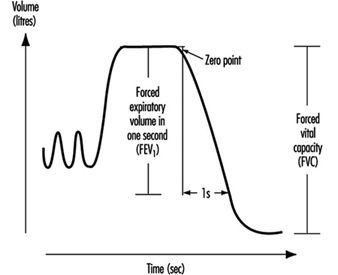
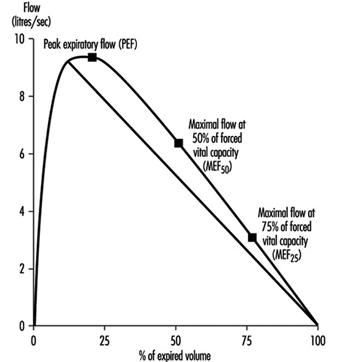
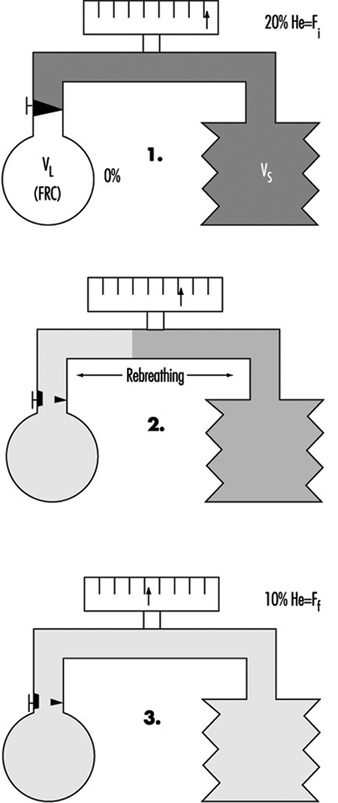
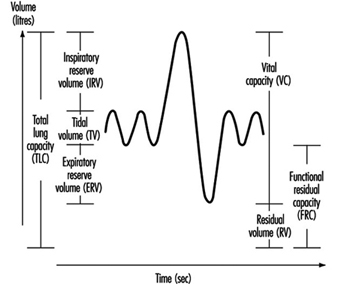
Exame de Função Pulmonar
Ulf Ulfvarson e Monica Dahlqvist
Doenças Causadas por Irritantes Respiratórios e Produtos Químicos Tóxicos
David LS Ryon e William N. Rom
Asma Ocupacional
George Friedman-Jimenez e Edward L. Petsonk
Doenças Causadas por Poeiras Orgânicas
Ragnar Rylander e Richard SF Schilling
Doença do berílio
Homayoun Kazemi
Pneumoconioses: Definição
Alois David
Classificação Internacional de Radiografias de Pneumoconioses da OIT
Michel Lesage
Etiopatogenia das Pneumoconioses
Patrick Sébastien e Raymond Bégin
Silicose
John E. Parker e Gregory R. Wagner
Doenças Pulmonares dos Carvoeiros
Michael D. Attfield, Edward L. Petsonk e Gregory R. Wagner
Doenças Relacionadas ao Amianto
Margaret R. Becklake
Doença do Metal Duro
Gerolamo Chiappino
Sistema respiratório: a variedade de pneumoconioses
Steven R. Short e Edward L. Petsonk
Doença de obstrução pulmonar crônica
Kazimierz Marek e Jan E. Zejda
Efeitos para a saúde de fibras sintéticas
James E. Lockey e Clara S. Ross
Câncer Respiratório
Paolo Boffetta e Elisabete Weiderpass
Infecções pulmonares adquiridas ocupacionalmente
Anthony A. Marfin, Ann F. Hubbs, Karl J. Musgrave e John E. Parker
Tabelas
Clique em um link abaixo para visualizar a tabela no contexto do artigo.
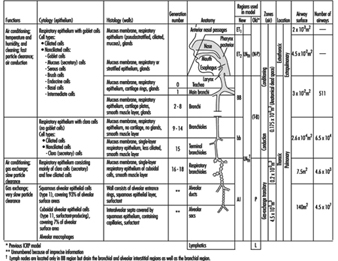
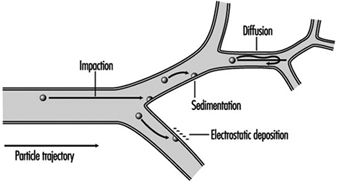
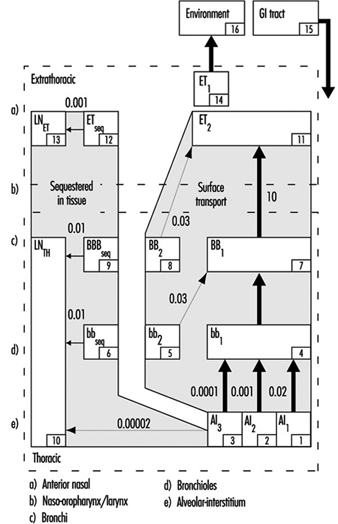
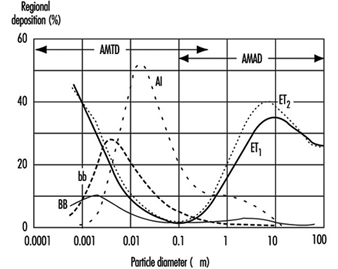
1. Regiões do trato respiratório e modelos de deposição de partículas
2. Critérios de poeira inalável, torácica e respirável
3. Resumo de irritantes respiratórios
4. Mecanismos de lesão pulmonar por substâncias inaladas
5. Compostos capazes de toxicidade pulmonar
6. Definição de caso médico de asma ocupacional
7. Passos na avaliação diagnóstica da asma no local de trabalho
8. Agentes sensibilizantes que podem causar asma ocupacional
9. Exemplos de fontes de perigos de exposição a poeira orgânica
10. Agentes em poeiras orgânicas com potencial atividade biológica
11. Doenças induzidas por poeiras orgânicas e seus códigos CID
12. Critérios diagnósticos para bissinose
13. Propriedades do berílio e seus compostos
14. Descrição das radiografias padrão
15. Classificação OIT 1980: Radiografias de Pneumoconioses
16. Doenças e condições relacionadas ao amianto
17. Principais fontes comerciais, produtos e usos do amianto
18. Prevalência de DPOC
19. Fatores de risco implicados na DPOC
20. Perda da função ventilatória
21. Classificação diagnóstica, bronquite crônica e enfisema
22. Teste de função pulmonar na DPOC
23. Fibras sintéticas
24. Carcinógenos respiratórios humanos estabelecidos (IARC)
25. Prováveis carcinógenos respiratórios humanos (IARC)
26. Doenças Infecciosas Respiratórias Adquiridas Ocupacionalmente
figuras
Aponte para uma miniatura para ver a legenda da figura, clique para ver a figura no contexto do artigo.

11. Sistemas sensoriais (8)

11. Sistemas Sensoriais
Editor de Capítulo: Heikki Savolainen
Conteúdo
Tabelas e Figuras
A orelha
Marcel-André Boillat
Distúrbios auditivos induzidos quimicamente
Peter Jacobsen
Distúrbios auditivos induzidos fisicamente
Pedro L. Pelmear
Equilíbrio
Lucy Yardley
Visão e Trabalho
Paule Rey e Jean-Jacques Meyer
Gosto
April E. Mott e Norman Mann
Cheiro
Abril E. Mott
Receptores cutâneos
Robert Dykes e Daniel McBain
Tabelas
Clique em um link abaixo para visualizar a tabela no contexto do artigo.
1. Cálculo típico de perda funcional de um audiograma
2. Requisitos visuais para diferentes atividades
3. Valores de iluminância recomendados para o projeto de iluminação
4. Requisitos visuais para uma carteira de motorista na França
5. Agentes/processos relatados para alterar o sistema de sabor
6. Agentes/processos associados a anormalidades olfativas
figuras
Aponte para uma miniatura para ver a legenda da figura, clique para ver a figura no contexto do artigo.

12. Doenças de pele (7)

12. Doenças da Pele
Editor de Capítulo: Louis-Philippe Durocher
Conteúdo
Tabelas e Figuras
Visão geral: doenças ocupacionais da pele
Donald J.Birmingham
Câncer de pele não melanocítico
Elisabete Weiderpass, Timo Partanen, Paolo Boffetta
Melanoma maligno
Timo Partanen, Paolo Boffetta, Elisabete Weiderpass
Dermatite de contato ocupacional
Denis Sasseville
Prevenção de Dermatoses Ocupacionais
Louis Philippe Durocher
Distrofia Ocupacional das Unhas
CD Calnan
Stigmata
H. Mierzecki
Tabelas
Clique em um link abaixo para visualizar a tabela no contexto do artigo.
1. Ocupações de risco
2. Tipos de dermatite de contato
3. irritantes comuns
4. Alérgenos comuns da pele
5. Fatores predisponentes para dermatite ocupacional
6. Exemplos de irritantes e sensibilizadores da pele com ocupações
7. Dermatoses ocupacionais em Quebec em 1989
8. Fatores de risco e seus efeitos na pele
9. Medidas coletivas (abordagem de grupo) para prevenção
figuras
Aponte para uma miniatura para ver a legenda da figura, clique para ver a figura no contexto do artigo.

13. Condições Sistêmicas (3)

13. Condições Sistêmicas
Editor de Capítulo: Howard M. Kipen
Conteúdo
figuras
Condições Sistêmicas: Uma Introdução
Howard M. Kipen
Síndrome do Edifício Doente
Michael J. Hodgson
Múltiplas sensibilidades químicas
Mark R. Cullen
figuras
Aponte para uma miniatura para ver a legenda da figura, clique para ver a figura no contexto do artigo.
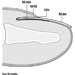
Estrutura do Sistema Reprodutivo Feminino e Vulnerabilidade do Órgão Alvo
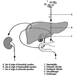
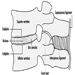
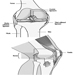
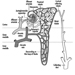
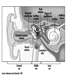
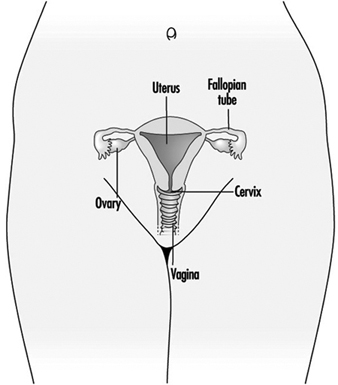
Figura 1. O sistema reprodutor feminino.
O sistema reprodutor feminino é controlado por componentes do sistema nervoso central, incluindo o hipotálamo e a hipófise. Consiste nos ovários, nas trompas de Falópio, no útero e na vagina (Figura 1). Os ovários, as gônadas femininas, são a fonte dos ovócitos e também sintetizam e secretam estrogênios e progestagênios, os principais hormônios sexuais femininos. As trompas de falópio transportam os oócitos e os espermatozóides do útero. O útero é um órgão muscular em forma de pêra, cuja parte superior se comunica através das trompas de Falópio com a cavidade abdominal, enquanto a parte inferior é contígua através do estreito canal do colo do útero com a vagina, que passa para o exterior. A Tabela 1 resume compostos, manifestações clínicas, local e mecanismos de ação de potenciais tóxicos reprodutivos.
Tabela 1. Potenciais tóxicos reprodutivos femininos
| Compound | Manifestação clínica | Local | Mecanismo/alvo |
| Reatividade química | |||
| Alquilante agentes |
menstruação alterada Amenorreia atrofia ovariana Diminuição da fertilidade Menopausa prematura |
ovário Útero |
Citotoxicidade das células da granulosa Citotoxicidade do oócito Citotoxicidade de células endometriais |
| Conduzir | menstruação anormal atrofia ovariana Diminuição da fertilidade |
hipotálamo Pituitário ovário |
FSH diminuído Progesterona diminuída |
| Mercúrio | menstruação anormal | hipotálamo ovário |
Produção e secreção alteradas de gonadotrofinas Toxicidade folicular Proliferação de células da granulosa |
| Cádmio | atresia folicular diestro persistente |
ovário Pituitário hipotálamo |
Toxicidade vascular Citotoxicidade das células da granulosa Citotoxicidade |
| Semelhança estrutural | |||
| Azatioprina | Número reduzido de folículos | ovário Oogênese |
Análogo de purina Interrupção da síntese de DNA/RNA |
| clordecona | Fertilidade prejudicada | hipotálamo | Agonista de estrogênio |
| DDT | menstruação alterada | Pituitário | Disrupção de FSH, LH |
| 2,4-D | Infertilidade | ||
| Lindano | Amenorreia | ||
| Toxafeno | Hipermenorreia | ||
| PCB, PBB | menstruação anormal | Disrupção de FSH, LH | |
Fonte: De Plowchalk, Meadows e Mattison 1992. Sugere-se que esses compostos sejam tóxicos reprodutivos de ação direta com base principalmente em testes de toxicidade em animais experimentais.
O Hipotálamo e a Hipófise
O hipotálamo está localizado no diencéfalo, que fica no topo do tronco cerebral e é cercado pelos hemisférios cerebrais. O hipotálamo é o principal intermediário entre os sistemas nervoso e endócrino, os dois principais sistemas de controle do corpo. O hipotálamo regula a glândula pituitária e a produção hormonal.
Os mecanismos pelos quais um produto químico pode interromper a função reprodutiva do hipotálamo geralmente incluem qualquer evento que possa modificar a liberação pulsátil do hormônio liberador de gonadotrofina (GnRH). Isso pode envolver uma alteração na frequência ou na amplitude dos pulsos de GnRH. Os processos suscetíveis à lesão química são aqueles envolvidos na síntese e secreção de GnRH – mais especificamente, transcrição ou tradução, empacotamento ou transporte axonal e mecanismos secretores. Esses processos representam locais onde os compostos quimicamente reativos de ação direta podem interferir na síntese hipotalâmica ou na liberação de GnRH. Uma frequência ou amplitude alterada dos pulsos de GnRH pode resultar de interrupções nas vias estimulatórias ou inibitórias que regulam a liberação de GnRH. Investigações sobre a regulação do gerador de pulsos de GnRH mostraram que catecolaminas, dopamina, serotonina, ácido γ-aminobutírico e endorfinas têm algum potencial para alterar a liberação de GnRH. Portanto, xenobióticos que sejam agonistas ou antagonistas desses compostos poderiam modificar a liberação de GnRH, interferindo na comunicação com a hipófise.
A prolactina, o hormônio folículo-estimulante (FSH) e o hormônio luteinizante (LH) são três hormônios proteicos secretados pela hipófise anterior que são essenciais para a reprodução. Estes desempenham um papel crítico na manutenção do ciclo ovariano, governando o recrutamento e maturação dos folículos, esteroidogênese, finalização da maturação dos óvulos, ovulação e luteinização.
O controle preciso e afinado do sistema reprodutivo é realizado pela hipófise anterior em resposta a sinais de retroalimentação positivos e negativos das gônadas. A liberação adequada de FSH e LH durante o ciclo ovariano controla o desenvolvimento folicular normal, e a ausência desses hormônios é seguida por amenorreia e atrofia gonadal. As gonadotrofinas desempenham um papel crítico no início de mudanças na morfologia dos folículos ovarianos e em seus microambientes esteróides por meio da estimulação da produção de esteróides e da indução de populações de receptores. A liberação oportuna e adequada dessas gonadotrofinas também é essencial para eventos ovulatórios e uma fase lútea funcional. Como as gonadotrofinas são essenciais para a função ovariana, síntese, armazenamento ou secreção alterados podem prejudicar seriamente a capacidade reprodutiva. A interferência com a expressão gênica - seja na transcrição ou tradução, eventos pós-traducionais ou empacotamento ou mecanismos secretores - pode modificar o nível de gonadotrofinas que atingem as gônadas. Substâncias químicas que atuam por meio de similaridade estrutural ou homeostase endócrina alterada podem produzir efeitos por interferência nos mecanismos normais de feedback. Os agonistas e antagonistas dos receptores de esteróides podem iniciar uma liberação inadequada de gonadotrofinas da hipófise, induzindo assim enzimas metabolizadoras de esteróides, reduzindo a meia-vida dos esteróides e subsequentemente o nível circulante de esteróides que atingem a hipófise.
O ovário
O ovário em primatas é responsável pelo controle da reprodução através de seus principais produtos, ovócitos e hormônios esteroides e proteicos. A foliculogênese, que envolve mecanismos regulatórios intra e extraovarianos, é o processo pelo qual os oócitos e os hormônios são produzidos. O próprio ovário possui três subunidades funcionais: o folículo, o oócito e o corpo lúteo. Durante o ciclo menstrual normal, esses componentes, sob a influência do FSH e LH, funcionam em conjunto para produzir um óvulo viável para fertilização e um ambiente adequado para implantação e subsequente gestação.
Durante o período pré-ovulatório do ciclo menstrual, o recrutamento e o desenvolvimento folicular ocorrem sob a influência do FSH e LH. O último estimula a produção de andrógenos pelas células da teca, enquanto o primeiro estimula a aromatização de andrógenos em estrogênios pelas células da granulosa e a produção de inibina, um hormônio protéico. A inibina atua na hipófise anterior para diminuir a liberação de FSH. Isso evita o excesso de estimulação do desenvolvimento folicular e permite o desenvolvimento contínuo do folículo dominante – o folículo destinado a ovular. A produção de estrogênio aumenta, estimulando tanto o pico de LH (resultando na ovulação) quanto as alterações celulares e secretoras na vagina, colo do útero, útero e oviduto que aumentam a viabilidade e o transporte dos espermatozóides.
Na fase pós-ovulatória, as células da teca e da granulosa que permanecem na cavidade folicular do óvulo ovulado, formam o corpo lúteo e secretam progesterona. Esse hormônio estimula o útero a fornecer um ambiente adequado para a implantação do embrião se ocorrer a fertilização. Ao contrário da gônada masculina, a gônada feminina tem um número finito de células germinativas no nascimento e, portanto, é exclusivamente sensível a tóxicos reprodutivos. Essa exposição da mulher pode levar à diminuição da fecundidade, aumento do desperdício da gravidez, menopausa precoce ou infertilidade.
Como unidade reprodutiva básica do ovário, o folículo mantém o delicado ambiente hormonal necessário para sustentar o crescimento e a maturação de um ovócito. Como observado anteriormente, esse processo complexo é conhecido como foliculogênese e envolve regulação intra e extraovariana. Numerosas alterações morfológicas e bioquímicas ocorrem à medida que um folículo primordial progride para um folículo pré-ovulatório (que contém um ovócito em desenvolvimento), e cada estágio de crescimento folicular exibe padrões únicos de sensibilidade à gonadotrofina, produção de esteróides e vias de feedback. Essas características sugerem que vários locais estão disponíveis para interação xenobiótica. Além disso, existem diferentes populações foliculares dentro do ovário, o que complica ainda mais a situação ao permitir toxicidade folicular diferencial. Isso cria uma situação em que os padrões de infertilidade induzidos por um agente químico dependeriam do tipo de folículo afetado. Por exemplo, a toxicidade aos folículos primordiais não produziria sinais imediatos de infertilidade, mas acabaria encurtando o tempo reprodutivo. Por outro lado, a toxicidade aos folículos antrais ou pré-ovulatórios resultaria em perda imediata da função reprodutiva. O complexo folicular é composto por três componentes básicos: células da granulosa, células da teca e o oócito. Cada um desses componentes tem características que podem torná-lo exclusivamente suscetível a danos químicos.
Vários investigadores exploraram a metodologia para triagem de xenobióticos quanto à toxicidade das células da granulosa, medindo os efeitos na produção de progesterona pelas células da granulosa em cultura. A supressão do estradiol da produção de progesterona pelas células da granulosa tem sido utilizada para verificar a capacidade de resposta das células da granulosa. O pesticida p,p'-DDT e seu isômero o,p'-DDT produzem supressão da produção de progesterona aparentemente com potências iguais às do estradiol. Em contraste, os pesticidas malation, aration e dieldrin e o fungicida hexaclorobenzeno não têm efeito. Uma análise mais detalhada das respostas isoladas das células da granulosa aos xenobióticos é necessária para definir a utilidade deste sistema de ensaio. A atratividade de sistemas isolados como esse é a economia e a facilidade de uso; entretanto, é importante lembrar que as células da granulosa representam apenas um componente do sistema reprodutivo.
As células da teca fornecem precursores para esteroides sintetizados pelas células da granulosa. Acredita-se que as células da teca sejam recrutadas das células do estroma ovariano durante a formação e crescimento do folículo. O recrutamento pode envolver proliferação celular estromal, bem como migração para regiões ao redor do folículo. Os xenobióticos que prejudicam a proliferação, migração e comunicação celular terão impacto na função celular tecal. Os xenobióticos que alteram a produção tecal de andrógenos também podem prejudicar a função folicular. Por exemplo, os androgênios metabolizados em estrogênios pelas células da granulosa são fornecidos pelas células da teca. Espera-se que alterações na produção de andrógenos nas células da teca, sejam elas aumentadas ou diminuídas, tenham um efeito significativo na função folicular. Por exemplo, acredita-se que a produção excessiva de andrógenos pelas células da teca levará à atresia folicular. Além disso, a produção prejudicada de andrógenos pelas células da teca pode levar à diminuição da produção de estrogênio pelas células da granulosa. Qualquer uma das circunstâncias terá um impacto claro no desempenho reprodutivo. Atualmente, pouco se sabe sobre a vulnerabilidade das células tecais aos xenobióticos.
Embora haja uma acuidade de informação definindo a vulnerabilidade das células ovarianas aos xenobióticos, existem dados que demonstram claramente que os oócitos podem ser danificados ou destruídos por tais agentes. Agentes alquilantes destroem oócitos em humanos e animais experimentais. O chumbo produz toxicidade ovariana. O mercúrio e o cádmio também produzem dano ovariano que pode ser mediado pela toxicidade do oócito.
Fertilização para Implantação
Gametogênese, liberação e união de células germinativas masculinas e femininas são eventos preliminares que levam a um zigoto. Os espermatozóides depositados na vagina devem entrar no colo do útero e se mover através do útero e na trompa de falópio para encontrar o óvulo. a penetração do óvulo pelo esperma e a fusão de seus respectivos DNAs compreendem o processo de fertilização. Após a fertilização, a divisão celular é iniciada e continua durante os próximos três ou quatro dias, formando uma massa sólida de células chamada mórula. As células da mórula continuam a se dividir e, quando o embrião em desenvolvimento chega ao útero, é uma bola oca chamada blastocisto.
Após a fertilização, o embrião em desenvolvimento migra através da trompa de Falópio para o útero. O blastocisto entra no útero e se implanta no endométrio aproximadamente sete dias após a ovulação. Neste momento, o endométrio está na fase pós-ovulatória. A implantação permite que o blastocisto absorva nutrientes ou substâncias tóxicas das glândulas e vasos sanguíneos do endométrio.
Exposições ocupacionais maternas e resultados adversos da gravidez
O emprego remunerado entre as mulheres está crescendo em todo o mundo. Por exemplo, quase 70% das mulheres nos Estados Unidos trabalham fora de casa durante a idade reprodutiva predominante (de 20 a 34 anos). Além disso, desde a década de 1940 tem havido uma tendência quase linear na produção de produtos químicos orgânicos sintéticos, criando um ambiente mais perigoso para a trabalhadora grávida e seus filhos.
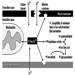
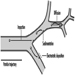
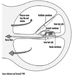
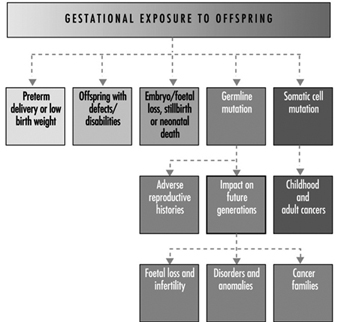
Em última análise, o sucesso reprodutivo de um casal depende de um delicado equilíbrio físico-químico entre o pai, a mãe e o feto. As alterações metabólicas que ocorrem durante a gravidez podem aumentar a exposição a substâncias tóxicas perigosas tanto para o trabalhador quanto para o feto. Essas alterações metabólicas incluem aumento da absorção pulmonar, aumento do débito cardíaco, retardo do esvaziamento gástrico, aumento da motilidade intestinal e aumento da gordura corporal. Conforme mostrado na figura 1, a exposição do concetus pode produzir efeitos variados, dependendo da fase de desenvolvimento - embriogênese precoce ou tardia ou período fetal.
Figura 1. Consequências da exposição materna a tóxicos na prole.
O tempo de transporte de um óvulo fertilizado antes da implantação é entre dois e seis dias. Durante esse estágio inicial, o embrião pode ser exposto a compostos químicos que penetram nos fluidos uterinos. A absorção de compostos xenófobos pode ser acompanhada por alterações degenerativas, alteração no perfil da proteína blastocística ou falha no implante. O insulto durante este período provavelmente levará a um aborto espontâneo. Com base em dados experimentais, acredita-se que o embrião seja bastante resistente ao insulto teratogênico neste estágio inicial porque as células não iniciaram a sequência complexa de diferenciação química.
O período da embriogênese posterior é caracterizado pela diferenciação, mobilização e organização de células e tecidos em rudimentos de órgãos. A patogênese precoce pode induzir morte celular, falha na interação celular, biossíntese reduzida, movimento morfogênico prejudicado, ruptura mecânica, aderências ou edema (Paul 1993). Os fatores mediadores que determinam a suscetibilidade incluem via e nível de exposição, padrão de exposição e genótipo fetal e materno. Fatores extrínsecos, como deficiências nutricionais ou efeitos aditivos, sinérgicos ou antagônicos associados a múltiplas exposições, podem afetar ainda mais a resposta. Respostas indesejáveis durante a embriogênese tardia podem culminar em aborto espontâneo, defeitos estruturais graves, perda fetal, retardo de crescimento ou anormalidades do desenvolvimento.
O período fetal se estende desde a embriogênese até o nascimento e é definido como começando em 54 a 60 dias de gestação, com o concetus tendo um comprimento de coroa de 33 mm. A distinção entre o período embrionário e fetal é um tanto arbitrária. O período fetal é caracterizado desenvolvimentalmente pelo crescimento, histogênese e maturação funcional. A toxicidade pode se manifestar por uma redução no tamanho e número de células. O cérebro ainda é sensível a lesões; a mielinização é incompleta até depois do nascimento. Retardo do crescimento, defeitos funcionais, interrupção da gravidez, efeitos comportamentais, carcinogênese translacental ou morte podem resultar de toxicidade durante o período fetal. Este artigo discute os efeitos biológicos, sociológicos e epidemiológicos das exposições ambientais/ocupacionais maternas.
Perda Embrionária/Fetal
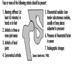
Os estágios de desenvolvimento do zigoto, definidos em dias a partir da ovulação (DOV), procedem do estágio de blastocisto nos dias 15 a 20 (um a seis DOV), com implantação ocorrendo no dia 20 ou 21 (seis ou sete DOV), até o período embrionário dos dias 21 a 62 (sete a 48 VD) e o período fetal do dia 63 (49+ VD) até o período designado de viabilidade, variando de 140 a 195 dias. As estimativas da probabilidade de interrupção da gravidez em um desses estágios dependem tanto da definição de perda fetal quanto do método usado para mensurar o evento. Existe uma variabilidade considerável na definição de perda fetal precoce versus tardia, variando do final da semana 20 à semana 28. As definições de morte fetal e infantil recomendadas pela Organização Mundial da Saúde (1977) estão listadas na tabela 1. Nos Estados Unidos a idade gestacional que define o limite inferior para natimortos agora é amplamente aceita como 20 semanas.
Tabela 1. Definição de perda fetal e óbito infantil
| Aborto espontâneo | ≤500 g ou 20-22 semanas ou 25 cm de comprimento |
| Natimorto | 500 g (1000 g Internacional) inviável |
| Morte neonatal precoce | Óbito de nascido vivo ≤ 7 dias (168 horas) |
| Morte neonatal tardia | 7 dias a ≤28 dias |
Fonte: Organização Mundial da Saúde 1977.
Como a maioria dos fetos abortados precocemente tem anomalias cromossômicas, foi sugerido que, para fins de pesquisa, uma distinção mais precisa deveria ser feita – entre perda fetal precoce, antes de 12 semanas de gestação, e perda fetal posterior (Källén 1988). Ao examinar perdas fetais tardias, também pode ser apropriado incluir mortes neonatais precoces, pois a causa pode ser semelhante. A OMS define morte neonatal precoce como a morte de uma criança com sete dias ou menos e morte neonatal tardia como ocorrendo entre sete e 29 dias. Em estudos realizados em países em desenvolvimento, é importante distinguir entre mortes pré-parto e intraparto. Devido a partos problemáticos, as mortes intraparto representam uma grande parte dos natimortos em países menos desenvolvidos.
Em uma revisão de Kline, Stein e Susser (1989) de nove estudos retrospectivos ou transversais, as taxas de perda fetal antes de 20 semanas de gestação variaram de 5.5 a 12.6%. Quando a definição foi ampliada para incluir perdas até 28 semanas de gestação, a taxa de perda fetal variou entre 6.2 e 19.6%. As taxas de perda fetal entre gestações clinicamente reconhecidas em quatro estudos prospectivos, no entanto, tiveram uma faixa relativamente estreita de 11.7 a 14.6% para o período gestacional de u a 28 semanas. Essa taxa mais baixa, observada em projetos prospectivos versus retrospectivos ou transversais, pode ser atribuída a diferenças nas definições subjacentes, relatórios incorretos de abortos induzidos como espontâneos ou classificação incorreta de menstruações atrasadas ou abundantes como perda fetal.
Quando abortos ocultos ou perdas “químicas” precoces identificadas por um nível elevado de gonadotrofinas coriônicas humanas (hCG) são incluídos, a taxa total de abortos espontâneos salta dramaticamente. Em um estudo usando métodos de hCG, a incidência de perda subclínica pós-implantação de óvulos fertilizados foi de 22% (Wilcox et al. 1988). Nestes estudos, o hCG urinário foi medido com ensaio imunorradiométrico usando um anticorpo de detecção. O ensaio originalmente usado por Wilcox empregou um agora extinto anticorpo policlonal de coelho de alta afinidade. Estudos mais recentes usaram um anticorpo monoclonal inesgotável que requer menos de 5 ml de urina para replicar amostras. O fator limitante para o uso desses ensaios em estudos de campo ocupacional não é apenas o custo e os recursos necessários para coordenar a coleta, armazenamento e análise de amostras de urina, mas também a grande população necessária. Em um estudo sobre perdas gestacionais precoces em trabalhadoras expostas a terminais de exibição de vídeo (VDTs), aproximadamente 7,000 mulheres foram rastreadas para adquirir uma população utilizável de 700 mulheres. Essa necessidade de dez vezes o tamanho da população para obter uma amostra adequada decorre da redução do número de mulheres disponíveis devido à inelegibilidade por idade, esterilidade e inscrição exclusivamente de mulheres que não usam contraceptivos ou formas relativamente ineficazes de contracepção .
Estudos ocupacionais mais convencionais usaram dados gravados ou de questionários para identificar abortos espontâneos. As fontes de dados gravadas incluem estatísticas vitais e registros hospitalares, de médicos particulares e de clínicas ambulatoriais. O uso de sistemas de registro identifica apenas um subconjunto de todas as perdas fetais, principalmente aquelas que ocorrem após o início do pré-natal, geralmente após dois a três períodos perdidos. Os dados do questionário são coletados por correio ou em entrevistas pessoais ou por telefone. Ao entrevistar mulheres para obter histórias reprodutivas, é possível obter uma documentação mais completa de todas as perdas reconhecidas. As perguntas que geralmente são incluídas nas histórias reprodutivas incluem todos os resultados da gravidez; cuidados pré-natais; história familiar de resultados adversos da gravidez; história conjugal; Estado nutricional; peso da re-gravidez; altura; ganho de peso; uso de cigarro, álcool e medicamentos prescritos e não prescritos; estado de saúde da mãe durante e antes da gravidez; e exposições em casa e no local de trabalho a agentes físicos e químicos, como vibração, radiação, metais, solventes e pesticidas. Dados de entrevistas sobre abortos espontâneos podem ser uma fonte válida de informação, especialmente se a análise incluir aqueles de oito semanas de gestação ou mais e aqueles que ocorreram nos últimos 10 anos.
Os principais fatores físicos, genéticos, sociais e ambientais associados ao aborto espontâneo estão resumidos na tabela 2. Para garantir que a relação exposição-efeito observada não se deva a uma relação de confusão com outro fator de risco, é importante identificar os fatores de risco que podem estar associados ao desfecho de interesse. As condições associadas à perda fetal incluem sífilis, rubéola, infecções genitais por micolasma, herpes simples, infecções uterinas e hiperpirexia geral. Um dos fatores de risco mais importantes para o aborto espontâneo clinicamente reconhecido é uma história de gravidez que terminou em perda fetal. Maior gravidade está associada a maior risco, mas isso pode não ser independente de uma história de aborto espontâneo. Existem interpretações conflitantes da gravidez como fator de risco por causa de sua associação com a idade materna, história reprodutiva e heterogeneidade das mulheres em diferentes níveis de gravidez. As taxas de aborto espontâneo são maiores para mulheres com menos de 16 anos e mais de 36 anos. Depois de ajustar para gravidez e história de perda de gravidez, as mulheres com mais de 40 anos demonstraram ter o dobro do risco de perda fetal do que as mulheres mais jovens. O risco aumentado para mulheres mais velhas tem sido associado a um aumento de anomalias cromossômicas, particularmente trissomia. os possíveis efeitos mediados por homens associados à perda fetal foram recentemente revisados (Savitz, Sonnerfeld e Olshaw 1994). Uma relação mais forte foi demonstrada com a exposição paterna a mercúrio e gases anestésicos, bem como uma relação sugestiva, mas inconsistente, com exposição a chumbo, fabricação de borracha, solventes selecionados e alguns pesticidas.
Tabela 2. Fatores associados ao pequeno para idade gestacional e perda fetal
| Pequeno para a idade gestacional | |
| Físico-genético | Ambiental-social |
| Parto prematuro Nascimentos múltiplos Feto malformado Hipertensão Anomalia da placenta ou cordão História médica materna História de resultados adversos da gravidez Corrida Anomalias cromossômicas Sexo Altura materna, peso, ganho de peso Altura paterna Paridade Duração da gestação Intervalo curto entre as gestações |
subnutrição Baixa renda/educação ruim Tabagismo materno Consumo materno de álcool Exposição profissional Estresse psicossocial Altitude Histórico de infecções Uso de maconha |
| Perda fetal | |
| Físico-genético | Ambiental-social |
| Maior gravidade Idade maternal Ordem de nascimento Corrida Aborto espontâneo de repetição Diabetes dependente de insulina Distúrbios uterinos Geminação Fator imunológico Fatores hormonais |
Status socioeconômico História de tabagismo Drogas prescritas e recreativas Uso de álcool A má nutrição Infecções/febre materna Espermicidas Fatores de emprego Exposição química Irradiação |
O status do emprego pode ser um fator de risco independentemente de um perigo físico ou químico específico e pode atuar como um fator de confusão na avaliação da exposição ocupacional e aborto espontâneo. Alguns investigadores sugerem que as mulheres que permanecem no mercado de trabalho têm maior probabilidade de ter um histórico adverso de gravidez e, como resultado, podem continuar trabalhando; outros acreditam que esse grupo é uma subpopulação inerentemente mais apta devido a rendas mais altas e melhor assistência pré-natal.
Anomalias congênitas
Durante os primeiros 60 dias após a concepção, o bebê em desenvolvimento pode ser mais sensível aos tóxicos xenobióticos do que em qualquer outro estágio do ciclo de vida. Historicamente, terata e malformações congênitas referem-se a defeitos estruturais reenviados ao nascimento que podem ser macroscópicos ou microscópicos, internos ou externos, hereditários ou não hereditários, únicos ou múltiplos. A anomalia congênita, no entanto, é mais amplamente definida como incluindo comportamento, função e bioquímica anormais. As malformações podem ser únicas ou múltiplas; defeitos cromossômicos geralmente produzem defeitos múltiplos, enquanto alterações em um único gene ou exposição a agentes ambientais podem causar defeitos únicos ou uma síndrome.
A incidência de malformações depende do estado do feto - nascido vivo, aborto espontâneo, natimorto. No geral, a taxa de anormalidade em abortos espontâneos é de aproximadamente 19%, um aumento de dez vezes em relação ao observado em nascidos vivos (Sheard, Fantel e Fitsimmons 1989). Uma taxa de 32% de anomalias foi encontrada entre fetos natimortos com peso superior a 500 g. A incidência de defeitos graves em nascidos vivos é de cerca de 2.24% (Nelson e Holmes 1989). A prevalência de defeitos menores varia entre 3 e 15% (média de cerca de 10%). As anomalias de nascimento estão associadas a fatores genéticos (10.1%), herança multifatorial (23%), fatores uterinos (2.5%), gemelaridade (0.4%) ou teratógenos (3.2%). As causas dos defeitos remanescentes são desconhecidas. As taxas de malformação são aproximadamente 41% maiores para os meninos do que para as meninas e isso é explicado pela taxa significativamente maior de anomalias dos órgãos genitais masculinos.
Um desafio no estudo das malformações é decidir como agrupar os defeitos para análise. As anomalias podem ser classificadas por vários parâmetros, incluindo gravidade (maior, menor), patogênese (deformação, interrupção), associada versus isolada, anatômica por sistema de órgãos e etiológica (por exemplo, defeitos cromossômicos, de um único gene ou induzidos por teratógenos). Frequentemente, todas as malformações são combinadas ou a combinação é baseada na categorização maior ou menor. Uma malformação maior pode ser definida como aquela que resulta em morte, requer cirurgia ou tratamento médico ou constitui uma deficiência física ou psicológica substancial. A justificativa para combinar anomalias em grandes grupos é que a maioria surge, aproximadamente no mesmo período de tempo, durante a organogênese. Assim, ao manter tamanhos amostrais maiores, o número total de casos é aumentado com um aumento concomitante no poder estatístico. Se, no entanto, o efeito da exposição for específico para um determinado tipo de malformação (por exemplo, sistema nervoso central), tal agrupamento pode mascarar o efeito. Alternativamente, as malformações podem ser agrupadas por sistema orgânico. Embora esse método possa ser uma melhoria, certos defeitos podem dominar a classe, como deformidades em varo dos pés no sistema músculo-esquelético. Dada uma amostra suficientemente grande, a abordagem ideal é dividir os defeitos em grupos embriologicamente ou patogenicamente homogêneos (Källén 1988). Considerações devem ser feitas para a exclusão ou inclusão de certas malformações, como aquelas que provavelmente são causadas por defeitos cromossômicos, condições autossômicas dominantes ou mau posicionamento no útero. Em última análise, ao analisar anomalias congênitas, deve-se manter um equilíbrio entre manter a precisão e comprometer o poder estatístico.
Vários tóxicos ambientais e ocupacionais têm sido associados a anomalias congênitas na prole. Uma das associações mais fortes é o consumo materno de alimentos contaminados com metilmercúrio causando anormalidades morfológicas, do sistema nervoso central e neurocomportamentais. No Japão, o conjunto de casos foi relacionado ao consumo de peixes e mariscos contaminados com mercúrio proveniente do efluente de uma fábrica química. A prole mais severamente afetada desenvolveu paralisia cerebral. A ingestão materna de bifenilos policlorados (CBs) de óleo de arroz contaminado deu origem a bebês com vários distúrbios, incluindo retardo de crescimento, pigmentação marrom escura da pele, erupção precoce dos dentes, hiperplasia gengival, sutura sagital larga, edema facial e exoftalmoses. Ocupações que envolvem exposições a misturas têm sido associadas a uma variedade de resultados adversos. Os descendentes de mulheres que trabalham na indústria de ul e aer, em trabalhos de laboratório ou em empregos que envolvam “conversões” ou refinamento de aer, também apresentam risco aumentado de defeitos do sistema nervoso central, cardíacos e fendas orais. As mulheres que trabalham em trabalhos industriais ou de construção com exposições não especificadas tiveram um aumento de 50% nos defeitos do sistema nervoso central, e as mulheres que trabalham em transporte e comunicação tiveram duas vezes o risco de ter um filho com fissura oral. Os veterinários representam um grupo único de profissionais de saúde expostos a gases anestésicos, radiação, traumas causados por coices de animais, inseticidas e doenças zoonóticas. Embora nenhuma diferença tenha sido encontrada na taxa de abortos espontâneos ou no peso ao nascer da prole entre veterinárias e advogadas, houve um excesso significativo de defeitos congênitos entre os veterinários (Schenker et al. 1990). Listas de teratógenos conhecidos, possíveis e improváveis estão disponíveis, bem como bancos de dados de computador e linhas de risco para obter informações atuais sobre teratógenos potenciais (Paul 1993). Avaliar anomalias congênitas em uma coorte ocupacional é particularmente difícil, no entanto, devido ao grande tamanho da amostra necessário para poder estatístico e nossa capacidade limitada de identificar exposições específicas que ocorrem durante uma janela de tempo estreita, principalmente nos primeiros 55 dias de gestação.
Pequeno para idade gestacional
Entre os muitos fatores ligados à sobrevivência infantil, o subdesenvolvimento físico associado ao baixo peso ao nascer (BPN) representa um dos maiores riscos. O ganho de peso significativo do feto não começa até o segundo trimestre. O concetus pesa 1 g com oito semanas, 14 g com 12 semanas e atinge 1.1 kg com 28 semanas. Um adicional de 1.1 kg é ganho a cada seis semanas até o termo. O recém-nascido normal pesa aproximadamente 3,200 g a termo. O peso do recém-nascido depende de sua taxa de crescimento e de sua idade gestacional no momento do parto. Um bebê com crescimento retardado é considerado pequeno para a idade gestacional (PIG). Se um bebê nascer antes do termo, terá um peso reduzido, mas não necessariamente terá retardo de crescimento. Os fatores associados ao parto prematuro são discutidos em outro lugar, e o foco dessa discussão é o recém-nascido com retardo de crescimento. Os termos SGA e LBW serão usados indistintamente. Uma criança com baixo peso ao nascer é definida como uma criança com peso inferior a 2,500 g, muito baixo peso ao nascer é definida como inferior a 1,500 g e extremamente baixo peso ao nascer é inferior a 1,000 g (OMS 1969).
Ao examinar as causas de crescimento reduzido, é importante distinguir entre retardo de crescimento assimétrico e simétrico. O retardo de crescimento assimétrico, ou seja, onde o peso é mais afetado do que a estrutura esquelética, está associado principalmente a um fator de risco que opera durante o final da gravidez. Por outro lado, o retardo de crescimento simétrico pode estar mais provavelmente associado a uma etiologia que ocorre durante todo o período da gestação (Kline, Stein e Susser, 1989). A diferença nas taxas entre retardo de crescimento assimétrico e simétrico é especialmente aparente quando se comparam países desenvolvidos e em desenvolvimento. A taxa de retardo de crescimento nos países em desenvolvimento é de 10 a 43% e é basicamente simétrica, sendo o fator de risco mais importante a má nutrição. Nos países desenvolvidos, o retardo do crescimento fetal é geralmente muito menor, de 3 a 8%, e geralmente é assimétrico com uma etiologia multifatorial. Portanto, em todo o mundo, a proporção de bebês com baixo peso ao nascer definidos como crescimento intrauterino retardado, em vez de prematuros, varia drasticamente. Na Suécia e nos Estados Unidos, a proporção é de aproximadamente 45%, enquanto em países em desenvolvimento, como a Índia, a proporção varia entre aproximadamente 79 e 96% (Villar e Belizan 1982).
Estudos da fome holandesa mostraram que a fome confinada ao terceiro trimestre deprimia o crescimento fetal em um padrão assimétrico, com o peso ao nascer sendo afetado principalmente e a circunferência da cabeça menos afetada (Stein, Susser e Saenger 1975). A assimetria de crescimento também foi observada em estudos de exposições ambientais. Em um estudo com 202 gestantes residentes em bairros com alto risco de exposição ao chumbo, amostras de sangue materno pré-natal foram coletadas entre a sexta e a 28ª semana de gestação (Bornschein, Grote e Mitchell 1989). Os níveis de chumbo no sangue foram associados a uma diminuição do peso e comprimento ao nascer, mas não da circunferência da cabeça, após o ajuste para outros fatores de risco relevantes, incluindo duração da gestação, status socioeconômico e uso de álcool ou cigarros. A descoberta de chumbo no sangue materno como um fator no comprimento ao nascer foi observada inteiramente em bebês caucasianos. O comprimento ao nascer de bebês caucasianos diminuiu aproximadamente 2.5 cm por unidade logarítmica de chumbo no sangue materno. Deve-se ter cuidado na seleção da variável de resultado. Se apenas o peso ao nascer tivesse sido selecionado para estudo, a descoberta dos efeitos do chumbo em outros parâmetros de crescimento poderia ter sido perdida. Além disso, se caucasianos e afro-americanos tivessem sido agrupados na análise acima, os efeitos diferenciais sobre os caucasianos, talvez devido a diferenças genéticas no armazenamento e na capacidade de ligação do chumbo, podem ter sido perdidos. Um efeito de confusão significativo também foi observado entre o chumbo no sangue pré-natal e a idade materna e o peso ao nascer da prole após o ajuste para outras covariáveis. Os resultados indicam que para uma mulher de 30 anos com um nível estimado de chumbo no sangue de cerca de 20 mg/dl, a prole pesava aproximadamente 2,500 g em comparação com aproximadamente 3,000 g para uma jovem de 20 anos com níveis de chumbo semelhantes. Os investigadores especularam que essa diferença observada pode indicar que as mulheres mais velhas são mais sensíveis ao insulto adicional da exposição ao chumbo ou que as mulheres mais velhas podem ter uma carga total de chumbo maior devido a um número maior de anos de exposição ou níveis ambientais mais altos de chumbo quando eram crianças. Outro fator pode ser o aumento da pressão arterial. No entanto, a lição importante é que o exame cuidadoso de subpopulações de alto risco por idade, raça, status econômico, hábitos de vida diários, sexo da prole e outras diferenças genéticas pode ser necessário para descobrir os efeitos mais sutis das exposições sobre o crescimento fetal. e o desenvolvimento.
Os fatores de risco associados ao baixo peso ao nascer estão resumidos na Tabela 5. A classe social, medida por renda ou escolaridade, persiste como fator de risco em situações nas quais não há diferenças étnicas. Outros fatores que podem estar operando sob classe social ou raça podem incluir tabagismo, trabalho físico, cuidados pré-natais e nutrição. As mulheres entre 25 e 29 anos têm menos probabilidade de ter filhos com retardo de crescimento. O tabagismo materno aumenta o risco de filhos com baixo peso ao nascer em cerca de 200% para fumantes inveterados. As condições médicas maternas associadas ao BPN incluem anormalidades placentárias, doença cardíaca, pneumonia viral, doença hepática, re-eclamsia, eclamsia, hipertensão crônica, ganho de peso e hieremese. Uma história gestacional adversa de perda fetal, parto prematuro ou recém-nascido de baixo peso aumenta de duas a quatro vezes o risco de um bebê pré-termo com baixo peso ao nascer. Um intervalo entre nascimentos de menos de um ano triplica o risco de ter uma criança com baixo peso ao nascer. As anomalias cromossômicas associadas ao crescimento anormal incluem a síndrome de Down, a trissomia do cromossomo 18 e a maioria das síndromes de malformação.
Fumar cigarros é um dos principais comportamentos mais diretamente relacionados com filhos com baixo peso. Foi demonstrado que o tabagismo materno durante a gravidez aumenta o risco de uma criança com baixo peso ao nascer em duas a três vezes e causa um déficit de peso total entre 150 e 400 g. A nicotina e o monóxido de carbono são considerados os agentes causadores mais prováveis, uma vez que ambos são transferidos rápida e referencialmente através da placenta. A nicotina é um poderoso vasoconstritor, e diferenças significativas no tamanho dos vasos umbilicais de mães fumantes foram demonstradas. Os níveis de monóxido de carbono na fumaça do cigarro variam de 20,000 a 60,000 m210. O monóxido de carbono tem uma afinidade pela hemoglobina XNUMX vezes maior que a do oxigênio e, devido à menor tensão arterial de oxigênio, o feto fica especialmente comprometido. Outros sugeriram que esses efeitos não são devidos ao fumo, mas atribuíveis às características dos fumantes. Certamente ocupações com potencial exposição ao monóxido de carbono, como aquelas associadas a ul e aer, altos-fornos, acetileno, cervejarias, negro de fumo, fornos de coque, garagens, sintetizadores de produtos químicos orgânicos e refinarias de petróleo devem ser consideradas possíveis ocupações de alto risco para funcionárias grávidas.
O etanol também é um agente amplamente utilizado e pesquisado associado ao retardo do crescimento fetal (assim como a anomalias congênitas). Em um estudo prospectivo de 9,236 nascimentos, descobriu-se que o consumo materno de álcool de mais de 1.6 onças por dia estava associado a um aumento de natimortos e bebês com retardo de crescimento (Kaminski, Rumeau e Schwartz 1978). Menor comprimento infantil e circunferência da cabeça também estão relacionados à ingestão materna de álcool.
Ao avaliar os possíveis efeitos das exposições sobre o peso ao nascer, algumas questões problemáticas devem ser consideradas. o parto prematuro deve ser considerado como um possível resultado mediador e os efeitos potenciais na idade gestacional considerados. Além disso, gestações com maior duração gestacional também têm maior oportunidade de exposição. Se um número suficiente de mulheres trabalhar no final da gravidez, a exposição cumulativa mais longa pode estar associada às idades gestacionais mais antigas e aos bebês mais pesados puramente como um artefato. Há vários procedimentos que podem ser usados para superar esse problema, incluindo uma variante do modelo de regressão de tabela de vida de Cox, que tem a capacidade de lidar com covariáveis dependentes do tempo.
Outro problema centra-se em como definir baixo peso ao nascer. Muitas vezes os estudos definem o menor peso ao nascer como uma variável dicotômica, inferior a 2,500 g. A exposição, no entanto, deve ter um efeito muito poderoso para produzir uma queda drástica no peso da criança. O peso ao nascer definido como variável contínua e analisado em modelo de regressão múltipla é mais sensível para detectar efeitos sutis. A relativa escassez de achados significativos na literatura em relação a exposições ocupacionais e bebês PIG pode, na arte, ser causada por ignorar essas questões de projeto e análise.
Conclusões
Estudos de resultados adversos da gravidez devem caracterizar as exposições durante uma janela de tempo bastante estreita. Se a mulher foi transferida para outro emprego ou dispensada do trabalho durante um período crítico, como a organogênese, a relação exposição-efeito pode ser severamente alterada. Portanto, o investigador tem um alto padrão de identificação da exposição da mulher durante um pequeno período crítico de tempo em comparação com outros estudos de doenças crônicas, onde erros de alguns meses ou mesmo anos podem ter impacto mínimo.
Retardo do crescimento uterino, anomalia congênita e abortos espontâneos são frequentemente avaliados em estudos de exposição ocupacional. Há mais de uma abordagem disponível para avaliar cada resultado. Esses pontos finais são de importância para a saúde pública devido aos custos psicológicos e financeiros. Geralmente, observa-se falta de segurança nas relações exposição-resultado, por exemplo, com exposição a chumbo, gases anestésicos e solventes. Devido ao potencial de falta de segurança na relação exposição-efeito, estudos devem ser planejados para avaliar vários pontos finais associados a uma variedade de possíveis mecanismos.
Parto prematuro e trabalho
A conciliação entre trabalho e maternidade é uma importante questão de saúde pública nos países industrializados, onde mais de 50% das mulheres em idade reprodutiva trabalham fora de casa. Mulheres trabalhadoras, sindicatos, empregadores, políticos e médicos estão todos procurando maneiras de prevenir resultados reprodutivos desfavoráveis induzidos pelo trabalho. As mulheres querem continuar trabalhando durante a gravidez e podem até considerar o conselho de seu médico sobre modificações no estilo de vida durante a gravidez como superprotetor e desnecessariamente restritivo.
Consequências fisiológicas da gravidez
Neste ponto, seria útil rever algumas das consequências fisiológicas da gravidez que podem interferir no trabalho.
A mulher grávida sofre profundas alterações que lhe permitem adaptar-se às necessidades do feto. A maioria dessas mudanças envolve a modificação de funções fisiológicas que são sensíveis a mudanças de postura ou atividade física – o sistema circulatório, o sistema respiratório e o equilíbrio hídrico. Como resultado, gestantes fisicamente ativas podem apresentar reações fisiológicas e fisiopatológicas únicas.
As principais modificações fisiológicas, anatômicas e funcionais sofridas pelas mulheres grávidas são (Mamelle et al. 1982):
- Aumento da demanda periférica de oxigênio, levando à modificação dos sistemas respiratório e circulatório. O volume corrente começa a aumentar no terceiro mês e pode atingir 40% dos valores de re-gravidez no final da gravidez. O aumento resultante na troca gasosa pode aumentar o risco de inalação de voláteis tóxicos, enquanto a hiperventilação relacionada ao aumento do volume corrente pode causar falta de ar ao esforço.
- O débito cardíaco aumenta desde o início da gravidez, como resultado do aumento do volume sanguíneo. Isso reduz a capacidade de adaptação do coração ao esforço e também aumenta a pressão venosa nos membros inferiores, dificultando a permanência em pé por longos períodos.
- Modificações anatômicas durante a gravidez, incluindo exagero da lordose dorsolombar, alargamento do polígono de sustentação e aumento do volume abdominal, afetam as atividades estáticas.
- Uma variedade de outras modificações funcionais ocorre durante a gravidez. Náuseas e vômitos resultam em fadiga; a sonolência diurna resulta em desatenção; mudanças de humor e sentimentos de ansiedade podem levar a conflitos interpessoais.
- Finalmente, é interessante notar que as necessidades diárias de energia durante a gravidez são equivalentes às necessidades de duas a quatro horas de trabalho.
Devido a essas mudanças profundas, as exposições ocupacionais podem ter consequências especiais em mulheres grávidas e podem resultar em resultados desfavoráveis da gravidez.
Estudos epidemiológicos das condições de trabalho e parto prematuro
Embora existam muitos desfechos desfavoráveis da gravidez, revisamos aqui os dados sobre parto prematuro, definido como o nascimento de uma criança antes da 37ª semana de gestação. o parto prematuro está associado ao baixo peso ao nascer e a complicações significativas para o recém-nascido. Continua sendo uma grande preocupação de saúde pública e é uma reocupação contínua entre os obstetras.
Quando começamos a pesquisa neste campo em meados da década de 1980, havia uma proteção legislativa relativamente forte da saúde das mulheres grávidas na França, com a licença-maternidade pré-natal obrigatória para começar seis semanas antes da data prevista. Embora a taxa de parto prematuro tenha caído de 10 para 7% desde então, parece ter se estabilizado. Como a prevenção médica aparentemente atingiu o limite de seus poderes, investigamos os fatores de risco passíveis de intervenção social. Nossas hipóteses foram as seguintes:
- O trabalho per se é um fator de risco para o parto prematuro?
- Certas ocupações estão associadas a um risco aumentado de parto prematuro?
- Certas condições de trabalho constituem um perigo para a gestante e o feto?
- Existem medidas sociais preventivas que podem ajudar a reduzir o risco de parto prematuro?
Nosso primeiro estudo, realizado em 1977-78 em duas maternidades de hospital, examinou 3,400 mulheres, das quais 1,900 trabalharam durante a gravidez e 1,500 permaneceram em casa (Mamelle, Laumon e Lazar 1984). As mulheres foram entrevistadas imediatamente após o parto e solicitadas a descrever seu estilo de vida em casa e no trabalho durante a gravidez com a maior precisão possível.
Obtivemos os seguintes resultados:
Trabalho em si
O simples fato de trabalhar fora não pode ser considerado fator de risco para parto prematuro, pois as mulheres que ficaram em casa apresentaram taxa de prematuridade maior do que as mulheres que trabalhavam fora (7.2 versus 5.8%).
Condições de trabalho
Uma semana de trabalho excessivamente longa parece ser um fator de risco, pois houve aumento regular da taxa de parto prematuro com o número de horas de trabalho. Trabalhadores do setor de varejo, assistentes sociais médicos, trabalhadores especializados e pessoal de serviço estavam em maior risco de parto prematuro do que trabalhadores de escritório, professores, gerentes, trabalhadores qualificados ou supervisores. As taxas de prematuridade nos dois grupos foram de 8.3 e 3.8%, respectivamente.
Tabela 1. Fontes identificadas de fadiga ocupacional
| Índice de fadiga ocupacional | Índice “ALTO” se: |
| Postura | Ficar em pé por mais de 3 horas por dia |
| Trabalho em máquinas | Trabalho em correias transportadoras industriais; trabalho independente em máquinas industriais com esforço extenuante |
| Carga física | Esforço físico contínuo ou periódico; transportar cargas superiores a 10kg |
| carga mental | Trabalho de rotina; tarefas variadas que requerem pouca atenção sem estimulação |
| Meio Ambiente | Nível de ruído significativo; temperatura fria; atmosfera muito úmida; manuseio de substâncias químicas |
Fonte: Mamelle, Laumon e Lazar 1984.
A análise de tarefas permitiu a identificação de cinco fontes de fadiga ocupacional: postura, trabalho com máquinas industriais, carga física, carga mental e ambiente de trabalho. Cada uma dessas fontes de fadiga ocupacional constitui um fator de risco para parto prematuro (ver tabelas 1 e 2).
Tabela 2. Riscos relativos (RR) e índices de fadiga para parto prematuro
| Índice | Índice baixo % | índice alto % | RR | Significado estatístico |
| Postura | 4.5 | 7.2 | 1.6 | Significativo |
| Trabalho em máquinas | 5.6 | 8.8 | 1.6 | Significativo |
| Carga física | 4.1 | 7.5 | 1.8 | altamente significativo |
| carga mental | 4.0 | 7.8 | 2.0 | altamente significativo |
| Meio Ambiente | 4.9 | 9.4 | 1.9 | altamente significativo |
Fonte: Mamelle, Laumon e Lazar 1984.
A exposição a múltiplas fontes de fadiga pode resultar em resultados desfavoráveis da gravidez, conforme evidenciado pelo aumento significativo da taxa de parto prematuro com aumento do número de fontes de fadiga (tabela 3). Assim, 20% das mulheres tiveram exposição concomitante a pelo menos três fontes de fadiga e experimentaram uma taxa de parto prematuro duas vezes maior do que outras mulheres. Fadiga ocupacional e semanas de trabalho excessivamente longas exercem efeitos cumulativos, de modo que as mulheres que experimentam fadiga intensa durante longas semanas de trabalho apresentam uma taxa ainda maior de prematuridade. as taxas de parto prematuro aumentam ainda mais se a mulher também tiver um fator de risco médico. A detecção de fadiga ocupacional é, portanto, ainda mais importante do que a detecção de fatores de risco médicos.
Tabela 3. Risco relativo de prematuridade segundo número de índices de fadiga ocupacional
| número de alta índices de fadiga |
Proporção de mulheres expostas % |
Estimado risco relativo |
| 0 | 24 | 1.0 |
| 1 | 28 | 2.2 |
| 2 | 25 | 2.4 |
| 3 | 15 | 4.1 |
| 4-5 | 8 | 4.8 |
Fonte: Mamelle, Laumon e Lazar 1984
Estudos europeus e norte-americanos confirmaram nossos resultados, e nossa escala de fadiga tem se mostrado reprodutível em outras pesquisas e países.
Em um estudo de acompanhamento de caso-controle realizado na França alguns anos depois nas mesmas maternidades (Mamelle e Munoz 1987), apenas dois dos cinco índices de fadiga previamente definidos foram significativamente relacionados ao parto prematuro. Refira-se, no entanto, que as mulheres tiveram maior oportunidade de se sentar e foram afastadas de tarefas fisicamente exigentes em resultado das medidas preventivas implementadas nos locais de trabalho durante este período. A escala de fadiga, no entanto, permaneceu um preditor de parto prematuro neste segundo estudo.
Em um estudo em Montreal, Quebec (McDonald et al. 1988), 22,000 mulheres grávidas foram entrevistadas retrospectivamente sobre suas condições de trabalho. Longas semanas de trabalho, trabalho em turnos alternados e carregamento de cargas pesadas demonstraram exercer efeitos significativos. Os outros fatores estudados não parecem estar relacionados ao parto prematuro, embora pareça haver uma associação significativa entre parto prematuro e uma escala de fadiga baseada no número total de fontes de fadiga.
Com exceção do trabalho com máquinas industriais, nenhuma associação significativa entre condições de trabalho e parto prematuro foi encontrada em um estudo retrospectivo francês de uma amostra representativa de 5,000 mulheres grávidas (Saurel-Cubizolles e Kaminski 1987). No entanto, uma escala de fadiga inspirada na nossa foi significativamente associada ao parto prematuro.
Nos Estados Unidos, Homer, Beredford e James (1990), em estudo de coorte histórica, confirmaram a associação entre carga de trabalho físico e risco aumentado de parto prematuro. Teitelman e colaboradores (1990), em estudo prospectivo com 1,200 gestantes, cujo trabalho foi classificado como sedentário, ativo ou em pé, com base na descrição do trabalho, demonstraram associação entre trabalho em pé e parto prematuro.
Barbara Luke e colaboradores (no prelo) conduziram um estudo retrospectivo de enfermeiras americanas que trabalharam durante a gravidez. Utilizando nossa escala de risco ocupacional, ela obteve resultados semelhantes aos nossos, ou seja, associação entre parto prematuro e longas semanas de trabalho, trabalho em pé, carga de trabalho pesada e ambiente de trabalho desfavorável. Além disso, o risco de parto prematuro foi significativamente maior entre as mulheres com exposição concomitante a três ou quatro fontes de fadiga. Deve-se notar que este estudo incluiu mais da metade de todas as enfermeiras nos Estados Unidos.
No entanto, resultados contraditórios foram relatados. Isso pode ser devido a pequenos tamanhos de amostra (Berkowitz 1981), diferentes definições de prematuramente (Launer et al. 1990) e classificação das condições de trabalho com base na descrição do trabalho em vez da análise real da estação de trabalho (Klebanoff, Shiono e Carey 1990). Em alguns casos, as estações de trabalho foram caracterizadas apenas em bases teóricas – pelo médico do trabalho, por exemplo, e não pelas próprias mulheres (peoples-Shes et al. 1991). Sentimos que é importante levar em consideração a fadiga subjetiva – ou seja, a fadiga como é descrita e experimentada pelas mulheres – nos estudos.
Por fim, é possível que os resultados negativos estejam relacionados à implementação de medidas preventivas. Este foi o caso do estudo prospectivo de Ahlborg, Bodin e Hogstedt (1990), no qual 3,900 mulheres suecas ativas preencheram um questionário autoaplicável em sua primeira consulta pré-natal. O único fator de risco relatado para parto prematuro foi carregar cargas com peso superior a 12 kg mais de 50 vezes por semana, e mesmo assim o risco relativo de 1.7 não foi significativo. O próprio Ahlborg aponta que medidas preventivas na forma de licença-maternidade de auxílio e o direito de realizar um trabalho menos cansativo durante os dois meses anteriores à data de vencimento foram implementadas para mulheres grávidas em trabalhos cansativos. As licenças-maternidade foram cinco vezes mais frequentes entre as mulheres que descreveram seu trabalho como cansativo e que envolvia o transporte de cargas pesadas. Ahlborg conclui que o risco de parto prematuro pode ter sido minimizado por essas medidas preventivas.
Intervenções preventivas: exemplos franceses
Os resultados dos estudos etiológicos são convincentes o suficiente para que intervenções preventivas sejam aplicadas e avaliadas? A primeira questão que deve ser respondida é se existe uma justificativa de saúde pública para a aplicação de medidas preventivas sociais destinadas a reduzir a taxa de parto prematuro.
Usando dados de nossos estudos anteriores, estimamos a proporção de partos prematuros causados por fatores ocupacionais. Assumindo uma taxa de parto prematuro de 10% em populações expostas a fadiga intensa e uma taxa de 4.5% em populações não expostas, estimamos que 21% dos partos prematuros são causados por fatores ocupacionais. Reduzir a fadiga ocupacional poderia, portanto, resultar na eliminação de um quinto de todos os nascimentos prematuros em mulheres trabalhadoras francesas. Esta é uma ampla justificativa para a implementação de medidas sociais preventivas.
Que medidas preventivas podem ser aplicadas? Os resultados de todos os estudos levam à conclusão de que a jornada de trabalho pode ser reduzida, a fadiga pode ser diminuída por meio da modificação do posto de trabalho, as pausas de trabalho podem ser permitidas e a licença pré-natal pode ser prolongada. Três alternativas de custo equivalente estão disponíveis:
- redução da jornada de trabalho para 30 horas a partir da 20ª semana de gestação
- prescrever uma pausa no trabalho de uma semana por mês a partir da 20ª semana de gestação
- início da licença pré-natal na 28ª semana de gestação.
É relevante lembrar aqui que a legislação francesa prevê as seguintes medidas preventivas para mulheres grávidas:
- emprego garantido após o parto
- redução da jornada de trabalho em 30 a 60 minutos, aplicada por meio de convenções coletivas
- modificação da estação de trabalho em casos de incompatibilidade com a gravidez
- pausas de trabalho durante a gravidez, prescritas pelos médicos assistentes
- licença maternidade pré-natal seis semanas antes da data prevista, com mais duas semanas disponíveis em caso de complicações
- licença de maternidade pós-natal de dez semanas.
Um estudo observacional prospectivo de um ano com 23,000 mulheres empregadas em 50 empresas na região de Rhône-Ales, na França (Bertucat, Mamelle e Munoz, 1987), examinou o efeito de condições de trabalho cansativas no parto prematuro. Durante o período do estudo, 1,150 bebês nasceram na população estudada. Analisamos as modificações das condições de trabalho para acomodar a gravidez e a relação dessas modificações com o parto prematuro (Mamelle, Bertucat e Munoz 1989), e observamos que:
- A modificação da estação de trabalho foi reformada para apenas 8% das mulheres.
- 33% das mulheres cumpriram o seu turno normal, tendo as restantes reduzido a jornada de trabalho de 30 a 60 minutos.
- 50% das mulheres tiveram pelo menos uma folga no trabalho, além da licença pré-natal; fadiga foi a causa em um terço dos casos.
- 90% das mulheres pararam de trabalhar antes do início da licença legal de maternidade e obtiveram pelo menos as duas semanas de licença permitidas em caso de complicações na gravidez; a fadiga foi a causa em metade dos casos.
- Ao todo, dado o período legal de licença pré-natal de seis semanas antes do vencimento (com duas semanas adicionais disponíveis em alguns casos), a duração real da licença pré-natal foi de 12 semanas nessa população de mulheres sujeitas a condições de trabalho cansativas.
Essas modificações de trabalho têm algum efeito sobre o resultado da gravidez? A modificação do posto de trabalho e a redução discreta da jornada de trabalho (30 a 60 min) foram associadas a reduções não significativas do risco de parto prematuro. Acreditamos que novas reduções da semana de trabalho teriam um efeito maior (tabela 4).
Tabela 4. Riscos relativos de prematuridade associados a modificações nas condições de trabalho
| modificações trabalhando condições |
Número de mulheres | Prematuro taxas de nascimento (%) |
Risco relativo (intervalos de confiança de 95%) |
| Mudança na situação de trabalho | |||
| Não Sim |
1,062 87 |
6.2 3.4 |
0.5 (0.2-1.6) |
| Redução da jornada de trabalho semanal | |||
| Não Sim |
388 761 |
7.7 5.1 |
0.7 (0.4-1.1) |
| Episódios de licença médica1 | |||
| Não Sim |
357 421 |
8.0 3.1 |
0.4 (0.2-0.7) |
| Aumento da licença maternidade pré-natal1 | |||
| Nenhum ou apenas 2 semanas adicionais Sim |
487 291 |
4.3 7.2 |
1.7 (0.9-3.0) |
1 Em uma amostra reduzida de 778 mulheres sem patologia obstétrica anterior ou atual.
Fonte: Mamelle, Bertucat e Munoz 1989.
Para analisar a relação entre licença pré-natal, folgas e parto prematuro, é necessário discriminar entre folgas preventivas e curativas. Isso requer a restrição da análise a mulheres com gestações sem complicações. Nossa análise desse subgrupo revelou uma redução da taxa de parto prematuro entre as mulheres que fizeram pausas no trabalho durante a gravidez, mas não naquelas que tiveram licença pré-natal prolongada (Tabela 9).
Este estudo observacional demonstrou que as mulheres que trabalham em condições cansativas fazem mais pausas durante a gravidez do que as outras mulheres, e que essas pausas, principalmente quando motivadas por fadiga intensa, estão associadas à redução do risco de parto prematuro (Mamelle, Bertucat e Muñoz 1989).
Escolha de estratégias preventivas na França
Como epidemiologistas, gostaríamos de ver essas observações verificadas por estudos preventivos experimentais. Devemos, no entanto, nos perguntar o que é mais razoável: esperar por tais estudos ou recomendar medidas sociais para prevenir o parto prematuro agora?
O Governo francês decidiu recentemente incluir um “guia de trabalho e gravidez”, idêntico à nossa escala de fadiga, no registo médico de cada grávida. As mulheres podem, assim, calcular sua pontuação de fadiga por si mesmas. Se as condições de trabalho forem árduas, podem solicitar ao médico do trabalho ou ao responsável pela segurança do trabalho de sua empresa que implementem modificações visando aliviar sua carga de trabalho. Em caso de recusa, podem solicitar ao seu médico assistente que lhe prescreva semanas de repouso durante a gravidez, podendo mesmo prolongar a licença de maternidade pré-natal.
O desafio agora é identificar estratégias preventivas bem adaptadas à legislação e às condições sociais de cada país. Isso requer uma abordagem de economia da saúde para a avaliação e comparação de estratégias preventivas. Antes que qualquer medida preventiva possa ser considerada de aplicação geral, muitos fatores devem ser levados em consideração. Isso inclui eficácia, é claro, mas também baixo custo para o sistema de seguridade social, criação de empregos resultante, referências para mulheres e aceitação por empregadores e sindicatos.
Esse tipo de problema pode ser resolvido usando métodos multicritério, como o método Electra. Esses métodos permitem tanto a classificação de estratégias preventivas com base em cada uma de uma série de critérios quanto a ponderação dos critérios com base em considerações políticas. Desta forma, pode ser dada especial importância ao baixo custo para o sistema de segurança social ou à capacidade de escolha das mulheres, por exemplo (Mamelle et al. 1986). Embora as estratégias recomendadas por esses métodos variem de acordo com os tomadores de decisão e as opções políticas, a eficácia é sempre mantida do ponto de vista da saúde pública.
Exposições ocupacionais e ambientais ao recém-nascido
Perigos ambientais representam um risco especial para bebês e crianças pequenas. As crianças não são “pequenos adultos”, seja na forma como absorvem e eliminam os produtos químicos ou na sua resposta a exposições tóxicas. As exposições neonatais podem ter um impacto maior porque a área de superfície corporal é desproporcionalmente grande e a capacidade metabólica (ou a capacidade de eliminar substâncias químicas) é relativamente subdesenvolvida. Ao mesmo tempo, os potenciais efeitos tóxicos são maiores, porque o cérebro, os pulmões e o sistema imunológico ainda estão em desenvolvimento durante os primeiros anos de vida.
Existem oportunidades de exposição em casa, em creches e playgrounds:
- As crianças pequenas podem absorver agentes ambientais do ar (por inalação) ou através da pele.
- A ingestão é uma das principais vias de exposição, especialmente quando as crianças começam a exibir a atividade mão-boca.
- Substâncias no cabelo, roupas ou mãos dos pais podem ser transferidas para a criança.
- O leite materno é outra fonte potencial de exposição para bebês, embora os benefícios potenciais da amamentação superem em muito os efeitos tóxicos potenciais dos produtos químicos no leite materno.
Para uma série de efeitos na saúde discutidos em relação às exposições neonatais, é difícil distinguir eventos pré-natais de eventos pós-natais. As exposições que ocorrem antes do nascimento (através da placenta) podem continuar a se manifestar na primeira infância. Tanto a fumaça de chumbo quanto a fumaça ambiental do tabaco foram associadas a déficits no desenvolvimento cognitivo e na função pulmonar antes e depois do nascimento. Nesta revisão, tentamos focar nas exposições pós-natais e seus efeitos na saúde de crianças muito pequenas.
Chumbo e outros metais pesados
Entre os metais pesados, o chumbo (b) é o elemento de exposição mais importante para os seres humanos, tanto em circunstâncias ambientais quanto ocupacionais. Exposições ocupacionais significativas ocorrem na fabricação de baterias, fundições, soldagem, soldagem, construção e remoção de tinta. pais empregados nessas indústrias há muito são conhecidos por trazer poeira para casa em suas roupas que podem ser absorvidas por seus filhos. A principal via de absorção pelas crianças é através da ingestão de lascas de tinta contaminadas com chumbo, poeira e água. A absorção respiratória é eficiente e a inalação torna-se uma via de exposição significativa se um aerossol de chumbo ou chumbo de alquila for reenviado (Clement International Corporation 1991).
O envenenamento por chumbo pode danificar praticamente todos os sistemas de órgãos, mas os níveis atuais de exposição têm sido associados principalmente a alterações neurológicas e de desenvolvimento em crianças. Além disso, doenças renais e hematológicas foram observadas entre adultos e crianças intensamente expostas ao chumbo. Doenças cardiovasculares e disfunções reprodutivas são sequelas conhecidas da exposição ao chumbo entre adultos. Suspeita-se que efeitos renais, cardiovasculares e reprodutivos subclínicos surjam de uma exposição menor e crônica ao chumbo, e dados limitados apóiam essa ideia. Dados de animais dão suporte a achados humanos (Sager e Girard 1994).
Em termos de dose mensurável, os efeitos neurológicos variam de déficits de QI em baixas exposições (chumbo no sangue = 10 μg/dl) a encefalopatia repulsiva (80 μg/dl). Os níveis preocupantes em crianças em 1985 eram de 25 μg/dl, que foram reduzidos para 10 μg/dl em 1993.
A exposição neonatal, por resultar da poeira trazida para casa pelos pais que trabalham, foi descrita como “sujar o ninho” por Chisholm em 1978. Desde então, medidas preventivas, como tomar banho e trocar de roupa antes de deixar o local de trabalho, reduziram carga de poeira doméstica. No entanto, o chumbo de origem ocupacional ainda é uma importante fonte potencial de exposição neonatal hoje. Uma pesquisa com crianças na Dinamarca descobriu que o chumbo no sangue era aproximadamente duas vezes maior entre os filhos de trabalhadores expostos do que em lares com apenas exposições não ocupacionais (Grandjean e Bach 1986). A exposição de crianças ao chumbo de origem ocupacional foi documentada entre emendadores de cabos elétricos (Rinehart e Yanagisawa 1993) e trabalhadores da fabricação de capacitores (Kaye, Novotny e Tucker 1987).
Fontes não ocupacionais de exposição ambiental ao chumbo continuam a ser um sério perigo para crianças pequenas. Desde a proibição gradual do chumbo tetraetila como aditivo de combustível nos Estados Unidos (em 1978), os níveis médios de chumbo no sangue em crianças diminuíram de 13 para 3 μg/dl (Pirkle et al. 1994). lascas de tinta e pó de tinta são agora a principal causa de intoxicação infantil por chumbo nos Estados Unidos (Roer 1991). Por exemplo, em um relatório, crianças mais novas (recém-nascidos com menos de 11 meses) com excesso de chumbo no sangue corriam maior risco de exposição por meio de poeira e água, enquanto crianças mais velhas (com 24 meses de idade) corriam mais risco de ingestão de lascas de tinta ( ica) (Shannon e Graef 1992). A redução do chumbo por meio da remoção de tinta tem sido bem-sucedida em proteger as crianças da exposição à poeira e lascas de tinta (Farfel, Chisholm e Rohde, 1994). Ironicamente, os trabalhadores envolvidos nesta empresa carregam poeira de chumbo em suas roupas para casa. Além disso, observou-se que a exposição contínua de crianças pequenas ao chumbo afeta desproporcionalmente crianças economicamente desfavorecidas (Brody et al. 1994; Goldman e Carra 1994). A arte dessa iniquidade decorre das más condições das moradias; já em 1982, foi demonstrado que a extensão da deterioração da habitação estava diretamente relacionada aos níveis de chumbo no sangue em crianças (Clement International Corporation 1991).
Outra fonte potencial de exposição ocupacional para o recém-nascido é o chumbo no leite materno. Níveis mais altos de chumbo no leite materno têm sido associados a fontes ocupacionais e ambientais (Ryu, Ziegler e Fomon 1978; Dabeka et al. 1986). As concentrações de chumbo no leite são pequenas em relação ao sangue (aproximadamente 1/5 a 1/2) (Wolff 1993), mas o grande volume de leite materno ingerido por uma criança pode adicionar quantidades de miligramas à carga corporal. Em comparação, há normalmente menos de 0.03 mg b no sangue circulante de uma criança e a ingestão usual é inferior a 20 mg por dia (Clement International Corporation 1991). De fato, a absorção do leite materno se reflete no nível de chumbo no sangue dos bebês (Rabinowitz, Leviton e Needleman 1985; Ryu et al. 1983; Ziegler et al. 1978). Deve-se notar que os níveis normais de chumbo no leite materno não são excessivos, e a lactação contribui com uma quantidade semelhante à de outras fontes de nutrição infantil. Em comparação, um pequeno chi de tinta pode conter mais de 10 mg (10,000 mg) de chumbo.
Decréscimos no desenvolvimento de crianças têm sido associados a exposições pré-natais e pós-natais ao chumbo. Acredita-se que a exposição pré-natal seja responsável por déficits relacionados ao chumbo no desenvolvimento mental e comportamental que foram encontrados em crianças até a idade de dois a quatro anos (Landrigan e Cambell 1991; Bellinger et al. 1987). Os efeitos da exposição pós-natal ao chumbo, como a experimentada pelo recém-nascido de fontes ocupacionais, podem ser detectados em crianças de dois a seis anos e até mais tarde. Entre eles estão o comportamento problemático e a inteligência inferior (Bellinger et al. 1994). Esses efeitos não se limitam apenas a altas exposições; eles foram observados em níveis relativamente baixos, por exemplo, onde os níveis de chumbo no sangue estão na faixa de 10 mg/dl (Needleman e Bellinger 1984).
A exposição ao mercúrio (Hg) do ambiente pode ocorrer nas formas inorgânica e orgânica (principalmente metil). Exposições ocupacionais recentes ao mercúrio foram encontradas entre trabalhadores na fabricação de termômetros e no reparo de equipamentos de alta tensão contendo mercúrio. Outras ocupações com exposição potencial incluem pintura, odontologia, encanamento e fabricação de cloro (Agency for Toxic Substance and Disease Registry 1992).
A intoxicação pré-natal e pós-natal por mercúrio foi bem documentada entre crianças. As crianças são mais suscetíveis aos efeitos do metilmercúrio do que os adultos. Isso ocorre principalmente porque o sistema nervoso central humano em desenvolvimento é tão “notavelmente sensível” ao metilmercúrio, um efeito também observado em níveis baixos em animais (Clarkson, Nordberg e Sager 1985). As exposições ao metilmercúrio em crianças surgem principalmente da ingestão de peixe contaminado ou do leite materno, enquanto o mercúrio elementar é derivado de exposições ocupacionais. A exposição doméstica incidental à exposição ocupacional foi observada (Zirschky e Wetherell 1987). Exposições acidentais em casa foram relatadas nos últimos anos em indústrias domésticas (Meeks, Keith e Tanner 1990; Rowens et al. 1991) e em soleiras acidentais de mercúrio metálico (Florentine e Sanfilio 1991). A exposição ao mercúrio elementar ocorre principalmente por inalação, enquanto o alquil mercúrio pode ser absorvido por ingestão, inalação ou contato dérmico.
No episódio de envenenamento mais bem estudado, disfunção sensorial e motora e retardo mental foram encontrados após exposições muito altas ao metilmercúrio ou in utero ou do leite materno (Bakir et al. 1973). As exposições maternas resultaram da ingestão de metilmercúrio que havia sido usado como fungicida em grãos.
pesticidas e produtos químicos relacionados
Várias centenas de milhões de toneladas de pesticidas são produzidas em todo o mundo a cada ano. Herbicidas, fungicidas e inseticidas são empregados principalmente na agricultura por países desenvolvidos para melhorar o rendimento e a qualidade das culturas. Os conservantes de madeira são uma arte muito menor, mas ainda importante, do mercado. O uso doméstico e no jardim representa uma proporção relativamente menor do consumo total, mas do ponto de vista da toxicidade neonatal, as intoxicações domésticas são talvez as mais numerosas. A exposição ocupacional também é uma fonte potencial de exposição indireta para bebês se um dos pais estiver envolvido em trabalho que usa pesticidas. A exposição a pesticidas é possível através da absorção dérmica, inalação e ingestão. Mais de 50 pesticidas foram declarados cancerígenos em animais (McConnell 1986).
Pesticidas organoclorados incluem compostos aromáticos, como DDT (bis(4-clorohenil)-1,1,1-tricloroetano) e ciclodienos, como dieldrin. O DDT começou a ser usado no início da década de 1940 como um meio eficaz para eliminar os mosquitos transmissores da malária, uma aplicação que ainda hoje é amplamente empregada nos países em desenvolvimento. O lindano é um organoclorado amplamente utilizado no controle de piolhos do corpo e na agricultura, especialmente em países em desenvolvimento. os bihenilos oliclorados (CBs), outra mistura de organoclorados solúveis em gordura usada desde a década de 1940, representam um risco potencial à saúde de crianças pequenas expostas através do leite materno e outros alimentos contaminados. Tanto o lindano quanto os CBs são discutidos separadamente neste capítulo. bihenilos olibromados (BBs) também foram detectados no leite materno, quase exclusivamente em Michigan. Aqui, um retardador de fogo inadvertidamente misturado na alimentação do gado em 1973-74 tornou-se amplamente disperso por todo o estado por meio de laticínios e produtos à base de carne.
O clordano tem sido usado como pesticida e como termiticida em residências, onde é eficaz há décadas, sem dúvida por causa de sua persistência. A exposição a este produto químico pode ser proveniente da ingestão alimentar e respiratória direta ou dérmica. Os níveis no leite humano no Japão podem estar relacionados tanto à dieta quanto à forma como as casas foram tratadas recentemente. As mulheres que viviam em casas tratadas há mais de dois anos tinham níveis de clordano no leite três vezes maiores do que as mulheres que viviam em casas não tratadas (Taguchi e Yakushiji 1988).
A dieta é a principal fonte de organoclorados persistentes, mas fumar, ar e água também podem contribuir para a exposição. Essa classe de pesticidas, também denominada de hidrocarbonetos halogenados, é bastante persistente no meio ambiente, pois são lipofílicos, resistentes ao metabolismo ou à biodegradação e apresentam baixa volatilidade. Várias centenas de m foram encontradas na gordura humana e animal entre aqueles com maior exposição. Por causa de sua toxicidade reprodutiva na vida selvagem e sua tendência à bioacumulação, os organoclorados foram amplamente proibidos ou restritos em países desenvolvidos.
Em doses muito altas, a neurotoxicidade foi observada com organoclorados, mas os efeitos potenciais à saúde a longo prazo são mais preocupantes entre os seres humanos. Embora os efeitos crônicos na saúde não tenham sido amplamente documentados, calortoxicidade, câncer e disfunção reprodutiva foram encontrados em animais experimentais e na vida selvagem. As preocupações com a saúde surgem principalmente de observações em estudos com animais sobre carcinogênese e profundas alterações no fígado e no sistema imunológico.
Organohoshates e carbamatos são menos persistentes do que os organoclorados e são a classe de inseticidas mais amplamente utilizada internacionalmente. pesticidas desta classe são degradados de forma relativamente rápida no ambiente e no corpo. Alguns dos organohoshatos e carbamatos exibem alta neurotoxicidade aguda e, em certos casos, neurotoxicidade crônica também. A dermatite também é um sintoma amplamente relatado de exposição a pesticidas.
Os produtos à base de petróleo usados para aplicar alguns pesticidas também são uma preocupação potencial. Efeitos crônicos, incluindo cânceres hematológicos e outros cânceres infantis, foram associados a exposições familiares ou residenciais a pesticidas, mas os dados epidemiológicos são bastante limitados. No entanto, com base nos dados de estudos com animais, a exposição a pesticidas deve ser evitada.
Para o recém-nascido, um amplo espectro de possibilidades de exposição e efeitos tóxicos foi relatado. Entre as crianças que necessitaram de hospitalização por envenenamento agudo, a maioria ingeriu inadvertidamente produtos pesticidas, enquanto um número significativo foi exposto enquanto se deitava em carets pulverizados (Casey, Thomson e Vale 1994; Zwiener e Ginsburg 1988). A contaminação das roupas dos trabalhadores por pó ou líquido de pesticidas é reconhecida há muito tempo. Portanto, esta rota oferece ampla oportunidade para exposições domésticas, a menos que os trabalhadores tomem as devidas precauções de higiene após o trabalho. Por exemplo, uma família inteira tinha níveis elevados de clordecona (Keone) no sangue, atribuídos à lavagem doméstica das roupas de um trabalhador (Grandjean e Bach 1986). A exposição domiciliar ao TCDD (dioxina) foi documentada pela ocorrência de cloracne no filho e na esposa de dois trabalhadores expostos após uma explosão (Jensen, Sneddon e Walker 1972).
A maioria das possíveis exposições a bebês decorre de aplicações de pesticidas dentro e fora de casa (Lewis, Fortmann e Camann 1994). A poeira nos cuidados domésticos foi amplamente contaminada com vários pesticidas (Fenske et al. 1994). Grande parte da contaminação doméstica relatada foi atribuída ao extermínio de pulgas ou à aplicação de pesticidas em gramados e jardins (Davis, Bronson e Garcia, 1992). Prevê-se que a absorção infantil de cloririfós após o tratamento de pulgas em casa exceda os níveis seguros. De fato, os níveis do ar interno após tais procedimentos de fumigação nem sempre diminuem rapidamente para níveis seguros.
O leite materno é uma fonte potencial de exposição a pesticidas para o recém-nascido. A contaminação do leite humano com agrotóxicos, principalmente os organoclorados, é conhecida há décadas. Exposições ocupacionais e ambientais podem levar à contaminação significativa do leite materno por pesticidas (D'Ercole et al. 1976; McConnell 1986). Os organoclorados, que no passado eram reenviados para o leite materno em níveis excessivos, estão diminuindo nos países desenvolvidos, paralelamente ao declínio nas concentrações adiposas que ocorreu após a restrição desses compostos. Portanto, a contaminação do leite humano por DDT é agora mais alta nos países em desenvolvimento. Há pouca evidência de organohoshatos no leite materno. Isso pode ser atribuído às propriedades de solubilidade em água e ao metabolismo desses compostos no corpo.
A ingestão de água contaminada com pesticidas também é um risco potencial à saúde do recém-nascido. Este problema é mais resolvido onde a fórmula infantil deve ser criada usando água. Caso contrário, as fórmulas infantis comerciais são relativamente livres de contaminantes (National Research Council 1993). A contaminação dos alimentos com pesticidas também pode levar à exposição infantil. A contaminação de leite comercial, frutas e vegetais com pesticidas existe em níveis muito baixos, mesmo em países desenvolvidos, onde a regulamentação e o monitoramento são mais vigorosos (The Referee 1994). Embora o leite constitua a maior parte da dieta infantil, frutas (especialmente cervejas) e vegetais (especialmente cenouras) também são consumidos em quantidade significativa por crianças pequenas e, portanto, representam uma possível fonte de exposição a pesticidas.
Nos países industrializados, incluindo os Estados Unidos e a Europa Ocidental, a maioria dos pesticidas organoclorados, incluindo DDT, clordano, dieldrin e lindano, foram banidos, suspensos ou restritos desde a década de 1970 (Maxcy Rosenau-Last 1994). pesticidas ainda usados para fins agrícolas e não agrícolas são regulamentados em termos de seus níveis em alimentos, água e produtos farmacêuticos. Como resultado dessa regulamentação, os níveis de pesticidas no tecido adiposo e no leite humano diminuíram significativamente nas últimas quatro décadas. No entanto, os organoclorados ainda são amplamente utilizados nos países em desenvolvimento, onde, por exemplo, o lindano e o DDT estão entre os pesticidas mais usados na agricultura e no controle da malária (Awumbila e Bokuma 1994).
Lindano
O lindano é o isômero γ e ingrediente ativo do grau técnico do hexacloreto de benzeno (BHC). O BHC, também conhecido como hexaclorociclohexano (HCH), contém 40 a 90% de outros isômeros - α, β e δ. Este organoclorado tem sido usado como pesticida agrícola e não agrícola em todo o mundo desde 1949. Exposições ocupacionais podem ocorrer durante a fabricação, formulação e aplicação do BHC. O lindano como reparador farmacêutico em cremes, loções e xampus também é amplamente utilizado para tratar sarna e piolhos. Como essas condições de pele ocorrem comumente entre bebês e crianças, o tratamento médico pode levar à absorção de BHC por bebês através da pele. A exposição neonatal também pode ocorrer por inalação de vapor ou poeira que pode ser trazida para casa pelos pais ou que pode persistir após o uso doméstico. A ingestão dietética também é um possível meio de exposição a lactentes, uma vez que o BHC foi detectado no leite humano, laticínios e outros alimentos, assim como muitos inseticidas organoclorados. A exposição através do leite materno era mais prevalente nos Estados Unidos antes da proibição da produção comercial de lindano. De acordo com a IARC (International Agency for Research on Cancer 1987), é possível que o hexaclorociclohexano seja carcinogênico para humanos. No entanto, evidências de resultados adversos à saúde entre bebês foram relatadas principalmente como efeitos nos sistemas neurológico e hematológico.
A exposição domiciliar ao lindano foi descrita na esposa de um formulador de pesticidas, demonstrando o potencial para exposições neonatais semelhantes. A esposa tinha 5 ng/ml de γ-BHC em seu sangue, uma concentração menor que a de seu marido (tabela 1) (Starr et al. 1974). presumivelmente, γ-BHC foi trazido para casa no corpo e/ou roupas do trabalhador. Os níveis de γ-BHC na mulher e em seu marido foram maiores do que os relatados em crianças tratadas com loção contendo 0.3 a 1.0% de BHC.
O BHC no leite materno existe principalmente como o isômero β (Smith 1991). A meia-vida do isômero γ no corpo humano é de aproximadamente um dia, enquanto o isômero β se acumula.
Tabela 1. Fontes potenciais e níveis de exposição aos recém-nascidos
| Fonte de exposição | g-BHC no sangue (ng/ml; ppb) |
|
| Exposições ocupacionais | Baixas exposições Altas exposições |
5 36 |
| Homem adulto | Tentativa de suicídio | 1300 |
| Criança | Envenenamento agudo | 100-800 |
| Crianças | 1% loção BHC (média) | 13 |
| Relato de caso de exposição domiciliar1 | Marido Esposa |
17 5 |
| Populações não expostas desde 1980 | Jugoslávia África Brazil Índia |
52 72 92 752 |
1Starr et ai. (1974); outros dados de Smith (1991).
2Principalmente b-isômero.
A absorção dérmica do lindano de produtos farmacêuticos é uma função da quantidade aplicada na pele e da duração da exposição. Em comparação com adultos, bebês e crianças pequenas parecem ser mais suscetíveis aos efeitos tóxicos do lindano (Clement International Corporation 1992). Uma razão pode ser que a absorção dérmica é aumentada pelo aumento da permeabilidade da pele do bebê e uma grande relação superfície-volume. Os níveis no recém-nascido podem persistir por mais tempo porque o metabolismo do BHC é menos eficiente em lactentes e crianças pequenas. Além disso, a exposição em recém-nascidos pode ser aumentada ao lamber ou morder as áreas tratadas (Kramer et al. 1990). Um duche ou banho quente antes da aplicação dérmica de produtos médicos pode facilitar a absorção dérmica, exacerbando assim a toxicidade.
Em vários casos relatados de envenenamento acidental por lindano, foram descritos efeitos tóxicos evidentes, alguns em crianças pequenas. Em um caso, um bebê de dois meses morreu após múltiplas exposições a 1% de loção de lindano, incluindo uma aplicação de corpo inteiro após um banho quente (Davies et al. 1983).
A produção e o uso de lindano são restritos na maioria dos países desenvolvidos. O lindano ainda é amplamente utilizado em outros países para fins agrícolas, conforme observado em um estudo sobre o uso de pesticidas em fazendas em Gana, onde o lindano representou 35 e 85% do uso de pesticidas para agricultores e pastores, respectivamente (Awumbila e Bokuma 1994).
bienilos oliclorados
os bihenilos oliclorados foram usados desde meados da década de 1940 até o final da década de 1970 como fluidos isolantes em capacitores e transformadores elétricos. Os resíduos ainda são reenviados ao meio ambiente por causa da poluição, que se deve em grande parte ao descarte inadequado ou soleiras acidentais. Alguns equipamentos ainda em uso ou armazenados continuam sendo uma fonte potencial de contaminação. Foi relatado um incidente no qual crianças apresentaram níveis detectáveis de CBs no sangue após exposição enquanto deitavam com capacitores (Wolff e Schecter 1991). A exposição na esposa de um trabalhador exposto também foi relatada (Fishbein e Wolff 1987).
Em dois estudos de exposições ambientais, a exposição re e pós-natal a CBs foi associada a efeitos pequenos, mas significativos, em crianças. Em um estudo, o desenvolvimento motor ligeiramente prejudicado foi detectado entre crianças cujas mães tiveram níveis de CB no leite materno pós-natal imediato no percentil 95 superior do grupo de estudo (Rogan et al. 1986). No outro, déficits sensoriais (assim como tamanho gestacional menor) foram observados entre crianças com níveis sanguíneos de aproximadamente 25% (Jacobson et al. 1985; Fein et al. 1984). Esses níveis de exposição estavam na faixa superior para os estudos (acima de 3 m no leite materno (base de gordura) e acima de 3 ng/ml no sangue de crianças), mas não são excessivamente altos. Exposições ocupacionais comuns resultam em níveis dez a 100 vezes maiores (Wolff 1985). Em ambos os estudos, os efeitos foram atribuídos à exposição pré-natal. Tais resultados, no entanto, soam como uma nota de advertência para a exposição indevida de recém-nascidos a tais produtos químicos, tanto no pré quanto no pós-natal.
solventes
Solventes são um grupo de líquidos voláteis ou semivoláteis que são usados principalmente para dissolver outras substâncias. A exposição a solventes pode ocorrer em processos de fabricação, por exemplo, exposição a hexano durante a destilação de produtos petrolíferos. Para a maioria das pessoas, as exposições a solventes ocorrerão enquanto eles estiverem sendo usados no trabalho ou em casa. Aplicações industriais comuns incluem limpeza a seco, desengorduramento, pintura e remoção de tinta e impressão. Dentro de casa, é possível o contato direto com solventes durante o uso de produtos como limpadores de metal, produtos de limpeza a seco, diluentes ou sprays.
As principais vias de exposição de solventes em adultos e crianças são através da absorção respiratória e dérmica. A ingestão de leite materno é um meio de exposição neonatal a solventes derivados do trabalho dos pais. Devido à curta meia-vida da maioria dos solventes, sua duração no leite materno será igualmente curta. No entanto, após a exposição materna, alguns solventes serão retransmitidos para o leite materno, pelo menos por um curto período de tempo (pelo menos uma meia-vida). Os solventes que foram detectados no leite materno incluem tetracloroetileno, dissulfeto de carbono e halotano (um anestésico). Uma revisão detalhada da potencial exposição infantil ao tetracloroetileno (TCE) concluiu que os níveis no leite materno podem facilmente exceder as diretrizes de risco à saúde recomendadas (Schreiber 1993). O risco excessivo foi maior para bebês cujas mães podem estar expostas no local de trabalho (58 a 600 por milhão de pessoas). Para as exposições não ocupacionais mais altas, foram estimados riscos de excesso de 36 a 220 por 10 milhões de pessoas; tais exposições podem existir em residências diretamente acima de lavanderias. Foi ainda estimado que as concentrações de TCE no leite retornariam aos níveis “normais” (reexposição) quatro a oito semanas após o término da exposição.
Exposições não ocupacionais são possíveis para o bebê em casa onde solventes ou produtos à base de solventes são usados. O ar interno tem níveis muito baixos, mas consistentemente detectáveis, de solventes como o tetracloroetileno. A água também pode conter compostos orgânicos voláteis do mesmo tipo.
Poeiras e fibras minerais: amianto, fibra de vidro, lã de rocha, zeólitos, talco
A exposição à poeira e fibras minerais no local de trabalho causa doenças respiratórias, incluindo câncer de pulmão, entre os trabalhadores. A exposição à poeira é um problema potencial para o recém-nascido se um dos pais carregar objetos para dentro de casa nas roupas ou no corpo. Com o amianto, fibras do local de trabalho foram encontradas no ambiente doméstico e as exposições resultantes de membros da família foram denominadas exposições de espectadores ou familiares. A documentação da doença familiar do amianto foi possível devido à ocorrência de um tumor de sinal, o mesotelioma, que está principalmente associado à exposição ao amianto. O mesotelioma é um câncer da leura ou eritônio (revestimento do pulmão e abdômen, respectivamente) que ocorre após um longo período de latência, geralmente 30 a 40 anos após a primeira exposição ao amianto. A etiologia desta doença parece estar relacionada apenas ao tempo após a exposição inicial, não à intensidade ou duração, nem à idade na primeira exposição (Nicholson 1986; Otte, Sigsgaard e Kjaerulff 1990). Anormalidades respiratórias também foram atribuídas à exposição de pessoas ao amianto (Grandjean e Bach 1986). Extensas experiências com animais suportam as observações humanas.
A maioria dos casos de mesotelioma familiar foi relatada entre esposas de mineiros, moleiros, fabricantes e isoladores expostos. No entanto, várias exposições na infância também foram associadas a doenças. Muitas dessas crianças tiveram contato inicial que ocorreu em uma idade precoce (Dawson et al. 1992; Anderson et al. 1976; Roggli e Longo 1991). Por exemplo, em uma investigação de 24 contatos familiares com mesotelioma que viviam em uma cidade de mineração de amianto crocidolita, foram identificados sete casos cujas idades eram de 29 a 39 anos no momento do diagnóstico ou morte e cuja exposição inicial ocorreu com menos de um ano de idade ( n=5) ou aos três anos (n=2) (Hansen et al. 1993).
A exposição ao amianto é claramente causadora do mesotelioma, mas um mecanismo epigenético foi proposto para explicar o agrupamento incomum de casos em certas famílias. Assim, a ocorrência de mesotelioma entre 64 pessoas em 27 famílias sugere um traço genético que pode tornar certos indivíduos mais sensíveis ao insulto do amianto levando a esta doença (Dawson et al. 1992; Bianchi, Brollo e Zuch 1993). No entanto, também foi sugerido que a exposição isolada pode fornecer uma explicação adequada para a agregação familiar relatada (Alderson 1986).
Outras poeiras inorgânicas associadas a doenças ocupacionais incluem fibra de vidro, zeólitas e talco. Tanto o amianto quanto a fibra de vidro têm sido amplamente utilizados como materiais isolantes. a fibrose pulmonar e o câncer estão associados ao amianto e muito menos claramente à fibra de vidro. O mesotelioma foi relatado em áreas da Turquia com exposições indígenas a zeólitos naturais. As exposições ao amianto também podem surgir de fontes não ocupacionais. Diaers (“naies”) construídos com fibra de amianto foram apontados como uma fonte de exposição infantil ao amianto (Li, Dreyfus e Antman 1989); no entanto, as roupas dos pais não foram excluídas como fonte de contato com o amianto neste relatório. O amianto também foi encontrado em cigarros, secadores de cabelo, pisos e alguns tipos de pó de talco. Seu uso foi eliminado em muitos países. No entanto, uma consideração importante para as crianças é o isolamento de amianto residual nas escolas, que tem sido amplamente investigado como um problema potencial de saúde pública.
Fumaça de tabaco ambiental
A fumaça ambiental do tabaco (ETS) é uma combinação de fumaça exalada e fumaça emitida pelo cigarro aceso. Embora o ETS não seja em si uma fonte de exposição ocupacional que possa afetar o recém-nascido, ele é revisado aqui devido ao seu potencial de causar efeitos adversos à saúde e porque fornece um bom exemplo de outras exposições a aerossóis. A exposição de um não fumante ao FAT é frequentemente descrita como tabagismo passivo ou involuntário. a exposição pré-natal ao ETS está claramente associada a déficits ou deficiências no crescimento fetal. É difícil distinguir os resultados pós-natais dos efeitos da FTA no período pré-natal, uma vez que o tabagismo dos pais raramente se limita a um momento ou outro. No entanto, há evidências para apoiar uma relação de exposição pós-natal ao ETS com doença respiratória e função pulmonar prejudicada. A semelhança desses achados com experiências entre adultos fortalece a associação.
O ETS foi bem caracterizado e extensivamente estudado em termos de exposição humana e efeitos na saúde. ETS é um carcinógeno humano (Agência de proteção ambiental dos EUA 1992). A exposição ao ETS pode ser avaliada pela medição dos níveis de nicotina, um componente do tabaco, e cotinina, seu principal metabólito, em fluidos biológicos, incluindo saliva, sangue e urina. Nicotina e cotinina também foram detectadas no leite materno. A cotinina também foi encontrada no sangue e na urina de crianças que foram expostas ao ETS apenas pela amamentação (Charlton 1994; National Research Council 1986).
A exposição do recém-nascido ao FAT foi claramente estabelecida como resultado do tabagismo paterno e materno no ambiente doméstico. O tabagismo materno fornece a fonte mais significativa. Por exemplo, em vários estudos, a cotinina urinária em crianças mostrou correlação com o número de cigarros fumados pela mãe por dia (Marbury, Hammon e Haley 1993). As principais vias de exposição do neonato à FAT são a respiratória e a dietética (através do leite materno). As creches representam outra situação potencial de exposição; muitas creches não têm uma política de não-fumantes (Sockrider e Coultras 1994).
A hospitalização por doenças respiratórias ocorre com mais frequência entre os recém-nascidos cujos pais fumam. Além disso, a duração das visitas hospitalares é maior entre os lactentes expostos à ETS. Em termos de causalidade, a exposição ao ETS não foi associada a doenças respiratórias específicas. Há evidências, entretanto, de que fumar passivo aumenta a gravidade de doenças reexistentes, como bronquite e asma (Charlton 1994; Chilmonczyk et al. 1993; Rylander et al. 1993). Crianças e bebês expostos ao ETS também têm frequências mais altas de infecções respiratórias. Além disso, pais fumantes com doenças respiratórias podem transmitir infecções transmitidas pelo ar aos bebês pela tosse.
Crianças expostas a ETS pós-natal apresentam pequenos déficits na função pulmonar que parecem ser independentes de exposições pré-natais (Frischer et al. 1992). Embora as alterações relacionadas ao ETS sejam pequenas (redução de 0.5% por ano do volume expiratório forçado), e embora esses efeitos não sejam clinicamente significativos, eles sugerem alterações nas células do pulmão em desenvolvimento que podem indicar risco posterior. o tabagismo dos pais também foi associado ao aumento do risco de otite média, ou efusão da orelha média, em crianças desde a infância até os nove anos de idade. Esta condição é uma causa comum de surdez entre as crianças, o que pode causar atrasos no progresso educacional. O risco associado é apoiado por estudos que atribuem um terço de todos os casos de otite média ao tabagismo dos pais (Charlton 1994).
Exposições à radiação
A exposição à radiação ionizante é um perigo estabelecido para a saúde que geralmente é resultado de exposição intensa, seja acidental ou para fins médicos. Pode ser prejudicial para células altamente proliferativas e, portanto, pode ser muito prejudicial para o feto ou recém-nascido em desenvolvimento. As exposições à radiação que resultam de raios-x diagnósticos são geralmente de nível muito baixo e consideradas seguras. Uma potencial fonte doméstica de exposição à radiação ionizante é o radônio, que existe em certas áreas geográficas em formações rochosas.
efeitos pré-natais e pós-natais da radiação incluem retardo mental, menor inteligência, retardo de crescimento, malformações congênitas e câncer. A exposição a altas doses de radiação ionizante também está associada ao aumento da prevalência de câncer. A incidência desta exposição depende da dose e da idade. De fato, o maior risco relativo observado para câncer de mama (~9) está entre as mulheres que foram expostas à radiação ionizante em uma idade jovem.
Recentemente, a atenção se concentrou nos possíveis efeitos da radiação não ionizante, ou campos eletromagnéticos (CEM). A base de uma relação entre a exposição a CEM e o câncer ainda não é conhecida, e as evidências epidemiológicas ainda não estão claras. No entanto, em vários estudos internacionais, foi relatada uma associação entre EMF e leucemia e câncer de mama masculino.
A exposição infantil à luz solar excessiva tem sido associada ao câncer de pele e melanoma (Marks 1988).
Câncer infantil
Embora substâncias específicas não tenham sido identificadas, as exposições ocupacionais dos pais têm sido associadas ao câncer infantil. O período de latência para o desenvolvimento de leucemia infantil pode ser de dois a 10 anos após o início da exposição, indicando que as exposições in utero ou no início do período pós-natal podem estar implicados na causa desta doença. A exposição a vários pesticidas organoclorados (BHC, DDT, clordano) tem sido tentativamente associada à leucemia, embora esses dados não tenham sido confirmados em estudos mais detalhados. Além disso, foi relatado risco elevado de câncer e leucemia para crianças cujos pais se envolvem em trabalhos que envolvem pesticidas, produtos químicos e fumaça (O'Leary et al. 1991). Da mesma forma, o risco de sarcoma ósseo de Ewing em crianças foi associado às ocupações dos pais na agricultura ou à exposição a herbicidas e pesticidas (Holly et al. 1992).
Sumário
Muitas nações tentam regular os níveis seguros de produtos químicos tóxicos no ar ambiente e nos produtos alimentícios e no local de trabalho. No entanto, as oportunidades de exposição são abundantes e as crianças são particularmente suscetíveis tanto à absorção quanto aos efeitos de substâncias químicas tóxicas. Observou-se que “muitas das 40,000 vidas infantis perdidas no mundo em desenvolvimento todos os dias são consequência de abusos ambientais refletidos em abastecimento de água inseguro, doenças e desnutrição” (Schaefer 1994). Muitas exposições ambientais são evitáveis. Portanto, a prevenção de doenças ambientais tem alta prioridade como defesa contra efeitos adversos à saúde das crianças.
Proteção à Maternidade na Legislação
Durante a gravidez, a exposição a certos riscos de saúde e segurança do trabalho ou do ambiente de trabalho pode ter efeitos adversos na saúde de uma trabalhadora e de seu filho ainda não nascido. Antes e depois do parto, ela também precisa de uma folga razoável do trabalho para se recuperar, amamentar e se relacionar com o filho. Muitas mulheres querem e precisam poder voltar ao trabalho após o parto; isso é cada vez mais reconhecido como um direito básico em um mundo onde a participação das mulheres na força de trabalho está aumentando continuamente e se aproximando da dos homens em muitos países. Como a maioria das mulheres precisa sustentar a si mesmas e suas famílias, a continuidade da renda durante a licença-maternidade é vital.
Ao longo do tempo, os governos promulgaram uma série de medidas legislativas para proteger as mulheres trabalhadoras durante a gravidez e o parto. Uma característica das medidas mais recentes é a proibição de discriminação no emprego com base na gravidez. Outra tendência é proporcionar o direito de mães e pais compartilharem os direitos de licença após o nascimento, para que qualquer um possa cuidar da criança. A negociação coletiva em muitos países contribui para a aplicação mais eficaz de tais medidas e muitas vezes melhora-as. Os empregadores também desempenham um papel importante na promoção da proteção à maternidade por meio dos termos de contratos individuais de trabalho e políticas empresariais.
Os Limites da Proteção
As leis que fornecem proteção à maternidade para mulheres trabalhadoras são geralmente restritas ao setor formal, que pode representar uma pequena proporção da atividade econômica. Isso não se aplica às mulheres que trabalham em atividades econômicas não registradas no setor informal, que em muitos países representam a maioria das mulheres trabalhadoras. Embora haja uma tendência mundial para melhorar e ampliar a proteção à maternidade, como proteger o grande segmento da população que vive e trabalha fora da economia formal continua sendo um grande desafio.
Na maioria dos países, a legislação trabalhista oferece proteção à maternidade para mulheres empregadas em empresas industriais e não industriais no setor privado e, muitas vezes, também no setor público. Os trabalhadores a domicílio, os empregados domésticos, os trabalhadores por conta própria e os trabalhadores em empresas que empregam apenas membros da família são frequentemente excluídos. Uma vez que muitas mulheres trabalham em pequenas empresas, é preocupante a exclusão relativamente frequente de empresas que empregam menos do que um certo número de trabalhadores (por exemplo, cinco trabalhadores permanentes na República da Coreia).
Muitas mulheres trabalhadoras em empregos precários, como trabalhadoras temporárias ou ocasionais na Irlanda, estão excluídas do escopo da legislação trabalhista em vários países. Dependendo do número de horas que trabalham, os trabalhadores a tempo parcial também podem ser excluídos. Outros grupos de mulheres podem ser excluídos, como gerentes (por exemplo, Cingapura, Suíça), mulheres cujos ganhos excedem um determinado máximo (por exemplo, Maurício) ou mulheres que são pagas por resultados (por exemplo, Filipinas). Em casos raros, mulheres solteiras (por exemplo, professoras em Trinidad e Tobago) não se qualificam para licença maternidade. No entanto, na Austrália (federal), onde a licença paternidade está disponível para funcionários e seus cônjuges, o termo “cônjuge” é definido para incluir um cônjuge de fato. Onde os limites de idade são estabelecidos (por exemplo, em Israel, mulheres com menos de 18 anos), eles geralmente não excluem muitas mulheres, pois normalmente são fixados abaixo ou acima da idade reprodutiva.
Os funcionários públicos são muitas vezes abrangidos por regras especiais, que podem prever condições mais favoráveis do que as aplicáveis ao setor privado. Por exemplo, a licença de maternidade pode ser mais longa, as prestações pecuniárias podem corresponder ao salário integral em vez de uma percentagem do mesmo, é mais provável que haja licença parental ou o direito à reintegração pode ser mais claramente estabelecido. Em um número significativo de países, as condições no serviço público podem atuar como um agente de progresso, uma vez que os acordos coletivos de trabalho no setor privado são muitas vezes negociados de acordo com as regras de proteção à maternidade no serviço público.
Semelhante à legislação trabalhista, as leis previdenciárias podem limitar sua aplicação a determinados setores ou categorias de trabalhadores. Embora esta legislação seja muitas vezes mais restritiva do que as leis trabalhistas correspondentes em um país, ela pode fornecer acesso a benefícios monetários de maternidade para grupos não cobertos por leis trabalhistas, como mulheres autônomas ou mulheres que trabalham com seus maridos autônomos. Em muitos países em desenvolvimento, devido à falta de recursos, a legislação previdenciária pode ser aplicada apenas a um número limitado de setores.
Ao longo das décadas, no entanto, a cobertura da legislação foi estendida a mais setores econômicos e categorias de trabalhadores. No entanto, embora um funcionário possa estar coberto por uma lei, o gozo de certos benefícios, em particular licença-maternidade e benefícios em dinheiro, pode depender de certos requisitos de elegibilidade. Assim, enquanto a maioria dos países protege a maternidade, as mulheres trabalhadoras não gozam de um direito universal a tal proteção.
Licença maternidade
O afastamento do trabalho para o parto pode variar de algumas semanas a vários meses, muitas vezes dividido em duas partes, antes e depois do parto. Um período de proibição de trabalho pode ser estipulado para uma parte ou todo o direito para garantir que as mulheres tenham descanso suficiente. A licença-maternidade é comumente estendida em caso de doença, parto prematuro ou tardio e nascimentos múltiplos, ou encurtada em caso de aborto espontâneo, natimorto ou morte infantil.
Duração normal
De acordo com a Convenção de Proteção à Maternidade da OIT, 1919 (No. 3), “uma mulher não poderá trabalhar durante as seis semanas seguintes ao seu parto; [e] terá o direito de deixar seu trabalho se apresentar um atestado médico afirmando que seu parto provavelmente terminará dentro de seis semanas”. A Convenção de Proteção à Maternidade (Revisada), 1952 (No. 103), confirma a licença de 12 semanas, incluindo uma proibição de emprego por seis semanas após o nascimento, mas não prescreve o uso das seis semanas restantes. A Recomendação de proteção à maternidade, 1952 (nº 95), sugere uma licença de 14 semanas. A Recomendação de proteção à maternidade, 2000 (No. 191) sugere uma licença de 18 semanas [Editado, 2011]. A maioria dos países pesquisados atende ao padrão de 12 semanas e pelo menos um terço concede períodos mais longos.
Vários países oferecem a possibilidade de escolha na distribuição da licença de maternidade. Em alguns, a lei não prescreve a distribuição da licença-maternidade (por exemplo, Tailândia), e as mulheres têm o direito de começar a licença tão cedo ou tão tarde quanto desejarem. Em outro grupo de países, a lei indica o número de dias a serem gozados após o parto; o saldo pode ser retirado antes ou depois do nascimento.
Outros países não permitem flexibilidade: a lei prevê dois períodos de licença, antes e depois do confinamento. Esses períodos podem ser iguais, especialmente quando o total de férias é relativamente curto. Nos casos em que o direito total à licença excede 12 semanas, o período pré-natal costuma ser mais curto do que o período pós-natal (por exemplo, na Alemanha, seis semanas antes e oito semanas após o parto).
Em um número relativamente pequeno de países (por exemplo, Benin, Chile, Itália), o emprego de mulheres é proibido durante todo o período de licença maternidade. Em outros, é prescrito um período de licença obrigatória, muitas vezes após o parto (por exemplo, Barbados, Irlanda, Índia, Marrocos). O requisito mais comum é um período obrigatório de seis semanas após o nascimento. Na última década, aumentou o número de países que prevêem alguma licença compulsória antes do parto. Por outro lado, em alguns países (por exemplo, Canadá) não há período de licença obrigatória, pois considera-se que a licença é um direito que deve ser exercido livremente e que o tempo livre deve ser organizado de acordo com as necessidades individuais da mulher e preferências.
Elegibilidade para licença de maternidade
A legislação da maioria dos países reconhece o direito das mulheres à licença de maternidade, estabelecendo o período de licença a que as mulheres têm direito; uma mulher só precisa estar empregada no momento da licença para ser elegível para a licença. Em vários países, no entanto, a lei exige que as mulheres tenham trabalhado por um período mínimo antes da data em que se ausentarem. Este período varia de 13 semanas em Ontário ou na Irlanda a dois anos na Zâmbia.
Em vários países, as mulheres devem ter trabalhado um determinado número de horas na semana ou no mês para ter direito à licença ou benefícios de maternidade. Quando esses limiares são elevados (como em Malta, 35 horas por semana), podem resultar na exclusão de um grande número de mulheres, que constituem a maioria dos trabalhadores a tempo parcial. Em vários países, no entanto, os limites foram reduzidos recentemente (por exemplo, na Irlanda, de 16 para oito horas por semana).
Um pequeno número de países limita o número de vezes que uma mulher pode solicitar licença maternidade durante um determinado período (por exemplo, dois anos) ou restringe a elegibilidade a um determinado número de gestações, seja com o mesmo empregador ou ao longo da vida da mulher (por exemplo, Egito, Malásia). No Zimbábue, por exemplo, as mulheres têm direito à licença maternidade uma vez a cada 24 meses e no máximo três vezes durante o período em que trabalham para o mesmo empregador. Em outros países, as mulheres que têm mais filhos do que o prescrito são elegíveis para licença maternidade, mas não para benefícios em dinheiro (por exemplo, Tailândia), ou são elegíveis para um período mais curto de licença com benefícios (por exemplo, Sri Lanka: 12 semanas para os dois primeiros filhos, seis semanas para o terceiro e filhos subsequentes). O número de países que limitam a elegibilidade para licença ou benefícios de maternidade a um certo número de gestações, filhos ou filhos sobreviventes (entre dois e quatro) parece estar crescendo, embora não seja de forma alguma certo que a duração da licença de maternidade seja um fator decisivo importante na motivação de decisões sobre o tamanho da família.
Aviso prévio ao empregador
Na maioria dos países, o único requisito para que as mulheres tenham direito à licença de maternidade é a apresentação de um atestado médico. Em outros lugares, as mulheres também são obrigadas a notificar seu empregador de sua intenção de tirar a licença maternidade. O período de aviso prévio varia desde que a gravidez é conhecida (por exemplo, Alemanha) até uma semana antes de sair de licença (por exemplo, Bélgica). O incumprimento do requisito de aviso prévio pode fazer com que as mulheres percam o direito à licença de maternidade. Assim, na Irlanda, as informações sobre o momento da licença de maternidade devem ser fornecidas o mais rapidamente possível, mas não mais de quatro semanas antes do início da licença. A funcionária perde o direito à licença de maternidade se não cumprir este requisito. No Canadá (federal), a exigência de notificação é dispensada quando há uma razão válida pela qual a notificação não pode ser fornecida; a nível provincial, o período de notificação varia de quatro meses a duas semanas. Se o período de aviso prévio não for cumprido, a trabalhadora ainda tem direito à licença maternidade normal em Manitoba; ela tem direito a períodos mais curtos (geralmente seis semanas em vez de 17 ou 18) na maioria das outras províncias. Em outros países, a lei não esclarece as consequências da falta de notificação.
Benefícios em dinheiro
A maioria das mulheres não pode perder sua renda durante a licença maternidade; se fosse necessário, muitos não usariam todas as suas licenças. Uma vez que o nascimento de crianças saudáveis beneficia toda a nação, por uma questão de equidade, os empregadores não devem arcar com o custo total das ausências de seus trabalhadores. Desde 1919, os padrões da OIT determinam que, durante a licença maternidade, as mulheres devem receber benefícios em dinheiro e que devem ser pagos com fundos públicos ou por meio de um sistema de seguro. A Convenção n.º 103 exige que as contribuições devidas ao abrigo de um regime de segurança social obrigatório sejam pagas com base no número total de homens e mulheres empregados pelas empresas em causa, sem distinção baseada no sexo. Embora em alguns países os benefícios de maternidade representem apenas uma porcentagem relativamente pequena dos salários, o nível de dois terços exigido na Convenção No. 103 é alcançado em vários e superado em muitos outros. Em mais da metade dos países pesquisados, os benefícios de maternidade constituem 100% do salário segurado ou do salário integral.
Muitas leis de seguridade social podem fornecer um benefício de maternidade específico, reconhecendo assim a maternidade como uma contingência por direito próprio. Outros prevêem que, durante a licença-maternidade, a trabalhadora terá direito a auxílio-doença ou auxílio-desemprego. Tratar a maternidade como uma deficiência ou a licença como um período de desemprego pode ser considerado tratamento desigual, pois, em geral, esses benefícios só estão disponíveis durante um determinado período, e as mulheres que os utilizam em conexão com a maternidade podem descobrir que não têm mais o suficiente para cobrir períodos reais de doença ou desemprego posteriormente. De fato, quando a Diretiva do Conselho Europeu de 1992 foi redigida, uma proposta de que durante a licença maternidade as mulheres receberiam benefícios de doença foi fortemente contestada; argumentou-se que em termos de igualdade de tratamento entre homens e mulheres, a maternidade deveria ser reconhecida como fundamento independente para a obtenção de benefícios. Como compromisso, o subsídio de maternidade foi definido como a garantia de um rendimento pelo menos equivalente ao que a trabalhadora auferiria em caso de doença.
Em quase 80 dos países pesquisados, os benefícios são pagos pelos regimes nacionais de seguridade social e, em mais de 40, são pagos pelo empregador. Em cerca de 15 países, a responsabilidade pelo financiamento das prestações de maternidade é partilhada entre a segurança social e o empregador. Quando os benefícios são financiados conjuntamente pela previdência social e pelo empregador, cada um pode ser obrigado a pagar metade (por exemplo, Costa Rica), embora outras porcentagens possam ser encontradas (por exemplo, Honduras: dois terços pela previdência social e um terço pelo empregador ). Pode ser exigido outro tipo de contribuição aos empregadores: quando o montante do subsídio de maternidade pago pela segurança social se baseia num rendimento estatutário sujeito a contribuição e representa uma percentagem baixa do salário integral da mulher, a lei prevê por vezes que o empregador pagará o saldo entre o salário da mulher e o subsídio de maternidade pago pelo fundo de segurança social (por exemplo, no Burkina Faso). O pagamento adicional voluntário pelo empregador é uma característica de muitos acordos coletivos e também de contratos individuais de trabalho. A participação dos empregadores no pagamento das prestações pecuniárias de maternidade pode ser uma solução realista para o problema colocado pela falta de outros fundos.
Proteção da Saúde das Mulheres Grávidas e Lactantes
De acordo com os requisitos da Recomendação de proteção à maternidade de 1952 (nº 95), muitos países estabelecem várias medidas para proteger a saúde das mulheres grávidas e de seus filhos, buscando minimizar a fadiga pela reorganização do horário de trabalho ou proteger as mulheres contra trabalho perigoso ou insalubre.
Em alguns países (por exemplo, Holanda, Panamá), a lei especifica a obrigação do empregador de organizar o trabalho de forma que não afete o resultado da gravidez. Esta abordagem, que está de acordo com as práticas modernas de saúde e segurança no trabalho, permite adequar as necessidades de cada mulher às medidas preventivas correspondentes e, portanto, é a mais satisfatória. De maneira muito mais geral, a proteção é buscada através da proibição ou limitação do trabalho que pode ser prejudicial à saúde da mãe ou da criança. Tal proibição pode ser redigida em termos gerais ou pode ser aplicada a certos tipos de trabalho perigoso. No entanto, no México, a proibição de empregar mulheres em trabalhos insalubres ou perigosos não se aplica se as medidas necessárias de proteção à saúde tiverem sido tomadas, na opinião da autoridade competente; também não se aplica a mulheres em cargos de chefia ou que possuam diploma universitário ou técnico, ou conhecimento e experiência necessários para o exercício da função.
Em muitos países, a lei prevê que mulheres grávidas e lactantes não podem fazer trabalhos “além de suas forças”, que “envolvam riscos”, “perigosos à sua saúde ou à de seus filhos” ou “requeiram um esforço físico inadequado à sua condição”. A aplicação de tal proibição geral, no entanto, pode apresentar problemas: como e por quem deve ser determinado que um trabalho está além das forças de uma pessoa? Pelo trabalhador em questão, pelo empregador, pelo fiscal do trabalho, pelo médico do trabalho, pelo próprio médico da mulher? As diferenças de apreciação podem fazer com que uma mulher seja afastada do trabalho que ela poderia de fato fazer, enquanto outra pode não ser afastada do trabalho que é muito desgastante.
Outros países listam, às vezes com muitos detalhes, o tipo de trabalho que é proibido para mulheres grávidas e lactantes (por exemplo, Áustria, Alemanha). A movimentação de cargas é frequentemente regulada. A legislação de alguns países proíbe especificamente a exposição a certos produtos químicos (por exemplo, benzeno), agentes biológicos, chumbo e radiação. O trabalho clandestino é proibido no Japão durante a gravidez e um ano após o parto. Na Alemanha, o trabalho por peça e o trabalho em uma linha de montagem com um ritmo fixo são proibidos. Em alguns países, as trabalhadoras grávidas não podem ser designadas para trabalhar fora de seu local de residência permanente (por exemplo, Gana, após o quarto mês). Na Áustria, não é permitido fumar em locais onde mulheres grávidas trabalham.
Em vários países (por exemplo, Angola, Bulgária, Haiti, Alemanha), o empregador é obrigado a transferir o trabalhador para um trabalho adequado. Muitas vezes, a trabalhadora deve manter seu antigo salário mesmo que o salário do cargo para o qual é transferida seja inferior. Na República Democrática Popular do Laos, a mulher mantém o seu salário anterior durante um período de três meses, sendo depois remunerada de acordo com o trabalho que efectivamente desempenha. Na Federação Russa, onde um posto adequado deve ser dado a uma mulher que não pode mais exercer seu trabalho, ela retém seu salário durante o período em que um novo posto é encontrado. Em certos casos (por exemplo, Roménia), a diferença entre os dois salários é paga pela segurança social, uma disposição que deve ser referida, uma vez que o custo da proteção da maternidade não deve, tanto quanto possível, ser suportado por empregadores individuais.
A transferência também pode estar disponível a partir de um trabalho que não seja perigoso em si, mas que um médico tenha certificado como prejudicial ao estado de saúde de uma determinada mulher (por exemplo, França). Em outros países, uma transferência é possível a pedido do trabalhador em questão (por exemplo, Canadá, Suíça). Quando a lei permitir que o empregador sugira a transferência, havendo desacordo entre o empregador e o trabalhador, o médico do trabalho determinará se há necessidade médica de mudança de emprego e se o trabalhador está apto a assumir o cargo que foi sugerido a ela.
Alguns países esclarecem o fato de que a transferência é temporária e que a trabalhadora deve ser reatribuída ao seu antigo emprego quando ela retornar da licença de maternidade ou em um determinado momento posterior (por exemplo, França). Quando a transferência não é possível, alguns países prevêem que a trabalhadora receba licença médica (por exemplo, Seychelles) ou, como discutido acima, que a licença-maternidade comece mais cedo (por exemplo, Islândia).
Não discriminação
Medidas são tomadas em um número crescente de países para garantir que as mulheres não sofram discriminação por causa da gravidez. O seu objetivo é garantir que as mulheres grávidas sejam consideradas para o emprego e tratadas durante o emprego em igualdade de condições com os homens e com as outras mulheres e, em particular, não sejam rebaixadas, não percam a antiguidade ou não tenham negada a promoção apenas em razão da gravidez. Agora é cada vez mais comum que a legislação nacional proíba a discriminação em razão do sexo. Tal proibição poderia ser, e de fato tem sido, em muitos casos, interpretada pelos tribunais como uma proibição de discriminação por causa da gravidez. O Tribunal Europeu de Justiça tem seguido esta abordagem. Num acórdão de 1989, o Tribunal decidiu que um empregador que despedisse ou recusasse contratar uma mulher por estar grávida violava a Diretiva 76/207/CEE do Conselho Europeu sobre igualdade de tratamento. Esse julgamento foi importante para esclarecer o fato de que existe discriminação sexual quando as decisões de emprego são tomadas com base na gravidez, embora a lei não cite especificamente a gravidez como motivo proibido de discriminação. É costume em casos de igualdade de sexo comparar o tratamento dado a uma mulher com o tratamento dado a um homem hipotético. O Tribunal decidiu que tal comparação não era necessária no caso de uma mulher grávida, uma vez que a gravidez era exclusiva da mulher. Quando o tratamento desfavorável é feito com base na gravidez, há, por definição, discriminação com base no sexo. Isso é consistente com a posição do Comitê de Exercícios da OIT sobre a Aplicação de Convenções e Recomendações sobre o escopo da Convenção sobre Discriminação (Emprego e Ocupação), 1958 (nº 111), que observa a natureza discriminatória das distinções com base em gravidez, parto e condições médicas relacionadas (ILO 1988).
Vários países prevêem uma proibição explícita de discriminação com base na gravidez (por exemplo, Austrália, Itália, EUA, Venezuela). Outros países definem a discriminação com base no sexo para incluir a discriminação com base na gravidez ou ausência na licença de maternidade (por exemplo, Finlândia). Nos EUA, a proteção é ainda assegurada através do tratamento da gravidez como uma deficiência: nas empresas com mais de 15 trabalhadores, é proibida a discriminação contra mulheres grávidas, mulheres no parto e mulheres afetadas por condições médicas relacionadas; e as políticas e práticas relacionadas à gravidez e assuntos relacionados devem ser aplicadas nos mesmos termos e condições aplicadas a outras deficiências.
Em vários países, a lei contém requisitos precisos que ilustram casos de discriminação com base na gravidez. Por exemplo, na Federação Russa, um empregador não pode se recusar a contratar uma mulher porque ela está grávida; caso a gestante não seja contratada, o empregador deverá informar por escrito os motivos da não contratação. Na França, é ilegal que um empregador leve em consideração a gravidez ao se recusar a contratar uma mulher, ao rescindir seu contrato durante um período de experiência ou ao ordenar sua transferência. Também é ilegal que o empregador procure determinar se uma candidata está grávida ou fazer com que tal informação seja solicitada. Da mesma forma, as mulheres não podem ser obrigadas a revelar o facto de estarem grávidas, quer se candidatem a um emprego, quer estejam empregadas num, exceto quando solicitem o benefício de qualquer lei ou regulamento que regule a proteção das mulheres grávidas.
Transferências impostas unilateral e arbitrariamente a uma mulher grávida podem constituir discriminação. Na Bolívia, como em outros países da região, a mulher está protegida contra a transferência involuntária durante a gravidez e até um ano após o nascimento de seu filho.
A questão de combinar o direito das mulheres trabalhadoras à proteção da saúde durante a gravidez e seu direito de não sofrer discriminação coloca uma dificuldade especial no momento do recrutamento. A candidata grávida deve revelar sua condição, principalmente aquela que se candidata a um cargo que envolva trabalho vedado à gestante? Em um julgamento de 1988, o Tribunal Federal do Trabalho da Alemanha decidiu que uma mulher grávida que se candidatasse a um emprego exclusivamente noturno, proibido para mulheres grávidas pela legislação alemã, deveria informar um possível empregador sobre sua condição. O julgamento foi rejeitado pelo Tribunal Europeu de Justiça por ser contrário à Diretiva CE de 1976 sobre igualdade de tratamento. O Tribunal considerou que a directiva impedia que um contrato de trabalho fosse considerado nulo em virtude da proibição legal do trabalho nocturno ou evitado pelo empregador por erro da sua parte quanto a uma característica pessoal essencial do trabalhador a mulher no momento da celebração do contrato. A incapacidade da trabalhadora, por motivo de gravidez, para o desempenho do trabalho para o qual estava a ser contratada foi temporária, uma vez que o contrato não foi celebrado por tempo determinado. Seria, portanto, contrário ao objetivo da diretiva considerá-la inválida ou nula devido a tal incapacidade.
Segurança no emprego
Muitas mulheres perderam seus empregos por causa de uma gravidez. Hoje em dia, embora a extensão da proteção varie, a segurança no emprego é um componente significativo das políticas de proteção à maternidade.
As normas internacionais do trabalho abordam a questão de duas maneiras diferentes. As convenções de protecção da maternidade proíbem o despedimento durante a licença de maternidade e qualquer prorrogação da mesma, ou quando o aviso de despedimento expirar durante a licença, nos termos da Convenção n.º 3, artigo 4.º e da Convenção n.º 103, artigo 6.º. motivos que possam ser considerados legítimos não são considerados permitidos durante esse período (ILO 1965). Caso a mulher tenha sido dispensada antes de entrar em licença-maternidade, o aviso deverá ser suspenso pelo tempo que ela estiver ausente e continuar após o seu retorno. A Recomendação de proteção à maternidade, 1952 (nº 95), exige a proteção do emprego de uma mulher grávida desde a data em que o empregador é informado da gravidez até um mês após o retorno da licença de maternidade. Identifica os casos de falta grave da trabalhadora trabalhadora, o encerramento da empresa e a caducidade do contrato a termo como fundamentos legítimos do despedimento durante o período protegido. A Convenção de Rescisão do Emprego, 1982 (Nº 158; Artigo 5(d)–(e)), não proíbe a demissão, mas estabelece que a gravidez ou ausência do trabalho em licença de maternidade não constituem motivos válidos para rescisão do contrato de trabalho.
A nível da União Europeia, a Diretiva de 1992 proíbe o despedimento desde o início da gravidez até ao termo da licença de maternidade, salvo em casos excecionais não relacionados com a condição da trabalhadora.
Normalmente, os países fornecem dois conjuntos de regras em relação à demissão. O despedimento com pré-aviso aplica-se em casos como o encerramento da empresa, redundância e quando, por motivos diversos, o trabalhador não puder desempenhar o trabalho para o qual foi contratado ou não o executar a contento do empregador . A demissão sem aviso prévio é usada para rescindir os serviços de um trabalhador culpado de negligência grave, falta grave ou outras instâncias graves de comportamento, geralmente listadas de forma abrangente na legislação.
No caso do despedimento com pré-aviso, é evidente que os empregadores podem decidir arbitrariamente que a gravidez é incompatível com as funções da trabalhadora e despedi-la por motivo de gravidez. Quem pretender furtar-se às obrigações para com as grávidas, ou mesmo simplesmente não gostar de ter grávidas no local de trabalho, poderia encontrar um pretexto para despedir trabalhadoras durante a gravidez ainda que, face à existência de regras de não discriminação, não abster-se de usar a gravidez como motivo para demissão. Muitas pessoas concordam que é legítimo proteger os trabalhadores contra tais decisões discriminatórias: a proibição de despedimento com pré-aviso por motivo de gravidez ou durante a gravidez e licença de maternidade é muitas vezes vista como uma medida de equidade e está em vigor em muitos países.
O Comitê de Atuação da OIT sobre a Aplicação de Convenções e Recomendações considera que a proteção contra a demissão não impede o empregador de rescindir o vínculo empregatício por ter detectado falta grave da empregada: ao contrário, quando há motivos como esta para justificar o despedimento, o empregador é obrigado a prorrogar o prazo legal de pré-aviso por qualquer período necessário para completar o período de proteção ao abrigo das Convenções. Esta é a situação, por exemplo, na Bélgica, onde um empregador que tem motivos legais para despedir uma mulher não pode fazê-lo enquanto ela estiver em licença de maternidade, mas pode notificá-lo para que expire quando a mulher regressar da licença.
A protecção das mulheres grávidas contra o despedimento em caso de encerramento da empresa ou de recessão económica coloca um problema semelhante. É efectivamente um encargo para uma empresa que cessa a sua actividade continuar a pagar o salário de uma pessoa que já não trabalha para ela, mesmo que por um curto período. No entanto, as perspectivas de recrutamento costumam ser mais sombrias para mulheres grávidas do que para mulheres que não estão grávidas, ou para homens, e as mulheres grávidas precisam particularmente da segurança emocional e financeira de continuar empregadas. Nos casos em que as mulheres não podem ser despedidas durante a gravidez, podem adiar a procura de emprego até depois do parto. De fato, onde a legislação prevê a ordem em que várias categorias de trabalhadores a serem demitidos devem ser demitidos, as mulheres grávidas estão entre as últimas ou penúltimas demitidas (por exemplo, Etiópia).
Licença e benefícios para pais e pais
Indo além da proteção da saúde e situação profissional de mulheres grávidas e lactantes, muitos países fornecem licença paternidade (um curto período de licença no momento do nascimento ou próximo a ele). Outras formas de licença estão ligadas às necessidades das crianças. Um tipo é a licença de adoção e outro é a licença para facilitar a criação dos filhos. Muitos países prevêem o último tipo de licença, mas usam abordagens diferentes. Um grupo oferece folga para a mãe de crianças muito pequenas (licença maternidade opcional), enquanto outro oferece licença adicional para ambos os pais (licença parental). A visão de que tanto o pai quanto a mãe precisam estar disponíveis para cuidar de crianças pequenas também se reflete nos sistemas integrados de licença parental, que fornecem um longo período de licença disponível para ambos os pais.
Gravidez e recomendações de trabalho nos EUA
As mudanças na vida familiar nas últimas décadas tiveram efeitos dramáticos na relação entre trabalho e gravidez. Estes incluem o seguinte:
- As mulheres, particularmente aquelas em idade reprodutiva, continuam a entrar na força de trabalho em números consideráveis.
- Desenvolveu-se em muitas dessas mulheres uma tendência de adiar a constituição de uma família até que sejam mais velhas, quando já alcançaram posições de responsabilidade e se tornaram membros importantes do aparato produtivo.
- Ao mesmo tempo, há um número crescente de gestações na adolescência, muitas das quais são gestações de alto risco.
- Refletindo taxas crescentes de separação, divórcio e escolhas de estilos de vida alternativos, bem como um aumento no número de famílias em que ambos os pais devem trabalhar, as pressões financeiras estão forçando muitas mulheres a continuar trabalhando o máximo possível durante a gravidez.
O impacto das faltas relacionadas à gravidez e da produtividade perdida ou prejudicada, bem como a preocupação com a saúde e o bem-estar das mães e de seus bebês, levaram os empregadores a se tornarem mais proativos ao lidar com o problema da gravidez e do trabalho. Onde os empregadores pagam a totalidade ou parte dos prêmios de seguro de saúde, a perspectiva de evitar os custos às vezes surpreendentes de gestações complicadas e problemas neonatais é um incentivo poderoso. Certas respostas são ditadas por leis e regulamentações governamentais, por exemplo, proteção contra possíveis riscos ocupacionais e ambientais e concessão de licença maternidade e outros benefícios. Outros são voluntários: educação pré-natal e programadores de cuidados, acordos de trabalho modificados, como horários flexíveis e outros acordos de horário de trabalho, cuidados dependentes e outros benefícios.
Gestão da gravidez
De primordial importância para a gestante - e para seu empregador - quer ela continue ou não trabalhando durante a gravidez, é o acesso a um programa profissional de gerenciamento de saúde destinado a identificar e evitar ou minimizar os riscos para a mãe e seu feto, permitindo-lhe assim permanecer no trabalho sem preocupação. Em cada uma das consultas pré-natais agendadas, o médico ou parteira deve avaliar as informações médicas (gravidez e outros antecedentes médicos, queixas atuais, exames físicos e exames laboratoriais) e informações sobre seu trabalho e ambiente de trabalho, e desenvolver recomendações apropriadas.
É importante que os profissionais de saúde não se baseiem em simples descrições de funções relativas ao trabalho de seus pacientes, pois muitas vezes são imprecisas e enganosas. As informações sobre o trabalho devem incluir detalhes sobre atividade física, exposição a substâncias químicas e outras e estresse emocional, a maioria dos quais pode ser fornecida pela própria mulher. Em alguns casos, no entanto, a entrada de um supervisor, muitas vezes retransmitida pelo departamento de segurança ou pelo serviço de saúde do funcionário (quando houver), pode ser necessária para fornecer um quadro mais completo das atividades de trabalho perigosas ou difíceis e a possibilidade de controlar suas potencial de dano. Isso também pode servir como um controle sobre os pacientes que inadvertidamente ou deliberadamente enganam seus médicos; eles podem exagerar os riscos ou, se acharem importante continuar trabalhando, podem subestimá-los.
Recomendações para Trabalho
As recomendações relativas ao trabalho durante a gravidez dividem-se em três categorias:
A mulher pode continuar trabalhando sem mudanças em suas atividades ou no ambiente. Isso é aplicável na maioria dos casos. Após extensa deliberação, a Força-Tarefa sobre a Incapacidade da Gravidez, composta por profissionais de saúde obstétrica, médicos do trabalho e enfermeiras, e representantes de mulheres reunidas pelo ACOG (American College of Obstetricians and Gynecologists) e NIOSH (National Institute for Occupational Safety and Health) concluiu que “a mulher normal com uma gravidez sem complicações que está em um trabalho que não apresenta maiores riscos do que os encontrados na vida diária normal na comunidade, pode continuar a trabalhar sem interrupção até o início do trabalho de parto e pode retomar o trabalho várias semanas após um parto sem complicações entrega” (Isenman e Warshaw, 1977).
A mulher pode continuar trabalhando, mas apenas com algumas modificações no ambiente de trabalho ou em suas atividades laborais. Essas modificações seriam “desejáveis” ou “essenciais” (neste último caso, ela deveria parar de trabalhar se não pudessem ser feitas).
A mulher não deve trabalhar. É opinião do médico ou da parteira que qualquer trabalho provavelmente seria prejudicial à sua saúde ou à do feto em desenvolvimento.
As recomendações devem não apenas detalhar as modificações necessárias no cargo, mas também estipular o tempo em que devem vigorar e indicar a data do próximo exame profissional.
Considerações não médicas
As recomendações sugeridas acima são baseadas inteiramente em considerações sobre a saúde da mãe e do feto em relação aos requisitos do trabalho. Eles não levam em consideração o fardo de atividades fora do trabalho, como deslocamento de e para o local de trabalho, tarefas domésticas e cuidado de outras crianças e familiares; estes às vezes podem ser ainda mais exigentes do que os do trabalho. Quando for necessária a modificação ou restrição de atividades, deve-se considerar se deve ser implementada no trabalho, em casa ou em ambos.
Além disso, as recomendações a favor ou contra a continuação do trabalho podem formar a base de uma variedade de considerações não médicas, por exemplo, elegibilidade para benefícios, licença remunerada versus não remunerada ou garantia de retenção no emprego. Uma questão crítica é se a mulher é considerada deficiente. Alguns empregadores consideram categoricamente todas as trabalhadoras grávidas como deficientes e se esforçam para eliminá-las da força de trabalho, embora muitas possam continuar trabalhando. Outros empregadores assumem que todas as funcionárias grávidas tendem a ampliar qualquer deficiência para serem elegíveis para todos os benefícios disponíveis. E alguns até desafiam a noção de que uma gravidez, seja ou não incapacitante, é um assunto para eles se preocuparem. Assim, a deficiência é um conceito complexo que, embora baseado fundamentalmente em achados médicos, envolve considerações legais e sociais.
Gravidez e Deficiência
Em muitas jurisdições, é importante distinguir entre a incapacidade da gravidez e a gravidez como um período da vida que exige benefícios e dispensas especiais. A deficiência da gravidez cai em três categorias:
- Incapacidade após o parto. Do ponto de vista puramente médico, a recuperação após a interrupção da gravidez por meio de um parto sem complicações dura apenas algumas semanas, mas convencionalmente se estende por seis ou oito semanas, porque é quando a maioria dos obstetras costuma agendar seu primeiro check-up pós-natal. No entanto, do ponto de vista prático e sociológico, uma licença mais longa é considerada por muitos como desejável para aumentar os laços familiares, facilitar a amamentação e assim por diante.
- Incapacidade resultante de complicações médicas. Complicações médicas como eclamsia, ameaça de aborto, problemas cardiovasculares ou renais e assim por diante ditarão períodos de atividade reduzida ou mesmo hospitalização que durarão enquanto a condição médica persistir ou até que a mulher se recupere tanto do problema médico quanto da gravidez .
- Incapacidade refletindo a necessidade de evitar a exposição a riscos de toxicidade ou estresse físico anormal. Devido à maior sensibilidade do feto a muitos riscos ambientais, a gestante pode ser considerada deficiente, mesmo que sua própria saúde não corra o risco de ser comprometida.
Conclusão
O desafio de equilibrar as responsabilidades familiares e o trabalho fora de casa não é novidade para as mulheres. O que pode ser novo é uma sociedade moderna que valoriza a saúde e o bem-estar das mulheres e de seus filhos, enquanto as confronta com o duplo desafio de alcançar a realização pessoal por meio do emprego e lidar com as pressões econômicas de manter um padrão de vida aceitável. O número crescente de pais solteiros e de casais casados que precisam trabalhar sugere que as questões trabalho-família não podem ser ignoradas. Muitas mulheres empregadas que engravidam simplesmente devem continuar trabalhando.
De quem é a responsabilidade de atender às necessidades desses indivíduos? Alguns argumentariam que é puramente um problema pessoal a ser tratado inteiramente pelo indivíduo ou pela família. Outros consideram isso uma responsabilidade social e promulgariam leis e forneceriam benefícios financeiros e outros em toda a comunidade.
Quanto deve ser carregado no empregador? Isso depende em grande parte da natureza, da localização e, muitas vezes, do tamanho da organização. O empregador é movido por dois conjuntos de considerações: aquelas impostas por leis e regulamentos (e às vezes pela necessidade de atender demandas conquistadas pelo trabalho organizado) e aquelas ditadas pela responsabilidade social e pela necessidade prática de manter a produtividade ideal. Em última análise, depende de atribuir um alto valor aos recursos humanos e reconhecer a interdependência das responsabilidades do trabalho e dos compromissos familiares e seus efeitos, por vezes, contrabalançados na saúde e na produtividade.
Estrutura e função
O sistema respiratório se estende desde a zona respiratória fora do nariz e da boca através das vias aéreas condutivas na cabeça e no tórax até os alvéolos, onde ocorre a troca gasosa respiratória entre os alvéolos e o sangue capilar que flui ao redor deles. Sua principal função é fornecer oxigênio (O2) para a região de troca gasosa do pulmão, onde pode se difundir para e através das paredes dos alvéolos para oxigenar o sangue que passa pelos capilares alveolares conforme necessário em uma ampla gama de trabalho ou níveis de atividade. Além disso, o sistema também deve: (1) remover um volume igual de dióxido de carbono que entra nos pulmões pelos capilares alveolares; (2) manter a temperatura corporal e a saturação do vapor de água nas vias aéreas pulmonares (para manter a viabilidade e as capacidades funcionais dos fluidos e células superficiais); (3) manter a esterilidade (para prevenir infecções e suas consequências adversas); e (4) eliminar o excesso de fluidos e detritos superficiais, como partículas inaladas e células fagocíticas e epiteliais senescentes. Ele deve realizar todas essas tarefas exigentes continuamente ao longo da vida, e fazê-lo com alta eficiência em termos de desempenho e utilização de energia. O sistema pode ser abusado e sobrecarregado por insultos severos, como altas concentrações de fumaça de cigarro e poeira industrial, ou por baixas concentrações de patógenos específicos que atacam ou destroem seus mecanismos de defesa, ou causam seu mau funcionamento. Sua capacidade de superar ou compensar tais insultos com tanta competência quanto costuma fazer é uma prova de sua elegante combinação de estrutura e função.
Transferência de massa
A complexa estrutura e numerosas funções do trato respiratório humano foram resumidas de forma concisa por um Grupo de Trabalho da Comissão Internacional de Proteção Radiológica (ICRP 1994), conforme mostrado na figura 1. As vias aéreas condutivas, também conhecidas como espaço morto respiratório, ocupam cerca de 0.2 litros. Eles condicionam o ar inalado e o distribuem, por fluxo convectivo (volume), para os aproximadamente 65,000 ácinos respiratórios que saem dos bronquíolos terminais. À medida que os volumes correntes aumentam, o fluxo convectivo domina as trocas gasosas mais profundas nos bronquíolos respiratórios. Em qualquer caso, dentro do ácino respiratório, a distância da frente de maré convectiva às superfícies alveolares é curta o suficiente para que o CO eficiente2-O2 a troca ocorre por difusão molecular. Por outro lado, as partículas em suspensão no ar, com coeficientes de difusão menores em ordens de grandeza do que os gases, tendem a permanecer suspensas no ar das marés e podem ser exaladas sem deposição.
Figura 1. Morfometria, citologia, histologia, função e estrutura do trato respiratório e regiões utilizadas no modelo de dosimetria 1994 ICRP.
Uma fração significativa das partículas inaladas se deposita no trato respiratório. Os mecanismos responsáveis pela deposição de partículas nas vias aéreas pulmonares durante a fase inspiratória de uma respiração corrente estão resumidos na figura 2. Partículas maiores que cerca de 2 mm de diâmetro aerodinâmico (diâmetro de uma esfera de densidade unitária com a mesma velocidade de acomodação terminal (Stokes)) pode ter impulso significativo e depósito por impactação nas velocidades relativamente altas presentes nas vias aéreas maiores. Partículas maiores que cerca de 1 mm podem se depositar por sedimentação nas vias aéreas condutoras menores, onde as velocidades de fluxo são muito baixas. Finalmente, partículas com diâmetros entre 0.1 e 1 mm, que têm uma probabilidade muito baixa de se depositar durante uma única respiração corrente, podem ser retidas em aproximadamente 15% do ar corrente inspirado que é trocado com o ar pulmonar residual durante cada ciclo de maré. Essa troca volumétrica ocorre devido às constantes de tempo variáveis para o fluxo de ar nos diferentes segmentos dos pulmões. Devido aos tempos de residência muito mais longos do ar residual nos pulmões, os baixos deslocamentos intrínsecos de partículas de 0.1 a 1 mm dentro desses volumes aprisionados de ar corrente inalado tornam-se suficientes para causar sua deposição por sedimentação e/ou difusão ao longo do curso de respirações sucessivas.
Figura 2. Mecanismos de deposição de partículas nas vias aéreas pulmonares
O ar pulmonar residual essencialmente livre de partículas, responsável por cerca de 15% do fluxo corrente expiratório, tende a agir como uma bainha de ar limpo ao redor do núcleo axial do ar corrente que se move distalmente, de modo que a deposição de partículas no ácino respiratório é concentrada no interior. superfícies como as bifurcações das vias aéreas, enquanto as paredes das vias aéreas interbranquiais têm pouca deposição.
O número de partículas depositadas e sua distribuição ao longo das superfícies do trato respiratório são, juntamente com as propriedades tóxicas do material depositado, os determinantes críticos do potencial patogênico. As partículas depositadas podem danificar as células epiteliais e/ou fagocíticas móveis no local ou próximo ao local de deposição, ou podem estimular a secreção de fluidos e mediadores derivados de células que têm efeitos secundários no sistema. Materiais solúveis depositados como, sobre ou dentro de partículas podem se difundir para dentro e através de fluidos e células superficiais e serem rapidamente transportados pela corrente sanguínea por todo o corpo.
A solubilidade aquosa de materiais a granel é um guia ruim para a solubilidade de partículas no trato respiratório. A solubilidade é geralmente grandemente aumentada pela proporção muito grande de superfície para volume de partículas pequenas o suficiente para entrar nos pulmões. Além disso, os conteúdos iônicos e lipídicos dos fluidos superficiais dentro das vias aéreas são complexos e altamente variáveis e podem levar a uma maior solubilidade ou à rápida precipitação de solutos aquosos. Além disso, as vias de depuração e os tempos de residência das partículas nas superfícies das vias aéreas são muito diferentes nas diferentes partes funcionais do trato respiratório.
O modelo de depuração revisado do ICRP Task Group identifica as principais vias de depuração dentro do trato respiratório que são importantes para determinar a retenção de vários materiais radioativos e, portanto, as doses de radiação recebidas pelos tecidos respiratórios e outros órgãos após a translocação. O modelo de deposição ICRP é usado para estimar a quantidade de material inalado que entra em cada via de depuração. Essas vias discretas são representadas pelo modelo de compartimento mostrado na figura 3. Correspondem aos compartimentos anatômicos ilustrados na Figura 1 e estão resumidos na tabela 1, juntamente com os de outros grupos que fornecem orientações sobre a dosimetria de partículas inaladas.
Figura 3. Modelo de compartimento para representar o transporte de partículas dependente do tempo de cada região no modelo ICRP de 1994
Tabela 1. Regiões do trato respiratório definidas em modelos de deposição de partículas
| Estruturas anatômicas incluídas | Região ACGIH | Regiões ISO e CEN | Região do Grupo de Tarefas do ICRP de 1966 | Região do Grupo de Tarefas do ICRP de 1994 |
| Nariz, nasofaringe Boca, orofaringe, laringofaringe |
Vias aéreas da cabeça (HAR) | Extratorácica (E) | Nasofaringe (NP) | Passagens nasais anteriores (ET1 ) Todos os outros extratorácicos (ET2 ) |
| Traquéia, brônquios | Traqueobrônquica (TBR) | Traqueobrônquica (B) | Traqueobrônquica (TB) | Traquéia e grandes brônquios (BB) |
| Bronquíolos (para os bronquíolos terminais) | Bronquíolos (bb) | |||
| bronquíolos respiratórios, ductos alveolares, sacos alveolares, alvéolos |
Troca gasosa (RGE) | Alveolar (A) | Pulmonar (P) | Alveolar-intersticial (AI) |
Vias aéreas extratorácicas
Conforme mostrado na figura 1, as vias aéreas extratorácicas foram divididas por ICRP (1994) em duas regiões distintas de depuração e dosimetria: as passagens nasais anteriores (ET1) e todas as outras vias aéreas extratorácicas (ET2) — isto é, as passagens nasais posteriores, nasofaringe e orofaringe e a laringe. Partículas depositadas na superfície da pele que revestem as passagens nasais anteriores (ET1) são considerados sujeitos apenas à remoção por meios extrínsecos (assoar o nariz, limpar e assim por diante). A maior parte do material depositado na naso-orofaringe ou laringe (ET2) está sujeito a rápida depuração na camada de fluido que recobre essas vias aéreas. O novo modelo reconhece que a deposição por difusão de partículas ultrafinas nas vias aéreas extratorácicas pode ser substancial, enquanto os modelos anteriores não.
vias aéreas torácicas
O material radioativo depositado no tórax é geralmente dividido entre a região traqueobrônquica (TB), onde as partículas depositadas estão sujeitas a uma depuração mucociliar relativamente rápida, e a região alvéolo-intersticial (AI), onde a depuração das partículas é bem mais lenta.
Para fins de dosimetria, o ICRP (1994) dividiu a deposição do material inalado na região da TB entre a traqueia e os brônquios (BB) e as pequenas vias aéreas mais distais, os bronquíolos (bb). No entanto, a eficiência subsequente com a qual os cílios em qualquer tipo de via aérea são capazes de limpar as partículas depositadas é controversa. Para ter certeza de que as doses nos epitélios brônquicos e bronquiolares não seriam subestimadas, o Grupo de Trabalho assumiu que até metade do número de partículas depositadas nessas vias aéreas está sujeita a uma depuração mucociliar relativamente “lenta”. A probabilidade de uma partícula ser eliminada de forma relativamente lenta pelo sistema mucociliar parece depender de seu tamanho físico.
O material depositado na região AI é subdividido em três compartimentos (AI1, IA2 e AI3) que são eliminados mais lentamente do que a deposição de TB, com as sub-regiões eliminadas em taxas características diferentes.
Figura 4. Deposição fracionada em cada região do trato respiratório para o trabalhador leve de referência (respirador nasal normal) no modelo ICRP de 1994.
A Figura 4 mostra as previsões do modelo ICRP (1994) em termos da deposição fracionada em cada região em função do tamanho das partículas inaladas. Reflete a deposição pulmonar mínima entre 0.1 e 1 mm, onde a deposição é determinada em grande parte pela troca, no pulmão profundo, entre o ar pulmonar corrente e residual. A deposição aumenta abaixo de 0.1 mm à medida que a difusão se torna mais eficiente com a diminuição do tamanho das partículas. A deposição aumenta com o aumento do tamanho da partícula acima de 1 mm à medida que a sedimentação e a compactação se tornam cada vez mais efetivas.
Modelos menos complexos para deposição seletiva de tamanho foram adotados por profissionais e agências de saúde ocupacional e poluição do ar da comunidade, e estes têm sido usados para desenvolver limites de exposição por inalação dentro de faixas específicas de tamanho de partícula. As distinções são feitas entre:
- aquelas partículas que não são aspiradas para o nariz ou boca e, portanto, não representam risco de inalação
- o inalável (também conhecido como inspirável) massa particulada (IPM)—aquelas que são inaladas e são perigosas quando depositadas em qualquer lugar dentro do trato respiratório
- a massa particulada torácica (TPM) - aqueles que penetram na laringe e são perigosos quando depositados em qualquer lugar dentro do tórax e
- a massa particulada respirável (RPM) - aquelas partículas que penetram através dos bronquíolos terminais e são perigosas quando depositadas na região de troca gasosa dos pulmões.
No início da década de 1990, houve uma harmonização internacional das definições quantitativas de IPM, TPM e RPM. As especificações de entrada com seleção de tamanho para amostradores de ar que atendem aos critérios da Conferência Americana de Higienistas Industriais Governamentais (ACGIH 1993), da Organização Internacional de Padronização (ISO 1991) e do Comitê Europeu de Padronização (CEN 1991) são enumeradas na tabela 2. diferem das frações de deposição de ICRP (1994), especialmente para partículas maiores, porque eles assumem a posição conservadora de que a proteção deve ser fornecida para aqueles envolvidos na inalação oral e, assim, contornam a eficiência de filtração mais eficiente das passagens nasais.
Tabela 2. Critérios de poeira inalável, torácica e respirável da ACGIH, ISO e CEN, e PM10 critérios da EPA dos EUA
| Inalável | Thoracic | Respirável | PM10 | ||||
| partícula aero- diâmetro dinâmico (mm) |
Inalável Particulado Massa (IPM) (%) |
partícula aero- diâmetro dinâmico (mm) |
Thoracic Particulado Massa (TPM) (%) |
partícula aero- diâmetro dinâmico (mm) |
Respirável Particulado Massa (RPM) (%) |
partícula aero- diâmetro dinâmico (mm) |
Thoracic Particulado Massa (TPM) (%) |
| 0 | 100 | 0 | 100 | 0 | 100 | 0 | 100 |
| 1 | 97 | 2 | 94 | 1 | 97 | 2 | 94 |
| 2 | 94 | 4 | 89 | 2 | 91 | 4 | 89 |
| 5 | 87 | 6 | 80.5 | 3 | 74 | 6 | 81.2 |
| 10 | 77 | 8 | 67 | 4 | 50 | 8 | 69.7 |
| 20 | 65 | 10 | 50 | 5 | 30 | 10 | 55.1 |
| 30 | 58 | 12 | 35 | 6 | 17 | 12 | 37.1 |
| 40 | 54.5 | 14 | 23 | 7 | 9 | 14 | 15.9 |
| 50 | 52.5 | 16 | 15 | 8 | 5 | 16 | 0 |
| 100 | 50 | 18 | 9.5 | 10 | 1 | ||
| 20 | 6 | ||||||
| 25 | 2 | ||||||
O padrão da Agência de Proteção Ambiental dos EUA (EPA 1987) para concentração de partículas no ar ambiente é conhecido como PM10, ou seja, material particulado com menos de 10 mm de diâmetro aerodinâmico. Ele tem um critério de entrada do amostrador que é semelhante (funcionalmente equivalente) ao TPM, mas, conforme mostrado na Tabela 2, especificações numéricas um pouco diferentes.
Poluentes do ar
Os poluentes podem ser dispersos no ar em temperaturas e pressões ambientes normais nas formas gasosa, líquida e sólida. Os dois últimos representam suspensões de partículas no ar e receberam o termo genérico aerossóis por Gibbs (1924) com base na analogia com o termo hidrossol, usado para descrever sistemas dispersos em água. Gases e vapores, que estão presentes como moléculas discretas, formam verdadeiras soluções no ar. Partículas que consistem em materiais de pressão de vapor moderada a alta tendem a evaporar rapidamente, porque aquelas pequenas o suficiente para permanecer suspensas no ar por mais de alguns minutos (ou seja, aquelas menores que cerca de 10 mm) têm grandes proporções superfície-volume. Alguns materiais com pressões de vapor relativamente baixas podem ter frações apreciáveis nas formas de vapor e aerossol simultaneamente.
Gases e vapores
Uma vez dispersos no ar, os gases e vapores contaminantes geralmente formam misturas tão diluídas que suas propriedades físicas (como densidade, viscosidade, entalpia e assim por diante) são indistinguíveis das do ar limpo. Tais misturas podem ser consideradas como seguindo as relações da lei dos gases ideais. Não há diferença prática entre um gás e um vapor, exceto que o último é geralmente considerado a fase gasosa de uma substância que pode existir como sólido ou líquido à temperatura ambiente. Enquanto dispersas no ar, todas as moléculas de um determinado composto são essencialmente equivalentes em tamanho e probabilidade de captura por superfícies ambientais, superfícies do trato respiratório e coletores ou amostradores de contaminantes.
Aerossóis
Os aerossóis, sendo dispersões de partículas sólidas ou líquidas no ar, têm a variável adicional muito significativa do tamanho de partícula. O tamanho afeta o movimento das partículas e, portanto, as probabilidades de fenômenos físicos como coagulação, dispersão, sedimentação, impactação em superfícies, fenômenos interfaciais e propriedades de dispersão de luz. Não é possível caracterizar uma dada partícula por um único parâmetro de tamanho. Por exemplo, as propriedades aerodinâmicas de uma partícula dependem da densidade e da forma, bem como das dimensões lineares, e o tamanho efetivo da dispersão da luz depende do índice de refração e da forma.
Em alguns casos especiais, todas as partículas são essencialmente do mesmo tamanho. Esses aerossóis são considerados monodispersos. Exemplos são pólens naturais e alguns aerossóis gerados em laboratório. Mais tipicamente, os aerossóis são compostos de partículas de muitos tamanhos diferentes e, portanto, são chamados heterodispersos ou polidispersos. Diferentes aerossóis têm diferentes graus de dispersão de tamanho. É, portanto, necessário especificar pelo menos dois parâmetros na caracterização do tamanho do aerossol: uma medida de tendência central, como uma média ou mediana, e uma medida de dispersão, como um desvio padrão aritmético ou geométrico.
Partículas geradas por uma única fonte ou processo geralmente têm diâmetros seguindo uma distribuição log-normal; isto é, os logaritmos de seus diâmetros individuais têm uma distribuição Gaussiana. Nesse caso, a medida de dispersão é o desvio padrão geométrico, que é a razão entre o tamanho do percentil 84.1 e o tamanho do percentil 50. Quando mais de uma fonte de partículas é significativa, o aerossol misto resultante geralmente não segue uma única distribuição log-normal e pode ser necessário descrevê-lo pela soma de várias distribuições.
Características das partículas
Existem muitas propriedades das partículas, além de seu tamanho linear, que podem influenciar muito seu comportamento no ar e seus efeitos no meio ambiente e na saúde. Esses incluem:
Surface. Para partículas esféricas, a superfície varia com o quadrado do diâmetro. No entanto, para um aerossol de determinada concentração de massa, a superfície total do aerossol aumenta com a diminuição do tamanho da partícula. Para partículas não esféricas ou agregadas, e para partículas com rachaduras ou poros internos, a proporção de superfície para volume pode ser muito maior do que para esferas.
Volume. O volume da partícula varia com o cubo do diâmetro; portanto, as poucas partículas maiores em um aerossol tendem a dominar sua concentração de volume (ou massa).
Forma. A forma de uma partícula afeta seu arrasto aerodinâmico, bem como sua área de superfície e, portanto, suas probabilidades de movimento e deposição.
Densidade. A velocidade de uma partícula em resposta a forças gravitacionais ou inerciais aumenta com a raiz quadrada de sua densidade.
Diâmetro aerodinâmico. O diâmetro de uma esfera de densidade unitária com a mesma velocidade de sedimentação terminal que a partícula em consideração é igual ao seu diâmetro aerodinâmico. A velocidade de sedimentação terminal é a velocidade de equilíbrio de uma partícula que está caindo sob a influência da gravidade e da resistência do fluido. O diâmetro aerodinâmico é determinado pelo tamanho real da partícula, a densidade da partícula e um fator de forma aerodinâmica.
tipos de aerossóis
Os aerossóis são geralmente classificados em termos de seus processos de formação. Embora a classificação a seguir não seja precisa nem abrangente, ela é comumente usada e aceita nos campos de higiene industrial e poluição do ar.
Poeira. Um aerossol formado pela subdivisão mecânica de material a granel em finos transportados pelo ar com a mesma composição química. As partículas de poeira são geralmente sólidas e de forma irregular e têm diâmetros superiores a 1 mm.
Fumaça. Um aerossol de partículas sólidas formado pela condensação de vapores formados por combustão ou sublimação em temperaturas elevadas. As partículas primárias são geralmente muito pequenas (menos de 0.1 mm) e têm formas cristalinas esféricas ou características. Eles podem ser quimicamente idênticos ao material original ou podem ser compostos de um produto de oxidação, como óxido de metal. Uma vez que podem ser formados em altas concentrações numéricas, muitas vezes coagulam rapidamente, formando aglomerados agregados de baixa densidade geral.
Fumaça. Aerossol formado pela condensação dos produtos da combustão, geralmente de materiais orgânicos. As partículas são geralmente gotículas líquidas com diâmetros inferiores a 0.5 mm.
Névoa. Um aerossol de gotículas formado por cisalhamento mecânico de um líquido a granel, por exemplo, por atomização, nebulização, borbulhamento ou pulverização. O tamanho da gota pode cobrir uma faixa muito grande, geralmente de cerca de 2 mm a mais de 50 mm.
Fog. Um aerossol aquoso formado pela condensação de vapor d'água em núcleos atmosféricos em altas umidades relativas. Os tamanhos das gotas são geralmente maiores que 1 mm.
fumaça Um termo popular para um aerossol de poluição derivado de uma combinação de fumaça e neblina. Agora é comumente usado para qualquer mistura de poluição atmosférica.
Neblina. Um aerossol de tamanho submicrômetro de partículas higroscópicas que absorvem vapor de água em umidades relativas relativamente baixas.
Aitken ou núcleos de condensação (CN). Partículas atmosféricas muito pequenas (na maioria menores que 0.1 mm) formadas por processos de combustão e por conversão química de precursores gasosos.
Modo de acumulação. Um termo dado às partículas na atmosfera ambiente variando de 0.1 a cerca de 1.0 mm de diâmetro. Essas partículas geralmente são esféricas (com superfícies líquidas) e se formam por coagulação e condensação de partículas menores que derivam de precursores gasosos. Sendo muito grandes para uma coagulação rápida e muito pequenos para uma sedimentação efetiva, eles tendem a se acumular no ar ambiente.
Modo de partícula grossa. Partículas de ar ambiente maiores que cerca de 2.5 mm de diâmetro aerodinâmico e geralmente formadas por processos mecânicos e ressuspensão de poeira superficial.
Respostas Biológicas do Sistema Respiratório aos Poluentes do Ar
As respostas aos poluentes atmosféricos variam de incômodo a necrose e morte dos tecidos, de efeitos sistêmicos generalizados a ataques altamente específicos a tecidos individuais. Fatores do hospedeiro e ambientais servem para modificar os efeitos dos produtos químicos inalados, e a resposta final é o resultado de sua interação. Os principais fatores do hospedeiro são:
- idade - por exemplo, pessoas idosas, especialmente aquelas com função cardiovascular e respiratória cronicamente reduzida, que podem não ser capazes de lidar com estresses pulmonares adicionais
- estado de saúde - por exemplo, doença ou disfunção concomitante
- Estado nutricional
- estado imunológico
- sexo e outros fatores genéticos - por exemplo, diferenças relacionadas a enzimas nos mecanismos de biotransformação, como vias metabólicas deficientes e incapacidade de sintetizar certas enzimas de desintoxicação
- estado psicológico – por exemplo, estresse, ansiedade e
- fatores culturais – por exemplo, tabagismo, que pode afetar as defesas normais ou potencializar o efeito de outras substâncias químicas.
Os fatores ambientais incluem a concentração, estabilidade e propriedades físico-químicas do agente no ambiente de exposição e a duração, frequência e via de exposição. Exposições agudas e crônicas a um produto químico podem resultar em diferentes manifestações patológicas.
Qualquer órgão pode responder apenas de um número limitado de maneiras, e existem vários rótulos diagnósticos para as doenças resultantes. As seções a seguir discutem os amplos tipos de respostas do sistema respiratório que podem ocorrer após a exposição a poluentes ambientais.
resposta irritante
Os irritantes produzem um padrão de inflamação tecidual generalizada e inespecífica, e a destruição pode resultar na área de contato do contaminante. Alguns irritantes não produzem efeito sistêmico porque a resposta irritante é muito maior do que qualquer efeito sistêmico, enquanto alguns também têm efeitos sistêmicos significativos após a absorção - por exemplo, sulfeto de hidrogênio absorvido pelos pulmões.
Em altas concentrações, os irritantes podem causar sensação de queimação no nariz e na garganta (e geralmente também nos olhos), dor no peito e tosse produzindo inflamação da mucosa (traqueíte, bronquite). Exemplos de irritantes são gases como cloro, flúor, dióxido de enxofre, fosgênio e óxidos de nitrogênio; névoas de ácidos ou álcalis; vapores de cádmio; poeiras de cloreto de zinco e pentóxido de vanádio. Altas concentrações de irritantes químicos também podem penetrar profundamente nos pulmões e causar edema pulmonar (os alvéolos estão cheios de líquido) ou inflamação (pneumonite química).
Concentrações altamente elevadas de poeiras que não possuem propriedades químicas irritantes também podem irritar mecanicamente os brônquios e, após entrarem no trato gastrointestinal, também podem contribuir para o câncer de estômago e cólon.
A exposição a irritantes pode resultar em morte se órgãos críticos forem gravemente danificados. Por outro lado, o dano pode ser reversível ou resultar em perda permanente de algum grau de função, como capacidade de troca gasosa prejudicada.
Resposta fibrótica
Várias poeiras levam ao desenvolvimento de um grupo de distúrbios pulmonares crônicos denominados pneumoconioses. Este termo geral abrange muitas condições fibróticas do pulmão, ou seja, doenças caracterizadas pela formação de cicatriz no tecido conjuntivo intersticial. As pneumoconioses decorrem da inalação e posterior retenção seletiva de certas poeiras nos alvéolos, de onde ficam sujeitas ao sequestro intersticial.
As pneumoconioses são caracterizadas por lesões fibróticas específicas, que diferem em tipo e padrão de acordo com a poeira envolvida. Por exemplo, a silicose, devido à deposição de sílica isenta de cristalino, é caracterizada por um tipo de fibrose nodular, enquanto uma fibrose difusa é encontrada na asbestose, devido à exposição às fibras de amianto. Certos pós, como o óxido de ferro, produzem apenas radiologia alterada (siderose) sem prejuízo funcional, enquanto os efeitos de outros vão desde uma incapacidade mínima até a morte.
Resposta alérgica
As respostas alérgicas envolvem o fenômeno conhecido como sensibilização. A exposição inicial a um alérgeno resulta na indução da formação de anticorpos; a exposição subsequente do indivíduo agora “sensibilizado” resulta em uma resposta imune – ou seja, uma reação anticorpo-antígeno (o antígeno é o alérgeno em combinação com uma proteína endógena). Essa reação imune pode ocorrer imediatamente após a exposição ao alérgeno ou pode ser uma resposta tardia.
As reações alérgicas respiratórias primárias são asma brônquica, reações no trato respiratório superior que envolvem a liberação de histamina ou mediadores semelhantes à histamina após reações imunes na mucosa e um tipo de pneumonite (inflamação pulmonar) conhecida como alveolite alérgica extrínseca. Além dessas reações locais, uma reação alérgica sistêmica (choque anafilático) pode ocorrer após a exposição a alguns alérgenos químicos.
resposta infecciosa
Agentes infecciosos podem causar tuberculose, antraz, ornitose, brucelose, histoplasmose, doença dos legionários e assim por diante.
resposta cancerígena
Câncer é um termo geral para um grupo de doenças relacionadas caracterizadas pelo crescimento descontrolado de tecidos. Seu desenvolvimento se deve a um complexo processo de interação de múltiplos fatores no hospedeiro e no ambiente.
Uma das grandes dificuldades em tentar relacionar a exposição a um agente específico ao desenvolvimento de câncer em humanos é o longo período de latência, tipicamente de 15 a 40 anos, entre o início da exposição e a manifestação da doença.
Exemplos de poluentes atmosféricos que podem produzir câncer de pulmão são o arsênico e seus compostos, cromatos, sílica, partículas contendo hidrocarbonetos aromáticos policíclicos e certas poeiras contendo níquel. As fibras de amianto podem causar câncer brônquico e mesotelioma da pleura e do peritônio. Partículas radioativas depositadas podem expor o tecido pulmonar a altas doses locais de radiação ionizante e ser a causa do câncer.
Resposta sistêmica
Muitos produtos químicos ambientais produzem uma doença sistêmica generalizada devido aos seus efeitos sobre vários locais-alvo. Os pulmões não são apenas o alvo de muitos agentes nocivos, mas o local de entrada de substâncias tóxicas que passam pelos pulmões para a corrente sanguínea sem causar danos aos pulmões. No entanto, quando distribuídos pela circulação sanguínea para vários órgãos, podem danificá-los ou causar intoxicação geral e ter efeitos sistêmicos. Este papel dos pulmões na patologia ocupacional não é objeto deste artigo. No entanto, deve ser mencionado o efeito de partículas finamente dispersas (fumos) de vários óxidos metálicos que estão frequentemente associados a uma síndrome sistêmica aguda conhecida como febre dos fumos metálicos.
Exame de Função Pulmonar
A função pulmonar pode ser medida de várias maneiras. No entanto, o objetivo das medições deve estar claro antes do exame, para que os resultados sejam interpretados corretamente. Neste artigo abordaremos o exame de função pulmonar com especial atenção ao campo ocupacional. É importante lembrar as limitações em diferentes medições da função pulmonar. Efeitos agudos temporários na função pulmonar podem não ser perceptíveis em caso de exposição a poeira fibrogênica como quartzo e amianto, mas efeitos crônicos na função pulmonar após exposição prolongada (> 20 anos) podem ser. Isso se deve ao fato de que os efeitos crônicos ocorrem anos após a poeira ser inalada e depositada nos pulmões. Por outro lado, efeitos temporários agudos de poeira orgânica e inorgânica, bem como mofo, fumaça de soldagem e exaustão de motor, são adequados para estudo. Isso se deve ao fato de que o efeito irritativo dessas poeiras ocorrerá após algumas horas de exposição. Efeitos agudos ou crônicos na função pulmonar também podem ser percebidos em casos de exposição a concentrações de gases irritantes (dióxido de nitrogênio, aldeídos, ácidos e cloretos ácidos) nas proximidades de valores-limite de exposição bem documentados, especialmente se o efeito for potencializado por contaminação do ar por partículas .
As medições da função pulmonar devem ser seguras para os indivíduos examinados e o equipamento de função pulmonar deve ser seguro para o examinador. Um resumo dos requisitos específicos para diferentes tipos de equipamentos de função pulmonar está disponível (por exemplo, Quanjer et al. 1993). Obviamente, o equipamento deve ser calibrado de acordo com padrões independentes. Isso pode ser difícil de conseguir, especialmente quando o equipamento computadorizado está sendo usado. O resultado do teste de função pulmonar depende tanto do sujeito quanto do examinador. Para obter resultados satisfatórios do exame, os técnicos devem ser bem treinados, capazes de instruir o paciente com cuidado e também incentivá-lo a realizar o teste corretamente. O examinador também deve ter conhecimento sobre as vias aéreas e pulmões para interpretar corretamente os resultados dos registros.
Recomenda-se que os métodos utilizados tenham uma reprodutibilidade razoavelmente alta entre e dentro dos indivíduos. A reprodutibilidade pode ser medida como o coeficiente de variação, ou seja, o desvio padrão multiplicado por 100 dividido pelo valor médio. Valores abaixo de 10% em medições repetidas no mesmo sujeito são considerados aceitáveis.
Para determinar se os valores medidos são patológicos ou não, eles devem ser comparados com equações de previsão. Normalmente as equações de predição para variáveis espirométricas são baseadas em idade e estatura, estratificadas por sexo. Os homens têm, em média, valores de função pulmonar mais elevados do que as mulheres, da mesma idade e altura. A função pulmonar diminui com a idade e aumenta com a altura. Um indivíduo alto terá, portanto, maior volume pulmonar do que um indivíduo baixo da mesma idade. O resultado das equações de previsão pode diferir consideravelmente entre diferentes populações de referência. A variação de idade e estatura na população de referência também influenciará os valores previstos. Isso significa, por exemplo, que uma equação de predição não deve ser usada se a idade e/ou a altura do sujeito examinado estiverem fora dos intervalos da população que é a base da equação de predição.
Fumar também diminui a função pulmonar e o efeito pode ser potencializado em indivíduos expostos ocupacionalmente a agentes irritantes. A função pulmonar costumava ser considerada não patológica se os valores obtidos estivessem dentro de 80% do valor previsto, derivado de uma equação de predição.
Medidas
As medições da função pulmonar são realizadas para julgar a condição dos pulmões. As medições podem referir-se a volumes pulmonares medidos únicos ou múltiplos ou às propriedades dinâmicas das vias aéreas e dos pulmões. Este último é geralmente determinado por meio de manobras dependentes de esforço. As condições dos pulmões também podem ser examinadas em relação à sua função fisiológica, ou seja, capacidade de difusão, resistência e complacência das vias aéreas (ver abaixo).
As medidas relativas à capacidade ventilatória são obtidas por espirometria. A manobra respiratória é geralmente realizada como uma inspiração máxima seguida de uma expiração máxima, capacidade vital (VC, medida em litros). Devem ser feitos pelo menos três registros tecnicamente satisfatórios (isto é, esforço total de inspiração e expiração e nenhum vazamento observado), e o valor mais alto relatado. O volume pode ser medido diretamente por um selo de água ou um sino de baixa resistividade, ou medido indiretamente por pneumotacografia (ou seja, integração de um sinal de fluxo ao longo do tempo). É importante observar aqui que todos os volumes pulmonares medidos devem ser expressos em BTPS, ou seja, temperatura corporal e pressão ambiente saturada com vapor de água.
A capacidade vital expirada forçada (CVF, em litros) é definida como uma medida de CV realizada com um esforço expiratório máximo forçado. Devido à simplicidade do teste e ao equipamento relativamente barato, o expirograma forçado tornou-se um teste útil na monitorização da função pulmonar. No entanto, isso resultou em muitas gravações ruins, cujo valor prático é discutível. Para realizar registros satisfatórios, a diretriz atualizada para a coleta e uso do expirograma forçado, publicada pela American Thoracic Society em 1987, pode ser útil.
Os fluxos instantâneos podem ser medidos em curvas de fluxo-volume ou fluxo-tempo, enquanto os fluxos ou tempos médios são derivados do espirograma. As variáveis associadas que podem ser calculadas a partir do expirograma forçado são o volume expirado forçado em um segundo (VEF1, em litros por segundo), em porcentagem de CVF (FEV1%), pico de fluxo (PEF, l/s), fluxos máximos a 50% e 75% da capacidade vital forçada (MEF50 e MEF25, respectivamente). Uma ilustração da derivação do FEV1 do expirograma forçado é descrito na figura 1. Em indivíduos saudáveis, as taxas de fluxo máximo em grandes volumes pulmonares (ou seja, no início da expiração) refletem principalmente as características de fluxo das grandes vias aéreas, enquanto aquelas em pequenos volumes pulmonares (ou seja, o final de expiração) são geralmente consideradas para refletir as características das pequenas vias aéreas, figura 2. Nestas o fluxo é laminar, enquanto nas grandes vias aéreas pode ser turbulento.
Figura 1. Espirograma expiratório forçado mostrando a derivação do VEF1 e CVF de acordo com o princípio da extrapolação.
Figura 2. Curva fluxo-volume mostrando a derivação do pico de fluxo expiratório (PFE), fluxos máximos a 50% e 75% da capacidade vital forçada (![]() e
e ![]() , respectivamente).
, respectivamente).
O PFE também pode ser medido por um pequeno dispositivo portátil, como o desenvolvido por Wright em 1959. Uma vantagem desse equipamento é que o sujeito pode realizar medições seriadas, por exemplo, no local de trabalho. Para obter gravações úteis, no entanto, é necessário instruir bem os sujeitos. Além disso, deve-se ter em mente que as medidas de PFE com, por exemplo, um medidor de Wright e as medidas por espirometria convencional não devem ser comparadas devido às diferentes técnicas de sopro.
As variáveis espirométricas CV, CVF e VEF1 mostram uma variação razoável entre indivíduos onde idade, altura e sexo costumam explicar 60 a 70% da variação. Distúrbios restritivos da função pulmonar resultarão em valores mais baixos para CV, CVF e VEF1. As medidas dos fluxos durante a expiração apresentam grande variação individual, pois os fluxos medidos são dependentes do esforço e do tempo. Isso significa, por exemplo, que um indivíduo terá um fluxo extremamente alto em caso de diminuição do volume pulmonar. Por outro lado, o fluxo pode ser extremamente baixo em caso de volume pulmonar muito alto. No entanto, o fluxo geralmente diminui em caso de doença obstrutiva crônica (por exemplo, asma, bronquite crônica).
Figura 3. Esquema principal do equipamento para determinação da capacidade pulmonar total (CPT) pela técnica de diluição do hélio.
A proporção do volume residual (VR), ou seja, o volume de ar que ainda está nos pulmões após uma expiração máxima, pode ser determinada pela diluição dos gases ou pela pletismografia corporal. A técnica de diluição gasosa requer equipamentos menos complicados e, portanto, mais conveniente para uso em estudos realizados no local de trabalho. Na figura 3, o princípio da técnica de diluição de gás foi delineado. A técnica é baseada na diluição de um gás indicador em um circuito de reinalação. O gás indicador deve ser pouco solúvel nos tecidos biológicos para que não seja absorvido pelos tecidos e sangue no pulmão. O hidrogênio foi inicialmente usado, mas por sua capacidade de formar misturas explosivas com o ar foi substituído pelo hélio, que é facilmente detectado por meio do princípio da condutividade térmica.
O sujeito e o aparelho formam um sistema fechado, e a concentração inicial do gás é assim reduzida quando ele é diluído no volume de gás nos pulmões. Após o equilíbrio, a concentração do gás indicador é a mesma nos pulmões e no aparelho, e a capacidade residual funcional (CRF) pode ser calculada por meio de uma equação de diluição simples. O volume do espirômetro (incluindo a adição da mistura de gases no espirômetro) é denotado por VS, VL é o volume do pulmão, Fi é a concentração inicial de gás e Ff é a concentração final.
CRF = VL = [(VS · Fi) / Ff] - VS
Duas a três manobras de VC são realizadas para fornecer uma base confiável para o cálculo do TLC (em litros). As subdivisões dos diferentes volumes pulmonares estão descritas na figura 4.
Figura 4. Espirograma rotulado para mostrar as subdivisões da capacidade total.
Devido à mudança nas propriedades elásticas das vias aéreas, o VR e a CRF aumentam com a idade. Nas doenças obstrutivas crônicas, geralmente observam-se valores aumentados de VR e CRF, enquanto a CV está diminuída. No entanto, em indivíduos com áreas pulmonares mal ventiladas - por exemplo, indivíduos com enfisema - a técnica de diluição de gás pode subestimar VR, CRF e também CPT. Isso se deve ao fato de que o gás indicador não se comunicará com vias aéreas fechadas e, portanto, a diminuição na concentração do gás indicador fornecerá valores erroneamente pequenos.
Figura 5. Um esboço principal do registro do fechamento das vias aéreas e da inclinação do platô alveolar (%![]() ).
).
Medidas de fechamento de vias aéreas e distribuição de gás nos pulmões podem ser obtidas em uma mesma manobra pela técnica de lavagem de respiração única, figura 5. O equipamento consiste em um espirômetro conectado a um sistema bag-in-box e um registrador para medições contínuas da concentração de nitrogênio. A manobra é realizada por meio de uma inspiração máxima de oxigênio puro da bolsa. No início da expiração, a concentração de nitrogênio aumenta em decorrência do esvaziamento do espaço morto do sujeito, contendo oxigênio puro. A expiração continua com o ar das vias aéreas e alvéolos. Finalmente, o ar dos alvéolos, contendo 20 a 40% de nitrogênio, é expirado. Quando a expiração das partes basais dos pulmões aumenta, a concentração de nitrogênio aumentará abruptamente em caso de fechamento das vias aéreas em regiões pulmonares dependentes, figura 5. Esse volume acima do VD, no qual as vias aéreas se fecham durante uma expiração, geralmente é expresso como volume de fechamento (CV) em percentual de VC (CV%). A distribuição do ar inspirado nos pulmões é expressa como a inclinação do platô alveolar (%N2 ou fase III, %N2/eu). É obtido tomando-se a diferença da concentração de nitrogênio entre o ponto em que 30% do ar é expirado e o ponto de fechamento das vias aéreas, dividindo-se pelo volume correspondente.
O envelhecimento, bem como os distúrbios obstrutivos crônicos, resultarão em valores aumentados para CV% e fase III. No entanto, nem mesmo indivíduos saudáveis apresentam uma distribuição uniforme de gases nos pulmões, resultando em valores ligeiramente elevados para a fase III, ou seja, 1 a 2% de N2/eu. As variáveis CV% e fase III são consideradas para refletir as condições nas pequenas vias aéreas periféricas com diâmetro interno de cerca de 2 mm. Normalmente, as vias aéreas periféricas contribuem com uma pequena parte (10 a 20%) da resistência total das vias aéreas. Alterações bastante extensas que não são detectáveis por testes de função pulmonar convencionais, como a espirometria dinâmica, podem ocorrer, por exemplo, como resultado de uma exposição a substâncias irritantes no ar nas vias aéreas periféricas. Isso sugere que a obstrução das vias aéreas começa nas pequenas vias aéreas. Os resultados dos estudos também mostraram alterações no CV% e na fase III antes de ocorrer qualquer alteração da espirometria dinâmica e estática. Essas alterações iniciais podem entrar em remissão quando a exposição a agentes perigosos cessar.
O fator de transferência do pulmão (mmol/min; kPa) é uma expressão da capacidade de difusão do transporte de oxigênio para os capilares pulmonares. O fator de transferência pode ser determinado usando técnicas de respiração única ou múltipla; a técnica de respiração única é considerada a mais adequada em estudos no local de trabalho. O monóxido de carbono (CO) é usado porque a contrapressão do CO é muito baixa no sangue periférico, em contraste com a do oxigênio. Supõe-se que a absorção de CO segue um modelo exponencial, e essa suposição pode ser usada para determinar o fator de transferência para o pulmão.
Determinação de TLCO (fator de transferência medido com CO) é realizada por meio de uma manobra respiratória incluindo uma expiração máxima, seguida de uma inspiração máxima de uma mistura gasosa contendo monóxido de carbono, hélio, oxigênio e nitrogênio. Após um período de apneia, é feita uma expiração máxima, refletindo o conteúdo no ar alveolar, Figura 10. O hélio é usado para a determinação do volume alveolar (VA). Assumindo que a diluição de CO é a mesma do hélio, a concentração inicial de CO, antes do início da difusão, pode ser calculada. TLCO é calculado de acordo com a equação abaixo, onde k depende das dimensões dos termos componentes, t é o tempo efetivo para prender a respiração e log é o logaritmo de base 10. O volume inspirado é denotado Vi e as frações F de CO e hélio são representados por i e a para inspirado e alveolar, respectivamente.
TLCO = k Vi (Fa,Ele/Fi,He) registro (Fi,CO Fa,He/Fa, CO Fi,Ele) (t)-1
Figura 6. Um esboço principal do registro do fator de transferência
O tamanho de TLCO dependerá de uma variedade de condições - por exemplo, a quantidade de hemoglobina disponível, o volume de alvéolos ventilados e capilares pulmonares perfundidos e sua relação entre si. Valores para TLCO diminuem com a idade e aumentam com a atividade física e aumento dos volumes pulmonares. diminuiu TLCO serão encontrados em doenças pulmonares restritivas e obstrutivas.
A complacência (l/kPa) é uma função, inter alia, da propriedade elástica dos pulmões. Os pulmões têm uma tendência intrínseca de colaborar - isto é, de colapsar. A capacidade de manter os pulmões alongados dependerá do tecido pulmonar elástico, da tensão superficial nos alvéolos e da musculatura brônquica. Por outro lado, a parede torácica tende a se expandir em volumes pulmonares de 1 a 2 litros acima do nível da CRF. Em volumes pulmonares mais altos, a força deve ser aplicada para expandir ainda mais a parede torácica. No nível da CRF, a tendência correspondente nos pulmões é equilibrada pela tendência de expansão. O nível de CRF é, portanto, denotado pelo nível de repouso do pulmão.
A complacência do pulmão é definida como a variação do volume dividida pela variação da pressão transpulmonar, ou seja, a diferença entre as pressões na boca (atmosférica) e no pulmão, como resultado de uma manobra respiratória. As medições da pressão no pulmão não são facilmente realizadas e, portanto, são substituídas por medições da pressão no esôfago. A pressão no esôfago é quase igual à pressão no pulmão e é medida com um fino cateter de polietileno com um balão cobrindo os 10 cm distais. Durante as manobras inspiratórias e expiratórias, as mudanças de volume e pressão são registradas por meio de um espirômetro e transdutor de pressão, respectivamente. Quando as medições são realizadas durante a respiração corrente, a complacência dinâmica pode ser medida. A complacência estática é obtida quando uma manobra lenta de VC é realizada. Neste último caso, as medidas são realizadas em um pletismógrafo corporal e a expiração é interrompida intermitentemente por meio de um obturador. No entanto, as medições de complacência são difíceis de realizar ao examinar os efeitos da exposição na função pulmonar no local de trabalho, e essa técnica é considerada mais apropriada no laboratório.
Uma complacência diminuída (elasticidade aumentada) é observada na fibrose. Para causar uma mudança no volume, grandes mudanças na pressão são necessárias. Por outro lado, observa-se uma alta complacência, por exemplo, no enfisema como resultado da perda de tecido elástico e, portanto, também da elasticidade no pulmão.
A resistência nas vias aéreas depende essencialmente do raio e comprimento das vias aéreas, mas também da viscosidade do ar. A resistência das vias aéreas (RL em (kPa/l) /s), pode ser determinado pelo uso de um espirômetro, transdutor de pressão e um pneumotacógrafo (para medir o fluxo). As medições também podem ser realizadas usando um pletismógrafo corporal para registrar as mudanças no fluxo e na pressão durante as manobras ofegantes. Pela administração de um medicamento destinado a causar broncoconstrição, podem ser identificados indivíduos sensíveis, como resultado de suas vias aéreas hiper-reativas. Indivíduos com asma geralmente têm valores aumentados para RL.
Efeitos agudos e crônicos da exposição ocupacional na função pulmonar
A medição da função pulmonar pode ser usada para revelar um efeito de exposição ocupacional nos pulmões. O exame pré-emprego da função pulmonar não deve ser usado para excluir indivíduos em busca de emprego. Isso ocorre porque a função pulmonar de indivíduos saudáveis varia dentro de amplos limites e é difícil traçar um limite abaixo do qual se pode afirmar com segurança que o pulmão é patológico. Outra razão é que o ambiente de trabalho deve ser bom o suficiente para permitir que até mesmo indivíduos com leve comprometimento da função pulmonar trabalhem com segurança.
Os efeitos crônicos nos pulmões em indivíduos expostos ocupacionalmente podem ser detectados de várias maneiras. As técnicas são projetadas para determinar os efeitos históricos, no entanto, e são menos adequadas para servir como diretrizes para prevenir o comprometimento da função pulmonar. Um projeto de estudo comum é comparar os valores reais em indivíduos expostos com os valores de função pulmonar obtidos em uma população de referência sem exposição ocupacional. Os sujeitos de referência podem ser recrutados nos mesmos locais de trabalho (ou próximos) ou na mesma cidade.
A análise multivariada tem sido usada em alguns estudos para avaliar as diferenças entre os sujeitos expostos e os correspondentes não expostos. Os valores de função pulmonar em indivíduos expostos também podem ser padronizados por meio de uma equação de referência baseada nos valores de função pulmonar em indivíduos não expostos.
Outra abordagem é estudar a diferença entre os valores de função pulmonar em trabalhadores expostos e não expostos após ajuste para idade e estatura com o uso de valores de referência externos, calculados por meio de uma equação de predição baseada em indivíduos saudáveis. A população de referência também pode ser combinada com os indivíduos expostos de acordo com grupo étnico, sexo, idade, altura e hábitos tabágicos, a fim de controlar ainda mais os fatores que influenciam.
O problema é, no entanto, decidir se uma diminuição é grande o suficiente para ser classificada como patológica, quando valores de referência externos estão sendo usados. Embora os instrumentos dos estudos devam ser portáteis e simples, deve-se atentar tanto para a sensibilidade do método escolhido para detectar pequenas anomalias em vias aéreas e pulmões quanto para a possibilidade de combinação de diferentes métodos. Há indícios de que indivíduos com sintomas respiratórios, como dispneia de esforço, correm maior risco de apresentar um declínio acelerado da função pulmonar. Isso significa que a presença de sintomas respiratórios é importante e, portanto, não deve ser negligenciada.
O sujeito também pode ser acompanhado por espirometria, por exemplo, uma vez por ano, durante vários anos, a fim de alertar contra o desenvolvimento de doenças. Existem limitações, no entanto, uma vez que isso será muito demorado e a função pulmonar pode ter se deteriorado permanentemente quando a diminuição pode ser observada. Esta abordagem, portanto, não deve ser uma desculpa para o atraso na execução de medidas destinadas a diminuir as concentrações nocivas de poluentes atmosféricos.
Finalmente, os efeitos crônicos na função pulmonar também podem ser estudados examinando as mudanças individuais na função pulmonar em indivíduos expostos e não expostos ao longo de vários anos. Uma vantagem do desenho do estudo longitudinal é que a variabilidade intersujeitos é eliminada; no entanto, o projeto é considerado demorado e caro.
Indivíduos suscetíveis também podem ser identificados comparando sua função pulmonar com e sem exposição durante os turnos de trabalho. A fim de minimizar os possíveis efeitos das variações diurnas, a função pulmonar é medida na mesma hora do dia em uma ocasião não exposta e outra exposta. A condição não exposta pode ser obtida, por exemplo, movendo ocasionalmente o trabalhador para uma área não contaminada ou pelo uso de um respirador adequado durante todo o turno ou, em alguns casos, realizando medições da função pulmonar na tarde do dia de folga do trabalhador.
Uma preocupação especial é que efeitos repetidos e temporários podem resultar em efeitos crônicos. Uma diminuição temporária aguda da função pulmonar pode ser não apenas um indicador de exposição biológica, mas também um preditor de uma diminuição crônica da função pulmonar. A exposição a poluentes atmosféricos pode resultar em efeitos agudos perceptíveis na função pulmonar, embora os valores médios dos poluentes atmosféricos medidos estejam abaixo dos valores-limite higiênicos. Surge então a questão de saber se esses efeitos são realmente prejudiciais a longo prazo. Esta questão é difícil de responder diretamente, especialmente porque a poluição do ar nos locais de trabalho geralmente tem uma composição complexa e a exposição não pode ser descrita em termos de concentrações médias de compostos individuais. O efeito de uma exposição ocupacional também se deve, em parte, à sensibilidade do indivíduo. Isso significa que alguns sujeitos reagirão mais cedo ou em maior grau do que outros. A base fisiopatológica subjacente para uma diminuição aguda e temporária da função pulmonar não é totalmente compreendida. A reação adversa à exposição a um contaminante irritante do ar é, no entanto, uma medida objetiva, em contraste com experiências subjetivas como sintomas de origem diferente.
A vantagem de detectar alterações precoces nas vias aéreas e nos pulmões causadas por poluentes atmosféricos perigosos é óbvia – a exposição predominante pode ser reduzida para prevenir doenças mais graves. Portanto, um objetivo importante a esse respeito é usar as medições de efeitos temporários agudos na função pulmonar como um sistema de alerta precoce sensível que pode ser usado ao estudar grupos de trabalhadores saudáveis.
Monitoramento de Irritantes
A irritação é um dos critérios mais frequentes para definir valores-limite de exposição. No entanto, não é certo que o cumprimento de um limite de exposição baseado em irritação proteja contra irritação. Deve-se considerar que um limite de exposição para um contaminante do ar geralmente contém pelo menos duas partes - um limite de média ponderada no tempo (TWAL) e um limite de exposição de curto prazo (STEL), ou pelo menos regras para exceder a média ponderada no tempo limite, “limites de excursão”. No caso de substâncias altamente irritantes, como dióxido de enxofre, acroleína e fosgênio, é importante limitar a concentração mesmo durante períodos muito curtos e, portanto, tem sido prática comum fixar valores-limite de exposição ocupacional na forma de limites máximos, com um período de amostragem tão curto quanto as instalações de medição permitirem.
Os valores-limite médios ponderados pelo tempo para um dia de oito horas combinados com regras para excursão acima desses valores são fornecidos para a maioria das substâncias na lista de valores-limite (TLV) da Conferência Americana de Higienistas Industriais Governamentais (ACGIH). A lista TLV de 1993-94 contém a seguinte declaração sobre os limites de excursão para exceder os valores limite:
“Para a grande maioria das substâncias com um TLV-TWA, não há dados toxicológicos suficientes disponíveis para justificar um STEL = limite de exposição de curto prazo). No entanto, as excursões acima do TLV-TWA devem ser controladas mesmo quando o TWA de oito horas estiver dentro dos limites recomendados.”
Medições de exposição de contaminantes do ar conhecidos e comparação com valores-limite de exposição bem documentados devem ser realizadas rotineiramente. Existem, no entanto, muitas situações em que a determinação do cumprimento dos valores-limite de exposição não é suficiente. Este é o caso nas seguintes circunstâncias (entre outras):
- quando o valor limite é muito alto para proteção contra irritação
- quando o irritante é desconhecido
- quando o irritante é uma mistura complexa e não há indicador adequado conhecido.
Conforme defendido acima, a medição dos efeitos agudos e temporários na função pulmonar pode ser usada nesses casos como um alerta contra a superexposição a irritantes.
Nos casos (2) e (3), efeitos agudos e temporários na função pulmonar também podem ser aplicados ao testar a eficiência de medidas de controle para diminuir a exposição à contaminação do ar ou em investigações científicas, por exemplo, ao atribuir efeitos biológicos a componentes do ar contaminantes. Seguem-se vários exemplos nos quais efeitos agudos e temporários da função pulmonar foram empregados com sucesso em investigações de saúde ocupacional.
Estudos de efeitos agudos e temporários da função pulmonar
A diminuição temporária da função pulmonar relacionada ao trabalho durante um turno de trabalho foi registrada em trabalhadores do algodão no final de 1950. Mais tarde, vários autores relataram alterações agudas e temporárias relacionadas ao trabalho da função pulmonar em trabalhadores têxteis e de cânhamo, mineiros de carvão, trabalhadores expostos a diisocianato de tolueno, bombeiros, trabalhadores de processamento de borracha, moldadores e coremakers, soldadores, enceradores de esqui, trabalhadores expostos a poeira orgânica e irritantes em tintas à base de água.
No entanto, também existem vários exemplos em que as medições antes e depois da exposição, geralmente durante um turno, falharam em demonstrar quaisquer efeitos agudos, apesar de uma alta exposição. Isso provavelmente se deve ao efeito da variação circadiana normal, principalmente nas variáveis da função pulmonar, dependendo do tamanho do calibre das vias aéreas. Assim, a diminuição temporária dessas variáveis deve exceder a variação circadiana normal para ser reconhecida. O problema pode ser contornado, no entanto, medindo a função pulmonar na mesma hora do dia em cada ocasião do estudo. Ao usar o funcionário exposto como seu próprio controle, a variação interindividual diminui ainda mais. Os soldadores foram estudados dessa maneira e, embora a diferença média entre os valores de CVF não expostos e expostos fosse inferior a 3% em 15 soldadores examinados, essa diferença foi significativa no nível de confiança de 95% com um poder de mais de 99%.
Os efeitos transitórios reversíveis nos pulmões podem ser usados como um indicador de exposição de componentes irritantes complicados. No estudo citado acima, as partículas no ambiente de trabalho foram cruciais para os efeitos irritantes nas vias aéreas e nos pulmões. As partículas foram removidas por um respirador composto por um filtro combinado com um capacete de soldagem. Os resultados indicaram que os efeitos nos pulmões foram causados pelas partículas nos fumos de soldagem e que o uso de um respirador particulado pode prevenir esse efeito.
A exposição à exaustão de diesel também causa efeitos irritantes mensuráveis nos pulmões, mostrados como uma diminuição aguda e temporária da função pulmonar. Filtros mecânicos montados nos canos de escapamento de caminhões usados em operações de carregamento por estivadores aliviavam distúrbios subjetivos e reduziam a diminuição aguda e temporária da função pulmonar observada quando nenhuma filtração era feita. Os resultados indicam, portanto, que a presença de partículas no ambiente de trabalho desempenha um papel no efeito irritativo nas vias aéreas e nos pulmões, e que é possível avaliar o efeito por meio de medições de alterações agudas na função pulmonar.
Uma multiplicidade de exposições e um ambiente de trabalho em constante mudança podem apresentar dificuldades em discernir a relação causal dos diferentes agentes existentes em um ambiente de trabalho. O cenário de exposição em serrarias é um exemplo esclarecedor. Não é possível (por exemplo, por razões econômicas) realizar medições de exposição de todos os agentes possíveis (terpenos, poeira, mofo, bactérias, endotoxinas, micotoxinas, etc.) neste ambiente de trabalho. Um método viável pode ser acompanhar o desenvolvimento da função pulmonar longitudinalmente. Em um estudo com trabalhadores de serraria no departamento de corte de madeira, a função pulmonar foi examinada antes e depois de uma semana de trabalho, e nenhuma diminuição estatisticamente significativa foi encontrada. No entanto, um estudo de acompanhamento realizado alguns anos depois revelou que os trabalhadores que realmente tiveram uma diminuição numérica na função pulmonar durante uma semana de trabalho também tiveram um declínio acelerado de longo prazo na função pulmonar. Isso pode indicar que indivíduos vulneráveis podem ser detectados medindo as mudanças na função pulmonar durante uma semana de trabalho.
Doenças Causadas por Irritantes Respiratórios e Produtos Químicos Tóxicos
A presença de irritantes respiratórios no local de trabalho pode ser desagradável e causar distração, levando ao desânimo e à diminuição da produtividade. Certas exposições são perigosas, até letais. Em ambos os extremos, é comum o problema de irritantes respiratórios e produtos químicos tóxicos inalados; muitos trabalhadores enfrentam uma ameaça diária de exposição. Esses compostos causam danos por uma variedade de mecanismos diferentes, e a extensão da lesão pode variar amplamente, dependendo do grau de exposição e das propriedades bioquímicas do inalante. No entanto, todos eles têm a característica de inespecificidade; isto é, acima de um certo nível de exposição, praticamente todas as pessoas experimentam uma ameaça à sua saúde.
Existem outras substâncias inaladas que causam problemas respiratórios apenas em indivíduos suscetíveis; tais queixas são mais apropriadamente abordadas como doenças de origem alérgica e imunológica. Certos compostos, como isocianatos, anidridos ácidos e resinas epóxi, podem atuar não apenas como irritantes não específicos em altas concentrações, mas também podem predispor certos indivíduos à sensibilização alérgica. Esses compostos provocam sintomas respiratórios em indivíduos sensibilizados em concentrações muito baixas.
Irritantes respiratórios incluem substâncias que causam inflamação das vias aéreas após serem inaladas. Danos podem ocorrer nas vias aéreas superiores e inferiores. Mais perigosa é a inflamação aguda do parênquima pulmonar, como na pneumonia química ou no edema pulmonar não cardiogênico. Os compostos que podem causar danos ao parênquima são considerados produtos químicos tóxicos. Muitos produtos químicos tóxicos inalados também atuam como irritantes respiratórios, alertando-nos de seu perigo com seu odor nocivo e sintomas de irritação do nariz e garganta e tosse. A maioria dos irritantes respiratórios também são tóxicos para o parênquima pulmonar se inalados em quantidade suficiente.
Muitas substâncias inaladas têm efeitos tóxicos sistêmicos após serem absorvidas por inalação. Efeitos inflamatórios no pulmão podem estar ausentes, como no caso de chumbo, monóxido de carbono ou cianeto de hidrogênio. Inflamação pulmonar mínima é normalmente observada no febres de inalação (por exemplo, síndrome da poeira orgânica tóxica, febre da fumaça de metal e febre da fumaça de polímero). Danos graves aos pulmões e órgãos distais ocorrem com exposição significativa a toxinas como cádmio e mercúrio.
As propriedades físicas das substâncias inaladas preveem o local de deposição; irritantes produzirão sintomas nesses locais. Partículas grandes (10 a 20mm) depositam-se no nariz e vias aéreas superiores, partículas menores (5 a 10mm) depositam-se na traqueia e brônquios, e partículas menores que 5mm podem atingir os alvéolos. Partículas com menos de 0.5 mm são tão pequenas que se comportam como gases. Os gases tóxicos depositam-se de acordo com a sua solubilidade. Um gás solúvel em água será adsorvido pela mucosa úmida da via aérea superior; gases menos solúveis se depositarão mais aleatoriamente ao longo do trato respiratório.
Irritantes respiratórios
Irritantes respiratórios causam inflamação não específica do pulmão após serem inalados. Essas substâncias, suas fontes de exposição, propriedades físicas e outras, e efeitos sobre a vítima são descritos na Tabela 1. Os gases irritantes tendem a ser mais solúveis em água do que os gases mais tóxicos para o parênquima pulmonar. Os vapores tóxicos são mais perigosos quando têm um alto limiar de irritação; ou seja, há poucos avisos de que a fumaça está sendo inalada porque há pouca irritação.
Tabela 1. Resumo dos irritantes respiratórios
|
Produtos Químicos |
Fontes de exposição |
Propriedades importantes |
Lesão produzida |
Nível de exposição perigosa abaixo de 15 min (PPM) |
|
Acetaldeído |
Plásticos, indústria de borracha sintética, produtos de combustão |
Alta pressão de vapor; alta solubilidade em água |
Lesão das vias aéreas superiores; raramente causa edema pulmonar tardio |
|
|
Ácido acético, ácidos orgânicos |
Indústria química, eletrônica, produtos de combustão |
solúvel em água |
Lesão ocular e das vias aéreas superiores |
|
|
Anidridos ácidos |
Indústrias químicas, de tintas e de plásticos; componentes de resinas epóxi |
Solúvel em água, altamente reativo, pode causar sensibilização alérgica |
Ocular, lesão das vias aéreas superiores, broncoespasmo; hemorragia pulmonar após exposição maciça |
|
|
Acroleína |
Plásticos, têxteis, indústria farmacêutica, produtos de combustão |
Alta pressão de vapor, solubilidade intermediária em água, extremamente irritante |
Lesão difusa das vias aéreas e do parênquima |
|
|
Amônia |
Fabricação de fertilizantes, ração animal, produtos químicos e farmacêuticos |
Gás alcalino, solubilidade em água muito alta |
Queimadura principalmente ocular e das vias aéreas superiores; exposição maciça pode causar bronquiectasia |
500 |
|
Tricloreto de antimônio, pentacloreto de antimônio |
Ligas, catalisadores orgânicos |
Pouco solúvel, lesão provavelmente devido ao íon haleto |
Pneumonite, edema pulmonar não cardiogênico |
|
|
Berílio |
Ligas (com cobre), cerâmica; equipamentos eletrônicos, aeroespaciais e de reatores nucleares |
Metal irritante, também atua como um antígeno para promover uma resposta granulomatosa de longo prazo |
Lesão aguda das vias aéreas superiores, traqueobronquite, pneumonite química |
25 μg/m3 |
|
Boranos (diborano) |
Combustível para aeronaves, fabricação de fungicidas |
Gás solúvel em água |
Lesão das vias aéreas superiores, pneumonite com exposição maciça |
|
|
Brometo de hidrogênio |
refinamento de petróleo |
Lesão das vias aéreas superiores, pneumonite com exposição maciça |
||
|
Brometo de metilo |
Refrigeração, produção de fumigação |
Gás moderadamente solúvel |
Lesão das vias aéreas superiores e inferiores, pneumonite, depressão do SNC e convulsões |
|
|
Cádmio |
Ligas com Zn e Pb, galvanoplastia, baterias, inseticidas |
Efeitos respiratórios agudos e crônicos |
Traqueobronquite, edema pulmonar (frequentemente com início tardio em 24–48 horas); exposição crônica de baixo nível leva a alterações inflamatórias e enfisema |
100 |
|
Óxido de cálcio, hidróxido de cálcio |
Cal, fotografia, bronzeamento, inseticidas |
Moderadamente cáustico, doses muito altas necessárias para toxicidade |
Inflamação das vias aéreas superiores e inferiores, pneumonite |
|
|
Cloro |
Branqueamento, formação de compostos clorados, produtos de limpeza doméstica |
Solubilidade intermediária em água |
Inflamação das vias aéreas superiores e inferiores, pneumonite e edema pulmonar não cardiogênico |
5-10 |
|
cloroacetofenona |
Agente de controle de multidão, “gás lacrimogêneo” |
Qualidades irritantes são usadas para incapacitar; agente alquilante |
Inflamação ocular e das vias aéreas superiores, vias aéreas inferiores e lesão do parênquima com exposição maciça |
1-10 |
|
o-Clorobenzomalo-nitrilo |
Agente de controle de multidão, “gás lacrimogêneo” |
Qualidades irritantes são usadas para incapacitar |
Inflamação ocular e das vias aéreas superiores, lesão das vias aéreas inferiores com exposição maciça |
|
|
éteres clorometílicos |
Solventes, usados na fabricação de outros compostos orgânicos |
Irritação das vias aéreas superiores e inferiores, também um carcinógeno do trato respiratório |
||
|
chloropicrin |
Fabricação química, componente fumigante |
Ex-gás da Primeira Guerra Mundial |
Inflamação das vias aéreas superiores e inferiores |
15 |
|
Ácido crômico (Cr(IV)) |
Soldagem, chapeamento |
Irritante solúvel em água, sensibilizador alérgico |
Inflamação e ulceração nasal, rinite, pneumonite com exposição maciça |
|
|
Cobalto |
Ligas de alta temperatura, ímãs permanentes, ferramentas de metal duro (com carboneto de tungstênio) |
Irritante não específico, também sensibilizador alérgico |
Broncoespasmo agudo e/ou pneumonite; exposição crônica pode causar fibrose pulmonar |
|
|
Formaldeído |
Fabricação de espumas isolantes, compensados, têxteis, papel, fertilizantes, resinas; agentes de embalsamamento; produtos de combustão |
Altamente solúvel em água, rapidamente metabolizado; atua principalmente através da estimulação do nervo sensorial; sensibilização relatada |
Irritação ocular e das vias aéreas superiores; broncoespasmo em exposição grave; dermatite de contato em pessoas sensibilizadas |
3 |
|
Ácido clorídrico |
Refino de metais, fabricação de borracha, fabricação de compostos orgânicos, materiais fotográficos |
Altamente solúvel em água |
Inflamação ocular e das vias aéreas superiores, inflamação das vias aéreas inferiores apenas com exposição maciça |
100 |
|
Acido hidrosulfurico |
Catalisador químico, pesticidas, branqueamento, soldagem, corrosão |
Altamente solúvel em água, poderoso e rápido oxidante, reduz o cálcio sérico em exposição massiva |
Inflamação ocular e das vias aéreas superiores, traqueobronquite e pneumonite com exposição maciça |
20 |
|
Isocianatos |
Produção de poliuretano; tintas; produtos herbicidas e inseticidas; laminação, móveis, esmaltação, trabalhos em resina |
Compostos orgânicos de baixo peso molecular, irritantes, causam sensibilização em pessoas susceptíveis |
Inflamação ocular, superior e inferior; asma, pneumonite de hipersensibilidade em pessoas sensibilizadas |
0.1 |
|
Hidreto de lítio |
Ligas, cerâmica, eletrônica, catalisadores químicos |
Baixa solubilidade, altamente reativo |
Pneumonite, edema pulmonar não cardiogênico |
|
|
Mercúrio |
Eletrólise, extração de minério e amálgama, fabricação de eletrônicos |
Sem sintomas respiratórios com baixo nível, exposição crônica |
Inflamação ocular e do trato respiratório, pneumonite, SNC, rins e efeitos sistêmicos |
1.1 mg/m3 |
|
níquel carbonil |
Refino de níquel, galvanoplastia, reagentes químicos |
Toxina potente |
Irritação do trato respiratório inferior, pneumonite, efeitos tóxicos sistêmicos retardados |
8 μg/m3 |
|
Dióxido de nitrogênio |
Silos após novo armazenamento de grãos, fabricação de fertilizantes, soldagem a arco, produtos de combustão |
Baixa solubilidade em água, gás marrom em alta concentração |
Inflamação ocular e das vias aéreas superiores, edema pulmonar não cardiogênico, bronquiolite de início tardio |
50 |
|
Mostardas nitrogenadas; mostardas de enxofre |
gases militares |
Causa lesões graves, propriedades vesicantes |
Inflamação ocular, das vias aéreas superiores e inferiores, pneumonite |
20mg / m3 (N) 1 mg/m3 Diversidade, Igualdade e Compromisso para com a Sociedade |
|
Tetróxido de ósmio |
Refino de cobre, liga com irídio, catalisador para síntese de esteroides e formação de amônia |
O ósmio metálico é inerte, o tetróxido se forma quando aquecido ao ar |
Irritação severa ocular e das vias aéreas superiores; dano renal transitório |
1 mg/m3 |
|
ozono |
Soldagem a arco, copiadoras, branqueamento de papel |
Gás de cheiro doce, solubilidade moderada em água |
Inflamação das vias aéreas superiores e inferiores; asmáticos mais suscetíveis |
1 |
|
Fosgênio |
Fabricação de pesticidas e outros produtos químicos, soldagem a arco, remoção de tinta |
Pouco solúvel em água, não irrita as vias respiratórias em doses baixas |
inflamação das vias aéreas superiores e pneumonite; edema pulmonar tardio em doses baixas |
2 |
|
Sulfetos fosfóricos |
Produção de inseticidas, compostos de ignição, fósforos |
Inflamação ocular e das vias aéreas superiores |
||
|
Cloretos fosfóricos |
Fabricação de compostos orgânicos clorados, corantes, aditivos para gasolina |
Forma ácido fosfórico e ácido clorídrico em contato com superfícies mucosas |
Inflamação ocular e das vias aéreas superiores |
10 mg/m3 |
|
Dióxido de selênio |
Fundição de cobre ou níquel, aquecimento de ligas de selênio |
Vessicante forte, forma ácido selenioso (H2SeO3) em superfícies mucosas |
Inflamação ocular e das vias aéreas superiores, edema pulmonar em exposição maciça |
|
|
Seleneto de hidrogênio |
Refino de cobre, produção de ácido sulfúrico |
Solúvel em água; exposição a compostos de selênio dá origem a hálito com odor de alho |
Inflamação ocular e das vias aéreas superiores, edema pulmonar tardio |
|
|
Estireno |
Fabricação de poliestireno e resinas, polímeros |
Altamente irritante |
Inflamação ocular, das vias aéreas superiores e inferiores, comprometimentos neurológicos |
600 |
|
Dióxido de enxofre |
Refino de petróleo, fábricas de celulose, plantas de refrigeração, fabricação de sulfito de sódio |
Gás altamente solúvel em água |
Inflamação das vias aéreas superiores, broncoconstrição, pneumonite em exposição maciça |
100 |
|
Tetracloreto de titânio |
Corantes, pigmentos, escrita do céu |
Os íons cloreto formam HCl na mucosa |
Lesão das vias aéreas superiores |
|
|
Hexafluoreto de urânio |
Removedores de revestimento de metal, selantes de piso, tintas em spray |
Toxicidade provável de íons de cloreto |
Lesão das vias aéreas superiores e inferiores, broncoespasmo, pneumonite |
|
|
Pentóxido de vanádio |
Limpeza de tanques de óleo, metalurgia |
Sintomas oculares, das vias aéreas superiores e inferiores |
70 |
|
|
Cloreto de zinco |
Granadas de fumaça, artilharia |
Mais grave do que a exposição ao óxido de zinco |
Irritação das vias aéreas superiores e inferiores, febre, pneumonia de início tardio |
200 |
|
Tetracloreto de zircônio |
Pigmentos, catalisadores |
Toxicidade do íon cloreto |
Irritação das vias aéreas superiores e inferiores, pneumonite |
Acredita-se que essa condição resulte de inflamação persistente com redução da permeabilidade da camada de células epiteliais ou limiar de condutância reduzido para terminações nervosas subepiteliais. Adaptado de Sheppard 1988; Graham 1994; Rom 1992; Blanc e Schwartz 1994; Nemery 1990; Skornik 1988.
A natureza e extensão da reação a um irritante depende das propriedades físicas do gás ou aerossol, da concentração e tempo de exposição, e também de outras variáveis, como temperatura, umidade e presença de patógenos ou outros gases (Man e Hulbert 1988). Fatores do hospedeiro, como idade (Cabral-Anderson, Evans e Freeman 1977; Evans, Cabral-Anderson e Freeman 1977), exposição prévia (Tyler, Tyler e Last 1988), nível de antioxidantes (McMillan e Boyd 1982) e presença de infecção podem desempenham um papel na determinação das alterações patológicas observadas. Essa ampla gama de fatores dificulta o estudo sistemático dos efeitos patogênicos dos irritantes respiratórios.
Os irritantes mais bem compreendidos são aqueles que infligem lesão oxidativa. A maioria dos irritantes inalados, incluindo os principais poluentes, agem por oxidação ou dão origem a compostos que agem dessa forma. A maioria dos vapores de metal são na verdade óxidos do metal aquecido; esses óxidos causam lesão oxidativa. Os oxidantes danificam as células principalmente por peroxidação lipídica, e pode haver outros mecanismos. Em um nível celular, há inicialmente uma perda bastante específica de células ciliadas do epitélio das vias aéreas e de células epiteliais alveolares tipo I, com subsequente violação da interface de junção apertada entre as células epiteliais (Man e Hulbert 1988; Gordon, Salano e Kleinerman 1986 ; Stephens et al. 1974). Isso leva a danos subepiteliais e submucosos, com estimulação do músculo liso e das terminações nervosas aferentes sensoriais parassimpáticas, causando broncoconstrição (Holgate, Beasley e Twentyman 1987; Boucher 1981). Segue-se uma resposta inflamatória (Hogg 1981), e os neutrófilos e eosinófilos liberam mediadores que causam mais dano oxidativo (Castleman et al. 1980). Os pneumócitos tipo II e as células cubóides atuam como células-tronco para reparo (Keenan, Combs e McDowell 1982; Keenan, Wilson e McDowell 1983).
Outros mecanismos de lesão pulmonar eventualmente envolvem a via oxidativa do dano celular, particularmente após o dano à camada celular epitelial protetora ter ocorrido e uma resposta inflamatória ter sido provocada. Os mecanismos mais comumente descritos são descritos na tabela 2.
Tabela 2. Mecanismos de lesão pulmonar por substâncias inaladas
|
Mecanismo de lesão |
Exemplos de compostos |
Danos que ocorrem |
|
Oxidação |
Ozônio, dióxido de nitrogênio, dióxido de enxofre, cloro, óxidos |
Danos epiteliais irregulares das vias aéreas, com aumento da permeabilidade e exposição das terminações das fibras nervosas; perda de cílios de células ciliadas; necrose de pneumócitos tipo I; formação de radicais livres e subsequente ligação a proteínas e peroxidação lipídica |
|
formação ácida |
Dióxido de enxofre, cloro, halogenetos |
O gás se dissolve na água para formar um ácido que danifica as células epiteliais por oxidação; ação principalmente nas vias aéreas superiores |
|
formação alcalina |
Amônia, óxido de cálcio, hidróxidos |
O gás se dissolve na água para formar uma solução alcalina que pode causar liquefação do tecido; dano predominante das vias aéreas superiores, vias aéreas inferiores em exposições pesadas |
|
Ligação proteica |
Formaldeído |
Reações com aminoácidos levam a intermediários tóxicos com danos à camada de células epiteliais |
|
Estimulação do nervo aferente |
amônia, formaldeído |
A estimulação direta das terminações nervosas provoca sintomas |
|
Antigenicidade |
Platina, anidridos ácidos |
Moléculas de baixo peso molecular servem como haptenos em pessoas sensibilizadas |
|
Estimulação da resposta inflamatória do hospedeiro |
Óxidos de cobre e zinco, lipoproteínas |
Estimulação de citocinas e mediadores inflamatórios sem dano celular direto aparente |
|
formação de radicais livres |
paraquat |
Promoção da formação ou retardo da depuração de radicais superóxidos, levando à peroxidação lipídica e dano oxidativo |
|
Depuração atrasada de partículas |
Qualquer inalação prolongada de pó mineral |
Sobrecarga de escadas rolantes mucociliares e sistemas de macrófagos alveolares com partículas, levando a uma resposta inflamatória inespecífica |
Trabalhadores expostos a baixos níveis de irritantes respiratórios podem apresentar sintomas subclínicos rastreáveis à irritação da membrana mucosa, como olhos lacrimejantes, dor de garganta, coriza e tosse. Com exposição significativa, a sensação adicional de falta de ar geralmente leva a atenção médica. É importante obter um bom histórico médico para determinar a provável composição da exposição, a quantidade de exposição e o período de tempo durante o qual ocorreu a exposição. Sinais de edema laríngeo, incluindo rouquidão e estridor, devem ser procurados, e os pulmões devem ser examinados quanto a sinais de envolvimento das vias aéreas inferiores ou do parênquima. A avaliação das vias aéreas e da função pulmonar, juntamente com a radiografia de tórax, são importantes no tratamento de curto prazo. A laringoscopia pode ser indicada para avaliar as vias aéreas.
Se a via aérea estiver ameaçada, o paciente deve ser submetido a intubação e cuidados de suporte. Pacientes com sinais de edema laríngeo devem ser observados por pelo menos 12 horas para garantir que o processo seja autolimitado. O broncoespasmo deve ser tratado com beta-agonistas e, se refratário, com corticosteroides intravenosos. A mucosa oral e ocular irritada deve ser bem irrigada. Pacientes com crepitações ao exame ou anormalidades na radiografia de tórax devem ser hospitalizados para observação devido à possibilidade de pneumonia ou edema pulmonar. Esses pacientes correm o risco de superinfecção bacteriana; no entanto, nenhum benefício foi demonstrado pelo uso de antibióticos profiláticos.
A esmagadora maioria dos pacientes que sobrevivem ao insulto inicial se recupera totalmente das exposições irritantes. As chances de sequelas a longo prazo são mais prováveis com maior lesão inicial. O termo síndrome de disfunção reativa das vias aéreas (RADS) foi aplicado à persistência de sintomas semelhantes aos da asma após exposição aguda a irritantes respiratórios (Brooks, Weiss e Bernstein 1985).
Exposições de alto nível a álcalis e ácidos podem causar queimaduras no trato respiratório superior e inferior que levam a doenças crônicas. A amônia é conhecida por causar bronquiectasia (Kass et al. 1972); o gás cloro (que se transforma em HCl na mucosa) é relatado como causador de doença pulmonar obstrutiva (Donelly e Fitzgerald 1990; Das e Blanc 1993). Exposições crônicas de baixo nível a irritantes podem causar sintomas oculares e das vias aéreas superiores contínuos (Korn, Dockery e Speizer 1987), mas a deterioração da função pulmonar não foi documentada de forma conclusiva. Estudos dos efeitos de irritantes crônicos de baixo nível na função das vias aéreas são dificultados pela falta de acompanhamento de longo prazo, confundindo-se com o tabagismo, o “efeito do trabalhador saudável” e o mínimo, se houver, efeito clínico real (Brooks e Kalica 1987).
Depois que um paciente se recupera da lesão inicial, é necessário acompanhamento regular por um médico. Claramente, deve haver um esforço para investigar o local de trabalho e avaliar as precauções respiratórias, ventilação e contenção dos irritantes culpados.
Químicos tóxicos
Substâncias químicas tóxicas para o pulmão incluem a maioria dos irritantes respiratórios devido à alta exposição, mas existem muitas substâncias químicas que causam lesão significativa do parênquima pulmonar, apesar de possuírem propriedades irritantes de baixa a moderada. Esses compostos exercem seus efeitos por mecanismos revisados na Tabela 3 e discutidos acima. As toxinas pulmonares tendem a ser menos solúveis em água do que os irritantes das vias aéreas superiores. Exemplos de toxinas pulmonares e suas fontes de exposição são revistos na tabela 3.
Tabela 3. Compostos capazes de toxicidade pulmonar após exposição baixa a moderada
|
Compound |
Fontes de exposição |
Toxicidade |
|
Acroleína |
Plásticos, têxteis, indústria farmacêutica, produtos de combustão |
Lesão difusa das vias aéreas e do parênquima |
|
Tricloreto de antimônio; antimônio |
Ligas, catalisadores orgânicos |
Pneumonite, edema pulmonar não cardiogênico |
|
Cádmio |
Ligas com zinco e chumbo, galvanoplastia, baterias, inseticidas |
Traqueobronquite, edema pulmonar (muitas vezes com início tardio em 24 a 48 horas), dano renal: proteinúria tubular |
|
chloropicrin |
Fabricação química, componentes fumigantes |
Inflamação das vias aéreas superiores e inferiores |
|
Cloro |
Branqueamento, formação de compostos clorados, produtos de limpeza doméstica |
Inflamação das vias aéreas superiores e inferiores, pneumonite e edema pulmonar não cardiogênico |
|
Sulfureto de hidrogênio |
Poços de gás natural, minas, estrume |
Irritação ocular, das vias aéreas superiores e inferiores, edema pulmonar tardio, asfixia por hipóxia tecidual sistêmica |
|
Hidreto de lítio |
Ligas, cerâmica, eletrônica, catalisadores químicos |
Pneumonite, edema pulmonar não cardiogênico |
|
Isocianato de metilo |
Síntese de pesticidas |
Irritação do trato respiratório superior e inferior, edema pulmonar |
|
Mercúrio |
Eletrólise, extração de minério e amálgama, fabricação de eletrônicos |
Inflamação ocular e do trato respiratório, pneumonite, SNC, rins e efeitos sistêmicos |
|
níquel carbonil |
Refino de níquel, galvanoplastia, reagentes químicos |
Irritação do trato respiratório inferior, pneumonite, efeitos tóxicos sistêmicos retardados |
|
Dióxido de nitrogênio |
Silos após novo armazenamento de grãos, fabricação de fertilizantes, soldagem a arco; produtos de combustão |
Inflamação ocular e das vias aéreas superiores, edema pulmonar não cardiogênico, bronquiolite de início tardio |
|
Mostardas Nitrogenadas, Enxofre |
Agentes militares, vesicantes |
Inflamação ocular e do trato respiratório, pneumonite |
|
paraquat |
Herbicidas (ingeridos) |
Dano seletivo aos pneumócitos tipo 2 levando a RADS, fibrose pulmonar; insuficiência renal, irritação GI |
|
Fosgênio |
Fabricação de pesticidas e outros produtos químicos, soldagem a arco, remoção de tinta |
inflamação das vias aéreas superiores e pneumonite; edema pulmonar tardio em doses baixas |
|
Cloreto de zinco |
Granadas de fumaça, artilharia |
Irritação das vias aéreas superiores e inferiores, febre, pneumonia de início tardio |
Um grupo de toxinas inaláveis é denominado asfixiantes. Quando presentes em concentrações altas o suficiente, os asfixiantes, dióxido de carbono, metano e nitrogênio, deslocam o oxigênio e sufocam a vítima. O cianeto de hidrogênio, o monóxido de carbono e o sulfeto de hidrogênio atuam inibindo a respiração celular, apesar do fornecimento adequado de oxigênio ao pulmão. As toxinas inaladas não asfixiantes danificam os órgãos-alvo, causando uma ampla variedade de problemas de saúde e mortalidade.
O tratamento médico de toxinas pulmonares inaladas é semelhante ao tratamento de irritantes respiratórios. Essas toxinas muitas vezes não provocam seu efeito clínico máximo por várias horas após a exposição; monitoramento noturno pode ser indicado para compostos conhecidos por causarem edema pulmonar de início tardio. Uma vez que a terapia de toxinas sistêmicas está além do escopo deste capítulo, o leitor deve consultar as discussões sobre as toxinas individuais em outras partes deste capítulo. enciclopédia e em outros textos sobre o assunto (Goldfrank et al. 1990; Ellenhorn e Barceloux 1988).
Febres por Inalação
Certas exposições por inalação que ocorrem em uma variedade de ambientes ocupacionais diferentes podem resultar em doenças debilitantes semelhantes à gripe que duram algumas horas. Estes são referidos coletivamente como febres de inalação. Apesar da gravidade dos sintomas, a toxicidade parece ser autolimitada na maioria dos casos, e há poucos dados que sugiram sequelas a longo prazo. A exposição maciça a compostos desencadeantes pode causar uma reação mais grave envolvendo pneumonite e edema pulmonar; esses casos incomuns são considerados mais complicados do que a simples febre inalatória.
As febres inalatórias têm em comum a característica de inespecificidade: a síndrome pode ser produzida em quase qualquer pessoa, desde que haja exposição adequada ao agente desencadeante. A sensibilização não é necessária e nenhuma exposição prévia é necessária. Algumas das síndromes exibem o fenômeno da tolerância; ou seja, com a exposição repetida regular, os sintomas não ocorrem. Pensa-se que este efeito esteja relacionado com um aumento da atividade dos mecanismos de depuração, mas não foi adequadamente estudado.
Síndrome Tóxica de Poeira Orgânica
Síndrome tóxica da poeira orgânica (ODTS) é um termo amplo que denota os sintomas autolimitados semelhantes aos da gripe que ocorrem após exposição intensa a poeiras orgânicas. A síndrome abrange uma ampla gama de doenças febris agudas que têm nomes derivados das tarefas específicas que levam à exposição à poeira. Os sintomas ocorrem apenas após uma exposição maciça à poeira orgânica, e a maioria dos indivíduos assim expostos desenvolverá a síndrome.
A síndrome tóxica da poeira orgânica já foi chamada micotoxicose pulmonar, devido à sua suposta etiologia na ação de esporos de fungos e actinomicetos. Com alguns pacientes, pode-se cultivar espécies de Aspergillus, Penicilliume mesofílicos e termofílicos actinomicetos (Emmanuel, Marx e Ault 1975; Emmanuel, Marx e Ault 1989). Mais recentemente, foi proposto que as endotoxinas bacterianas desempenham um papel pelo menos tão grande. A síndrome foi provocada experimentalmente pela inalação de endotoxina derivada de Enterobacter aglomerantes, um dos principais componentes da poeira orgânica (Rylander, Bake e Fischer 1989). Os níveis de endotoxinas foram medidos no ambiente da fazenda, com níveis variando de 0.01 a 100μg/m3. Muitas amostras tinham um nível superior a 0.2μg/m3, que é o nível onde os efeitos clínicos são conhecidos (May, Stallones e Darrow 1989). Especula-se que as citocinas, como a IL-1, possam mediar os efeitos sistêmicos, dado o que já se sabe sobre a liberação de IL-1 dos macrófagos alveolares na presença de endotoxina (Richerson 1990). Mecanismos alérgicos são improváveis, dada a falta de necessidade de sensibilização e a exigência de alta exposição à poeira.
Clinicamente, o paciente geralmente apresenta sintomas 2 a 8 horas após a exposição a grãos (geralmente mofados), feno, algodão, linho, cânhamo ou lascas de madeira, ou após a manipulação de porcos (Do Pico 1992). Frequentemente os sintomas iniciam-se com irritação ocular e das mucosas com tosse seca, evoluindo para febre, e mal-estar, aperto torácico, mialgias e cefaléia. O paciente parece doente, mas normal ao exame físico. A leucocitose ocorre com frequência, com níveis de até 25,000 glóbulos brancos (WBC)/mm3. A radiografia de tórax é quase sempre normal. A espirometria pode revelar um defeito obstrutivo modesto. Nos casos em que a broncoscopia com fibra óptica foi realizada e lavados brônquicos foram obtidos, uma elevação de leucócitos foi encontrada no fluido de lavagem. A porcentagem de neutrófilos foi significativamente maior do que o normal (Emmanuel, Marx e Ault 1989; Lecours, Laviolette e Cormier 1986). A broncoscopia 1 a 4 semanas após o evento mostra uma celularidade persistentemente alta, predominantemente linfócitos.
Dependendo da natureza da exposição, o diagnóstico diferencial pode incluir exposição a gases tóxicos (como dióxido de nitrogênio ou amônia), principalmente se o episódio ocorreu em um silo. Pneumonite de hipersensibilidade deve ser considerada, especialmente se houver radiografia de tórax significativa ou anormalidades nos testes de função pulmonar. A distinção entre pneumonite de hipersensibilidade (HP) e ODTS é importante: a HP exigirá prevenção rigorosa da exposição e tem um prognóstico pior, enquanto a ODTS tem um curso benigno e autolimitado. A ODTS também se distingue da HP porque ocorre com mais frequência, requer níveis mais altos de exposição à poeira, não induz a liberação de anticorpos precipitantes séricos e (inicialmente) não dá origem à alveolite linfocítica que é característica da HP.
Os casos são tratados com antipiréticos. Um papel para esteroides não foi defendido dada a natureza autolimitada da doença. Os pacientes devem ser instruídos sobre como evitar a exposição maciça. O efeito a longo prazo de ocorrências repetidas é considerado insignificante; no entanto, esta questão não foi adequadamente estudada.
Febre do metal
A febre da fumaça de metal (MFF) é outra doença autolimitada, semelhante à gripe, que se desenvolve após a exposição por inalação, neste caso, a fumaça de metal. A síndrome se desenvolve mais comumente após a inalação de óxido de zinco, como ocorre em fundições de latão e na fundição ou soldagem de metal galvanizado. Óxidos de cobre e ferro também causam MFF, e vapores de alumínio, arsênico, cádmio, mercúrio, cobalto, cromo, prata, manganês, selênio e estanho foram ocasionalmente implicados (Rose 1992). Os trabalhadores desenvolvem taquifalaxia; ou seja, os sintomas aparecem apenas quando a exposição ocorre após vários dias sem exposição, e não quando há exposições repetidas regulares. Um TLV de oito horas de 5 mg/m3 para o óxido de zinco foi estabelecido pela Administração de Saúde e Segurança Ocupacional dos EUA (OSHA), mas os sintomas foram provocados experimentalmente após uma exposição de duas horas a esta concentração (Gordon et al. 1992).
A patogênese da MFF permanece obscura. O início reprodutível dos sintomas, independentemente do indivíduo exposto, argumenta contra uma sensibilização imune ou alérgica específica. A ausência de sintomas associados à liberação de histamina (rubor, coceira, chiado no peito, urticária) também milita contra a probabilidade de um mecanismo alérgico. Paul Blanc e colaboradores desenvolveram um modelo que implica a liberação de citocinas (Blanc et al. 1991; Blanc et al.1993). Eles mediram os níveis do fator de necrose tumoral (TNF) e das interleucinas IL-1, IL-4, IL-6 e IL-8 no fluido lavado dos pulmões de 23 voluntários expostos experimentalmente a vapores de óxido de zinco (Blanc et al. 1993). Os voluntários desenvolveram níveis elevados de TNF em seu fluido de lavagem broncoalveolar (BAL) 3 horas após a exposição. Vinte horas depois, foram observados níveis elevados de IL-8 (um potente atrativo de neutrófilos) e uma alveolite neutrofílica impressionante. Foi demonstrado que o TNF, uma citocina capaz de causar febre e estimular células imunes, é liberado de monócitos em cultura expostos ao zinco (Scuderi 1990). Assim, a presença de TNF aumentado no pulmão é responsável pelo início dos sintomas observados na MFF. Sabe-se que o TNF estimula a liberação tanto de IL-6 quanto de IL-8, em um período de tempo correlacionado com os picos das citocinas no líquido BAL desses voluntários. O recrutamento dessas citocinas pode ser responsável pela alveolite de neutrófilos resultante e pelos sintomas semelhantes aos da gripe que caracterizam a MFF. Por que a alveolite se resolve tão rapidamente permanece um mistério.
Os sintomas começam 3 a 10 horas após a exposição. Inicialmente, pode haver um gosto doce metálico na boca, acompanhado de piora da tosse seca e falta de ar. Febre e calafrios freqüentemente se desenvolvem, e o trabalhador sente-se mal. O exame físico é normal. A avaliação laboratorial mostra uma leucocitose e uma radiografia de tórax normal. Estudos de função pulmonar podem mostrar um FEF ligeiramente reduzido25-75 e níveis de DLCO (Nemery 1990; Rose 1992).
Com uma boa história, o diagnóstico é prontamente estabelecido e o trabalhador pode ser tratado sintomaticamente com antipiréticos. Os sintomas e anormalidades clínicas desaparecem dentro de 24 a 48 horas. Caso contrário, as etiologias bacteriana e viral dos sintomas devem ser consideradas. Em casos de exposição extrema, ou exposições envolvendo contaminação por toxinas como cloreto de zinco, cádmio ou mercúrio, o MFF pode ser um prenúncio de uma pneumonia química clínica que evoluirá nos próximos 2 dias (Blount 1990). Esses casos podem exibir infiltrados difusos na radiografia de tórax e sinais de edema pulmonar e insuficiência respiratória. Embora essa possibilidade deva ser considerada na avaliação inicial de um paciente exposto, esse curso fulminante é incomum e não é característico de MFF não complicada.
O MFF não requer uma sensibilidade específica do indivíduo para os fumos metálicos; ao contrário, indica controle ambiental inadequado. O problema da exposição deve ser tratado para evitar sintomas recorrentes. Embora a síndrome seja considerada benigna, os efeitos a longo prazo de episódios repetidos de MFF não foram adequadamente investigados.
Febre da fumaça de polímero
A febre dos vapores de polímeros é uma doença febril autolimitada semelhante à MFF, mas causada por produtos de pirólise inalados de fluoropolímeros, incluindo politetrafluoretano (PTFE; nomes comerciais Teflon, Fluon, Halon). O PTFE é amplamente utilizado por seu lubrificante, estabilidade térmica e propriedades isolantes elétricas. É inofensivo a menos que aquecido acima de 30°C, quando começa a liberar produtos de degradação (Shusterman 1993). Esta situação ocorre durante a soldagem de materiais revestidos com PTFE, aquecimento de PTFE com uma borda de ferramenta durante usinagem de alta velocidade, operação de máquinas de moldagem ou extrusão (Rose 1992) e raramente durante cirurgia a laser endotraqueal (Rom 1992a).
Uma causa comum de febre dos vapores de polímeros foi descoberta após um período clássico de trabalho de detetive de saúde pública no início dos anos 1970 (Wegman e Peters 1974; Kuntz e McCord 1974). Trabalhadores têxteis estavam desenvolvendo doenças febris autolimitadas com exposição a formaldeído, amônia e fibra de náilon; eles não foram expostos a vapores de fluoropolímero, mas manusearam polímero triturado. Depois de descobrir que os níveis de exposição de outros possíveis agentes etiológicos estavam dentro dos limites aceitáveis, o trabalho do fluoropolímero foi examinado mais de perto. Como se viu, apenas os fumantes que trabalhavam com o fluoropolímero eram sintomáticos. Foi hipotetizado que os cigarros estavam sendo contaminados com fluoropolímero nas mãos do trabalhador, então o produto foi queimado no cigarro quando este foi fumado, expondo o trabalhador a fumaça tóxica. Depois de proibir o fumo de cigarros no local de trabalho e estabelecer regras estritas de lavagem das mãos, nenhuma outra doença foi relatada (Wegman e Peters 1974). Desde então, esse fenômeno foi relatado após o trabalho com compostos impermeabilizantes, compostos desmoldantes (Albrecht e Bryant 1987) e após o uso de certos tipos de cera de esqui (Strom e Alexandersen 1990).
A patogênese da febre dos vapores de polímeros não é conhecida. Acredita-se que seja semelhante às outras febres inalatórias devido à sua apresentação semelhante e resposta imune aparentemente inespecífica. Não houve estudos experimentais em humanos; no entanto, ratos e pássaros desenvolvem danos epiteliais alveolares graves quando expostos a produtos de pirólise de PTFE (Wells, Slocombe e Trapp 1982; Blandford et al. 1975). A medição precisa da função pulmonar ou das alterações do LBA não foi realizada.
Os sintomas aparecem várias horas após a exposição e não há tolerância ou efeito de taquifalaxia, como observado na MFF. Fraqueza e mialgias são seguidas de febre e calafrios. Muitas vezes há aperto no peito e tosse. O exame físico geralmente é normal. A leucocitose é frequentemente observada e a radiografia de tórax geralmente é normal. Os sintomas desaparecem espontaneamente em 12 a 48 horas. Houve alguns casos de pessoas que desenvolveram edema pulmonar após a exposição; em geral, acredita-se que os vapores de PTFE sejam mais tóxicos do que os vapores de zinco ou cobre em causar MFF (Shusterman 1993; Brubaker 1977). A disfunção crônica das vias aéreas foi relatada em pessoas que tiveram múltiplos episódios de febre dos vapores de polímeros (Williams, Atkinson e Patchefsky 1974).
O diagnóstico de febre dos fumos de polímeros requer uma história cuidadosa com alta suspeição clínica. Depois de determinar a origem dos produtos de pirólise de PTFE, esforços devem ser feitos para evitar mais exposição. As regras obrigatórias de lavagem das mãos e a eliminação do fumo no local de trabalho eliminaram efetivamente os casos relacionados a cigarros contaminados. Trabalhadores que tiveram múltiplos episódios de febre dos vapores de polímeros ou edema pulmonar associado devem ter acompanhamento médico de longo prazo.
Asma Ocupacional
A asma é uma doença respiratória caracterizada por obstrução das vias aéreas parcial ou totalmente reversível, espontaneamente ou com tratamento; inflamação das vias aéreas; e aumento da capacidade de resposta das vias aéreas a uma variedade de estímulos (NAEP 1991). A asma ocupacional (OA) é a asma causada por exposições ambientais no local de trabalho. Várias centenas de agentes foram relatados como causadores de OA. Asma pré-existente ou hiperresponsividade das vias aéreas, com sintomas agravados pela exposição no trabalho a irritantes ou estímulos físicos, geralmente é classificada separadamente como asma agravada pelo trabalho (WAA). Existe um consenso geral de que a OA se tornou a doença pulmonar ocupacional mais prevalente nos países desenvolvidos, embora as estimativas de prevalência e incidência reais sejam bastante variáveis. É claro, no entanto, que em muitos países a asma de etiologia ocupacional causa uma carga de doença e incapacidade em grande parte não reconhecida, com altos custos econômicos e não econômicos. Grande parte dessa carga econômica e de saúde pública é potencialmente evitável identificando e controlando ou eliminando as exposições no local de trabalho que causam asma. Este artigo irá resumir as abordagens atuais para o reconhecimento, gestão e prevenção da OA. Várias publicações recentes discutem essas questões com mais detalhes (Chan-Yeung 1995; Bernstein et al. 1993).
Magnitude do problema
As prevalências de asma em adultos geralmente variam de 3 a 5%, dependendo da definição de asma e variações geográficas, e podem ser consideravelmente maiores em algumas populações urbanas de baixa renda. A proporção de casos de asma em adultos na população em geral relacionada ao ambiente de trabalho varia de 2 a 23%, com estimativas recentes tendendo para o limite superior da faixa. As prevalências de asma e OA foram estimadas em pequenos estudos de coorte e transversais de grupos ocupacionais de alto risco. Em uma revisão de 22 estudos selecionados de locais de trabalho com exposição a substâncias específicas, as prevalências de asma ou OA, definidas de várias maneiras, variaram de 3 a 54%, com 12 estudos relatando prevalências acima de 15% (Becklake, em Bernstein et al. 1993 ). A ampla variação reflete a variação real na prevalência real (devido a diferentes tipos e níveis de exposição). Também reflete diferenças nos critérios diagnósticos e variação na força dos vieses, como o “viés do sobrevivente”, que pode resultar da exclusão de trabalhadores que desenvolveram OA e deixaram o local de trabalho antes da realização do estudo. As estimativas populacionais de incidência variam de 14 por milhão de adultos empregados por ano nos Estados Unidos a 140 por milhão de adultos empregados por ano na Finlândia (Meredith e Nordman 1996). A verificação dos casos foi mais completa e os métodos de diagnóstico geralmente mais rigorosos na Finlândia. A evidência dessas diferentes fontes é consistente em sua implicação de que a OA é frequentemente subdiagnosticada e/ou subnotificada e é um problema de saúde pública de maior magnitude do que geralmente reconhecido.
Causas da asma ocupacional
Mais de 200 agentes (substâncias específicas, ocupações ou processos industriais) foram relatados como causadores de OA, com base em evidências epidemiológicas e/ou clínicas. Na OA, a inflamação das vias aéreas e a broncoconstrição podem ser causadas por resposta imunológica a agentes sensibilizantes, por efeitos irritantes diretos ou por outros mecanismos não imunológicos. Alguns agentes (por exemplo, inseticidas organofosforados) também podem causar broncoconstrição por ação farmacológica direta. Acredita-se que a maioria dos agentes relatados induzem uma resposta de sensibilização. Irritantes respiratórios muitas vezes pioram os sintomas em trabalhadores com asma pré-existente (ou seja, WAA) e, em altos níveis de exposição, podem causar novo aparecimento de asma (denominado síndrome de disfunção reativa das vias aéreas (RADS) ou asma induzida por irritante) (Brooks, Weiss e Bernstein 1985; Alberts e Do Pico 1996).
A OA pode ocorrer com ou sem um período de latência. O período de latência refere-se ao tempo entre a exposição inicial e o desenvolvimento dos sintomas e é altamente variável. Geralmente é inferior a 2 anos, mas em cerca de 20% dos casos é de 10 anos ou mais. A OA com latência é geralmente causada por sensibilização a um ou mais agentes. O RADS é um exemplo de OA sem latência.
Agentes sensibilizantes de alto peso molecular (5,000 daltons (Da) ou mais) muitas vezes agem por um mecanismo dependente de IgE. Agentes sensibilizantes de baixo peso molecular (menos de 5,000 Da), que incluem produtos químicos altamente reativos como isocianatos, podem atuar por mecanismos independentes de IgE ou podem atuar como haptenos, combinando-se com proteínas corporais. Uma vez que um trabalhador se torna sensibilizado a um agente, a reexposição (frequentemente em níveis muito abaixo do nível que causou a sensibilização) resulta em uma resposta inflamatória nas vias aéreas, muitas vezes acompanhada por aumentos na limitação do fluxo de ar e responsividade brônquica inespecífica (NBR).
Em estudos epidemiológicos de OA, as exposições no local de trabalho são consistentemente os determinantes mais fortes da prevalência de asma, e o risco de desenvolver OA com latência tende a aumentar com a intensidade estimada da exposição. A atopia é um determinante importante e um pouco menos consistente da ocorrência de asma em estudos de agentes que atuam por meio de um mecanismo dependente de IgE. Nem a atopia nem o tabagismo parecem ser determinantes importantes da asma em estudos de agentes que agem por mecanismos independentes de IgE.
Apresentação Clínica
O espectro de sintomas da OA é semelhante ao da asma não ocupacional: chiado, tosse, aperto no peito e falta de ar. Os pacientes às vezes apresentam asma variante da tosse ou asma noturna. A OA pode ser grave e incapacitante, e mortes foram relatadas. O início da OA ocorre devido a um ambiente de trabalho específico, portanto, identificar as exposições que ocorreram no momento do início dos sintomas asmáticos é fundamental para um diagnóstico preciso. Na WAA, as exposições no local de trabalho causam um aumento significativo na frequência e/ou gravidade dos sintomas de asma pré-existente.
Várias características da história clínica podem sugerir etiologia ocupacional (Chan-Yeung 1995). Os sintomas freqüentemente pioram no trabalho ou à noite após o trabalho, melhoram nos dias de folga e recorrem no retorno ao trabalho. Os sintomas podem piorar progressivamente no final da semana de trabalho. O paciente pode observar atividades ou agentes específicos no local de trabalho que desencadeiam sintomas de forma reproduzível. Irritação ocular relacionada ao trabalho ou rinite podem estar associadas a sintomas asmáticos. Esses padrões de sintomas típicos podem estar presentes apenas nos estágios iniciais da OA. A resolução parcial ou completa nos fins de semana ou férias é comum no início do curso da OA, mas com exposições repetidas, o tempo necessário para a recuperação pode aumentar para uma ou duas semanas, ou a recuperação pode deixar de ocorrer. A maioria dos pacientes com OA cujas exposições são interrompidas continuam a ter asma sintomática mesmo anos após a interrupção da exposição, com comprometimento e incapacidade permanentes. A exposição contínua está associada ao agravamento da asma. A curta duração e a gravidade leve dos sintomas no momento da cessação da exposição são bons fatores de prognóstico e diminuem a probabilidade de asma permanente.
Vários padrões temporais característicos de sintomas foram relatados para OA. As reações asmáticas precoces geralmente ocorrem logo (menos de uma hora) após o início do trabalho ou a exposição específica ao trabalho que causa a asma. As reações asmáticas tardias começam 4 a 6 horas após o início da exposição e podem durar de 24 a 48 horas. Combinações desses padrões ocorrem como reações asmáticas duplas com resolução espontânea dos sintomas, separando uma reação precoce e tardia, ou como reações asmáticas contínuas sem resolução dos sintomas entre as fases. Com exceções, as reações precoces tendem a ser mediadas por IgE e as reações tardias tendem a ser independentes de IgE.
NBR aumentado, geralmente medido por desafio com metacolina ou histamina, é considerado uma característica fundamental da asma ocupacional. O curso de tempo e o grau de NBR podem ser úteis no diagnóstico e monitoramento. A NBR pode diminuir dentro de várias semanas após o término da exposição, embora a NBR anormal geralmente persista por meses ou anos após o término das exposições. Em indivíduos com asma ocupacional induzida por irritantes, não se espera que a NBR varie com a exposição e/ou sintomas.
Reconhecimento e Diagnóstico
O diagnóstico preciso da OA é importante, dadas as consequências negativas substanciais do subdiagnóstico ou do superdiagnóstico. Em trabalhadores com OA ou em risco de desenvolver OA, o reconhecimento, identificação e controle oportunos das exposições ocupacionais causadoras da asma aumentam as chances de prevenção ou recuperação completa. Essa prevenção primária pode reduzir muito os altos custos financeiros e humanos da asma crônica e incapacitante. Por outro lado, uma vez que um diagnóstico de OA pode obrigar a uma mudança completa de ocupação ou intervenções dispendiosas no local de trabalho, distinguir com precisão a OA da asma não ocupacional pode evitar custos sociais e financeiros desnecessários para empregadores e trabalhadores.
Várias definições de caso de OA foram propostas, apropriadas em diferentes circunstâncias. As definições consideradas valiosas para triagem ou vigilância de trabalhadores (Hoffman et al. 1990) podem não ser totalmente aplicáveis para fins clínicos ou compensações. Um consenso de pesquisadores definiu a OA como “uma doença caracterizada por limitação variável do fluxo de ar e/ou hiperresponsividade das vias aéreas devido a causas e condições atribuíveis a um ambiente ocupacional específico e não a estímulos encontrados fora do local de trabalho” (Bernstein et al. 1993) . Essa definição foi operacionalizada como uma definição de caso médico, resumida na tabela 1 (Chan-Yeung 1995).
Tabela 1. Definição de caso médico ACCP de asma ocupacional
Critérios para diagnóstico de asma ocupacional1 (requer todos os 4, AD):
(A) Diagnóstico médico de asma e/ou evidência fisiológica de hiperresponsividade das vias aéreas
(B) A exposição ocupacional precedeu o início dos sintomas asmáticos1
(C) Associação entre sintomas de asma e trabalho
(D) Exposição e/ou evidência fisiológica da relação da asma com o ambiente de trabalho (O diagnóstico de OA requer um ou mais de D2-D5, provavelmente OA requer apenas D1)
(1) Exposição no local de trabalho ao agente relatado para dar origem a OA
(2) Mudanças relacionadas ao trabalho no VEF1 e/ou PEF
(3) Mudanças relacionadas ao trabalho em testes seriados para responsividade brônquica não específica (por exemplo, teste de desafio com metacolina)
(4) Teste de provocação brônquica específico positivo
(5) Início de asma com clara associação com exposição sintomática a um irritante inalado no local de trabalho (geralmente RADS)
Critérios para diagnóstico de RADS (deve atender a todos os 7):
(1) Ausência documentada de queixas pré-existentes semelhantes à asma
(2) Início dos sintomas após um único incidente de exposição ou acidente
(3) Exposição a um gás, fumaça, fumaça, vapor ou poeira com propriedades irritantes presentes em alta concentração
(4) Início dos sintomas dentro de 24 horas após a exposição com persistência dos sintomas por pelo menos 3 meses
(5) Sintomas consistentes com asma: tosse, pieira, dispneia
(6) Presença de obstrução do fluxo aéreo nas provas de função pulmonar e/ou presença de hiperresponsividade brônquica inespecífica (teste deve ser feito logo após a exposição)
(7) Excluídas outras doenças pulmonares
Critérios para diagnóstico de asma agravada pelo trabalho (WAA):
(1) Atende aos critérios A e C da definição de caso médico ACCP de OA
(2) Asma pré-existente ou história de sintomas asmáticos, (com sintomas ativos durante o ano anterior ao início do emprego ou exposição de interesse)
(3) Aumento claro nos sintomas ou necessidade de medicação, ou documentação de mudanças relacionadas ao trabalho no PFER ou VEF1 após o início do emprego ou exposição de interesse
1 Uma definição de caso que exija A, C e qualquer um de D1 a D5 pode ser útil na vigilância de OA, WAA e RADS.
Fonte: Chan-Yeung 1995.
A avaliação clínica completa da OA pode ser demorada, cara e difícil. Pode exigir testes diagnósticos de remoção e retorno ao trabalho e, muitas vezes, requer que o paciente faça um gráfico confiável das medições de pico de fluxo expiratório (PFE). Alguns componentes da avaliação clínica (por exemplo, provocação brônquica específica ou testes quantitativos seriados para NBR) podem não estar prontamente disponíveis para muitos médicos. Outros componentes podem simplesmente não ser alcançáveis (por exemplo, paciente que não está mais trabalhando, recursos diagnósticos indisponíveis, medições seriadas inadequadas do PFE). É provável que a precisão diagnóstica aumente com o rigor da avaliação clínica. Em cada paciente individual, as decisões sobre a extensão da avaliação médica precisarão equilibrar os custos da avaliação com as consequências clínicas, sociais, financeiras e de saúde pública do diagnóstico incorreto ou exclusão da OA.
Considerando essas dificuldades, uma abordagem gradual para o diagnóstico de OA é descrita na tabela 2. Ela pretende ser um guia geral para facilitar uma avaliação diagnóstica precisa, prática e eficiente, reconhecendo que alguns dos procedimentos sugeridos podem não estar disponíveis em alguns locais . O diagnóstico de OA envolve estabelecer tanto o diagnóstico de asma quanto a relação entre asma e exposições no local de trabalho. Após cada etapa, para cada paciente, o médico precisará determinar se o nível de certeza diagnóstica alcançado é adequado para apoiar as decisões necessárias ou se a avaliação deve continuar para a próxima etapa. Se houver instalações e recursos disponíveis, o tempo e o custo da continuação da avaliação clínica geralmente são justificados pela importância de se fazer uma determinação precisa da relação da asma com o trabalho. Os destaques dos procedimentos de diagnóstico para OA serão resumidos; detalhes podem ser encontrados em várias das referências (Chan-Yeung 1995; Bernstein et al. 1993). A consulta com um médico experiente em OA pode ser considerada, uma vez que o processo de diagnóstico pode ser difícil.
Tabela 2. Etapas da avaliação diagnóstica da asma no ambiente de trabalho
Passo 1 Histórico médico e ocupacional completo e exame físico dirigido.
Passo 2 Avaliação fisiológica para obstrução reversível das vias aéreas e/ou hiperresponsividade brônquica inespecífica.
Passo 3 Avaliação imunológica, se apropriado.
Avalie o status do trabalho:
Atualmente trabalhando: Prossiga para a Etapa 4 primeiro.
Não está trabalhando no momento, tentativa de diagnóstico de retorno ao trabalho viável: Etapa 5 primeiro, depois Etapa 4.
Não está trabalhando no momento, tentativa diagnóstica de retorno ao trabalho inviável: Passo 6.
Passo 4 Avaliação clínica da asma no trabalho ou ensaio diagnóstico de retorno ao trabalho.
Passo 5 Avaliação clínica da asma fora do trabalho ou tentativa diagnóstica de afastamento do trabalho.
Passo 6 Teste de desafio no local de trabalho ou teste de desafio brônquico específico. Se disponível para exposições causais suspeitas, esta etapa pode ser realizada antes da Etapa 4 para qualquer paciente.
Este destina-se a ser um guia geral para facilitar a avaliação diagnóstica prática e eficiente. Recomenda-se que os médicos que diagnosticam e tratam a OA também consultem a literatura clínica atual.
A RADS, quando causada por uma exposição ocupacional, é geralmente considerada uma subclasse da OA. É diagnosticado clinicamente, usando os critérios da Tabela 6. Pacientes que apresentaram lesão respiratória significativa devido à inalação de irritantes de alto nível devem ser avaliados quanto à persistência de sintomas e presença de obstrução do fluxo aéreo logo após o evento. Se a história clínica for compatível com RADS, a avaliação adicional deve incluir testes quantitativos para NBR, se não for contraindicado.
WAA pode ser comum e pode causar uma carga evitável substancial de incapacidade, mas pouco foi publicado sobre diagnóstico, tratamento ou prognóstico. Conforme resumido na Tabela 6, a WAA é reconhecida quando os sintomas asmáticos precederam a suspeita de exposição causal, mas são claramente agravados pelo ambiente de trabalho. A piora no trabalho pode ser documentada por evidências fisiológicas ou por avaliação de prontuários e uso de medicamentos. É um julgamento clínico se os pacientes com história de asma em remissão, que apresentam recorrência de sintomas asmáticos que preenchem os critérios para OA, são diagnosticados com OA ou WAA. Um ano foi proposto como um período assintomático suficientemente longo para que o início dos sintomas provavelmente represente um novo processo causado pela exposição no local de trabalho, embora ainda não haja consenso.
Passo 1: Histórico médico e ocupacional completo e exame físico direcionado
A suspeita inicial de possível OA em situações clínicas e de trabalho apropriadas é fundamental, dada a importância do diagnóstico precoce e intervenção na melhoria do prognóstico. O diagnóstico de OA ou WAA deve ser considerado em todos os pacientes asmáticos nos quais os sintomas se desenvolveram como um adulto trabalhador (especialmente de início recente) ou nos quais a gravidade da asma aumentou substancialmente. A OA também deve ser considerada em quaisquer outros indivíduos que apresentem sintomas semelhantes aos da asma e trabalhem em ocupações nas quais estejam expostos a agentes causadores de asma ou que estejam preocupados com o fato de seus sintomas estarem relacionados ao trabalho.
Pacientes com possível OA devem ser solicitados a fornecer uma história médica e ocupacional/ambiental completa, com documentação cuidadosa da natureza e data de início dos sintomas e diagnóstico de asma, e quaisquer exposições potencialmente causais naquele momento. A compatibilidade da história médica com a apresentação clínica da OA descrita acima deve ser avaliada, especialmente o padrão temporal dos sintomas em relação ao horário de trabalho e mudanças nas exposições laborais. Padrões e mudanças nos padrões de uso de medicamentos para asma e o período mínimo de afastamento do trabalho necessário para a melhora dos sintomas devem ser observados. Doenças respiratórias anteriores, alergias/atopia, tabagismo e outras exposições tóxicas e história familiar de alergia são pertinentes.
Exposições ocupacionais e outras exposições ambientais a potenciais agentes ou processos causadores de asma devem ser minuciosamente exploradas, com documentação objetiva das exposições, se possível. Exposições suspeitas devem ser comparadas com uma lista abrangente de agentes relatados como causadores de OA (Harber, Schenker e Balmes 1996; Chan-Yeung e Malo 1994; Bernstein et al. 1993; Rom 1992b), embora a incapacidade de identificar agentes específicos não seja incomum e também é possível a indução de asma por agentes não descritos anteriormente. Alguns exemplos ilustrativos são mostrados na tabela 3. A história ocupacional deve incluir detalhes do emprego atual e anterior relevante com datas, cargos, tarefas e exposições, especialmente o trabalho atual e o trabalho exercido no momento do início dos sintomas. Outra história ambiental deve incluir uma revisão de exposições em casa ou na comunidade que possam causar asma. É útil começar o histórico de exposição de forma aberta, perguntando sobre amplas categorias de agentes transportados pelo ar: poeiras (especialmente poeiras orgânicas de origem animal, vegetal ou microbiana), produtos químicos, farmacêuticos e gases ou vapores irritantes ou visíveis. O paciente pode identificar agentes específicos, processos de trabalho ou categorias genéricas de agentes que desencadearam sintomas. Pedir ao paciente para descrever passo a passo as atividades e exposições envolvidas no dia de trabalho sintomático mais recente pode fornecer pistas úteis. Materiais usados por colegas de trabalho, ou aqueles liberados em alta concentração de um derramamento ou outra fonte, podem ser relevantes. Muitas vezes, informações adicionais podem ser obtidas sobre o nome do produto, ingredientes e nome do fabricante, endereço e número de telefone. Agentes específicos podem ser identificados ligando para o fabricante ou através de uma variedade de outras fontes, incluindo livros didáticos, bancos de dados de CD-ROM ou Centros de Controle de Venenos. Como a OA é freqüentemente causada por baixos níveis de alérgenos transportados pelo ar, as inspeções de higiene industrial no local de trabalho que avaliam qualitativamente as exposições e as medidas de controle são frequentemente mais úteis do que a medição quantitativa dos contaminantes do ar.
Tabela 3. Agentes sensibilizantes que podem causar asma ocupacional
|
Classificação |
Subgrupos |
Exemplos de substâncias |
Exemplos de empregos e indústrias |
|
Antígenos proteicos de alto peso molecular |
Substâncias derivadas de animais Substâncias derivadas de plantas |
Animais de laboratório, caranguejo/frutos do mar, ácaros, insetos Pó de farinha e grãos, luvas de látex de borracha natural, enzimas bacterianas, pó de mamona, gomas vegetais |
Manipuladores de animais, agricultura e processamento de alimentos Padarias, profissionais de saúde, fabricação de detergentes, processamento de alimentos |
|
Baixo peso molecular/químico |
Plastificantes, tintas bicomponentes, adesivos, espumas Metais pó de madeira Farmacêuticos, drogas |
Isocianatos, anidridos ácidos, aminas Sais de platina, cobalto Cedro (ácido plicatico), carvalho Psyllium, antibióticos |
Pintura automática em spray, envernizamento, marcenaria Refinarias de platina, moagem de metal Trabalho de serraria, carpintaria Fabricação e embalagem farmacêutica |
|
Outros produtos químicos |
Cloramina T, vapores de cloreto de polivinila, inseticidas organofosforados |
Trabalho de zeladoria, embalagem de carne |
A história clínica parece ser melhor para excluir do que para confirmar o diagnóstico de OA, e uma história aberta obtida por um médico é melhor do que um questionário fechado. Um estudo comparou os resultados de uma história clínica aberta tomada por especialistas treinados em OA com um “padrão ouro” de teste de broncoprovocação específico em 162 pacientes encaminhados para avaliação de possível OA. Os investigadores relataram que a sensibilidade de uma história clínica sugestiva de OA foi de 87%, especificidade de 55%, valor preditivo positivo de 63% e valor preditivo negativo de 83%. Nesse grupo de pacientes encaminhados, a prevalência de asma e OA foi de 80% e 46%, respectivamente (Malo et al. 1991). Em outros grupos de pacientes encaminhados, os valores preditivos positivos de um questionário fechado variaram de 8 a 52% para uma variedade de exposições no local de trabalho (Bernstein et al. 1993). A aplicabilidade desses resultados a outras configurações precisa ser avaliada pelo médico.
Às vezes, o exame físico é útil e achados relevantes para asma (por exemplo, sibilância, pólipos nasais, dermatite eczematosa), irritação respiratória ou alergia (por exemplo, rinite, conjuntivite) ou outras causas potenciais de sintomas devem ser observados.
Passo 2: Avaliação fisiológica para obstrução reversível das vias aéreas e/ou hiperresponsividade brônquica inespecífica
Se evidências fisiológicas suficientes apoiando o diagnóstico de asma (NAEP 1991) já estiverem no prontuário médico, a Etapa 2 pode ser ignorada. Caso contrário, a espirometria orientada pelo técnico deve ser realizada, preferencialmente após o expediente em um dia em que o paciente apresente sintomas asmáticos. Se a espirometria revelar obstrução das vias aéreas que reverte com um broncodilatador, isso confirma o diagnóstico de asma. Em pacientes sem evidência clara de limitação do fluxo aéreo na espirometria, testes quantitativos para NBR usando metacolina ou histamina devem ser feitos no mesmo dia, se possível. O teste quantitativo para NBR nessa situação é um procedimento fundamental por dois motivos. Primeiro, muitas vezes pode identificar pacientes com OA leve ou em estágio inicial que têm o maior potencial de cura, mas que seriam perdidos se o teste fosse interrompido com espirometria normal. Em segundo lugar, se o NBR for normal em um trabalhador que tenha exposição contínua no ambiente de trabalho associado aos sintomas, a OA geralmente pode ser descartada sem testes adicionais. Se anormal, a avaliação pode prosseguir para a Etapa 3 ou 4, e o grau de NBR pode ser útil no monitoramento do paciente para melhora após o teste diagnóstico de remoção da exposição causal suspeita (Etapa 5). Se a espirometria revelar limitação significativa do fluxo de ar que não melhora após broncodilatador inalado, deve ser considerada uma reavaliação após uma tentativa mais prolongada de terapia, incluindo corticosteróides (ATS 1995; NAEP 1991).
Passo 3: Avaliação imunológica, se apropriado
Testes cutâneos ou sorológicos (por exemplo, RAST) podem demonstrar sensibilização imunológica a um agente específico do local de trabalho. Esses testes imunológicos têm sido usados para confirmar a relação da asma com o trabalho e, em alguns casos, eliminar a necessidade de testes específicos de provocação por inalação. Por exemplo, entre os pacientes expostos ao psyllium com histórico clínico compatível com OA, asma documentada ou hiperresponsividade das vias aéreas e evidência de sensibilização imunológica ao psyllium, aproximadamente 80% tiveram OA confirmada em testes de provocação brônquica específicos subsequentes (Malo et al. 1990 ). Na maioria dos casos, o significado diagnóstico de testes imunológicos negativos é menos claro. A sensibilidade diagnóstica dos testes imunológicos depende criticamente se todos os prováveis antígenos causais no local de trabalho ou complexos hapteno-proteína foram incluídos no teste. Embora a implicação da sensibilização para um trabalhador assintomático não esteja bem definida, a análise de resultados agrupados pode ser útil na avaliação dos controles ambientais. A utilidade da avaliação imunológica é maior para agentes para os quais existem in vitro testes ou reagentes cutâneos, como sais de platina e enzimas detergentes. Infelizmente, a maioria dos alérgenos ocupacionais de interesse não está atualmente disponível comercialmente. O uso de soluções não comerciais em testes cutâneos em picada foi ocasionalmente associado a reações graves, incluindo anafilaxia e, portanto, é necessário cautela.
Se os resultados das Etapas 1 e 2 forem compatíveis com OA, uma avaliação mais aprofundada deve ser realizada, se possível. A ordem e a extensão da avaliação adicional dependem da disponibilidade de recursos diagnósticos, status de trabalho do paciente e viabilidade de testes diagnósticos de remoção e retorno ao trabalho, conforme indicado na Tabela 7. Se uma avaliação adicional não for possível, um diagnóstico deve ser baseado em as informações disponíveis neste momento.
Etapa 4: Avaliação clínica da asma no trabalho ou teste diagnóstico de retorno ao trabalho
Freqüentemente, o teste fisiológico de obstrução das vias aéreas mais prontamente disponível é a espirometria. Para melhorar a reprodutibilidade, a espirometria deve ser orientada por um técnico treinado. Infelizmente, a espirometria de turno cruzado de um dia, realizada antes e depois do turno de trabalho, não é sensível nem específica na determinação da obstrução das vias aéreas associada ao trabalho. É provável que, se múltiplas espirometrias forem realizadas todos os dias durante e após vários dias de trabalho, a precisão diagnóstica possa ser melhorada, mas isso ainda não foi adequadamente avaliado.
Devido às dificuldades com a espirometria de turno cruzado, a medição seriada do PFE tornou-se uma importante técnica diagnóstica para OA. Usando um medidor portátil barato, as medições do PFE são registradas a cada duas horas, durante as horas de vigília. Para melhorar a sensibilidade, as medições devem ser feitas durante um período em que o trabalhador está exposto aos agentes causais suspeitos no trabalho e apresenta um padrão de sintomas relacionados ao trabalho. Três repetições são realizadas de cada vez, e as medições são feitas todos os dias no trabalho e fora do trabalho. As medições devem continuar por pelo menos 16 dias consecutivos (por exemplo, duas semanas de trabalho de cinco dias e 3 fins de semana de folga) se o paciente puder tolerar com segurança continuar trabalhando. As medições do PEF são registradas em um diário, juntamente com a anotação das horas de trabalho, sintomas, uso de medicamentos broncodilatadores e exposições significativas. Para facilitar a interpretação, os resultados do diário devem ser plotados graficamente. Certos padrões sugerem OA, mas nenhum é patognomônico, e a interpretação por um leitor experiente costuma ser útil. As vantagens do teste de PEF serial são o baixo custo e a correlação razoável com os resultados do teste de provocação brônquica. As desvantagens incluem o grau significativo de cooperação necessária do paciente, incapacidade de confirmar definitivamente que os dados são precisos, falta de método padronizado de interpretação e a necessidade de alguns pacientes tirarem 1 ou 2 semanas consecutivas de folga para mostrar melhora significativa. Espirômetros portáteis de registro eletrônico projetados para automonitoramento do paciente, quando disponíveis, podem abordar algumas das desvantagens do PFE serial.
Medicamentos para asma tendem a reduzir o efeito das exposições de trabalho nas medidas de fluxo de ar. No entanto, não é aconselhável interromper os medicamentos durante o monitoramento do fluxo de ar no trabalho. Em vez disso, o paciente deve ser mantido com uma dosagem segura mínima constante de medicamentos anti-inflamatórios durante todo o processo diagnóstico, com monitoramento rigoroso dos sintomas e do fluxo aéreo, e o uso de broncodilatadores de curta duração para controlar os sintomas deve ser anotado no diário.
A não observação de alterações relacionadas ao trabalho no PFE enquanto o paciente está trabalhando em horário rotineiro não exclui o diagnóstico de OA, pois muitos pacientes precisarão de mais de dois dias de semana para apresentar melhora significativa do PFE. Nesse caso, uma tentativa diagnóstica de afastamento prolongado do trabalho (Etapa 5) deve ser considerada. Caso o paciente ainda não tenha feito o teste quantitativo para NBR e não tenha contra-indicação médica, deve ser feito neste momento, imediatamente após pelo menos duas semanas de exposição no local de trabalho.
Etapa 5: Avaliação clínica da asma fora do trabalho ou teste diagnóstico de afastamento prolongado do trabalho
Esta etapa consiste na conclusão do diário PEF serial de 2 horas por pelo menos 9 dias consecutivos de afastamento do trabalho (por exemplo, 5 dias de afastamento do trabalho mais fins de semana antes e depois). Se esse registro, comparado com o diário seriado do PFE no trabalho, não for suficiente para o diagnóstico de OA, ele deve ser continuado por uma segunda semana consecutiva de afastamento do trabalho. Após 2 ou mais semanas longe do trabalho, testes quantitativos para NBR podem ser realizados e comparados com NBR durante o trabalho. Se o PFE serial ainda não tiver sido feito durante pelo menos duas semanas de trabalho, um teste diagnóstico de retorno ao trabalho (ver Etapa 4) pode ser realizado, após aconselhamento detalhado e em contato próximo com o médico assistente. A etapa 5 costuma ser extremamente importante para confirmar ou excluir o diagnóstico de OA, embora também possa ser a etapa mais difícil e cara. Se for tentada uma remoção prolongada do trabalho, é melhor maximizar o rendimento e a eficiência do diagnóstico incluindo PEF, FEV1, e testes NBR em uma avaliação abrangente. Visitas médicas semanais para aconselhamento e revisão do gráfico PFE podem ajudar a garantir resultados completos e precisos. Se, após monitorar o paciente por pelo menos duas semanas no trabalho e duas semanas fora dele, as evidências diagnósticas ainda não forem suficientes, o Passo 6 deve ser considerado a seguir, se disponível e viável.
Etapa 6: teste de desafio brônquico específico ou teste de desafio no local de trabalho
O teste de provocação brônquica específico usando uma câmara de exposição e níveis de exposição padronizados foi rotulado como o “padrão ouro” para o diagnóstico de OA. As vantagens incluem a confirmação definitiva da OA com a capacidade de identificar a resposta asmática a níveis sub-irritantes de agentes sensibilizantes específicos, que podem ser escrupulosamente evitados. De todos os métodos diagnósticos, é o único que pode distinguir com segurança a asma induzida por sensibilizadores da provocação por irritantes. Vários problemas com esta abordagem incluíram o custo inerente do procedimento, exigência geral de observação rigorosa ou hospitalização por vários dias e disponibilidade em poucos centros especializados. Podem ocorrer falsos negativos se a metodologia padronizada não estiver disponível para todos os agentes suspeitos, se houver suspeita dos agentes errados ou se tiver decorrido muito tempo entre a última exposição e o teste. Podem ocorrer falsos positivos se níveis irritantes de exposição forem obtidos inadvertidamente. Por essas razões, o teste de broncoprovocação específico para OA continua sendo um procedimento de pesquisa na maioria das localidades.
O teste de desafio no local de trabalho envolve espirometria em série treinada por um técnico no local de trabalho, realizada em intervalos frequentes (por exemplo, de hora em hora) antes e durante a exposição de um dia de trabalho aos agentes ou processos causais suspeitos. Pode ser mais sensível do que o teste de provocação brônquica específico porque envolve exposições da “vida real”, mas como a obstrução das vias aéreas pode ser desencadeada por irritantes e também por agentes sensibilizantes, testes positivos não indicam necessariamente sensibilização. Também requer cooperação do empregador e muito tempo do técnico com um espirômetro móvel. Ambos os procedimentos apresentam algum risco de precipitar um ataque asmático grave e, portanto, devem ser realizados sob supervisão rigorosa de especialistas experientes nos procedimentos.
Tratamento e Prevenção
O manejo da OA inclui intervenções médicas e preventivas para pacientes individuais, bem como medidas de saúde pública em locais de trabalho identificados como de alto risco para OA. O tratamento médico é semelhante ao da asma não ocupacional e é bem revisado em outros lugares (NAEP 1991). O tratamento médico sozinho raramente é adequado para controlar os sintomas de forma ideal, e a intervenção preventiva por controle ou cessação da exposição é parte integrante do tratamento. Este processo começa com um diagnóstico preciso e identificação de exposições e condições causais. Na OA induzida por sensibilizador, a redução da exposição ao sensibilizador geralmente não resulta na resolução completa dos sintomas. Episódios asmáticos graves ou agravamento progressivo da doença podem ser causados por exposições a concentrações muito baixas do agente e recomenda-se a cessação completa e permanente da exposição. O encaminhamento oportuno para reabilitação vocacional e retreinamento profissional pode ser um componente necessário do tratamento para alguns pacientes. Se a cessação completa da exposição for impossível, pode ser uma opção uma redução substancial da exposição acompanhada de monitoramento e tratamento médico rigoroso, embora essa redução da exposição nem sempre seja viável e a segurança a longo prazo dessa abordagem não tenha sido testada. Por exemplo, seria difícil justificar a toxicidade do tratamento prolongado com corticosteroides sistêmicos para permitir que o paciente continue no mesmo emprego. Para asma induzida e/ou desencadeada por irritantes, a resposta à dose pode ser mais previsível, e a redução dos níveis de exposição a irritantes, acompanhada de monitoramento médico rigoroso, pode ser menos arriscada e mais provável de ser eficaz do que para OA induzida por sensibilizadores. Se o paciente continuar a trabalhar em condições modificadas, o acompanhamento médico deve incluir consultas médicas frequentes com revisão do diário PFE, acesso bem planejado aos serviços de emergência e espirometria seriada e/ou teste de provocação com metacolina, conforme apropriado.
Quando um determinado local de trabalho é suspeito de ser de alto risco, devido à ocorrência de um caso sentinela de OA ou ao uso de agentes conhecidos como causadores de asma, os métodos de saúde pública podem ser muito úteis. O reconhecimento precoce e o tratamento eficaz e a prevenção da incapacidade dos trabalhadores com OA existente e a prevenção de novos casos são prioridades claras. A identificação do(s) agente(s) causal(is) específico(s) e dos processos de trabalho é importante. Uma abordagem inicial prática é uma pesquisa por questionário no local de trabalho, avaliando os critérios A, B, C e D1 ou D5 na definição de caso de OA. Essa abordagem pode identificar indivíduos para os quais uma avaliação clínica adicional pode ser indicada e ajudar a identificar possíveis agentes ou circunstâncias causais. A avaliação dos resultados do grupo pode ajudar a decidir se uma investigação ou intervenção adicional no local de trabalho é indicada e, em caso afirmativo, fornecer orientação valiosa para direcionar futuros esforços de prevenção da maneira mais eficaz e eficiente. Uma pesquisa por questionário não é adequada, no entanto, para estabelecer diagnósticos médicos individuais, uma vez que os valores preditivos positivos de questionários para OA não são altos o suficiente. Se for necessário um maior nível de certeza diagnóstica, a triagem médica utilizando procedimentos de diagnóstico, como espirometria, teste quantitativo para NBR, registro seriado de PFE e teste imunológico também pode ser considerada. Em locais de trabalho com problemas conhecidos, programas contínuos de vigilância e triagem podem ser úteis. No entanto, a exclusão diferencial de trabalhadores assintomáticos com histórico de atopia ou outros fatores de suscetibilidade potenciais de locais de trabalho considerados de alto risco resultaria na remoção de um grande número de trabalhadores para prevenir relativamente poucos casos de OA e não é apoiado pela literatura atual.
O controle ou eliminação de exposições causais e a prevenção e gerenciamento adequado de derramamentos ou episódios de exposições de alto nível podem levar à prevenção primária eficaz de sensibilização e OA em colegas de trabalho do caso sentinela. A hierarquia usual de controle de exposição de substituição, controles de engenharia e administrativos e equipamentos de proteção individual, bem como a educação de trabalhadores e gerentes, devem ser implementadas conforme apropriado. Os empregadores proativos iniciarão ou participarão de algumas ou de todas essas abordagens, mas no caso de uma ação preventiva inadequada ser tomada e os trabalhadores continuarem em alto risco, as agências governamentais de fiscalização podem ser úteis.
Deficiência e Incapacidade
Comprometimento médico é uma anormalidade funcional resultante de uma condição médica. Incapacidade refere-se ao efeito total da deficiência médica na vida do paciente e é influenciado por muitos fatores não médicos, como idade e status socioeconômico (ATS 1995).
A avaliação da deficiência médica é feita pelo médico e pode incluir um índice de deficiência calculado, bem como outras considerações clínicas. O índice de comprometimento é baseado em (1) grau de limitação do fluxo aéreo após broncodilatador, (2) grau de reversibilidade da limitação do fluxo aéreo com broncodilatador ou grau de hiperresponsividade das vias aéreas em testes quantitativos para NBR e (3) medicação mínima necessária para controlar asma. O outro componente importante da avaliação da deficiência médica é o julgamento médico da capacidade do paciente para trabalhar no ambiente de trabalho que causa a asma. Por exemplo, um paciente com OA induzida por sensibilizador pode ter uma deficiência médica que é altamente específica do agente ao qual ele ou ela se tornou sensibilizado. O trabalhador que apresenta sintomas apenas quando exposto a esse agente pode estar apto a trabalhar em outros empregos, mas permanentemente incapacitado para o trabalho específico para o qual tem mais treinamento e experiência.
A avaliação da incapacidade decorrente da asma (incluindo OA) requer a consideração da deficiência médica, bem como de outros fatores não médicos que afetam a capacidade de trabalhar e funcionar na vida cotidiana. A avaliação da incapacidade é inicialmente feita pelo médico, que deve identificar todos os fatores que afetam o impacto da deficiência na vida do paciente. Muitos fatores, como ocupação, nível educacional, posse de outras habilidades comercializáveis, condições econômicas e outros fatores sociais podem levar a níveis variados de deficiência em indivíduos com o mesmo nível de deficiência médica. Essas informações podem ser usadas pelos administradores para determinar a incapacidade para fins de compensação.
A deficiência e a incapacidade podem ser classificadas como temporárias ou permanentes, dependendo da probabilidade de melhora significativa e se os controles de exposição eficazes são implementados com sucesso no local de trabalho. Por exemplo, um indivíduo com OA induzida por sensibilizador é geralmente considerado permanentemente, totalmente incapacitado para qualquer trabalho que envolva exposição ao agente causal. Se os sintomas desaparecerem parcial ou totalmente após o término da exposição, esses indivíduos podem ser classificados com menos ou nenhum comprometimento para outros trabalhos. Muitas vezes, isso é considerado deficiência/incapacidade parcial permanente, mas a terminologia pode variar. Um indivíduo com asma desencadeada de forma dose-dependente por irritantes no local de trabalho seria considerado como tendo prejuízo temporário enquanto sintomático, e menos ou nenhum prejuízo se controles de exposição adequados forem instalados e forem eficazes na redução ou eliminação dos sintomas. Se não forem implementados controles efetivos de exposição, o mesmo indivíduo pode ter que ser considerado incapacitado permanentemente para trabalhar naquele trabalho, com recomendação para afastamento médico. Se necessário, a avaliação repetida para comprometimento/incapacidade de longo prazo pode ser realizada dois anos após a exposição ser reduzida ou encerrada, quando se espera que a melhora da OA tenha estabilizado. Se o paciente continuar a trabalhar, o acompanhamento médico deve ser contínuo e a reavaliação do comprometimento/incapacidade deve ser repetida conforme necessário.
Os trabalhadores que se tornam incapacitados por OA ou WAA podem se qualificar para compensação financeira por despesas médicas e/ou salários perdidos. Além de reduzir diretamente o impacto financeiro da deficiência sobre os trabalhadores individuais e suas famílias, pode ser necessária uma compensação para fornecer tratamento médico adequado, iniciar intervenção preventiva e obter reabilitação profissional. A compreensão do trabalhador e do médico sobre questões médico-legais específicas pode ser importante para garantir que a avaliação diagnóstica atenda aos requisitos locais e não resulte no comprometimento dos direitos do trabalhador afetado.
Embora as discussões sobre economia de custos freqüentemente se concentrem na inadequação dos sistemas de compensação, reduzir genuinamente a carga financeira e de saúde pública imposta à sociedade pela OA e WAA dependerá não apenas de melhorias nos sistemas de compensação, mas, mais importante, da eficácia dos sistemas implantados para identificar e corrigir, ou prevenir totalmente, as exposições no local de trabalho que estão causando o aparecimento de novos casos de asma.
Conclusões
A OA tornou-se a doença respiratória ocupacional mais prevalente em muitos países. É mais comum do que geralmente reconhecido, pode ser grave e incapacitante e geralmente evitável. O reconhecimento precoce e intervenções preventivas eficazes podem reduzir substancialmente o risco de incapacidade permanente e os altos custos humanos e financeiros associados à asma crônica. Por muitas razões, a OA merece atenção mais ampla entre médicos, especialistas em saúde e segurança, pesquisadores, formuladores de políticas de saúde, higienistas industriais e outros interessados na prevenção de doenças relacionadas ao trabalho.
Mais...
Doenças Causadas por Poeiras Orgânicas
Poeira Orgânica e Doenças
As poeiras de origem vegetal, animal e microbiana sempre fizeram parte do ambiente humano. Quando os primeiros organismos aquáticos se mudaram para a terra há cerca de 450 milhões de anos, logo desenvolveram sistemas de defesa contra as muitas substâncias nocivas presentes no ambiente terrestre, a maioria delas de origem vegetal. A exposição a esse ambiente geralmente não causa problemas específicos, embora as plantas contenham várias substâncias extremamente tóxicas, principalmente aquelas presentes ou produzidas por fungos.
Durante o desenvolvimento da civilização, as condições climáticas em algumas partes do mundo exigiram que certas atividades fossem realizadas em ambientes fechados. A debulha nos países escandinavos era realizada dentro de casa durante o inverno, prática mencionada por cronistas da antiguidade. O fechamento de processos empoeirados levou a doenças entre as pessoas expostas, e um dos primeiros relatos publicados sobre isso é do bispo dinamarquês Olaus Magnus (1555, conforme citado por Rask-Andersen 1988). Ele descreveu uma doença entre debulhadores na Escandinávia da seguinte forma:
“Ao separar o grão do joio, deve-se tomar cuidado para escolher um momento em que haja um vento adequado que varra o pó do grão, de modo que não danifique os órgãos vitais dos debulhadores. Essa poeira é tão fina que penetra quase imperceptivelmente na boca e se acumula na garganta. Se isso não for resolvido rapidamente bebendo cerveja fresca, o debulhador nunca mais ou apenas por um curto período comerá o que debulhou.
Com a introdução do processamento mecânico de materiais orgânicos, o tratamento de grandes quantidades de materiais em ambientes fechados com pouca ventilação levou a altos níveis de poeira no ar. As descrições do bispo Olaus Magnus e mais tarde de Ramazzini (1713) foram seguidas por vários relatos sobre doenças e poeiras orgânicas no século XIX, particularmente entre trabalhadores de fábricas de algodão (Leach 1863; Prausnitz 1936). Mais tarde, também foi descrita a doença pulmonar específica comum entre os agricultores que manuseiam materiais mofados (Campbell 1932).
Durante as últimas décadas, um grande número de relatórios sobre doenças entre pessoas expostas a poeiras orgânicas foi publicado. Inicialmente, a maioria deles baseava-se em pessoas que procuravam ajuda médica. Os nomes das doenças, quando publicados, eram freqüentemente relacionados ao ambiente particular onde a doença foi reconhecida pela primeira vez, resultando em uma desconcertante variedade de nomes, como pulmão do fazendeiro, pulmão do cultivador de cogumelos, pulmão marrom e febre do umidificador.
Com o advento da epidemiologia moderna, números mais confiáveis foram obtidos para a incidência de doenças respiratórias ocupacionais relacionadas à poeira orgânica (Rylander, Donham e Peterson 1986; Rylander e Peterson 1990). Também houve avanço na compreensão dos mecanismos patológicos subjacentes a essas doenças, particularmente a resposta inflamatória (Henson e Murphy 1989). Isso abriu caminho para uma imagem mais coerente das doenças causadas por poeiras orgânicas (Rylander e Jacobs 1997).
A seguir serão descritos os diferentes ambientes de poeira orgânica onde a doença foi relatada, as próprias entidades da doença, a clássica doença da bissinose e medidas preventivas específicas.
Ambientes
As poeiras orgânicas são partículas transportadas pelo ar de origem vegetal, animal ou microbiana. A Tabela 1 lista exemplos de ambientes, processos de trabalho e agentes que envolvem risco de exposição a poeiras orgânicas.
Tabela 1. Exemplos de fontes de perigos de exposição a poeira orgânica
Agricultura
Manuseio de grãos, feno ou outras culturas
Processamento de cana-de-açúcar
Estufas
Silos
Animais
Edifícios de confinamento de suínos/laticínios
Aviários e plantas de processamento
Animais de laboratório, animais de fazenda e animais de estimação
Processamento de resíduos
Água de esgoto e lodo
Lixo doméstico
Compostagem
Indústria
Processamento de fibras vegetais (algodão, linho, cânhamo, juta, sisal)
Fermentação
Madeira e processamento de madeira
Padarias
Processamento de biotecnologia
Edifícios
Água contaminada em umidificadores
Crescimento microbiano em estruturas ou em dutos de ventilação
Agentes
Agora é entendido que os agentes específicos nas poeiras são a principal razão pela qual a doença se desenvolve. Poeiras orgânicas contêm uma infinidade de agentes com potenciais efeitos biológicos. Alguns dos principais agentes são encontrados na tabela 2.
Tabela 2. Principais agentes em poeiras orgânicas com potencial atividade biológica
Agentes vegetais
Taninos
histamina
ácido plicatico
Alcaloides (por exemplo, nicotina)
Citocalasinas
Agentes animais
Proteínas
Enzimas
agentes microbianos
Endotoxinas
(1→3)–β–D-glucanos
Proteases
Micotoxinas
O papel relativo de cada um desses agentes, isoladamente ou em combinação com outros, para o desenvolvimento da doença é praticamente desconhecido. A maioria das informações disponíveis refere-se a endotoxinas bacterianas que estão presentes em todas as poeiras orgânicas.
As endotoxinas são compostos lipopolissacarídeos que estão ligados à superfície celular externa de bactérias Gram-negativas. A endotoxina tem uma ampla variedade de propriedades biológicas. Após a inalação, causa uma inflamação aguda (Snella e Rylander 1982; Brigham e Meyrick 1986). Um influxo de neutrófilos (leucócitos) no pulmão e nas vias aéreas é a marca registrada dessa reação. É acompanhada pela ativação de outras células e secreção de mediadores inflamatórios. Após exposições repetidas, a inflamação diminui (adaptação). A reação é limitada à mucosa das vias aéreas, não havendo envolvimento extenso do parênquima pulmonar.
Outro agente específico na poeira orgânica é o (1→3)-β-D-glucano. Este é um composto de poliglicose presente na estrutura da parede celular de fungos e algumas bactérias. Aumenta a resposta inflamatória causada pela endotoxina e altera a função das células inflamatórias, particularmente macrófagos e células T (Di Luzio 1985; Fogelmark et al. 1992).
Outros agentes específicos presentes nas poeiras orgânicas são proteínas, taninos, proteases e outras enzimas e toxinas de bolores. Muito poucos dados estão disponíveis sobre as concentrações desses agentes em poeiras orgânicas. Vários dos agentes específicos em poeiras orgânicas, como proteínas e enzimas, são alérgenos.
Doenças
As doenças causadas por poeiras orgânicas são apresentadas na tabela 3 com os números correspondentes da Classificação Internacional de Doenças (CID) (Rylander e Jacobs 1994).
Tabela 3. Doenças induzidas por poeiras orgânicas e seus códigos CID
Bronquite e pneumonite (CID J40)
Pneumonite tóxica (febre por inalação, síndrome de poeira orgânica tóxica)
Inflamação das vias aéreas (inflamação da membrana mucosa)
Bronquite crônica (CID J42)
Pneumonite por hipersensibilidade (alveolite alérgica) (CID J67)
Asma (CID J45)
Rinite, conjuntivite
A principal via de exposição para poeiras orgânicas é por inalação e, consequentemente, os efeitos nos pulmões receberam a maior parte da atenção na pesquisa, bem como no trabalho clínico. Há, no entanto, um crescente corpo de evidências de estudos epidemiológicos publicados e relatos de casos, bem como relatos anedóticos, de que também ocorrem efeitos sistêmicos. O mecanismo envolvido parece ser uma inflamação local no local alvo, o pulmão, e uma subsequente liberação de citocinas com efeitos sistêmicos (Dunn 1992; Michel et al. 1991) ou um efeito no epitélio do intestino (Axmacher et al . 1991). Os efeitos clínicos não respiratórios são febre, dores nas articulações, efeitos neurossensoriais, problemas de pele, doenças intestinais, fadiga e dor de cabeça.
As diferentes entidades de doença descritas na tabela 3 são fáceis de diagnosticar em casos típicos, e a patologia subjacente é distintamente diferente. Na vida real, no entanto, um trabalhador que tenha uma doença devido à exposição à poeira orgânica, muitas vezes apresenta uma mistura de diferentes entidades de doença. Uma pessoa pode ter inflamação das vias aéreas por vários anos, desenvolver repentinamente asma e, além disso, apresentar sintomas de pneumonia tóxica durante uma exposição particularmente intensa. Outra pessoa pode ter pneumonite de hipersensibilidade subclínica com linfocitose nas vias aéreas e desenvolver pneumonia tóxica durante uma exposição particularmente intensa.
Um bom exemplo da mistura de entidades patológicas que podem aparecer é a bissinose. Esta doença foi descrita pela primeira vez nas fábricas de algodão, mas as entidades individuais da doença também são encontradas em outros ambientes de poeira orgânica. Segue uma visão geral da doença.
Bissinose
A doença
A bissinose foi descrita pela primeira vez em 1800, e um relato clássico envolvendo trabalhos clínicos e experimentais foi feito por Prausnitz (1936). Ele descreveu os sintomas entre os trabalhadores da fábrica de algodão da seguinte forma:
“Depois de trabalhar durante anos sem nenhum problema apreciável, exceto uma pequena tosse, os trabalhadores da fábrica de algodão notam um súbito agravamento de sua tosse, que se torna seca e extremamente irritante¼ Esses ataques geralmente ocorrem às segundas-feiras ¼, mas gradualmente os sintomas começam a se espalhar nos dias seguintes da semana; com o tempo a diferença desaparece e eles sofrem continuamente.”
As primeiras investigações epidemiológicas foram realizadas na Inglaterra na década de 1950 (Schilling et al. 1955; Schilling 1956). O diagnóstico inicial foi baseado no aparecimento de um aperto torácico típico na manhã de segunda-feira, diagnosticado por meio de um questionário (Roach e Schilling 1960). Foi desenvolvido um esquema para classificar a gravidade da bissinose com base no tipo e na periodicidade dos sintomas (Mekky, Roach e Schilling 1967; Schilling et al. 1955). A duração da exposição foi utilizada como medida da dose e esta foi relacionada com a gravidade da resposta. Com base em entrevistas clínicas de um grande número de trabalhadores, esse esquema de classificação foi posteriormente modificado para refletir com mais precisão os intervalos de tempo para a diminuição do VEF1 (Berry et al. 1973).
Em um estudo, foi encontrada uma diferença na prevalência de bissinose em fábricas que processam diferentes tipos de algodão (Jones et al. 1979). As fábricas que usam algodão de alta qualidade para produzir fios mais finos tiveram uma menor prevalência de bissinose do que as fábricas que produzem fios grossos e usam algodão de qualidade inferior. Assim, além da intensidade e duração da exposição, ambas variáveis relacionadas à dose, o tipo de poeira tornou-se uma variável importante para avaliar a exposição. Mais tarde, foi demonstrado que as diferenças na resposta dos trabalhadores expostos a algodão grosso e médio dependiam não apenas do tipo de algodão, mas de outras variáveis que afetam a exposição, incluindo: variáveis de processamento, como velocidade de cardagem, variáveis ambientais, como umidificação e ventilação e variáveis de fabricação, como diferentes tratamentos de fios (Berry et al. 1973).
O próximo refinamento da relação entre a exposição ao pó de algodão e uma resposta (seja sintomas ou medidas objetivas da função pulmonar) foram os estudos dos Estados Unidos, comparando aqueles que trabalhavam em algodão 100% com trabalhadores que usavam o mesmo algodão, mas em um Mistura 50:50 com sintéticos e trabalhadores sem exposição ao algodão (Merchant et al. 1973). Os trabalhadores expostos ao algodão 100% tiveram a maior prevalência de bissinose independente do tabagismo, um dos fatores de confusão da exposição ao pó de algodão. Essa relação semiquantitativa entre dose e resposta ao pó de algodão foi refinada em um grupo de trabalhadores têxteis estratificados por sexo, tabagismo, área de trabalho e tipo de fábrica. Foi observada uma relação em cada uma dessas categorias entre a concentração de poeira nas faixas de poeira mais baixas e a prevalência de bissinose e/ou alteração no volume expiratório forçado em um segundo (VEF1).
Em investigações posteriores, o VEF1 a diminuição ao longo do turno de trabalho tem sido usada para avaliar os efeitos da exposição e também faz parte do Padrão de Pó de Algodão dos EUA.
A bissinose foi por muito tempo considerada uma doença peculiar com uma mistura de diferentes sintomas e nenhum conhecimento da patologia específica. Alguns autores sugeriram que era uma asma ocupacional (Bouhuys 1976). Uma reunião do grupo de trabalho em 1987 analisou a sintomatologia e a patologia da doença (Rylander et al. 1987). Concordou-se que a doença envolvia várias entidades clínicas, geralmente relacionadas à exposição a poeiras orgânicas.
Pneumonite tóxica pode aparecer na primeira vez que um funcionário trabalha na fábrica, principalmente quando trabalha nas seções de abertura, sopro e cardagem (Trice 1940). Embora a habituação se desenvolva, os sintomas podem reaparecer após uma exposição extraordinariamente intensa mais tarde.
inflamação das vias aéreas é a doença mais disseminada e aparece em diferentes graus de gravidade, desde uma leve irritação no nariz e vias aéreas até tosse seca severa e dificuldades respiratórias. A inflamação causa constrição das vias aéreas e redução do VEF1. A capacidade de resposta das vias aéreas é aumentada conforme medido com um teste de provocação com metacolina ou histamina. Discute-se se a inflamação das vias aéreas deve ser aceita como uma entidade patológica isoladamente ou se representa apenas um sintoma. Como o quadro clínico de tosse intensa com estreitamento das vias aéreas pode levar à diminuição da capacidade para o trabalho, justifica-se considerá-la uma doença ocupacional.
A inflamação contínua das vias aéreas ao longo de vários anos pode evoluir para bronquite crônica, particularmente entre os trabalhadores altamente expostos nas áreas de sopro e cardagem. O quadro clínico seria de doença pulmonar obstrutiva crônica (DPOC).
Asma ocupacional desenvolve-se em uma pequena porcentagem da força de trabalho, mas geralmente não é diagnosticada em estudos transversais, pois os trabalhadores são forçados a deixar o trabalho por causa da doença. Pneumonite de hipersensibilidade não foi detectado em nenhum dos estudos epidemiológicos realizados, nem houve relatos de casos relacionados à exposição ao pó de algodão. A ausência de pneumonite de hipersensibilidade pode ser devida à quantidade relativamente baixa de bolores no algodão, uma vez que o algodão mofado não é aceitável para processamento.
Um sentimento subjetivo de aperto no peito, mais comum às segundas-feiras, é o sintoma clássico da exposição ao pó de algodão (Schilling et al. 1955). Não é, entretanto, uma característica exclusiva da exposição ao pó de algodão, pois também aparece entre pessoas que trabalham com outros tipos de pó orgânico (Donham et al. 1989). O aperto no peito se desenvolve lentamente ao longo de vários anos, mas também pode ser induzido em pessoas não expostas anteriormente, desde que o nível de dose seja alto (Haglind e Rylander 1984). A presença de aperto no peito não está diretamente relacionada à diminuição do VEF1.
A patologia por trás do aperto no peito não foi explicada. Sugeriu-se que os sintomas se deviam a um aumento da adesividade das plaquetas que se acumulam nos capilares pulmonares e aumentam a pressão da artéria pulmonar. É provável que o aperto no peito envolva algum tipo de sensibilização celular, pois são necessárias exposições repetidas para que o sintoma se desenvolva. Esta hipótese é apoiada por resultados de estudos sobre monócitos sanguíneos de trabalhadores do algodão (Beijer et al. 1990). Uma maior capacidade de produzir fator pró-coagulante, indicativo de sensibilização celular, foi encontrada entre os trabalhadores do algodão em comparação com os controles.
O ambiente
A doença foi originalmente descrita entre trabalhadores de fábricas de algodão, linho e cânhamo macio. Na primeira fase do tratamento do algodão nas fábricas – abertura do fardo, sopro e cardagem – mais da metade dos trabalhadores pode apresentar sintomas de aperto no peito e inflamação das vias aéreas. A incidência diminui à medida que o algodão é processado, refletindo a limpeza sucessiva do agente causador da fibra. A bissinose foi descrita em todos os países onde foram realizadas investigações em fábricas de algodão. Alguns países como a Austrália têm, no entanto, números de incidência excepcionalmente baixos (Gun et al. 1983).
Atualmente, há evidências uniformes de que as endotoxinas bacterianas são o agente causador da pneumonia tóxica e inflamação das vias aéreas (Castellan et al. 1987; Pernis et al. 1961; Rylander, Haglind e Lundholm 1985; Rylander e Haglind 1986; Herbert et al. 1992; Sigsgaard e outros 1992). As relações dose-resposta foram descritas e os sintomas típicos foram induzidos pela inalação de endotoxina purificada (Rylander et al. 1989; Michel et al. 1995). Embora isso não exclua a possibilidade de que outros agentes possam contribuir para a patogênese, as endotoxinas podem servir como marcadores de risco de doença. É improvável que as endotoxinas estejam relacionadas ao desenvolvimento de asma ocupacional, mas podem atuar como adjuvantes para potenciais alérgenos no pó de algodão.
O caso
O diagnóstico de bissinose é feito classicamente por meio de questionários com a pergunta específica “Você sente um aperto no peito e, em caso afirmativo, em que dia da semana?”. Pessoas com aperto no peito na segunda-feira de manhã são classificadas como bissinóticas de acordo com um esquema sugerido por Schilling (1956). A espirometria pode ser realizada e, de acordo com as diferentes combinações de aperto no peito e diminuição do VEF1, o esquema de diagnóstico ilustrado na tabela 4 evoluiu.
Tabela 4. Critérios diagnósticos para bissinose
Grau ½. Aperto no peito no primeiro dia de algumas semanas de trabalho
Grau 1. Aperto no peito no primeiro dia de cada semana de trabalho
Grau 2. Aperto no peito no primeiro e nos demais dias da semana de trabalho
Grau 3. Sintomas de grau 2 acompanhados por evidência de incapacidade permanente na forma de diminuição da intolerância ao esforço e/ou redução da capacidade ventilatória
foliar
O tratamento nos estágios leves da bissinose é sintomático, e a maioria dos trabalhadores aprende a conviver com o leve aperto no peito e broncoconstrição que sentem às segundas-feiras ou ao limpar máquinas ou realizar tarefas semelhantes com uma exposição maior do que o normal. Estágios mais avançados de inflamação das vias aéreas ou aperto regular no peito vários dias da semana requerem transferência para operações menos empoeiradas. A presença de asma ocupacional requer principalmente mudança de trabalho.
Prevenção
A prevenção em geral é tratada em detalhes em outras partes do enciclopédia. Os princípios básicos de prevenção em termos de substituição do produto, limitação da exposição, proteção do trabalhador e triagem de doenças também se aplicam à exposição à poeira do algodão.
Em relação aos substitutos de produtos, tem sido sugerido o uso de algodão com baixo índice de contaminação bacteriana. Uma prova inversa deste conceito é encontrada em relatórios de 1863 onde a mudança para o algodão sujo provocou um aumento na prevalência de sintomas entre os trabalhadores expostos (Leach 1863). Existe também a possibilidade de mudança para outras fibras, nomeadamente fibras sintéticas, embora nem sempre seja viável do ponto de vista do produto. Não há atualmente nenhuma técnica aplicada na produção para diminuir o teor de endotoxina das fibras de algodão.
Com relação à redução de poeira, programas bem-sucedidos foram implementados nos Estados Unidos e em outros lugares (Jacobs 1987). Tais programas são caros e os custos para remoção de pó altamente eficiente podem ser proibitivos para os países em desenvolvimento (Corn 1987).
Em relação ao controle de exposição, o nível de poeira não é uma medida suficientemente precisa do risco de exposição. Dependendo do grau de contaminação com bactérias Gram-negativas e, portanto, endotoxinas, um determinado nível de poeira pode ou não estar associado a um risco. Para endotoxinas, nenhuma diretriz oficial foi estabelecida. Tem sido sugerido que um nível de 200 ng/m3 é o limiar para pneumonia tóxica, 100 a 200 ng/m3 para constrição aguda das vias aéreas durante o turno de trabalho e 10 ng/m3 para inflamação das vias aéreas (Rylander e Jacobs 1997).
O conhecimento sobre os fatores de risco e as consequências da exposição são importantes para a prevenção. A base de informações expandiu-se rapidamente nos últimos anos, mas muito dela ainda não está presente em livros didáticos ou outras fontes facilmente disponíveis. Outro problema é que os sintomas e achados em doenças respiratórias induzidas por poeira orgânica são inespecíficos e ocorrem normalmente na população. Eles podem, portanto, não ser diagnosticados corretamente nos estágios iniciais.
A disseminação adequada do conhecimento sobre os efeitos do algodão e outras poeiras orgânicas requer o estabelecimento de programas de treinamento apropriados. Estas devem ser dirigidas não apenas aos trabalhadores com exposição potencial, mas também aos empregadores e profissionais de saúde, particularmente inspetores e engenheiros de saúde ocupacional. As informações devem incluir identificação da fonte, sintomas e descrição da doença e métodos de proteção. Um trabalhador informado pode reconhecer mais prontamente os sintomas relacionados ao trabalho e se comunicar de forma mais eficaz com um profissional de saúde. Em relação à vigilância e triagem em saúde, os questionários são um importante instrumento a ser utilizado. Várias versões de questionários projetados especificamente para diagnosticar doenças induzidas por poeira orgânica foram relatadas na literatura (Rylander, Peterson e Donham 1990; Schwartz et al. 1995). O teste de função pulmonar também é uma ferramenta útil para vigilância e diagnóstico. As medições da responsividade das vias aéreas têm se mostrado úteis (Rylander e Bergström 1993; Carvalheiro et al. 1995). Outras ferramentas diagnósticas, como medidas de mediadores inflamatórios ou atividade celular, ainda estão em fase de pesquisa.
Doença do berílio
A berílio doença é um distúrbio sistêmico envolvendo múltiplos órgãos, sendo as manifestações pulmonares as mais proeminentes e comuns. Ocorre na exposição ao berílio em sua forma de liga ou em um de seus vários compostos químicos. A via de exposição é por inalação e a doença pode ser aguda ou crônica. A doença aguda é extremamente rara atualmente, e nenhuma foi relatada desde o primeiro uso industrial generalizado de berílio na década de 1940, depois que medidas de higiene industrial foram implementadas para limitar exposições a altas doses. A berílio doença crônica continua a ser relatada.
Berílio, Ligas e Compostos
O berílio, substância industrial suspeita de potencial cancerígeno, destaca-se por sua leveza, alta resistência à tração e resistência à corrosão. A Tabela 1 descreve as propriedades do berílio e seus compostos.
Tabela 1. Propriedades do berílio e seus compostos
|
Fórmula |
Específico |
Ponto de fusão/ebulição (ºC) |
Solubilidade |
Descrição |
|
|
Berílio (Be) |
9.01 (aw) |
1.85 |
1,298 ± 5/2,970 |
- |
Cinza ao metal prateado |
|
Óxido de berílio (BeO) |
25 |
3.02 |
2,530±30/— |
Solúvel em ácidos e álcalis; Insolúvel em água |
Pó amorfo branco |
|
Fluoreto de berílio1 (BeF2 ) |
47.02 |
1.99 |
Sublime 800 °C |
Facilmente solúvel em água; pouco solúvel em álcool etílico |
Sólido higroscópico |
|
cloreto de berílio2 (BeCl2 ) |
79.9 |
1.90 |
405/520 |
Muito solúvel em água; solúvel em álcool etílico, benzeno, éter etílico e dissulfeto de carbono |
Cristais deliquescentes brancos ou ligeiramente amarelos |
|
nitrato de berílio3 (Ser(NÃO3 )2 · 3H2 O) |
187.08 |
1.56 |
60/142 |
Solúvel em água e álcool etílico |
Cristais deliquescentes brancos a ligeiramente amarelos |
|
nitreto de berílio4 (Ser3 N2 ) |
55.06 |
- |
2,200±100/— |
- |
Cristais brancos duros e refratários |
|
Sulfato de berílio |
177.2 |
1.71 |
100/— |
Solúvel em água; insolúvel em álcool etílico |
cristais incolores |
1 O fluoreto de berílio é produzido pela descompensação a 900–950 ºC do fluoreto de berílio de amônio. Seu principal uso é na produção de berílio metálico por redução com magnésio.
2 O cloreto de berílio é fabricado pela passagem de cloro sobre uma mistura de óxido de berílio e carbono.
3 O nitrato de berílio é produzido pela ação do ácido nítrico sobre o óxido de berílio. É usado como reagente químico e como endurecedor de manto de gás.
4 O nitreto de berílio é preparado pelo aquecimento do pó de berílio metálico em uma atmosfera de nitrogênio livre de oxigênio a 700–1,400 ºC. É usado em reações de energia atômica, incluindo a produção do isótopo de carbono radioativo carbono-14.
5 O sulfato de berílio hidratado é produzido pelo tratamento do minério fritado com ácido sulfúrico concentrado. É utilizado na produção de berílio metálico pelo processo de sulfato.
Fontes
Berilo (3BeO·Al2O3·6SiO2) é a principal fonte comercial de berílio, o mais abundante dos minerais que contém altas concentrações de óxido de berílio (10 a 13%). As principais fontes de berilo podem ser encontradas na Argentina, Brasil, Índia, Zimbábue e República da África do Sul. Nos Estados Unidos, o berilo é encontrado no Colorado, Dakota do Sul, Novo México e Utah. Bertrandita, um minério de baixo teor (0.1 a 3%) com teor de berílio solúvel em ácido, está sendo extraído e processado em Utah.
Produção
Os dois métodos mais importantes de extração de berílio do minério são o processo de sulfato e o processo de flúor.
No processo de sulfato, o berilo triturado é derretido em um forno a arco a 1,65°C e vertido através de uma corrente de água de alta velocidade para formar uma frita. Após o tratamento térmico, a frita é moída em um moinho de bolas e misturada com ácido sulfúrico concentrado para formar uma pasta, que é pulverizada na forma de um jato em um moinho rotativo de sulfato diretamente aquecido. O berílio, agora em uma forma solúvel em água, é lixiviado do lodo e o hidróxido de amônio é adicionado ao licor de lixiviação, que é então alimentado a um cristalizador onde o alúmen de amônio é cristalizado. Agentes quelantes são adicionados ao licor para manter o ferro e o níquel em solução, o hidróxido de sódio é então adicionado e o berilato de sódio assim formado é hidrolisado para precipitar o hidróxido de berílio. Este último produto pode ser convertido em fluoreto de berílio para redução por magnésio em berílio metálico ou em cloreto de berílio para redução eletrolítica.
No processo de flúor (figura 1), uma mistura briquetada de minério triturado, silicofluoreto de sódio e carbonato de sódio é sinterizada em um forno rotativo. O material sinterizado é triturado, moído e lixiviado. O hidróxido de sódio é adicionado à solução de fluoreto de berílio assim obtida e o precipitado de hidróxido de berílio é filtrado em um filtro rotativo. O berílio metálico é obtido como no processo anterior pela redução do magnésio do fluoreto de berílio ou pela eletrólise do cloreto de berílio.
Figura 1. Produção de óxido de berílio pelo processo de flúor
Uso
O berílio é usado em ligas com vários metais, incluindo aço, níquel, magnésio, zinco e alumínio, sendo a liga mais amplamente utilizada o berílio-cobre - apropriadamente chamado de "bronze" - que possui alta resistência à tração e capacidade de endurecimento por tratamento térmico. Os bronzes de berílio são usados em ferramentas antifaíscas, peças de interruptores elétricos, molas de relógios, diafragmas, calços, cames e buchas.
Um dos maiores usos do metal é como moderador de nêutrons térmicos em reatores nucleares e como refletor para reduzir o vazamento de nêutrons do núcleo do reator. Uma fonte mista de urânio-berílio é freqüentemente usada como fonte de nêutrons. Como folha, o berílio é usado como material de janela em tubos de raios-x. Sua leveza, alto módulo de elasticidade e estabilidade térmica o tornam um material atrativo para a indústria aeronáutica e aeroespacial.
O óxido de berílio é feito por aquecimento de nitrato ou hidróxido de berílio.
É usado na fabricação de cerâmica, materiais refratários e outros compostos de berílio. Foi utilizado para a fabricação de fósforos para lâmpadas fluorescentes até que a incidência da doença do berílio na indústria fez com que seu uso para esse fim fosse abandonado (em 1949 nos Estados Unidos).
Riscos
Riscos de incêndio e saúde estão associados a processos envolvendo berílio. O pó de berílio finamente dividido queimará, sendo o grau de combustibilidade uma função do tamanho da partícula. Incêndios ocorreram em unidades de filtragem de poeira e durante a soldagem de dutos de ventilação nos quais estava presente berílio finamente dividido.
O berílio e seus compostos são substâncias altamente tóxicas. O berílio pode afetar todos os sistemas de órgãos, embora o principal órgão envolvido seja o pulmão. O berílio causa doenças sistêmicas por inalação e pode se distribuir amplamente por todo o corpo após a absorção pelos pulmões. Pouco berílio é absorvido pelo trato gastrointestinal. O berílio pode causar irritação cutânea e sua introdução traumática no tecido subcutâneo pode causar irritação local e formação de granuloma.
Patogênese
O berílio em todas as suas formas, exceto o minério de berilo, tem sido associado a doenças. A via de entrada é a inalatória e na doença aguda ocorre efeito tóxico direto tanto na mucosa nasofaríngea quanto em toda a árvore traqueobrônquica, causando edema e inflamação. No pulmão causa uma pneumonia química aguda. A principal forma de toxicidade do berílio neste momento é a doença crônica do berílio. Um tipo retardado de hipersensibilidade específica ao berílio é a principal via de doença crônica. A entrada de berílio no sistema através dos pulmões leva à proliferação de CD específicos+ linfócitos, com o berílio atuando como antígeno específico, isoladamente ou como hapteno, por meio da via do receptor da interleucina-2 (IL2). A suscetibilidade individual ao berílio, portanto, pode ser explicada com base no CD individual+ resposta. A liberação de linfocinas dos linfócitos ativados pode levar à formação de granulomas e recrutamento de macrófagos. O berílio pode ser transportado para locais fora do pulmão, onde pode causar a formação de granulomas. O berílio é liberado lentamente de diferentes locais e é excretado pelos rins. Essa liberação lenta pode ocorrer em um período de 20 a 30 anos. A cronicidade e a latência da doença provavelmente podem ser explicadas com base no metabolismo lento e no fenômeno de liberação. Os mecanismos imunológicos envolvidos na patogênese da berílio também permitem abordagens específicas para o diagnóstico, que serão discutidas a seguir.
Histopatologia
O principal achado patológico na berílio é a formação de granulomas não caseosos nos pulmões, linfonodos e em outros locais. Estudos histopatológicos de pulmões em pacientes com doença aguda por berílio mostraram um padrão inespecífico de bronquite e pneumonite aguda e subaguda. Na berílio doença crônica, há vários graus de infiltração linfocítica do interstício pulmonar e formação de granuloma não caseoso (figura 2).
Figura 2. Tecido pulmonar em paciente com berílio crônico
Ambos granulomas e infiltração de células redondas são visíveis
Muitos dos granulomas estão localizados nas áreas peribronquiolares. Além disso, pode haver histiócitos, plasmócitos e células gigantes com corpos de inclusão calcificados. Se for um caso apenas de formação de granuloma, o prognóstico a longo prazo é melhor. A histologia do pulmão na berílio doença crônica é indistinguível da da sarcoidose. Granulomas não caseosos também são encontrados em linfonodos, fígado, baço, músculo e pele.
Manifestações clínicas
Lesões de pele
Os sais ácidos de berílio causam dermatite alérgica de contato. Tais lesões podem ser eritematosas, papulares ou papulovesiculares, são comumente pruriginosas e são encontradas em partes expostas do corpo. Geralmente há um atraso de 2 semanas desde a primeira exposição até a ocorrência da dermatite, exceto no caso de exposições intensas, quando uma reação irritante pode ser imediata. Este atraso é considerado como o tempo necessário para desenvolver o estado de hipersensibilidade.
A implantação acidental de berílio metálico ou cristais de um composto solúvel de berílio em uma abrasão, uma rachadura na pele ou sob a unha pode causar uma área endurecida com supuração central. Granulomas também podem se formar nesses locais.
A conjuntivite e a dermatite podem ocorrer sozinhas ou juntas. Em casos de conjuntivite, o edema periorbitário pode ser grave.
Doença aguda
A nasofaringite por berílio é caracterizada por membranas mucosas edemaciadas e hiperêmicas, pontos hemorrágicos, fissuras e ulceração. A perfuração do septo nasal foi descrita. A remoção da exposição resulta na reversão desse processo inflamatório dentro de 3 a 6 semanas.
O envolvimento da traquéia e da árvore brônquica após a exposição a níveis mais elevados de berílio causa tosse não produtiva, dor subesternal e falta de ar moderada. Rhônquios e/ou estertores podem ser audíveis, e a radiografia de tórax pode mostrar marcações broncovasculares aumentadas. O caráter e a velocidade de início e a gravidade desses sinais e sintomas dependem da qualidade e quantidade da exposição. A recuperação é esperada dentro de 1 a 4 semanas se o trabalhador for removido de exposição adicional.
O uso de esteróides é bastante útil no combate à doença aguda. Nenhum novo caso de doença aguda foi relatado ao Registro de Casos de Berílio dos EUA em mais de 30 anos. O Registro, iniciado por Harriet Hardy em 1952, possui quase 1,000 registros de casos, entre os quais estão listados 212 casos agudos. Quase todos eles ocorreram na indústria de fabricação de lâmpadas fluorescentes. Quarenta e quatro indivíduos com a doença aguda desenvolveram posteriormente a doença crônica.
Doença crônica do berílio
A berílio doença crônica é uma doença granulomatosa pulmonar e sistêmica causada pela inalação de berílio. A latência da doença pode ser de 1 a 30 anos, ocorrendo mais comumente 10 a 15 anos após a primeira exposição. A berílio doença crônica tem curso variável com exacerbações e remissões em suas manifestações clínicas. No entanto, a doença geralmente é progressiva. Houve alguns casos com anormalidades na radiografia de tórax com curso clínico estável e sem sintomas significativos.
A dispneia de esforço é o sintoma mais comum da berílio doença crônica. Outros sintomas são tosse, fadiga, perda de peso, dor no peito e artralgias. Os achados físicos podem ser totalmente normais ou podem incluir crepitações bibasilares, linfadenopatia, lesões cutâneas, hepatoesplenomegalia e baqueteamento digital. Sinais de hipertensão pulmonar podem estar presentes na doença grave e de longa duração.
Cálculos renais e hiperuricemia podem ocorrer em alguns pacientes e houve relatos raros de aumento da glândula parótida e envolvimento do sistema nervoso central. As manifestações clínicas da berílio crônica são muito semelhantes às da sarcoidose.
Características radiológicas
O padrão radiográfico na berílio crônica é inespecífico e semelhante ao que pode ser observado na sarcoidose, fibrose pulmonar idiopática, tuberculose, micoses e poeira (figura 3). No início do curso da doença, os filmes podem mostrar densidades granulares, nodulares ou lineares. Essas anormalidades podem aumentar, diminuir ou permanecer inalteradas, com ou sem fibrose. O envolvimento do lobo superior é comum. A adenopatia hilar, observada em aproximadamente um terço dos pacientes, geralmente é bilateral e acompanhada de manchas nos campos pulmonares. A ausência de alterações pulmonares na presença de adenopatia é uma consideração diferencial relativa, mas não absoluta, a favor da sarcoidose em oposição à berílio doença crônica. Adenopatia hilar unilateral foi relatada, mas é bastante rara.
Figura 3. Radiografia de tórax de paciente com berílio crônico, mostrando infiltrados fibronodulares difusos e hilos proeminentes
A imagem de raio-x não se correlaciona bem com o estado clínico e não reflete aspectos qualitativos ou quantitativos particulares da exposição causal.
Testes de função pulmonar
Os dados do Registro de casos de berílio mostram que 3 padrões de comprometimento podem ser encontrados na doença crônica de berílio. Dos 41 pacientes estudados durante um período médio de 23 anos após a exposição inicial ao berílio, 20% tinham um defeito restritivo, 36% tinham um defeito intersticial (volumes pulmonares e taxas de fluxo de ar normais, mas capacidade de difusão reduzida para monóxido de carbono), 39% tinham um defeito obstrutivo e 5% eram normais. O padrão obstrutivo, que ocorreu tanto em fumantes quanto em não fumantes, foi associado a granulomas na região peribrônquica. Este estudo indicou que o padrão de comprometimento afeta o prognóstico. Os pacientes com defeito intersticial se saíram melhor, com a menor deterioração em um intervalo de cinco anos. Pacientes com defeitos obstrutivos e restritivos apresentaram piora de seu comprometimento, apesar da terapia com corticosteroides.
Estudos da função pulmonar em extratores de berílio assintomáticos mostraram a presença de hipoxemia arterial leve. Isso ocorreu geralmente nos primeiros 10 anos de exposição. Em trabalhadores expostos ao berílio por 20 anos ou mais houve redução da capacidade vital forçada (CVF) e do volume expiratório forçado no primeiro segundo (VEF1). Esses achados sugerem que a hipoxemia leve inicial pode ser devida à alveolite precoce e que, com maior exposição e decurso do tempo, a redução do VEF1 e a CVF poderia representar fibrose e formação de granulomas.
Outros testes de laboratório
Testes laboratoriais anormais inespecíficos foram relatados na doença crônica do berílio e incluem taxa de sedimentação elevada, eritrocitose, aumento dos níveis de gamaglobulina, hiperuricemia e hipercalcemia.
O teste cutâneo de Kveim é negativo na berílio, enquanto pode ser positivo na sarcoidose. O nível da enzima conversora de angiotensina (ECA) geralmente é normal na berílio, mas pode estar aumentado em 60% ou mais dos pacientes com sarcoidose ativa.
Diagnóstico
O diagnóstico da doença crônica por berílio por muitos anos foi baseado nos critérios desenvolvidos por meio do Registro de casos de berílio, que incluía:
- uma história de exposição significativa ao berílio
- evidência de doença do trato respiratório inferior
- radiografia de tórax anormal com doença fibronodular intersticial
- testes de função pulmonar anormais com diminuição da capacidade de difusão do monóxido de carbono (DLCO)
- alterações patológicas consistentes com exposição ao berílio nos linfonodos pulmonares ou torácicos
- a presença de berílio no tecido.
Quatro dos seis critérios deveriam ser atendidos e deveriam incluir (1) ou (6). Desde a década de 1980, os avanços na imunologia tornaram possível o diagnóstico da berílio sem a necessidade de amostras de tecido para exame histológico ou análise do berílio. A transformação de linfócitos no sangue em resposta à exposição ao berílio (como no teste de transformação de linfócitos, LTT) ou linfócitos do lavado broncoalveolar (BAL) foi proposta por Newman et al. (1989) como ferramentas de diagnóstico úteis para fazer o diagnóstico da doença do berílio em indivíduos expostos. Seus dados sugerem que um LTT positivo no sangue é indicativo de sensibilização. No entanto, dados recentes mostram que o LTT sanguíneo não se correlaciona bem com a doença pulmonar. A transformação de linfócitos BAL se correlaciona muito melhor com a função pulmonar anormal e não se correlaciona bem com anormalidades concomitantes no sangue LTT. Assim, para fazer o diagnóstico de berílio, é necessária uma combinação de anormalidades clínicas, radiológicas e da função pulmonar e um LTT positivo no LBA. Um LTT sanguíneo positivo por si só não é diagnóstico. A análise microprobe de pequenas amostras de tecido para berílio é outra inovação recente que pode ajudar no diagnóstico de doenças em pequenas amostras de tecido pulmonar obtidas por biópsia pulmonar transbrônquica.
A sarcoidose é a doença que mais se assemelha à berílio crônica, e a diferenciação pode ser difícil. Até agora, nenhuma doença óssea cística ou envolvimento do olho ou da amígdala apareceu na doença crônica do berílio. Da mesma forma, o teste de Kveim é negativo na doença de berílio. O teste cutâneo para demonstrar a sensibilização ao berílio não é recomendado, pois o teste em si é sensibilizante, pode possivelmente desencadear reações sistêmicas em pessoas sensibilizadas e não estabelece por si só que a doença apresentada está necessariamente relacionada ao berílio.
Abordagens imunológicas mais sofisticadas no diagnóstico diferencial devem permitir uma melhor diferenciação da sarcoidose no futuro.
Prognóstico
O prognóstico da doença crônica do berílio alterou-se favoravelmente ao longo dos anos; foi sugerido que os atrasos mais longos no início observados entre os trabalhadores do berílio podem refletir menor exposição ou menor carga corporal de berílio, resultando em um curso clínico mais brando. A evidência clínica é que a terapia com esteróides, se usada quando a incapacidade mensurável aparece pela primeira vez, em doses adequadas por períodos suficientemente longos, melhorou o estado clínico de muitos pacientes, permitindo que alguns deles retornem a empregos úteis. Não há evidências claras de que os esteróides tenham curado o envenenamento crônico por berílio.
Berílio e câncer
Em animais, o berílio administrado experimentalmente é cancerígeno, causando sarcoma osteogênico após injeção intravenosa em coelhos e câncer de pulmão após inalação em ratos e macacos. Se o berílio pode ser um carcinógeno humano é uma questão controversa. Alguns estudos epidemiológicos sugeriram uma associação, particularmente após a berílio doença aguda. Esta descoberta foi contestada por outros. Pode-se concluir que o berílio é cancerígeno em animais e pode haver uma ligação entre câncer de pulmão e berílio em humanos, particularmente naqueles com doença aguda.
Medidas de Segurança e Saúde
As precauções de segurança e saúde devem abranger o risco de incêndio, bem como o perigo de toxicidade muito mais grave.
Prevenção de incêndio
Devem ser tomadas providências para evitar possíveis fontes de ignição, como faíscas ou arcos de aparelhos elétricos, fricção e assim por diante, nas proximidades de pó de berílio finamente dividido. O equipamento no qual este pó esteve presente deve ser esvaziado e limpo antes de usar acetileno ou aparelho de solda elétrica. O pó ultrafino de berílio isento de óxidos, preparado em gás inerte, pode inflamar-se espontaneamente quando exposto ao ar.
Pó seco adequado - não água - deve ser usado para extinguir um incêndio de berílio. Equipamento de proteção individual completo, incluindo equipamento de proteção respiratória, deve ser usado e os bombeiros devem tomar banho depois e providenciar a lavagem de suas roupas separadamente.
Proteção da saúde
Os processos de berílio devem ser conduzidos de maneira cuidadosamente controlada para proteger tanto o trabalhador quanto a população em geral. O principal risco assume a forma de contaminação aérea e o processo e a planta devem ser projetados para produzir o mínimo possível de poeira ou fumaça. Processos úmidos devem ser usados em vez de processos secos, e os ingredientes das preparações contendo berílio devem ser unificados como suspensões aquosas em vez de pós secos; sempre que possível, a planta deve ser projetada como grupos de unidades fechadas separadas. A concentração permitida de berílio na atmosfera é tão baixa que o isolamento deve ser aplicado mesmo em processos úmidos, caso contrário, respingos e derramamentos podem secar e a poeira pode entrar na atmosfera.
As operações que possam produzir poeira devem ser realizadas em áreas com grau máximo de enclausuramento compatível com as necessidades de manipulação. Algumas operações são realizadas em porta-luvas, mas muitas outras são realizadas em compartimentos providos de ventilação de exaustão semelhante à instalada em capelas de exaustão química. As operações de usinagem podem ser ventiladas por sistemas de exaustão locais de alta velocidade e baixo volume ou por compartimentos cobertos com ventilação de exaustão.
Para verificar a eficácia dessas medidas de precaução, o monitoramento da atmosfera deve ser feito de forma que a exposição média diária dos trabalhadores ao berílio respirável possa ser calculada. A área de trabalho deve ser limpa regularmente por meio de um aspirador adequado ou um esfregão úmido. Os processos de berílio devem ser segregados das outras operações na fábrica.
Equipamentos de proteção individual devem ser fornecidos para trabalhadores envolvidos em processos de berílio. Quando forem empregados integralmente em processos que envolvam a manipulação de compostos de berílio ou em processos associados à extração do metal do minério, deve-se providenciar uma troca completa de vestuário para que os trabalhadores não voltem para casa com roupas que Tenho estado trabalhando. Devem ser tomadas providências para a lavagem segura de tais roupas de trabalho, e macacões de proteção devem ser fornecidos até mesmo aos trabalhadores da lavanderia para garantir que eles também não sejam expostos a riscos. Esses arranjos não devem ser deixados para os procedimentos normais de lavagem doméstica. Casos de envenenamento por berílio nas famílias dos trabalhadores foram atribuídos a trabalhadores que levaram roupas contaminadas para casa ou as usaram em casa.
Um padrão de saúde ocupacional de 2μg/m3, proposto em 1949 por um comitê operando sob os auspícios da Comissão de Energia Atômica dos EUA, continua a ser amplamente observado. As interpretações existentes geralmente permitem flutuações para um “teto” de 5μg/m3 contanto que a média ponderada no tempo não seja excedida. Além disso, um “pico máximo aceitável acima da concentração máxima para um turno de oito horas” de 25μg/m3 por até 30 min também é permitido. Esses níveis operacionais são atingíveis na prática industrial atual e não há evidências de experiência adversa à saúde entre pessoas que trabalham em um ambiente assim controlado. Devido a uma possível ligação entre berílio e câncer de pulmão, foi sugerido que o limite permitido seja reduzido para 1μg/m3, mas nenhuma ação oficial foi tomada sobre essa sugestão nos Estados Unidos.
A população em risco de desenvolver beriliose é aquela que de alguma forma lida com o berílio na sua extração ou uso posterior. No entanto, alguns casos de “vizinhança” foram relatados a uma distância de 1 a 2 km de plantas de extração de berílio.
Os exames médicos pré-emprego e periódicos dos trabalhadores expostos ao berílio e seus compostos são obrigatórios em vários países. A avaliação recomendada inclui um questionário respiratório anual, uma radiografia de tórax e testes de função pulmonar. Com os avanços da imunologia, o LTT também pode se tornar uma avaliação de rotina, embora neste momento não haja dados suficientes para recomendar seu uso rotineiramente. Com evidências de berílio, não é sensato permitir que um trabalhador seja exposto ao berílio ainda mais, mesmo que o local de trabalho atenda aos critérios de limite para concentração de berílio no ar.
foliar
O principal passo na terapia é evitar uma maior exposição ao berílio. Os corticosteróides são o principal modo de terapia na berílio doença crônica. Os corticosteróides parecem alterar favoravelmente o curso da doença, mas não a “curam”.
Os corticosteróides devem ser iniciados diariamente com uma dose relativamente alta de Prednisona de 0.5 a 1 mg por kg ou mais, e continuados até que ocorra melhora ou não ocorra mais deterioração nos testes clínicos ou de função pulmonar. Normalmente, isso leva de 4 a 6 semanas. A redução lenta dos esteróides é recomendada e, eventualmente, a terapia em dias alternados pode ser possível. A terapia com esteroides geralmente se torna uma necessidade vitalícia.
Outras medidas de suporte, como oxigênio suplementar, diuréticos, digitálicos e antibióticos (quando houver infecção), são indicadas conforme a condição clínica do paciente. A imunização contra influenza e pneumococo também deve ser considerada, como em qualquer paciente com doença respiratória crônica.
Pneumoconioses: Definição
A expressão pneumoconiose, do grego pneuma (ar, vento) e Konis (poeira) foi cunhado na Alemanha por Zenker em 1867 para denotar mudanças nos pulmões causadas pela retenção de poeira inalada. Aos poucos, tornou-se evidente a necessidade de distinção entre os efeitos dos vários tipos de poeira. Era preciso discriminar entre pó mineral ou vegetal e seu componente microbiológico. Consequentemente, a Terceira Conferência Internacional de Especialistas em Pneumoconiose, organizada pela OIT em Sydney em 1950, adotou a seguinte definição: “Pneumoconiose é uma doença diagnosticável dos pulmões produzida pela inalação de poeira, entendendo-se o termo 'poeira' a matéria particulada na fase sólida, mas excluindo os organismos vivos”.
No entanto, a palavra doença parece implicar algum grau de comprometimento da saúde, o que pode não ser o caso de pneumoconioses não relacionadas ao desenvolvimento de fibrose/cicatrização pulmonar. Em geral, a reação do tecido pulmonar à presença de poeira varia com as diferentes poeiras. Poeiras não fibrogênicas evocam uma reação tecidual nos pulmões caracterizada por reação fibrótica mínima e ausência de comprometimento da função pulmonar. Essas poeiras, exemplos das quais são poeiras finamente divididas de caulinite, dióxido de titânio, óxido estanoso, sulfato de bário e óxido férrico, são frequentemente referidas como biologicamente inertes.
A poeira fibrogênica, como sílica ou amianto, causa uma reação fibrogênica mais pronunciada, resultando em cicatrizes no tecido pulmonar e doenças óbvias. A divisão das poeiras em variedades fibrogênicas e não fibrogênicas não é nítida porque existem muitos minerais, principalmente silicatos, que são intermediários em sua capacidade de produzir lesões fibróticas nos pulmões. No entanto, mostrou-se útil para fins clínicos e se reflete na classificação das pneumoconioses.
Uma nova definição de pneumoconiose foi adotada na Quarta Conferência Internacional sobre Pneumoconiose, Bucareste, 1971: “Pneumoconiose é o acúmulo de poeira nos pulmões e as reações dos tecidos à sua presença. Para o propósito desta definição, 'poeira' é um aerossol composto de partículas sólidas inanimadas.”
Para evitar qualquer má interpretação, a expressão não neoplásico às vezes é adicionado às palavras “reação tecidual”.
O Grupo de Trabalho na Conferência fez a seguinte declaração abrangente:
A definição de pneumoconiose
Anteriormente, em 1950, uma definição de pneumoconiose foi estabelecida na 3ª Conferência Internacional de Especialistas em Pneumoconiose e continuou a ser usada até o presente. Nesse ínterim, o desenvolvimento de novas tecnologias resultou em mais riscos ocupacionais, principalmente os relacionados à inalação de contaminantes transportados pelo ar. O aumento do conhecimento no campo da medicina ocupacional permitiu o reconhecimento de novas doenças pulmonares de origem ocupacional, mas também demonstrou a necessidade de um reexame da definição de pneumoconiose estabelecida em 1950. A OIT, portanto, organizou a convocação de um Grupo de Trabalho no âmbito da IVª Conferência Internacional de Pneumoconiose, a fim de examinar a questão da definição de pneumoconiose. O Grupo de Trabalho realizou uma discussão geral sobre o assunto e procedeu ao exame de algumas propostas apresentadas por seus membros. Por fim, adotou uma nova definição de pneumoconiose, que foi elaborada juntamente com um comentário. Este texto é reproduzido abaixo.
Nos últimos anos, vários países incluíram na pneumoconiose, por razões socioeconômicas, condições que manifestamente não são pneumoconiose, mas são doenças pulmonares ocupacionais. Sob o termo “doença” estão incluídas, por razões preventivas, as primeiras manifestações que não são necessariamente incapacitantes ou abreviam a vida. Portanto, o Grupo de Trabalho se comprometeu a redefinir a pneumoconiose como o acúmulo de poeira nos pulmões e as reações dos tecidos à sua presença. Para o propósito desta definição, “poeira” significa um aerossol composto de partículas sólidas inanimadas. Do ponto de vista patológico, a pneumoconiose pode ser dividida por conveniência em formas colagenosas ou não colagenosas. Uma pneumoconiose não colagenosa é causada por uma poeira não fibrogênica e tem as seguintes características:
- a arquitetura alveolar permanece intacta
- a reação estromal é mínima e consiste principalmente em fibras de reticulina
- a reação do pó é potencialmente reversível.
Exemplos de pneumoconiose não colagenosa são aquelas causadas por poeiras puras de óxido de estanho (estanose) e sulfato de bário (baritose).
A pneumoconiose colagenosa caracteriza-se por:
- alteração permanente ou destruição da arquitetura alveolar
- reação estromal colagenosa de grau moderado a máximo, e
- cicatriz permanente do pulmão.
Essa pneumoconiose colagenosa pode ser causada por poeiras fibrogênicas ou por uma resposta tecidual alterada a uma poeira não fibrogênica.
Exemplos de pneumoconiose colagenosa causada por poeiras fibrogênicas são a silicose e a asbestose, enquanto a complicada pneumoconiose dos mineiros ou fibrose maciça progressiva (PMF) é uma resposta tecidual alterada a uma poeira relativamente não fibrogênica. Na prática, a distinção entre pneumoconiose colagenosa e não colagenosa é difícil de estabelecer. A exposição contínua ao mesmo pó, como pó de carvão, pode causar a transição de uma forma não colágena para uma forma colágena. Além disso, a exposição a uma única poeira está se tornando menos comum e as exposições a poeiras mistas com diferentes graus de potencial fibrogênico podem resultar em pneumoconiose, que pode variar desde as formas não colagenosas até as formas colagenosas. Além disso, existem doenças pulmonares crônicas ocupacionais que, embora se desenvolvam a partir da inalação de poeira, são excluídas da pneumoconiose porque as partículas não se acumulam nos pulmões. A seguir, exemplos de doenças pulmonares crônicas ocupacionais potencialmente incapacitantes: bissinose, beriliose, pulmão do fazendeiro e doenças relacionadas. Eles têm um denominador comum, ou seja, o componente etiológico da poeira sensibilizou o tecido pulmonar ou brônquico, de modo que, se o tecido pulmonar responder, a inflamação tende a ser granulomatosa e, se o tecido brônquico responder, poderá haver constrição brônquica. As exposições a materiais nocivos inalados em certas indústrias estão associadas a um risco aumentado de mortalidade por carcinoma do trato respiratório. Exemplos de tais materiais são minérios radioativos, amianto e cromatos.
Adotado na IVª Conferência Internacional da OIT sobre Pneumoconiose. Bucareste, 1971.
Classificação Internacional de Radiografias de Pneumoconioses da OIT
Apesar de todas as energias nacionais e internacionais dedicadas à sua prevenção, as pneumoconioses ainda estão muito presentes tanto nos países industrializados como nos países em desenvolvimento, sendo responsáveis pela incapacidade e incapacidade de muitos trabalhadores. É por isso que a Organização Internacional do Trabalho (OIT), a Organização Mundial da Saúde (OMS) e muitos institutos nacionais de saúde e segurança ocupacional continuam sua luta contra essas doenças e propõem programas sustentáveis para preveni-las. Por exemplo, a OIT, a OMS e o Instituto Nacional de Segurança e Saúde Ocupacional dos EUA (NIOSH) propuseram em seus programas trabalhar em cooperação na luta global contra a silicose. Parte deste programa baseia-se na vigilância médica que inclui a leitura de radiografias torácicas para ajudar no diagnóstico desta pneumoconiose. Este é um exemplo que explica por que a OIT, em cooperação com muitos especialistas, desenvolveu e atualizou continuamente uma classificação de radiografias de pneumoconioses que fornece um meio de registrar sistematicamente as anormalidades radiográficas no tórax provocadas pela inalação de poeira. O esquema é projetado para classificar as aparências das radiografias de tórax póstero-anteriores.
O objetivo da classificação é codificar as anormalidades radiográficas das pneumoconioses de maneira simples e reprodutível. A classificação não define entidades patológicas, nem leva em conta a capacidade de trabalho. A classificação não implica definições legais de pneumoconioses para fins de compensação, nem implica um nível em que a compensação seja devida. No entanto, descobriu-se que a classificação tem usos mais amplos do que o previsto. Agora é amplamente utilizado internacionalmente para pesquisa epidemiológica, para a vigilância dessas ocupações da indústria e para fins clínicos. O uso do esquema pode levar a uma melhor comparabilidade internacional das estatísticas de pneumoconioses. Também é utilizado para descrever e registrar, de forma sistemática, parte das informações necessárias para avaliar a remuneração.
A condição mais importante para usar este sistema de classificação com valor total do ponto de vista científico e ético é ler, em todos os momentos, os filmes a serem classificados, referindo-se sistematicamente aos 22 filmes padrão fornecidos no conjunto de padrões da Classificação Internacional da OIT filmes. Se o leitor tentar classificar um filme sem se referir a nenhum dos filmes padrão, nenhuma menção à leitura de acordo com a Classificação Internacional de Radiografias da OIT deve ser feita. A possibilidade de se desviar da classificação por super ou subleitura é tão arriscada que sua leitura não deve ser utilizada ao menos para pesquisas epidemiológicas ou comparabilidade internacional de estatísticas de pneumoconioses.
A primeira classificação para silicose foi proposta na Primeira Conferência Internacional de Especialistas em Pneumoconioses, realizada em Joanesburgo em 1930. Combinava aspectos radiográficos e comprometimento das funções pulmonares. Em 1958, uma nova classificação baseada puramente em alterações radiográficas foi estabelecida (classificação de Genebra de 1958). Desde então, ele foi revisado várias vezes, a última vez em 1980, sempre com o objetivo de fornecer versões aprimoradas para serem amplamente utilizadas para fins clínicos e epidemiológicos. Cada nova versão da classificação promovida pela OIT trouxe modificações e mudanças com base na experiência internacional adquirida no uso de classificações anteriores.
A fim de fornecer instruções claras para o uso da classificação, a OIT emitiu em 1970 uma publicação intitulada Classificação Internacional de Radiografias de Pneumoconioses/1968 na Série Segurança e Saúde Ocupacional (nº 22). Esta publicação foi revisada em 1972 como Classificação Internacional de Radiografias de Pneumoconioses/1971 da OIT U/C e novamente em 1980 como Diretrizes para o uso da Classificação Internacional de Radiografias de Pneumoconioses da OIT, edição revisada de 1980. A descrição das radiografias padrão é fornecida na tabela 1.
Tabela 1. Descrição das radiografias padrão
| 1980 Radiografias padrão mostrando | Pequenas opacidades | Espessamento pleural | ||||||||||
| Parede torácica | ||||||||||||
| Qualidade técnica | Profusão | tamanho da forma | Extensão | Grandes opacidades | circunscrito (placas) | Difuso | Diafragma | Obliteração do ângulo costofrênico | calcificação pleural | Símbolos | Comentários | |
| 0/0 (exemplo 1) | 1 | 0/0 | - | - | Não | Não | Não | Não | Não | Não | nenhum | O padrão vascular é bem ilustrado |
| 0/0 (exemplo 2) | 1 | 0/0 | - | - | Não | Não | Não | Não | Não | Não | nenhum | Também mostra padrão vascular, mas não tão claramente quanto o exemplo 1 |
| 1/1; p/p | 1 | 1/1 | p/p | R L x x x x x x | A | Não | Não | Não | Não | Não | Rp. | Pneumoconiose reumatóide na zona inferior esquerda. Pequenas opacidades estão presentes em todas as zonas, mas a profusão na zona superior direita é típica (alguns diriam um pouco mais profusa) daquela classificável como categoria 1/1 |
| 2/2; p/p | 2 | 2/2 | p/p | R L x x x x x x | Não | Não | Não | Não | Não | Não | pi; tb. | Defeito de qualidade: a radiografia é muito clara |
| 3/3; p/p | 1 | 3/3 | p/p | R L x x x x x x | Não | Não | Não | Não | Sim R L x – | Não | machado. | nenhum |
| 1/1; q/q | 1 | 1/1 | q / q | R L x x x x – – | Não | Não | Não | Não | Não | Não | nenhum | Ilustra profusão 1/1 melhor que forma ou tamanho |
| 2/2; q/q | 1 | 2/2 | q / q | R L x x x x x x | Não | Não | Sim R L x x largura: a a extensão: 1 1 | Não | Sim R L x x | Não | nenhum | nenhum |
| 3/3; q/q | 2 | 3/3 | q / q | R L x x x x x x | Não | Não | Não | Não | Não | Não | pés | Defeitos de qualidade: má definição da pleura e corte dos ângulos basais |
| 1/1; r/r | 2 | 1/1 | y / y | R L x x x x – – | Não | Não | Não | Não | Sim R L – x | Não | nenhum | Defeito de qualidade: movimento do sujeito. A profusão de pequenas opacidades é mais acentuada no pulmão direito |
| 2/2; r/r | 2 | 2/2 | y / y | R L x x x x x x | Não | Não | Não | Não | Não | Não | nenhum | Defeitos de qualidade: radiografia muito clara e contraste muito alto. A sombra do coração está ligeiramente deslocada para a esquerda |
| 3/3; r/r | 1 | 3/3 | y / y | R L x x x x x x | Não | Não | Não | Não | Não | Não | machado; ih. | nenhum |
| 1/1; s/t | 2 | 1/1 | s / t | R L x – x x x x | Não | Não | Não | Não | Não | Não | kl. | Defeito de qualidade: bases cortadas. Linhas de Kerley na zona inferior direita |
| 2/2; s/s | 2 | 2/2 | s / s | R L – – x x x x | Não | Não | Não | Não | Não | Não | em. | Defeito de qualidade: distorção das bases devido ao encolhimento. Enfisema nas zonas superiores |
| 3/3; s/s | 2 | 3/3 | s / s | R L x x x x x x | Não | Não | Sim R L x x largura: a a extensão: 3 3 | Não | Não | Não | ho; eu; pi. | Defeito de qualidade: a radiografia é muito clara. A aparência do pulmão em favo de mel não é marcada |
| 1/1; obliteração do ângulo costofrênico t/t | 1 | 1/1 | t / t | R L – – x x x x | Não | Não | Sim R L x x largura: a a extensão: 2 2 | Não | Sim R L x – | Sim R L - x extensão: 2 | nenhum | Esta radiografia define o limite inferior para a obliteração do ângulo costofrênico. Observe o encolhimento nos campos pulmonares inferiores |
| 2/2; t/t | 1 | 2/2 | t / t | R L x x x x x x | Não | Não | Sim R L x x largura: a a extensão: 1 1 | Não | Não | Não | ei. | Espessamento pleural está presente nos ápices do pulmão |
| 3/3; t/t | 1 | 3/3 | t / t | R L x x x x x x | Não | Não | Não | Não | Não | Não | Oi; ho; Eu iria; eu; tb. | nenhum |
| 1/1; u/u 2/2; u/u 3/3; u/u | - | - | - | - | - | - | - | - | - | - | - | Esta radiografia composta ilustra as categorias intermediárias de profusão de pequenas opacidades classificadas quanto à forma e tamanho como u/u. |
| A | 2 | 2/2 | p/q | R L x x x x x x | A | Não | Não | Não | Não | Não | Não | Defeitos de qualidade: a radiografia é muito clara e a definição pleural é ruim |
| B | 1 | 1/2 | p/q | R L x x x x x x | B | Não | Não | Não | Não | Não | machado; co. | A definição da pleura é ligeiramente imperfeita |
| C | 1 | 2/1 | q/t | R L x x x x x x | C | Não | Não | Não | Não | Não | bu; di; em; es; Oi; ih. | As pequenas opacidades são difíceis de classificar devido à presença das grandes opacidades. Observe a obliteração do ângulo costofrênico esquerdo. Não é classificável porque não atinge o limite inferior definido pela radiografia padrão 1/1; t/t |
| Espessamento pleural (circunscrito) | - | - | - | - | - | Sim | Não | Não | Não | Não | O espessamento pleural presente na face, é de largura indeterminada e extensão 2 | |
| Espessamento pleural (difuso) | - | - | - | - | - | Não | Sim | Não | Não | Sim | O espessamento pleural presente em perfil, é de largura a, e extensão 2. Não há pequenas calcificações associadas | |
| Espessamento pleural (calcificação) diafragma | - | - | - | - | - | Não | Não | Sim | Não | Sim | Espessamento pleural circunscrito e calcificado de extensão 2 | |
| Espessamento pleural (calcificação) da parede torácica | - | - | - | - | - | Sim | Não | Não | Não | Sim | Espessamento pleural calcificado e não calcificado presente na face, é de largura indeterminada e extensão 2 | |
Classificação da OIT 1980
A revisão de 1980 foi realizada pela OIT com a cooperação da Comissão das Comunidades Européias, do NIOSH e do Colégio Americano de Radiologia. O resumo da classificação é apresentado na tabela 2. Manteve o princípio das classificações anteriores (1968 e 1971).
Tabela 2. Classificação Internacional de Radiografias de Pneumoconioses de 1980 da OIT: Resumo dos detalhes da classificação
| Funcionalidades | códigos | Definições | |
| Qualidade técnica | |||
| 1 | Boa. | ||
| 2 | Aceitável, sem defeito técnico que prejudique a classificação da radiografia de pneumoconiose. | ||
| 3 | Ruim, com algum defeito técnico mas ainda aceitável para efeitos de classificação. | ||
| 4 | Inaceitável. | ||
| Anormalidades parenquimatosas | |||
| Pequenas opacidades | Profusão | A categoria de profusão é baseada na avaliação da concentração de opacidades em comparação com as radiografias padrão. | |
| 0/- 0/0 0/1 1/0 1/1 1/2 2/1 2/2 2/3 3/2 3/3 3/+ | Categoria O — pequenas opacidades ausentes ou menos profusas que o limite inferior da categoria 1. Categorias 1, 2 e 3 — profusão crescente de pequenas opacidades conforme definido pelas radiografias padrão correspondentes. | ||
| Extensão | RU RM RL LU LM LL | As zonas em que as opacidades são vistas são registradas. O tórax direito (R) e esquerdo (L) são divididos em três zonas - superior (U), médio (M) e inferior (L). A categoria de profusão é determinada considerando a profusão como um todo nas zonas afetadas do pulmão e comparando-a com as radiografias padrão. | |
| Forma e tamanho | |||
| Arredondado | p/p q/q r/r | As letras p, q e r denotam a presença de pequenas opacidades arredondadas. Três tamanhos são definidos pelas aparências em radiografias padrão: p = diâmetro até cerca de 1.5 mm q = diâmetro superior a cerca de 1.5 mm e até cerca de 3 mm r = diâmetro superior a cerca de 3 mm e até cerca de 10 mm | |
| Irregular | s/s t/t u/u | As letras s, t e u denotam a presença de pequenas opacidades irregulares. Três tamanhos são definidos pelas aparências em radiografias padrão: s = largura até cerca de 1.5 mm t = largura superior a cerca de 1.5 mm e até cerca de 3 mm u = largura superior a 3 mm e até cerca de 10 mm | |
| Misto | p/s p/t p/u p/q p/r q/s q/t q/u q/p q/r r/s r/t r/u r/p r/q s/p s/q s/r s/t s/u t/p t/q t/r t/s t/ u u/p u/q u/r u/s u/t | Para formas mistas (ou tamanhos) de pequenas opacidades, a forma e o tamanho predominantes são registrados primeiro. A presença de um número significativo de outra forma e tamanho é registrada após o traço oblíquo. | |
| Grandes opacidades | A B C | As categorias são definidas em termos das dimensões das opacidades. Categoria A - uma opacidade com um diâmetro máximo superior a cerca de 10 mm e até 50 mm, inclusive, ou várias opacidades, cada uma maior que cerca de 10 mm, cuja soma dos maiores diâmetros não exceda cerca de 50 mm. Categoria B – uma ou mais opacidades maiores ou mais numerosas que as da categoria A cuja área combinada não exceda o equivalente à zona superior direita. Categoria C – uma ou mais opacidades cuja área combinada excede o equivalente à zona superior direita. | |
| Anormalidades pleurais | |||
| Espessamento pleural | |||
| Parede torácica | Formato | Dois tipos de espessamento pleural da parede torácica são reconhecidos: circunscrito (placas) e difuso. Ambos os tipos podem ocorrer juntos | |
| Local | RL | O espessamento pleural da parede torácica é registrado separadamente para o tórax direito (R) e esquerdo (L). | |
| Largura | a b c | Para espessamento pleural visto ao longo da parede torácica lateral, a medida da largura máxima é feita a partir da linha interna da parede torácica até a margem interna da sombra vista mais nitidamente no limite parênquima-pleural. A largura máxima geralmente ocorre na margem interna da sombra da nervura em seu ponto mais externo. a = largura máxima até cerca de 5 mm b = largura máxima acima de cerca de 5 mm e até cerca de 10 mm c = largura máxima acima de cerca de 10 mm | |
| De cara | S N | A presença de espessamento pleural visto de frente é registrada mesmo que possa ser vista também de perfil. Se o espessamento pleural for visto apenas de face, a largura geralmente não pode ser medida. | |
| Extensão | 1 2 3 | A extensão do espessamento pleural é definida em termos do comprimento máximo do envolvimento pleural, ou como a soma dos comprimentos máximos, seja visto de perfil ou de frente. 1 = comprimento total equivalente até um quarto da projeção da parede torácica lateral 2 = comprimento total superior a um quarto, mas não a metade da projeção da parede torácica lateral 3 = comprimento total superior a metade da projeção da parede torácica lateral muro | |
| Diafragma | Presença | S N | Uma placa envolvendo a pleura diafragmática é registrada como presente (Y) ou ausente (N), separadamente para o tórax direito (R) e esquerdo (L). |
| Local | RL | ||
| Obliteração do ângulo costofrênico | Presença | S N | A presença (Y) ou ausência (N) de obliteração do ângulo costofrênico é registrada separadamente do espessamento sobre outras áreas, para o tórax direito (R) e esquerdo (L). O limite inferior para esta obliteração é definido por uma radiografia padrão |
| Local | RL | Se o espessamento se estender até a parede torácica, tanto a obliteração do ângulo costofrênico quanto o espessamento pleural devem ser registrados. | |
| calcificação pleural | Local | O local e a extensão da calcificação pleural são registrados separadamente para os dois pulmões e a extensão definida em termos de dimensões. | |
| Parede torácica | RL | ||
| Diafragma | RL | ||
| Outros | RL | “Outros” inclui calcificação da pleura mediastinal e pericárdica. | |
| Extensão | 1 2 3 | 1 = uma área de pleura calcificada com maior diâmetro até cerca de 20 mm, ou várias dessas áreas cuja soma dos maiores diâmetros não exceda cerca de 20 mm. 2 = uma área de pleura calcificada com maior diâmetro excedendo cerca de 20 mm e até cerca de 100 mm, ou várias dessas áreas cuja soma dos maiores diâmetros excede cerca de 20 mm, mas não excede cerca de 100 mm. 3 = uma área de pleura calcificada com maior diâmetro excedendo cerca de 100 mm, ou várias dessas áreas cuja soma dos maiores diâmetros excede cerca de 100 mm. | |
| Símbolos | |||
| Deve-se considerar que a definição de cada um dos símbolos é precedida por uma palavra ou frase apropriada, como “suspeito”, “alterações sugestivas de” ou “opacidades sugestivas de”, etc. | |||
| ax | Coalescência de pequenas opacidades pneumoconióticas | ||
| bu | Bola(e) | ||
| ca | Câncer de pulmão ou pleura | ||
| cn | Calcificação em pequenas opacidades pneumoconióticas | ||
| co | Anormalidade do tamanho ou forma cardíaca | ||
| cp | cor pulmonale | ||
| cv | Cavidade | ||
| di | Distorção acentuada dos órgãos intratorácicos | ||
| ef | Efusão | ||
| em | enfisema definitivo | ||
| es | Calcificação em casca de ovo de linfonodos hilares ou mediastinais | ||
| fr | Costela(s) fraturada(s) | ||
| hi | Aumento dos gânglios linfáticos hilares ou mediastínicos | ||
| ho | Pulmão de favo de mel | ||
| id | diafragma mal definido | ||
| ih | Contorno do coração mal definido | ||
| kl | Linhas septais (Kerley) | ||
| od | Outra anormalidade significativa | ||
| pi | Espessamento pleural na fissura interlobar do mediastino | ||
| px | pneumotórax | ||
| rp | Pneumoconiose reumatóide | ||
| tb | Tuberculose | ||
| Comentários | |||
| Presença | S N | Comentários devem ser registrados referentes à classificação da radiografia, particularmente se alguma outra causa for considerada responsável por uma sombra que poderia ser considerada por outros como sendo devido a pneumoconiose; também para identificar radiografias para as quais a qualidade técnica pode ter afetado significativamente a leitura. | |
A Classificação é baseada em um conjunto de radiografias padrão, um texto escrito e um conjunto de notas (OHS No. 22). Não há características a serem observadas em uma radiografia de tórax que sejam patognomônicas de exposição à poeira. O princípio essencial é que todas as aparências consistentes com aquelas definidas e representadas nas radiografias padrão e na diretriz para o uso da Classificação Internacional da OIT devem ser classificadas. Se o leitor acreditar que alguma aparência provavelmente ou definitivamente não está relacionada à poeira, a radiografia não deve ser classificada, mas um comentário apropriado deve ser adicionado. As 22 radiografias padrão foram selecionadas após testes internacionais, de forma a ilustrar os padrões das categorias intermediárias de profusão de pequenas opacidades e dar exemplos de padrões das categorias A, B e C para grandes opacidades. Anormalidades pleurais (espessamento pleural difuso, placas e obliteração do ângulo costofrênico) também são ilustradas em diferentes radiografias.
A discussão em particular na Sétima Conferência Internacional de Pneumoconioses, realizada em Pittsburgh em 1988, indicou a necessidade de aprimoramento de algumas partes da classificação, em particular as relativas às alterações pleurais. Uma reunião do grupo de discussão sobre a revisão da Classificação Internacional de Radiografias de Pneumoconioses da OIT foi convocada em Genebra pela OIT em novembro de 1989. Os especialistas sugeriram que a classificação curta não traz vantagens e pode ser excluída. Em relação às anormalidades pleurais, o grupo concordou que essa classificação passaria a ser dividida em três partes: “Espessamento pleural difuso”; “Placas pleurais”; e “obliteração do ângulo costofrênico”. O espessamento pleural difuso pode ser dividido em parede torácica e diafragma. Eles foram identificados de acordo com as seis zonas - superior, média e inferior, dos pulmões direito e esquerdo. Se um espessamento pleural for circunscrito, pode ser identificado como uma placa. Todas as placas devem ser medidas em centímetros. A obliteração do ângulo costofrênico deve ser anotada sistematicamente (quer exista ou não). É importante identificar se o ângulo costofrênico é visível ou não. Isso se deve à sua especial importância em relação ao espessamento pleural difuso. Se as placas são classificadas ou não, deve ser apenas indicado por um símbolo. O achatamento do diafragma deve ser registrado por um símbolo adicional, pois é uma característica muito importante na exposição ao amianto. A presença de placas deve ser registrada nessas caixas usando o símbolo apropriado “c” (calcificado) ou “h” (hialino).
Uma descrição completa da classificação, incluindo suas aplicações e limitações, encontra-se na publicação (ILO 1980). A revisão da classificação das radiografias é um processo contínuo da OIT, e uma diretriz revisada deve ser publicada em um futuro próximo (1997-98) levando em consideração as recomendações desses especialistas.
" ISENÇÃO DE RESPONSABILIDADE: A OIT não se responsabiliza pelo conteúdo apresentado neste portal da Web em qualquer idioma que não seja o inglês, que é o idioma usado para a produção inicial e revisão por pares do conteúdo original. Algumas estatísticas não foram atualizadas desde a produção da 4ª edição da Enciclopédia (1998)."